II.4.2. Types de coagulation
La coagulation du lait est une étape importante dans la
préparation du fromage. Il s'agit de la transformation du lait liquide
en un gel, appelé aussi coagulum ou caillé. On distingue deux
types de coagulation : la coagulation acide et la coagulation enzymatique.
Cependant, en fromagerie, la coagulation du lait résulte le plus souvent
de l'action combinée d'une enzyme et de l'acidification, seule varie
l'importance relative de leur action coagulante respective (Soumeya, 2017).
II.4.2.1. Coagulation acide
Le mécanisme de la coagulation par voie fermentaire
dite coagulation acide est de nature électrochimique. Elle est induite
par les ferments lactiques. Les genres Lactobacillus, Lactococcus,
Leuconostoc, et Streptococcus sont les plus utilisés tout
en variant en fonction des fromages et des technologies. Le Camembert
présente par exemple une majorité de Lactococcus, et
seuls les laits fermentés par Streptococcus thermophilus et
Lactobacillus bulgaricus peuvent prétendre à
l'appellation yaourt (Ronez, 2012).
Elle consiste à précipiter les caséines
à leur point isoélectrique (pHi = 4,6) soit :
? par acidification biologique à l'aide de
bactéries productrices d'acide lactique (bactéries lactiques
contaminant à l'état naturel le lait ou apportées sous
forme de levains) (Jeantet et Garric, 2005).
? par acidification chimique (injection de CO2 addition de
gluconodeltalactone) (Jeantet et Garric, 2005).
Le gel formé présente une
perméabilité satisfaisante, mais une friabilité
élevée avec une élasticité et plasticité
pratiquement nulles dues au manque de structuration du réseau (Figure
9).

25
Figure 9. Modification de la structure micellaire au
cours de l'acidification
(Jeantet et Garric, 2005)
II.4.2.2. Coagulation enzymatique
Il s'agit de l'action de la présure (plus
précisément de la chymosine) qui va hydrolyser
préférentiellement la caséine á en un site
préférentiel de coupure (Figure 10). La coagulation de type
présure a généralement lieu pour des pH compris entre 6.2
et 6.7, pH pour lesquels la déminéralisation de la micelle est
nulle ou faible. Dans ces conditions, la structure de la micelle est
stabilisée (Lenoir et al., 1985).
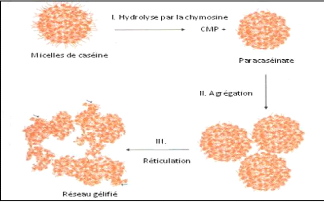
Figure 10. Modification de la structure micellaire au
cours de la coagulation présure
(Jeantet et Garric,
2005).
26
II.4.2.3. Coagulation mixte
Ce type de coagulation consiste en l'action de la
présure et l'acidification du lait. C'est la voie la plus
utilisée dans les industries fromagères en particuliers pour la
fabrication des fromages frais (petit suisse, demi sels....) et des fromages
à pâte molle (Camembert, Brie...) (Soumeya, 2017).
Dans les deux cas, après formation de coagulum,
celui-ci s'exsude et se détache du lactosérum : c'est la
synérèse de caillé ou égouttage. Ce
phénomène de synérèse est rapide pour le coagulum
par emprésurage et lent pour le coagulum acide (Lenoir et al., 1985).
II.4.3. Mécanismes d'action de coagulation
On distingue 3 phases de coagulation :
V' Phase primaire ou hydrolyse enzymatique.
V' Phase secondaire ou agrégation des micelles.
V' Phase tertiaire ou réticulation du gel (Jeantet et
Garric, 2005).
? La phase primaire est la phase enzymatique.
Le caséinomacropeptide, qui constitue un fragment hydrophile et
chargé de la caséine K, est hydrolysé par l'action
enzymatique de la présure (Figure 11) et est éliminé dans
le lactosérum. Le fragment de caséine restant est appelé
paracaséine K et possède des propriétés
hydrophobes. Dans les premières minutes suivant l'apport de l'enzyme
coagulante dans le lait, une diminution de la viscosité du lait
apparaît; elle s'explique par la diminution de la dimension moyenne des
micelles suite à leur hydrolyse (Fox, 2011; Soumeya, 2017).
? La phase secondaire est le début du
rapprochement des micelles (Figure 11). Cette phase démarre lorsque
environ 85 à 90% des caséines K sont hydrolysées à
un pH 6,6
( Soumeya, 2017). La paracaséine K va alors
s'agréger aux caséines hydrophobes áS1 et áS2. Les
caséines K formant le manteau hydrophile délimitant les micelles
voient alors leur hydrophobicité augmenter. Les micelles de
caséine perdent alors leur affinité pour la phase aqueuse et vont
se rapprocher et s'agréger entre elles sous l'effet des interactions
hydrophobes, faisant ainsi cailler le lait (Ronez, 2012).
Le segment 1-105 ou para caséine k est hydrophobe,
basique et reste intégré à la micelle, le segment 106-169
ou caséinomacropeptide est très hydrophile, acide et passe dans
le lactosérum. Des liaisons hydrophobes et électrostatiques
s'établissent alors entre les micelles modifiées et vont
entrainer la formation du gel (Zikiou, 2013).
27
? La phase tertiaire est ce que l'on appelle
la phase de réticulation du gel. Celui-ci devient de plus en plus
organisé et structuré. Au niveau microscopique, on observe un
accroissement des liaisons entre les micelles modifiées (Figure 11),
principalement des interactions hydrophobes et électrostatiques, ainsi
que la formation des ponts phosphocalciques. Elle correspond au niveau
macroscopique au durcissement du gel. (Ronez, 2012).
Les micelles agrégées subissent de profondes
réorganisations par la mise en place de liaisons phosphocalciques et
peut être de ponts disulfures entre les para caséines (Zikiou,
2013). Des liaisons électrostatiques et des liaisons hydrophobes
participent à la formation du gel. Le calcium ionique et le phosphate de
calcium colloïdal jouent aussi un rôle déterminant dans le
phénomène (Soumeya, 2017).
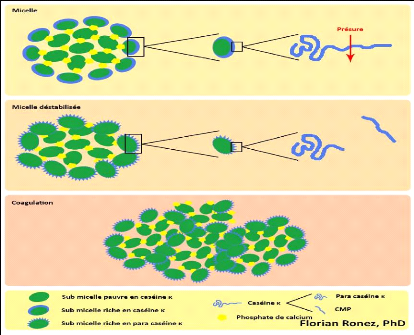
Figure 11. Formation d'un caillé par action de
la présure sur les caséines du lait
(d'après
de modèle de Schmidt & Walstra, 2012)
28
| 


