1.1 Biologie, écologie et gestion de I.
cylindrica
1.1.1 Systématique
I. cylindrica est un végétal de
l'embranchement des Spermaphytes, du sous-
embranchement des Angiospermes, de la classe des
Monocotylédones, de l'ordre des Cyperales, de la famille des
Poaceae, de la sous famille des Panicoidae, de la tribu des
Andropogoneae, de la sous tribu des Saccharinae, du genre
Imperata et de l'espèce cylindrica. C'est est une
graminée monocotylédone, ainsi son méristème apical
reste proche de la surface du sol alors que les feuilles sont
érigées. Hubbard et al. (1944), reconnaissent cinq
variétés de I. cylindrica: Var. condensata
(2n=10), Var. major (2n = 20), Var. lactifolia (2n=30),
Var. africana (2n = 40), Var. europa (2n = 60).
1.1.2 Description morphologique
I. cylindrica est une herbe érigée
à rhizome dont la pousse est un chaume cylindrique
formé de gaines de feuilles roulées les unes
aux autres. Le rhizome est blanc segmenté, pointu et peut percer les
tubercules sous terre, voire piquer les pieds et mains des personnes
travaillant dans les champs infestés. Le système racinaire est
fibreux et se développe au niveau des noeuds des rhizomes. La tige est
pratiquement invisible et donne l'impression que les feuilles sortent
directement de terre. Les feuilles de la plante adulte mesurent 1,25 cm
à 2,5 cm de large et sont généralement de 30 cm à
75 cm de long. Elles sont rarement d'une couleur vert foncée mais
tendent sur du vert pâle avec une bordure tranchante grâce à
leur richesse en silice. Contrairement à la plupart des plantes, la
nervure blanchâtre qui traverse la surface supérieure n'est pas
médiane et permet de distinguer aisément l'espèce.
L'inflorescence est une panicule cylindrique de couleur blanchâtre ou or.
La panicule mesure en moyenne 10 à 20 cm de long sur 0,5 à 2,5 cm
de large (MacDonald, 2004). Les pédicelles sont inégaux et les
pollens allongés ou lancéolés sont entourés de
poils soyeux. Chaque graine est munie d'une queue ou d'une plume.
1.1.3 Biologie
I. cylindrica se reproduit aussi bien de façon
sexuée, par les graines, que de façon
asexuée, par les rhizomes (Bryson and Carter, 1993). En
effet, c'est une plante qui
produit plus de 3000 graines par plante.
L'inflorescence est induite par les conditions
rudes telles que le fauchage et le brûlis, et les
graines peuvent être transportées sur des centaines de
mètres.
Une plante obtenue à partir d'un semis peut donner des
rhizomes en 4 semaines (Bryson et Carter, 1993). Les rhizomes
représentent plus de 60% de la biomasse totale, et le faible rapport
pousse/rhizome contribue à sa régénération rapide
après un brûlis, un sarclage ou un labour (MacDonald, 2004). La
capacité de régénération des rhizomes augmente avec
leur âge et leur poids car les rhizomes matures sont plus riches en
nutriments que les jeunes rhizomes (MacDonald, 2004). De même, les
bourgeons des rhizomes matures qui sont proches de l'apex sont les premiers
à régénérer lorsqu'ils sont séparés
de la plante mère. En revanche, leur diamètre et leur nombre de
noeuds n'influencent pas de façon significative leur croissance (Ayeni
et Duke, 1985). Les rhizomes tolèrent bien la dessiccation et se
reproduisent mieux sur les sols acide (Wilcut et al., 1988). Chaque
segment de rhizome peut produire une nouvelle plante, ce qui peut arriver avec
les pratiques culturales et les applications partielles d'herbicide. La
régénération des bourgeons est favorisée par leur
exposition à la lumière (MacDonald, 2004 ; Atchade, 2004) alors
que l'enfouissement des fragments de rhizomes à plus de 8 cm de
profondeur peut limiter la propagation de l'adventice (Wilcut et al.,
1988).
1.1.4 Distribution Géographique
I. cylindrica pousse souvent dans les régions
sub-tropicales et se développe bien dans les milieux où la
pluviométrie annuelle se situe entre 750 mm et 5000 mm (Bryson and
Carter, 1993). Elle envahit les régions qui sont soumises à de
fortes pressions humaines et atteint sa croissance maximale sur les sols
fertiles mais son développement normal n'est pas limité par la
fertilité du sol.
I. cylindrica est enregistrée comme mauvaise
herbe dans 73 pays de par le monde et est présente sur tous les 5
continents. Sa présence est remarquable en Afrique, en Australie, en
Asie du sud et dans le Pacific tandis qu'elle est moins abondante ou constitue
un problème mineur en Europe du sud, en Méditerranée et en
Amérique du sud (Van Loan et al, 2002). Selon Hubbard et
al (1944) et Santiago (1980), I. cylindrica var europa
est rencontrée en Afrique du Nord et en Europe autour de la
Méditerranée, et à l'Est de l'Afghanistan, I.
cylindrica var. major est indigène à l'Afrique de
l'Est, à l'Asie, à l'Australie, et aux Iles de l'Océan
pacifique. I. cylindrica var africana est rencontrée
en
Afrique de l'Ouest, I. cylindrica var.
lactifolia se développe seulement au Nord de l'Inde, alors que
I. cylindrica var condensata est retrouvée en Chili et
en Amérique du Sud (MacDonald, 2004).
Selon une prospection couvrant le Bénin, le Cameroun,
le Ghana et le Nigéria, la fréquence d'apparition de I.
cylindrica diffère suivant les zones agroécologiques mais
pas suivant la saison de collection (Chikoye et al, 2001). Ceci
suppose que dans une région de forte infestation, l'herbe est aussi
présente en saison pluvieuse qu'en saison sèche (Ayeni, 2004).
Selon Ayeni et al, 2004, au Bénin, les taux
moyens d'infestation dans les champs cultivés, étaient
respectivement de 67%, 45% et 6% (Figure 1) dans la zone humide au sud (2
saisons pluvieuses avec 1200 - 1300 mm de pluies annuelles), dans la zone
subhumide au centre (1100 - 1200 mm), et dans la zone subaride au nord (900 -
1000 mm avec une saison de pluie).
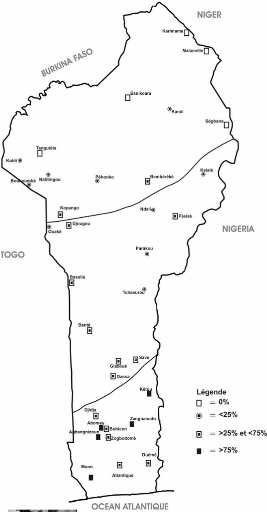
Zone subhumide
Zone humide
Zone subaride
1.1.5 Importance agronomique et économique de
Imperata cylindrica dans la problématique du
développement
I. cylindrica a été
désignée parmi 88 autres espèces comme la pire des
mauvaises herbes, par la majorité des paysans interviewés dans
différentes zones agro-écologiques des zones humides et
subhumides au Bénin, au Nigéria et en Côte d'Ivoire
(Chikoye et al., 2000; Ayeni et al, 2004 ; Vissoh et
al., 2004). Elle est classée 7ème mauvaise herbe
sur le plan mondial (Holm et al, 1977).
Sur le plan économique, I. cylindrica est
considérée comme un sérieux problème en Afrique
occidentale et centrale. Les pertes qu'elle inflige aux cultures à
tubercules telles que le manioc et l'igname, ne sont pas seulement dues
à la compétition directe, mais aussi aux infections qui
surviennent lorsque les rhizomes de l'herbe percent les tubercules. De
même, par exemple au Bénin, l'enlèvement manuel de I.
cylindrica coûte, 40.000 à 50.000 FCFA par ha (Vissoh et
al., 2004). Le coût de l'enlèvement de I. cylindrica
par l'usage des herbicides est estimé à $400 par hectare (Van
Loan et al., 2002). I. cylindrica est un fourrage de peu
d'importance parce que le bord tranchant des feuilles (riches en silice), la
rend indésirable par les animaux (Coile et Shilling, 1993). Selon
Hubbard et al. (1944) I. cylindrica est utilisée pour
l'emballage des biens en milieu rural en Afrique. En Irak, elle sert à
fabriquer des brosses ; en Egypte elle sert dans la fabrication des cordes et
des tapis, des nattes, des tapis-brosses et en Union Soviétique dans la
fabrication des essuie-pieds. Au sud et au centre du Bénin, I.
cylindrica est utilisée pour couvrir les cases (Ayeni et
al, 2004). Certaines populations l'utilisent dans le domaine
médicinal. En effet dans la région de Dangbo au Bénin, les
rhizomes de I. cylindrica sont utilisés comme aphrodisiaque, ou
pour renforcer la santé des enfants en période de dentition
(Ayeni et al, 2004).
Sur le plan social, on assiste à l'abandon de terres
cultivables envahies par I. cylindrica à cause du
caractère compétitif de l'herbe, mais aussi à cause de sa
capacité de repousse (Terry et al., 1997).
Sur le plan environnemental, même si l'herbe est une
des rares espèces qui oeuvrent à la réduction de
l'érosion du sol, elle a indirectement des effets nuisibles sur la
nature. Entre autres effets, on peut signaler que la grande capacité
d'extension de I. cylindrica entraînant l'abandon des terres
infestées, favorise l'exploitation abusive d'autres surfaces
avec comme corollaire la destruction des espaces
boisés. De même, cet abandon pousse les jeunes paysans à
l'exode rural dans les grandes villes où ils s'adonnent à la
vente de l'essence au bord des voies, puis à la conduite de taxi-moto,
contribuant ainsi à augmenter les risques de pollution.
A la lumière de cette analyse, il est évident
que I. cylindrica est une herbe qui présente d'avantages
minimes par rapports aux dommages qu'elle cause à la
société. Ainsi, en 2004 au Bénin, la perception des
paysans dans toutes les trois zones ci-dessus décrites étaient
que I. cylindrica évolue plus comme une herbe
indésirable qu'une herbe utile (Ayeni, 2004). C'est pourquoi dans les
régions de fortes infestations, 96% des paysans interviewés
pensent que l'herbe est nuisible, tandis 89% d'entre eux souhaitent une
éradication totale (Ayéni, 2004) et en attendant une meilleure
solution, ils développent diverses stratégies pour ramener les
taux d'infestation à des niveaux acceptables.
1.1.6 Méthodes classiques de lutte contre I.
cylindrica 1.1.6.1 Lutte mécanique
Une lutte mécanique réussie nécessite la
destruction de la capacité de repousse des rhizomes et des graines,
habituellement par des perturbations physiques, enfouissement ou
enlèvement complet de l'herbe pour empêcher sa croissance. Ainsi,
elle a pour but de couper les rhizomes en morceaux et de les exposer au soleil
ou les enfouir en profondeur afin de prévenir leur repousse (Brook,
1989).
Dans la pratique, un tel but est impossible à
atteindre, cependant la lutte mécanique reste de loin, une des
méthodes les plus largement répandues.
Les paysans à faibles revenus se limitent au fauchage,
à l'enlèvement manuel ou au brûlis parce que ces techniques
ne nécessitent que l'énergie humaine et l'usage d'instruments
simples (Brook, 1989). Mais elles ne garantissent pas à elles seules une
réduction de la biomasse des rhizomes et du feuillage (Willard et
al., 1996).
Le brûlis utilise le même principe que le
fauchage, c'est-à-dire l'enlèvement de la partie aérienne.
Il est préféré en Afrique centrale et occidentale au
fauchage mais il induit les repousses (Avocanh, 2005) et accentue
l'inflorescence, et par conséquent la production de graines (CABI,
2005). De plus, il comporte les risques d'extension du feu à d'autres
champs ou aux agglomérations mais aussi un risque de pollution
environnementale (Menz et al., 1998) et de l'érosion des
sols.
Au sud-Bénin, les paysans billonnent les terres, ce qui
a un double avantage de recycler la fertilité et de réduire
l'infestation du sol (Vissoh et al., 2004).
1.1.6.2 Lutte culturale
La fumure et l'utilisation des jachères constituent les
principales méthodes culturales. L'utilisation de la fumure est
basée sur le principe que la fumure, en particulier l'azote, peut
favoriser la compétitivité des cultures désirées en
défaveur de I. cylindrica (MacDonald, 2004). En effet, l'apport
d'engrais influence très peu le développement de I.
cylindrica (Atchade, 2004) et permet aux cultures d'être
compétitives par leur couverture végétale dont l'ombrage
peut réduire le développement de l'herbe.
L'observance des jachères, utilise également
comme principe, le caractère héliophile de I. cylindrica
(Brook, 1989 ; Atchade, 2004). Une période de jachère naturelle
adéquate pour venir à bout de l'herbe peut durer plusieurs
années. Or, la pression démographique et l'augmentation des
besoins alimentaires ont conduit à la nécessité de
réduire les périodes de jachères. Au sud Bénin, par
exemple, les périodes traditionnelles de jachères ne sont plus
respectées. C'est seulement dans quelques régions comme
Pobè et Bonou que certains paysans continuent à observer entre 4
à 5 années de jachère (Vissoh et al., 2004).
L'utilisation des plantes de couverture peut permettre de réduire le
temps de jachère et par conséquent, limiter la contrainte
liée aux jachères naturelles. En effet, selon Vissoh et
al., (2004), les plantes de couverture permettent de réduire le
temps de jachère jusqu'à 2- 5 ans. Selon Brook (1989), les
espèces recommandées sont : Calopogonium mucunoides
Desv., Centrosema pubescens BTH, Pueraria phaseoloides
(Roxb.) BTH, Psophocarpus palustris Desv., Crotolaria spp.,
Styloxanthes spp., Moghania macrophylla (Willd.) et
Gliciridia maculata HBK.
Déjà en 1992 le projet Sasakawa Global 2000 a
entrepris au Bénin la vulgarisation de Mucuna spp pour lutter
contre I. cylindrica. Après 3 années consécutives
d'utilisation du Mucuna spp, 100% des exploitants avaient reconnu que
cette plante de couverture contribuait à améliorer la
fertilité des sols tandis que 84% d'entre eux ont confirmé son
pouvoir d'éradication de I. cylindrica en deux années
(Galiba et al, 1998). Paradoxalement de nos jours l'utilisation de
Mucuna se raréfie de plus en plus à causes de plusieurs
contraintes. Selon une enquête menée au Bénin, au
Nigéria et en Côte d'Ivoire par Chikoye et al., 2000,
seulement 12,7% des paysans interviewés utilisaient les
jachères améliorées (utilisation de
Mucuna spp.). Ceci montre que des réticences persistent par
rapport à l'adoption de cette technique pour venir à bout de
I. cylindrica, car les plantes de couverture occupent des espaces
réservés aux cultures. C'est comme si les investissements
nécessaires pour leur établissement ne sont pas
bénéfiques par rapport aux avantages qu'elles
génèrent (Manyong et al., 1999). Selon Chikoye et
al., (2002), il est invraisemblable que les plantes de couverture soient
totalement adoptées dans une condition de manque cruel d'espaces
cultivables. Ainsi, au Bénin, les plantes de couverture, comme
Mucuna spp, et Aeschynomene histrix qui occupent le sol pour
une courte durée sont peu adoptées (Vissoh et al., 2004)
alors que les espèces pérennes comme Cajanus cajan,
Acacia auriculiformis sont mieux adoptées parce qu'elles sont
également exploitées pour leurs bois, leurs graines et feuilles
comestibles (Vissoh et al., 2004). Comme les graines de Mucuna
spp. n'ont aucune valeur alimentaire (Vissoh et al.,
2004), Versteeg et al. (1998) avaient initié au Bénin un
processus de désintoxication des graines de Mucuna spp., pour
pouvoir l'utiliser dans les principaux plats. Or les études
menées par Ayeni et al. (2004), confirment toujours la
non-adoption de cette plante par les paysans. Cette réticence dans
l'adoption des plantes de couvertures au sud Bénin peut être
expliquée par l'augmentation de la pression démographique. En
réalité, l'importance économique des plantes de couverture
peut varier selon les cultures. Elles sont par exemple en général
bénéfiques dans un champ de manioc tandis que l'effet contraire
est observé pour le maïs (Chikoye et al., 2001). Face
à ces faiblesses, d'autres auteurs ont tendance à
privilégier la lutte chimique.
1.1.6.3 Lutte chimique
La lutte chimique permet d'obtenir un résultat rapide
et en plus elle n'est pas fastidieuse dans sa mise en oeuvre. Comparativement
aux méthodes de lutte mécanique, elle évite la
perturbation du sol qui entraîne l'érosion (Brook, 1989).
Plusieurs herbicides existent et ont été testés pour leur
efficacité contre I. cylindrica (Brook, 1989; MacDonald, 2004).
Les herbicides usuels sont Dalapon, Glufosinate, Imazapyr et Glyphosate qui est
le plus fréquent sur le marché. Cette préférence au
Glyphosate est due à sa faible toxicité pour les
mammifères et son absence de résidus phytotoxiques sur le sol
(Terry et al., 1997) et son coût relativement faible.
Malheureusement, les herbicides sont seulement utilisés par les paysans
à forts revenus; ils ne sont pas spécifiques et
nécessitent la disponibilité de
grandes quantités d'eau. Mal utilisés, les
herbicides peuvent entraîner des problèmes sur la santé et
sur l'environnement. La limitation de l'utilisation des herbicides dans les
pays au sud du Sahara est due à quatre facteurs majeurs : la non
disponibilité d'herbicide de bonne qualité, la non
disponibilité d'équipements adéquats, l'absence de
formation adéquate et les coûts élevés. Sur 300
paysans interviewés au Bénin aucun n'utilisait d'herbicide contre
I. cylindrica (Ayeni et al, 2004).
Si le problème constitué par I.
cylindrica augmente d'année en année (Ayeni, 2004), ceci
suppose qu'aucune des méthodes ci-dessus mentionnées n'est encore
suffisante et par conséquent de nouvelles méthodes de lutte telle
que la lutte biologique peuvent être envisagées.
1.2 Théorie et principes de la lutte
biologique
Les végétaux, tout comme les animaux,
possèdent des ennemis naturels (insectes ou pathogènes) qui
coexistent normalement dans un certain équilibre, mais qui peuvent dans
certaines conditions occasionner leur destruction partielle ou totale. La lutte
biologique est l'étude et l'utilisation de ces ennemis naturels pour
réguler la densité d'une population d'hôte donnée
qui croit à cause du déséquilibre de l'environnement
original (Harlet et Forno, 1992). La lutte biologique peut
être classique (inoculative) ou
inondative.
1.2.1 Lutte biologique classique
La plupart des pestes ne sont des contraintes que dans leur
nouveau milieu d'introduction, où elles rencontrent des conditions
favorables à leur développement pendant que leurs ennemis
naturels sont absents. La lutte biologique classique consiste à : «
introduire l'agent de lutte biologique dans une région qui n'est pas son
origine afin de réduire de façon significative une population
d'hôte qui est le plus souvent introduite ». Les cas de
succès de cette technique sont légion. C'est par exemple
l'utilisation d'un parasitoïde, Anagyrus (Epidinocarsis)
lopezi De Santis originaire d'Argentine du Nord, qui a permis de
lutter efficacement contre la cochenille farineuse du manioc Phenacoccus
manihoti Matile-Ferrero (Homoptera, Pseudococcidae) au Nigéria et
au Bénin (Neuenschwander, 2002). De même, Typhlodromalus
aripo De Leon un prédateur originaire du Brésil, qui s'est
établi rapidement en Afrique subsaharienne, a réduit
considérablement la population de l'acarien vert du manioc,
Mononychelus tanajoa (Bondar) (A cari Tetranychidae).
(Yaninek et Hanna, 2003). De 1995 à 1998 le
succès des lâchers de Pareuchaetes pseudoinsulata Rego
Barros (Lepidoptera, Arctiidae) au Ghana a permis de réduire
l'infestation de Chromolaena odorata (L.) (Asteraceae) de 85%
à 32% (James et al., 2002). Au Bénin, dans les
localités de Tévèdji, Lihu, et Kafedji, sur le fleuve
Ouémé la jacinthe d'eau, Eichhornia crassipes (Mart.)
Solms-Laubach (Pontederiaceae) a été réduite de
la surface du fleuve Ouémé, de 100% à 5%, en 8
années par les lâchers de Neochetina eichhorniae Warner
(Coleoptera curculionidea) et de Neochetina bruchi Hustache
(Coleoptera curculionidea) (Ajuona et al., 2003).
Dans le cas d'utilisation des champignons pathogènes,
cette forme de lutte peut être assimilée au lâcher des
champignons biotrophes contre une cible. L'un des succès en
matière de ce genre de lutte est l'utilisation de la rouille (champignon
biotrophe) Uromycladium tepperianum pour contrôler Acacia
saligna en Afrique du sud (Charudattan, 2001). Ce champignon a
été importé de l'Australie vers l'Afrique du Sud
après des tests de spécificité effectués sur une
large variété de culture d'importance économique (Morris,
1987). C'est aussi le cas de l'établissement de Neozygites
tanajoae (Entomophtorales, Neozygitaceae) d'origine
brésilienne, causant une infection moyenne de 25% des populations
d'acarien vert au Bénin (Hountondji et al., 2002).
La lutte biologique classique contre les mauvaises herbes
implique le plus souvent l'utilisation des champignons pathogènes. Pour
être efficace, elle doit prendre en compte l'écologie de l'herbe,
sa biologie et les informations climatiques et géographiques sur les
régions où l'herbe constitue un problème. Si dans le cas
d'utilisation des insectes comme agent de lutte contre les mauvaises herbes, de
grands succès ont été obtenus avec des insectes exotiques,
dans le cas de l'utilisation des microbes (le plus souvent des champignons),
les problèmes d'homologation constituent une contrainte majeure. En
effet, l'évaluation de l'effet des microorganismes lâchés
dans l'environnement nécessite des connaissances et moyens
spécifiques qui font défauts dans les pays africains. Ceci
suscite une méfiance à l'égard des microorganismes
d'origine exogène d'où des difficultés d'homologation.
Depuis les années 2000 certains champignons
pathogènes sont déjà classés
ou
commercialisés comme des agents de lutte biologique contre les
mauvaises herbes dans
les pays développés comme les Etats-Unis,
l'Italie, le Canada et l'Australie, mais aussi en Inde et en Chine (Tableau
1).
Tableau 1: Quelques champignons commercialisés
ou utilisés comme agents de lutte biologique Champignons Noms
commerciaux Herbes cibles
Acremonium diospyri - Diospyros virginiania
Alternaria zinniae - Xanthium occidentale
Alternaria eichhorniae - Eicchornia
crassipes
Alternaria cassiae CASST Cassia obtusifolia
Cercospora rodmanii ABG 5003 Eicchornia
crassipes
Colletotrichum coccodes VELGO Abutilon
theophrasti
Colletotrichum gloesporiodes f. sp LUBOA 2 Cuscuta
chinensis et, Cuscuta
cuscutae australis
Colletotrichum gloesporiodes f. sp COLLEGO
Aeschynomene virginica
aeschynomene
Colletotrichum orbiculare - Xanthium
spinosum
Condrosterium purpureum BIOCHON Prunus
serotina
Phytophtora palmivora DEVINE Morrenia
odorata
Source: Les champignons agents de lutte biologiques,
Butt et al., 2001
En Afrique, des efforts sont aussi déployés
dans la recherche d'agents microbiens de lutte contre les mauvaises herbes.
C'est le cas de Sporisorium ophiuri (P. Henn) Vanky (Ustilaginales),
un charbon bactérien utilisé dans la lutte contre Rottboellia
cochinchinensis (Lour.) Clayton, appelée encore herbe queue de rat
(Valverde, 2005). Il en est de même pour les isolats de Fusarium
oxysporum f. sp. Striga qui réduisent significativement
l'émergence de Striga hermonthica dans les champs de
céréales (Kroschel et al., 1996; Ciotola et
al., 1999, Elzein et Kroschel, 2004).
1.2.2 Lutte biologique inondative
Selon Harley et Forno (1992), contrairement à la lutte
biologique classique où l'agent de lutte biologique reste permanent et
se perpétue une fois établie, dans le cadre de la lutte
biologique inondative, l'agent n'est pas un élément permanent du
biotype. Même lorsqu'il y est présent, sa densité n'est pas
à même d'assurer une maîtrise de l'hôte. Il s'agit
donc de l'introduction dans l'environnement à plus d'une fois, une
grande quantité d'inoculum pour induire une population d'agent de lutte
biologique capable de contrôler efficacement l'hôte (approche
inondative), ou pour compléter périodiquement
l'effectif
d'une population d'agent de lutte biologique existante, afin de
maîtriser l'hôte (approche augmentative).
Le type de formulation utilisé pour un biopesticide
prend en compte les exigences écologiques, les techniques d'application
disponibles, la biologie de l'hôte et celle du pathogène, mais
aussi le mode d'action de ce dernier. C'est ainsi que dans le cadre de la lutte
contre les sauteriaux, le projet LUBILOSA (IITA-Benin) a fait le
développement de la formulation huileuse des spores du champignon
Metarhizium anisopliae. Ce type de formulation favorise
l'adhésion des spores à la cuticule des insectes mais garantit
aussi l'infection dans les conditions d'humidité relative faible comme
dans le désert (Bateman, 1997) en ce sens que l'émulsion huileuse
protège les propagules contre la dessiccation et les rayons UV. Dans le
cadre de la lutte biologique contre les adventices, le choix de l'approche
inondative a pour finalité le développement d'un mycoherbicide.
Le mot mycoherbicide se décompose en `'Myco» qui signifie : «
champignon » et `'Herbicide» qui signifie : « qui tue les herbes
». Un mycoherbicide est un herbicide dont le principe actif est une
propagule de champignon (mycélium, conidies, sclérotes,
chlamydospores, etc.) mélangé à d'autres
ingrédients (sources d'énergie et surfactants), le tout dans un
support convenablement choisi pour faciliter le début de l'infection, le
développement de l'infection, l'application du produit, sa conservation,
et sa durée de vie (formulation). L'apport de tween 80 dans certaines
formulations facilite par exemple, la dispersion uniforme des propagules et
assure un début d'infection correct. Il faut aussi signaler l'usage
d'abrasives comme le Gasil dans les formulations mycoherbicidiques qui permet
de faciliter l'infection des herbes hôtes par le pathogène
inoculé en causant préalablement des dommages dans le tissus
foliaire.
1.3 Les options de la lutte biologique contre I.
cylindrica
Imperata cylindrica importé aux Etats Unis
pour lutter contre l'érosion de sols s'est propagé rapidement
pour devenir une adventice. Alors des chercheurs de l'université des
Florides ont entamé des prospections sur les ennemis naturels et ont
abouti à la découverte de pathogènes, d'arthropodes et
d'autres invertébrés capables d'attaquer I. cylidrica
(Van Loan et al., 2002).
Parmi les insectes reportés de par le monde, seul
Orseolia javanica Kieffer et van Leeuwen-Reijnvaan (Cecidomyidae), est
spécifique à I. cylindrica (Van loan et al.,
2002). Il se trouve en abondance dans les endroits où I.
cylindrica est régulièrement coupé ou fauché.
Ses femelles pondent des oeufs qui, après éclosion, donnent des
larves qui pénètrent dans la plante pour y créer des
galles. Mais les chances de considérer O. javanica comme un
agent potentiel de lutte biologique efficace sont réduites par
l'existence de Platygaster oryzae (Hym., Platygasteridae) qui est son
prédateur (Van Loan et al., 2002).
Plusieurs pathogènes sont associés à
I. cylindrica. On peut citer par exemple Myrellina imperatae
Sankaran et Sutton qui causent en Malaisie des taches et des chloroses sur les
feuilles (Sankran and Sutton 1992). De même on peut citer,
Xanthomonas albilineans (Ashby) Dowson en Australie, qui est
responsable d'une décoloration foliaire (Persley, 1973). Beaucoup
d'autres pathogènes sont cités dans le monde incluant Puccina
rufipes Diet., Claviceps imperatae Tanda et Kawatani,
Monodisma fragilis Alcorn, Deightoniella africana Hughes,
Mycosphaerella imperatae Sawada, Bipolaris maydis (Y. Nisik.)
Shoemaker, Colletotrichum caudatum (Sacc.) Peck, C. graminicola
(Ces.) G.W. Wilson, Aschochyta sp., Didymaria sp.,
Dinemasporium sp., Chaetomium fusiforme Chivers et
Helminthosporium, Curvularia et Fusarium species
(Chadrasrikul, 1962; Chase et al., 1996; Caunter, 1996).
Déjà en 1985, 12 champignons pathogènes
de I. cylindrica avaient été listés en Albanie
(Ravenell, 1985). En Afrique on peut citer Giberella imperatae C.
Booth et Prior qui cause des dessèchements au niveau de I.
cylindrica en Nouvelle Guinée (Booth et Prior 1984).
D'autres études effectuées aux Etats-Unis ont
montré d'une part, l'efficacité d'un
mélange de
pathogènes (Drechslera gigantea et Bipolaris sacchari)
en formulation sur
plusieurs adventices de la famille des Poacae
dont I. cylindrica (Yandoc et al., 1999), et d'autre part,
l'efficacité de Drechslera gigantea (Heald et Wolf)
(Pleosporaceae), Exserohilum rostratum (Drechsler) Leonard et
Suggs (Pleosporaceae), Exserohilum longirostratum
(Pleosporaceae) et Bipolaris sacchari
(Pleosporaceae) sur I. cylindrica (Charudattan, 1996).
Des efforts de collection de pathogènes au niveau de
rhizomes ont été faits en 2005 au Bénin et ont permis
d'identifier Fusarium oxysporum Schlecht. Emend. Synd.et Hans.
(Tuberculariaceae), Macrophomina phaseolina (Tassi) Goid et
Chaetomium spp (Kunze) (Chaetomiaceae) (Ali-Bidjowe, 2006) mais aucun
espoir de lutte n'est obtenu après leur application. L'utilisation des
champignons foliaires reste donc à ce jour la seule
possibilité.


CHAPITRE 2 : MATERIEL ET METHODES
2.1 Production de plants de I.
cylindrica
De jeunes plants de 6 semaines d'âge ayant une hauteur
comprise entre 8-10 cm et 4
feuilles, ont été utilisés pour le test de
pathogénicité tandis que des plantes adultes à feuilles
lignifiées ont servi pour le test de virulence.


b
Les jeunes plantes ont été produites à
partir de semis de graines de I. cylindrica sur du coton
humidifié (Figure 2a). Quatorze jours après germination, chaque
plantule a été transplantée dans un pot en plastique (4 cm
x 7 cm x 10 cm) rempli de sol stérilisé à l'autoclave
(121 OC et 1,2 bar) (Figure 2b) pour être utilisée 4
semaines après. Pour les tests de pathogénicité.
a
Figure 2: Semis de I. cylindrica sur du coton
(a) jeunes plantes de I. cylindrica transplantées après
semis ( b)
Les plants adultes avec des feuilles lignifiées et
riches en silice ont été transférés directement
d'un champ naturellement infesté dans la station de l'IITA-Bénin,
à raison d'un plant par pot, ceci afin d'être proche des
conditions et aspects naturels des plants. Lorsque les plants
transplantés ont un minimum de deux nouvelles feuilles, toutes les
anciennes feuilles ont été enlevées. Lorsque tous les
plants ont eu un minimum de cinq feuilles, les plus vieilles feuilles ont
été enlevées pour laisser les trois plus jeunes feuilles.
Ces trois feuilles ont été marquées de fines ficelles de
couleur jaune, verte, bleue pour identifier respectivement la plus jeune, la
moins jeune et la plus vieille feuille.
2.2 Prospection des champignons pathogènes 2.2.1
Collecte des feuilles avec symptômes
Pour la collecte des pathogènes foliaires de I.
cylindrica, le Bénin a été subdivisé en trois
zones agroécologiques selon la segmentation de Ker (1992). Il s'agit de
:
- la zone humide (ZH) au
sud, située au dessous de la 7ème
parallèle Nord, qui regroupe les départements de l'Atlantique, de
l'Ouémé, du Plateau, du Mono, du Couffo et du Zou. Elle a une
pluviométrie bimodale, caractérisée par une moyenne
annuelle de 1200 - 1300 mm de pluie s'étendant sur 190 - 230 jours de
mars à juillet et de septembre à novembre. La température
moyenne annuelle est de 26,5°C avec une humidité
relative de 75% en moyenne par an. L'insolation moyenne annuelle est de 2290
heures ;
- la zone subhumide (ZSH), se situant entre la 7è et
la 9è parallèle Nord, regroupe les départements des
Collines, du Borgou et de la Donga. Elle est caractérisée par une
transition allant d'une pluviométrie de type bimodal à monomodal
avec une moyenne annuelle de 1100-1200 mm couvrant 140-190 jours d'avril
à octobre. La température moyenne annuelle est de
27°C avec une humidité relative de 60% en moyenne par
an. L'insolation moyenne annuelle est de 2305 heures.
- la zone subaride (ZSA) située au Nord de la
9è parallèle, est constituée de l'Atacora et de l'Alibori.
Elle a un régime de pluie monomodal caractérisé par une
moyenne annuelle de 900 - 1000 mm de pluie couvrant 90-140 jours de mai
à septembre. La température moyenne annuelle est de
27,5°C, l'humidité relative est de 50% en moyenne par an
et l'insolation est de 2862 heures.
Les prospections ont été conduites en 2003 et
en 2004. En 2003, elles ont été conduites en avril à
raison de 60 champs par zone correspondant à la saison pluvieuse pour la
ZH et la ZSH, et à la saison sèche pour la ZSA. En 2004, les
prospections ont eu lieu en Août, ce qui correspond à la saison
pluvieuse pour la ZSA et à la saison sèche pour les deux autres
zones. Ici aussi, 60 champs ont été visités par zone. Au
total, 360 champs ont été visités au cours des deux
années. Pour chaque prospection, les coordonnées
géographiques (GPS) des champs ont été enregistrées
par un enregistreur de type «MAGELAN SporTrak PRO».
Les dimensions des champs étant variables selon les
sites, une portion de champ
d'environ 0,5 ha est délimitée au
hasard dans chaque champ. L'échantillonnage des
feuilles ayant présenté des lésions
s'est fait sur cette portion de champ délimitée, en suivant les
deux diagonales en zigzagant sur une bande de 4 m de large. Sur chaque plant,
les feuilles présentant des symptômes sont délicatement
coupées, étalées et mises en presse afin de les garder
dans leurs formes initiales. Chaque échantillon est
étiqueté par rapport au nom du village, au GPS du champ, la date
de collection et la description du symptôme observé. Le nombre
d'échantillons collectés par champ a varié de 0 à
10 en fonction de la fréquence des symptômes sur feuille.
2.2.2 Isolement des champignons à partir des
feuilles malades
Une fois au laboratoire, les échantillons de feuilles
ont été dépouillés, triés et soumis selon le
cas, à un isolement direct ou indirect.
L'isolement direct a été réalisé
lorsque des propagules (spores ou mycélium) du champignon
suspecté ont été perceptibles à l'oeil nu ou au
binoculaire à travers le symptôme. Il a consisté à
enlever avec une aiguille stérilisée au feu d'un bec bunsen, la
structure visible et de la transférer sur une boîte de
Pétri stérile en plastique (9 cm diamètre) contenant du
milieu gélosé (Eau-Agar, Annexe 1). Ce milieu est utilisé
parce qu'il ne contient pas de substances nutritives, ce qui limite
l'émergence des saprophytes qui pourraient se développer au
détriment du pathogène recherché.
Lorsque les propagules n'ont pas été
perceptibles nous avions suscité leur apparition en utilisant des
chambres humides. Les chambres humides ont été faites de
boîtes de Pétri dont l'intérieur est tapissé de deux
papiers filtres humidifiés à l'eau stérile. Sur ces
papiers filtres nous avions déposé le morceau de feuille
prélevé à l'intersection de la lésion et du tissu
sain, car le champignon est plus actif à cet endroit (Baxter et Van der
Linde, 1997), ce qui facilite son isolement en culture pure. Après 3
à 5 jours d'incubation, les structures émergées
grâce à la forte humidité de la chambre humide ont
été transférées sur le milieu Eau-Agar.
L'isolement indirect a été
réalisé dans les cas où la méthode des chambres
humides n'a abouti à l'émergence d'aucune structure. Nous avions
d'abord procédé à une stérilisation de surface par
trempages successifs de petits morceaux (4 mm2) de feuille
(prélevés à l'intersection de la lésion et du tissu
sain), dans une solution d'hypochlorite de sodium à 1% pendant 1-2 mn,
puis dans de l'alcool éthylique à 70% pendant 1-2 mn, suivi d'un
triple rinçage dans l'eau distillée stérile. Après
cette stérilisation de surface, les morceaux
de feuilles ont été séchés sur du
papier filtre stérile avant d'être transférés
aseptiquement sur le milieu Eau-Agar pour permettre l'émergence du
pathogène à partir du morceau de feuille.
Dans tous les cas, les boîtes ont été
incubées à 25oC pendant 4-7 jours, puis les colonies
développées ont été aseptiquement
transférées sur du milieu gélosé de Potato Dextrose
Agar (PDA, Annexe 2). Ce milieu contient d'élément nutritif et
permet le développement rapide du champignon isolé en culture
pure. Pour chaque isolat, la forme, la couleur, la pigmentation de la culture
pure obtenue ont été notées et les types de conidies
produites ont été décrits.
2.2.3 Détermination de la
pathogénicité: vérification du postulat de
Koch
Les colonies d'isolats cultivés sur PDA ont
été utilisées pour inoculer les jeunes plants obtenus
à partir des semis (cf 2.1). L'inoculation a été faite
à l'aide de minces couches (4 mm2) de blocs d'Agar contenant
le pathogène, maintenus à la surface des feuilles à l'aide
d'une mince mèche de coton préalablement mouillée à
l'eau stérile. Les plants inoculés ont été par la
suite incubés (28-30 0C) sous des sachets de plastique
pendant 48 heures. Par traitement, trois plants ont été
inoculés par isolat et sur chaque plant, c'est la feuille la plus
âgée (5-7mm de large) qui a reçu l'inoculât.
Après cinq jours, les feuilles nécrosées sont
prélevées et les symptômes sont comparés à
ceux observés au champ, puis l'agent responsable a été
isolé à l'aide du milieu Eau-Agar à nouveau, en utilisant
l'une des méthodes précédemment décrites au
paragraphe 2.2.2. Les colonies obtenues après ce nouvel isolement ont
été comparées (formes et couleurs des mycelia, couleur de
la pigmentation et conidies produites) aux colonies ayant servi à
l'inoculation. Lorsque celles-ci étaient identiques, et que les
symptômes aussi étaient identiques à ceux observés
au champ, nous avions conclu à la vérification du postulat de
Koch.
2.2.4 Identification et conservation des
pathogènes
L'identification des isolats ayant satisfait au postulat de
Koch a été faite en se basant sur les structures (mycelia et
conidies), à l'aide de clés dichotomiques et d'ouvrages
d'identification. Deux documents principaux ont été
utilisés. Il s'agit de :
- Cours Internationnal sur l'Identification des Champignon
Agricoles et Evironnementaux (CABI, 2001)
- Genres illustrés des champignons imparfaits (Barnett
et Hunter).
Après identification, les pathogènes ont
été conservés au laboratoire sur silicagel, ou par la
méthode de la cryopréservation (Nakasone et al, 2004)
pour une conservation à long terme (Annexe 3).
Pour les prospections, les isolements, et la
pathogénicité, les proportions des pathogènes, et les
proportions de chaque espèce de pathogène ont été
calculées par zone et ont été représentés
par des digrammes de pie. Les nombres des différentes espèces
collectionnées par zone et par département ont été
présentés sous forme de Tableaux. Les proportions des
pathogènes isolés ont été présentées
sous forme de diagramme de pie, en fonction des zones et des saisons et les
coordonnées géographiques de leurs origines ont été
utilisées pour construire une carte de distribution.
2.3 Etude des caractéristiques physiques des
isolats 2.3.1 Choix des isolats pour l'étude
Afin de réduire le nombre d'isolats pour
l'étude des caractéristiques et les tests de virulence, et pour
répondre aux contraintes de matériel et de temps, une double
sélection a été faite pour réduire les isolats
retrouvés sur I. cylindrica de soixante quatre (64) à
douze (12).
La première sélection qui a tenu compte des
espèces, des périodes de collection (année et saison), et
des coordonnées géographiques, a permis de choisir quarante et un
(41) isolat. Pour la deuxième sélection, les quarante et un (41)
isolats ont été soumis à un test préliminaire sur
de jeunes plantes exactement comme au paragraphe 2.2.3. Ce test
préliminaire a été considéré comme le test
de pathogénicité. Les symptômes obtenus après deux
semaines d'infection ont été évaluées par notation
du pourcentage de symptômes sur chaque feuille inoculée. Les
moyennes de pourcentage de symptôme produit par chaque isolat pour 3
répétitions ont été alors calculées et les
12 isolats qui ont présenté un pourcentage de lésion
supérieur à 3% ont été choisis. Cette limite est
choisie parce qu'à partir des observations au champ et les tests
préliminaires, nous avons constaté qu'une lésion due
à un isolat donné est nettement visible à partir de 3% de
la surface foliaire attaquée. Pour une comparaison des
caractères, quatre (4) autres isolats, de D. gigantea, B.
sacchari, E. longirostatum et E. rostratum,
préalablement utilisés avec succès en formulation
mycoherbicidique à l'Université des Florides (isolats
exogènes)
ont été ajoutés aux 12 isolats
indigènes pour la suite de l'étude. Ces 4 isolats stockés
en tubes sur du PDA, ont été importés des Florides sous
signature de certificat d'importation délivré par le Service de
Protection de Végétaux du Bénin, et de d'accord de
transfert de matériel délivré par l'Université des
Florides.
2.3.2 Aspects et croissance radiale des colonies des
isolats choisis sur Potato Dextrose Agar (PDA)
Des boîtes de PDA ont été
ensemencées en pré-culture avec les isolats
sélectionnés. Après une semaine d'incubation à
25oC à l'obscurité permanente, ces cultures ont servi
à ensemencer les boîtes destinées à l'étude
des aspects physiques et de croissance radiale. L'inoculation a
été faite en utilisant une emporte stérilisée
à l'alcool (96o) et au feu d'un bec bunsen, pour
prélever sous une hotte à flux laminaire, un morceau de culture
(5 mm de diamètre). Le morceau a été déposé
au centre du milieu de culture avec la face mycélienne contre la surface
de ce dernier. Ces morceaux ont été prélevés en
bordure de culture où le mycélium est plus actif, et à un
endroit équidistant du centre de la colonie mère. Quatre (4)
boîtes (répétitions) ont été faites par
isolat. Pendant sept (7) jours d'incubation à 25oC les
variables suivantes ont été mesurées ou observées
chaque jour pour déterminer les différences morphologiques entre
isolats de même espèce et entre espèces.
· La croissance radiale ou diamètre (mm) des
colonies est mesurée à l'aide d'une règle
graduée;
· L'aspect physique des mycélia a été
décrit après observation macroscopique: la
couleur de la colonie et la pigmentation en arrière de
la boîte ont été déterminées
par simple observation, de même il a été
vérifié si la colonie est adhésive ou
aérienne par rapport au milieu de culture. Lorsque la
colonie a présenté des
mycélia aériens, il a été
vérifié si ces mycélia sont abondants, cotonneux
(semblable à du coton), ou floconneux (en petites boules
comme des flocons).
La croissance moyenne par isolat a été
déterminée pour les quatre répétitions de
même que les écarts types. Ceci a permis de faire des courbes
d'évolution de la croissance radiale. Quant à l'aspect physique
des colonies il a été décrit et présenté
sous forme de photo.
2.3.3 Production en masse des spores
Le PDA n'a pas permis une production suffisante (106
spores/ml) de spores pour tous les
isolats. Alors pour étudier les formes et dimensions des
spores, nous avons testé quatre (4) milieux et substrats.
2.3.3.1 Les milieux et substrats
utilisés
- Le V8AGAR a été préparé en prenant
20% v/v de jus deV8 manufacturé auquel ont été
ajouté 2% p/v de la gélose (Agar) et 3g de
carbonate de calcium (CaCO3) pour un litre de milieu de culture (Harigan,
1998). Ce milieu a été distribué dans des boîtes de
15 cm de diamètre après stérilisation pendant 15 mn
à 121 0C à une pression de 1,2 bar.
- Le Bouillon de pomme terre enrichi aux sels minéraux
(spécifique pour la production des spores de C. caudatum) a
été choisi comme milieu liquide. Il a été
préparé en râpant 200g de pomme de terre dans 1 litre d'eau
distillée et en les laissant en solution pendant 1 heure de temps avant
de les faire bouillir (5mn). Après filtration, il a été
ajusté à 1 litre, puis il a été ajouté 20g
de sucrose, 10g de Nitrate de potassium (KNO3), 5g dihydrogénophosphate
de potassium (KH2PO4), 2,5g de sulfate de magnésium (MgSO4), 0,02g de
chlorure de fer (FeCl2) avant que le pH n'ait été ajusté
à 6. La solution ainsi obtenue a été distribuée
dans des erlenmeyer de 250 ml à raison de 100 ml par flacon avant
d'être stérilisé.
- Le substrat à base de rhizome de I.
cylindrica (les tests préliminaires ont montré qu'il produit
facilement les spores de Exserohilum) a été
préparé en immergeant 100g de morceaux (1 cm) dans l'eau toute
une nuit, puis en les stérilisant (121 0C à une
pression de 1,2 bar) dans un erlenmeyer de 500 ml après avoir
versé le liquide d'immersion.
- Le substrat à base de riz (utilisé par le
projet LUBILOSA pour la production en masse des spores de M.
anisopliae) a été préparé de la même
façon que précédemment tout en utilisant des graines de
riz enveloppées de la variété Nerica en place des morceaux
de rhizomes.
2.3.3.2 Inoculation des milieux et substrats
Le V8Agar et le milieu liquide ont été
ensemencés d'un explant (5 mm2) de culture de
champignon (5 jours d'âge). Pour le V8AGAR, l'explant a
été déposé au centre du milieu
de culture et les
boîtes ont été incubées à 25 0C
pendant 15 jours. Les spores sont raclées
à l'aide de l'eau
distillée et le mélange obtenu a été filtré
à l'aide d'un morceau de
mousseline. Pour le milieu liquide, l'explant a
été introduit dans les flacons contenant le milieu, puis ces
flacons ont été soumis à une agitation de 200 tours/mn
à la température ambiante (25 - 28 0C) pendant 15
jours.
Pour inoculer les substrats, nous avions
récupéré les surfaces des cultures sur PDA dans 4 ml d'eau
distillée stérile qui ont permis par la suite d'inoculer les 100g
de substrat. Les flacons sont laissés incubés à la
température ambiante (25 - 28 0C) sur les paillasses au
laboratoire pendant 15 jours mais ils ont été agités
fréquemment pour favoriser une bonne colonisation des substrats. Les
substrats colonisés ont été par la suite suspendus dans
100 ml d'eau pour en extraire les spores produites après filtration.
La concentration des spores en filtrats (nombre de spores/ml)
a été déterminée à l'aide d'un
hématimètre (de type Neubauer (Hawhsley) avec un microscope
à axes gradués de type Leitz qui permet de mesurer les dimensions
des spores. L'hématimètre de NEUBAUER est une lame épaisse
quadrillée. L'intersection du quadrillage donne une configuration de 25
carrés subdivisés en 16 autres petits carrés. Chaque petit
carré à une surface de 1/400mm2 et une profondeur de
0,1 mm. Avant d'introduire la suspension à évaluer, on a
placé la lamelle sur l'hématimètre. Pour respecter la
profondeur de 0,1mm prescrite par le fabriquant il est important que la lamelle
soit correctement adhérée à l'hématimètre
(présence d'empreintes digitales). Une fois la lamelle placée, on
a introduit à l'aide d'une micropipette une goutte de la suspension
entre lame et lamelle. Cette dernière a migré par
capillarité pour occuper l'intersection entre lame et lamelle donc le
quadrillage qui a permis de compter aisément les spores.
Les formes et couleurs des spores (pigmentées ou non)
sont décrites et leur dimensions sont prises sur un échantillon
de 50 spores à l'aide de la graduation des axes du microscope à
un grossissement X 100. Les dimensions sont données en
micromètres en considérant les intervalles entre les minima et
maxima. Pour les conidies ayant de flagelles, les dimensions de ces
dernières sont prises en compte.
2.4 Etude de la virulence des isolats
La virulence des isolats a été
étudiée aussi bien in vitro qu'in vivo. Les
tests in vitro sont plus faciles (conditions d'expérimentation stables)
et ont permis d'avoir rapidement d'information sur les isolats en peu de temps
(6 jours). Cependant pour vérifier si dans le futur nous pourrions nous
baser uniquement sur les tests in vitro pour conclure de la
performance des isolats, il a été
nécessaire de compléter les résultats du test in
vitro par un test in vivo qui prend en compte la plante
entière avec toute sa physiologie.
2.4.1 Préparations des inocula
utilisés
2.4.1.1 Les Suspensions de mycélia
Le mycélium de chaque isolat a été produit
dans des flacons de 250 ml contenant 100ml
du milieu liquide Potato Dextrose Broth (PDB, 24 g/L). La
production a été faite à l'aide d'un agitateur
électrique de type GFL de fabrication allemande à raison de 120
tours/mn pendant 15 jours. Les mycélia produits ont été
filtrés et séchés pendant 4 heures, sous la ventilation
d'une hotte à flux laminaire de type ESCO, Classe II (Singapoure). Ils
ont été ensuite mélangés dans une proportion de 5 g
de mycélium pour 5 g de poudre de kaolin auquel a été
ajouté le filtrat de culture jusqu'à avoir 100 ml de suspension.
Ce mélange a été ensuite enrichi de la gélatine
à 1% (pour assurer l'adhésion des morceaux de mycelium au tissu
végétal) et de Tween 80 à 0,02 % (pour disperser les
morceaux de mycelium) avant d'avoir été broyé à
l'aide d'un moulinex pendant 30 secondes.
2.4.1.2 Les Suspensions de spores
Les spores ont été produites en utilisant les
substrats ou milieux de cultures convenables à
chaque type d'isolat, après les résultats de
l'étude sur la production en masse des spores (paragraphe 2.3.3). Les
suspensions de spores obtenues ont été recueillies dans une
solution de PDB enrichie de la gélatine à 1% et du tween 80
à 0,02%, puis ajusté à 106 spores/ml. à
l'aide de l'hématocimètre.
2.4.2 Virulence in vitro
Nous avons utilisé des boîtes de pétri
stérile, en plastique de 15 cm de diamètre
manufacturées par Fisher Brand, dont
l'intérieur est tapissé de 2 papiers filtre de 15 cm de
diamètre. Avant d'être déposés au fond des
boîtes, ces papiers ont été imbibés de 4 ml d'une
solution de glycérol à 20 % (pour éviter le
dessèchement) et garder pendant longtemps l'humidité dans les
boîtes. Au dessus des papiers filtres ont été
déposées des pièces foliaires (13 cm de long)
prélevées à la partie médiane (largeur
homogène) des feuilles adultes (lignifiées) de I.
cylindrica. Ces pièces ont été déposées
(3 par boîte) de façon que leur surface adaxiale soit visible.
La suspension mycélienne de chaque isolat a
constitué un traitement et chaque traitement a été
répété trois fois (3 boîtes par traitement). La
pulvérisation a été faite à l'aide d'un
pulvérisateur en plastique de 22 ml à raison de 250 litres/ha
(Bateman, 2002) soit 0,4ml (4 pulvérisations) d'inoculum (4
pulvérisations) par boîte de Pétri. Les témoins ont
été pulvérisés uniquement d'une solution de PDB
enrichie de 1 % de gélatine et de 0,02 % de tween seulement. Les
boîtes ont été ensuite incubées sur les paillasses
au laboratoire à une température de 25 - 280C.
Les symptômes ont été
évalués chaque jour pendant 6 jours à l'aide de
l'échelle suivante: 0= 0%, 1= 0-3%, 2 = 3-6%, 3 = 6-12%, 4 = 12-25%, 5 =
25-50%, 6 = 50-75%, 7 = 75- 88%, 8 = 88-94%, 9 =94-97%, 10 = 97-100%. Cette
échelle a été inspirée des images de Clives, 1971
(Pourcentage de symptôme sur feuille de céréale
après une infection causée par Drechslera gigantea).
2.4.3 Virulence in vivo
Le test de virulence in vivo est fait dans des pots
installés dans des cages grillagés (pour éviter la
confusion qui pourrait provenir d'éventuelles attaques d'insectes)
où la température variait entre 24,4oC et
30oC et une humidité relative variant entre 60 et 96% (Figure
3). Les 16 isolats ont été inoculés
séparément sous forme de suspension de mycélium et de
suspension de spores pour comparer les deux méthodes d'inoculation (pour
déterminer la meilleur façon de formuler chaque isolat). Les
traitements ont été appliqués dans un dispositif de bloc
complètement randomisé à quatre
répétitions.



