V. Méthodes microbiologiques
5.1 Méthodes directes (in vivo)
Selon D EMA RQU ILLY et BOISSA U (1978) cité par B
ENCHERCHALI (1994), elle constitue la méthode de
référence. La mesure de la digestibilité se fait sur 4
à 6 béliers, de préférence castrés,
âgé de 2 à 5 ans, en bonne santé et qui
représentent une résistance à la cage de
métabolisme.
5.2 Méthodes indirectes 5.2.1 Digestibilité
in sacco
La méthode in sacco consiste à introduire
des petits sachets de nylon qui ont une grandeur de 10 - 20 centimètres,
une grandeur de pore de 50 um (+/-10) dans le sac ventral de rumen, ces sachets
contiennent environ 5 g de l'aliment. La période d'incubation se fait
à 0, 3, 6, 9, 12, 24, 36, 48 et 72 heures. Après chaque
période d'incubation, les sacs de nylon sont enlevés de rumen et
lavés avec l'eau distillée pour enlever le jus de rumen. Puis
séchés à 65°C pendant 48 heures (PAMUNGKAS et
SEVILLA, 2005).
5.2.2 Digestibilité in vitro
Généralement, les techniques in vitro sont
basées sur la mesure des résidus de fermentation ou les produits
non fermentés après incubation dans le jus de rumen. (GETACHEW
& al, 2004). Parmi les méthodes les plus exactes et
pratiques disponibles celle de TILLEY & TERRY annoncée en 1963
(MABJEESH & al, 2000).
La méthode du gaz test a été aussi
utilisée avec succès pour prédire la digestibilité
d'un aliment. La mesure du gaz produit donne une meilleure estimation de la
valeur nutritive. (GETACHEW & al, 2004)
Chapitre I : Matériel et méthodes
I. Matériel
1.1 les échantillons
Notre échantillon d'étude est constitue de la
pulpe des fruits de l'arganier obtenue de l'échantillon utilisé
par monsieur Kouidri(2008) dans ses travaux de thèse et de feuilles
recueillies à partir de jeunes arbres (4ans) implantées au
service de forêts à CHLEF.
1.2 Appareillage
Au cours de notre expérimentation au laboratoire de
zootechnie et physiologie animale, nous avons utilisé le matériel
mentionné dans le tableau IV :
Tableau IV : Matériel et appareillage
utilisés durant l'expérimentation
Appareils
|
Objectif et utilisation
|
Verrerie.
|
Préparation des solutions, titrage, filtration....
|
Broyeur.
|
Broyage des échantillons.
|
Etuve.
|
Séchage de l'échantillon pour déterminer la
MS
|
Four à moufle.
|
Incinération pour déterminer la MM
|
Balance de précision.
|
La pesée des échantillons à analyser
|
soxhlet.
|
Détermination de la MG.
|
Büchi.
|
Distillation lors de détermination de la MAT.
|
Spectrophotomètre UV-V.
|
Lecture de DO pour déterminer la teneur en ST.
|
Bain marie.
|
Fermentation des échantillons.
|
pH mètre.
|
Ajustement du pH de milieu de LOWE.
|
Plaques résistantes
|
Minéralisation pour convertir l'azote organique en azote
minérale.
|
|
II. Méthodes d'analyses
fourragères
Avant d'effectuer les analyses, les échantillons sont
finement broyés (annexe 01),
et conservés dans des flacons hermétiquement
fermés nettoyés et séchés au
préalable
Tous les dosages sont effectués en triple, et les
résultats sont rapportés par
rapport à 100g de matière sèche (%MS).
2.1 Détermination de la composition
chimique
Les méthodes utilisées sont des méthodes
classiques de l'analyse fourragère (annexe 02).
2.1.1 Dosage de la matière sèche
(MS)
Principe : La teneur en matière sèche par un
double séchage des aliments est déterminée
conventionnellement par le poids de ces aliments après séchage
dans une étuve à circulation d'air.
2.1.2 Dosage des matières minérales
(MM)
Principe : La teneur en MM d'un produit est, son résidu
après destruction de la matière organique par
incinération.
2.1.3 Dosage des matières grasses (MG)
Principe : Les matières grasses des aliments sont
obtenues par extraction directe au moyen d'un solvant, puis élimination
du solvant par distillation et déssication. Pesé du
résidu.
2.1.4 Dosage de la cellulose brute (CB)
Principe : La teneur en cellulose brute d'un aliment est le
résidu insoluble après traitement par un acide puis par une base,
elle est déterminée par la méthode de WEENDE, ce
procédé a été normalisé aux Etats-Unis, et y
utilisé pour établir les tables alimentaires modernes (GAUTIER
& al, 1991).
2.1.5 Dosage des matières azotées totales
(MAT)
Principe : L'azote total est dosé par la méthode
de KJELDAHL : on minéralise le produit par l'acide sulfurique en
présence d'un catalyseur ; l'azote organique est transformé en
azote ammoniacal ; on déplace l'ammoniac par la soude et on le dose
après avoir reçu dans une solution d'acide borique. (Lecoq,
1965).
2.1.6 Dosage des sucres totaux (ST)
Principe : La méthode de DUBOIS et al (1956)
permet de doser les oses en utilisant le phénol et l'acide sulfurique
concentré, en présence de ces deux réactifs, les oses
donnent une couleur jaune-orange dont l'intensité est proportionnelle
à la concentration des glucides, la densité optique est
déterminée entre 450 à 550 nm (NIELSEN, 1997)
2.2 Méthode de prévision par les
équations d'INRA
La prévision de la valeur alimentaire,
particulièrement de la valeur énergétique, des alimentes
des ruminants, a toujours été une préoccupation constante
de tous ceux qui s'intéressaient à l'élevage et à
l'alimentation de ces animaux.
Tenant compte du progrès considérable des
connaissances acquises depuis 1950, sur les besoins des animaux et sur
l'utilisation digestive et métabolique des alimentes, l'INRA proposait
en 1978, de nouveaux système pour exprimer les besoins des animaux et la
valeur nutritive des aliments (UFL, UFV, MAD...).
Après avoir fait le point des connaissances actuelles
sur la composition chimique (constituant glucidiques, azotés, lipidique,
minéraux) des fourrages et alimentes concentrés ou
composés, nous avons utilisé les équations de l'INRA pour
prévoir la valeur énergétique et azotées des sous
produits d'arganier étudiées.
2.3 Méthode de prévision par gaz
test
2.3.1 Méthode de fermentation
La digestibilité des aliments peut être
estimée par les méthodes biologiques connues comme les techniques
in vitro, qui sont conduites hors de l'animal, ces techniques sont
basées sur la mesure des résidus de fermentation.
Les méthodes les plus récentes mesurent les
produits de fermentation anaérobique. La fermentation par jus de rumen a
pour résultat la production d'acides gras volatils, gaz (le dioxyde de
carbone [CO2] et méthane [CH4]) et la masse microbienne. La
quantité de gaz produite pendant l'incubation est mesurée pour
prévoir la digestion de l'aliment. (GETACHEW & al,
2004).
2.3.2 Animaux donneurs de jus
Vue l'absence des animaux donneurs de jus dans la station
expérimentale, nous avons ramené le jus de rumen qu'on a
utilisé pour fermenter la pulpe et les feuilles de la battoire de CH L
EF, dans un thermos pour le conserver à sa température de
sortie.
1er essai, l'animal donneur est un boeuf pesant en moyenne 400 Kg
âgé de 4ans.
2eme essai, l'animal donneur est une vache pesant en moyenne 450
Kg âgée de
4ans.
2.3.3 Solution tampon
La principale fonction de salive est ce d'un lubrifiant pour
aider la mastication et déglutition, et la plupart des solutions tampon
sont basées sur la solution de McDOUGALL reconstitué à
partir des analyses de salive d'ovins (McDOUGALL, 1947), et parmi eux le milieu
de LOWE, proposé par LOWE et al (1956) qui comporte
essentiellement des composants de salive artificielle, solution
résazurine et des traces éléments minéraux.
2.3.4 Mode opératoire
Dans notre expérimentation nous avons utilisé la
méthode de « gaz test », où la fermentation aura lieu
dans un Erlen Meyer Connecté par un tuyau à un flacon rempli
d'eau, et ce dernier connecté à une éprouvette
graduée. La quantité de gaz produite et évacuée est
proportionnelle au volume d'eau évacué dans l'éprouvette
(figure04).
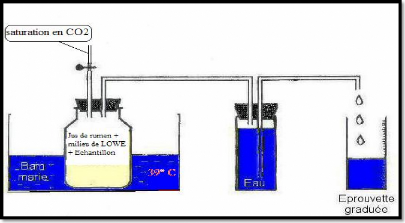
Figure 04 : Dispositif de fermentation.
2.3.4.1 Début d'incubation
Le jus de rumen est mélangé avec le milieu de
LOWE à raison de 1/3 et 2/3 (KHAZAAL, 1995), soit 100 ml jus de rumen et
200 ml de milieu de LOWE plus 500 mg de l'échantillon dans un bain marie
réglé à 39°C. (DEMARQUILLY et JARRIGE, 1981et
BENCHERCHALI., 1999).
On agite le contenu de temps en temps.
Deux séries de mesures sont effectuées, chaque
échantillon est traité en triple, soit six
répétitions, deux blanc (jus de rumen + solution tampon) sont
utilisés simultanément.
La saturation en CO2 est réalisée à l'aide
de la fermentation à la levure de bière (figure05) pour assurer
les conditions d'anaérobiose.
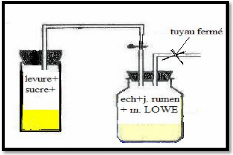
Figure 05 : La saturation en CO2 par la levure
de bière.
2.3.4.2 la lecture
Le gaz produit est lu dans des intervalles de temps : 0-4h, 4-8h,
8-12h, 12-24h, 24-36h, 36-48h, 48-72h., 72-96h.
Chapitre II : Résultats et discussion
I. La composition chimique
Les résultats de l'analyse fourragère des
échantillons étudiés, ainsi que celle de deux fourrages de
comparaison soit un fourrage de qualité: luzerne et un aliment
médiocre: paille sont répertoriés dans le tableau V.
Tableau V: La composition chimique (% de MS) des
sous produits étudiés et deux autres fourrages.
|
Composant Aliment
|
MS
|
MM
|
MG
|
MAT
|
CB
|
ST
|
|
PULPE
|
85.41 %
|
9.44 %
|
8.84 %
|
4.74 %
|
8.85 %
|
15.32 %
|
|
FEUILLE
|
85.56 %
|
8.04 %
|
3.37%
|
12.46 %
|
5.91 %
|
2.30%
|
|
LUZERNE*
|
80 %
|
2.2 %
|
0.7 %
|
16.5 %
|
33.5 %
|
19 %
|
|
PAILLE**
|
93.8 %
|
6.9 %
|
-
|
3.4 %
|
41.70 %
|
-
|
* : JARRIGE et al (1995). ** : NOURA (2001).
1.1 Teneur en MS
Généralement, les éléments
déshydratés présentent une teneur en MS assez importante.
La pulpe et les feuilles se rapprochent dans leur teneur en MS soient 85.41%
pour la pulpe et 85.56% pour les feuilles. Ces résultats sont
légèrement élevés par rapport à ceux obtenus
par CHERROUF, (1998) (80% de MS pour la pulpe).cette différence peut
être expliqué par les conditions de séchage ainsi que les
conditions de culture de nos arganiers.
1.2Teneur en MM
Les analyses ont révélé des compositions
minérales respectives de la pulpe et les feuilles : 9.44 %MS et 8.04 %MS
ces valeurs sont nettement supérieures à celle obtenues par
CHERROUF (1998) (4.1% MS) et DEBBOU & CHOUANA (2003) (2.58% MS) du fait que
une part de nos échantillons proviennent d'arbres cultivés
à MOSTAGANEM pour la pulpe et à CHLEF pour les feuilles où
les sols sont relativement riches en minéraux.
1.3Teneur en MG
La fraction lipidique des aliments concentrés est d'une
importance primordiale puisque leurs valeurs nutritives en dépend et que
son état de conservation peut avoir un effet direct sur
l'appétibilité de ces aliments. La connaissance de cette
composition est donc intéressante.
Selon MORAND-FEHR (1979) la teneur en MG des aliments
concentrés se situent entre 15 et 65g/Kg de MS, mais il existe d'autres
aliments plus riches comme les graines oléagineuses et notre
échantillon de pulpe a une valeur nettement supérieure soit 88.4
g/Kg de MS, cette valeur se rapproche plus ou moins des valeur apporté
par CHERROUF (1998) soit 60g/Kg de MS, mais relativement faible par rapport au
résultat de DEBBOU & CHOUANA (2003) soit 31,20%MS.
Nos résultats révèlent que les feuilles
sont trois fois moins riche que la pulpe en MG soit de 3.37% MS à ce
moment les feuilles ne peuvent pas être considérées comme
une source lipidique en alimentation animale bien quelles soient plus riches
que la luzerne (0.7 %MS) (JARRIGE & al, 1995).
1.4Teneur en ST
Nos résultats n'appellent pas de commentaires
particuliers, comparés aux résultats de CHERROUF (1998) la teneur
en sucre de la pulpe est assez proche soit 15.32%MS contre 18.5%MS, alors que
par rapport aux résultats de DEBBOU & CHOUANA (2003) on se trouve
avec des valeurs trois fois plus élevée (49.83%MS),
Les feuilles présentent une valeur faible
comparée à la pulpe, cette différence peut être
expliquée par l'état physiologique de es feuilles
prélevées d'arbres très jeunes en début de leur
développement.
On constate que la pulpe présente une valeur comparable
à celle de la luzerne (1 9%MS).
1.5Teneur en CB
Contrairement a ce qu'a été observé pour
les composants précédents on distingue une faible teneur en CB
soit 8.85%MS par rapport au résultat de CHERROUF (1998) qui est de
l'ordre de 12.9% MS et celle obtenue par DEBBOU & CHOUANA (2003), 10.94%MS.
Cette différence pourrait s'expliquer par l'état de la
maturité de la pulpe et le moment de récolte des fruits.
La faible valeur en CB des feuilles (5.91 %MS) pourrait avoir
les mêmes raisons que
pour la faible teneur en ST ; Comparé
à la luzerne et aux pailles qui ont respectivement
les valeurs de 33.5%MS et de 41%MS, les sous produits de
l'arganier sont considérés comme des aliments très riches
en éléments solubles et pauvres en CB.
1.6Teneur en MAT
L'apport d'azote dans les sous produits de l'arganier
étudié est considérablement variable, plus
élevé dans les feuilles (12.46 % MS) et faible dans la pulpe
(4.74 %MS), ce dernier résultat concorde avec celui obtenu par CHERROUF
(1998) (5.9%MS) ainsi que celui DEBBOU.B & CHOUANA.T (2003) (5.35%MS).
De point de vue valeur azotée les feuilles de
l'arganier se rapprochent à la luzerne (1 6.5%MS), elles sont donc
considérés comme une source d'azote non négligeable pour
les ruminants des zones sahariennes où les fourrages de qualité
font défaut et compléter ainsi des rations à base de
paille qui n'apportent que de faibles quantités en azote soit 3.4%MS.
La pulpe est moins riche que les feuilles en azote et selon
JARRIGE & al (1995) de très nombreuses protéines se
trouvent au niveau de feuilles dont la plupart ayant des activités
enzymatiques, les chloroplastes à eux seuls contiennent plus de la
moitié des protéines foliaires en plus des protéines
membranaires.
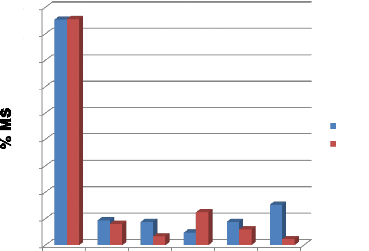
Pour une étude comparative entre la composition chimique
des feuilles et celle de la pulpe, les résultats sont
représentés sous forme d'histogrammes (figure N°06)
MS MM MG MAT CB ST
40
90
80
70
60
50
30
20
10
0
PULPE FEUILLE
Figure 06 : comparaison de la composition
chimique des sous produits étudiés.
De point de vue valeur alimentaire, nous constatons que la
pulpe est une source énergétique assez intéressante vue sa
richesse en MG et en ST comparé aux feuilles qui apportent une
quantité considérable en MAT ; l'idéal serait que les
animaux consomment les deux produits en même temps pour en faire une
ration complète.
Dans le cas du développement de l'extraction de l'huile
d'argan la pulpe pourrait être utilise comme concentré pour
compléter les rations pauvres en produits rapidement fermentescibles.
II. Prévision de la valeur alimentaire des sous
produits de
l'arganier à partir de la composition
chimique
2.1 Les équations de prévision pour la
pulpe
2.1.1 Valeur énergétique
Vue la difficulté de la détermination de la
digestibilité et de la valeur nutritive due à la faible
quantité d'échantillon disponible nous avons jugé
intéressant d'utiliser les équations de prévision de l
'INRA en utilisant les résultats de l'analyse fourragère, en
effet la valeur énergétique ou azotée d'un aliment
dépend avant tous de sa composition chimique et particulièrement
sa teneur en MAT.
Les équations que nous avons utilisées sont le
fruit d'un très grand nombre de travaux (JARRIGE, 1980 et MORRISON
(1976), le choix de ces équations ne rencontre aucun inconvénient
vue la faible teneur en CB (SAUVANT, 1981).
dMO = 91,7 - 1,48 CB. R=0,95
UFL = 121,80 + 0,11 MAT - 1,81 CB + 1 ,26MG.
UFV= 124,15 + 0,06 MAT - 2,20 CB + 1,22 MG.
En remplaçant dans les équations chaque
paramètre par une moyenne rapportée à 100g de MO, les
résultats sont répertoriées dan le tableau VI.
Tableau VI : Valeur énergétique de
la pulpe
|
MG%MO
|
MAT%MO
|
CB%MO
|
dMO
|
UFL
|
UFV
|
|
9.37%
|
5.02%
|
9.38%
|
77.82%
|
0,93
|
0,92
|
Comparé aux différents aliments
concentrés dont la valeur énergétique varie de 1,17
à 0,16 pour les UFL et de 1,26 à 0,07 pour les UFV la pulpe est
considérée comme un aliment de qualité ayant 0,93 UFL et
0,92 UFV.
En vue de développement de la production de l'huile
d'argan il serait intéressant d'utiliser ce sous produit comme aliment
pour toute type de productions.
2.1.2Valeur azotée
Nous avons fait de même pour la prévision de la
valeur azotée de la pulpe, on utilisant les équations (VERITE et
SAUVANT, 1981).
MAD1= 0,914 MAT (g/kg / MO)
MAD2= 0,917 MAT - 0,055 CB (g/kg / MO)
Tableau VII : la valeur azotée de la
pulpe
|
MG%MO
|
MAT%MO
|
CB%MO
|
MAD1
|
MAD2
|
|
9.37%
|
5.02%
|
9.38%
|
4.71
|
4.09
|
Les résultats obtenus n'appellent pas de commentaire
particulier car comme pour tous les aliments lorsque la teneur en MAT est
faible la quantité en MAD l'est aussi, nous constatons une
légère surestimation lorsque les équations n'utilisent pas
la CB.
La pulpe seule ne peut être considérée comme
un apport d'azote.
2.2Les équations de prévision pour les
feuilles
2.2.1valeur énergétique
Pour prédire la valeur énergétique des
feuilles des équations de prévision de
|
l'INRA (JARRIGE et al, 1981) sont utilisés,
|
|
|
dMO = 0.717+0.001222 MAT-0.000748 CB.
|
R=0,833
|
|
UFL = 0.840 + 0.001 330 MAT - 0.000832 CB.
|
R=0,833
|
|
UFV= 0.762 + 0.001443 MAT - 0.000946 CB.
|
R=0,848
|
En remplaçant, chacun des paramètres de
l'équation par les valeurs moyennes trouvées, les
résultats sont répertoriés dans le tableau IIX.
Tableau IIX : Valeur énergétique
des feuilles
|
MG%MO
|
MAT%MO
|
CB%MO
|
dMO
|
UFL
|
UFV
|
|
3.62%
|
13.39%
|
6.35%
|
72%
|
0,85
|
0,77
|
La majorité des foins ont une valeur
énergétique située entre 1,03 à 0,16 pour les UFL
et de 0,99 à 0,16 pour les UFV donc les feuilles peuvent être
considérées comme un bon foin ayant 0,85 UFL et 0,77 UFV.
La richesse des feuilles en MAT et leur faible teneur en CB
explique la valeur élevée de la dMO (0.72%), cette valeur est
comparable à celles des fourrages de qualité.
Grâce à sa teneur élevé en UFL, les
feuilles peuvent être utilisées en alimentation des ruminants en
vue de la production laitière dans les régions où pousse
l'arganier. 2.2.2 Valeur azotée
Pour la prévision de la valeur azotée des feuilles,
nous avons utilisé l'équation suivante :
MAD = 0,742 MAT. (JARRIGE et al, 1981)
Tableau IX : la valeur azotée
prédite des feuilles
Ce résultat n'appelle pas de commentaires particulier
car il est naturel que la quantité en MAD des feuilles soit
élevée soit environ 10g/kg de MO vue leur teneur en MAT qui est
supérieur à 13% MO.
Comparée aux valeurs de la table INRA (1988) les
feuilles ont la même valeur azotée que la plupart des
légumineuses, à cet effet les feuilles de l'arganier peuvent
êtres considérer comme une source d'azotée compensant ainsi
la rareté des fourrages de qualité dans les zones
désertiques.
III. Résultats de la fermentation par " gaz test
"
Les résultats bruts du gaz test sont
représentés en annexe (02), le tableau X présente la
production moyenne de gaz de 500mg d'échantillon.
Tableau X: Résultats de la fermentation
des échantillons [volume de gaz produit (en ml) pendant des
intervalles de temps].
|
Temps
|
0 - 4
|
4 -8
|
8 - 12
|
12 - 24
|
24 - 36
|
36 - 48
|
48 - 72
|
72 - 96
|
|
h
|
h
|
h
|
h
|
h
|
h
|
h
|
h
|
|
Ech
|
|
|
|
|
|
|
|
|
|
Pulpe
|
136,83
|
139
|
98,66
|
115,5
|
67,5
|
42,33
|
31,33
|
5,16
|
|
Feuille
|
146,83
|
147,33
|
89,5
|
121,33
|
90,16
|
70,83
|
42
|
14,83
|
|
Blanc
|
76,5
|
84
|
82
|
79
|
43
|
27.5
|
10
|
00
|
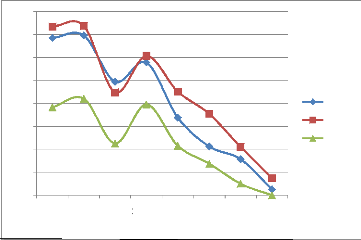
L'évolution de la cinétique de la production de gaz
durant la fermentation des échantillons est représentée
par la figure (07).
Partie pratique Chapitre II : résultats et
discussion
160
140
120
100
80
40
60
20
0
0 -4 04_08 8 -12
h
12 -24
h
24 -36
h
36 -48
h
48 -72
h
72 -96
h
Pulpe Feuille Blanc
Figure 07: Evolution de la production du gaz
pendant l'incubation de la pulpe et des feuilles de l'arganier.
La figure montre une production importante de gaz pendant les
premières heures d'incubation (140 à 150 ml), ceci est due en
grande partie à la composition de jus utilisé pour la
fermentation, qui atteint à lui seul environ 80ml, ce dernier doit
être très riche en produits solubles (concentré) rapidement
fermentescibles, ce qui nous a amené à faire une correction en
considérant que le blanc ne produit que très peu ou pas de gaz au
cours de l'incubation, les résultats après correction et en
comparaison avec deux aliments de valeurs nutritives très distinctes
sont représentés dans la figure 08.
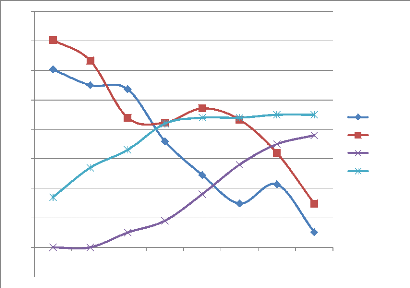
-10
40
70
60
50
30
20
10
0
0-4h 4 -8h 8 -12 h 12 -24 h24 -36 h36 -48 h48 -72 h72 -96 h
Pulpe Feuille- paille luzerne
Figure 08 : Evolution de la production de gaz
des produits de l'arganier après correction.
La dégradation des aliments dans le rumen s'accompagne
d'une importante production de gaz, le CO2 (60 à 70 %) qui provient des
bicarbonates apportées par la salive et de nombreux processus de
fermentation, et du CH4 (25 à 35%) qui provient de la réduction
du CO2 par l'hydrogène avec toutefois de fortes variations (JARRIGE,
1980 & JOUANY & al (1995).
Les résultats de NOURA(2001) pour les pailles et de
GETACHEW & al (2004) pour le foin de luzerne montrent que
l'évolution de la production de gaz suit une progression linéaire
où les courbes représentent trois parties distinctes :
-Une partie de démarrage où les valeurs
initiales sont relativement faibles bien que la luzerne démarre avec une
production de 27 ml par rapport à une valeur relativement nulle pour les
pailles;
-Après un séjour en contact de la flore
ruminale, la production augmente progressivement jusqu'à une valeur
optimale ; atteinte après 12h pour le foin de luzerne et 48h pour la
paille;
-La production de gaz devient stationnaire et forme un
plateau.
Pour l'évolution de la production de gaz de nos
échantillons, nous observons une allure tout à fait
différente, où on distingue quartes parties:
Fraction A : son intervalle se situe entre 0
et 8h pour la pulpe alors que pour les feuilles c'est entre 0 à 12h, la
production de gaz démarre avec une production maximale puis diminue, la
fermentation des feuilles est plus importante (70ml) par rapport
à celle de la pulpe (60ml), cela peut être
argumenté par la présence des éléments rapidement
fermentescibles (ST, MG et MAT) par rapport à la paille et le foin de
luzerne, la différence entre les feuilles et la pulpe peut être
expliquée par la teneur élevée en MAT des feuilles.
Fraction B : limitée entre 8 -12h, se
caractérise par une production constante alors que pour les feuilles,
l'évolution se stabilise entre 12 et 24h. Cet état peut
être expliqué par la résistance des particules insolubles
à l'attaque microbienne et le temps d'adhésion sur les parois.
Fraction C : cette troisième partie se
limite dans l'intervalle de [12 _ 48h] pour la pulpe où on observe une
diminution très nette de la production de gaz, ce qui reflète
l'activité microbienne qui devient de plus en plus faible en
conséquence de l'épuisement rapide de la MO ; pour les feuilles
l'intervalle se situe entre [12 _ 36h] et contrairement à la pulpe on
observe un rebondissement de la courbe due à sa richesse en azote.
Fraction D : à partir de 36h, on
constate une diminution progressive du volume de gaz produit, expliquée
également par la diminution de l'activité microbienne et la
solubilisation complète de la MO contenues dans les feuilles;
La pulpe, riche en MG et en CB, permet durant cette phase une
augmentation de la production de gaz qui dure environ 12h, suivie d'une
diminution ayant les mêmes raisons que pour les feuilles.
Par comparaison de la cinétique de production de gaz
entre nos échantillons et celle de la paille ou de foin de luzerne, la
différence réside dans le temps de latence très important
pour ces derniers soient respectivement plus de 48h et plus de 12h. Cette
différence s'explique par la teneur de ces derniers en CB soit
respectivement 41 .7%MS 33.5%MS contre 8.85%MS et 5.91%MS pour la pulpe et les
feuilles ; en effet la teneur en CB conditionne la vitesse de la production de
gaz et la fermentation des produits solubles.
| 


