2.2. Le ciblage
Si les nano vecteurs « furtifs » permettent
l'extravasation sélective au niveau tumoral, ils nécessitent
néanmoins, dans certains cas, d'être équipés de
ligands capables de reconnaître des récepteurs spécifiques
afin de pouvoir délivrer les médicaments qu'ils transportent
à l'intérieur de la cellule cible. À titre d'exemple,
citons [16] :
? Des Ligands de cellules tumorales
différentielles ciblés par des anticorps anti HER2 (Herceptin
®) et anti-CD20 (Mabthera ®) couplé à des
NP.
University of Geneva, University of Lausanne
Switzerland 2007 [18].
Dans cette étude ,295 anticorps monoclonaux (mAb)
anti-HER2 et 557 anti-CD20, respectivement, ont été couplé
de manière covalente avec des NP (250 nm). L'interaction
spécifique entre des cellules tumorales et mAb-NP a été
déterminée par microscopie confocale en utilisant deux
lignées cellulaires: SKOV-3 cellules
cancéreuses ovariennes humaines
(surexprimant HER2)
et Daudi les cellules de lymphomes surexprimant (CD20). Les résultats
ont montré le ciblage sélectif de mAb-NP aux cellules tumorales
surexprimant l'antigène spécifique. Les (anti-HER2 NP)
étaient internalisé efficacement. En outre, on a montré
une localisation cellulaire différente des NP en fonction du type
d'interaction anticorps antigène impliqué (Fig24).

41
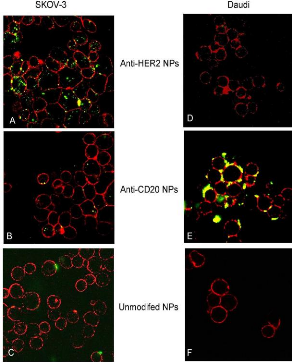
Figure 24: Specific interaction of mAb-NPs in
SKOV-3 and Daudi cells studied by confocal laser scanning microscopy (objectif:
63×). Cell membranes were stained in red with Concanavalin A
AlexaFluor® 594 conjugate, whereas NPs were stained in green with DiO. The
cells were incubated with 1mg/ml mAb labeled NPs or non-conjugated NPs at 37 ?C
for 6 h. (A and D) Anti-HER2 NPs; (B and E) anti-CD20 NPs; (C and F) unmodified
NPs. Note: In (A) the clear distinction of red membranes and green
anti-HER2 NPs, since the latter are internalized and therefore dissociated from
the cell membrane, while in (E) the binding of anti-CD20 NPs to the cell
membrane leads to the superposition of green and red fluorescence and
appearance in yellow.
Chapitre III Essais
Précliniques
? Des NP de poly (lactide-co-glycolide)
décoré de Folate-vitamine E (TPGS) pour la
livraison ciblée de Doxorubicine. National
University of Singapore 2007 [19].
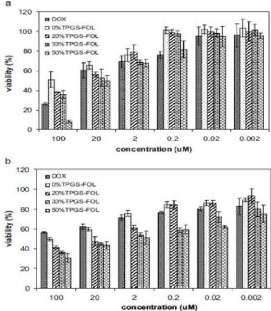
Figure 25: (a) MCF-7 and (b) C6 cancer cell
viability of DOX in free form or formulated in the 0% , 20%,33% and 50%
TPGS-FOL NPs (n 1/4 6).
Dans cette étude, des NP conjugué à la
DOX et le poly (lactide-coglycolide) et vitamine E TPGS (DOX-PLGA-TPGS)
conjugué ont été synthétisé par
l'équipe de Z. Zhang pour cibler des tumeurs riches ayant comme
récepteur surexprimé le folate. Les NP (350nm) ont montré
un effet significatif in vitro sur les MCF-7 (les cellules du cancer du sein)
et (des cellules tumorales du cerveauC6), ce qui a entraîné une
cytotoxicité supérieure et une meilleure absorption cellulaire en
comparaison avec la DOX libre. Les résultats impliquent que les NP
décorés en folate (TPGS-FOL et DOX-PLGATPGS) pourraient avoir un
grand potentiel pour l'utilisation des chimiothérapies
ciblées (Fig25).


42
Figure 26: Confocal laser scanning microscopy
(CLSM) of C6 cancer cells incubated with DOX (a) in free form, or formulated
(b) in the NPs of noTPGS-FOL component in the blend matrix (i.e., the 0%
TPGS-FOL NPs) or (c) in the 50% TPGS-FOL NPs for 3 h at 37 1C.
Chapitre III Essais
Précliniques

43
? Cytotoxicité accrue des PEG-liposomes
chargés en Doxorubicine et modifiés
par des anticorps monoclonaux 2C5 in vitro.
Northeastern University USA 2007 [20].
L'équipe d'A. Elbayoumi a lié des Liposomes
pegylé chargé en Doxorubicine (Doxil) avec l'anticorps monoclonal
2C5 nucléosome spécifique (mAb 2C5) pour la reconnaissance d'une
large variété de cellules tumorales par les nucléosomes
liés à la surface des cellules. Ils ont démontré
une augmentation de la liaison in vitro et l'intériorisation
par plusieurs lignées de cellules cancéreuses (murine LLC, 4T1, 6
et humaines BT-20, MCF-7 et PC3), par cytométrie en flux (FACS) et la
microscopie confocale. En conséquence, L'internalisation
spécifique de l'anticorps monoclonal 2C5-Doxil TM dans le cytosol, ainsi
que la localisation nucléaire de la charge de médicament,
à l'intérieur des cellules cancéreuses a donné une
cytotoxicité nettement plus élevé, y compris celles
résistantes à la DOX (Fig27).

Figure 27: In vitro cytotoxicity
results using different cancer cell lines. Upper panels -cytoxic effect of
different concentrations of IgG-DoxilTM () and mAb 2C5-DoxilTM () on cancer
cells; lower panels - cytotoxicity of various preparations at the fixed
concentration of IgG-DoxilTM and 2C5-DoxilTM (as 100ug/ml free doxorubicin) and
same concentration of 2C5-liposomes (as lipid). 4T1 murine cell line, I; murine
6 cell line, II; and human PC3 cell line, III.
Chapitre III Essais
Précliniques

44
? Administration ciblée de Paclitaxel en utilisant
des NP de poly (lactide)
décorées de folate vitaminE (TPGS).
Feng National University of Singapore 2008 [21].
L'équipe de J. Pan a synthétisé des NP de
copolymères pour la chimiothérapie ciblée avec le
Paclitaxel conjugué au folate pour le ciblage. L'efficacité
d'encapsulation de médicaments et la libération du
médicament in vitro ont été mesurées par
une chromatographie en phase liquide de haute performance (HPLC).la formulation
NP a un grand avantage par rapport au PA libre à atteindre un meilleur
effet thérapeutique, qui a augmenté de 8,68% pour les
MCF-7cellules, le ciblage par les folates peut favoriser
considérablement la délivrance du médicament dans les
cellules cancéreuses correspondantes et renforcer ainsi son effet
thérapeutique (Fig28).
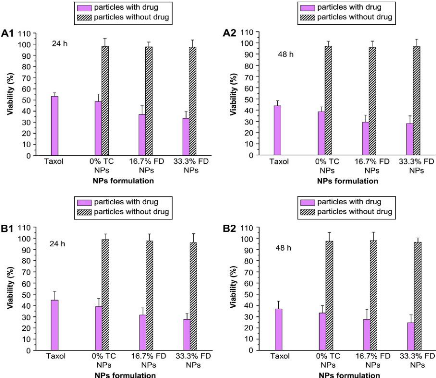
Figure 28: In vitro viability of (A)
MCF-7 and (B) C6 cells after 24 h (A1, B1) or 48 h (A2, B2) treatment of
paclitaxel formulated in the 0% TC NPs, 16.7% FD NPs,33.3% FD NPs or in its
current clinical dosage form Taxol® at the
same 25 mg/ml drug concentration at 37 °C (n 1/4 6).
Chapitre III Essais
Précliniques
? L'Efficacité de micelles
chargées de Doxorubicine ciblé par des
galactopeptides
contre les hépatomes. Chinese Academy of
Sciences 2013 [22].
Des micelles de Polymères portant un groupe galactosyl
sont utilisées par l'équipe de J Ding pour l'administration
ciblée de DOX aux cellules d'hépatome (HepG2 et SMMC7721) avec
récepteur asialoglycoprotéine (ASGP-R) qui sera comparé
avec des NP pégylées et DOX libre:
? In vitro, la libération de DOX s'est
accélérée grâce à la reconnaissance entre le
ligand galactose et les cellules ASGP-R de HepG2, l'endocytose des NP a
été considérablement favorisé, ce qui a
été démontré par microscopie confocale et la
cytométrie en flux.
? In vivo, en utilisant un HepG2 modèle de
xénogreffe de souris nude .Le volume de la tumeur et le poids corporel
ont été contrôlée sur une période de
traitement de 11 jours, les NP galactosylées étaient les plus
efficaces pour supprimer la croissance de la tumeur par rapport à la DOX
libre et NP pégylées. L'efficacité antitumorale
inférieure des NP pégylées était probablement
attribuée à sa mauvaise absorption cellulaire par les cellules
HepG2, indiquant la
nécessité d'introduire le ligand de ciblage
(Fig29).


45
Figure 29: Antitumor efficacies in vivo
(A) and body weight changes (B) of HepG2 human hepatoma xenografted female
BALB/c nude mice treated with PBS (a), free DOX (b), and nanomedicines from
PMLG7-b-PLGA22 (c) and PGLG7-b-PLGA22 (d). Each formulation was administered on
days 0, 3, 6 and 9 by tail-vein injection with a dosage of2.0 mg DOX per kg
body weight for injection of free DOX and nanomedicines. Data were presented as
mean#177;standard deviation (n=6) (*pb0.001).
Chapitre III Essais
Précliniques

46
La principale difficulté d'application du ciblage actif
réside dans la relative rareté de ligands spécifiques,
Afin de contourner cette limitation, l'équipe de Kohane propose une
nouvelle idée innovante et assez pertinente en sortant du principe
générale du ciblage par contradiction [16].
? Le ciblage des NP par la lumière. MIT &
Harvard Medical School 2010 [23].
Les auteurs de cette publication ont pu recouvrir les
nanoparticules non pas par des molécules ciblant spécifiquement
un type de cellules mais au contraire par des peptides qui permettent
l'accrochage des nanoparticules sur un grand nombre de types dans un premier
temps et à inhiber l'interaction de ce peptide, puis à le rendre
actif seulement dans la zone à traiter.
Cette stratégie a été validée in
vitro en fonctionnalisant des nanoparticules commerciales par le peptide (des
acides aminés : GGGGYIGSR Alors que YIGSR est connu pour interagir avec
les intégrines ß 1 présentes sur la quasi-totalité
des types cellulaires, le greffage du4,5-diméthoxy-2-nitrobenzyl (DMNB)
sur ce peptide inactive sa capacité à adhérer sur
l'intégrine Ainsi l'illumination de cellules en présence des
particules couvertes par le peptide inactif favorise l'accrochage des
nanoparticules sur les cellules en raison du départ du groupement
inhibiteur DMNB induit par les photons UV .
L'équipe de Kohane a donc réussi à
développer une stratégie permettant un ciblage actif et
spécifique commandé par la lumière. En raison de son
caractère universel cette preuve de concept obtenue par des
expériences in vitro mérite d'être validée
in vivo. Ainsi pour Atteindre un tel objectif nécessite
l'utilisation de fibres optiques pour acheminer la lumière dans la zone
à traiter (Fig30).

Figure 30: The photo-targeted nanoparticle
concept. A non-specific ligand on the surface of the nanoparticles is caged,
rendering it non-functional. Upon illumination, the caging group is released,
the ligand is activated and the nanoparticle can bind to the illuminated
tissue. The lower portion of the figure shows the chemistry of the targeting
moiety as it relates to the events schematized above. The GGGGYIGSR-NH2 peptide
is caged on tyrosine with a 4, 5-dimethoxy-2-nitrobenzyl group (DMNB, Blue).
After illumination the caging group is released and the targeter becomes
active.
Chapitre III Essais
Précliniques
| 


