Il apparait clair, après une simple lecture du
tableau, que les meilleurs rendements ont été obtenus pour
l'ensemble des échantillons incubés pour une durée de 8h
et ceci quelque soit la nature du solvant utilisé.
Les rendements obtenus pour les échantillons
incubés pendant 4h varient de 3,411% à 15,804%, alors que ceux
ayant subi une extraction qui a durée 8h, ils varient de 3,696 %
à 18,744% (figure18) V.2.1.2.Influence du type de solvant
:
Les PP sont une famille de composé très vaste,
regroupant de substances de solubilité très
hétérogène. En se référant à la
méthode d'Akowauh et al., 2005, on a utilisé dans notre
expérimentation cinq solvants de polarité décroissante:
l'Eau, le Méthanol 50%, l'Acétone 70%, le Méthanol pure et
le Chloroforme.
Il ressort de l'étude du tableau10 que les meilleurs
rendements sont obtenus respectivement pour les trois solvants; Eau (18,744%),
Méthanol 50% (14,33) et l'Acétone 70% (11,65%).
Les plus faibles rendements sont observés pour le
méthanol pur (9,804 %) et le chloroforme (3,696%).
Ces résultats (figure18) peuvent êtres
expliquées par la solubilité différentielle des
différents composées phénoliques ou les PP polaires sont
solubles dans les solvants polaires et les PP apolaires sont solubles dans les
solvants apolaires.
La lecture des rendements d'extraction permet de constater que
les plus grands rendements ont été obtenus avec les solvants
polaires (Eau, Méthanol 50% et l'Acétone 70%).
De ces résultats, on peu en conclure que notre plante
d'étude Centaurea microcarpa Coss et Dur. contient beaucoup
plus de PP polaires qu'apolaires, ceci peut ~tre confirmé par des
dosages dosages ultérieurs.
20
18
16
14
12
10
8
4
0
6
2
3,411
chloroforme methanol pure acétone 70% methanol 50% eau
3,696
8,04
9,804
9,751
4h 8h
11,65
11,776
14,33
15,804
18,744
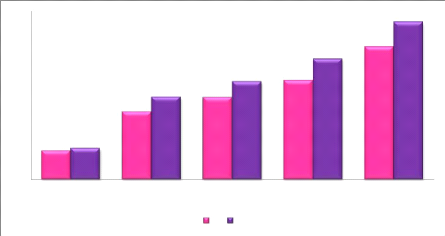
Figure18 : Rendements d'extraction en fonction
du type de solvant et du temps d'extraction des
parties aériennes de Centaurea microcarpa Coss
et Dur.
V.2.2. Méthode d'extraction d'Owen et Johns
(1999) :
Le tableau12 donne le rendement EPB, exprimé en
pourcentage de la matière sèche (%ms), obtenu avec la
méthode d'Owen et Johns (1999).
Tableau 12 : Rendement de l'extrait
méthanolique.
Partie de la plante Solvant Temps d'extraction
Température Rendement (% ms)
(h)
Partie aérienne Méthanol pur 168 Ambiante 21
L'extraction solide-liquide utilisée et l'état
physique de la plante, réduite en poudre, à permis au solvant,
méthanol pure de franchir la barrière de l'interface
solide-liquide, dissoudre le principe actif a l'intérieur du solide
(matière végétale) et ressortir le soluté
(Matière organique) du solide. La plupart des auteurs
suggèrent que l'entrée du solvant se fait par un mécanisme
osmotique et la sortie du soluté par dialyse ou par diffusion.
Le solvant utilisé, le méthanol pur (99%),
donne généralement de meilleurs rendements d'extraction et de ce
fait il est très utilisées par rapport aux solvants, et le plus
efficace (CastanedaOvando et al., 2009).
On peut dire que les résultats des deux
méthodes montrent que le rendement de l'extraction de la deuxième
méthode, celle d'Owens et Johns (1999), avec le méthanol pure
(21%) est plus élevé que celui obtenus avec la première
méthode, celle d'Akowuah et al., 2005, utilisant plusieurs solvants
(cinq solvants de polarités différentes), pour une durée
d'extraction de 8h, ou le plus grand rendement n'a pas dépassé
les 18,744%.
Ceci peut être expliqué par :
· Nature du solvant d'extraction : méthanol pur.
· Temps d'extraction : 1 semaine (168 heures).
· Le rapport masse/solvant : 200 mg / 500 ml de solvant.
· Condition d'extraction : agitation continue qui permet
une meilleure infiltration du solvant.
En terme général, l'extraction des
composés phénoliques à partir de la matière
végétale dépend de leur structure chimique, du type de
solvant utilisé, de la méthode d'extraction de la
granulométrie et du temps de macération. Les extraits
phénoliques des plantes sont généralement des
mélanges des différentes classes de composés
phénoliques qui sont solubles dans le solvant utilisé. La
solubilité de ces derniers dépend du type de solvant
utilisé (polarité) et de leur degré de
polymérisation.



