2.4. Capacité d'adsorption
La capacité d'adsorption d'un adsorbant est
définie comme étant la quantité de substrat (masse ou
volume) adsorbée par unité de masse d'adsorbant pour une
température donnée. Elle nécessite la prise en compte de
nombreux paramètres aussi bien pour l'adsorbat (taille des
molécules, solubilité dans l'eau, etc.) que pour l'adsorbant
(surface spécifique, structure et type de particules, le constituant,
etc.). Elle est exprimée par la relation suivante (Benmakhlouf et
Bouiche, 2015) :
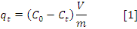
Avec :
V : Volume de la solution (L) ;
m : Masse de l'adsorbant (g) ;
C0 : Concentration initiale de la solution
(mg.L-1) ;
Ct: Concentration résiduelle de la solution
à l'instant t (mg.L-1).
2.5. Cinétique d'adsorption
2.1.1.
Définition
La cinétique d'adsorption est le second
paramètre indicateur de la performance épuratoire d'un adsorbant.
Elle permet d'estimer la quantité de polluants adsorbée en
fonction du temps. La cinétique fournit des informations relatives au
mécanisme d'adsorption et sur le mode de transfert des particules du
soluté de la phase liquide à la phase solide (Ben Haoued,
2017).
Les vitesses d'adsorption sont beaucoup plus faibles en phase
liquide qu'en phase gazeuse. Cette cinétique, relativement lente, se
traduit par des délais assez importants pour atteindre
l'équilibre d'adsorption.
2.1.2. Modèles de la cinétique
d'adsorption
La cinétique d'adsorption d'un matériau peut
être modélisée. A cet effet, la littérature rapporte
un certain nombre de modèles tels que le modèle de Lagergren
(modèle de pseudo-premier ordre), le modèle cinétique de
pseudo-second ordre et le modèle de diffusion intra particulaire
(BenHaoued, 2017).
2.1.2.1. Modèle de pseudo-premier
ordre
Il a été supposé dans ce modèle
que la vitesse d'adsorption à l'instant t est proportionnelle à
la différence entre la quantité adsorbée à
l'équilibre qe et la quantité qt
adsorbée à cet instant et que l'adsorption est
réversible. La constante de vitesse d'adsorption du premier ordre est
déduite à partir du modèle exprimé par
l'équation de Langergren:
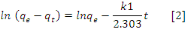
Avec :
qt : est la quantité du colorant
adsorbée (mg/g) à l'instant t,
qe : la capacité d'adsorption à
l'équilibre (mg/g).
t : temps de contact (min)
k1: constante de vitesse
d'adsorption pour le premier ordre (min-1)
2.1.2.2. Modèle de la cinétique du
pseudo- second ordre
L'équation du pseudo-second ordre est souvent
utilisée avec succès pour décrire la cinétique de
la réaction de fixation des polluants sur l'adsorbant. Le modèle
du pseudo-second ordre permet de caractériser la cinétique
d'adsorption en prenant en compte à la fois le cas d'une fixation rapide
des solutés sur les sites les plus réactifs et celui d'une
fixation lente sur les sites d'énergie faible. Ce modèle est
donné par l'équation suivante :
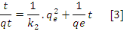
Avec :
k2: constante de vitesse d'adsorption pour le
pseudo-second ordre (g.mol-1.min-1).
qe : quantité d'adsorbât à
l'équilibre par gramme d'adsorbant (mg/g).
qt : la quantité du colorant adsorbée (mg/g)
à l'instant t,
1/qe : la pente de la droite de régression
linéaire.
| 


