II.1.3 Classification des alcaloïdes suivant leur
biogenèse
Du point de vue biogénétique et selon Hegmauer,
il existe trois classes d'alcaloïdes: les alcaloïdes vrais, les
protoalcaloïdes et les pseudoalcaloïdes (Milcent, 2003).
Les alcaloïdes vrais, qui
représentent le plus grand nombre, ont un large spectre
d'activité biologique et sont très basiques. Leur basicité
est due à un atome d'azote contenu dans un hétérocycle
(Milcent, 2003); leur biosynthèse s'effectue à partir des acides
aminés tel que la L-lysine, la L-ornitine, la L-tryptophane, la
L-tyrosine, la L-phénylalanine, la L-histidine (Aniszewski, 2007). Ils
sont sous forme de sels de divers acides dans la plante. Le représentant
simple de cette classe est la pyrrolidine 51 (Milcent,
2003).
N
H
51
la pyrrolidine
Les protoalcaloïdes sont des
alcaloïdes dont l'atome d'azote ne fait pas partie de
l'hétérocycle. Ils dérivent aussi des acides aminés
et sont souvent appelés « alcaloïdes biologiques ». Ils
sont solubles dans l'eau. C'est le cas de la mescaline 52
(Milcent, 2003).
OMe
52
Mescaline
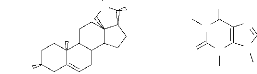
Les pseudoalcaloïdes ne dérivent
pas d'acides aminés. Ils sont pour la plupart basique; et
sontreprésentés par les alcaloïdes stéroïdaux et
les purines telles que la conessine
53 et la caféine54
(Milcent, 2003).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 20
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Me
N Me
Me
(Me)2N
O
N N
N
N
O
54
53
Conessine
Cafeine
II.1.4 Caractérisation des alcaloïdes
La caractérisation des alcaloïdes se fait sur des
extraits aqueux acides; par précipitation des sels d'alcaloïdes
avec des réactifs généraux: Avec le réactif de
Valser-Meyer, on obtient un précipité blanc-jaunâtre et un
précipité rouge-orangé avec le réactif de
Dragendorf. Le réactif iodoplatinate de potassium est un
révélateur utilisé pour les alcaloïdes en CCM
(Bassène, 2012).
II.1.5 Propriétés physicochimiques des
alcaloïdes
II.1.5.1 Caractère physique
Les alcaloïdes sont des solides cristallisés
lorsqu'ils sont oxygénés avec un poids moléculaire
élevé; et des liquides entrainables à la vapeur d'eau
s'ils sont non oxygénés et de faible poids moléculaire.
Leur saveur est généralement amère (Bassène,
2012).
? Solubilité
La solubilité des alcaloïdes dépend de la
forme dans laquelle ils se trouvent. En milieu alcalin; les alcaloïdes
sont sous forme de base (libre) et sont insolubles dans l'eau; mais soluble
dans les solvants apolaires (éther, benzène, chloroforme,
etc...). En milieu acide les alcaloïdes sont sous forme de sels; ils sont
solubles dans l'eau, mais insolubles dans les solvants organiques apolaires.
L'alcool est capable de dissoudre les deux formes (base; sels). Ce comportement
intéressant va engendrer trois méthodes d'extractions à
savoir: extraction par l'eau acide, extraction par l'alcool, extraction par
solvant organique (Bassène, 2012).
II.1.5.2 Caractère chimique
Les alcaloïdes donnent des précipités avec
certains réactifs tels que l'acide picrique, l'acide phosphotungstique
et les réactifs iodés tel que le réactif iodoioduré
(Boucharat ); le
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
réactif iodomercurate de potassium (reactif de
Velsermeyer): le réactif iodobismutite de potassium (réactif de
dragendorff) (Bassène, 2012).
| 


