3) NEURiNFARCT : un nouveau système de
pronostic basé sur l'IRM de diffusion.
L'étude est basée sur 98 patients de 60 ans de
moyenne d'âge. Le premier IRM a été passé en moyenne
2,3 h après les premiers symptômes. NEURiNFARCT a pour but
d'établir une image de prédiction automatique du devenir de
l'infarctus et de sa progression potentielle dans le cerveau du patient, ce qui
permettrait au neurologue d'estimer le rapport bénéfice/risque
des traitements existants pour limiter cette progression. Il s'agit d'un
algorithme obtenu grâce à la carte d'ADC créée suite
à l'IRM faite dès admission des patients.
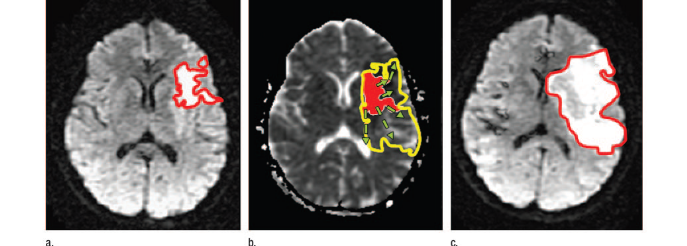
Source [8] : Principe de fonctionnement de
NEURiNFARCT, observation chez un patient de 49 ans
A: A l'admission (104 min) l'infarctus déjà
formé (16,3 cm3)est identifié grâce à une
séquence IRM de diffusion classique.
B: L'infarctus déjà formé est
reporté sur la carte du coefficient apparent de diffusion
(dérivée automatiquement de l'IRM de diffusion A). Le logiciel
estime la taille finale de l'infarctus à 84,1 cm3.
C : Infarctus final mesuré en IRM de
diffusion : 126,9 cm3 .
Cet algorithme procède à une simulation de
manière itérative (voxel par voxel) de l'évolution de
l'infarctus. Ici encore un ratio d'ADC a été pratiqué et
les résultats montrent qu'une valeur seuil d'ADCr peut être
établie à 0,93 (ADClésion = 0,93ADCmirroir). Ce seuil est
différent de celui décrit par l'étude
précédente faite aux UCL. Cela peut s'expliquer par l'utilisation
de machines ou de séquences différentes. Comme le montre ces
graphiques, l'étude montra une corrélation entre le volume final
de l'infarctus et le volume prédit par l'algorithme.
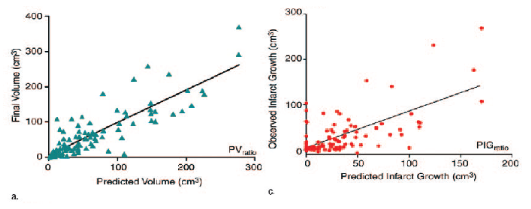
Les chercheurs voulurent ensuite observer s'il y avait une
corrélation entre la prédiction faite par le logiciel et la
revascularisation. Ils étudièrent également l'effet de
l'heure où la première IRM fut prise. Ils n'observèrent
aucune corrélation entre l'heure où l'IRM fut prise et la
prédiction de l'infarctus. Une revascularisation complète ou
partielle fut observée chez 70 patients et il n'y eut aucune
revascularisation chez 20 patients (1 individu eut un IRM non
interprétable). Ils constatèrent que chez les patients ayant eut
une revascularisation, la réelle croissance de l'infarctus était
même plus faible que celle prédite.
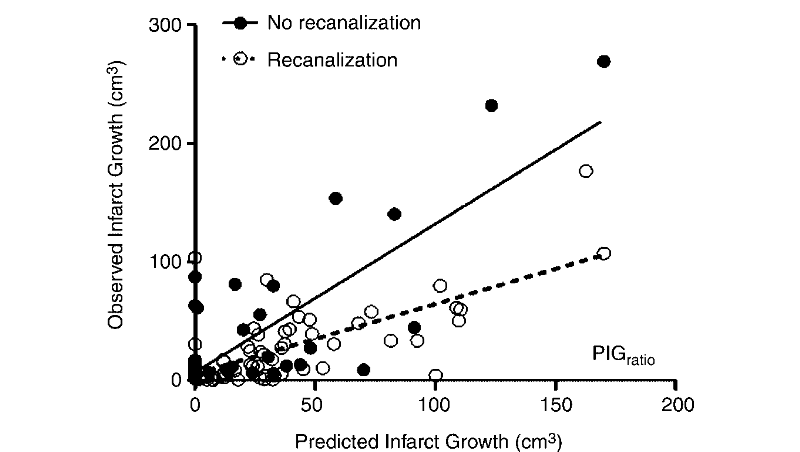
Le graphique ci dessus, la corrélation entre la
possible revascularisation et la prédiction de la croissance de
l'infarctus établie par leur algorithme.
La méthode NEURiNFARCT permet également de
prévoir la zone de pénombre et présente l'avantage de
n'utiliser que des images faites en IRM de diffusion.. Ainsi l'injection de
produit de contraste (effectué pour l'IRM de perfusion) n'est plus
nécessaire. Elle est entièrement automatisée ce qui
apporte un gain de temps dans les situations d'urgence.
Cette méthode a quelques limitations : il n'a pas
encore été prouvé que la méthode peut travailler
avec des données provenant de différents systèmes
d'imagerie par résonance magnétique dans d'autres centres. Une
version de l'algorithme pouvant être distribué à d'autres
centres est en cours de développement.
Conclusion :
L'inconvénient sur les valeurs seuil d'ADC et de l'ADCr
est que ces valeurs seuil varient en fonction de l'étude. Cela pourrait
être du aux paramètres d'acquisition variant entre
différentes machines (nombre de Tesla, temps d'écho, angle de
bascule etc.) . Cependant une équipe a montré que deux examens
réalisés chez des rats à 15 minutes d'intervalle
révélait déjà des différences dans les
valeurs d'ADC (Shen et al., 2003). évolue avec le temps.
Etant donné les variations de valeurs d'ADC en fonction
des appareils, des séquences et du temps, le développement de
l'algorithme de NEURiNFARCT sera difficile.
Les nombreuses corrélations définies au cours de
ce mémoire offrent d'intéressantes perspectives d'avenir. La mise
au point d'un algorithme permettant d'évaluer l'évolution de la
taille de la zone nécrosée à partir de l'ADCr dans un
centre IRM semble être un premier pas vers la mise au point de
méthodes automatiques permettant de prévoir le risque
hémorragique et l'évolution des symptômes. En effet, si
cela s'avère possible, l'intégration de tous paramètres
présentant une corrélation avec la taille de l'infarctus et le
NIHSS dans un unique algorithme, permettrait une prise en charge optimale de
l'AVC. Cela nécessiterait cependant une standardisation des
échelles de rCBF et rCBV ainsi que l'évaluation des modifications
de tous les paramètres au cours du temps.
La variation des paramètres d'acquisition (puissance du
champ magnétique, temps d'Echo, temps de relaxation etc.) entre les
différents centres d'examen n'a pas encore permis de consensus sur une
méthode de pronostic fiable et applicable partout.
A l'heure actuelle, aucune étude IRM de grande
envergure (sur quelques milliers de patients) n'a été
menée dans la phase hyperaiguë de l'AVC. Une telle étude
intégrant toutes les variables connues (facteurs de risque,
paramètres radiologiques et scores cliniques) et établissant
toutes éventuelles corrélation entre eux pourrait permettre une
avancée majeur dans la prédiction de l'évolution de l'AVC
et de ses symptômes. De plus, la mesure des différents
coefficients de diffusion et perfusion pourraient permettre d'obtenir des
données précises sur l'évolution de l'ischémie dans
les premières heures. La détermination de valeurs seuils pour
plusieurs paramètres pourrait permettre d'établir
précisément la réversibilité ou non d'une zone
lésion.
| 


