II.3.2. Réticulation
La synthèse d'un polymère époxyde est une
réaction de réticulation entre le pré-polymère
époxyde et le durcisseur, donnant naissance ainsi à une structure
tridimensionnelle. La réticulation peut être
Chapitre II Réactions chimiques et mode
opératoire
Page 31
accélérée par ajout de catalyseurs. Gillham
et al, ont largement étudié les phénomènes de
réticulation et établi des diagrammes d'état Temps -
Température - Transformation (TTT) [GAN 89J et [PANG 90J.
Ces diagrammes (Figure II.5) permettent de suivre l'évolution
du système en fonction du temps et de la température de
réticulation.
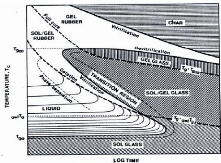
Figure II.5 : Diagramme :
Temps-Température-Transformation (TTT)
Le durcissement se fait : soit par homopolymérisation
(action d'amorceurs) ; soit par
copolymérisation (avec des agents réticulants de
différents types).
Réaction avec les anhydrides d'acides :
Il y a trois types de réactions principales :
Réaction 1
L'anhydride attaque un des groupes OH (Hydroxyle) de la
résine époxyde qui initient la réaction
(Figure II.6).

Figure II.6 : Structure chimique de la
réaction 1
Réaction 2
Le groupe OH formé sur l'anneau phtalique va réagir
avec un groupe époxydique d'une autre
molécule.
Réaction 3
Le groupe époxydique d'une molécule peut attaquer
le groupe OH d'une autre molécule sous
l'effet catalytique du durcisseur (Figure II.7) :

Figure II.7 : Structure chimique de la
réaction 3
Chapitre II Réactions chimiques et mode
opératoire
Page 32
Chapitre II Réactions chimiques et mode
opératoire
II.3.3. Polyépoxydes

Figure II.8 : Représentation
schématique de la résine époxyde La cuisson des
polyépoxydes passe par deux étapes importantes :
· La gélification correspondant
à la formation d'un réseau tridimensionnel infini et par passage
de l'état liquide à l'état caoutchoutique, et apparition
d'une première molécule tridimensionnelle occupant tout le volume
réactionnel (percolation).
· La vitrification qui se produit
lorsque la température de transition vitreuse du système devient
égale à la température de cuisson. Le système passe
de l'état liquide ou caoutchoutique à l'état vitreux, ce
qui s'accompagne d'une importante chute de la mobilité
moléculaire et, par conséquent, d'un arrêt des
réactions chimiques.
De plus, on constate que pour les températures de
réticulation élevées, il y a compétition entre la
polymérisation et la dégradation thermique. Les mécanismes
réactionnels gouvernant le processus de réticulation sont
complexes et dépendent des conditions de température, des
proportions des différents intervenants chimiques et de la
présence ou non d'un catalyseur.
Les différentes réactions chimiques
envisageables sont :
· Attaque nucléophile de l'amine primaire
(R-NH2) sur le cycle époxyde.
· Attaque nucléophile par l'oxygène du
groupement hydroxyle (-OH) sur le cycle époxyde.
· Attaque nucléophile de l'amine secondaire (RR'-NH)
sur le cycle époxyde.
· Attaque nucléophile de l'oxygène d'un cycle
époxyde sur un autre cycle époxyde.
Différentes études résumées par
Wright concluent que la réaction principale est l'attaque
nucléophile d'un groupement amine primaire sur le cycle oxiranne
(époxyde) tant que la température de transition vitreuse du
réseau formé reste inférieure à celle de la
vitrification [WRIG 89J. Passé ce stade, la
mobilité moléculaire est faible et la réaction
hydroxyle/époxyde devient majoritaire. Les réactions
époxyde/époxyde et amine secondaire/époxyde sont quasiment
inexistantes. Néanmoins, la contribution de chaque type de
réaction à la structure du réseau final dépend
fortement des compositions relatives de chacun des constituants. Morgan et al.
observent que la Tg la plus élevée d'un mélange
TGMDA/DDS est obtenue pour un taux de durcisseur qui implique
théoriquement la moitié des cycles oxirannes [MORG
79J. Ils en concluent que les réactions secondaires jouent un
rôle
Page 33
important lors de la réticulation ce qui permettrait
d'expliquer qu'un réseau qui devrait être aussi mal
réticulé possède des propriétés
mécaniques remarquables. Morgan et Mones observent qu'il est impossible
d'obtenir une réticulation complète d'une résine TGMDA/DDS
à 180°C sans ajout d'au moins 5% de catalyseur de type
BF3 [MORG 87J. Enfin, selon Morgan, on obtient,
après réticulation d'une résine TGMDA/DDS en
présence de catalyseur de type BF3, une structure fortement
hétérogène avec des nodules. Comme le note Galy, il existe
une controverse dans la littérature sur la morphologie nodulaire des
résines époxydes [GALY 85J. Certains auteurs
certifient l'existence de nodules au sein de la matrice alors que d'autre les
attribuent à un artefact de la méthode d'observation optique.
Pour Wright, même s'ils existaient, il n'y a néanmoins aucune
preuve que ces nodules soient des régions de degré de
réticulation différent de celui de la matrice [WRIG
89J.
Le monomère époxyde est
polymérisé avec un agent de réticulation qui peut
être un anhydride d'acide, un phénol, ou le plus souvent une
amine. La DETA, ayant fait l'objet de nombreux travaux précédents
(comme ceux de POSSART), est utilisée dans l'industrie comme durcisseur
(colles Araldite). Quant à l'IPDA, elle est la seule amine jouant le
rôle de catalyseur par action sur les métaux ou leurs oxydes. La
DAE, choisie comme molécule sonde par François DEBONTRIDDER pour
sa simplicité, est une diamine aliphatique de masse molaire faible.
Enfin les Propane Diamine, butane diamine et Penta Diamine
ont été utilisées, avec la DAE (ou EthaneDiamine), pour
étudier l'influence de la longueur de la chaine carbonée
fixée sur les fonctions amine, et les propriétés
physico-chimiques et mécaniques des interfaces formées.
Nom usuel
|
DiEthyléneTriAmine
|
Abbreviation
|
DETA
|
Nom chimique
|
DiEthyléneTriAmine
|
Formule chimique
|
NH2-CH2-CH2-NH-CH2-CH2-NH2
|
Etat à 25°C
|
Liquide transparent
|
Masse molaire
|
103,17g/mol
|
Fonctionnalité
|
5
|
Densité
|
0,955g/cm3
|
Température de fusion
|
- 35°C
|
Température d'évaporation
|
199°C à 209°C
|
Viscosité
|
0.071Pa.s à 25°C
|
|
Caractéristiques chimiques de la DETA
Chapitre II Réactions chimiques et mode
opératoire
Page 35
| 


