I.4.5.6 La vitesse d'agitation
Afin d'obtenir une conversion importante lors de la
transestérification, le milieu biphasique de la réaction impose
une agitation suffisamment vigoureuse pour que la surface d'échange
entre les deux phases soit la plus grande possible. De plus, la vitesse
d'agitation est non seulement importante lors de l'amorçage de la
réaction de transestérification, mais également durant le
déroulement du processus réactionnel. Pour certains auteurs
[39], l'étude de ce paramètre à trois
vitesses d'agitation (110, 220 et 330 tr/min) en fonction du temps de
réaction (1, 2 et 3 min), a montré que, pour une durée de
réaction donnée les rendements sont maximums, pour une
durée de réaction donnée, à la vitesse d'agitation
la plus élevée [29].
13
I.5 Le biodiesel
I.5.1 Définition du biodiesel
Le biodiesel est le nom qui a été donné
aux huiles végétales transestérifiées. C'est une
réaction entre l'huile et l'alcool, formant ainsi les esters
méthyliques ou éthyliques d'huiles végétales et du
glycérol, désigné sous le nom de glycérine, qui est
un produit de grande valeur, sa valorisation est déterminante pour
l'équilibre économique de la filière
[40].
I.5.2 L'utilité du biodiesel
Le biodiesel présente certains avantages en tant que
carburant, issu de produits d'agriculture, qui ont des propriétés
proches de celle du gasoil, sont faciles à transporter, disponibles,
renouvelables, biodégradables et qui présentent une
efficacité à la combustion plus élevée. La faible
teneur en soufre et en aromatiques dans le biodiesel a un effet positif sur les
gaz à effet de serre. De plus le biodiesel possède des
caractéristiques intéressantes à savoir un indice de
cétane supérieur et un point d'éclair élevé
[41].
Le biodiesel est un solvant léger, il nettoie et
maintient les réservoirs, les conduits et le système d'injection
propres. Son onctuosité est de loin supérieure à celle du
diesel. L'usure du moteur est par conséquent réduite et sa
durée de vie prolongée. Les mélanges de biodiesel avec le
diesel sont stables sur le plan thermique, ils ne changent pas de façon
significative même en étant exposés à des
températures supérieures à 70 °C. Parce qu'il est
davantage chargé en oxygène (11%), le biodiesel assure une
meilleure combustion du carburant auquel il est mélangé et
diminue les émissions d'hydrocarbures (HC), de monoxyde de carbone (CO)
et de particules mais augmente les émissions d'oxydes d'azote (NOx).
Actuellement, l'utilisation du biodiesel en mélange
avec le diesel à raison de 5%, 10%, et 20 % en volume, montre que les
performances du moteur sont presque identiques à celles du diesel pur et
que le biodiesel offre également une meilleure sécurité de
stockage, de manipulation et d'utilisation par rapport au diesel
conventionnel.
La qualité de biodiesel (Tableau I.3)
dépend de la matière première et du procédé
de production utilisés. Par conséquent, un des principaux
défis lors de la production de biodiesel consiste à
améliorer ses caractéristiques physico-chimiques, à
diminuer sa viscosité et son point de trouble et à augmenter son
indice de cétane.
14
Par exemple, la viscosité du biodiesel produit à
partir de matières premières telles que les huiles de colza, de
soja, de tournesol et d'olive entre autres, varie de 2.83 à 5.12 cSt
[42], tandis que la viscosité du pétrodiesel est
d'environ 3.0 cSt [43] Le pouvoir calorifique du
pétrodiesel, compris entre 42.5 et 45 MJ/kg, est supérieur
à celui du biodiesel [44 ; 45] qui varie entre 35 et 42
MJ/kg [16].
Tableau I.3 :Propriétés physico-chimiques de
biodiesels produits à partir de diverses matières
premières.
|
Source
|
Masse
volumique
(g/l)
|
Viscosité
(Cste à
40°C)
|
Pouvoir
calorifique
(Mj/kg)
|
Point
d'éclair
(°C)
|
Point
de
trouble
(°C)
|
Point
d'écoulement (°C)
|
Références
|
|
Huile de
palme
|
880
|
5,7
|
34
|
164
|
13
|
/
|
[44]
|
|
Huile de
soja
|
885
|
4,1
|
40
|
69
|
-2
|
-3
|
[45]
|
|
Huile de
colza
|
882
|
4,5
|
37
|
170
|
-4
|
-12
|
[16]
|
|
Huile de
tournesol
|
860
|
4,6
|
34
|
183
|
1
|
/
|
[44]
|
|
Huile de
microalgues
|
864
|
5,2
|
41
|
115
|
-12
|
-11
|
[16]
|
I.5.3 Caractéristiques physiques et chimiques du
biodiesel
Tenant compte de son utilisation comme carburant dans un
moteur diesel, les caractéristiques du biodiesel les plus
intéressantes à étudier sont :
1. Densité
Il est connu que la densité du biodiesel dépend
principalement de sa teneur en esters méthyliques et la quantité
résiduelle de méthanol [46]. La densité
d'un biodiesel a un effet important sur les performances du moteur. En effet,
les pompes d'injection du biodiesel sont des pompes volumétriques et le
dosage se fait en calculant la masse du volume injecté en passant par la
densité.
15
Un carburant ayant une densité élevée
conduit à une masse de carburant injectée plus importante et
augmente la consommation. Cette propriété est influencée
principalement par le type d'huile végétale utilisée
[47], et dans une certaine mesure par les étapes de
production appliquées.
2. Viscosité
La viscosité est la plus importante
propriété de biodiesel, elle joue un rôle très
important dans la combustion et affecte les performances du moteur et ses
émissions polluantes. La viscosité élevée conduit
à une mauvaise pulvérisation, ce qui réduit la surface de
contact air biodiesel. Cette mauvaise pulvérisation liée à
une mauvaise volatilité provoque une combustion incomplète dans
le moteur.
Cette mauvaise combustion se traduit par des performances
dégradées du moteur et des émissions polluantes plus
élevées (suies, monoxydes de carbone et hydrocarbures
imbrûlés). Plus la viscosité est dans les normes, plus il
sera facile de pomper le carburant et de le pulvériser en fines
gouttelettes.
La conversion des triglycérides en esters
méthyliques ou éthyliques à travers le processus de
transestérification réduit le poids moléculaire au tiers
de celui du triglycéride et réduit la viscosité par un
facteur d'environ huit [48]. Le biodiesel a une
viscosité proche de celle des carburants diesel.
3. Le point d'éclair (flash point)
Le point d'éclair est la température la plus
basse où la concentration des vapeurs émises est suffisante pour
s'enflammer en présence de l'air au contact d'une flamme pilote, il sert
à classer les liquides en fonction de leurs risques d'inflammation. En
d'autres termes, il est un indice de la présence des matières
volatiles et inflammables dans le biodiesel. Un point d'éclair
élevé indique que la matière présente moins de
risques à s'enflammer lors du stockage ou de la manipulation.
4. Point de trouble (Cloud Point)
Le point de trouble est la température à partir
de laquelle apparaît un début de cristallisation se traduisant par
une altération de la limpidité. Le point de trouble fait partie
des propriétés à froid du biocarburant comme le point
d'écoulement où la température limite de
filtrabilité (TLF). À basse température (en hiver) la
formation des cristaux peut conduire au colmatage du filtre à carburant
et à une panne d'alimentation du moteur.
16
5. Point d'écoulement (Pour Point)
Le point d'écoulement est la température
à partir de laquelle le liquide cesse de s'écouler. À
partir de cette température, on estime que le pompage du carburant n'est
plus possible. Le biodiesel a des points de trouble et d'écoulement
supérieurs par rapport à ceux du pétrodiesel.
6. Pouvoir calorifique
Le pouvoir calorifique mesure la quantité de chaleur
libérée lors de la combustion d'une masse donnée du
biodiesel. Elle s'exprime en kJ/kg. Cette valeur permet de comparer
différents produits de natures différentes.
7. L'indice d'acide
L'acidité ou l'indice d'acide est mesurée par
la quantité d'hydroxyde de potassium en mg nécessaire pour
neutraliser un gramme de biodiesel. Il indique la teneur du liquide en acides
organiques. Les hautes teneurs en acides organiques favorisent la corrosion des
pièces du moteur. L'indice d'acide permet aussi de juger leur
état de détérioration.
On distingue deux formes d'acidité :
? Acidité totale : c'est la quantité de base,
nécessaire pour neutraliser tous les constituants acides présents
dans un gramme de matière grasse.
? Acidité forte : c'est la quantité de base,
nécessaire pour neutraliser les constituants à acidité
forte présentes dans un gramme de matière grasse.
8. Indice d'iode
C'est la masse d'iode (en grammes) absorbée par 100
grammes de biodiesel par réaction d'addition. L'indice d'iode permet de
mesurer le nombre de liaisons doubles ou triples qui se trouvent dans le
biodiesel, c'est-à-dire son degré d'insaturation. La
présence de liaisons multiples favorise les réactions d'oxydation
et de formation de gommes suite à des phénomènes de
polymérisation lors du stockage.
L'indice d'iode dépend de l'origine des
matières premières et influence grandement la tendance à
l'oxydation du biodiesel. Par conséquent, afin d'éviter
l'oxydation, des précautions particulières doivent être
prises lors du stockage de biodiesel. Des antioxydants sont ajoutés au
biodiesel ayant des indices d'iode élevés.
9. Teneur en esters
Théoriquement le biodiesel est composé d'esters
éthyliques ou méthyliques d'acides gras. Mais en pratique, le
biodiesel contient aussi des impuretés qui viennent soit de l'huile qui
n'est pas complètement convertie en esters, d'où la
génération des mono, di et triglycérides. D'autre part,
Les auteurs ont attribué cette différence de
performances à la présence de l'excès d'alcool et des
traces de glycérine dans le biodiesel non lavé
[52].
17
des quantités résiduelles d'alcool, de
glycérine, et des impuretés peuvent se retrouver dans le
biodiesel.
10. Teneur en eau
La teneur en eau est considérée comme un
indicateur de pureté du carburant. Dans le biodiesel, l'eau peut se
retrouver sous deux formes, dissoute ou dispersée sous forme de
gouttelettes [50]. Le biodiesel doit être
séché avant son injection dans le moteur, l'eau pouvant provoquer
la corrosion des pièces du système d'injection de carburant. La
présence d'eau favorise aussi la croissance microbienne qui peut
encrasser le filtre à carburant [50].
Dans les procédés d'estérification, la
présence d'eau a des effets négatifs sur les rendements en esters
méthyliques. Ce paramètre est donc étroitement
surveillé et dépendra de l'humidité de la graine et des
conditions de stockage de l'huile.
11. Teneur en alcool
La présence d'alcool résiduel dans le biodiesel
réduit son point d'auto-inflammation qui risque de tomber en au-dessous
des seuils recommandés par les normes.
I.5.4 Utilisation du biodiesel dans les
moteurs
On peut utiliser le biodiesel pour les moteurs diesel dans
plusieurs secteurs, comme carburant alternatif ou comme complément du
gazole. Plusieurs études ont porté sur l'utilisation du biodiesel
en mélanges avec le gazole ou bien sous forme pure. En
général, la plupart des recherches montrent que les performances
du moteur diesel avec le biodiesel sont similaires à celles du gazole,
mais avec une augmentation de la consommation spécifique en raison de
son pouvoir calorifique plus bas.
Meng et al, ont étudié l'effet de l'utilisation
du biodiesel de l'huile de friture usagée sur un moteur diesel. Pour
cela, ils ont utilisé des mélanges contenant 20% et 50% de
biodiesel. Les mélanges non lavés donnaient des performances
inférieures à celles du biodiesel lavé qui étaient
très proches de celles du gasoil. En termes d'émissions
polluantes, les mélanges du biodiesel non lavé ont conduit
à des émissions de CO et des imbrûlés non
satisfaisantes aux normes. Par contre le mélange du biodiesel
lavé a diminué les imbrûlés, le CO et le NOx.
18
I.5.5.1 Mélanges de
biodiesel-pétrodiesel
Le biodiesel peut être mélangé à
différentes proportions avec le gazole. Les plus courants sont : B100
(biodiesel pur), B20 (20% de biodiesel, 80% de gazole), B5 (5% de biodiesel,
95% de gazole) et B2 (2% de biodiesel, 98% de gazole).
a. Le mélange B100 et mélanges à
haute teneur en biodiesel
Le « B100 » et d'autres mélanges à
haute teneur en biodiesel sont moins fréquents que le mélange B20
en raison d'un manque d'incitations réglementaires et les prix. Les
mélanges à haute teneur en biodiesel nécessitent des
modifications majeures du moteur, L'utilisation de biodiesel pur (B100)
accroît les émissions d'oxydes d'azote, mais réduit
considérablement les autres émissions toxiques. Le « B100
» a un pouvoir solvant élevé, pouvant nettoyer les
dépôts accumulés lors de l'utilisation du gazole
[53].
b. Le mélange B20
Le B20 est le mélange de biodiesel le plus
utilisé aux États-Unis. Il représente en effet, un bon
compromis entre les coûts, les émissions, les performances par
temps froid, la compatibilité des matériaux et la capacité
à agir en tant que solvant. Généralement le B20 est le
mélange qui ne nécessite pas de modifications du moteur. Les
moteurs fonctionnant au B20 développent une puissance similaire à
celle des moteurs fonctionnant au gazole. Les consommations en carburant sont
également similaires. Le B20 doit répondre aux normes de
qualité prescrites par la norme ASTM D7467.
c. Le mélange B5
La plupart des fabricants de moteurs nord-américains
acceptent désormais les mélanges de biodiesel jusqu'à une
teneur de 5%. L'utilisation de B5 ne devrait pas causer de problèmes
pour le système d'alimentation ou le moteur. Le B5 doit être
conforme aux spécifications du gazole, norme ASTM D975 pour être
commercialisé.
I.5.5.2 Comparaison biodiesel - gazole
Le biodiesel a des propriétés chimiques qui sont
voisines de celles du gazole. Le biodiesel est un carburant 100% renouvelable,
et contribue à réduire de manière significative les
niveaux de polluants nocifs et les émissions de gaz à effet de
serre. Le biodiesel est également plus efficient que le gazole lorsqu'on
analyse son cycle de vie total. Selon une étude récente
menée par le Département américain de l'énergie, le
rendement énergétique du biodiesel est de 280% supérieur
à celui du carburant diesel. Le biodiesel peut également apporter
une contribution significative à la sécurité
énergétique.
19
Le biodiesel a de meilleures propriétés
lubrifiantes que le gazole, ce qui améliore la durée de vie du
moteur diesel. Le biodiesel a également un indice de cétane plus
élevé, ce qui signifie qu'il a une meilleure aptitude à
l'auto-inflammation tout en réduisant le niveau de bruit du moteur.
Comme le montre le Tableau I.4 ci-dessous le point
d'éclair du biodiesel est significativement plus élevé que
le diesel (130°C comparé à 60°C pour le gazole, ce qui
en fait un carburant plus sûr). L'inconvénient majeur du biodiesel
comparé au gazole est son coût plus élevé.
Tableau I.4 : La comparaison de certains paramètres
clés pour le carburant B100 par rapport au
gazole [54].
|
Propriété
|
Diesel
|
Biodiesel (B100)
|
Unités
|
|
La norme
|
ASTM D975
|
ASTM D6751
|
|
|
Pouvoir calorifique inférieur
|
~ 129.050
|
~118.170
|
btu/gal
|
|
Viscosité cinématique à 40°C
|
1.3 - 4.1
|
1.9 -6.0
|
mm2/s
|
|
Densité à 60°C
|
0.85
|
0.88
|
kg/l
|
|
Densité
|
7.079
|
7.328
|
lb/gal
|
|
L'eau et les sédiments
|
0.05 max
|
0.05 max
|
% volume
|
|
Carbone
|
87
|
77
|
% masse
|
|
Hydrogène
|
13
|
12
|
% masse
|
|
Oxygène
|
0
|
11
|
% masse
|
|
Soufre
|
0.0015 max
|
0.0 à 0.0024
|
% masse
|
|
Point d'ébullition
|
180 - 340
|
315 -350
|
°C
|
|
Point d'éclair
|
60 - 80
|
130 - 170
|
°C
|
|
Point trouble
|
(-15) - 5
|
(-3) - 12
|
°C
|
|
Point d'écoulement
|
(-35) - (-15)
|
(-15) - 10
|
°C
|
|
Indice de cétane
|
40 - 55
|
47 - 65
|
|
|
Lubrifiant SLBOCLE
|
2.000 - 5.000
|
>7,000
|
grams
|
|
Lubrifiant HFRR
|
300 à 600
|
<300
|
microns
|
20
I.5.5 Avantages et inconvénients du
biodiesel
I.5.5.1 Avantages
Il est vrai que le biodiesel constitue une alternative
intéressante sur le plan environnemental. Son premier avantage est qu'il
pollue moins et a un bilan carbone à peu près neutre. Il peut
être aussi fabriqué à partir des déchets comme les
huiles de friture et les graisses animales, ce qui permet de régler un
problème environnemental. Un carburant qui n'aggrave pas les
émissions de gaz à effet de serre est indispensable aujourd'hui
pour la sauvegarde de notre planète, le biodiesel est facile à
manipuler et à transporter.
La viscosité plus élevée que celle du
gazole lui offre un meilleur pouvoir lubrifiant dans la chambre de combustion
réduisant le travail des frottements et l'usure des pièces
mécaniques, le biodiesel a également un indice de cétane
plus élevé, lui offre une combustion plus rapide et moins
bruyante [53].
En termes de composition chimique, le biodiesel est
essentiellement composé d'esters (éthyliques ou
méthyliques) La présence d'oxygène combinée avec
l'absence de soufre et de composés aromatiques lui offre l'avantage de
réduire les émissions d'hydrocarbures imbrûlés et
des particules ainsi que d'oxydes de soufre lors de sa combustion dans le
moteur [54].
Le biodiesel est non-toxique et se dégrade quatre fois
plus rapidement que le gazole, grâce à sa teneur en oxygène
qui améliore le processus de biodégradation. Il améliore
la performance environnementale du transport routier et il réduit les
émissions des gaz à effet de serre.
D'autre part, tous les produits générés
par les réactions chimiques lors de la production du biodiesel sont
réutilisables, soit pour d'autres réactions chimiques, soit dans
d'autres secteurs industriels. Par exemple le glycérol peut être
utilisé comme lubrifiant dans les moteurs de véhicules.
I.5.5.2 Inconvénients
À côté de ces avantages, le biodiesel
comporte quelques inconvénients comme son point de fusion, son point
trouble et point d'écoulement élevés qui rendent son
utilisation en hiver sous forme pure difficile sur les véhicules dans
les pays à climats froids.
Une solution probable de ce problème consiste à
l'utiliser sous forme de mélanges ou de le préchauffer avant son
injection au moteur, cette deuxième solution est possible sur les
moteurs stationnaires à cogénération, une troisième
solution consiste à séparer la fraction des esters
méthyliques à longues chaînes saturées qui ont des
points de fusion et des points troubles élevés.
21
Un autre problème de biodiesel est sa stabilité
lors du stockage à longue durée, en fait les liaisons doubles et
triples présentes dans les acides gras, sont instables et ont tendance
à s'oxyder ou à former des gommes.
Ce type de problème est résolu soit par
l'addition des antioxydants, soit par l'utilisation directe après la
production. La teneur en acides gras libres peut aussi conduire à des
problèmes de corrosion dans le circuit d'alimentation et d'injection des
moteurs diesel [57] si elle dépasse un certain seuil.
Aussi, il faut bien respecter les normes concernant l'indice d'acide afin
d'éviter ce type de problèmes. La présence
d'oxygène améliore la combustion du carburant mais entraîne
des températures plus élevées dans la chambre de
combustion, ce qui favorise la formation des NOx [58, 59].
Le principal inconvénient du biodiesel est lié
à son prix élevé provenant du prix des huiles
végétales constituant de 70 à 95% du prix total. Un autre
problème associé est la compétition entre l'alimentation
et la production des carburants. D'où la nécessité
d'utiliser les déchets comme matière première de
production du biodiesel (l'huile de friture usagée).
22
CHAPITRE II. NOTIONS SUR LA
MODÉLISATION
EXPÉRIMENTALE
Ce chapitre propose une approche méthodologique pour
étudier et analyser les biocarburants. Il présente les
différentes techniques et outils de modélisation utilisés
pour simuler et prédire le comportement des biocarburants, que ce soit
au niveau de leur production, de leur combustion ou de leur impact
environnemental. Le chapitre aborde également les principes de base de
la modélisation expérimentale, tels que la conception des
expériences, la collecte des données, l'analyse statistique et
l'interprétation des résultats. En mettant en avant l'importance
de la modélisation expérimentale dans le domaine des
biocarburants, ce chapitre vise à fournir aux lecteurs les connaissances
et les compétences nécessaires pour mener des études
approfondies et fiables dans ce domaine en constante évolution.
II.1 PLANS D'EXPÉRIENCES
Tout d'abord, il est primordial de comprendre certains termes
qui interviendront dans la suite de cette étude entre autres :
? Un modèle est une représentation d'un
système réel, capable de reproduire son fonctionnement. Son
principe est de remplacer un système réel en un objet ou
operateur simple reproduisant les aspects ou comportements principaux de
l'original.
? Un facteur (quantitatif ou qualitatif) est un
paramètre ou état du système étudié
(phénomène ou procédé) dont la
variation est susceptible d'en modifier le fonctionnement (ex :
température, concentration d'un réactif...). La réponse
(ou critère) du système correspond au paramètre
mesuré ou observé pour connaître l'effet des facteurs
étudiés sur le système (ex : rendement d'une
réaction...)
Les plans d'expériences permettent d'organiser au mieux
les essais qui accompagnent une recherche scientifique ou des études
industrielles [27].
Les plans d'expériences permettent d'obtenir le maximum
d'informations avec le minimum d'expériences. Pour cela, il convient de
suivre des règles mathématiques et adopter une démarche
rigoureuse [28].
Environ 80 % des applications courantes utilisent les plans
dont les facteurs prennent deux niveaux et dont le modèle
mathématique de la réponse est du premier degré. Mais il
arrive assez
23
souvent que le modèle du premier degré soit
insuffisant pour expliquer les réponses mesurées. Dans ce cas, il
faut passer à un modèle du second degré.
Il existe plusieurs types de plans du second degré,
mais ils permettent tous de trouver les mêmes surfaces de
réponse.
Pour 2 facteurs, on peut représenter la surface de
réponse dans un espace à 3 dimensions. Il y a 2 dimensions pour
les facteurs et 1 pour la réponse.
En général, l'objectif des plans du second
degré est la modélisation du phénomène.
Dans notre travail, nous avons opté pour un plan
factoriel complet. Ce plan est le plus fréquemment utilisé car il
est simple et rapide à mettre en oeuvre, on le note par 2K
où le 2 correspond aux niveaux maximal et minimal qui délimitent
le domaine d'étude d'un facteur Z et k représente le nombre des
facteurs étudiés.
Pour un plan factoriel complet à k facteurs, le nombre
total d'expériences est noté :
|
Exemples :
? Si k = 2, N =
? Si k = 3, N =
? Si k = 4, N =
? Si k = 5, N =
|
22
23
24
25
|
N = 2K
= 4 essais = 8 essais = 16 essais = 32 essais
|
|
?
|
Etc.
|
|
|
L'étude a été réalisée sur
base d'un plan factoriel utilisant un plan factoriel complet à 3
variables et deux niveaux, qui a abouti à 10 expériences dont
deux étaient au centre. Le Tableau II.1 montre les
variables analysées dans l'expérience et leurs niveaux :
Tableau II.1 : Les niveaux de facteurs pour le plan
factoriel complet.
|
Niveau
|
-1
|
0
|
+1
|
|
Concentration de catalyseur (g)
|
M1
|
M2
|
M3
|
|
Temps de réaction (min)
|
t1
|
t2
|
t3
|
|
Rapport molaire
|
RM1
|
RM2
|
RM3
|
Les facteurs variables et leurs valeurs utilisés pour
l'optimisation de processus de transestérification étaient les
suivants : (a) rapports molaires éthanol : huile de 3 :1 ; 4.5 :1 et 6
:1 ; (b) des concentrations de catalyseur de 3% ; 4% et 5% par rapport à
la masse de l'huile initiale et (c) des temps de réaction de 45 ; 60 et
75 minutes.
24
Les conditions opératoires appliquées dans les
expériences étaient les suivantes : (a) température de
réaction 65°C et (b) masse de l'huile 138.3gr.
Volume de l'huile utilisée = 150ml dHU =
0.922gr/cm3
mHU = volume de l'huile utilisée X dHU
mHU = 150 × 0.922
mHU = 138.3gr d'huile usagée
|
% (m /m) =
|
msoluté
|
× 100
|
|
msolution
|
II.2 MODÉLISATION MATHÉMATIQUE
On choisit a priori une fonction mathématique qui relie
la réponse aux facteurs. On prend un développement limité
de la série de Taylor-Mac Laurin. Les dérivées sont
supposées constantes et le développement prend la forme d'un
polynôme de degré plus ou moins élevé :
Y = a0 + ?aiXi + ?aijXij + ?
+ ?aiiXii +
Avec :
Y : la réponse ou la grandeur d'intérêt.
Elle est mesurée au cours de l'expérimentation et elle est
obtenue avec une précision donnée.
Xi : représente le niveau attribué au facteur i
par l'expérimentateur pour réaliser un essai. Cette valeur est
parfaitement connue. On suppose même que ce niveau est
déterminé sans erreur (hypothèse classique de la
régression).
a0, ai, aii, aij sont les coefficients du modèle
mathématique adopté a priori. Ils ne sont pas connus et doivent
être calculés à partir des résultats des
expériences.
L'intérêt de modéliser la réponse
par un polynôme est de pouvoir calculer ensuite toutes les
réponses du domaine d'étude sans être obligé de
faire les expériences. Ce modèle est appelé «
modèle postulé » ou « modèle a priori »
[64].
II.2.1 SYSTEME D'EQUATIONS
Chaque point expérimental permet d'obtenir une valeur
de la réponse. Cette réponse est modélisée par un
polynôme dont les coefficients sont les inconnues qu'il faut
déterminer. À la fin du plan d'expériences, on a un
système de n équations (s'il y a n essais) à p inconnues
(s'il y
La matrice d'expérience reprend les conditions
expérimentales en unité codée (VCR). Les valeurs
réelles sont reprises ans un plan d'expérience.
25
a p coefficients dans le modèle choisi a priori). Ce
système s'écrit d'une manière simple en notation
matricielle :
Y = Xa + e
Avec :
Y est le vecteur des réponses.
X est la matrice de calcul ou matrice du modèle, qui
dépend des points expérimentaux
choisis pour exécuter le plan et du modèle
postulé.
a est le vecteur des coefficients.
e est le vecteur des écarts.
Ce système possède un nombre d'équations
inférieur au nombre d'inconnues. Il y a n équations
et p + n inconnues. Pour le résoudre, on utilise une
méthode de régression basée sur le critère
des moindres carrés. On obtient ainsi les estimations des
coefficients que l'on note : â.
Le résultat de ce calcul est :
â = (tXX)-1 tXY
Formule dans laquelle la matrice tX est la matrice
transposée de X. De nombreux logiciels
exécutent ce calcul et donnent directement les valeurs des
coefficients [64].
II.3 PLAN FACTORIEL COMPLET À DEUX
NIVEAUX
Un plan factoriel est un type de plan d'expérience qui
permet d'étudier les effets que plusieurs facteurs peuvent avoir sur une
réponse.
Ce plan est celui qu'il faut utiliser pour rechercher les
facteurs agissant sur une réponse mesurée. C'est le plu simple
à interpréter et il présente le meilleur rapport
coût/efficacité
Sa notation est 2k où le chiffre 2
correspond au niveau maximal et au niveau minimal, qui délimite le
domaine d'étude d'un facteur X, et la lettre k représente le
nombre des facteurs étudiés.
Pour un plan factoriel complet de 3 facteurs à 2
niveaux, 3 facteurs à 2 niveaux définissent 8 conditions
expérimentales, soit 8 essais s'il n'est pas prévu de
répétitions. Le modèle mathématique de ce plan est
de la forme [64] :
Y = A0 + A1X1 + A2X2 +
A3X3 + A12X1X2 + A13X1X3 + A23X2X3
+ A123X1X2X3 + e
II.3.1 Matrice d'expérience
26
C'est ainsi que notre plan d'expériences a
été conçues en partant de la littérature
précédente.
Tout d'abord, il est important de connaitre qu'une matrice
d'expérience est le plan d'expérience en unité
codée.
Le Tableau II.2 montre la matrice
d'expériences en unité centrée réduite
Tableau II.2 : Matrice d'expérience en unité
centrée réduite.
|
Essais
|
Pourcentage du
catalyseur (X1)
|
Ratio huile :
alcool (X2)
|
Temps de la
réaction (X3)
|
Réponses
|
|
1
|
-1
|
-1
|
-1
|
Y1
|
|
2
|
+1
|
-1
|
-1
|
Y2
|
|
3
|
-1
|
+1
|
-1
|
Y3
|
|
4
|
+1
|
+1
|
-1
|
Y4
|
|
5
|
0
|
0
|
0
|
Y5
|
|
6
|
0
|
0
|
0
|
Y6
|
|
7
|
-1
|
-1
|
+1
|
Y7
|
|
8
|
+1
|
-1
|
+1
|
Y8
|
|
9
|
-1
|
+1
|
+1
|
Y9
|
|
10
|
+1
|
+1
|
+1
|
Y10
|
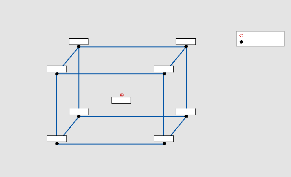
La figure II.2 nous donne les domaines expérimentaux pour
3 facteurs et pour 2 facteurs.
-1
1
Ratio molaire
Graphique en cube (moyennes ajustées) de
Rendements
79,065
89,237
-1
94,390
76,492
Catalyseur
82,873
79,254
Temps de la reaction
87,306
1
-1
79,127
74,354
1
Point central
Point factoriel
Figure II.1 : Le domaine expérimental de nos
études.
27
CHAPITRE III. MATÉRIELS ET
MÉTHODE
Ce chapitre est une section essentielle d'un rapport de
recherche, car il décrit en détail les procédures et les
outils utilisés pour mener l'étude. Ce chapitre permet aux
lecteurs de comprendre comment l'étude a été menée
et de juger de la validité des résultats obtenus.
III.1 PRÉSENTATION DES MATIÈRES
PREMIÈRES III.1.1 Oxyde de fer (III)
L'oxyde de fer (III), également appelé oxyde
ferrique et sesquioxyde de fer, est le composé chimique de formule
Fe2O3, où le fer a le nombre d'oxydation +III.
L'oxyde de fer III est connu pour sa capacité à
catalyser la réaction de transestérification de manière
efficace, favorisant la conversion des triglycérides en esters
éthyliques ou méthyliques, principaux composants du biodiesel. La
surface spécifique du sesquioxyde de fer influence directement sa
capacité à absorber les réactifs et à fournir des
sites actifs pour la catalyse. Une surface spécifique plus
élevée peut généralement augmenter
l'efficacité du catalyseur.
Ce catalyseur présente généralement une
bonne stabilité et durabilité, ce qui en fait un choix attrayant
pour les applications industrielles à grande échelle mais
également à l'échelle laboratoire.
Il est souvent sous forme de poudre ou de particules, ce qui
facilite sa manipulation dans les réacteurs de
transestérification.
Comparé à d'autres catalyseurs, le sesquioxyde
de fer est généralement économique, ce qui en fait un
choix rentable pour les processus de production du biodiesel.
III.1.2 Huile de soja
L'huile de soja utilisée pour la réaction est
une huile de friture usagée obtenue localement dans la ville de
Lubumbashi dans diverses habitations. Le tableau III.1 suivant indique les
caractéristiques physico-chimiques de l'huile de soja classique selon
différents auteurs.
Le Tableau III.1 représente la
composition de l'huile de soja en acide gras :
L'huile SOYOLA est essentiellement constituée du soja
à 100%, sa composition chimique est reprise dans le Tableau
III.1.
28
Tableau III.1 : Composition de l'huile de soja en acide
gras.
|
Acides gras
|
Symbole
|
Pourcentage en acide gras
|
|
Acide palmitique
|
C16 :0
|
7 à 12
|
|
Acide stéarique
|
C18 :0
|
2 à 5,5
|
|
Acide oléique
|
C18 :1
|
20 à 50
|
|
Acide linoléique
|
C18 :2
|
35 à 60
|
|
Acide arachidique
|
C20 :1
|
1
|
|
Acide gadoléique
|
C20 :1
|
1
|
|
Acide béhénique
|
C22 :0
|
0,5
|
L'huile de soja est riche en acide linoléique (50%) et
en acide oléique (24%) et comprend 15% d'acides gras saturés. La
présence de 7% d'acide linolénique la rend très fragile
à la chaleur et on doit l'utiliser uniquement que pour les
assaisonnements (à froid) [60 ; 61].
III.1.3 Éthanol
De la classe des alcools primaires, l'éthanol de
formule CH3-CH2OH à usage des boissons et usage industriel, est obtenu
par fermentation de solutions sucrées, naturelles (jus de raisin, canne
à sucre, etc.) ou artificielles (hydrolyse de l'amidon). La majeure
partie de l'éthanol à usage industriel est
synthétisé à partir de l'éthanal ou de
l'éthylène issu du pétrole.
L'éthanol a une température de fusion de -
114,1°C, une température d'ébullition de 78,3°C et une
densité de 0,789 à 20°C [62].
L'éthanol est plus soluble mais moins réactif
que le méthanol ce qui a un impact positif sur le rendement mais
négatif sur la vitesse [63] lors des réactions
de transestérification.
III.2 PRODUCTION DU BIOCARBURANT III.2.1
Échantillonnage
La matière première qui a servi à notre
étude est un échantillon obtenu en mélangeant des
équivolumes d'huiles de friture usagées (de la marque SOYOLA)
collectées auprès de trois restaurants de la ville de Lubumbashi
et deux habitations au quartier Gambella II toujours dans la capitale
cuprifère.
29
Calcul des masses de l'éthanol et du
catalyseur
La quantité de l'éthanol à utiliser pour
chaque expérience est déterminée en utilisant
l'équation III.1 suivante :
mEtOH = MEtOH X rapport
mhuile Mhuile
Équation III.1 : Calcul de la masse de
l'éthanol.
Avec :
MEtOH : masse molaire de l'éthanol = 46,068 g/mol
Mhuile: masse de l'huile (utilisée pour chaque
expérience) = 138,3g
Mhuile : Masse molaire de l'huile (g/mol)
Rapport : ratio molaire EtOH/huile
La masse du catalyseur à utiliser pour chaque
expérience est calculée en fonction du
pourcentage de celui-ci par rapport à la masse d'huile
(138,3 g) suivant l'équation III.2 ci-
dessous :
(mhuile X %cat)
Équation III.2 : Calcul de la masse du
catalyseur.
Le Tableau III.2 suivant résume les
conditions opératoires choisies pour les expériences
menées :
Tableau III.2 : Conditions opératoires choisies pour
les expériences.
|
% Catalyseur
Fe2O3
|
Masse du
catalyseur (g)
|
Ratio molaire
EtOH : huile
|
Masse de
l'éthanol (g)
|
Temps de la
réaction (min)
|
|
3
|
4,149
|
3 : 1
|
21,666
|
45
|
|
4
|
5,532
|
4,5 : 1
|
32,499
|
60
|
|
5
|
6,915
|
6 : 1
|
43,332
|
75
|
III.2.2 Synthèse du biodiesel
L'appareil utilisé durant nos expériences, consiste
en un réacteur en verre de 1 L de capacité, muni d'un
réfrigérant, et d'un thermomètre. Le réacteur est
immergé dans un bain marie qui est chauffé à l'aide d'une
plaque chauffante avec agitation magnétique.
Les étapes suivantes ont été suivies pour la
production de nos échantillons :
30
· Mettre à chauffer un bain marie sur une plaque
chauffante ;
· Immerger le réacteur dans le bain marie ;
· Introduire 150 ml de l'huile de friture usagée et
mettre en route le chauffage ;
· Dissoudre le catalyseur dans un peu d'alcool
jusqu'à dissolution totale pour obtenir un mélange
homogène ;
· Le mélange homogène obtenu sera
versé dans le ballon contenant l'huile de friture chaude ;
· Le mélange est agité à l'aide du
barreau magnétique préalablement introduit dans le ballon (600
tr/min) tout en chauffant jusqu'à la température de consigne ;
· Maintenir la température consigne pendant les
minutes choisies (45, 60 et 70) puis arrêter la réaction.
Il est nécessaire de rappeler que l'oxyde ferrique et
l'éthanol ne réagissent pas directement ensemble pour former du
biodiesel.
a. La phase de séparation
À la fin de la réaction, le contenu du ballon
sera versé dans une ampoule à décantation et laisser au
repos pour quelques heures. Durant ce temps-là, la glycérine qui
est immiscible avec les esters se dépose au fond de l'ampoule en gardant
la majorité de catalyseur. La phase supérieure contenant les
esters ou le biodiesel contenant des traces d'alcool, sera
récupéré.
b. Étape de neutralisation
Après récupération du biodiésel,
ce dernier sera neutralisé avec une solution d'acide acétique
jusqu'à pH neutre. Le pH est contrôlé à l'aide de
papier pH.
c. Étape de lavage ou purification
L'étape de lavage de biodiesel est destinée
à éliminer les impuretés du biodiesel telles que la
glycérine résiduelle et l'excès de l'éthanol, les
traces du catalyseur, savons et sels formés par le catalyseur. Le lavage
se fait en ajoutant l'eau au biodiesel dans une ampoule à
décantation. Agiter d'une manière à créer un vortex
pour assurer un rinçage optimal, et répéter cette
étape jusqu'à ce que l'eau de lavage soit claire.
d. Étape de distillation
Pour éliminer les traces d'alcool et les
quantités d'eaux restantes pendant le lavage, l'étape de
distillation est primordiale pour améliorer les caractéristiques
du biodiesel obtenu.
La distillation consiste à chauffer
l'échantillon lentement jusqu'à température
d'ébullition de l'eau, ainsi on s'assure que l'eau et l'éthanol
sont évaporés (Téb de l'éthanol = 78°C).
31
III.2.3 Protocol expérimental
Nous avons réalisé 10 expériences. Elles
ont toutes été réalisées suivant le même
protocole en faisant varier les concentrations du catalyseur, du temps de
réaction et du rapport molaire et en fixant la température de la
réaction à 65°C [39]. Les étapes
suivies sont décrites dans ce qui suit.
III.2.3.1 Prétraitement de l'huile
usagée
a. Filtration
Afin d'éliminer les impuretés solides contenus
dans l'huile usagée, celle-ci a été, dans un premier
temps, filtrée à l'aide d'une passoire, et cela quatre fois pour
éliminer en grande majorité toutes les particules solides.
b. Séchage
La présence d'eau dans l'huile diminue le rendement de
la synthèse, d'où la nécessité de sécher
l'huile avant la réaction en utilisant un agent desséchant, dans
notre cas nous avons utilisé une solution de sulfate de sodium
(Na2SO4).
III.2.3.2 Préparation du mélange
catalyseur/alcool
Une masse du catalyseur est pesée sur un verre de
montre. Le catalyseur est dissout dans un volume adéquat
(Équation III.1) de l'éthanol sous agitation
magnétique et chauffage modéré.
III.2.3.3 Réaction de
transestérification
La solution éthanolique de catalyseur obtenue est
ajoutée à l'huile préchauffée dans un ballon
à la température T de la réaction (Tableau
III.2). La durée de la réaction est variée pour
toutes les expériences. Un montage de chauffage à reflux
thermostaté est utilisé tout en assurant une agitation
magnétique et en contrôlant la température pour la
maintenir constante à 65°C.
III.2.3.4 Purification du biocarburant
a. Décantation
Après la formation des esters au cours de la
transestérification, une étape de décantation du
mélange hétérogène est nécessaire. En effet,
la réaction génère deux nouveaux produits, le
glycérol et le biodiesel. Le glycérol de (couleur marron
foncé) plus dense que le biodiesel se condense dans la partie basse. Les
deux phases peuvent être séparées en soutirant le
glycérol par le bas de l'ampoule à décanter.
32
b. Lavage
Le biodiesel obtenu doit être lavé afin
d'éliminer l'excès d'alcool et de catalyseur résiduels.
Pour cela, le biodiesel est placé dans une ampoule à
décanter puis un volume de 40 ml d'eau distillée est
additionné lentement. Cette opération est délicate, elle
doit être réalisée avec le moins d'agitation possible au
risque de provoquer la formation d'une émulsion qui diminuerait le
rendement de la synthèse.
III.3 CARACTÉRISATION PHYSICO-CHIMIQUE DES
BIOCARBURANTS
III.3.1 Analyses chimiques
III.3.1.1 Indice d'acide
a. Principe
Il s'agit de dissoudre la matière grasse dans de
l'éthanol chaud neutralisé, puis titrer les acides gras libres
(AGL) présents au moyen d'une solution titrée de KOH en
présence de phénolphtaléine comme indicateur
coloré.
b. Mode opératoire
Pour réaliser ce test, une solution de KOH
éthanolique (0,1 M) et 50 ml de solvant constitué d'éther
di-éthylique et d'éthanol dans des proportions de volume à
volume sont préparées au préalable.
La prise d'essai est mise en solution dans 12,5 ml d'un
mélange d'éthanol et d'éther di-éthylique auquel
sont ajoutés quelques gouttes de phénolphtaléine puis
dosé par la solution basique d'hydroxyde de potassium à 0,1M
jusqu'à l'apparition d'une couleur rose persistante.
L'indice d'acide est calculé par l'équation IV.3
suivante :
IA =
V X 56,1 X N
m
Équation III.3 : Calcul de l'indice d'acide.
Avec :
56,1 : Masse molaire de KOH
V : Volume de KOH en ml
N : Concentration de la solution de KOH (0,1mole /l)
m : masse de la prise d'essai en g.
33
III.3.1.2 Indice de saponification
a. Principe
Un excès d'hydroxyde de potassium dans un alcool est
chauffé avec un échantillon de corps gras solubilisé dans
un solvant jusqu'à saponification complète. L'excès
d'alcalin est ensuite titré avec une solution d'acide chlorhydrique.
b. Mode opératoire
Deux solutions de KOH à 0,5 M et de HCl à 0,5 M
sont préparées au préalable.
Une masse d'un gramme du corps gras pesée dans un
bécher est solubilisée dans 12,5 ml du même solvant
utilisé pour l'indice d'acide, puis 25 ml de KOH (0,5 M) sont
ajoutés en prenant soin de maintenir une bonne agitation. Cette solution
du corps gras est placée dans un bain marie bouillant pendant 45
à 60 minutes. À l'issu de cette étape, la solution est
refroidie puis 2 à 3 gouttes de phénolphtaléine lui sont
additionnées.
Nous notons ici qu'un essai à blanc (sans le corps
gras) est traité dans les mêmes conditions. L'excès de
potasse est ensuite dosé par la solution de l'acide chlorhydrique (0,5
M) sous agitation magnétique jusqu'au virage ou à la
décoloration de la phénolphtaléine aussi bien pour la
solution de biocarburant que de l'essai à blanc.
Les volumes d'HCl utilisés pour les divers essais ont
permis grâce à l'équation IV.4 suivante de calculer les
indices de saponification correspondant.
|
IS =
|
V0-V
|
X CHCl X 56,1
|
|
m
|
|
Équation III.4 : Calcul de l'indice de
saponification.
Avec :
V0 : Volume en ml de HCl utilisé pour l'essai à
blanc
V : Volume en ml de HCl utilisé pour l'échantillon
à analyser
m : Masse du corps gras
CHCl : Concentration de la solution de HCl
56,1 : Masse molaire de KOH
III.3.1.3 Indice d'iode
a. Principe
C'est la quantité en grammes d'iode fixée par
addition par 100g de matière grasse en solution
chloroformique (les doubles liaisons des acides gras
insaturés sont capables de subir une
réaction d'addition soit avec I2, soit avec d'autres
halogènes). L'indice d'iode fournit un moyen
pour mesurer le degré d'insaturation de la matière
grasse.
34
b. Mode opératoire
Dissoudre 0,5 g de l'huile dans 10 ml de chloroforme, puis
dans 12,5 ml du diiode (I2) 1N et les mettre dans un erlenmeyer et bien fermer
le récipient, ensuite mettre ce mélange à l'abri de la
lumière pendant deux heures. Au terme de cette durée, on ajoute
10 ml d'une solution d'iodure de potassium (KI) à 50% et 10 ml d'eau
distillée sont ajoutés. Titrer cette solution avec le thiosulfate
en présence de l'empois d'amidon.
L'indice d'iode est calculé par l'équation IV.5
suivante :
II =
m
Équation III.5 : Calcul de l'indice d'iode.
(V1 - V2) X C
Avec :
II : Indice d'iode
C : Concentration de la solution de Na2S2O3 utilisée 1N
V1 : Volume de la solution de Na2S2O3 versée pour l'essai
à blanc (ml)
V2 : Volume de la solution de Na2S2O3 versée pour la prise
d'essai (ml) m : masse de la prise d'essai
III.3.2 Analyses physiques
III.3.2.1 Densité
Pour déterminer la densité du biodiesel produit,
nous avons pesé l'éprouvette vide puis, nous avons
prélevé 45 ml du biodiesel dans la même éprouvette.
Ensuite, nous avons pesé l'éprouvette contenant le biodiesel
à l'aide d'une balance de précision. Enfin, nous avons
prélevé 45 ml d'eau dans une éprouvette où nous
avons pesé cette éprouvette contenant de l'eau.
Nous avons déterminé la densité du
biodiesel en faisant le rapport entre la masse du biodiesel et celle de
référence (eau) par la formule suivante :
méch
d=
mréf
Équation III.6 : Calcul de la
densité.
Avec :
d : densité
méch : masse de l'échantillon (biodiesel) en g
mréf : masse de référence (eau) en g
35
III.3.2.2 Viscosité
Pour réaliser cette analyse, nous avons pesé
l'éprouvette graduée vide puis nous avons prélevé
25 ml du biodiesel dans la même éprouvette où nous avons
encore pesé l'éprouvette contenant l'échantillon à
l'aide d'une balance de précision. Nous avons pesé la bille en
acier, ensuite introduit cette bille en acier de diamètre connu à
l'aide d'un pied à coulisse dans une éprouvette contenant 25 ml
du biodiesel, puis nous avons chronométré le temps de parcours de
la bille dans l'éprouvette. Après, nous avons mesuré la
distance parcourue par la bille dans l'éprouvette à l'aide d'un
pied à coulisse tout en mesurant également le diamètre de
l'éprouvette.
La viscosité du biodiesel est calculée par la
formule de Stokes suivante :
|
ç =
|
ñbille - ñbiodiesel × vbille
× g × 6ð × r × v
|
1 ë
|
Équation III.7 : Calcul de la viscosité par
la formule de Stokes.
Or ë=(1+2,1× R)
Avec :
ç : viscosité dynamique en kg/m.s
ñ : masse volumique en kg/m3
Vbille : volume de la bille en m3
g : accélération de la pesanteur en
m/s2
r : rayon de la bille en m
v : vitesse parcourue par la bille dans l'éprouvette en
m/s
R : rayon de l'éprouvette en m
X : constante de Stokes
36
CHAPITRE IV. ANALYSE ET INTERPRÉTATION DES
RÉSULTATS
Dans ce chapitre, nous aborderons l'analyse et
l'interprétation des résultats obtenus à la suite de notre
étude ou de notre recherche. Nous examinerons les données
collectées, les méthodes statistiques utilisées pour les
analyser, et les conclusions que nous pouvons en tirer.
Ensuite, nous discuterons des résultats obtenus et de
leur signification. Nous mettrons en évidence les tendances
observées, les corrélations entre variables, et toute autre
information importante qui ressort de notre analyse. Nous soulignerons
également les limites de notre étude et les possibles biais qui
pourraient avoir influencé nos résultats.
| 


