III.1.1. Structure des minéraux argileux
Les cristallites d'argile sont formées par empilements
de feuillets bidimensionnels silicatés tétraédriques
condensés avec des octaèdres d'oxyde métalliques dans un
rapport 2:1 ou 1:1. Ainsi, les différents groupes de minéraux
argileux sont distingués par l'arrangement de leurs couches
tétraédriques et octaédriques (figure 4).
Couche tétraédrique
Cette couche est formée par l'enchaînement de
tétraèdres dont les sommets sont occupés par des atomes
d'Oxygène et le centre par un atome de Silicium, comme il peut
être aussi occupé par un atome trivalent Al+3.
Couche Octaédrique
Elle est constituée par un enchaînement de
plusieurs octaèdres dont les sommets sont occupés par des atomes
d'oxygènes et des groupements hydroxyles, conférant ainsi, une
structure hexagonale compacte. Les centres peuvent être occupés
par des atomes variés de valence trois (Al, Fe) ou deux (Fe, Mg)
(Figure I.1).
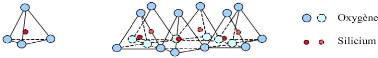
a) tétraèdre couche
tétraédrique
24
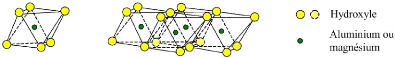
b) octaèdre couche octaédrique
Figure 4: Représentation des couches
octaédriques et tétraédriques. (Bouzid Samia, 2015).
25
III.1.2. Classification des argiles
La classification des minéraux argileux est
généralement basées sur les deux critères suivants
(Rauturreau,1982) :
- Type de feuillet ;
- Charge globale du feuillet.
La classification des minéraux argileux est
généralement basées sur les deux critères suivants
(Rauturreau,1982) :
Type de feuillet ; Charge globale du feuillet.
Les minéraux argileux sont classés en fonction de
différents paramètres : - Le type de feuillets, soit T-O ou
T-O-T
- La nature des cations interfoliaires, qui va influer sur la
capacité d'hydratation/gonflement du minéral argileux ainsi que
sur la propriété d'échange cationique
- La charge du feuillet, dépendant du nombre de
substitutions dites « isomorphiques » qui peuvent intervenir dans la
couche tétraédrique (e.g. Si4+ ? Al3+ ou Fe3+) ou dans la couche
octaédrique (e.g. Al3+ ? Fe2+, Mg2+) contrôlant directement la
capacité d'échange cationique du matériau
- Le type de substitutions, soit des substitutions
majoritairement dans la couche tétraédrique, dans ce cas
là l'argile est trioctaédrique, ou des substitutions
principalement dans la couche octaédrique avec des argiles dites
dioctaédriques
- Ces paramètres contrôlent donc la
classification des argiles de type T-O-T, telle que défnie par les
travaux de l'AIPEA (Association Internationale pour l'Etude des Argiles),
précisé dans (Bailey et al., 1980)
Type de feuillet
Selon le l'épaisseur du feuillet ou sa constitution, on
distingue trois familles principales des argiles (Yassine,2016 ;
Caillère,1982)
- Minéraux à 7Å ou de type 1 :1 (TO)
Le feuillet élémentaire de ces phyllosilicates
est formé par la combinaison d'une couche tétraédrique (T)
et une couche octaédrique (O), son épaisseur est d'environ
7Å. A ce type
26
correspond la kaolinite qui est l'un des minéraux
argileux le plus courant. Les argiles riches en ce type de minéraux sont
souvent valorisées en céramique notamment dans la fabrication de
la porcelaine. Le feuillet de la kaolinite est souvent neutre
dioctaédrique et alumineux de composition (Si2) (Al2) O5 (OH)4. La
distance entre les feuillets est faible vue la forte attraction due aux
liaisons hydrogènes établies entre les hydrogènes des
groupements hydroxyles de la couche octaédrique et les oxygènes
de la couche tétraédrique, outre les liaisons de Van der Waals,
ce qui rend les feuillets difficilement séparables. La kaolinite est
répertoriée parmi les argiles non gonflantes. Les substitutions
isomorphiques sont faibles d'où l'absence de déficit de charge.
La capacité d'échange cationique CEC est donc faible vue qu'elle
provient seulement du caractère amphotère des groupements de
surface. La kaolinite est parmi les rares argiles qui peuvent développer
une capacité d'échange anionique appréciable selon le pH.
Elle possède un point isoélectrique généralement
situé entre pH 2 et 3. Cette famille d'argile est
caractérisée par les réflexions suivantes : d001 aux
environs de 7,14 Å et d002 aux environs de 3,57 Å, et leurs raies
dérivées.
La première correspond à la distance
interlamellaire.
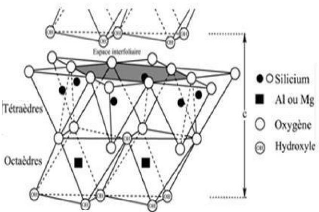
Figure 5:Représentation
schématique de la structure de la kaolinite
- Minéraux a 10 Å ou de type 2:1
(TOT)
Ce type de minéraux est constitué d'une couche
octaédrique située entre deux couches
tétraédriques. L'épaisseur de base du feuillet est de
10Å (figure 7). Cette épaisseur varie en générale
selon la nature du cation interfoliaire et sa sphère d'hydratation. On
distingue deux grandes familles pour ce type de minéraux à savoir
l'illite et les smectites.
27
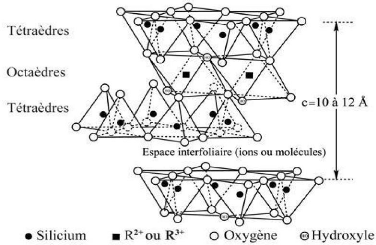
Figure 6:Représentation
schématique de la structure d'une argile de type TOT
- Minéraux à 14 Å ou de type 2 :1
:1 (TOTO)
Le feuillet de type 2 :1 :1 est constitué de
l'alternance de feuillet T-O-T et d'une couche octaédrique
interfoliaire. L'équidistance caractéristique est d'environ 14
Å. A ce type de minéraux appartient la famille du chlorite.
Les chlorites se subdivisent en deux feuillets : un feuillet
hydroxyde qui forme un octaèdre [(Mg, Fe)(OH)6] et un feuillet TOT. Le
déficit de charges du feuillet TOT est compensé par des cations
qui se logent dans les cavités hexagonales sous le feuillet hydroxyde ce
qui provoque la pénétration des molécules d'eau entre ces
deux types de feuillets et par conséquence l'accroissement de
l'équidistance fondamentale.
Minéraux interstratifiés
Ces minéraux interstatifiés se caractérisent
par la superposition de deux ou plusieurs feuillets de nature différente
dans une séquence verticale. Il existe deux types d'interstratification
: interstratification régulière caractérisée par
une périodicité d'empilement des différents feuillets et
interstratification irrégulière qui correspond à un
empilement aléatoire des feuillets de nature différente.
Par ailleurs il existe une cinquième catégorie
d'argiles qui n'est pas répertoriée parmi les argiles
phyllosilicatés. Il s'agit des argiles fibreuses à savoir la
sépiolite et la palygorskite.
28
III.1.3. Propriétés des argiles
Indices de gonflement
Généralement, toutes les argiles
possèdent une capacité de former facilement des complexes
lamellaires par l'insertion des molécules d'eau ou organique dans
l'espace interfoliaire (Figure 7). Ce phénomène est appelé
gonflement, le degré de gonflement ou degré d'hydratation varie
d'une famille argileuse à une autre (Beghou,2020).
Les smectites, les vermiculites et les minéraux
interstratifiés sans parmi les argiles qui se caractérisent par
une capacité d'expansion beaucoup plus importante que celles des autres
espèces argileuses. L'incorporation d'eau est réversible à
la pression atmosphérique et dépend de la température et
de l'humidité relative (la pression de vapeur d'eau) de l'air: plus
l'air est humide, plus l'argile pourra incorporer de l'eau jusqu'à sa
limite de saturation. La plupart des phyllosilicates possédant de telles
propriétés de gonflement sont classés dans la famille de
smectites
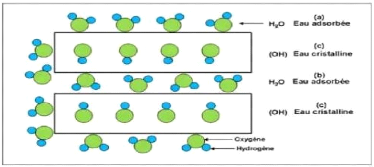
Figure 7:Localisation de l'eau dans les
particules argileuses, (Diatta, 2016).
Capacité d'échange
cationique
Les argiles ont la propriété de fixer de
façon réversible (échangeable) des cations contenusdans
les solutions environnantes, La capacité d'échange cationique
(CEC) est une caractéristique très importante, elle est
définie comme la quantité de cations monovalents et divalents
(Li+, Na+, K+, Ca2+, ou
Mg2+) susceptibles d'être substitués par des cations
compensateurs pour compenser la charge négative de 100 grammes
d'argiles. Elle est conventionnellement exprimée en
milliéquivalents pour 100 grammes d'argile (meq/100g). (Derafa 2014 )
Cette capacité d'échange cationique est considérée
de manière globale et concerne à la fois les cations de l'espace
interfoliaire, les cations de surface et de bordure de feuillets. Il existe
différentes méthodes de mesure de la CEC. En
général, on introduit une
29
montmorillonite naturelle dans une solution contenant un
excès de cations, puis on réalise une analyse
élémentaire afin d'évaluer la quantité de cations
échangés entre l'argile et la solution. Cette méthode se
fait généralement avec NH4 , ou Ba , le dosage est précis
à l'aide de microanalyse élémentaire. Les cations qui
restent dans la montmorillonite définissent la capacité
d'échange cationique qui dépend de l'argile étudie.
(Derafa,2014) Il y a dans les argiles deux principales causes d'existence d'une
capacité d'échange ionique, l'une interne et l'autre externe.
| 


