II.2. Les besoins en vitamines, minéraux
oligoéléments
Certains nutriments sont indispensables parce qu'ils ne
peuvent pas être synthétisés par l'organisme et doivent
donc être apportés par l'alimentation. Les vitamines et les
minéraux en font partie. Leur apport doit être quotidien et
suffisant selon les besoins de l'organisme.

Les besoins sont de 10 ìg/jour durant la grossesse ou
25 ìg/jour au dernier trimestre d'où l'intérêt de la
dose du 7èmemois.
18
Les vitamines
a) Vitamine A
C'est une vitamine indispensable à la
différenciation cellulaire. Il est nécessaire de faire attention
aux compléments vitaminiques car il existe un risque d'hypervitaminose A
qui est soupçonnée d'être
tératogène.[35]
b) Vitamines du groupe B
Les besoins sont souvent couverts par une alimentation
équilibrée (viande surtout le porc et le foie,
céréales, pomme de terre, légumineux.
Bien que l'anémie dans les pays en
développement soit majoritairement due à la déficience en
fer, une partie pourrait être attribuable à un manque de vitamines
du groupe B, en particulier en vitamine B9 (acide folique ou
folates) et en vitamine B12 (Cobalamines). Ces deux vitamines ont
plusieurs répercussions clés sur la santé, notamment au
cours de la grossesse, à la fois pour la mère et pour l'enfant
à naitre. En effet, les développements de l'embryon et du foetus
peuvent être retardés par une carence en vitamine B9 ou
B12. Un développement cognitif altéré et des
mortalités et morbidités augmentées à l'âge
adulte sont également des causes d'inquiétude, en plus des cas
parfaitement prouvés de risque accru de Spina bifida, défauts du
tube neural (DTN). Les principales sources sont la viande (surtout le porc et
le foie), céréales, pomme de terre, légumineux,
légumes verts, levures, abats, céréales,
légumineuses, épinards et fruits à coques.
En cas d'antécédents d'anomalie de fermeture du
tube neural ou de traitement antiépileptique, la supplémentation
périconceptionnelle de la vitamine B9 est de 4 à 5
mg/jour.[1]
c) Vitamine C
L'acide ascorbique est le seul composant usuel de
l'alimentation connu pour être capable d'augmenter la
biodisponibilité du fer non-héminique
Les apports sont couverts par l'alimentation. La
supplémentation à haute dose est dangereuse et réduit
l'assimilation des minéraux (magnésium, cuivre ou zinc).
[18]
d) Vitamine D

19
L'alimentation apporte de 2 à 4 ìg/jour (le lait
enrichi, l'huile de poisson, le beurre, le jaune d'oeuf, le foie) le reste
étant comblé par l'ensoleillement (15
minutes/jour).[35]
e) Vitamine E
Les apports sont souvent inférieurs aux
recommandations. La principale source est représentée par les
matières grasses végétales.[19]
Les minéraux et oligoéléments
1. Le Fer
Les besoins en fer sont considérablement importants
durant la grossesse du fait de l'augmentation physiologique de la masse
érythrocytaire, c'est-à-dire du nombre de globules rouges
maternels (nécessitant environ 500 mg de fer), de la constitution des
tissus du foetus (environ 290 mg de fer) et du placenta (environ 25 mg de fer).
Ces dépenses spécifiques viennent s'ajouter aux pertes basales
(0,8 mg/jour compte tenu de l'interruption des menstruations, soit 220 mg pour
l'ensemble de la gestation).
Au total, c'est plus de 1 000 mg de fer dont la femme enceinte
a besoin pour assurer sa balance en fer au cours de la grossesse ; ces besoins
sont particulièrement concentrés sur le 2ème et
le 3ème trimestre (Tableau III).
Par ailleurs, l'état des réserves en fer au
début de la grossesse est un facteur essentiel pour évaluer les
besoins en fer des femmes enceintes. Si les réserves en fer sont de
l'ordre de 500 mg en début de gestation, ils permettent d'assurer la
couverture des besoins liés à l'augmentation de la masse
érythrocytaire,si elles sont par contre faibles, voire nulles, les
besoins sont difficiles à couvrir par l'alimentation, malgré
l'augmentation de l'absorption du fer observée au cours de la
2èmemoitié de la grossesse.[33]
20
Tableau III. Répartition des besoins en fer (mg)
au cours de la grossesse
Période
Total
Besoins
1er trimestre 2ème trimestre
3ème
-
-
trimestre
Augmentation de la masse
250 250 500

érythrocytaire Fer foetal
Fer du placenta
Déperditions physiologiques
Total
60 230 290
- -
25 25
80 80 80 240
80 390 585 1055
Il convient de noter quela grossesse n'est pas le seul
état qui soit à la base de l'augmentation des besoins en fer,
certaines pathologies ou comportements en sont également responsables :
toutes les causes de saignements chroniques, quelle que soit leur origine
(Épistaxis, hématuries, métrorragies ou saignements du
tractus digestif) notamment lorsqu'ils sont minimes et
répétés favorisent un déséquilibre du bilan
du fer. De nombreuses pathologies peuvent être ainsi impliquées :
fibrome utérin, endométriose, varices oesophagiennes, hernie
hiatale, ulcère, polypes et tumeurs digestives, les
hémorroïdes, la prise de certains médicaments (aspirine, et
à un moindre degré anticoagulants, anti-inflammatoires...), la
géophagie ou les dons du sang (surtout lorsqu'ils sont
répétés plusieurs fois dans l'année) doivent
être pris en compte.[33]
a) Diagnostic de l'anémie ferriprive
La nutrition joue un rôle important dans l'anémie
et, de tous les nutriments impliqués, le fer se trouve être
l'élément le plus crucial. Par conséquent,
l'évaluation de la teneur en fer est bien souvent essentielle au
diagnostic de l'anémie. En général, la carence en fer se
met en place via trois étapes consécutives qui sont
l'épuisement des réserves en fer,
l'érythropoïèse et l'anémie ferriprive. Ces trois
étapes peuvent être analysées sur le plan biochimique par
une mesure de l'hémoglobine (Hb), de la ferritine et du récepteur
soluble à la transferrine (sTfR). Bien qu'il existe des indicateurs
cliniques et que l'évaluation des apports en fer puisse être
utile, le

21
diagnostic repose principalement sur ces marqueurs
biochimiques, qui sont les seuls à présenter la
spécificité et la sensibilité nécessaires.
Malheureusement, les méthodes permettant de les mesurer coutent cher et
sont pour la plupart, difficiles à réaliser.[11]
La ferritine sérique mesurée par un test
radio-immunologique est une glycoprotéine de réserve du fer qui
existe comme une isoferritine tissu spécifique. Les valeurs normales se
situent entre 30 et 300 ng/ml, la moyenne étant de 88 chez l'homme et 49
chez la femme. La ferritinémie est étroitement
corrélée avec les réserves totales en fer de l'organisme ;
c'est ainsi qu'une ferritinémie basse (< 12 ng/ml) n'est
observée que dans les déficits en fer, et une ferritinémie
haute dans les surcharges en fer.
Les récepteurs de transferrine sérique peuvent
être mesurés par le test enzymelinked immuno-absorbent assay
(ELISA) par l'utilisation d'un Ac monoclonal dirigé contre le
récepteur soluble. Les valeurs normales varient de 3,0 à 8,5
mg/ml. Les niveaux augmentent à la phase initiale d'un déficit en
fer ainsi que lorsque l'hématopoïèse est augmentée.
Les niveaux sont normaux dans l'anémie inflammatoire. [18]
b) Les apports alimentaires en fer
Pour faire face aux besoins en fer, l'organisme doit trouver
dans son alimentation la quantité de fer nécessaire. Il est
présent en quantité variable dans de nombreux aliments, mais
seule une fraction du fer consommé est réellement
absorbée, donc, les apports « réels » en fer
dépendent de la teneur en fer de l'alimentation (donc du contenu
variable en fer selon les aliments), mais également de la
biodisponibilité de ce fer (c'est-à-dire sa capacité
à être absorbé et utilisé) et du statut en fer des
individus.
Diverses études faites à l'aide d'aliments
marqués avec du fer radioactif (55Fe, 59Fe) ont mis en évidence
que l'absorption moyenne du fer chez des sujets en bonne santé est
très variable d'un aliment à l'autre. Ces différences
s'expliquent par la forme du fer contenu dans les aliments : fer
héminique ou fer non héminique. La première forme est
présente uniquement dans les aliments d'origine animale où elle
représente environ 40% du fer total, sa biodisponibilité est
d'environ 25% et n'est pas influencée par les autres constituants des
repas, la seconde forme existe, quant à elle à la fois dans les
aliments d'origine animale et dans ceux d'origine végétale.
Dans un régime de type occidental, les principales
sources du fer sont notamment les produits d'origine animale (30 à 35 %
du fer total), les céréales (20 à 30 %), les fruits et
légumes, les racines et tubercules amylacés tandis que dans les
pays en voie de développement, la place du fer fourni par les aliments
d'origine animale est beaucoup plus faible. Le fer non

22
héminique représente à lui seul 90
à 95 % du fer alimentaire consommé dans les types alimentaires
les plus fréquents dans le monde, sa biodisponibilité est faible
(généralement inférieure à 5 %) et peut être
influencée par diverses substances contenues dans d'autres aliments,
ceci aide à comprendre pourquoi, dans ces pays, les populations ont un
risque accru de carence en fer.[33]
Le moment le plus approprié pour se préoccuper
des réserves en fer des femmes en âge de procréer est bien
avant toute grossesse car si les apports alimentaires en fer sont
réguliers chez une femme et avec du fer héminique le mieux
absorbable, un stock suffisant peut être atteint pour aborder la
grossesse dans de bonnes conditions et ainsi éviter des risques
éventuels lors des grossesses ultérieures.
c) Absorption, métabolisme et stockage du
fer
L'absorption du fer est maximale au niveau du duodénum
et du jéjunum, où elle décroît de la partie
proximale à la partie distale. Chez l'homme, seules de petites
quantités de fer sont absorbées au niveau de l'estomac et
exceptionnellement au niveau du côlon. Si le site d'absorption est le
même pour le fer héminique et non héminique, le mode
d'absorption diffère profondément. Le fer non héminique
est libéré des complexes auxquels il est lié dans les
aliments par les sécrétions gastriques (sécrétion
peptique, acide chlorhydrique) ; une fois libéré, il entre dans
un pool où il peut être réduit, chélaté ou
rendu insoluble. Le fer pénètre dans la cellule muqueuse
intestinale en franchissant les microvillosités des cellules
intestinales (entérocytes). A l'intérieur de la cellule muqueuse,
une partie du fer non héminique est liée à des
transporteurs spécifiques et transférée rapidement au
pôle séreux où il se fixe à la transferrine
plasmatique.
L'absorption du fer étant très limitée,
l'organisme possède un mécanisme hautement régulé
de contrôle des besoins journaliers. Les globules rouges vieillis sont
phagocytés par les phagocytes mononucléaires. Une digestion
rapide permet la disponibilité du fer qui est capté par la
transferrine afin d'être réutilisé. Ce système de
réutilisation du fer est si efficace que 97 % des besoins journaliers
(approximativement 25 mg de fer) peuvent être couverts par ce pool de
récupération ; 1 autre mg provient de l'absorption
intestinale.
Le fer des cellules muqueuses intestinales est
transféré à la transferrine, qui est une protéine
de transport du fer avec 2 sites de liaison du fer, synthétisés
au niveau du foie ; ce système est capable de collecter le fer des
cellules (intestinales et macrophages) et de le libérer sur les
récepteurs spécifiques présents sur les
érythroblastes, les cellules placentaires et les cellules
hépatiques. La transferrine se lie aux récepteurs membranaires
spécifiques des érythroblastes, le

23
complexe transferrinefer pénètre à
l'intérieur du précurseur érythrocytaire par endocytose et
le fer est transféré aux mitochondries, qui l'insèrent
dans la protoporphyrine pour le transformer en hème. La transferrine est
recyclée.[18]
Le fer est stocké par la ferritine (dans la muqueuse
intestinale, le foie, la moelle osseuse, les érythrocytes et le plasma)
qui constitue une « poche » pour 4500 ions Fe3+est une
réserve de fer (environ 600 mg) rapidement disponible, alors que le Fe
combiné à l'hémosidérine est plus difficilement
mobilisable (250 mg de Fe dans les macrophages du foie et de la moelle
osseuse).[14]
d) Traitement de l'anémie ferriprive
Avant d'instaurer le traitement par le fer, il faut d'abord
rechercher l'étiologie de son déficit. La plupart des femmes ont
besoin d'une supplémentation en fer ; les sels de fer assurant un apport
de 30 mg de fer/j ou, si la femme est anémique, 60 mg/j doivent
être utilisés. 300 mg de sulfate ferreux per os 2 fois/j suffisent
habituellement, mais le gluconate ferreux à la dose de 450 mg per os 2
fois/j peut être mieux toléré. Des doses plus importantes
irritent le tube digestif de la mère, entraînant une faible
augmentation de la quantité de fer absorbée. De même, une
supplémentation en acide folique doit être prescrite car les
régimes typiques n'en contiennent pas assez.[18]
Dans l'ensemble, la composition en fer, en acide folique
(vitamine B9) et en cyanocobalamine (vitamine B12) des
molécules utilisée dans notre milieu est la suivante :
Acide folique : vitamine B9
FefolTM/FétonTM chaque capsule
contient : 150 mg de FeSO4 équivalent à 65 mg de fer
élémentaire, Acide folique (vitamine B9) 1,0 mg et
cyanocobalamine (vitamine B12) 7,5 mg.
HémoforceTM Sirop Chaque 15 ml (une
cuillerée à soupe) contient : 160 mg de citrate d'ammonium
ferrique équivalent à 32,8 mg de fer élémentaire,
Cyanocobalamine 7,5mg et Acide folique : 0,5 mg. 1 flacon = 200ml
Hémovit® chaque 5 ml contient :
200 mg de citrate d'ammonium ferrique équivalent à 43 mg de fer
élément, vitamine B12 50 mcg, Acide folique 1,5 mg. 1 flacon =
200 ml
Hifer-ZTM Chaque 15 ml (300 mg) contient : 150 mg de citrate
d'ammonium ferrique équivalent à 32 mg de fer
élémentaire, Sulfate de zinc 44 mg, Acide folique 1,0 mg et
vitamine B12 : 7,5 mg.

24
La dose à administrer est calculée selon la formule
:
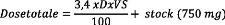
D : déficit en Hb par rapport à la valeur normale
minimale (11g%)
VS : Volume sanguin, chez la femme, VS = Poids (kg) x 65
Or l'absorption d'une tablette est de 25% et les tablettes
contiennent environ 20% de fer élémentaire. Pour parvenir
à une estimation de la dose totale orale qu'on doit donner, il faut
multiplier la dose totale de fer requise par 25. La valeur trouvée est
convertie en grammes et est divisée par le nombre de grammes
donnés par jour pour déterminer la durée de la
prise.[34]
e) Les activateurs de l'absorption du fer -
L'acide ascorbique
Il est le plus puissant facilitateur connu de l'absorption du
fer non héminique. Il n'y a pas de limite à son action
facilitatrice, même à des concentrations très
élevées ; mais au-delà de 100 mg d'acide ascorbique dans
un repas, son effet est moins prononcé. Il facilite l'absorption du fer
par formation d'un chélate de fer soluble à pH bas, qui reste
soluble au pH de l'intestin grêle. L'absorption du fer d'un repas peut
être multipliée par trois lorsqu'il est consommé
simultanément avec 100 ml de jus d'orange et par 7 avec un jus de
papaye. D'autres acides, tels que l'acide citrique et l'acide malique ont
également un effet activateur sur l'absorption du fer non
héminique. [33]
- Les tissus animaux
L'absorption du fer non héminique est
multipliée par 2 ou 3 quand on ajoute au repas des protéines
d'origine animale (viandes et poissons exclusivement). L'action de 1 gramme de
viande est à peu près équivalente à celle de 1 mg
d'acide ascorbique. Le mécanisme exact de cet effet activateur est
encore mal connu. Certaines études impliquent la cystéine comme
étant le facteur facilitateur. Mais cette hypothèse n'a pas
été totalement confirmée.[14]
f) Les inhibiteurs de l'absorption du fer
La meilleure absorption du fer se produit lorsque l'aliment
contient du fer héminique (viande notamment) mais certains produits
alimentaires dont les phytates et les polyphénols des fibres
végétales ; les tannins du thé, phospho-protéines
inclues et le sonréduisent

Récemment, a été également mis en
évidence un effet inhibiteur des protéines de soja sans que le
mécanisme en soit connu.[33]
25
l'absorption du fer non hémique. Ainsi, de nombreuses
interactions alimentaires provoquent une réduction de la
biodisponibilité du fer.
- Les tannins
Une seule tasse de thé prise au cours d'un repas peut
faire chuter l'absorption du fer de 11 % à 2,5 %. L'absorption du
chlorure de fer diminue de 22 à 6 % lorsque les comprimés sont
pris en même temps que du thé. L'effet inhibiteur des tannins
résulte de la formation de précipités insolubles de
tannates de fer. Le thé constitue expérimentalement le plus
puissant inhibiteur de l'absorption de fer actuellement connu.Par contre, le
thé sans tannin n'a pas d'action sur l'absorption du fer.
Les tannins sont également présents dans le
café, mais l'effet inhibiteur du café sur l'absorption du fer est
bien moindre que celui du thé. Cet effet pourrait être
également lié à la présence d'autres
composés poly phénoliques. Les tannins sont aussi largement
répandus dans les végétaux et leur présence
pourrait expliquer la faible absorption du fer contenu dans ce type
d'aliments.
- Le rapport calcium/phosphate
Ce fait a été attribué au vitellin,
principal complexe phosphorrotéique dans le jaune d'oeuf. Les
composés phosphatés contenus dans un repas constitueraient des
inhibiteurs de l'absorption du fer par la formation de phosphate ferrique
insoluble. Cet effet serait majoré par la présence
simultanée de calcium dans le repas ; le fer serait
co-précipité par un complexe insoluble calcium-phosphate.
[14]
- Les protéines
Il est difficile d'apprécier le rôle direct des
protéines sur l'absorption du fer. Bien que les pouvoirs facilitateurs
de la viande ont souvent été attribués aux
protéines (sans que ceci puisse être réellement
démontré), des études récentes ont montré
que certaines protéines semi purifiées peuvent inhiber
l'absorption du fer. Lorsque l'on double la quantité d'albumine de
l'oeuf dans un repas, l'absorption du fer chute de 2,3 à 1,4 %. A
l'inverse, lorsque l'on soustrait cette protéine, l'absorption du fer
augmente de 3,8 à 9,6 %.

Il faut encourager dans ce cas, une consommation d'aliments
riches en iode (produits laitiers, poissons, crustacés, oeufs et sel
enrichi).
26
- Les phytates
Des études utilisant des marqueurs radioactifs ont
confirmé l'effet inhibiteur du son et de nombreux travaux ont
rapporté cet effet à la présence de phytates. Cependant,
des études plus récentes chez l'homme et chez l'animal
considèrent que les phytates ont peu d'effet sur l'absorption du fer :
l'effet inhibiteur du son n'est pas modifié après destruction par
hydrolyse enzymatique des phytates. [18]
- Le cuivre et le zinc
Le cuivre et le zinc sont des nutriments essentiels et des
carences en ces deux minéraux conduisent à l'anémie. Les
études expérimentales ont montré un effet inhibiteur du
zinc sur l'absorption du fer et il a été proposé que ces
deux micronutriments rivalisent pour une voie d'absorption commune, toutefois
les mécanismes exacts impliqués dans cette interaction au niveau
de l'absorption ne sont pas encore totalement compris. Il a également
été démontré que de fortes doses de zinc inhibent
l'absorption du cuivre et peuvent produire un déficit en ce dernier
élément, ce qui pourrait indirectement affecter le statut en fer
et mener à l'anémie. Le zinc et le cuivre ont une interaction
antagoniste au sein de l'érythrocyte.[11]
2. Le Calcium
Le calcium contribue à la minéralisation du
squelette foetal. Pendant la grossesse, il y a une augmentation de l'absorption
intestinale du calcium.
Le statut maternel ne sera pas affecté si les apports
calciques sont adéquats soit une consommation quotidienne d'un litre de
lait + 30 g de fromage + 1 yaourt (environ 1 000 mg/j). Pour les femmes qui
n'aiment pas ou ne tolèrent pas les produits laitiers, une eau riche en
calcium ou des produits sans lactose sont conseillés.
De plus, il est recommandé la prescription d'unedose
unique de Vitamine D (100 000 UI) au début du 7èmemois, afin de
favoriser l'absorption intestinale du calcium.[33]
3. L'Iode
La grossesse augmente les besoins et contribue à
l'apparition ou à l'aggravation des déficiences
modérées.

6. Le Fluor
Si l'efficacité de l'administration systématique
de fluor de la naissance jusqu'à 12 ans est parfaitement
étayée dans la prévention des caries, aucune preuve ne
montre que l'administration systématique pendant la grossesse apporte
des bénéfices supplémentaires aux dents des
enfants.[33]
27
4. Le Magnésium
L'alimentation est généralement suffisante pour
faire face à la demande foetale et la croissance des tissus
maternels.
Le magnésium est présent surtout dans le
chocolat, les légumes, les fruits secs et les produits
céréaliers.
5. Le Zinc
Une alimentation riche en protéines animales suffit
à couvrir les besoins.Des carences peuvent apparaître en cas
d'alcoolisme, de tabagisme, de régime végétarien.

| 


