3.5. Etude de la capacité
d'adsorption du bioadsorbant vis-à-vis du BM
3.1.8. Essais d'adsorption
Les essais d'adsorption ont été effectués
dans un adsorbeur LACOPE avec 100 mL de solution du BM pour déterminer
l'adsorption en fonction de la masse, du temps, du pH et de la
concentration du bleu de méthylène.
Cette étude a permis de déterminer les
paramètres suivants : le temps nécessaire pour atteindre
l'équilibre entre l'adsorbant en solution et l'adsorbat fixé sur
le bioadsorbant, le pourcentage d'adsorption (%) et la capacité
d'adsorption (Q).
3.1.9. Capacité d'adsorption du
bioadsorbant en fonction du temps d'adsorption
Les expériences d'adsorption en fonction du temps
d'adsorption ont été effectuées suivant le mode
cuvé (batch ou discontinu) dans des adsorbeurs hermétiques
(LACOPE ADS X-3), avec les masses de 10 mg à 1000 mg de Bioadsorbant MA.
La solution de BM 50 mg L- 1 est utilisée pour toutes les
expériences d'adsorption en fonction du temps d'adsorption de
Bioadsorbant MA. L'adsorption en fonction du temps d'adsorption de bioadsorbant
BMA a été étudiée en solution aqueuse au pH
d'autoéquilibre (6,69).
Pour chaque expérience d'adsorption, une masse de
bioadsorbant est placée dans l'adsorbeur ; on ajoute 100 mL de la
solution de BM. La suspension est agitée pendant 1 à 450
minutes.
Après agitation, la suspension est centrifugée
(Centrifugeuse LABOFUGE 200 HERAEUS) pendant 30 minutes à 3000 rpm ; le
centrifugeât est alors analysé à la longueur d'onde
requise. La capacité d'adsorption du bioadsorbant MA a été
calculée selon la formule :
Q 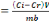 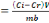 [11]
[11]
Avec :
Q : capacité d'adsorption
(mg/g) ;
Ci : concentration initiale (mg/L) ;
Cr : concentration résiduaire
(mg.L-1) ;
V : volume de la solution (L) ;
mb : masse du bioadsorbant
La concentration résiduelle de la solution après
adsorption est donnée par la relation suivante :
A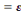 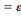 .l.Cr
[10] .l.Cr
[10]
Avec :
A : absorbance ou densité optique
(D.0) ;
å : coefficient d'absorption molaire
(L.mg-1.cm-1) ;
l : longueur du chemin optique (cm) ;
Cr : concentration résiduaire
(mg.L-1)
Le pourcentage d'adsorption est donné par
l'équation suivante :
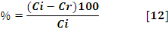
Avec :
Q : capacité d'adsorption (mg/g)
Ci : concentration initiale (mg/L)
Cr : concentration résiduaire
(mg.L-1).
3.1.10. Capacité d'adsorption du B.A en fonction de la
masse du Bioadsorbant
Les expériences d'adsorption en fonction de la masse du
Bioadsorbant ont été effectuées selon le même mode
et le même protocole expérimental que pour les expériences
d'adsorption en fonction du temps d'adsorption. Les masses de 10 mg à
1000 mg de Bioadsorbant ont été utilisées et le temps
d'agitation a été varié de 1 à 450 minutes. La
concentration résiduelle (Cr), la capacité d'adsorption (Q), le
pourcentage d'adsorption (% ads) ont été
calculés selon les formules présentées ci-haut.
3.1.11. Capacité d'adsorption du bioadsorbant en
fonction du pH
L'effet du pH de la solution de BM sur la capacité
d'adsorption du Bioadsorbant a été étudié aux pH
suivants : 3, 4, 5, 8, 10 et 12. Les expériences sont
réalisées suivant le mode discontinu en utilisant 100 mL de la
solution de BM 50 mg L-1 et 200 mg de Bioadsorbant, masse optimale
déterminée expérimentalement en étudiant
l'adsorption en fonction de la masse de bioadsorbant. Le temps d'adsorption est
varié de 0 à 450 minutes. Le même protocole
expérimental utilisé pour les expériences d'adsorption en
fonction du temps a été appliqué.
3.1.12. Capacité d'adsorption du
bioadsorbant en fonction de la concentration.
L'effet de la concentration initiale est réalisé
suivant le mode discontinu pour les concentrations des solutions de BM de 1 mg
L-1 à 100 mg L-1, en vue de déterminer les
isothermes d'adsorption. Le temps d'agitation est fixé à 240
minutes pour le pH 3 et pH 4 et à 300 minutes pour le pH 5, 8, 10 et 12,
temps se situant dans le domaine d'équilibre, pour tous les pH
étudiés. Le protocole expérimental est le même que
celui suivi pour l'adsorption en fonction du temps d'adsorption.
3.1.13. Isothermes d'adsorption
Les isothermes d'adsorption ont été obtenues en
étudiant l'adsorption de BM sur le Bioadsorbant 100 mL des solutions de
concentrations 1 mg L-1 à 100 mg L-1 ont
été utilisés. Les essais ont été
effectués avec 200 mg de bioadsorbant, masse optimale
déterminée expérimentalement.
3.1.14. Modélisation des isothermes
d'adsorption
La modélisation des isothermes d'adsorption a
été faite en recourant aux modèles d'équilibre de
Langmuir et de Freundlich (Kifuani, 2013).
a. Le modèle de Langmuir
Le modèle de Langmuir a été
utilisé sous sa forme linéaire donnée par
l'équation ci-dessous :
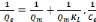 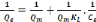 [13] [13]
Avec :
Qe: quantité du soluté
fixée par unité de masse de l'adsorbant (capacité
apparente d'adsorption) ;
Qm : quantité maximale du
soluté fixée par unité de masse d'adsorbant.
En portant 1/Qe en fonction de
1/Ce , Cette équation permet de calculer les
paramètres Qm et KL, à
partir de l'ordonnée à l'origine et de la pente,
respectivement.
b. Le modèle de Freundlich
L'équation linéaire de Freundlich a
été utilisée:
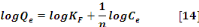
Avec
· Qe et Ce :
concentrations du soluté dans le complexe solide et en solution,
respectivement ;
· KF : constante de Freundlich,
une constante qui est relative à la capacité d'adsorption ;
C'est donc la capacité d'adsorption lorsque la
concentration à l'équilibre est unitaire.
La constante adimensionnelle n est en rapport avec
l'intensité d'adsorption. En portant log Qe en fonction de log
Ce, cette équation permet de calculer les paramètres
KL et 1/n à partir de l'ordonnée à
l'origine et de la pente, respectivement.
| 


