|

ÉíÈÚÔáÇ
ÉíØÇÑÞãíÏáÇ
ÉíÑÆÇÒÌáÇ
ÉíÑæåãÌáÇ
Ministère de l'Enseignement Supérieur et
de la Recherche Scientifique Université Ibn Khaldoun - Tiaret
-
Faculté des Sciences de la Nature et de la
Vie
Département des Sciences de la Nature et de la
Vie
Mémoire en vue de l'obtention du diplôme
de Master
académique
Domaine : "Sciences de la Nature et de la Vie"
Filière : "Sciences Biologiques"
Spécialité : "Microbiologie
Appliquée"
Présenté et soutenu publiquement par :
- LOUZIR Slimane - SEKKINE Ghania
Thème
Contribution à l'étude de
l'effet
bactéricide de l'argile sur
Escherichia
Membres du jury : Grade :
- Président : Mr HOCINE L. MCA
- Promoteur : Mr HADJ SAID A. MCA
- Co-Promoteur : Mme MOULAY M. MCA
- Examinateur : Mr BENBEGUARRA M. MCA
Année universitaire: 2019/2020

Remerciements
Nous tenons en premier à remercier Dieu Le Tout
Puissant de nous avoir donné le courage, la volonté, l'amour du
savoir et surtout la patience pour pouvoir produire ce modeste travail.
Nous tenons à remercier très chaleureusement
notre promoteur Mr HADJ Said. A pour sa sympathie, sa disponibilité,
d'être toujours accueillant à notre égard
et de nous avoir fait bénéficier de ses
grandes compétences scientifiques et intellectuelles, ses orientations,
ses conseils, ses remarques pertinents et surtout son aide pendant tout cette
année et tout au long de la réalisation de ce travail.
Nous tenons remercier aussi notre Co-promotrice Mme MOULAY M.
Pour son aide, ses orientations judicieuses, ses qualités d'ordre et
d'efficacité et pour l'élaboration de ce travail.
On exprime nos remerciements aux honorables membres de jury
:

Au président du jury : Monsieur HOUCINE L. qui nous a
fait l'honneur de
Présider le jury de notre mémoire.
Au Examinateur : BENBEGUARRA M. Nous avoir honorées
en acceptant de jurer ce modeste travail.
Au personnel de laboratoire de microbiologie
appliquée, à Mme Kheira et Mme

Zahra
Et a tous ceux qui ont participé de près ou de
loin à la réalisation de ce travail,
Trouvez ici l'expression de notre profonde
gratitude.

Dédicace
,fie remercie tout d'abord, Allah, le tout puissant et
clément de m'avoir aidé à réaliser ce
travail
,fie dédie ensuite ce fameux travail aux plus
exceptionnels qui existent dans le monde
Mon Père : Toute ma gratitude pour leur
soutien
tout au long de mes études Qu'Allah ,fie le garde
Ma Mère : C'était magnifique si vous
étiez présent
à voir votre fille diplômée.
Pas de basse c'est le
destin. ,fie vous le dit qu'une personne chère ne
nous
quitte jamais. Elle vit au plus profond de notre
coeur et pour la
revoir, il est suffit de fermer les
yeux ; Sois toujours fier de moi où tu es
A mes chères soeurs « Dalila, Naima,
Soundous,
Nada rawan »
A mes chères frères « Mohammed, Ali,
Nabil »
Et à toute la famille SEKKINE
A mes amies « Zahira, Chaima, Widad,
Manel,
Nessrin, Samia, Habiba et A ceux qui m'aiment, qui
font partie de
ma vie
A mon binôme « Slimane et sa
famille »
Et à toute la promotion de Microbiologie
appliquée
2019 -2020.
GHANIA

Dédicace
Je dédie ce modeste travail :
A la femme que j'aime le plus au monde, la lumière
de mes
jours, la source de mes efforts, la flamme de mon coeur, ma
vie et
mon bonheur, maman que j'adore.
A mon très cher père mon soutien moral et
source de joie et
de bonheur, qui a été toujours là
pour moi, que dieu te
procure bonne santé et longue vie.
A ma très chère tante que j'aime beaucoup,
qui s'est toujours sacrifié pour me voir réussir, qui
était toujours à mes côtés.
Aux personnes que j'adore ma deuxième maman «
Zohra »
mes soeurs : « Souad et Souassen », mes frères
: « Mohamed,
Riad et Sid Ahmed ».
A toute ma famille.
A ma binôme GHANIA et toute la
famille SEKKINE.
Aux personnes qui m'ont accompagné durant mon
chemin
d'études supérieures, mes aimables amis et
collègues d'étude.
Et à tous ceux qui ont contribué de
près ou de loin pour
que ce projet soit possible, je vous dis
merci.
LOUZIR SLIMANE
Citation

« Nul ne fait de bonnes actions aussi valeureuses
que
prier, réconcilier les gens et avoir un bon
comportement. »
Liste des abréviations I
Liste des tableaux II
Liste des figures III
Liste des photos IV
Table des matières
Introduction .. 1
Chapitre I Partie bibliographique
1. L'argile 2
1.1. Introduction 2
1.2 Origine de la bentonite 2
1.3. Structure et composition de la bentonite 2
1.4. Propriétés de la bentonite 3
1.5. Utilisation de la bentonite .. 3
2. Escherichia coui .. 4
2.1. Définition 4
2.2. Habitat 4
2.3. Classification . 4
2.4. Caractéristiques biochimiques et antigéniques
.. 5
2.5. Pouvoir pathogène naturel . 5
Partie expérimentale
Chapitre II Matériel et
méthodes
1. Objectif du travail .. 6
2. Lieu et période de travail 6
3. Matériel .. 6
4. Méthodes. .. 8
4.1. Protocole expérimental 8
4.2. Ré-identification des souches 9
4.2.1. Repiquage des souches 9
4.2.2. Tests d'identification d'E.coli
......................................................... 9
I. Etude morphologique 9
I. 1. Examens macroscopiques . 9
I. 2. Examens microscopiques .. 9
II. Etude biochimique 11
II. 1. Recherche des enzymes respiratoires 11
II. 1.1. Test de la catalase .. 11
II. 1.2. Test d'oxydase 11
II. 2. Recherche de type respiratoire .. 12
II. 3. Galerie biochimique classique .. 12
II. 4. Galerie API 20E 14
4.2.3. Standardisation de la souche à l'échelle
McFarland 0.5 . 15
4.3. Préparation de l'argile 15
4.3.1. Bentonite de Maghnia 16
4.3.2. Tamisage de la bentonite 16
4.3.3. Stérilisation de la bentonite 16
4.3.4. Taux d'humidité 16
4.3.5. Préparation de solution mère . 16
4.3.6. Détermination de pH 17
4.3.7. Préparation des dilutions 17
4.4. Préparation des disques .. 17
4.5. Activité antibactérienne .. 18
4.5.1. Antibiogramme 18
4.5.2. Les étapes de la préparation des deux 02
témoins et ceux avec une quantité
connue de l'argile 19
4.6. La concentration minimale inhibitrice (CMI) 19
Chapitre III Résultats et
discussion
1. Ré-identification d'E.coui
.................................................................................
21
1.1. Etude morphologique . 21
1.1.1. Observation macroscopique 21
1.1.2. Observation microscopique .. 21
1.2. Etude biochimique .. 22
1.2.1. résultats d'enzyme respiratoire 22
1.2.2. Galerie biochimique classique . 22
1.2.3. Galerie API 20E .. 23
2. Activité antibactérienne .. 24
2.1. Résultats des témoins .. 24
2.2. Activité antibactérienne de la bentonite sur
l'Escherichia coui 25
Conclusion . 30
Références bibliographiques 31
Annexes
I
Liste des abréviations
|
·
|
API
|
:
|
Appareils et procédés d'identification.
|
|
·
|
ATB
|
:
|
Antibiotique
|
|
·
|
CA -SFM
|
:
|
Comité d'antibiogramme de la société
française de microbiologie
|
|
·
|
CEC
|
:
|
Capacité d'Echange Cationique
|
|
·
|
CMI
|
:
|
Concentration minimale inhibitrice
|
|
·
|
COVID-19
|
:
|
Corona virus disease 2019.
|
|
·
|
E.coli
|
:
|
Escherichia coui
|
|
·
|
ENF
|
:
|
Enterprise Nationale de Fonderie
|
|
·
|
EUCAST
|
:
|
European Committee on Antimicrobial Susceptibility
|
|
|
|
Testing.
|
|
·
|
T.S.I
|
:
|
Triple-Sugar- Iron
|
|
·
|
UFC
|
:
|
Unité formant colonie
|
II
Liste des tableaux
Tableau 1. Classification d'Escherichia
coli ........................ 4
Tableau 2. Matériel utilisé
dans l'expérimentation . 7
Tableau 3. Galerie biochimique classique
d'identification d'Escherichia coui 12
Tableau 4. Antibiotiques utilisés pour
E.coli 19
Tableau 5. Résultats de la galerie
biochimique classique et type respiratoire sur milieu
Schubert cloche 22
Tableau 6. Résultats de la Galerie API
20 E .. 24
Tableau 7. L'antibiogramme d'E.coli
...........................................................25
Tableau 8. Article de Santos et al.,
2011 ... 26
Tableau 9. Article de Yuhang et al.,
2004 28
Tableau 10. Tests microbiologiques appliquant
la méthode de la concentration
minimale inhibitrice 27
Tableau 11. La capacité
antimicrobienne de cu2+/montmorillonite sur E.coli ..
28
III
Liste des figures
Figure 1. La structure d'une montmorillonite
... 3
Figure 2. Protocole expérimental 8
Figure 3. Les étapes de la
préparation de la bentonite 15
Figure4. Bentonite de Maghnia en poudre . 16
Figure 5. Préparation des dilutions
17
Figure 6. L'antibiogramme d'E.coli
25
Figure 7. Résultats microbiologiques
appliquant la méthode de diffusion sur gélose à la
bentonite brute 26
Figure 8. Tests microbiologiques appliquant la
méthode de diffusion sur gélose à la
bentonite échangée par Ag+ montant la
présence d'un effet bactéricide ... 26
Figure 9. Tests microbiologiques appliquant la
méthode de diffusion sur gélose
montrant une comparaison entre les effets bactéricides ..
27
Figure 10. Valeurs de diamètres ou halos
pour la bentonite échangée avec Ag+ activée par l'acide et
la bentonite échangée avec Ag+ prétraitée montrant
une comparaison
entre les effets bactéricides sur l'E.coli 26
IV
Liste des photos
Photo 1. Milieu Mannitol-Mobilité .
12
Photo 2. Milieu Citrate de simmon . 13
Photo 3. Milieu T.S.I 13
Photo 4. Aspect macroscopiques de souches
d'E.coli sur gélose Mac Conkey .. 21
Photo 5. Observation microscopique d'E.coli
après coloration de Gram 21
Photo 6. Milieu Mannitol-Mobilité
après incubation . 22
Photo 7. Milieu Citrate de simmon
après incubation .. 22
Photo 8. Milieu T.S.I après incubation
22
Photo 9. Milieu Schubert avec cloche
après incubation .. 22
Photo 10. Résultats API 20 E
d'E.coli après incubation 23
ntroduction
Page | 1
Introduction
Dans la lutte antibactérienne, les moyens d'action sont
de plus en plus limités. Les antibiotiques, qui semblaient être le
remède miracle contre de nombreuses infections il y a moins d'un
siècle, sont désormais obsolètes. Les bactéries
communiquent et s'échangent des gènes de résistance, ce
qui leur permet de lutter contre les antibactériens. La
multirésistance aux antibiotiques est devenue un problème de
santé publique majeure, et de nouveaux moyens de traitements sont
nécessaires.
En particulier, l'Escherichia coui est la
bactérie la mieux étudiée et également le
microorganisme expérimental de choix pour beaucoup de microbiologistes.
Cette bactérie majeure du colon humain et des animaux à sang
chaud est très utile pour l'analyse de la contamination fécale.
Par ailleurs, C'est la bactérie la plus fréquemment
impliqué dans les infections urinaires. Elle peut aussi provoquer des
diarrhées par des mécanismes très divers, ainsi que
diverses infections communautaires ou nosocomiales (Bourjilat,
2009).
A côté des antibiotiques, d'autres voies sont
explorées pour combattre les infections. Utilisées depuis
longtemps dans les anciens pays de l'Est, les bactériophages suscitent
un regain d'intérêt en France, où ils font l'objet de
recherches et bientôt d'un essai contrôlé. Aussi la
recherche de nouveaux antibiotiques qui sont efficaces sur les bactéries
résistantes. Et y'en a aussi la lutte biologique,
précisément par utilisation de micro-organismes
entomopathogènes (qui luttant les insectes) est une alternative
très prometteuse pour assurer une protection phytosanitaire. Il existe
des moyens de lutte par l'utilisation des agents naturels tels que l'argile
En effet, l'argile est un outil thérapeutique
très ancien. Les Égyptiens l'utilisaient dans le
procédé de momification et dans le traitement des
diarrhées, des abcès et des blessures. Durant la première
guerre mondiale, les médecins allemands et autrichiens s'en sont
également servis pour soigner la dysenterie, une maladie infectieuse du
côlon.
On ne trouve pas une mais des argiles. De part une structure
spécifique, ainsi que des propriétés multiples, les
argiles répondent à de nombreuses indications. Elle est
déformable, transformable, adhérente, coulante, glissante, et a
ainsi de nombreuses capacités parmi lesquelles le transport, la capture,
la libération de substances liquides, gazeuses...etc. Sa richesse
minérale et en oligo-éléments en fait un outil dans la
santé, le bien-être, la beauté, l'entretien du corps, de la
maison, des constructions, dans l'industrie (Adrianne, 2003).
L'argile était utilisée comme un antipoison naturel radicalement
efficace. Elle possède un fort pouvoir absorbant et adsorbant qui attire
les poisons, toxiques et impuretés du conduit digestif sans les
relâcher. Une manière efficace de nettoyer le système
digestif et de débarrasser l'intestin des toxines, germes, et
bactéries pathogènes sans pour autant détruire la flore
intestinale comme le feraient des antibiotiques (Theodorou et al.,
1994).
D'après le grand usage de la bentonite dans
différents domaines, la question qui vient à l'esprit dans ce
cas-là est : si la bentonite a un effet antibactérien ?
L'objet de ce travail est de savoir si la bentonite à
un effet sur la bactérie Escherichia
coui.

Chapitre I
Partie
bibliographique
Chapitre I Partie bibliographique
Page | 2
1. l'argile
1.1. Introduction
Les argiles présentent un intérêt
croissant car leurs applications industrielles ne cessent de se diversifier.
L'argile qui fait l'objet de ce travail est connue sous le nom de
"bentonite", largement utilisée dans de nombreux
secteurs industriels. Sous sa forme pâteuse ou à l'état de
poudre, ce type d'argile est employé dans la réalisation de
barrières étanches pour les déchets industriels,
ménagers (géomembranes bentonitiques) et radioactifs
(barrières ouvragées, poudre compactées). La bentonite est
utilisée également dans l'industrie agroalimentaire et dans la
composition des produits cosmétiques et pharmaceutiques... (Besq
et al., 2003).
En Algérie, les gisements de bentonite les plus
importants économiquement se trouvent dans l'Oranie (ouest
algérien). On relève en particulier la carrière de Maghnia
(Hammam Boughrara) dont les réserves sont estimées à un
million de tonnes et de celle de Mostaganem (M'zila) avec des réserves
de deux millions de tonnes. (Abderrahim et al.,
2006).
1.2. Origine de la bentonite
L'altération et la transformation hydrothermale de
cendres des tufs volcaniques riches en verre entraînent la
néoformation des minéraux argileux, qui font partie
principalement du groupe des Smectites. Les roches argileuses ainsi
formées portent le nom de bentonite, d'après le gisement
situé près de Fort Benton (Wyoming, Etats-Unis). Elle contient
plus de 75 % de montmorillonite ; cette dernière fut découverte
pour la première fois en 1847 près de Montmorillon, dans le
département de Vienne (France) (Airoldi et Critter.,
1997 ; Ferrah, 2013).
1.3. Structure et composition de la bentonite
Certaines bentonites sont riches en sodium, d'autres en
calcium, potassium ou magnésium. Les bentonites à base de sodium
sont dotées de très grandes capacités d'absorption des
liquides et susceptibles de se transformer en gel à partir d'une
certaine concentration. En présence d'eau la bentonite gonfle de 10
à 15 fois son volume initial et absorbe 6,5 fois son poids en eau. Ayant
la faculté de favoriser la pénétration des principes
actifs à travers la peau, elle est incorporée aux
cosmétiques naturels. Appelée également terre à
Foulon, la bentonite est aussi capable d'absorber les protéines et de
réduire l'activité des enzymes Ce sont les bentonites riches en
calcium qui sont utilisées au niveau de la sphère digestive.
Retrouvées dans la composition de pansements gastriques, dans le
traitement d'ulcère de l'estomac, constipation, diarrhée, reflux
gastrique... Elles sont aussi utilisées dans les litières pour
chat (Darcel, 1982).
La bentonite est une roche argileuse, friable, tendre et
onctueuse au toucher, sa teinte dépend des composés
minéraux et impuretés (matière organique et oxydes des
métaux) qui lui sont étroitement associés. Elle est
blanche, grise ou légèrement jaune. Elle se caractérise
par une capacité élevée d'adsorption, d'échange
ionique et de gonflement (Airoldi et Critter, 1997). Elle est
constituée, principalement, par un minéral argileux appelé
montmorillonite qui est représentée dans la figure
1.

Chapitre I Partie bibliographique
Page | 3
Figure 1 : La structure d'une montmorillonite
(d'après Grim, 1968).
1.4. Propriétés de la bentonite
Les propriétés sont définies par la
constitution chimique, l'épaisseur et l'écartement des feuillets
de l'argile.
Les substitutions isomorphiques dans la partie cristalline de
la montmorillonite sont à l'origine de la charge négative
à la surface des feuillets. Cette charge négative, appelée
charge permanente, permet à la montmorillonite d'échanger des
cations (capacité, CEC) et d'adsorber des molécules d'eau
(capacité de gonflement).
Elle a plusieurs autres caractéristiques
intéressantes qui peuvent être résumées par sa
grande surface spécifique, son coût modéré et son
état colloïdal (Wang et al., 2007).
1.5. Utilisation de la bentonite :
La bentonite est l'argile industrielle la plus importante en
raison de son principal composant de montmorillonite qui lui confère une
capacité d'absorption et de gonflement très élevées
qui sont exploités dans différents domaines dont :
§ Protection environnementale.
§ Forage.
§ Les céramiques.
§ Les peintures.
§
Chapitre I Partie bibliographique
Page | 4
L'agroalimentaire.
§ Décoloration des huiles.
§ Raffinage du pétrole.
§ Additif dans la fabrication du
papier.
§ Génie civil (additif dans le
ciment).
§ Traitement des eaux usées.
§ La pharmacie et la cosmétique.
Les bentonites sont largement utilisées dans l'industrie
cosmétique et pharmaceutique en tant qu'excipient, ingrédients
actifs et transporteur et libérateurs d'ingrédients
actifs (Lopez-galind et Viseras, 2004 ; Guenoun et Gada,
2017)
2. Escherichia coli
2.1. Définition
Escherichia coui est une bactérie
naturellement présente dans la flore intestinale. La plupart des souches
de cette bactérie sont sans danger pour la santé, certaines sont
à l'origine d'infections intestinales plus ou moins graves.
2.2. Habitat
E. coui est l'espèce prédominante de la
flore aéro-anaérobie facultative du tube digestif chez l'homme et
chez de nombreuses espèces animales (Mariani-Kurkdjian et
Bingen., 2012). La bactérie E. coui est
présente principalement au niveau du colon et du cæcum à
des concentrations supérieures à 106 UFC/g de contenu
intestinal (Lefebvre et al., 1988). Elle demeure
très souvent dans le mucus recouvrant les cellules
épithéliales de la paroi du tube digestif (Smati et
al., 2015).
2.3. Classification
E. coui est une espèce bactérienne du
genre Escherichia, appartenant à la famille des
Enterobacteriaceae, ordre des Enterobactériales, phylum des
Proteobacteria, classe des Gammaproteobacteria (Bergy's manuel, 2004 ;
Diassana, 2018). La classification est présentée dans le
tableau 1
Tableau 1 : classification d'Escherichia
coui
|
Règne
|
Procaryotae
|
|
Domaine
|
Bactéria
|
|
Phylum
|
Protéobacteria
|
|
Classe
|
Gammaproteobacteria
|
|
Ordre
|
Enterobacteriales
|
|
Famille
|
Enterobacteriaceae
|
|
Genre
|
Escherichia
|
|
Espèce
|
Escherichia coui
|
Chapitre I Partie bibliographique
Page | 5
2.4. Caractéristiques biochimique et
antigénique
Ce sont des bacilles à gram négatif,
chimio-organotrophes, parfois capsulés, ils possèdent une
ciliature péritriche pour les espèces mobiles. Ces bacilles
fermentent le glucose (avec ou sans production de gaz), ils sont
aéro-anaérobies facultatifs et possèdent à la fois
un métabolisme respiratoire et fermentatif (Loukiadis, 2007 ;
King et al., 2014)
2.5. Pouvoir pathogène naturel
E.coui est responsable d'infections
extra-intestinales, infections urinaires, infections abdominales et
septicémies avec choc septique dû à l'endotoxine O et
d'infections intestinales : l'existence des diarrhées à E.
coui est connue depuis 1940. Ces diarrhées sont dues à des
souches de sérotype particuliers qui provoquent soit des cas
sporadiques, soit des petites épidémies (Abhijit et
al., 2013).
Partie
expérimentale

Chapitre II
Matériel et
méthodes
Chapitre II Matériel et méthodes
Page | 6
1. Objectif du travail
Notre étude a pour objectif de savoir si l'argile de type
Bentonite a un effet sur la croissance de la bactérie Escherichia
coui.
2. Lieu et période de l'étude
Notre travail a été réalisé au niveau
du laboratoire de Microbiologie n°01 de la Faculté des Sciences de la
Nature et de la Vie, université Ibn Khaldoun de Tiaret, durant le mois
de mars 2020.
3. Matériel
3.1. Matériel biologique
v Souches bactériennes
Cette étude a été réalisée sur
02 souches d'Escherichia coui :
· Escherichia coui (ATCC 25922) : Souche
référenciée ;
· Escherichia coui : de laboratoire
prélevé à partir des urines d'un patient ;
3.2. Matériel naturel
v Argile
C'est l'argile de Maghnia qui a été mise à
notre disposition par l'ENF.
3.3. Appareillages et produits utilisés
Nous avons utilisé des instruments et produits chimiques
qui sont indiqués dans le tableau 1.
Chapitre II Matériel et
méthodes
Tableau 2 : Matériel et produits
utilisé dans l'expérimentation.
|
Appareillages
|
|
Verreries
|
|
Autres matériels
|
|
·
|
Microscope (Optika)
|
·
|
Béchers
|
·
|
Pince métallique
|
|
·
|
Incubateur (Memmert)
|
·
|
Éprouvettes graduées
|
·
|
Pince en bois
|
|
·
|
Agitateur magnétique
|
·
|
Lames
|
·
|
Anse de platine
|
|
(Stuart)
|
·
|
Lamelles
|
·
|
Portoirs
|
|
·
|
Balance électrique
|
·
|
Pipettes pasteur
|
·
|
Pissette
|
|
(Sartorius)
|
·
|
Flacons
|
·
|
Micropipette
|
|
·
|
Réfrigérateur (IRIS)
|
·
|
Tubes à essai
|
·
|
Boites de petri
|
|
·
|
Bec bunsen
|
·
|
Verre de montre
|
·
|
Papier Wathman n°3
|
|
|
·
|
Cloche de durham
|
·
|
Seringues
|
|
|
|
|
·
|
Papier aluminium
|
|
|
|
|
·
|
Papier hygiénique
|
|
Produits
|
|
Réactifs
|
|
Milieux de culture
|
|
|
|
|
|
(Annexe 1)
|
|
·
|
Eau distillée
|
·
|
Réactif TDA (tryptophane
|
·
|
Gélose Mac Konkey
|
|
·
|
Huile d'immersion
|
|
désaminase)
|
·
|
Gélose Muller Hinton
|
|
·
|
Galerie API 20 E
|
·
|
Réactif VP1 et VP2 (Voges
|
|
(MH)
|
|
·
|
Disque d'oxydase
|
|
Proskauer)
|
·
|
Bouillon nutritif (BN)
|
|
·
|
Eau oxygénée
|
·
|
Réactif Ehrlich Kovacs
|
·
|
Milieu Mannitol Mobilité
|
|
·
|
(H2O2)99.8%
Violet de Gentiane
|
·
|
Réactif NIT1 et NIT2
|
·
|
Milieu TSI
|
|
·
|
Lugol
|
|
|
·
|
Milieu citrate de simmon
|
|
·
|
Fuchsine
|
|
|
·
|
Milieu Schubert
|
|
·
|
Alcool
|
|
|
|
|
Page | 7
Page | 8
Chapitre II Matériel et
méthodes
4. Méthodes
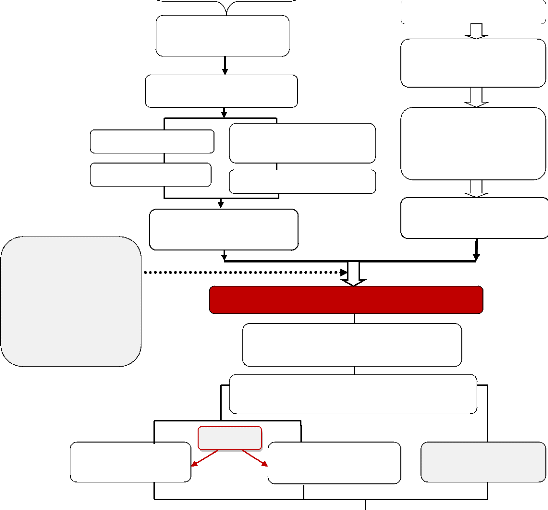
4.1. Protocole expérimental
Les étapes de l'expérimentation sont
résumées dans la figure 2
|
E. coli ATCC 25922
|
|
E. coli de laboratoire
|
Bentonite de Maghnia
|
Repiquage sur gélose
Mac Conkey
Ré-Identification
Tamisage à 40 ?m
Stérilisation de la
bentonite à
1100C / 1h
Test microscopique
Test macroscopique
Tests biochimiques classiques
Galerie API 20E
Préparation d'une
solution mère (100 g
/1L)
, et agitation pendant
2h
Préparation des dilutions
de 10/0 à
100/0
Standardisation McFarland 0.5
Antibiogramme
Méthode des disques de diffusion sur
gélose
Préparation des
disques à partir de
papier
wattman
imbibés dans les
différentes
dilutions
remplaçants les
disques d'antibiotiques
Témoins
Des disques
d'antibiotiques
Ensemencer l'E.coli sur la surface de la gélose MH puis
l'ajout :
Ne rien ajouter (ni ATB ni argile)
Des disques argileux
Calcule de CMI
Figure 2 : Protocole expérimental
Chapitre II Matériel et
méthodes
Page | 9
4.2. Ré-identification des souches
4.2.1. Repiquage des souches d'Escherichia coli
Cette opération consiste d'abord à
prélever quelques colonies d'E.coli à partir de ses
milieux et à procéder ensuite à l'ensemencement des boites
de pétri contenant le milieu de culture Mac Conkey :
· Refroidir et maintenir à 44-47 °C
· Couler en boîtes de Pétri stériles
· Laisser solidifier sur une surface froide
· Ensemencer l'E.coli à la surface des
boîtes afin d'obtenir des colonies isolées par la méthode
des stries serrées. Enfin, les boites sont incubées dans
l'étuve à 37 C° pendant 24h.
- Les colonies lactose-positif présentent une
coloration rouge et sont entourées d'un halo de sels biliaires
précipités. Les colonies lactose-négatif sont incolores
(Faure, 2010). (Annexe 1).
4.2.2. Tests d'identification d'Escherichia coui
I. Etude morphologique
I. 1. Examen macroscopique
Cet examen permet de déterminer la forme, la taille,
pigmentation, contour, aspect et viscosité des colonies sur boîte
de Pétri par une observation visuelle (Mami, 2013) ;
L'aspect des colonies dépend du milieu, de la durée et
la température d'incubation.
I. 2. Examen microscopique I. 2.1. Examen à
l'état frais
- Principe
Cet examen nous permet d'apprécier la forme, la
mobilité, le mode de regroupement, et l'abondance de notre
bactérie.
- Mise en oeuvre
· Déposer aseptiquement sur une lame porte objet,
quelques gouttes d'eau physiologique.
· Prélever à l'aide d'une anse de platine
stérile une à deux colonies à partir du milieu contenant
de la gélose nutritive.
· Emulsionner dans la goutte d'eau physiologique.
· Recouvrir d'une lamelle tout en évitant la
formation des bulles d'air.
· Observer sous microscope optique grossissement
(×40).
Chapitre II Matériel et
méthodes
Page | 10
- Lecture
A l'issu de cet examen microscopique, on peut observer la
forme, le mode de regroupement et la mobilité des souches
(Labiod, 2016).
I. 2.2. Coloration de Gram - Principe
La coloration de Gram est une technique qui permet de mettre
en évidence les propriétés de la paroi bactérienne.
Elle permet de colorer les bactéries et de distinguer leur aptitude
à fixer le violet de gentiane (Gram+) ou la fuchsine (Gram-). Cette
opération se déroule en sept étapes.
-Mise en oeuvre
Réaliser un frottis sur une lame de microscope
à partir d'une suspension bactérienne, agiter la suspension afin
de l'homogénéiser et d'éviter d'avoir un culot au fond du
tube.
· Etaler une goutte de la suspension bactérienne sur
une lame propre.
· Procéder à la fixation du frottis en
faisant passer la lame trois fois dans la flamme du bec bunsen.
· Plonger La lame pendant une minute dans le violet de
gentiane, puis rincée à l'eau
déminéralisée.
· Etaler le Lugol et laisser agir une minute puis rincer
à l'eau. Cette étape à pour but de stabiliser la
coloration violette.
· Verser goutte à goutte de l'alcool sur la lame
inclinée obliquement. Surveiller la coloration (15 à 30
secondes). Le filet doit être clair à la fin de la
décoloration. Rincer avec de l'eau.
- Si l'alcool pénètre dans la bactérie,
la coloration au violet de Gentiane disparait. Les bactéries donc sont
de type Gram-, si l'alcool ne traverse pas la paroi, on est en présence
de bactéries Gram+.
· Réaliser une contre coloration avec de la
fuchsine : laisser agir 30 secondes à une minute, laver doucement
à l'eau déminéralisée. Sécher la lame entre
2 feuilles de papier buvard.
Enfin, observer à l'objectif à immersion (X100)
après dépôt d'une goutte de l'huile de cèdre.
- Lecture :
Les bactéries Gram+ apparaissent en violet
foncé, tandis que les bactéries Gram- sont colorées en
rose (Labiod, 2016).
Chapitre II Matériel et
méthodes
Page | 11
II. Etude biochimique
II. 1. Recherche des enzymes respiratoires
II. 1.1. Test de la catalase -Principe
La catalase est une enzyme ayant la propriété
de décomposer le peroxyde d'hydrogène (H2O2) avec
dégagement d'oxygène selon la réaction suivante :
(Labiod, 2016).
- Mise en oeuvre
· Déposer sur une lame de verre une ou deux gouttes
d'eau oxygénée.
· Prélever à l'aide de l'effilure de pipette
pasteur un fragment de colonies et dissocier la culture dans l'eau
oxygénée.
- Lecture
La présence d'une catalase se traduit en quelque
seconde par la formation de bulles d'oxygène (Labiod,
2016).
II. 1.2. Test d'Oxydase -Principe
Ce test permet de mettre en évidence la
phényléne diamine oxydase ou cytochrome oxydase des
bactéries à partir de leur culture en milieu
gélosé. Le réactif utilisé est un
dérivé N-méthylé du paraphénylène
diamine (composé réduit incolore) qui, en présence de
l'enzyme, est oxydé et libère un composé rose
violacé (forme oxydée semi-quinone), noircissant à l'air.
La recherche de l'oxydase est un des critères les plus discriminatifs et
les plus employés pour l'identification des bactéries, surtout
celle des bacilles à Gram négatif en particulier pour
Escherichia coui (Hennia, 2016).
-Mise en -oeuvre
Une goutte de suspension bactérienne à
étudier a été déposée à l'aide d'une
pipette Pasteur stérile sur un disque pré- imprègne du
N-diméthylparaphénylene diamine
-lecture
Si le papier demeure incolore au bout de quelques secondes la
bactérie est alors oxydase négative par contre si le papier
devient violet la bactérie est considérée comme oxydase
positive (Essodolom, 2016).
Chapitre II Matériel et méthodes
Page | 12
II. 2. Recherche de type respiratoire
C'est le test de confirmation d'E.coli, par la
production ou non du gaz. Ce test est réalisé par le repiquage de
la bactérie dans le milieu Schubert munie d'une cloche de durham
qui permet de recueillir les gaz produits après 24
à 48 h à 44°C (Boumedjou et Fekih,
2014).
II. 2.1 milieu Schubert avec cloche de Durham II. 3.
Galerie biochimique classique
Elle permet l'étude de plusieurs caractères
biochimiques dont :
· Fermentation des sucres et production de gaz et d'H2S
· Etude de type fermentaire
· Utilisation du mannitol et détermination de la
mobilité
· Utilisation du citrate comme seule source de carbone
etc.
Le principe, les techniques et les règles
d'interprétation des tests effectués sont résumés
dans le tableau 3.
Tableau 3 : Galerie biochimique classique
d'identification d'Escherichia coui (Hennia,
2016).
Milieu /
principe
|
Aspect de
milieu
avant
l'ensemenceme-
nt
|
Mode
d'ensemencem
ent
|
Caractère
recherché
|
Lecture
|
|
|
Le milieu
|
|
Mannitol
|
|
Mannitol-mannitol
|
est
|
|
|
Mobilité
|
|
ensemencé par
|
|
. Mannitol (+) :
|
|
|
piqûre centrale à
|
-Fermentation
|
apparition d'une
|
-Principe :
|
|
l'aide d'une
|
de mannitol.
|
coloration jaune.
|
|
|
pipette Pasteur
|
-La mobilité.
|
Mannitol (-) :
|
Ce milieu
|
|
chargée de la
|
|
milieu reste rouge.
|
permet
l'étude de la
|
|
culture
bactérienne en
|
|
Mobilité
|
fermentation
|
|
milieu semi-
|
|
Mobilité (+) :
|
du mannitol,
il permet
|
|
solide. Incuber à 37°C pendant
|
|
Diffusion de la culture à partir de la
|
aussi la mise
en évidence
de la
mobilité
|
|
24h.
|
|
ligne
d'ensemencement en créant un trouble du
|
bactérienne
|
Laboratoire de
microbiologie 1
|
|
|
milieu
|
|
2020
|
|
|
Mobilité (-) : pas de diffusion
|
|
Chapitre II Matériel et
méthodes
Page | 13
Citrate
de
Simmons
|
|
Ce milieu peut
être utilisé aussi
bien en
tube
gélosé incliné
qu'en boîte de
|
- Utilisation
de
Citrate.
|
Citrate (+) :
Virage de milieu au
bleu et une culture
|
-Principe :
|
|
Pétri. Dans les
|
|
de colonie sur la
|
C'est un
milieu gélosé
utilisé
pour
l'identificatio
n des
entérobactéri-
es
par
l'utilisation
du citrate
|
|
deux cas,
ensemencer
légèrement
la
surface du
milieu par stries
et pour les tubes
en pente
jusque
dans le culot,
puis incubation
|
|
pente.
|
comme seule
source de
carbone.
|
Laboratoire de
microbiologie 1
2020
|
|
|
|
|
|
Ensemencement
|
- Lactose.
|
Lactose (+) : virage
|
TSI
|
|
de la pente de la
|
- Glucose.
|
de la pente au jaune
|
-Principe :
|
|
gélose par des
stries serrées,
puis le
culot par
|
- saccharose. - Gaz.
- Production
|
(la pente du milieu)
Saccharose (+) :
|
Ce milieu
|
|
piqûre centrale
|
d'H2S.
|
Virage au jaune au
|
permet
|
|
et l'incubation
|
|
milieu de tube (la
|
d'étudier la
fermentation
|
|
est réalisée à
37°C pendant
|
|
pente du milieu).
|
de trois
|
|
24h.
|
|
Glucose (+) :
|
sucres
|
|
-Le bouchon de
|
|
Virage de culot au
|
(glucose,
lactose, saccharose), d'apprécier la production ou non de
l'H2S et de noter la production ou non de gaz à
partir du
|
|
milieu ne doit pas être trop vissé.
|
|
jaune et bactérie
aéro-anaérobie.
Gaz (+) : apparition
des bulles ou des
poches gazeuses qui décalent la
gélose de fond de tube.
Production d'H2S :
|
glucose.
|
Laboratoire de
microbiologie 1
|
|
|
Noircissement du
milieu.
|
|
2020
|
|
|
|
|
Chapitre II Matériel et méthodes
Page | 14
II. 4. Galerie API 20 E
Après une identification des souches par la galerie
biochimique classique nous avons procédé à une autre
identification Par la galerie API 20 E pour la confirmation des
résultats.
-Principe d'API 20 E
La galerie API 20E est un système pour
l'identification des Enterobacteriaceae et autres bacilles Gram négatif,
utilisant 20 tests biochimiques miniaturisés, prêt à
l'emploi et standardisé. En effet, cette galerie comporte 20 micro-tubes
contenant des substrats déshydratés. Au-dessous de chaque tube,
un sigle indique la nature du test. Les tubes sont ensemencés avec une
suspension bactérienne effectuée en eau physiologique (milieu
"Suspension Medium"). Les réactions produites au cours de la
période d'incubation se traduisent par des virages colorés
spontanés ou révélés par l'addition de
réactifs (Bouchaala, 2017).
- Un fond et un couvercle complètent
la galerie et permettent de constituer une boîte d'incubation.
- Galerie API 20 E permet d'effectuer les tests 20 tests
biochimiques (Annexe 3)
- La galerie permet également la recherche de la nitrate
réductase qui se fait dans le Microtubule "GLU" (Bouchaala,
2017).
- Mode opératoire :
L'opération s'effectuée selon les étapes
suivantes :
· Placer de l'eau dans les alvéoles
présents dans le fond de la boite afin de créer une
atmosphère humide.
· Retirer la galerie de son emballage et la placer dans
le fond de la boîte.
· Prélever à l'aide d'une pipette Pasteur
boutonnée une colonie parfaitement isolée Dissocier soigneusement
la colonie dans une ampoule de "suspension Medium".
· A l'aide d'une micro-pipette remplir les micro-tubes
de la galerie. Au sein des micro-tubes, le fabriquant distingue deux parties,
le tube et la cupule. Selon les tests, la suspension bactérienne doit
être placée uniquement dans le tube ou dans le tube et la cupule
(Annexe 3).
· Refermer la boîte d'incubation, écrire
les références du prélèvement sur la languette du
fond de la boîte et placer la boîte à 37°C durant 24 h
(Bouchaala, 2017).
-lecture :
- Sortir la boîte de l'étuve et noter sur la
fiche de lecture les résultats obtenus pour les tests à lecture
spontanée.
- Révéler les tests nécessitant l'addition
de réactifs. - Noter les résultats sur la fiche de lecture.
Chapitre II Matériel et
méthodes
- Indiquer le profil numérique (Bouchaala,
2017)
4.2.3. Standardisation McFarland 0.5
Selon les recommandations du Comité de l'antibiogramme
de la Société Française de Microbiologie (CA-SFM /
EUCAST, 2020). La standardisation McFarland 0.5 est :
A partir d'une culture visible, réaliser une
suspension bactérienne en solution salée pour atteindre une
turbidité équivalente à celle de l'étalon 0,5 de la
gamme de McFarland, ce qui correspond à un inoculum d'environ 1 à
2 x108 UFC/ml pour Escherichia coui.
La suspension bactérienne est standardisée
à l'aide du témoin 0,5 McFarland. Un inoculum lourd engendre des
diamètres plus petits et inversement.
Il est recommandé d'employer un
spectrophotomètre pour ajuster l'inoculum. Cet appareil doit être
calibré contre un étalon de la gamme de McFarland selon les
recommandations du fabricant.
On peut également comparer à l'oeil nu la
turbidité de la suspension bactérienne à celle de
l'étalon 0,5 de la gamme de McFarland. Dans ce cas agiter vigoureusement
l'étalon de turbidité sur un Vortex avant usage Pour faciliter la
comparaison des deux échantillons, se placer face à un fond blanc
avec des lignes noires.
Pour ajuster la densité bactérienne au tube 0,5
McFarland, ajouter soit la solution salée soit les bactéries
(Annexe 5).
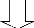
4.3. Préparation de l'argile
Les étapes de préparation de l'argile sont
résumées dans la figure 3 :
Bentonite de Maghnia
Tamisage 40 ì m
Stérilisation à 1100C / 1h
|
Mesurer le taux d'humidité
|
|
|
|
|
|
|
|
Préparation de la solution mère 100g
/1L + agitation pendant 2h
|
Détermination de pH
|
|
Préparation d'une série des dilutions
|
|
Figure 3 : les étapes de la
préparation de la bentonite
|
|
|
Page | 15
Chapitre II Matériel et
méthodes
Page | 16
4.3.1 Bentonite de Maghnia
L'argile utilisée au cours de notre étude est
une argile de type bentonite provient de gisement de Roussel, Hammam Boughrara
à 15 Km à l'Est de la ville de Maghnia, Wilaya de Tlemcen.
Situé à l`ouest d`Algérie.

Figure 4 : Bentonite de Maghnia en poudre
4.3.2. Tamisage de l'argile
La bentonite qui fait l'objet de ce travail a
été tamisée à travers un tamis dont la dimension
des mailles est de 40 ìm.
4.3.3. Stérilisation de la bentonite
Cette étape est effectuée dans une étuve
à 110° C dans le but d'éliminer les contaminants microbiens
de notre argile (Amari, 2019).
4.3.4. Taux d'humidité
La mesure du taux d'humidité consiste à
déterminer la masse d'eau éliminée par le séchage
d'un matériau humide jusqu'à l'obtention d'une masse constante
à une température de 105 #177; 5 °C pendant 24 heures, La
masse du matériau après l'étuvage est
considérée comme la masse des particules solides (ms). La
détermination du taux d'humidité a été
calculée à partir du rapport de la masse de l'eau
évaporée (m eau) sur la masse des particules solides (ms),
(Qlihaa et al., 2016).
H (%) = (m eau/ms) *100 = (mt-ms/ms)
*100 (1)
|
|
m eau : masse d'eau (g)
ms : masse de l'échantillon sec (g)
mt : masse de l'échantillon humide (g)
Chapitre II Matériel et
méthodes
Page | 17
4.3.5. Préparation de la solution
mère
Pour réaliser l'expérience, On doit
préparer une solution mère par dissolution de 100 g de la poudre
de bentonite dans un volume précis de 1 L d'eau distillée avec
une agitation pendant 2h à une température ambiante.
4.3.6. Détermination du pH
La solution d'argile obtenue est
homogénéisée par un agitateur magnétique et la
lecture est faite directement avec un pH-mètre.
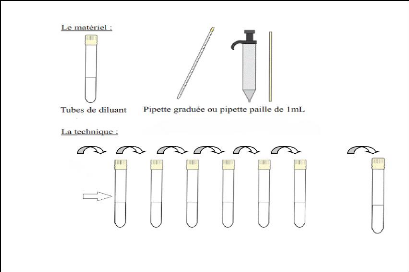
4.3.7. Préparation des dilutions
Pour préparer des solutions de concentrations
désirées, la solution mère est diluée dans Des
volumes connus d'eau distillée par la méthode suivante :
Solution
mère
argileuse
10% 9% 8% 7% 6% 5% 4% . 1%
.........
Figure 05 : préparation des dilutions.
4.4. Préparation des disques
Les disques sont confectionnés à partir de
papier filtre (Wattman n° 3), à raison de 5mm de diamètre.
Pour éviter tous risques de contamination aux germes exogènes au
cours de l'expérimentation, les disques sont mis dans un tube en verre
stérile et stérilisés à 120°C pendant 15
minutes dans un four pasteur (Ait chabane, 2018).
Chapitre II Matériel et
méthodes
Page | 18
4.5. L'activité antibactérienne de l'argile
4.5.1. Antibiogramme
Un antibiogramme est une technique de laboratoire visant
à tester la sensibilité d'une Bactérie vis-à-vis
d'un ou plusieurs antibiotiques.
Le principe consiste à placer la culture de
bactéries en présence des antibiotiques et à Observer les
conséquences sur le développement et la survie de celle -ci.
Il existe trois types d'interprétation selon le
diamètre du cercle qui entoure le disque d'antibiotique : souche ou
bactérie sensible, intermédiaire ou résistante.
La réalisation de l'antibiogramme se fait par
étapes : (Hnich, 2017).
· La préparation de l'inoculum bactérien ;
· Ajustement de la turbidité (densité) de
l'inoculum ;
· Ensemencement et séchage des boites ;
· Disposition des disques ATB ;
· Incubation ;
· Lecture et interprétation des antibiogrammes
4.5.2. Les étapes de préparation des deux
02 témoins et ceux avec une quantité connue de l'argile
Pour réaliser ce test il est nécessaire
d'utiliser le milieu Muller Hinton agar pour la culture de la souche
bactérienne examinée. Le milieu est coulé dans des boites
de pétri (9 cm de diamètre) avec une épaisseur de 4 mm,
puis les boites sont séchées à 37°C pendant 30 min
avant l'utilisation.
A partir d'une culture jeune et pure de 18 à 24 heures
sur milieu d'isolement bouillon nutritif on prépare une suspension
bactérienne dans l'eau physiologique stérile (0.9% NaCl) de
façon à obtenir un inoculum d'une opacité
équivalente à une DO de 0.08 à 0.1, lue à 625 nm,
ce qui correspond à une charge de 1.5×108 ufc /ml
à l'échelle de McFarland (Labiod, 2016).
Des dilutions sont faites en eau physiologiques
stériles (10-1,10-2), 5 ml de la dilution
10-2 est versée sur le milieu solidifié et
l'excès est éliminer après 2 à 3 min par
méthode d'inondation
Après chaque manipulation les boites vont subir une
incubation pendant 24 h d'incubation à 37° C les zones
d'inhibitions sont mesurées en millimètre par règle,
compas ou pied à coulisse (Belkhiri, 2009).
Chapitre II Matériel et
méthodes
Page | 19
I. Préparation des témoins
I. 1. ensemencent de la bactérie (T1)
Après coulage des boites on ensemence la
bactérie sur toute la surface de la gélose de Muller Hinton et
met la boite à l'étuve pour l'incubation.
I. 2. Antibiogramme par des disques de diffusion
(T2)
Les disques d'antibiotiques sont déposés sur la
gélose avec une pince métallique stérile, une fois
appliqué, le disque ne doit pas être déplacé.
Tableau 4 : Antibiotiques utilisés pour
Escherichia coli (Hennia, 2016).
|
Antibiotique
|
Signe
|
La charge du disque
|
|
Pipéracilline
|
PIP
|
75 jig
|
|
Céfazoline
|
CZ
|
30 jig
|
|
Amikacine
|
AN
|
30 jig
|
|
Doxycycline
|
DO
|
30 jig
|
|
Amoxilline + acide clavulanique
|
AMC
|
20/10 jig
|
|
Pénicilline
|
P
|
6 jig
|
II. Application des suspensions d'argile
A l'aide d'une pince stérile 1 ou 3 disques de diffusions
sont placés à la surface des boites inoculées et chacun
est injecté par 10 jil de la suspension argileuse de différentes
dilutions testées (Gulluce et al., 2003).
4.6. La concentration minimale inhibitrice
(CMI)
La CMI est définie comme la plus faible concentration du
produit inhibant totalement en 18 ou 24 heures à une température
de 37°C la multiplication des micro-organismes (Audrey,
2004).
La mesure de la CMI permet de déterminer si une souche est
sensible ou résistante à l'antibiotique testé.
La lecture est réalisée en plaçant les
boites de différentes concentrations sur une surface sombre, pour y
observer la présence (ou l'absence) de colonies, par rapport à la
boite témoin. Mesurer la zone d'inhibition en millimètre à
l'aide d'une règle. Se rapporter aux tableaux
Chapitre II Matériel et
méthodes
Page | 20
d'interprétation des zones d'inhibition fournis par les
fabricants de disques d'antibiotiques pour établir les
corrélations entre la zone d'inhibition et la concentration minimale
inhibitrice (CMI). La CMI est alors relevée Labiod, (2016) et
Bouarroudj, (2017).

Chapitre III
Résultats et
discussion
Chapitre III Résultats et discussion
Page | 21
1. Ré-identification d'E. coli
1.1. Etude morphologique
1.1.1. Observation macroscopique
Les résultats obtenus après 24h d'incubation
à 37°C sur le milieu Mac Conkey ont montré que les souches
d'Escherichia coli apparaissent en colonies :
· Rouges, Ronds, semi bombés, lisses,
Crémeuses, opaques. Ce résultat est identique à celui
trouvé par (Diassana, 2018).

Photo 5 : Aspect macroscopique des souches
d'Escherichia coli sur gélose Mac Conkey. 1.1.2.
Observation microscopique
L'observation microscopique d'E.coli entre lame et
lamelle nous a permis d'observer des coccobacilles, mobiles, et après la
réalisation de la coloration de Gram, on trouve de coccobacille
coloré en rose regroupé en amas ou isolé ou bien en petite
chênettes. Ce dernier a montré que la bactérie est à
Gram négatif.
Nos résultats concordent à ceux trouvés par
Lamouri et Messelem (2018) ; Merniez (2018)

Photo 6 : Observation microscopique
d'Escherichia coli après coloration de Gram
(×100)
Chapitre III Résultats et
discussion
Page | 22
1.2. Etude biochimique
1.2.1. Recherche d'enzyme respiratoire 1.2.1.1.
Catalase
D'après les résultats trouvés, nous
observons la présence des bulles d'air après le
dépôt de l'eau oxygénée sur la colonie d'E.coli,
cela confirme que la souche est de catalase positive, et ces
résultats sont identiques aux résultats trouvés par
avril et al (2000) ; benaissa et benamara (2016).
1.2.1.2. Oxydase
La bactérie d'E. Coli ne possède pas
une cytochrome-oxydase qui normalement se traduit après un contact
à N-diméthyl-1,4-phénylénediaminedichlorure en 20
à 60 secondes, par l'apparition d'une coloration rouge virant rapidement
en violet très foncé. Cet isolat obtenu est donc oxydase
négative.ces résultats conformes aux résultats
trouvés par avril et al (2000) ; benaissa et benamara
(2016).
1.2.2. Galerie biochimique classique et type
respiratoire
Les résultats des tests biochimiques classiques
après un temps d'incubation 24 h sont présentés dans le
tableau 05.
Tableau 5 : Résultats de la galerie
biochimiques classique et type respiratoire sur milieu Schubert.
Galerie biochimique classique
|
Type
respiratoire
|
Test
|
Mannitol-
mobilité
|
Citrate de
simmon
|
T.S.I
|
Milieu
Schubert
+cloche
|
|
Chapitre III Résultats et
discussion
Page | 23
Observation
|
|
|
|
|
Résultats
|
Manitole +
Mobilité +
|
Citrate -
|
Glucose + Saccharose +
Lactose +
H2s -
Gaz -
|
Gaz +
|
|
Les résultats obtenus sont identiques aux
résultats trouvés par Hennia, (2016) ; Lamouri et
Messelem, (2018).
1.2.3. Galerie API 20E

Photo 11 : API 20E d'E.coli
après incubation 24h à 37°C.
· Après incubation et selon le bio
Mérieux SA, 2010
· Si 3 tests ou plus (test GLU + ou -) sont positifs, noter
sur la fiche de résultats toutes les réactions spontanées
puis révéler les tests nécessitant l'addition de
réactifs :
Chapitre III Résultats et
discussion
Page | 24
- Test TDA : ajouter 1 goutte de
réactif TDA. Une couleur marron-rougeâtre indique une
réaction positive à noter sur la fiche de résultats.
- Test IND : ajouter 1 goutte de réactif
JAMES. Une couleur rose diffusant dans toute la cupule indique une
réaction positive à noter sur la fiche de résultats.
- Test VP : ajouter 1 goutte des
réactifs VP 1 et VP 2. Attendre au minimum 10 minutes. Une couleur rose
ou rouge indique une réaction positive à noter sur la fiche de
résultats. Une faible coloration rose apparaissant après 10
minutes doit être considérée négative.
Les résultats sont indiqués dans le
tableau 6 : Tableau 6 : résultats de la Galerie API 20
E.
Tests positifs(+)
|
ONPG
|
ADH
|
LDC
|
ODC
|
IND
|
VP
|
GLU
|
MAN
|
SOR
|
RHA
|
MEL
|
ARA
|
|
Tests négatifs(-)
|
CIT
|
H2S
|
URE
|
TDA
|
GEL
|
INO
|
SAC
|
AMY
|
|
· Confirmation de la présence de la souche
E.coli avec la galerie API 20 E (tableau d'identification
(Annexe 4).
2. Activité antibactérienne
2.1 Les témoins
2.1.1. Ensemencement de la bactérie (T1)
On observe une multiplication bactérienne qui est
indiqué par la présence des colonies dans la boite de
pétri.
Le résultat obtenu est concorde avec les recommandations
du Comité de l'antibiogramme de la Société
Française de Microbiologie et European Committee on Antimicicrobial
Susceptibility Testing (CA-SFM / EUCAST, 2020).
A cause de la richesse du milieu Muller Hinton en
composés favorables à la croissance d'E.coli autant
qu'une bactérie non exigeante.
Chapitre III Résultats et
discussion
Page | 25
2.1.2. Antibiogramme des disques de diffusion(T2).
Les résultats trouvés Selon le test de
l'antibiogramme effectué par Hennia (2016), de 05 types
d'antibiotique sur l'E.coli montrent que cette souche est sensible aux
trois antibiotiques : Amoxicilline +acide clavulanique (AMC) (20/10 ìg),
Amikacine (AN) (30 ìg) et Céfazoline (CZ) (30 ìg) mais
présente une sensibilité intermédiaire à la
pénicilline (P) (6 ìg) et la Doxycycline (DO) (30 ìg). Les
résultats sont représentés dans le tableau
7.
Tableau 07 : l'antibiogramme
d'E.coli.
Antibiotiques
|
Diamètre de zone
d'inhibition en
(mm)
|
Résultats
|
AMC
|
20
|
S
|
AN
|
24
|
S
|
CZ
|
20
|
S
|
P
|
8
|
I
|
DO
|
7
|
I
|
|

Figure 06 : l'antibiogramme
d'E.coli.
Les résultats présentés dans le
tableau 7 montrent que l'Escherichia coli est
résistante à tous les antibiotiques de la famille des
â-lactamines sauf Amoxicilline (AMC) et Céfazoline (CZ) et moins
résistante au pénicilline (P) et Doxycycline (DO).
On explique la résistance aux bêta-lactamines
par la production de bêta-lactamases qui inactive les
bêta-lactamines par hydrolyse du noyau bêta-lactame, une diminution
de la perméabilité de la membrane externe aux antibiotiques
hydrophiles par modification des porines chez les bacilles à Gram
négatif, ainsi que des phénomènes d'efflux Filali
et al f2000).
Chapitre III Résultats et
discussion
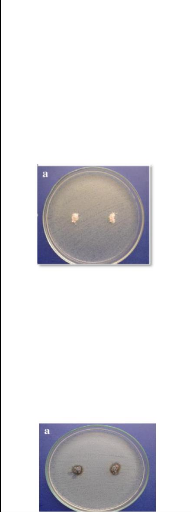
Ø Dans La figure 8 il se trouve les
résultats microbiologiques pour la masse de 2 g de bentonite
après le processus d'échange ionique avec la bactérie
E. coui. Il existe d'un halo d'inhibition bactérienne,
indiquant un effet bactéricide de la bentonite par incorporation
d'argent ionique.
Ø Dans La figure 7 il se trouve les
résultats microbiologiques de la diffusion sur gélose pour les 2
g de bentonite brute qui n'a pas été soumise à un
échange ionique avec la bactérie E. coui. Les
résultats montrent une absence d'effet bactéricide et l'effet
bactériostatique pour les bactéries testées, mis en
évidence par
l'absence d'halo d'inhibition
bactérienne.
Figure 7 : Résultats
microbiologiques
appliquant la méthode de diffusion
sur
gélose à la bentonite brute.
2.2. L'activité antibactérienne de la
bentonite sur l'Escherichia coui
A cause de la pandémie du Covid-19, on n'a pas pu
continuer notre travail au sein du laboratoire. Pour compléter notre
travail, on a synthétisé dans les tableaux 8 et 9,
02 articles scientifiques différents, qui ont des
thématiques proches de la nôtre.
Tableau 8. Représente l'article de Santos
et al., 2011
Page | 26
- Les résultats indiquent que le prétraitement
dans un environnement d'HCL confère à la bentonite de meilleures
propriétés microbiologiques que le prétraitement H2SO4
- L'effet le plus important de la bentonite traitée au
HCL peut être une indication que le traitement avec de l'acide
chlorhydrique améliore le processus d'échange ionique entre
Ag+ et les échantillons ioniques présents dans la
bentonite.
Figure 10 : Valeurs de diamètre des
halos pour la bentonite échangée avec Ag + activée par
l'acide et la bentonite échangée avec Ag +
prétraitée montrant une comparaison entre les effets
bactéricides sur E.coui.
- Tableau 10 présente des tests
microbiologiques utilisant la méthodologie CMI, comparant les effets
bactéricides de la bentonite brute avec de la bentonite
prétraitée avec HCL et H2SO4. Les résultats de la CMI
montrent que la bentonite brute ne présente pas de
propriétés bactéricides, tandis que la bentonite soumise
à un échange ionique dans des environnements contenant de
l'argent présente de tels effets. Les résultats indiquent une
plus grande capacité bactéricide pour les environnements
contenant
|
|
Chapitre III Résultats et
discussion
Figure 8 : Tests microbiologiques appliquant
la
méthode de diffusion sur gélose à la
bentonite
échangée par Ag + montrant la présence
d'un
effet bactéricide.
Ø Dans La figure 9 (a et c) :
(a) montre les résultats pour la
bentonite traitée dans une solution de HCl puis soumis à un
processus d'échange ionique. (c) montre les
résultats pour la bentonite traitée dans une solution de H2SO4,
puis soumis à un processus d'échange ionique. Les
résultats montrent la présence d'un halo d'inhibition
bactérienne, indiquant l'action bactéricide pour les deux
bentonites avec la bactérie, bien que celles traitées au HCl
présenté un effet bactéricide plus important que la
bentonite traitée avec acide sulfurique.
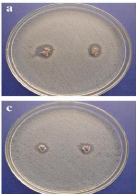
Figure 9 : Tests microbiologiques appliquant la
méthode de diffusion sur gélose montrant une comparaison entre
les effets bactéricides.
(a) Bentonite activée par HCL
après
échange d'ions avec AgNO3.
(c) Bentonite traitée en milieu H2SO4
après un processus d'échange d'ions avec AgNO3.
- dans La figure 10 il se
trouve une
comparaison entre les diamètres moyens des halos
d'inhibition bactérienne pour la bentonite soumise à un
échange ionique et sans et avec traitement d'acide avant échange
ionique.
Page | 27
d'acide chlorhydrique. Pour la concentration inhibitrice
minimale était de 0,012 g pour la bentonite activée par HCL et de
0,038 g pour l'échantillon prétraité avec H2SO4.
Cependant, cet effet n'est observé que pour la bentonite
prétraitée au HCL. Il est à noter que ces résultats
sont conformes aux résultats présentés par les tests de
diffusion d'agar. Les résultats microbiologiques montrent que le
traitement de la bentonite avec de l'acide est une étape importante pour
obtenir la bentonite bactéricide.
Tableau 10 : Tests microbiologiques appliquant
la méthode de la concentration minimale inhibitrice.
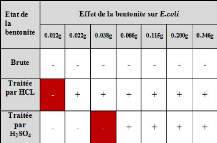
+ Inhibition
- Pas d'inhibition
Des études avec l'acide sulfurique ont montré que,
pendant le processus d'activation, la surface de la bentonite augmente
jusqu'à 200-400 m2/g. cette augmentation est habituellement
à 80% ou plus de la surface disponible correspond à des pores
avec des diamètres allant de 2,0 à 6,0 nm, (Francisco et
al., 2001).
La décomposition des structures de smectites de la
bentonite, permettant ainsi l'échange de cations avec les
échantillons présents dans la structure naturelle de bentonite et
les ions H+ présents dans la solution acide et favorisant
l'augmentation de la surface spécifique. Ces transformations
entraînent des changements importants dans la capacité
d'échange cationique (CEC) et dans les caractéristiques chimiques
et minéralogiques de la bentonite (Francisco et al.,
2001 et Demirbas et al., 2006). Ainsi, le processus de
traitement acide favorise l'incorporation de plus grandes quantités
d'espèces ioniques d'argent dans la bentonite. Après immersion de
la bentonite dans l'acide chlorhydrique, le processus d'échange ionique
avec l'argent ionique et les propriétés bactéricides
résultantes sont améliorés.
Chapitre III Résultats et
discussion
Tableau 09. Représente l'article de Yuhang et
al., 2004
·
- Le tableau 11 montre la quantité des
cellules viables d'E.coli en suspension dans 100 ml d'eau après
leur mise en contact avec différentes quantités de
Cu2+/montmorillonite. La teneur en cellules viables testé
diminuait avec l'augmentation du temps de contact. Lorsque 100 ml de milieu de
culture
contenaient 1 mg de
Cu2+/montmorillonite
(égale à une teneur en Cu2+ de 10 ppm), la
bactérie mourait en 24 h. Lorsque la teneur en
Cu2+/montmorillonite a été augmentée à 5
mg (50 ppm), E. coli a été tuée en 6h. Lorsque
E.coli a été en contact avec 20 mg de
Cu2+/montmorillonite en suspension dans l'eau distillée,
toutes les cellules sont mortes en moins de
2 h.
- Les résultats démontrent que la
capacité antimicrobienne de la Cu2+/montmorillonite
était très efficace sur Escherichia coli.
- Les parois cellulaires des bactéries viables
étaient généralement chargées négativement
en raison de groupes fonctionnels tels que les carboxylates présents
dans les lipoprotéines à la surface (Breen et
al., 1995). Le
Cu2+/montmorillonite attire les
bactéries
par des forces électrostatiques et les immobilise à la surface.
Cu2+ pourrait également se dissocier et exercer directement
son effet antimicrobien sur les bactéries de la dispersion. En raison de
la densité des ions Cu2+ sur la surface minérale qui
est beaucoup supérieure à celle du milieu, la capacité
antimicrobienne des particules de Cu2+/montmorillonite pourrait
dominer sur les cations Cu2+ libérés dans le
milieu.
Page | 28
Effet du Cu2+ sur E.coli
Tableau 11 : la capacité
antimicrobienne de Cu2+/montmorillonite sur E.coli
(cel/ml).
|
Temps d'incub -ation (h)
|
Cu2+/montmorillonite (mg/l)
|
|
0
|
10
|
25
|
50
|
100
|
200
|
|
0
|
(8.35#177;0.40) x 104
|
(8.35#177;0.40) x 104
|
(8.35#177;0.40) x 104
|
(8.35#177;0.40) x 104
|
(8.35#177;0.40) x 104
|
(8.35#177;0.40) x 104
|
|
2
|
(8.50#177;0.26) x104
|
(5.20#177;0.36) x104
|
(3.00#177;0.31) x104
|
(1.50#177;0.12) x104
|
(6.40#177;0.30)
x 103
|
0
|
|
4
|
(8.65#177;0.31) x104
|
(1.60#177;0.18) x104
|
(8.90#177;0.40) x103
|
(7.00#177;0.37)
x 101
|
0
|
0
|
|
6
|
(8.20#177;0.18) x104
|
(7.30#177;0.27) x102
|
0
|
0
|
0
|
0
|
|
24
|
(8.35#177;0.35) x104
|
0
|
0
|
0
|
0
|
0
|
onclusion
Page | 30
Conclusion générale
L'argile est liée à la vie. Elle a toujours fait
partie du quotidien. Elle représente surtout une alternative aux
thérapeutiques classiques dans les domaines du soin des plaies, la
cicatrisation, l'antalgie, l'inflammation... etc.
Cette étude vise à étudier l'effet
bactéricide de l'argile de type « Bentonite »
sur la bactérie Escherichia coui.
La première partie de la méthodologie
expérimentale consistait à faire une réidentification de
la bactérie par des tests microbiologiques et biochimiques.
La deuxième partie de la méthodologie
expérimentale consistait à faire un tamisage et
stérilisation de l'argile afin de l'utiliser dans l'étape de
l'antibiogramme et vérifier son effet bactéricide mais
malheureusement à cause des conditions de la pandémie du
COVID-19, on n'a pas pu continuer notre travail, mais on a jugé utile de
faire des synthèses bibliographiques sur des articles scientifiques
abordant la même thématique que la nôtre.
Nous avons trouvé comme résultats que la
bactérie est à : Gram négatif,
catalase +, oxydase-,
mobile, fermente le Glucose, Lactose, Saccharose et Mannitol,
sans production de H2S, aérobie et n'utilise pas le citrate comme seul
source de carbone.
Les principaux résultats obtenus dans l'article de
recherche de Santos et al., 2011, sur les tests
microbiologiques de diffusion de la gélose et de la concentration
minimale inhibitrice, ont montré que la présence d'effets
bactéricides significatifs pour la bentonite soumise à un
échange d'ions dans les mélanges de nitrate d'argent. La
bentonite activée par HCl a montré de meilleures
propriétés bactéricides que la bentonite activée
par H2SO4. Les procédures pour conférer des
propriétés bactéricides à la bentonite se sont
avérées efficaces et le potentiel d'incorporation de
propriétés microbiologiques dans la structure de la bentonite a
été vérifié.
Quant au deuxième article de Yuhang et al.,
2004, le Cu2+ a montré un effet
bactéricide qui devient plus efficace avec l'augmentation du couple
temps de contact et concentration du complexe Cu2+ /
montmorillonite.
Enfin, cette étude se voulait une source importante
d'informations sur la « Bentonite » plusieurs
données sur son effet antibactérien mais ce travail pourrait
être approfondi et complété.
Références
bibliographiques
Page | 31
Références
bibliographiques
.A.
Ø Abderrahim O., Didi M.A., Moreau B.,
Villemin D., (2006). « A new sorbent for selective separation of
metal polyethylenimine methylene phosphonicacid», Solv,Extr Ion, Exch 24:
943-955.
Ø Abhijit A., NighuteS., KhatoonM.,
(2013).Study of urinary isolates with reference to extended spectrum
beta lactamases detection and antibiogram.Vol 2, Issue 9: p1052.
Ø Adrianne P., (2003). L'argile,
médecine ancestrale de la tradition aux preuves scientifiques,
éditions Amirys SPRL, dépôt légal : 4e trimestre
Ø Airoldi C., Critter S. A.
M., (1997). « Thermodynamic
study involving Cu, Zn, Cd, Hg, Pb, Ca and Na', Clays and clay Minerals »
45 (2): P125.
Ø Ait chabane O., (2018). Etude des
effets antimicrobiens des extraits bruts, phénoliques et à base
d'huiles essentielles du Miswak (Salvadora persica) sur les microorganismes
responsables des infections buccales (caries dentaires, gingivite, parodontite,
candidoses...etc). Thèse de doctorat. Université Abdelhamid Ibn
Badis : Faculté des Sciences de la Nature et de la Vie, Laboratoire de
Technologie Alimentaire et Nutrition. Mostaganem. P 52.
Ø Amari H., (2019). Etude De
l'adsorption et teste d'élimination de phényle parabène
sur une argile naturelle. Mémoire de Master. Université Dr.
Moulay Tahar : Faculté des sciences. Saida : P 67.
Ø Audrey A., (2004). environnement
des bactéries et sensibilité aux biocides - Mise au point d'une
technique rapide pour déterminer in situ l'efficacité
bactéricide d'agents antimicrobiens-. Thèse de doctorat. Ecole
Nationale Supérieure des Industries Agricoles et Alimentaires : Ecole
Doctorale Agriculture Biologie et Santé. France. P 18
Ø Avril, J.L., Debarnat H., Denis F., Monteil
H., (2000). Bactériologie clinique. 2ed .Ellipses, Paris. pp.
171-177.
.B.
Ø Bahlouli S., et Idiri N., (2015).
Criblage de souches d'entérobactéries productrices de
carbapénèmases au niveau des laboratoires d'analyses
médicales de la wilaya de Béjaia. Mémoire de Master.
Université A. MIRA. Faculté des Sciences et de la Nature et de la
Vie. Béjaia. (Annexe)
Ø Bergy's manual of systematic bacteriology
(2004). The Proteobacteria. Volume 2: procaryotic Domains. Pp21-26
krieg , Noel R. Editors: Garriy, George (Ed)
Ø Besq A., Malfoy C., Pantet A.,
Monnet P., and Righi D., (2003).
«Physicochemical characterization and flow properties of some
bentonite muds,» Appl. Clay Sci. 23, 275-286.
Ø Breen P.J., Compadre C.M., Fifer, E.K.,
Salari, H., Serbus, D.D., Lattin, D.L., (1995). Quaternary ammonium
compounds inhibit and reduce the attachment of viable Salmonella typhimurium to
poultry tissues. J. Food Sci. 60 : 1191-1196.
Ø Belkhiri F., (2009).
Activité antimicrobienne et antioxydante des extraits du tamus
communis L. et Carthamus caeruleus L. Mémoire de Master.
Université Ferhat Abbes : Faculté des sciences .Sétif .p
60.
Page | 32
Références
bibliographiques
Ø Bouarroudj T., (2017). Contribution
à la connaissance de l'effet bactéricide et la
cytotoxicité des oxydes nanocristallins. Thèse de doctorat.
Université Badji Mokhtar : Faculté des sciences. Annaba. P 75.
Ø Bouchaala L., (2017). Contribution
à l'étude de la qualité physico-chimique et
microbiologique de l'eau des écosystèmes aquatiques de
Guerbes-Sanhadja (Skikda) et utilisation de l'espace par le Canard Siffleur
Anas penelope. Thèse de doctorat. Université Mouloud Mammeri
Faculté des sciences biologiques et des sciences agronomiques.
Tizi-Ouzou. P (68-69-70).
Ø Boumedjou F. Z., et Fekih M.,
(2014). Etude de la qualité de l'eau « Exquise»
destinée à l'irrigation des terres d'El Fehoul. Mémoire de
Master. Université Abo Bekr Belkaid : Faculté des Sciences de la
Nature et de la vie et des Sciences de la Terre et de l'Univers. Tlemcen. P
(96-70).
Ø BourjilaT M. (2009). Etude prospective
de la résistance chez E. coli dans l'hôpital de
Meknès. Maroc. Eline. Microbial. Rev. 22, p 120-123.
Ø Bouzeraa A., Berrihil H., (2018).
Bactériologie des Entérobactéries isolées
au niveau du Service de Réanimation de l'Hôpital Militaire
Régional Universitaire de Constantine (HMRUC). Mémoire de Master.
Université Frères Mentouri Constantine 1 : Faculté des
Sciences de la Nature et de la Vie. Constantine.
.C.
Ø Comité de l'antibiogramme de la
Société Française de Microbiologie.
Recommandations Avril 2020. V.1.1
.D.
Ø Darcel C. L. (1982). A" liver" antigen
associated with a vianery throblastosis: binding by bentonite and precipitation
with sodium dodecylsulphate. Canadian Journal of Comparative Medicine,
46(1), page 97.
Ø Debabza M., (2005). Analyse
microbiologique des eaux des plages de la ville de Annaba « Evaluation de
la résistance aux antibiotiques des microorganismes pathogènes
». Mémoire de Magister. Université Badji Mokhtar :
Faculté des sciences. Annaba(Annexe).
Ø Debbi S., et Saadi M., (2019).
Isolement, identification et étude de la résistance des
souches d'Escherichia coli isolées dans différents
service de l'hôpital de Lakhdaria. Mémoire de Master.
Université Akli Mohand Oulhadj : Faculté des sciences de la
nature et de la vie et des sciences de la terre. Bouira ( Annexe).
Ø Demirbas A., Sari A., Isildak O., (2006).
Adsorption thermodynamics of stearic acid onto bentonite. J. Hazard.
Mater. 31 (135(1-3)) : 226-231.
Ø Diassana A., (2018). Identification
des souches d'Escherichia coli dans les selles en rapport avec la
malnutrition à dioro. Thèse de doctorat. Université des
sciences, des techniques et des technologies de Bamako : Faculté de
pharmacie. Mali. P 25.
Page | 33
Références
bibliographiques
.E.
Ø Essodolom T., (2016). Recherche de
molécules bioactives d'origine microbienne : caractérisation
biochimique et moléculaire des souches de bactéries
isolées du Soumbala, du Bikalga et de certains yaourts consommés
au Burkina Faso, productrices de bactériocines. Thèse unique Pour
obtenir le grade de Docteur. Université ouaga I pr joseph ki-zerbo :
École Doctorale Sciences et Technologie. Burkina Faso. P 66.
Ø Euzéby J.P., (2008).
Abrégé de bactériologie générale et
médicale à l'usage des étudiants de l'Ecole Nationale
Vétérinaire de Toulouse.
http://www.bacteriologie.net.
Consultation le 10/03/202015.
.F.
Ø Faure M., (2010). Purification de
l'air ambiant par l'action bactéricide de la photocatalyse. Thèse
de doctorat. Université Henri Poincaré : Ecole doctorale RP2E,
Ressources Procédés Produits et Environnement. Nancy. P 69.
Ø Ferrah N., (2013). «
Fonctionnalisation de Matrices Polymériques et leurs Applications dansla
Rétention de Cd (II), Cu (II), U(VI) et Eu (III) », Thèse de
doctorat d'Université de Tlemcen.
Ø Filali B. k., Toufik J., Zeroual Y.F.A.Z.,
Dzairi F.Z., Talbi M & Blaghen M. (2000). Waste water bacterial
isolates resistant to heavy metals and antibiotics. Current microbiology
.41(3), 151-156.
Ø Francisco R., Valenzuela D., Persio D.E.S.,
(2001). Studies on the aid activation of Brazilian smectitic clays.
Quim. Nova 24 (3) : 345-353.
.ç.
Ø Guenoun N., Gada S., (2017).
Activation de la Bentonite de Maghnia pour usage pharmaceutique.
Mémoire de Master. Université Mouloud Mammeri : Faculté
des sciences. Tizi-Ouzou.
Ø Gulluce M., Sokman M., Daferera D., Agar G.,
Ozkan H., Kartal N., Polissiou M., Sokmen A., Shin F., (2003). Invitro
antibacterial, Antiflungal, and Antioxidant activities of the essential oil and
methanol extracts of herbalparts and callus cultures of Satureja hortensis L.
Journal of Agricultural and food chemistry. 51: 3958-3965.
.H.
Ø Hennia A., (2016). Extraction et
étude de l'activité biologique des huiles essentielles du Myrte
(Myrtus communis L). Thèse de doctorat. Université Abdelhamid ibn
Badis : Faculté des Sciences de la Nature et de la Vie. Mostaganem. p
(104-105-106-110111).
Ø Hnich H., (2017). La
résistance bactérienne: mécanismes et méthodes de
détection au laboratoire. Thèse de doctorat. Université
Sidi Mohammed Ben Abdellah : Faculté de médecine et de pharmacie.
Royaume du Maroc. P 62.
Page | 34
Références
bibliographiques
Ø
https://www.sensetsante.fr/bonnes-raisons-cure-d-argile/
Ø
https://www.futura-sciences.com/sante/actualites/biologie-argile-staphylocoque-dore-46562/
Ø
https://journals.openedition.org/vertigo/4091
Ø
https://sante.lefigaro.fr/actualite/2014/10/07/22876-antibiotiques-solutions-alternatives-prometteuses.
Ø
https://www.pasteur.fr/fr/centre-medical/fiches-maladies/resistance-aux-antibiotiques
.K.
Ø King L.A ., Loukiadis E ., Mariani-kurkdjian
P., Haeghebaert S., Weill F.X., Baliere C., Ganet S., Gouali M., Vaillant V.,
Pihier N., Callon H., Novo R., Gaillot O., Thevenot-sergentet D., Bingen E.,
Chaud P., De valk H. ( 2014). Foodborne transmission of
sorbitol-fermenting Escherichia coli O157: [H7] via ground beef: an outbreak in
northern France, 2011. Clinical Microbiology and Infection, 20:1136-1144.
.L.
Ø Labiod R., (2016). Valorisation des
huiles essentielles et des extraits de Satureja calamintha nepeta :
activité antibactérienne, activité antioxydante et
activité fongicide. Thèse de doctorat. Université Badji
Mokhtar. Faculté des sciences. Annaba. P (40-41-42-45).
Ø Lamouri N.S., et Messelem M.B., (2018).
Anitibiorésistance des souches Escherichia coli
d'origine aviaire. Mémoire de Master. Centre Universitaire Belhadj
Bouchaib : Faculté des sciences de la nature et de la vie.
Ain-Temouchent. P (26-27-28).
Ø Lefebvre P., Rigo J-M., Leprince P.,
Rogister B., Delrée P., Hans P., Born J-D., Moonen G. (1988).
Agressologie : revue internationale de physio-biologie et de
pharmacologie appliquées aux effets de l'agression. 0002-114829
[Internet]. [consulté
27 Mars 2018]; Disponible sur:
http://agris.fao.org/agris-
search/
search.do?recordID=BE2014104070
Ø Lopez-galindo A., Viseras C.,
(2004). Pharmaceutical and cosmetic application of clays, In. Clay
Surfaces, Fundamentals and Applications, Elsevier; Amsterdam, 267.
Ø Loukiadis E. (2007). Facteur de
virulence et dissémination dans l'environnement via les effluents
d'abattoirs d'animaux de boucherie d'Escherichia coli
entérohémoragique (EHEC). Thèse de doctorat
Université de Toulouse, France.
.M.
Ø Mariani-Kurkdjian P., Bingen É.
(2012). Physiopathologie et virulence des
Escherichia coli producteurs de Shiga-toxines
(Shiga-toxin producing by Escherichia coli: pathophysiology and
virulence). SRLF ET Springer-Verlag France. V 21: p 268279.
Ø Mami A., (2013). Recherche des
bactéries lactiques productrices de bactériocines à
large spectre d'action vis-à-vis des germes
impliqués dans les toxi-infections
Page | 35
Références
bibliographiques
alimentaires en Algérie. Thèse de doctorat.
Université d'Oran : Faculté des sciences. Oran. P 61.
Ø Merniez M., et Merniez S., (2018).
Etude de la résistance aux antibiotiques des souches d'Escherichia
coui isolées du lait de vache commercialise dans la région
d'Ain m'lila et Ain fakroun. Mémoire de master. Université larbi
ben m'hidi : Faculté des sciences exactes et des sciences de la nature
et de la vie. Oum el Bouaghi. P 26.
.Q.
Ø Qlihaa A., Dhimni S., Melrhaka F., Hajjaji N.,
Srhiri A., (2011). Caractérisation physico-chimique d'une
argile Marocaine [Physico-chemical characterization of a morrocan clay]. J.
Mater. Environ. Sci. 7 (5), 1741-1750.
.S.
Ø Santosa M.F., Oliveira C.M., Tachinski C.T.,
Fernandes M.P., Pich C.T., Angioletto E., Riella H.G., Fiori M.A., (2011).
Bactericidal properties of bentonite treated with Ag+ and acid.
International Journal of Mineral Processing, 100, 51-53.
Ø Smati M., Clermont O., Bleibtreu A.,
Fourreau F., David Anthony., Daubie AS.. (2015). Quantitative analysis
of commensal Escherichia coui populations reveals host-specific
enterotypes at the intra-species level. Microbiol Open. 4(4):604?15.
Ø Système d'identification des
Enterobacteriaceae et autres bacilles à Gram négatif non
fastidieux, bio Mérieux SA. Français - 1.2010.
.T.
Ø Theodorou V., Chrestian B.,
Fioramonti J., Droy-Lefaix M.T.,
Bueno M.T., (1994).Protective action of
diosmectite treatment on digestive disturbances induced by intestinal
anaphylaxis in the guineapig, Alimentary Pharmacology and Therapeutics 8, ,
pages 295-299.
.W.
Ø Wang X.S., Huanga J., Hu
H.Q., Wang J., Qin Y.
(2007). «Determination of kinetic and
equilibrium parameters of the batch adsorption of Ni (II) from aqueous
solutions by Namordenite», Journal of Hazardous Materials 142, 468-476.
.Y.
Ø Yuhang Z., Meisheng X., Ying Y., Caihong H.,
(2004). Antimicrobial ability of Cu2+-montmorillonite.
Applied Clay Science, 27, 215-218
nnexes
Annexes
Annexe 1 : Composition des milieux de culture et
solutions
1- Gélose Mac Conkey (Bahlouli et Idiri,
2015).
Peptone de caséine
|
17g
|
Peptone de viande
|
3g
|
Sels biliaires
|
1.5g
|
Cristal violet
|
0,001g
|
Lactose
|
10g
|
Rouge neuter
|
0,03g
|
Chlorure de sodium
|
5g
|
Agar
|
13,5g
|
ZnSO4
|
0,07g
|
pH : 7,1 #177; 0,2, Autoclavage à 120°C /20
min.
|
|

2- bouillon nutritif : (Mami, 2013).
|
Extrait de viande
|
|
1g
|
|
Extrait de levure
|
|
2g
|
|
Peptone
|
|
5g
|
|
Chlorure de sodium
|
|
5g
|
|
pH :
|
7.4 autoclavage à 120°C/ 20 min.
|

Annexes
3- Eau physiologique
|
Chlorure de sodium
|
|
8.5g
|
|
Peptone
|
|
0.5g
|
|
Eau distillée
|
|
1000 ml
|
|
pH : 7
|
, Autoclavage à 120°C / 20 min.
|
3- Milieu de Schubert (milieu indole-mannitol) :
(Debabza, 2005).
Tryptophane
|
0,2g
|
Acide glutamique
|
0,2g
|
Sulfate de magnésium
|
0,7g
|
Citrate de sodium
|
0,5g
|
Sulfate d'ammonium
|
0,4g
|
Chlorure de sodium
|
2g
|
Peptone
|
10g
|
Mannitol
|
7,5g
|
Phsphate disodique
|
4g
|
Phosphate monopotassique
|
0,6g
|
Eau distillée
|
1000ml
|
pH: 7,6 autoclavage 10 min à 115°C
|
|

4- Milieu citrate de Simmons
|
Citrate de sodium
|
1g
|
|
Chlorure de sodium
|
5g
|
|
Sulfate de magnésium
|
0, 2g
|
|
Monohydrogénophsphate de potassium
|
1g
|
|
Dihydrogénophsphate d'ammonium
|
1g
|
|
Bleu de bromothymol
|
0,08g
|
|
Agar
|
13g
|
|
Eau distillée
|
1000ml
|
|
pH: 6,8#177;0,2 autoclavage 20 min à 120°C
|
Annexes
5- Milieu mannitol-mobilité :
Peptone trypsique de viande
|
20g
|
Mannitol
|
2g
|
Rouge de phénol à 1%
|
4g
|
Agar
|
4g
|
Eau distillée
|
1000ml
|
pH: 7,6#177;0,2 autoclavage 30 min à 110°C
|
|
6- Milieu trois-sucres-fer : triple sugar iron -agar
(T.S.I)
Extrait de boeuf
|
3g
|
Extrait de levure
|
3g
|
Peptone
|
15g
|
Protéose peptone
|
5g
|
Lactose
|
10g
|
Saccharose
|
10g
|
Glucose
|
1g
|
Chlorure de sodium
|
5g
|
Sulfate de fer II (FeSO4)
|
0,2g
|
Thiosulfate de sodium
|
0,3g
|
Rouge de phénol
|
0,024g
|
Agar
|
12g
|
Eau distillée
|
1000ml
|
pH: 7,4#177;0,2 autoclavage 15 min à 120°C
|
|
7- Milieu de Mueller-Hinton (M.H)
|
Infusion de viande de boeuf
|
300g
|
|
Hydrolysat acide de caséine
|
17.5g
|
|
Amidon de maïs
|
1.5g
|
|
Agar
|
17g
|
|
Eau distillée
|
1000ml
|
|
pH: 7,3#177;0,1 Autoclavage 15 min à 121°C
|
Annexe 2 : Réactifs et colorants utilisés.
1- Violet de Gentiane (Debbi et Saadi, 2019).
|
Violet de Gentiane
|
10 g
|
|
Phénol
|
20 g
|
|
Éthanol (90 °GL)
|
100 ml
|
|
Eau distillée
|
1L
|
Annexes
2 - Logul
|
Iodure de potassium
|
2 g
|
|
Iode métalloïde I
|
2 1 g
|
|
Eau q.s. ad
|
100 g
|
|
q.s. ad 100 g signifie "quantité suffisante pour obtenir
100 g de solution"
|
3- Fuchsine
|
Fuchsine basique
|
10 g
|
|
Phénol
|
50 g
|
|
Éthanol
|
100 mL
|
|
Eau distillée
|
1 L
|
Annexe 3 : API 20 E.

1- comment remplir les tubules :
A l'aide d'une pipette munie d'une poire remplir les
micro-tubes de la galerie. Au sein des micro-tubes, le fabriquant distingue
deux parties, le tube et la cupule. Selon les tests, la suspension
bactérienne doit être placée uniquement dans le tube ou
dans le tube et la cupule.
v Lorsque le sigle du test est encadré, ce qui est le
cas des tests CIT, VP et GEL, la suspension doit remplir le tube et la
cupule.
v Lorsque que le sigle du test est souligné (ADH, LDC,
ODC, URE, H2S), la suspension doit remplir uniquement le tube. Après
ensemencement complet de la galerie, la cupule sera secondairement remplie
d'huile de paraffine.
v Lorsque le sigle du test n'est ni encadré ni
souligné (ONPG, TDA, IND, GLU, MAN, INO, SOR, RHA, SAC, MEL, AMY, ARA),
la suspension doit remplir uniquement le tube.
Annexes
2 - Lecture de la galerie API 20 E (Bouzeraa et
Berrihil, 2018).
|
Test
|
Composants actifs
|
QTE
|
Réactions-
enzymatique
|
Résultats
|
|
Négatif
|
Positif
|
|
ONPG
|
2-nitrophényl-âD-
galactopyranoside
|
0.223
|
B-galactosidase
|
Incolore
|
Jaune (1)
|
|
ADH
|
L-arginine
|
1.9
|
Arginine
DiHydrolase
|
Jaune
|
Rouge-orangé
(2)
|
|
|
LDC
|
L-lysine
|
1.9
|
Lysine
DéCarboxylase
|
Jaune
|
Rouge-orangé
(2)
|
|
|
ODC
|
L-omithine
|
1.9
|
Omithine
DéCarboxylase
|
Jaune
|
rouge
|
|
|
CIT
|
Trisodium citrate
|
0.756
|
utilisation du
CITrate
|
Vert pale-
jaune
|
bleu-vert -
bleu (3)
|
|
H2S
|
Sodium thiosulfate
|
0.075
|
production d'H2S
|
Incolore-
grisâtre
|
dépôt noir -
fin liseré
|
|
URE
|
Urée
|
0.75
|
UREase
|
jaune
|
rouge - orangé
(2)
|
|
TDA
|
L-trypyhophane
|
0.38
|
Tryptophane
DésAminas
|
TDA-immédiate
|
|
Jaune
|
marron -
rougeâtre
|
|
IND
|
L-trypthophane
|
0.19
|
production
d'indole
|
JAMES-immédiate
|
|
Incolore
|
Rose
|
|
VP
|
Sodium pyruvate
|
1.9
|
production
d'acétoine
|
VP1+VP2/10min
|
|
Incolore-rose
pale
|
Rose-rouge(5)
|
|
GEL
|
Gélatine
|
0.6
|
Gélatinase
|
non diffusion
|
Diffusion du
pigment noir
|
|
GLU
|
D-glucose
|
1.9
|
fermentation -
oxydation
(GLUcose) (4)
|
Bleu/bleu-vert
|
jaune
|
|
MAN
|
D-mannitol
|
1.9
|
fermentation -
oxydation
(MANnitol) (4)
|
Bleu/bleu-vert
|
jaune
|
|
INO
|
Inositol
|
1.9
|
fermentation -
oxydation
(INOsitol) (4)
|
Bleu/bleu-vert
|
jaune
|
|
SOR
|
D-sorbitol
|
1.9
|
fermentation -
oxydation
(SORbitol) (4)
|
Bleu/bleu-vert
|
Jaune
|
|
RHA
|
L-rhamnose
|
1.9
|
fermentation -
oxydation
(RHAmnose) (4)
|
Bleu/bleu-vert
|
Jaune
|
Annexes
|
SAC
|
D-saccharose
|
1.9
|
fermentation -
oxydation
(SACharose) (4)
|
Bleu/bleu-vert
|
jaune
|
|
MEL
|
D-melibiose
|
1.9
|
fermentation -
oxydation
(MELibiose) (4)
|
Bleu/bleu-vert
|
jaune
|
|
AMY
|
Amygdaline
|
0.57
|
fermentation -
oxydation
(AMYgdaline)
(4)
|
Bleu/bleu-vert
|
jaune
|
|
ARA
|
L-arabinose
|
1.9
|
fermentation -
oxydation
(ARAbinose) (4)
|
Bleu/bleu-vert
|
jaune
|
(1): Une très légère
couleur jaune également positive, (2): Une couleur
orange apparaissant après 36-48H d'incubation doit être
considérée négative, (3): Lecture dans la
cupule (zone aérobie), (4): La fermentation commence
dans la parte inférieure des tubes, l'oxydation commence dans la cupule,
(5): Une légère coloration rose apparaissant
après 10 minutes doit être lue négative.
Annexes
Annexe 4 : Tableau d'identification d'API 20E
(Bio Mérieux SA, 2010). - % de la
réaction positive après 18 - 24 / 48 h à 36 °C #177;
2

Annexes
Annexe 5 : standardisation McFarland 0.5
- réparation de l'étalon de
turbidité McFarland 0,5(CA-SFM / EUCAST, 2019).
1- Ajouter 0,5 mL d'une solution à 0,048 mol/L de BaCl2
(1,175% p/v BaCl2·2H20) à 99,5 mL d'une solution 0,18 mol/L (0,36
N) de H2SO4 (1% v/v) et agiter vigoureusement.
2- Vérifier la densité de la suspension à
l'aide d'Un spectrophotomètre avec un faisceau de 1 cm et des cuvettes
assorties. L'absorbance à 625 nm doit être comprise entre 0,08 et
0,13.
3- Distribuer la suspension dans des tubes de même taille
que ceux utilisés pour ajuster l'inoculum. Sceller les tubes.
4- Une fois scellés, conserver ces tubes à
température ambiante et à l'abri de la lumière.
5- Avant usage, mélanger vigoureusement le tube à
l'aide d'un Vortex.
6- Renouveler l'étalon ou vérifier son absorbance
après 6 mois de conservation.
7- Il convient de vérifier les étalons
achetés dans le commerce en s'assurant que l'absorbance se situe dans
les limites fixées.
Résumé
Nous avons réalisé une étude sur l'argile
de type de Bentonite de Maghnia pour voir son effet antibactérien sur la
bactérie Escherichia coli. En premiers lieu on a fait une
étape de ré -identification de la souche par des tests
microbiologique et biochimique, ces tests avaient donné des
résultats positifs, et la deuxième partie consiste l'argile :
tamisage, stérilisation et dilution enfin pour faire l'antibiogramme.
L'étude de l'effet synergique des acides et la
bentonite ont indiqué la présence d'effets bactéricides
significatifs. Et aussi les résultats démontrent que la
capacité antimicrobienne de la Cu2+/montmorillonite
était très efficace sur Escherichia coli.
Abstract
We conducted a study on Maghnia's Bentonite-clay to see its
antibacterial effect onto the bacteria Escherichia coli. The first
step was to re-identify the strain by microbiological and biochemical tests,
these tests had given positive results, and the second part is about the clay:
sieving, sterilization and finally dilution to do the antibiogram.
The study of the synergistic effect of acids and bentonite
indicated the presence of signify antbactericidal effects. And also the results
demonstrate that the antimicrobial capacity of Cu2 +/montmorillonite
was very effective on Escherichia coli.
|
ÊäÇß
|
.ÉíäæáæÞáÇ
|
ÉíßíÑÔáÅÇ
ÇíÑíÊßÈ ìáÚ
ÇíÑíÊßÈáá
ÏÇÖãáÇ
åÑíËÊ ÉÑÚãá
ÊíäæÊäÈáÇ
|
ÕÎáã
Úæä ÉíäÛã
äíØ ìáÚ
ÉÓÇÑÏ
ÇäíÑÌ
|
åÐå ÊØÚ ÏÞæ
ÉíæíÍáÇ
ÉíÆÇíãíßáÇæ
ÉíÌæáæíÈæÑßíãáÇ
ÊÇÑÇÈÊÎáÇÇ
ÞíÑØ äÚ
ÉááÇÓáÇ
ÏíÏÍÊ ÉÏÇÚÅ
íå ìáæáÇ
ÉæØÎáÇ
íæíÍáÇ
ÏÇÖãáÇ áãÚá
ÉáÈÑÛáÇ
íÎÊáÇæ
ãíÞÚÊáÇ :
äíØáÇ ÑíÖÍÊ
áæÍ ÑæÍãÊí
íäÇËáÇ
ÁÒÌáÇæ
ÉíÈÇÌíÅ
ÌÆÇÊä
ÊÇÑÇÈÊÎáÇÇ
ä ÇðÖí
ÌÆÇÊäáÇ
ÊÑåÙæ
.ãíËÇÑÌáÇ
ìáÚ ÊÇÑíËÊ
ÏæÌæ ìáÅ
ÊíäæÊäÈáÇ
Úã ÖÇãÍáá
íÑÒÂÊáÇ
ÑíËÊáÇ
ÉÓÇÑÏ
ÊÑÇÔ
.ÉíäæáæÞáÇ
ÉíßíÑÔáÅÇ
ìáÚ ÇðÏÌ
ÉáÇÚ ÊäÇß
ÓÇÍäáÇ
íÆÇäË/
ÊíäæáíÑæãÊäæã
íÆÇäËáÇ äã
ÊÇÈæÑßíãáá
ÉÏÇÖãáÇ
ÉÑÏÞáÇ
| 


