République Algérienne Démocratique
et Populaire
Ministère de l'Enseignement Supérieur et
de la Recherche Scientifique
Université d'Alger Centre

Faculté de Médecine d'ALGER
Département de PHARMACIE
SURVEILLANCE DES INFECTIONS NOSOCOMIALES
EN
PEDIATRIE AU CHU BENI MESSOUS
Session : 2019/2020
Présenté par : Le : 28/10/2020
Mohamed Anis SAIDOUNE
Encadré par :
Pr D. TOUATI
(Professeur en Microbiologie clinique)
Devant le Jury :
Président du jury : Professeur KEZZAL
Examinateurs : Professeur TALI MAAMAR
Docteur HAMIDI
À la mémoire des enfants malades
décédés lors
de cette étude
« Ce qui est le plus fondamental, c'est que les
gens connaissent la vérité plutôt que ma propre
justification. Une société saine devrait se faire à
plusieurs voix »
Docteur Li Wenliang, médecin et lanceur d'alerte Chinois,
harcelé par les autorités pour « diffusion de rumeurs
démoralisantes »
Il est décédé du Covid-19, virus contre
lequel il avait mis en garde l'opinion publique internationale.
Nous tenions à lui rendre hommage et à lui dire que
:
« Si l'humain est ingrat, l'humanité
est reconnaissante »
A ces professeurs qui nous ont donné le goût des
choses. Et à ma promotrice qui m'a (re)donné le goût de la
microbiologie clinique.
Citation d'Isaac Newton, en parlant de ses enseignants :
« Si j'ai pu voir plus loin, c'est que je me
tenais sur les épaules de
géants »
À la mémoire de mon grand père, dont l'amour
m'a sauvé de la prématurité émotionnelle « Tu
n'es plus là où tu étais mais tu es partout où je
suis » ;
À mes parents, à qui je dois mes « facteurs de
virulence » ;
À Hanifa et Layali, à qui je dédie mes
succès et auprès de qui j'oublie mes défaites ;
À ces « fluctuat nec mergitur » que sont mes
amis ; M.Ali, H.Jughurta, F. Louisa, S. Anne-Claire, R.Djidjik ;
À tonton et tata Kridi, pour leur hospitalité de
Pachas.

Aphorisme attribué à Hippocrate ; C'est le premier
principe
de prudence appris aux étudiants en sciences
médicales.
« Primum non nocere »
« Avant tout, ne pas nuire »
Plan
Liste des abréviations 7
Liste des figures 8
Liste des tableaux 9
Introduction et objectifs 10
I. Chapitre I : 13
I.1. Définition(s) des infections nosocomiales : 14
I.2. Modes de transmission : 15
I.3. Types d'infections nosocomiales 16
I.3.1. Les Infections urinaires 16
I.3.2. Infections du site opératoire 16
I.3.3. Infections pulmonaires nosocomiales 17
I.3.4. Bactériémies / Fongémies : 18
I.3.5. Les infections liées aux cathéters :
19
I.3.6. Autres infections nosocomiales 21
I.4. Les Facteurs de risque des IN 23
I.5. Les micro-organismes nosocomiaux 24
I.5.1. Bactéries 25
I.5.2. Parasites et champignons 27
I.5.3. Virus 27
I.6. Epidémiologie des IN 28
I.7. Aspects réglementaires : 33
II. Chapitre II : 35
II.1. Matériel et méthodes : 37
II.1.1. Matériel : 37
II.1.2. Méthodes : 38
II.1.2.1. Recueil de données : 38
II.1.2.2. Description des lieux de l'étude 38
II.1.2.3. Le déroulement de la surveillance : 41
II.1.2.4. Logigrammes de prise en charge des
prélèvements au laboratoire de microbiologie : 42
III. Chapitre III : 47
III.1. Résultats : 48
III.1.1. Résultats par phase : 48
III.1.1.1. Épisode de surveillance numéro 1 :
48
III.1.1.2. Épisode de surveillance numéro 2 :
49
III.1.1.3. Épisode de surveillance numéro 3 :
51
III.1.2. La variation de la prévalence des infections
nosocomiales durant l'étude 52
III.1.3. Résultats des trois épisodes de
surveillance des IN : 54
III.2. Commentaires et discussion : 61
Conclusion 68
Recommandations et mesures correctives 70
Références Bibliographiques 75
Annexes 78
Liste des abréviations
· °C : Degré Celsius
· ABRI : Acinetobacter baumannii
Résistant à l'Imipénème
· BHRe : Bactérie Hautement
Résistante émergente
· BGN : Bacilles Gram Négatif
· BLSE : Bêtalactamases à
Spectre Elargi
· BMR : Bactérie
Multi-Résistante
· CDC : Center for Disease Control and
prevention
· CHU : Centre Hospitalo-Universitaire
· CLIN : Comité de Lutte contre les
Infections Nosocomiales
· CMV : Cytomégalovirus
· CPAP : Continuos Positive Airway
Pressure
· CTINILS : Comité Technique des
Infections Nosocomiales et des Infections Liées aux Soins
· CVC : Cathéter Veineux
Périphérique
· DASRI : Déchets
d'activités de soins à risques infectieux et assimilés
· E-BLSE : Entérobactéries
productrices de bêtalactamases à spectre élargi
· ERV : Enterococcus faecium
résistant à la Vancomycine
· GB : Globules Blancs
· GN : Gélose Nutritive
· HUG : Hôpitaux Universitaires de
Genève
· IAS : Infection(s) associée(s)
aux Soins
· ILC : Infection Liée au
Cathéter
· IN : Infection(s) nosocomiale(s)
· KES : Klebsiella, Enterobacter,
Serratia
· KP : Klebsiella pneumoniae
· MMH : Maladie des Membranes Hyalines
· MSP : Ministère de la
Santé Publique
· lNHSN : National Healthcare Safety
Network
· OMS : Organisation Mondiale de la
Santé
· ORL : Otto, Rhino, Laryngo
· PARC : Pseudomonas aeruginosa
résistant à la Ceftazidime
· PAVM : Pneumopathie Associée
à la Ventilation Mécanique
· SARM : Staphylococcus aureus
résistant à la Méthicilline
· SCN : Staphylocoque à Coagulase
Négative
· SHA : Solution Hydro-Alcoolique
· UFC : Unit Forming Colony
· USI : Unité de Soins Intensifs
· VM : Ventilation Mécanique
· VNI : Ventilation Non Invasive
· VRS : Virus Respiratoire Syncytial
Liste des figures
Figure 1 - La surveillance des infections nosocomiales : un
processus circulaire. 30
Figure 2 - ARRÊTÉ N°64 MSP DU 17/11/1998
PORTANT CREATION D'UN COMITE DE LUTTE CONTRE LES INFECTIONS NOSOCOMIALES AU
NIVEAU DES
ETABLISSEMENTS DE SANTE. 33
Figure 3 - CHU Béni Messous 38
Figure 4 - Plan du service de pédiatrie du CHU Beni
Messous 39
Figure 5 - Logigramme de prise en charge des
prélèvements profonds au laboratoire de
microbiologie. 42
Figure 6 - Logigramme de prise en charge des hémocultures
au laboratoire de microbiologie. 43
Figure 7 - Logigramme de prise en charge des
prélèvements urinaires au laboratoire de
microbiologie. 44
Figure 8 - Logigramme de prise en charge
des prélèvements superficiels au laboratoire de
microbiologie. 45
Figure 9 - Répartition selon le type d'infection durant
la phase I. 48
Figure 10 - Répartition selon le type de micro-organismes
isolés durant la phase I. 49
Figure 11 - Répartition selon le type d'infection durant
la phase II. 50
Figure 12 - Répartition selon le type de micro-organismes
isolés durant la phase II. 50
Figure 13 - Répartition selon le type d'infections durant
la phase III. 51
Figure 14 - Répartition selon le type de micro-organismes
isolés durant la phase III. 51
Figure 15- Variation de la prévalence moyenne en
pédiatrie durant les trois enquêtes. 52
Figure 16 - Variation de la prévalence moyenne à
l'unité Mussy durant les trois enquêtes. 52
Figure 17 - Variation de la prévalence moyenne à
l'unité de soins intensifs (Nobecourt) durant les
trois enquêtes 53
Figure 18 - Variation de la
prévalence moyenne à l'unité de Néonatologie
(Nobecourt) durant les
trois enquêtes 53
Figure 19 - Distribution des patients infectés selon la
tranche d'âge. 55
Figure 20 - Répartition selon le nombre d'infections
contractées par le même malade 55
Figure 21- Répartition selon le type de micro-organismes
isolés durant l'étude. 56
Figure 22 - Répartition des micro-organismes
isolés durant l'étude par familles. 56
Figure 23 - Micro-organismes isolés durant l'étude
par espèce. 57
Figure 24 - Consommation en SHA du service de Pédiatrie
durant les mois de Janvier, Février et
Mars selon la pharmacie du CHU. 60
Figure 25 - Exemples de plaques signalétiques au lit du
patient 72
Figure 26 - Photos d'infections cutanées nosocomiales
contractées à l'unité Mussy 82
Figure 27 - Enterococcus faecium multirésistant
retrouvé en pédiatrie durant la pré-enquête sur
un
prélèvement d'abcès péri-anal. 83
Figure 28 - Corrélation consommation en antibiotiques et
résistance [30] 84
Liste des tableaux
Tableau 1 - Liste de BMR/BHRe 27
Tableau 2 - Indicateurs de fréquence des infections
nosocomiales [4] 29
Tableau 3 - Levures dans un examen direct à
l'état frais 46
Tableau 4 - Bourgeonnement caractéristique des levures
du genre Candida 46
Tableau 5- Candida albicans test de blastèse 46
Tableau 6 - Motifs d'hospitalisation des patients suivis.
54
Tableau 7 - Tableau récapitulatif. 58
Tableau 8 - Stratification des IN suivant le risque
infectieux selon guide pratique de lutte contre les
infections nosocomiales de l'OMS. 74
Introduction et objectifs
11
Introduction et objectifs
Malgré tout le progrès que la médecine
humaine connaît, et d'après des études
réalisées dans des pays très industrialisés, les
infections nosocomiales restent une cause majeure, ou du moins peu
négligeable de morbidité et même de mortalité.
Une enquête de prévalence réalisée
par l'OMS, dans 55 hôpitaux de 14 pays différents,
représentant quatre régions OMS, a montré qu'en moyenne
8,7 % des patients hospitalisés sont touchés par une infection
nosocomiale. A tout moment, plus de 1,4 million de personnes à travers
le monde souffrent de complications infectieuses acquises à
l'hôpital. [4]
Les organismes internationaux de santé sont dans une
posture de lanceurs d'alerte en ce qui concerne la microbiologie humaine
moderne. « Nous sommes dans une course aux armements contre les microbes
» martelait Sally Davies, médecin en chef du Royaume-Uni, dans une
tribune au magazine Nature.
Ce lexique va-t'en guerre pourrait, au premier abord,
s'apparenter à vision dystopique ; mais les récentes
données sur l'étonnante « plasticité génomique
» des bactéries semblent étayer ce paradigme de la
microbiologie humaine.
L'OMS est catégorique ; la résistance aux
antibiotiques est l'un des défis majeurs auquel fait face
l'humanité et selon une étude prospective, elle pourrait
être responsable d'ici 2050 de 10 millions de morts par un (soit bien
plus que le cancer).
« Le monde risque de sombrer dans une
ère post-antibiotiques : le moment est venu de prendre
des mesures
énergiques »
Que se passe-t-il quand la résistance aux
antibiotiques, de plus en plus grandissante, rencontre des hôpitaux
insalubres et très gourmands en antibiothérapie empirique.
Les infections nosocomiales ont des coûts, leurs
impacts étant directs et indirects (augmentation de la durée
d'hospitalisation, mobilisation du personnel, létalité, handicaps
temporaires ou permanents, nombre de jours non travaillés par patient
etc.)
Où en est la situation dans notre pays quant aux
infections nosocomiales et plus précisement en pédiatrie ? La
littérature ne semble pas vraiment foisonnante concernant ce sujet et
même si les autorités compétentes ont, semble-t-il, prit
des mesures pour la lutte contre les Infection Nosocomiales à travers
l'installation de réseaux de surveillance, l'efficience de ces
réseaux a-t-elle été dûment éprouvée
?
Les chiffres officiels ne semblent pas dans la
dénégation de la gravité de ce problème de
santé publique ; Selon le ministère de la santé, de la
population et de la réforme des hôpitaux Algérien, la
prévalence est estimée à environ 15 % en moyenne à
travers le territoire national.
Dans un système de santé où les soins
sont gratuits et accessibles à tous, et dans une perspective
économique qui s'annonce déjà tortueuse, il semble qu'en
plus d'épargner à nos patients des souffrances inutiles et
d'alléger le fardeau économique de ce problème, endiguer
ce phénomène est non seulement un devoir éthique mais
aussi, à terme, un investissement.
Aussi, un retour d'information régulier et rapide joue
un rôle important dans la motivation des professionnels hospitaliers. En
effet, pouvoir mesurer de manière concrète et observer l'impact
réel des mesures correctives entreprises permet de renforcer les bonnes
pratiques.
12
Introduction et objectifs
Pour toutes ces raisons, nous avons décidé de
nous engager dans ce modeste travail avec l'intention d'en faire bien plus
qu'un simple mémoire de fin d'études mais dans une approche de
porteurs de projet.
Suite à la pandémie de la Covid-19, la
perception du risque microbiologique a significativement changé. Les
mises en gardes sont devenues plus tangibles car vécues par
l'humanité à son corps défendant, et, les initiés
autant que les néophytes savent mieux désormais que ces risques
ne sont pas des fantasmes, mais bel et bien des menaces réelles.
Les gestes barrières, l'hygiène des mains, tout
cela a été à l'ordre du jour durant des mois et les
conséquences de cette crise seront certainement majeures. Un point
d'inflexion dans la perception du risque microbiologique à tous les
niveaux.
Nous avons tenu à vous dire que, de bout en bout, notre
souci a été de pouvoir diligenter une dynamique, et apporter une
valeur ajoutée, aussi modeste soit-elle, à la lutte contre les
infections nosocomiales dans notre pays.
Cet aspect élémentaire qui nous a
aiguillonné tout au long de ce travail.
Objectifs
Objectif Principal :
- Réaliser une surveillance
épidémiologique active sur trois périodes d'une semaine
chacune. Objectifs Secondaires :
- Rechercher les BMR/BHRe responsables
d'Infections Nosocomiales et connaitre l'écologie bactérienne du
service
- Démontrer au personnel de la
santé du service l'impact de l'observation des précautions
standards et spécifiques dans la lutte contre les infections
nosocomiales afin de renforcer les bonnes pratiques.
- Proposer des mesures correctives
réalistes, efficaces, et adaptées aux spécificités
du service.
Chapitre I :
REVUE DE LA LITTÉRATURE
14
Chapitre I : REVUE DE LA LITTÉRATURE
I.1. Définition(s) des infections nosocomiales :
Infections Associées aux Soins (IAS), qui, comme le
nom l'indique, concernent tous les types d'infections acquis dans n'importe
quelle structure de soin (Cabinets médicaux, gestes diagnostiques, etc.)
et n'est pas restreinte qu'aux cas d'infections lors d'une hospitalisation.
Les infections nosocomiales représentent une
catégorie des IAS.
Les infections nosocomiales - aussi appelées
infections hospitalières - sont des infections acquises pendant un
séjour à l'hôpital et qui n'étaient ni
présentes ni en incubation au moment de l'admission du patient. Les
infections survenant plus de 48 heures après l'admission sont
habituellement considérées comme nosocomiales.
Le délai peut s'étendre jusqu'à 30 jours
lors du cas précis d'une infection du site opératoire, voire
à une année en cas de pose de matériel étranger de
type prothèse, valve cardiaque, stimulateur cardiaque...
Des définitions permettant d'identifier les infections
nosocomiales de diverses localisations qui s'appuient sur des critères
cliniques, radiologiques et biologiques et portent sur une cinquantaine de
sites infectieux potentiels.
Aussi, la notion de période d'incubation est capitale
dans la délibération. Par exemple, la durée d'incubation
d'une pneumocystose s'étend de 1 à 3 mois ; Si un Pneumocystis
spp est diagnostiqué chez un patient, il sera de rigueur de
considérer avec prudence la notion de période d'incubation et de
manière générale, la délibération
obéit à tout un faisceau d'arguments et n'est pas
systématique dans les cas douteux où s'agira d'apprécier
la plausibilité du lien causal entre l'hospitalisation et l'infection
Il est nécessaire aussi d'exclure de la
définition : les réactivations d'infections latentes comme le
zona ou l'herpès , et les infections foeto-maternelles se
déclarant moins de 48 heures après la naissance , l'aggravation
d'une infection déjà existante à moins que la
causalité soit imputée à un nouveau pathogène ou
bien qu'une nouvelle porte d'entrée de l'infection soit
identifiée.[4]
La dichotomie qui oppose donc infections nosocomiales aux
infections communautaires est de plus en plus abstraite et tend à
être de plus en plus indéterminée, vu la multiplication des
parcours de soins et leur diversification.
Notons aussi que dans le cas d'IAS, les infections concernent
aussi le personnel soignant et autres visiteurs et ne sont pas restreintes aux
malades uniquement.
15
Chapitre I : REVUE DE LA LITTÉRATURE
I.2. Modes de transmission :
Les agents pathogènes nosocomiaux peuvent avoir deux
origines principales :
- Une origine endogène :
C'est à dire que le germe provient de la flore commensale
du patient lui-même.
Les Bactéries multi résistantes sont de plus en
plus retrouvées dans cette dernière. Par exemple, une
récente étude espagnole s'est intéressée au portage
digestif des souches E-BLSE :
« Le portage digestif de souches productrices de BLSE est
devenu non négligeable avec un réservoir de BLSE animal
important. Dans une étude récente espagnole, les taux de portage
de souches de E. coli productrices de BLSE étaient de 11,8 % chez les
patients hospitalisés et de 5,5 % chez les patients de ville »
[1]
- Une origine exogène :
Que cela soit la flore transitoire ou résidente du
personnel soignant, visiteurs, l'environnement, les dispositifs
médicaux, locaux, les sources de pathogènes sont multiples.
[2]
La transmission peut se faire soit par voie manuportée
(par contact direct) ou transmise par l'environnement, objets ou dispositifs
médicaux (par contact indirect) :
- Par contact direct :
Les mains du personnel soignant, visiteurs, patients jouent
un rôle dans le transfert passif des microorganismes d'un malade à
un autre.
Les mains du personnel peuvent contenir de 100 à 1000
bactéries/cm2 [4] En plus de la flore résidente, on
retrouve la flore transitoire : ce sont les germes de « l'ambiance
hospitalière ».
- Par contact indirect :
Les objets et les matériaux présents à
l'hôpital sont un réservoir de germes.
- Transmission par voie aérienne (patients
immunodéprimés+++)
- Transmission par l'intermédiaire d'un support
contaminé (nourriture dans le cas de Toxi-infections
alimentaires)
- Transmission par voie hydrique (la légionellose
nosocomiale). [3]
16
Chapitre I : REVUE DE LA LITTÉRATURE
I.3. Types d'infections nosocomiales
Les définitions peuvent légèrement varier
et la démarche à suivre est de s'appuyer sur des
définitions consensuelles et en harmonie avec les objectifs
(surveillance épidémiologique, procédures
d'évaluation, expertises judiciaires).
Des définitions standardisées sont
régulièrement publiées par différents
référents et sociétés savantes en microbiologie
humaine.
Par exemple, aux États-unis, et pour le compte du NHSN
(National Healthcare Safety Network), 9 règles rigoureuses sont
utilisées afin d'un côté harmoniser la démarche
(réseau de surveillance national et multisectoriel), et d'un autre
côté, éviter tous biais et confusions. [16]
Selon les critères diagnostiques publiés par le
CTINILS (Comité Technique des Infections Nosocomiales et des Infections
Liées aux Soins) [17] nous avons :
I.3.1. Les Infections urinaires
Au moins un des signes suivants :
Fièvre (> 38°C),
Impériosité mictionnelle,
Pollakiurie,
Brûlure mictionnelle, ou douleur sus-pubienne, en
l'absence d'autre cause, infectieuse ou non.
Et :
- Sans sondage vésical ni autre abord de l'arbre
urinaire : Leucocyturie (= 104 leucocytes/ml) et uroculture positive
(= 103 micro-organismes/ml) et au plus 2 micro-organismes
différents.
- Avec sondage vésical ou autre abord de l'arbre
urinaire, en cours ou dans les 7 jours précédents : Uroculture
positive (= 105 micro-organismes/ml) et au plus 2 micro-organismes
différents.
I.3.2. Infections du site opératoire
? Infection superficielle de l'incision
Infection survenant dans les 30 jours suivant l'intervention,
et affectant la peau (ou les muqueuses), les tissus sous-cutanés ou les
tissus situés au-dessus de l'aponévrose de revêtement,
diagnostiquée par :
Cas 1 : Écoulement purulent de
l'incision
Cas 2 : Micro-organisme associé
à des polynucléaires neutrophiles à l'examen direct,
isolé par culture obtenue de façon aseptique du liquide produit
par une incision superficielle ou d'un prélèvement tissulaire.
Cas 3: Ouverture de l'incision par le
chirurgien Et présence de l'un des signes suivants : douleur ou
sensibilité à la palpation, tuméfaction localisée,
rougeur, chaleur
17
Chapitre I : REVUE DE LA LITTÉRATURE
Et micro-organisme isolé par culture OU culture non
faite. (Une culture négative, en l'absence de traitement antibiotique,
exclut le cas)
? Infection profonde (de l'incision ou de
l'organe-espace)
Infection survenant dans les 30 jours suivant l'intervention,
ou dans l'année s'il y a eu mise en place d'un implant, d'une
prothèse ou d'un matériel prothétique, affectant les
tissus ou organes ou espaces situés au niveau ou au -dessous de
l'aponévrose de revêtement, ou encore ouverts ou manipulés
durant l'intervention, diagnostiquée par :
Cas 1 : Écoulement purulent provenant
d'un drain sous-aponévrotique ou placé dans l'organe ou le site
ou l'espace.
Cas 2 : Déhiscence spontanée
de l'incision ou ouverture par le chirurgien et au moins un des signes suivants
: fièvre > 38°C, douleur localisée, ou sensibilité
à la palpation Et micro-organisme isolé par culture, obtenue de
façon aseptique, d'un prélèvement de l'organe ou du site
ou de l'espace OU culture non faite (une culture négative, en l'absence
de traitement antibiotique, exclut le cas).
Cas 3 : Abcès ou autres signes
d'infection observés lors d'une réintervention chirurgicale, d'un
examen histopathologique, d'un examen d'imagerie ou d'un acte de radiologie
interventionnelle.Remarque : Il est important de collecter
systématiquement la nécessité de reprise
opératoire.
I.3.3. Infections pulmonaires nosocomiales
Elles sont divisées en deux entités :
- la pneumonie acquise sous ventilation mécanique
(PAVM), c.à.d. toute pneumonie survenant chez un malade dont la
respiration est assistée par une machine, soit de manière
invasive par l'intermédiaire d'un tube endotrachéal ou d'une
trachéotomie, soit de manière non invasive par
l'intermédiaire d'un masque facial ou d'un autre procédé,
dans les 48 heures précédant la survenue de l'infection,
- la pneumonie survenant en l'absence de ventilation
mécanique, pour lesquelles le diagnostic microbiologique, voire
radiologique peut être difficile et parfois impossible à
établir.
Pneumopathies en pédiatrie :
? Pneumopathies < à 1 an :
Signes radiologiques, et aggravation des gaz du sang
(désaturation) ou besoins accrus en oxygène ou en assistance
respiratoire, et au moins trois des signes suivants :
· Instabilité thermique
· Bradycardie ou tachycardie
· Toux
18
Chapitre I : REVUE DE LA LITTÉRATURE
· Apparition de sécrétions purulentes ou
modifications des caractéristiques (couleur, odeur, quantité,
consistance)
· Dyspnée ou tachypnée ou apnées ou
grunting;
· Auscultation évocatrice.
? Pneumopathies 1 an < âge < 12 ans
Signes radiologiques et au moins trois des signes suivants :
·
°
Aggravation des gaz du sang (désaturation) ou besoins
accrus en oxygène ou en assistance respiratoire ;
· Hyperthermie supérieure à 38,4 C ou
hypothermie inférieure à 36,5°C;
· Leucopénie (< 4000 GB/mm3) ou
hyperleucocytose (> 15 000 GB/mm3);
· Toux ;
· Apparition de sécrétions purulentes ou
modifications des caractéristiques (couleur, odeur, quantité,
consistance) ;
· Dyspnée ou tachypnée ou apnées ou
grunting;
· Auscultation évocatrice
Mis à part les pneumopathies associées à
la ventilation mécanique (PAVM), les patients atteints de convulsions ou
dont le niveau de conscience est altéré sont exposés au
risque d'infection nosocomiale même en l'absence d'intubation. Les
bronchiolites virales (VRS) sont fréquentes dans les services de
pédiatrie, et les pneumopathies par surinfection bactérienne
peuvent toucher les enfants. [4]
I.3.4. Bactériémies / Fongémies
:
Au moins une hémoculture positive (justifiée
par des signes cliniques), sauf pour les microorganismes suivants :
· Staphylocoques à coagulase négative
· Bacillus spp. (sauf B. anthracis)
· Corynebacterium spp.
· Propionibacterium spp.
· Micrococcus spp.
· Ou autres micro-organismes saprophytes ou commensaux
à potentiel pathogène comparable, pour lesquels deux
hémocultures positives au même micro-organisme,
prélevées lors de ponctions différentes, à des
moments différents, et dans un intervalle rapproché (un
délai maximal de 48h est habituellement utilisé), sont
exigées.
Spécificité des bactériémies
à micro-organismes de la flore cutanée commensale en
néonatologie :
Le micro-organisme est isolé sur une seule
hémoculture alors que le patient est porteur d'un cathéter
intravasculaire et qu'une antibiothérapie appropriée a
été mise en route par le médecin ; si le
19
Chapitre I : REVUE DE LA LITTÉRATURE
patient est déjà sous antibiotique et que
l'antibiothérapie n'est pas modifiée par le résultat de
l'hémoculture, on retiendra une contamination sauf si
l'antibiothérapie était déjà adaptée.
Les bactériémies et fongémies
(regroupées sous le terme générique de
bactériémies) sont recensées indépendamment des
infections qui en sont le point de départ. La porte d'entrée de
la bactériémie est systématiquement notée
(bactériémie secondaire, comprenant les infections liées
aux cathéters). En l'absence de porte d'entrée identifiée,
on parle alors de bactériémie primaire.
Le CDC subdivise les Bactériémies nosocomiales
[16] en deux :
- Bactériémie primaire :
Si hémoculture positive en l'absence de source
d'infection au niveau d'un autre site anatomique comprennent également
les infections compliquant l'insertion d'un cathéter intraveineux ou
intra-artériel.
- Bactériémie secondaire :
Infections documentées au niveau d'un autre site
anatomique (pneumonie, infection urinaire, infection de plaie, ...)
Le(s) même(s) micro-organisme(s) est / sont
identifié(s) soit simultanément, soit séquentiellement
(sang / site anatomique)
I.3.5. Les infections liées aux cathéters
:
Infections liées aux cathéters (ILC) La simple
présence d'hémocultures positives chez un malade porteur de
cathéter, sans porte d'entrée évidente sera
identifiée comme bactériémie primaire et non
rattachée à la présence du cathéter.
Cathéters veineux centraux La
bactériémie/fongémie liée au CVC est définie
par :
· l'association d'une
bactériémie/fongémie survenant dans les 48 h encadrant le
retrait du CVC (ou la suspicion diagnostique d'infection de cathéter si
celui-ci n'est pas retiré d'emblée).
Et :
· SOIT une culture positive avec le même
micro-organisme sur l'un des prélèvements suivants : culture du
site d'insertion ou culture du CVC = 103 UFC/ml.
· SOIT des hémocultures
périphérique et centrale positives au même micro-organisme
avec un rapport hémoculture quantitative centrale/hémoculture
périphérique > 5 ou un délai différentiel de
positivité des hémocultures centrale/périphérique
> 2 h, avec une positivité plus rapide pour l'hémoculture
centrale.
En l'absence de bactériémie le diagnostic d'ILC
repose sur :
· ILC locale :
- culture de CVC = 103 UFC/ml
- et la purulence de l'orifice d'entrée du
cathéter ou une tunnelite,
· ILC générale :
- culture de CVC = 103 UFC/ml
- et une régression totale ou partielle des signes
infectieux généraux dans les 48 h suivant l'ablation du
cathéter.
20
Chapitre I : REVUE DE LA LITTÉRATURE
Remarques : - Le rapport hémoculture quantitative
centrale/périphérique ou le délai différentiel de
positivité des hémocultures centrale/périphérique
peuvent être réalisés en utilisant le
prélèvement qui a servi à établir le diagnostic de
bactériémie - Il est déconseillé d'utiliser la
technique semi-quantitative de culture du cathéter selon la
méthode de Maki.
Cathéters veineux périphériques :
Bactériémie/fongémie liée au CVP :
· L'association d'une
bactériémie/fongémie survenant dans les 48 h encadrant le
retrait du CVP.
· Et l'un des éléments suivants :
- Culture du CVP = 103 UFC/ml avec le même
micro-organisme,
- Ou la présence de pus au site d'insertion du CVP, en
l'absence d'une autre porte d'entrée
identifiée.
En l'absence de bactériémie le diagnostic d'ILC
sur CVP repose sur :
· ILC locale :
- culture de CVP = 103 UFC/ml, si le CVP est
adressé en culture pour suspicion d'infection - ou la présence de
pus au site d'insertion du cathéter avec culture positive du site
d'insertion ou absence de culture du site d'insertion (une culture
négative, en l'absence de traitement antibiotique, exclut le cas).
· ILC générale
- Culture de CVP = 103 UFC/ml
- Et une régression totale ou partielle des signes
infectieux généraux dans les 48 h suivant l'ablation du
cathéter.
Cathéters artériels : La fréquence des
infections est classiquement plus faible que pour les voies veineuses
centrales. La définition est la même que pour les CVC.
Cathéters de dialyse et cathéters artériels pulmonaires.
La fréquence des infections est élevée du fait de
manipulations fréquentes qui doivent faire l'objet de recommandations
particulières. La définition est la même que pour les
CVC.
Cathéters de longue durée (cathéters
tunnellisés et cathéters implantables) L'ablation du
cathéter n'étant pas toujours réalisée, le
diagnostic d'ILC est souvent porté matériel en place. Dans ce
cas, les méthodes de diagnostic avec cathéter en place trouvent
toute leur importance : hémocultures différentielles,
prélèvements locaux lorsqu'il existe une émergence
cutanée.Par ailleurs, l'apparition de signes cliniques lors de
l'utilisation de la ligne veineuse (branchementd'une perfusion) est hautement
prédictive d'infection sur cathéter. Le délai
différentiel de positivité des hémocultures
centrale/périphérique permet alors d'en faire le diagnostic. La
définition est la même que pour les CVC, en prenant en compte
comme date d'inla date de suspicion diagnostique et non la date de retrait du
cathéter.
21
Chapitre I : REVUE DE LA LITTÉRATURE
I.3.6. Autres infections nosocomiales
- Infections de la peau des tissus mous : Les plaies ouvertes
(ulcères, escarres, brûlures).
- favorisent la colonisation bactérienne et peuvent
conduire à des infections parfois généralisées.
- La gastro-entérite est l'infection nosocomiale la plus
fréquente chez l'enfant, avec Rotavirus
comme principal agent pathogène. [4]
- Sinusites, autres infections de la sphère ORL,
infections de l'oeil et de la conjonctive.

« Béchamp avait raison ; le microbe
n'est rien, le terrain
est tout»
Louis Pasteur citant Antoine
Béchamp
23
Chapitre I : REVUE DE LA LITTÉRATURE
I.4. Les Facteurs de risque des IN Facteurs liés
au patient
Âge = 1 an ; le jeune enfant, alors même que ses
systèmes immunitaires innés et adaptatifs commencent à
mûrir, est vulnérable à de nombreux virus,
bactéries, champignons et parasites pathogènes.
En néonatologie, le risque infectieux est important
chez les faibles poids de naissance et les prématurés.
En fonction de son âge, l'enfant est exposé
à différents risques infectieux. Si le grand enfant est
exposé aux mêmes risques que l'adulte, le nourrisson est, lui,
plus exposé au risque viral, notamment en période hivernale alors
que le nouveau-né, dont le risque est variable selon le poids de
naissance, est plus exposé aux risques environnementaux.
En effet, le risque de survenue d'infections nosocomiales chez
l'enfant dépend non seulement de l'exposition à un
réservoir donné, mais aussi de la maturité du
système immunitaire et de l'existence ou non d'une protection maternelle
résiduelle.
- Traitement immunosuppressif à base de
chimiothérapie. - Traumatisme, brûlures ou Psoriasis.
- Diabète déséquilibré.
- La dénutrition sévère avec une
albuminémie inférieure à 30g/L est un facteur de risque de
pneumopathie nosocomiale.
L'environnement hospitalier
Les établissements de santé constituent un
environnement dans lequel se troublent rassemblées des personnes
infectées et des personnelles chez lesquelles le risque d'infection est
accru. Les hôpitaux surpeuplés , les fréquents transferts
de patients d'un service à l'autre et la concentration dans un
même secteur de patients hautement vulnérables à
l'infection tel que les nouveaux nés , les brûlés et les
patients en unités de soins intensifs sont des facteurs qui contribuent
au développement d'Infections nosocomiales.
La notion de travaux de construction dans et autour des
structures de santé est aussi retrouvée dans certaines
études ; la division des infections nosocomiales et professionnelles
Canadienne a publié un document intitulé « Infections
nosocomiales chez les patients d'établissements de santé
liés aux travaux de construction » , qui démontre une
incidence de l'augmentation de la mortalité par des germes fongiques (
Aspergillus spp, Candida albicans , Candida
parapsilosis, Candida tropicallis, ou bactériologiques
(Légionelles).
Facteurs liés à la prise en charge du
patient
Le recours à des gestes invasifs diagnostiques et
thérapeutiques et l'utilisation de différents dispositifs
médicaux, à savoir :
24
Chapitre I : REVUE DE LA LITTÉRATURE
- Le sondage vésical pour les infections nosocomiales
urinaires.
- La ventilation mécanique pour les pneumopathies
nosocomiales (Le risque augmente avec la durée de séjour)
- Le cathétérisme périphérique ou
central pour les infections sur cathéter.
- Différents implants.
- Les gestes invasifs comme les diverses interventions
chirurgicales.
-Une antibiothérapie peut sélectionner une
bactérie intestinale capable de translocation.
Facteurs liés aux micro-organismes
Les germes présents dans la flore microbienne peuvent
contaminer les objets, les dispositifs médicaux et des substances qui
entrent ensuite en contact avec des sites anatomiques vulnérables, des
bactéries véhiculées par l'eau (mycobactéries
atypiques, légionelles) et des virus ou parasites sont
régulièrement identifiées.
La résistance bactérienne par exemple est
induite par le trigger qu'est l'antibiotique. De nombreux patients
reçoivent des anti-infectieux et par le biais de la sélection et
de l'échange d'éléments de résistance
génétique, les antibiotiques favorisent l'émergence de
souches bactériennes multirésistances ; Ce
phénomène est appelé la pression de
sélection.
L'usage répandu des anti-infectieux pour le traitement
ou la prophylaxie (y compris en application locale) est le principal
déterminant de la résistance.
A mesure de l'utilisation croissante d'un anti infectieux, les
bactéries qui lui sont résistantes finissent par émerger
et peuvent se propager.
Des souches multirésistantes de Klebsiella et
de Pseudomonas aeruginosa sont prévalentes dans de nombreux
hôpitaux. Ce problème est particulièrement critique dans
les pays en développement où les antibiotiques de deuxième
intention peuvent ne pas être disponibles. [5]
La possibilité de produire du biofilm apparaît
aussi comme un facteur pouvant favoriser la pathogénicité des
micro-organismes associés à cette notion.
Par exemple, Pseudomonas aeruginosa
causant des infections sur cathéters sont de fréquents
producteurs de biofilms.
I.5. Les micro-organismes nosocomiaux
Beaucoup de germes, sont qualifiés de nosocomiaux
étant donné leur redondance dans les surveillances
épidémiologiques.
Il n'en demeure pas moins que chaque service a ses propres
spécificités et son « écologie microbienne ».
Nous citons, à titre d'exemple, une liste non
exhaustive des germes les plus fréquents dans la problématique
des Infections Nosocomiales.
25
Chapitre I : REVUE DE LA LITTÉRATURE
I.5.1. Bactéries
1) Bacilles Gram négatif fermentants : Les
Entérobactéries :
? Klebsiella pneumoniae :
C'est des BGN aerobie anaerobies facultatifs, appartenant
à la famille des Enterobacteriaceae
Klebsiella pneumoniae est un hôte
privilégié de certains plasmides à l'origine de
multi-résistances.Ces résistances aux antibiotiques concernent
les aminosides (depuis les années 1970), les céphalosporines de
troisième génération (depuis les années 1980), et
plus récemment les carbapénèmes. Klebsiella pneumoniae
est essentiellement responsable d'infections nosocomiales (infection
broncho-pulmonaires, urinaires, bactériémies, infections
méningées post-traumatiques ou post-chirurgicale.
? Enterobacter :
Plusieurs espèces : E.sakazakii, E.cloacae, E.
aerogenes et ; ces deux dernières étant les plus
retrouvées dans la surveillance des IN et sont des pathogènes
opportunistes.
Les espèces du genre Enterobacter sont souvent
rencontrées dans les unités de soins intensifs et sont à
l'origine de 8,6 % des infections nosocomiales, selon les Centers for Disease
Control and Prevention (CDC) des Etats-Unis. [18]
Les Infections à Enterobacter incluent les
bactériémies, les infections respiratoires basse, les infections
de la peau et des tissus mous, les infections urinaires et
intra-abdominales.
? Escherichia Coli :
Ce sont des Bacille Gram Négatif aérobie connue
aussi sous le nom de colibacille Elle constitue la majorité de la flore
intestinale aérobie ; peut se retrouver également au niveau des
muqueuses de l'homme et de l'animal.
Epidémiologiquement, c'est le germe le plus isolé
dans les infections urinaires.
Les E-BLSE ou Entérobactéries productrices de
béta-lactamases sont des BMR de plus en plus retrouvées en
routine.
2) Bacilles Gram Négatifs non fermentants
:
? Pseudomonas aeruginosa :
Le bacille pyocyanique est une bactérie de
l'environnement mais qui peut être commensale du tube digestif. Il est
considéré comme un opportuniste majeur particulièrement
redoutable chez les immunodéprimés par l'expression de ses
facteurs de pathogénicité à savoir les endotoxines,
exotoxines et enzymes protéolytiques favorisant sa propagation dans
l'organisme.
Dans l'environnement hospitalier, on le retrouve dans les
milieux humides comme les lavabos, robinets, siphons, nébuliseurs,
humidificateurs, et cette bactérie peut parfois contaminer les solutions
antiseptiques, le matériel hospitalier, et on la retrouve dans la flore
intestinale transitoire de l'homme. Les études disponibles montrent
majoritairement que les pneumopathies au bacille pyocyanique sont
généralement tardives.
On retrouve chez cette bactérie la notion de biofilm,
notamment sur les sondes urinaires.
Une étude microbiologique d'isolats de Pseudomonas
aeruginosa sur des patients sondés indique que 77 % des souches
isolées étaient productrices de biofilms.
La majorité des germes isolés étaient des
BMR (69%) et la production de biofilms était corrélée avec
la résistance à la gentamicine. l'association des infections
à Pseudomonas résistantes à la gentamicine et la notion de
biofilm expliquent en partie les résultats de cette étude. [6]
26
Chapitre I : REVUE DE LA LITTÉRATURE
Selon le CDC
Le bacille pyocyanique est :
La seconde cause des pneumopathies nosocomiales au monde (17 %)
La troisième cause d'infections urinaires (7 %)
La quatrième cause des infections du site
opératoire (8 %
Le septième pathogène isolé dans les
hémocultures (2 %) [7]
? Acinetobacter :
L'espèce A.baumanii, commensale de la flore
cutanée, est l'une des principales bactéries responsable
d'infections chez l'humain, surtout dans les unités de
soins intensifs.
Comme résistances acquises, nous retrouvons les ABRI A.
baumanni résistant à l'imipénème
En tant que bactéries multirésistantes.
3) Cocci Gram positif :
? Les Staphylocoques :
L'espèce la plus fréquente est le Staphylocoque
doré (Staphylococcus aureus), qui a pour habitat les fosses nasales et
les mains d'individus sains (portage). Ce genre est responsable d'infections
cutanées et muqueuses, ainsi que de septicémies. C'est l'un des
germes les plus isolés dans les septicémies en
néonatologie (l'opsonisation du staphylocoque doré est
très faible chez les nouveau nés).
Dans une moindre mesure, les SCN (Staphylocoques à
coagulase négative comme le Staphylococcus epidermidis sont
retrouvés généralement dans des bactériémies
sur cathéter).
Les SARM ou Staphylocoques dorés Méthicilline
résistants, sont régulièrement surveillés et font
partie des BMR qui inquiètent de plus en plus la communauté
scientifique.
? Les Entérocoques :
Les Espèces Enterococcus Faecalis et
Enterococcus faecium sont les plus retrouvées. Ils sont
généralement responsables de plus 10 % des Infections
nosocomiales. [8]
Ce sont souvent des commensaux minoritaires de l'intestin et
résistant à un grand nombre d'antibiotiques, dont des
résistances aux glycopeptides (Entérocoques Résistants
à la Vancomycine qui sont des Bactéries Hautement
Résistantes émergentes), en plus de leurs nombreuses
résistances naturelles.
4) Bacilles Gram positif :
? Clostridium difficile :
C'est un bacille anaérobie à Gram positif dont
les souches pathogènes ont la propriété de produire deux
toxines (tdcA et tdcB), il est responsable de près de 10 % des
diarrhées nosocomiales. Il existe entre 1 et 3 % de porteurs sains dans
le monde. [19]
27
Chapitre I : REVUE DE LA LITTÉRATURE
Tableau 1 - Liste de BMR/BHRe
|
BMR/ BHRe*
|
|
SARM : Staphylococcus aureus résistant à
la Méthicilline
|
|
EBLSE : Entérobactéries productrices de
betalactamases à spectre elargi
|
|
PARC : Pseudomonas aeruginosa résistant à
la ceftazidime
|
|
ERV* : E. faecium résistant à la
vancomycine
|
|
EPC* : Entérobactéries productrices de
carbapénèmases
|
|
ABRI : A. baumanni résistant à
l'imipénème
|
I.5.2. Parasites et champignons
Certains parasites (par exemple Giardia lamblia) se
transmettent facilement chez l'adulte et l'enfant. DE nombreux champignons et
autres parasites sont des agents opportunistes et provoquent des infections en
cas de traitement antibiotique prolongé et d'immunodépression
sévère (Candida albicans, Aspergillus spp,
Cryptococcus neoformans, Cryptosporidium).
Ils sont une cause majeure d'infection
généralisée chez les patients
immunodéprimés.
La contamination de l'environnement par des germes
aéroportés comme Aspergillus spp présent dans les
poussières et le sol est également préoccupante et en
particulier lors de la construction d'hôpitaux. Sarcoptes
scabies (agent de la gale) est un ectoparasite qui provoque
régulièrement des flambées épidémiques dans
les établissements de santé.
Il est important de noter l'augmentation des infections
liées à C. albicans et Candida parapsilosis
chez l'enfant. Ainsi Candida est le deuxième agent pathogène
isolé des hémocultures aux États-Unis et une candidose sur
deux est diagnostiquée chez l'enfant.
L'incidence chez l'enfant est de 50 cas pour 100 000
admissions. Cette augmentation chez l'enfant est liée à la
diffusion de C. parapsilosis en hématologie et
néonatalogie. [9,10,11]
I.5.3. Virus
Une des particularités du monde pédiatrique et
notamment chez les nourrissons est la prédominance des infections
virales en période épidémique ou non. [13]
En milieu hospitalier on retrouve des hépatites B et C
(transfusion, dialyse, injections, endoscopie), le virus respiratoire syncytial
(VRS), les rotavirus et les entérovirus.
D'autres virus comme le cytomégalovirus, le VIH, le
virus Ebola, les virus grippaux, les virus de l'herpès et le virus
varicelle-zona sont également transmissibles.
Une étude Allemande en Néonatologie retrouve les
viroses nosocomiales suivantes -Enterovirus et Parechovirus - 20 cas (39 %)
-Virus respiratoire syncytial (VRS) - 15 cas (29 %)
- Rotavirus - 5 cas (10 %)
-CMV - 3 cas (6 %)
Parainfluenza virus - 2 cases (4 %)
Adenovirus - 2 cases (4 %) [12]
28
Chapitre I : REVUE DE LA LITTÉRATURE
I.6. Epidémiologie des IN
Une des spécificités du monde pédiatrique
est la présence d'autres sources d'infections nosocomiales
représentées par les acteurs dits « extérieurs »
que sont les parents, la fratrie et les accompagnateurs que sont les
instituteurs, les clowns et autres animateurs. Ces différents acteurs
majorent le risque de transmission intra-hospitalière, notamment pendant
les périodes saisonnières pendant lesquelles ces acteurs peuvent
véhiculer les agents pathogènes circulants en communautaire vers
l'hôpital.
Les bactériémies représentent globalement
20 % des infections associées aux soins en pédiatrie, mais
peuvent atteindre le chiffre de 36 % en pédiatrie et 45 % en
néonatalogie.
L'incidence est de 1,1 cas/1000 patients admis en
pédiatrie générale et oscille entre 2 et 15 cas/1000
jours-cathéter en réanimation. Cette incidence varie en fonction
du type de cathéter (plus fréquente en cas de cathéter de
Hickman comparativement aux chambres implantables).
Parmi les bactéries rencontrées dans les
infections liées aux cathéters, il est important de souligner la
prédominance des Cocci à Gram positif et, parmi eux, les
Staphylocoques à coagulase négative qui représentent
jusqu'à 58 % des septicémies nosocomiales en réanimation
pédiatrique. [13]
En pédiatrie, les pneumonies acquises sous ventilation
mécanique représentent de 2,5 à 9 cas/1000 jours de
ventilation mécanique. Leur incidence est variable et dépend en
néonatalogie non seulement du poids du nouveau-né, mais de son
terme aussi. Enfin, il est important de noter que la méthode
diagnostique utilisée en pédiatrie est variable d'un centre
à l'autre, ce qui rend la comparaison entre différentes
unités difficile. [13]
Les infections urinaires représentent 6 à 18 %
des infections nosocomiales en pédiatrie générale, pour
une incidence de 6 à 7,8 cas/1000 admissions. Les principaux
pathogènes responsables sont E. coli (39 % des cas), P.
aeruginosa (12 %) et Enterococcus spp. (12 %). Ces infections
sont associées au sondage urinaire et à sa durée. [13]
Épidémiologie descriptive :
La finalité de l'épidémiologie
descriptive est la description d'un phénomène de santé
dans une population (fréquence, variations) en fonction des
caractéristiques de cette population et de paramètres tels que le
temps et l'espace. Elle est nécessaire pour mesurer l'importance d'un
problème de santé et soulever des hypothèses
étiologiques (facteurs de risque de survenue de cette maladie). Exemple
: on souhaite étudier l'évolution de la mortalité par
cancer du sein entre 1980 et 2012 en France.
Épidémiologie analytique
(étiologique ou causale) :
Elle a pour but de rechercher les causes des maladies et les
facteurs ou marqueurs de risque influençant leurs survenues au sein
d'une population. Elle permet ainsi d'établir des relations de
causalité entre l'exposition à un facteur ou marqueur de risque
et la maladie.
Le risque est défini comme la probabilité de
survenue d'un événement donné. Les facteurs de risque
augmentent la probabilité de survenue de la maladie.
Chapitre I : REVUE DE LA LITTÉRATURE Les
indicateurs de fréquence :
La Prévalence : C'est la proportion de
malades présents dans une population à un instant donné.
C'est une photographie qui permet d'avoir une évaluation d'ordre
général.
La période peut tout aussi bien s'étaler sur une
plage temporelle donnée (prévalence hebdomadaire, mensuelle,
annuelle)
Prévalence = m / N
· m = effectif de malades à l'instant t
· N = effectif total de la population à l'instant t
(N = malades + non-malade)
· 0 = ð = 1 (ou 0 % = ð = 100%) [20]
L'Enquête de prévalence des infections nosocomiales
un jour donné estime la proportion de patients ayant une infections
acquise à l'hôpital et active parmi tous les patients
présents le jour de l'enquête.
La prévalence intègre :
· la durée de la maladie.
· la vitesse d'apparition des nouveaux cas de la
maladie.
Tableau 2 - Indicateurs de fréquence des infections
nosocomiales [4]
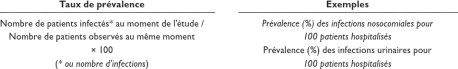
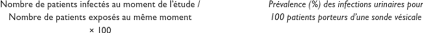
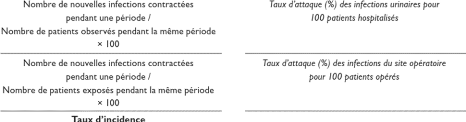
29

30
Chapitre I : REVUE DE LA LITTÉRATURE
INVESTIGATION EPIDEMIOLOGIQUE DES INFECTIONS NOSOCOMIALES :
Selon le manuel de lutte contre les infections nosocomiales de
l'OMS, 2ème édition, publié en 2008 :

Figure 1 - La surveillance des infections nosocomiales :
un
processus circulaire.
Objectifs d'une surveillance des infections nosocomiales
:
Le but ultime est la réduction des infections nosocomiales
et de leur coût.
Les objectifs spécifiques d'un programme de surveillance
sont :
l Améliorer la prise de conscience, chez le personnel
soignant et les autres catégories de personnel (y compris le personnel
de l'administration) du problème des infections nosocomiales et de la
résistance aux anti-infectieux, de façon qu'ils perçoivent
la nécessité des mesures préventives
l Surveiller les tendances : incidence et répartition des
infections nosocomiales, prévalence et, si possible, incidence
ajustée sur le risque aux fins de comparaison intra- et
inter-hôpitaux
l Identifier la nécessité de nouveaux programmes
de prévention ou de programmes renforcés et évaluer
l'impact des mesures préventives·
l Identifier les domaines possibles d'amélioration des
soins et d'élargissement des études
épidémiologiques (analyse des facteurs de risque)
Stratégie :
Un système de surveillance doit satisfaire aux
critères suivants :
l Simplicité, pour réduire les coûts et la
charge de travail, et promouvoir la participation des services concernés
grâce à un retour rapide d'information
l Flexibilité, pour pouvoir être modifié si
nécessaire
31
Chapitre I : REVUE DE LA LITTÉRATURE
l Acceptabilité (évaluée par exemple par le
taux de participation, la qualité des données)
l Régularité (utiliser des définitions et
une méthodologie standardisées)
l Sensibilité, même si une méthode de
dépistage des cas avec une faible sensibilité peut être
valable pour observer les tendances tant que la sensibilité ne varie pas
au cours du temps et que les cas identifiés sont
représentatifs
l Spécificité, ce qui nécessite des
définitions précises et des enquêteurs
entraînés. La mesure dans laquelle le système satisfait
à ces critères varie d'un établissement à
l'autre.
La lutte contre les infections nosocomiales ; un
processus circulaire :
L'humain étant au centre de la problématique, il
est capital dans le cadre d'un programme de lutte contre les infections
nosocomiales, d'offrir au personnel de la santé un retour rapide de
l'information. Ces données sont à même de produire un
déclic et par conséquent, une amélioration des pratiques
médicales.
Étude de prévalence (transversale)
:
Dans une étude de prévalence, on identifie les
infections présentes chez tous les patients hospitalisés à
un moment donné (prévalence ponctuelle), dans l'ensemble de
l'hôpital ou dans certains services. En règle
générale, une équipe d'investigateurs spécialement
formés visite chaque patient de l'hôpital un jour donné,
examine les dossiers médicaux et infirmiers, interroge le personnel
soignant pour identifier les patients infectés et recueille des
données sur les facteurs de risque. L'étude produit une mesure du
taux de prévalence. Les taux de prévalence sont influencés
par la durée du séjour du patient (les patients infectés
restent plus longtemps à l'hôpital, ce qui conduit à
surestimer le risque d'acquisition de l'infection) et par la durée de
l'infection. Un autre problème réside dans le fait de savoir si
une infection est encore « active » le jour de l'étude.
Dans les petits hôpitaux ou les petites unités,
le nombre de patients peut être trop faible pour qu'il soit possible
d'obtenir des taux fiables ou d'effectuer des comparaisons statistiquement
significatives. Une étude de prévalence est simple, rapide et
relativement peu coûteuse. En procédant à l'échelle
de l'hôpital, on favorise la prise de conscience du problème des
infections nosocomiales parmi le personnel soignant et on augmente la
visibilité de l'équipe de lutte contre l'infection. Il est utile,
au début d'un programme de surveillance, d'évaluer les
problèmes qui se posent alors dans toutes les unités, pour tous
les types d'infections et chez tous les patients, avant de poursuivre avec un
programme de surveillance active davantage ciblé. Des enquêtes de
prévalence répétées peuvent être utiles pour
surveiller les tendances en comparant les taux mesurés dans un
hôpital ou une unité au cours du temps.
Rôle du microbiologiste dans la lutte contre les
infections nosocomiales :
La lutte contre les Infections nosocomiales consacre un
principe fondamental ; elle est multidimensionnelle et seule une collaboration
entre différentes instances (Comités de Luttes contre les
infections nosocomiales, cliniciens, aide soignants, blanchisseries, services
de bio-nettoyage, services d'épidémiologie et de médecine
préventive ...etc.) est à même d'endiguer ce
phénomène qui coûte cher à la collectivité et
aux hôpitaux en matière de souffrance humaine, et de pertes
matérielles.
Le microbiologiste est un maillon important et a une place
indéniable dans toute stratégie de lutte contre les Infections
Nosocomiales. Il a donc les latitudes suivantes :
- Préparer des directives sur le recueil, le transport, et
la manipulation appropriés des échantillons
32
Chapitre I : REVUE DE LA LITTÉRATURE
- Assurer que les pratiques observées au laboratoire
répondent aux normes.
- Assurer la sécurité des pratiques de
laboratoire afin d'éviter la transmission d'infections au
personnel.
- effectuer les tests de sensibilité aux antibiotiques
et produire des rapports sur les fréquences de la
résistance.
- surveiller la stérilisation du matériel
médical et désinfection de l'environnement hospitalier.
- communiquer en temps utile les résultats au
comité de lutte contre les infections nosocomiales et
responsables de l'hygiène de l'hôpital.
- Procéder au typage épidémiologique des
micro-organismes présents à l'hôpital. [4]
33
Chapitre I : REVUE DE LA LITTÉRATURE I.7. Aspects
réglementaires :
Une batterie de textes réglementaires régissent
tout ce qui a attrait à la lutte contre les infections nosocomiales dont
le texte fondamental est l'ARRETE N°64 MSP DU 17/11/1998 PORTANT CREATION
D'UN COMITE DE LUTTE CONTRE LES INFECTIONS NOSOCOMIALES AU NIVEAU DES
ETABLISSEMENTS DE SANTE.

Figure 2 - ARRÊTÉ N°64 MSP DU 17/11/1998
PORTANT CREATION D'UN COMITE DE LUTTE CONTRE LES INFECTIONS NOSOCOMIALES AU
NIVEAU DES ETABLISSEMENTS DE SANTE.
- 01/12/1982 : création de commissions d'hygiène
au sein des établissements de santé suite à
l'arrêté N° 167.
- 04/11/1985 : Création d'un Service
d'Épidémiologie et de Médecine Préventive au sein
de chaque Secteur Sanitaire par arrêté n°00115. Il a pour
tâche notamment : la collecte, le traitement et la diffusion de
l'ensemble des informations sanitaires hospitalières et extra
hospitalières ; la surveillance et la lutte contre les maladies
transmissibles et les maladies non transmissibles les plus
préoccupantes, ainsi que le contrôle des normes d'hygiène
du milieu. Toutes ces activités devant se faire en collaboration avec
les Bureaux d'Hygiène Communale.
- Il y a eu ensuite le décret N°97-467 du 02
décembre 1997, fixant les règles de création,
d'organisation et de fonctionnement des centres hospitalo-universitaires, qui a
pour mission d'assurer les activités de diagnostic, de soins
d'hospitalisation et des urgences médico-
34
Chapitre I : REVUE DE LA LITTÉRATURE
chirurgicales de prévention, ainsi que toute
activité concourant à la protection et à la promotion de
la santé de la population.
- Au mois de novembre de l'année 1998, tous les
établissements de santé ont été destinataire d'une
instruction ministérielle portant création d'un comité de
lutte contre les infections nosocomiales (C.L.I.N) au niveau de chaque
structure sanitaire, suivant l'arrêté N° 64 du 07 Novembre
1998. En 2001, la loi N° 2001-19 du 12 décembre 2001 a
été promulguée, ayant pour objet la gestion, le
contrôle et élimination des déchets, et de fixer les
modalités de gestion, de contrôle et de traitement des
déchets, qui reposent sur les principes suivants : La prévention,
la réduction de la production et de la nocivité des
déchets à la source. [14]
En France, la loi Kouchner du 4 mars 2002 et la loi About,
conformément aux articles L.1142-1 et L.1142-1-1 du Code de la
Santé Publique Française, ouvrent droit à une
indemnisation pour toute personne qui arrive à établir le lien
entre un préjudice et une infection nosocomiale. [15]
Aspects réglementaires et directives nationales
:
Le « guide bleu », un guide complet traitant de
plusieurs aspects et rassemblant les recommandations nationales relatives
à l'hygiène de l'environnement dans les établissements de
santé publics et privés a été publié en
2015.
Ce guide complet, rédigé par un commité
d'experts Algériens, traite tous les aspects d'hygiène et de
prévention ( hygiène des mains , bio nettoyage des surfaces et du
sol , entretien des sanitaires , tenue du personnel , la lutte anti-vectorielle
, les déchets d'activités de soins , le nettoyage des
différents appareillages et instruments etc.) [29]
Chapitre II :
MATERIEL ET METHODES
«La chance ne sourit qu'aux esprits
bien
préparés »
Louis Pasteur
37
Chapitre II : MATERIEL ET METHODES
II.1. Matériel et méthodes :
Cette étude a consisté en une surveillance
active moyennant un recueil de données et l'observation en temps
réel de 91 patients, âgés de 1 jour à 15 ans avec
une moyenne d'âge de 16 mois, hospitalisés dans le service de
Pédiatrie du CHU Béni Messous.
Il s'agit d'une surveillance des infections nosocomiales en
pédiatrie discontinue avec trois phases de surveillance, d'une semaine
chacune.
Cet type de surveillance est une approche recommandée
par le Guide Pratique de Prévention des infections nosocomiales de L'OMS
2ème édition publié en 2008 qui cite
l'intérêt d'avoir une série d'enquêtes
répétitives afin de déceler les tendances par comparaison
entre les différents épisodes , dans le but de faire prendre
conscience de la problématique des infections associées aux soins
ainsi que de suggérer des mesures correctives au fur et à mesure
et les implémenter.
Les critères d'inclusion :
Tous les enfants hospitalisés dans les trois
unités concernés ; n'entrent dans l'étude que les patients
ayant séjourné à l'hôpital pour une période
dépassant les 48 heures.
Les critères de non inclusion :
-Les patients opérés en Chirurgie Infantile
(Infections du site opératoire), étant donné la
difficulté de suivre ces patients en dehors de l'hôpital pour les
Infections Associées aux Soins. Ce type d'infections est pris en charge
par un travail régulier du service d'épidémiologie du CHU
et les patients sont hospitalisés dans un service dédié
(CCI).
-Les enfants hospitalisés pour un séjour moindre
que 48h.
-Les patients admis aux urgences (non hospitalisés par la
suite).
II.1.1. Matériel :
Matériel biologique :
Patients pédiatriques âgés de 1 jour à
15 ans, hospitalisés dans différentes unités du service
de
pédiatrie du CHU de Béni Messous.
Escherichia coli ATCC®
25922
Staphylococcus aureus
ATCC® 25923
Pseudomonas aeruginosa
ATCC® 27853
Matériel non biologiques :
-Le formulaire de recueil de données (annexes).
-Tout a été mis à notre disposition au
niveau du laboratoire central de CHU, unité de microbiologie, que cela
soit le matériel pour l'identification (pipettes, paillasses, milieux de
culture, galeries d'identification, réactifs, disques d'antibiotiques)
que le matériel de prélèvement (écouvillons,
flacons d'hémoculture pédiatriques Bactec plus pédiatrie
et Bactec mycosis, seringues, matériel d'asepsie). Les moyens de
protection individuelle ont été utilisés afin
d'éviter d'être un vecteur de contamination ou de se
contaminer.
Sur le plan analyse de données, l'analyse a
été faite sur LibreOffice Calc 2020 pour
l'épidémiologie descriptive, et sur le logiciel EPIDATA 3,02 pour
une éventuelle analyse des causalités
(épidémiologie étiologique).
Chapitre II : MATERIEL ET METHODES
II.1.2. Méthodes :
II.1.2.1. Recueil de données :
Un code de confidentialité a été
assigné à chaque patient, la donnée était
collectée en temps réel moyennant un formulaire
standardisé (voir annexes) et contenant toutes les informations
nécessaires et potentiellement exploitables.
Les sources de données sont :
-L'observation en temps réel au lit du patient
-La revue des dossiers des patients
-Les fiches de soins au lit du patient
-Les résultats du laboratoire Central du CHU
(Microbiologie, Parasitologie et Mycologie), ainsi que
les résultats de la biochimie et de l'hémobiologie
(Laboratoire mère et enfant).
-Discussion des cas avec les cliniciens durant les
différents rapports de garde, visites et colloques de
l'équipe médicale.
-Validation des données par une équipe du service
d'épidémiologie du CHU.
La donnée est par la suite recoupée entre toutes
ces sources.
Aussi, pour la validité de la donnée, la
délibération finale se faisait à posteriori avec un
expert-métier
et nous n'avons pas retrouvé de dissonances majeures entre
la donnée collectée, la délibération initiale
et finale (Valeur prédictive positive favorable).
II.1.2.2. Description des lieux de
l'étude
L'étude se passe au niveau du service de
pédiatrie du CHU ISSAD HASSANI situé sur la commune de Beni
Messous dans la wilaya d'Alger. Le CHU a été construit entre 1948
et 1950 comme étant hôpital spécialisé pour les
tuberculeux, aujourd'hui il est l'un des hôpitaux les plus important du
pays et il compte une trentaine de services spécialisés.

38
Figure 3 - CHU Béni Messous
39
Chapitre II : MATERIEL ET METHODES

Figure 4 - Plan du service de pédiatrie du CHU Beni
Messous Un état des lieux descriptif est établi avant le
début des trois enquêtes.
Pédiatrie B / L'unité de
cancéreux au niveau de la salle Mussy
A l'entrée on trouve un couloir qui contient le bureau
du coordinateur, un petit espace où se trouvent les bureaux des
résidents, et une porte qui mène vers les chambres
d'hospitalisation.
En franchissant cette porte on trouve un petit hall avec :
A droite, un espace ouvert composé de 4 boxs
d'hospitalisation pour les malades, d'une superficie de 20m2, ces
boxs sont séparés par des murs à mi-hauteur, chaque box
contient 4 lits pour les mamans et 4 berceaux, devant chaque lit de maman se
trouvent de petites tables où sont déposés : les
ustensiles, la nourriture, les médicaments. (Les gardes malades se
transmettent denrées alimentaires et objets en permanence, il y'a un
flux permanent entre les lits).
Ces boxs sont destinés pour tous les malades du service
Mussy quel que soit leur pathologie.
Au bout de cet espace, la salle de soin où se font tous
les gestes médicaux et paramédicaux pour les
malades, d'une superficie de 25m2 avec :
-Une table d'examen vétuste.
-Un placard ou sont stockés les médicaments.
- Une table chauffante pour nourrissons.
- Support et conteneur pour DASRI.
A droite de l'espace d'hospitalisation, se trouve
La douche avec trois cabines dont l'une est fermée,
trois éviers qui sont visiblement sales, dont l'un est bouché.
On retrouve aussi une machine à laver et une
chaudière.
40
Chapitre II : MATERIEL ET METHODES
Les sanitaires au nombre de 3 (2 siège turques et 1
siège anglais) l'eau est présente :
-Absence de postes de lavage, et le sol est visiblement sali
par les déchets, il n'y a pas de sac ni de support poubelle.
-Présence d'infiltrats d'eau avec des moisissures au
plafond.
-La propreté du sol est mauvaise ainsi que celle des
murs et des surfaces, la poubelle est parterre (pas de support pour poubelle),
pas de distributeur de savon ni d'essuies mains.
En face : se trouve un grand espace qui sert d'un
côté pour le dépôt du matériel non utile et de
l'autre côté se trouve, un office, chambre des infirmiers et un
endroit où mangent les parents et les agents d'entretien.
Pédiatrie A / L'USI et la
néonatologie :
Le service de réanimation pédiatrique se trouve
au niveau de la pédiatrie « A ». L'entrée comprend un
petit hall qui dessert :
A droite, le bureau de la surveillante médicale
Une salle dédiée à la formation des
mamans pour l'allaitement maternel, dotée d'un poste de lavage des
mains.
L'entrée est commune pour la réanimation et la
néonatologie.
L'unité de réanimation est composée d'un
hall doté d'un poste de lavage des mains conforme et un espace de repos
pour le personnel paramédical. La salle d'hospitalisation contient 4
lits et une chambre d'isolement à 1 lit, elle est dotée d'un
poste de lavage des mains conforme et un évier avec paillasse.
L'unité dispose d'une fenêtre qui est ouverte en
permanence donnant sur l'extérieur du service. Un bureau situé
devant la chambre d'isolement aménagé en espace de travail
Les portes manteaux servent à disposer les sur-blouses
à usage unique (qui sont sur-utilisées et parfois non
disponibles. Des manteaux occupent donc ce support).
-L'unité de néonatologie :
On y retrouve 14 couveuses opérationnelles.
Une chambre dédiée au lavage et désinfection
du matériel médical comportant un évier avec une
palliasse. (Cette chambre sert souvent à la
désinfection de matériel médical venu de la
pédiatrie B
dont par exemple les VNI de type CPAPs)
Une chambre de stockage des couveuses en instance de nettoyage
Deux box avec deux couveuses chacun
Une chambre qui fait office d'un nursing avec 6 couveuses
Bureau des médecins
Un box de photothérapie
Deux box avec quatre couveuses chacun
Une Chambre qui contient un groupe électrogène et
un appareil de radiographie.
Tous les box de l'unité de néonatologie sont
dotés d'un poste de lavage des mains équipé d'un
distributeur de savon. Nous avons constaté que les distributeurs sont
remplis de façon aléatoire et que leur alimentation est
sporadique. Nous avons aussi noté l'absence de distributeur d'essuie
main à usage unique et une désuétude du robinet (manivelle
de distribution d'eau avec le pied mais qui reste mal calibrée)
En général, nous avons noté une notion de
flux entre les deux unités, surtout durant les gardes où le
personnel dédié est distribué entre les deux services.
41
Chapitre II : MATERIEL ET METHODES
II.1.2.3. Le déroulement de la surveillance
:
Episode numéro 1/ La pré-enquête
:
La pré-enquête s'est étalée sur la
période du 14 au 21 Janvier 2020, en ayant comme
spécificité d'avoir, dans la mesure du possible, des «
cliniciens enquêteurs ».
Notre idée a été d'amener le clinicien
à intégrer de manière continue la donnée de
l'aspect nosocomial d'infections contractées par leurs patients et donc
à être plus vigilants quant à ce problème
Ainsi, ce biais épidémiologique a
été exploité à des fins de sensibilisation mais
rattrapé par un second formulaire afin de recouper les
données.
Des indicateurs comme la prévalence journalière,
la nature des germes isolés, la problématique de flux
inter-unités nous ont permis d'aller, toujours plus loin, dans notre
démarche d'avoir des mesures correctives « evidence-based
».
Épisode de surveillance numéro 2 : Du
10/02 au 17/02/2020
Nous avons pu observer, suite au travail effectué en
amont, que les Infections nosocomiales ont été à l'ordre
du jour et dans l'esprit des collègues cliniciens. Une certaine
attention était portée à cette problématique et
nous avions des opportunités pour intervenir régulièrement
durant les rapports de garde.
Un courrier officiel a été rédigé
par professeur chef de service de la pédiatre B pour le service
d'épidémiologie. Un enquêteur de l'équipe
d'épidémiologie a été utile dans la mesure
où cette dernière a été menée de
manière collaborative. Nous avons donc pu recouper notre donnée
après avoir constitué des équipes.
L'Unité de Soins Intensifs a
bénéficié d'un bio nettoyage durant deux jours (Le 13 et
le 14 Février 2020).
A la fin de cet épisode de surveillance, les
responsables de la pédiatrie décident du déplacement de
l'unité Mussy, qui sera déplacée à l'étage
après un aménagement accéléré.
Épisode de surveillance numéro 3 : Du
14/03 au 21/03/2020
Un contexte exceptionnel, la pandémie du
Coronavirus est au centre de toutes les préoccupations au
niveau planétaire.
Les précautions standards, les mesures barrières
sont renforcées à tous les niveaux.
Dans un contexte de ruée sans précèdent
vers les solutions et les gels hydro-alcoolique, nous avons distribué
une quantité de 50 litres à tous les praticiens de la
pédiatrie et avons observé une utilisation conséquente et
régulière de cette dernière, dans un contexte de peur du
virus émergent.
Aussi, le comportement, le flux, et l'attitude des praticiens a
changé de manière significative.
42
Chapitre II : MATERIEL ET METHODES
II.1.2.4. Logigrammes de prise en charge des
prélèvements au
laboratoire de microbiologie :
*Prélèvements profonds :

Figure 5 - Logigramme de prise en charge des
prélèvements profonds au laboratoire de microbiologie.
43
Chapitre II : MATERIEL ET METHODES
*Hémocultures :

Figure 6 - Logigramme de prise en charge des
hémocultures au laboratoire de
microbiologie.
44
Chapitre II : MATERIEL ET METHODES *ECB des urines
:


Figure 7 - Logigramme de prise en charge des
prélèvements urinaires au laboratoire de
microbiologie.
Chapitre II : MATERIEL ET METHODES
*Prélèvements superficiels :



45
Figure 8 - Logigramme de prise en charge des
prélèvements superficiels au laboratoire
de microbiologie.
46
Chapitre II : MATERIEL ET METHODES
Identification des levures :
1. A partir d'un bouillon, ou d'un prélèvement
réaliser un examen direct par état frais Tableau 3 - Levures
dans un examen direct à l'état frais
|
Présence de levures avec
bourgeons
|
Présence d'arthrospores
|
Présence de capsules à l'état
frais +
encre de chine
|
|
|
|
|
|
|
|
|
|
|
Ex : Saccharomyces, Candida
|
Ex : Geotrichum
|
Ex : Cryptococcus
|
2. Ensemencer un milieu Sabouraud + chloramphénicol
incuber 24 à 48 h à 30°C
3. Identification
Cas 1 : si colonies blanches et crémeuses, et
présence de levures avec bourgeons acapsulées réaliser un
des tests suivant pour rechercher Candida albicans :
? Test de chlamydosporulation : Technique :
milieu PCB ou RAT + goutte ou stries avec suspension + lamelle 24
à 48 h à 30°C - Lecture : On recherche au
microscope les pseudomycélium spécifiques du genre Candida
et les chlamydospores spécifiques de l'espèce Candida
albicans.
Tableau 4 - Bourgeonnement caractéristique des levures
du genre Candida

Pseudomycélium ? genre Candida
Chlamydospore ? Candida albicans
? Test de Blastèse : Technique : 1
colonie dans 0,5 mL de milieu de blastèse - 3 h à 37°C
Lecture : réalisation d'un état frais et
recherche de tubes germinatifs spécifiques de Candida
albicans.
Tableau 5- Candida albicans test de blastèse
Tubes germinatifs ? Candida albicans

Cas 2 : pas d'aspect caractéristique ou Test de
chlamydosporulation ou de blastèse
négatifs : ensemencer une galerie d'identification : api
20C AUX ou Auxacolor.
Chapitre III :
RESULTATS ET DISCUSSION
Chapitre III : RESULTATS ET DISCUSSION III.1.
Résultats :
III.1.1. Résultats par phase :
III.1.1.1. Épisode de surveillance numéro 1
:
Le nombre de patient hospitalisés durant cette
période inclus dans l'étude était de 30 patients. Ce qui
équivaut à un taux moyen d'occupation des lits de 92,94
%.
Nombre de patients ayant contracté une Infection
Nosocomiale : 12.
Sur l'ensemble des patients infectés, 8 étaient de
sexe féminin et 4 de sexe masculin.
? Prévalence moyenne des IN en Pédiatrie durant la
Phase I : 32,752 %
? Prévalence moyenne durant la Phase I dans l'unité
Mussy : 24,6175 %
? Prévalence moyenne durant la Phase I dans l'Unité
de Soins Intensifs : 56,665 %
? Prévalence moyenne des infections nosocomiales durant la
Phase I dans l'unité Nobecourt
Néonatologie : 16,97 %
Les infections sont distribuées comme suivant :
Répartition par type d'infection - épisode I -

8,33%
16,67%
8,33%
33,33%
33,33%
Bactériémies/ fongémies Pneumopathies
Infections de la peau et des tissus mous Méningites
Infections de la sphère ORL
48
Figure 9 - Répartition selon le type
d'infection durant la phase I.
Chapitre III : RESULTATS ET DISCUSSION
Les micro-organismes isolés durant la phase I sont
distribués comme suit :
Micro-organismes isolés durant la phase I
23,07%
15,38%
7,69%
7,69%
15,38%
7,69%
15,38%
7,69%
Staphylococcus aureus Enterobacter cloacae Enterobacter
aerogenes Escherichia coli
Proteus mirabilis
Candida albicans
Pseudomonas aeruginosa Klebsiella pneumoniae
49
Figure 10 - Répartition selon le type de
micro-organismes isolés durant la phase I.
13 micro-organismes sont isolés, 10 bactéries et 3
candida spp.
BMR isolées durant la phase I : 3
E-BLSE (2 Klebsiella pneumoniae BLSE, 1 Enterobacter cloacae
BLSE).
III.1.1.2. Épisode de surveillance numéro 2
:
Le nombre de patients hospitalisés durant cette
période : 32, ce qui représente un taux d'occupation des lits de
: 91,81 %.
Le nombre de patients infectés : 12.
Dont 8 sont de sexe féminin et 4 de sexe masculin.
? Prévalence moyenne en pédiatrie durant la
phase II : 27,64 % ? Prévalence moyenne Unité
Mussy : 29,04 %,
? Prévalence moyenne unité Nobecourt (USI) :
41,66 %
? Prévalence moyenne unité Nobecourt
Néonatologie : 12,22 %
Chapitre III : RESULTATS ET DISCUSSION
Les infections sont distribuées comme suivant :
Repartition par type d'infection - épisode II -
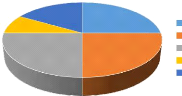
8,33%
25%
16,66%
25%
25%
Infections urinaires
Infections de la peau et des tissus mous Pneumopathies
Infections gastro-intestinales Bactériémies/
fongémies
Figure 11 - Répartition selon le type d'infection
durant la phase II.
Les micro-organismes isolés durant la phase II sont
distribués comme suit :
Micro-organismes isolés durant la phase II
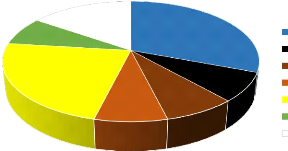
23,07%
7,69%
15,38%
7,69%
7,69%
30,76%
7,69%
Pseudomonas aeruginosa Enterobacter cloacae candida
albicans
candida parapsilosis Klebsiella pneumoniae Salmonella mineure
O:7 Escherichia coli
50
Figure 12 - Répartition selon le type de
micro-organismes isolés durant la phase II.
Nombre de microorganismes isolés : 13, dont 11
bactéries et 2 levures. BMR / BHRe : 1 E-BLSE, 1 SARM,
1 ERV.
Chapitre III : RESULTATS ET DISCUSSION
III.1.1.3. Épisode de surveillance numéro 3
:
Nombre de patients hospitalisés : 29, représentant
un taux moyen d'occupation des lits de 90,2 %. Nombre de
patients infectés : 2 de sexe masculin et 2 de sexe féminin.
Prévalence moyenne phase III : 19,76 %
Prévalence moyenne Mussy phase III : 15,68
%
Prévalence moyenne Nobecourt (USI) phase III : 33
% Prévalence moyenne Nobecourt Néonatologie :
10,60
Les infections sont distribuées comme suivant :
Répartition par type d'infection - épisode III
-

25%
25%
50%
Pneumopathies
Infections de la peau et des tissus mous
Bactériémies
Figure 13 - Répartition selon le type d'infections
durant la phase III.
Les micro-organismes isolés durant la phase III sont
distribués comme suit :
Micro-organismes isolés durant la phase III
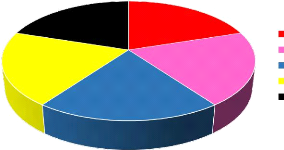
20%
20%
20%
20%
20%
Staphylococcus aureus Enterococcus faecium Pseudomonas
aeruginosa Klebsiella pneumoniae Enterobacter cloacae
51
Figure 14 - Répartition selon le type de
micro-organismes isolés durant la phase III.
Nombre de micro-organismes isolés : 5 bactéries.
BMR isolées : 2 E-BLSE (1 Kp BLSE, 1
Enterobacter cloacae BLSE).
52
Chapitre III : RESULTATS ET DISCUSSION
III.1.2. La variation de la prévalence des
infections nosocomiales
durant l'étude
La prévalence moyenne des IN durant l'étude
était de : 26,71 %, elle a évolué de la manière
suivante durant les trois épisodes de surveillance et dans chacune des
unités :
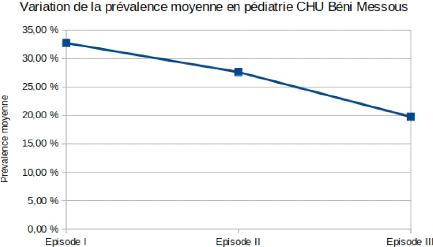
Figure 15- Variation de la prévalence moyenne en
pédiatrie durant les trois
enquêtes.

Figure 16 - Variation de la prévalence moyenne
à l'unité Mussy durant les trois
enquêtes.
53
Chapitre III : RESULTATS ET DISCUSSION
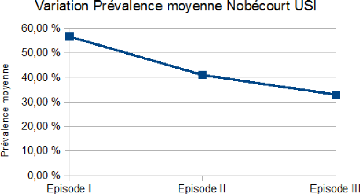
Figure 17 - Variation de la prévalence moyenne
à l'unité de soins intensifs (Nobecourt) durant les
trois enquêtes.
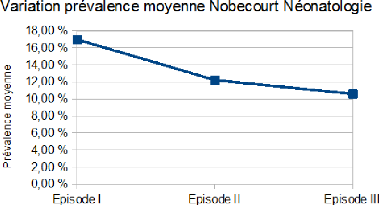
Figure 18 - Variation de la prévalence moyenne
à l'unité de Néonatologie (Nobecourt)
durant les trois
enquêtes.
54
Chapitre III : RESULTATS ET DISCUSSION
III.1.3. Résultats des trois épisodes de
surveillance des IN :
- Le nombre total de patients observés était de :
91 patients (dont 51,60% de sexe féminin et 48,40% de sexe masculin).
- L'âge des patients suivis varie de 1 jour à 5194
jours (15 ans).
- L'âge moyen des patients suivis est de 499 jours (16
mois).
- Le nombre de patients infectés : 23 (dont 38,69% de sexe
masculin et 61,31% de sexe féminin). Ce qui donne un ratio
d'infectés de 0,25 - 1 patient infecté pour 3 non
infectés.
- Le nombre total d'épisodes infectieux : 28.
- 5 patients (21,73 % des patients infectés) ont
contracté plus d'une seule infection durant l'étude (2
épisodes infectieux).
- l'âge moyen des patients infectés est de 426 jours
(14 mois).
- l'âge médian des patients infectés est de
135 jours.
- 61,33 % des patients infectés sont de sexe
féminin.
Distribution des patients suivis selon le motif
d'hospitalisation : Tableau 6 - Motifs d'hospitalisation des
patients suivis.
|
Motif d'hospitalisation
|
Nombre de patients
|
|
Détresse respiratoire
|
19 (6 ont été infectés)
|
|
Bronchiolite aiguë
|
12 (4 ont été infectés)
|
|
Prématurité (élevage)
|
10 (1 a été infecté)
|
|
Ictère(s)
|
8
|
|
Leucémie aiguë Lymphoblastique
|
6 (dont 3 ont été infectés)
|
|
Cardiopathies
|
6
|
|
Diabète
|
4
|
|
Méningites
|
4 (dont 1 a été infecté)
|
|
Néphropathies
|
3 (dont 1 a été infecté)
|
|
Neuroblastome
|
3 (dont 1 a été infecté)
|
|
Lymphomes non-hodgkiniens
|
3
|
|
Leucémie aiguë Myéloïde
|
3 (dont 2 ont été infectés)
|
|
Déficit immunitaire combiné
|
1
|
|
Maladie de Crohn
|
1
|
|
Asphyxie natale
|
1
|
|
syndrome de Guillain Barré
|
1
|
|
Adénome
|
1
|
|
Asthme
|
1
|
|
Mucopolysaccharidose
|
1 (dont 1 a été infecté)
|
|
Spina bifida
|
1 (dont 1 a été infecté)
|
|
Volvulus mésentérique
|
1 (dont 1 a été infecté)
|
|
Hépatoblastome
|
1 (dont 1 a été infecté)
|
|
Total : 91 patients
|

Chapitre III : RESULTATS ET DISCUSSION
Distribution des patients infectés par tranche
d'âge :
Figure 19 - Distribution des patients infectés selon
la tranche d'âge. 69,56 % des patients infectés
ont moins d'une année.
Répartition selon le nombre d'infections
contractées par le même malade :

55
Figure 20 - Répartition selon le nombre d'infections
contractées par le même malade
Chapitre III : RESULTATS ET DISCUSSION
Répartition par type d'infection (durant
l'étude)
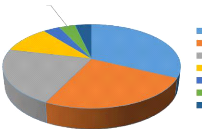
3,57%
3,57%
3,57%
10,70%
32,24%
21,42%
25,00%
Pneumopathies
Bactériémies/ fongémies
Infections de la peau et des tissus mous
infections urinaires
Infections de la sphère ORL
Infections gastro-intestinales
Méningites
Figure 21- Répartition selon le type de
micro-organismes isolés durant
l'étude.
Répartition des germes identifiés par famille
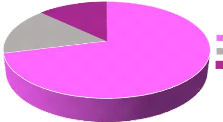
16,10%
12,91%
70,98%
Bacilles Gram négatifs Champignons/ lévures Cocci
Gram positifs
56
Figure 22 - Répartition des micro-organismes
isolés durant l'étude par familles.
57
Chapitre III : RESULTATS ET DISCUSSION
Isolats durant toute l'étude - selon le
micro-organisme -
Enterobacter aerogenes
Enterococcus faecium
Proteus mirabilis
Salmonella mineure O:7
candida parapsilosis
Staphylococcus aureus
Escherichia coli
Enterobacter cloacae
candida albicans
Klebsiella pneumoniae
Pseudomonas aeruginosa
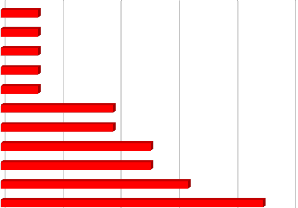
3,23%
3,23%
3,23%
3,23%
3,23%
9,67%
9,67%
12,90%
12,90%
16,12%
22,58%
0,00% 5,00% 10,00% 15,00% 20,00% 25,00%
Figure 23 - Micro-organismes isolés durant
l'étude par espèce.
Répartition des micro-organismes nosocomiaux :
31
Dont 5 Candida spp (4 Candida albicans + 1
Candida parapsilosis)
8 BMR ont été retrouvées :
- 6 E-BLSE - 1 SARM
- 1 ERV (BHRe)
58
Chapitre III : RESULTATS ET DISCUSSION
Tableau récapitulatif : Patients infectés,
type d'infection, micro-organismes et motifs d'hospitalisation :
Tableau 7 - Tableau récapitulatif.
|
Patient
|
IN contractée(s)
|
Micro-organismes
|
Motif d'hospitalisation/ comorbidités
|
|
Patient 1
|
Infection de la peau et des tissus mous
Infection de la peau et des tissus mous
|
E.coli
Candida albicans
|
Leucémie aiguë Lymphoide
|
|
Patient 2
|
Bactériémie
|
Enterobacter aerogenes
|
Mucopolysaccharidose
|
|
Patient 3
|
PAVM
|
Klebsiella pneumoniae BLSE
|
Bronchiolite aiguë
|
|
Patient 4
|
PAVM
|
Enterobacter cloacae BLSE
|
Bronchiolite aigue
|
|
Patient 5
|
Bactériémie
|
Enterobacter cloacae
|
Méningite virale
|
|
Patient 6
|
Méningite nosocomiale
|
Staphylococcus aureus
|
Spina Bifida
|
|
Patient 7
|
Bactériémie
|
Staphylococcus aureus
|
DR
|
|
Patient 8
|
PAVM
|
Pseudomonas aeruginosa
|
DR
|
|
Patient 9
|
PAVM
|
Pseudomonas aeruginosa + Enterobacter
cloacae
|
Bronchiolite aiguë sévère
|
|
Patient 10
|
Infection de la peau et des tissus mous
Bactériémie
|
Klebsiella pneumoniae BLSE
Klebsiella pneumoniae BLSE
|
Leucémie aiguë Lymphoblastique BII
|
|
Patient 11
|
Infection de la sphère ORL
Candididémie
|
Proteus mirabilis + Candida albicans
Candida parapsilosis
|
Leucémie aiguë Lymphoblastique
|
|
Patient 12
|
PAVM
|
Klebsiella pneumoniae BLSE
|
DR
|
|
patient 13
|
PAVM
|
Pseudomonas aeruginosa
|
Bronchiolite aiguë
|
|
Patient 14
|
Infection urinaire
Infection de la peau et des tissus mous
|
E.coli
Enterobacter cloacae BLSE
|
Neuroblastome
|
|
Patient 15
|
Bactériémie
|
Enterococcus faecium résistant à la
Vancomycine
|
Leucémie aiguë Myéloide
|
59
Chapitre III : RESULTATS ET DISCUSSION
|
Patient 16
|
PAVM
|
Pseudomonas aeruginosa
|
Hépatoblastome
|
|
Patient 17
|
Infection urinaire
Infection digestive
|
Pseudomonas aeruginosa
Salmonella O7
|
Néphropathie
|
|
Patient 18
|
PAVM
|
Pseudomonas aeruginosa
|
DR
|
|
Patient 19
|
PAVM
|
Staphylococcus aureus Méthicilline
résistant
|
DR
|
|
Patient 20
|
Infection urinaire
|
E.coli
|
Prématurité sévère
(élevage)
|
|
Patient 21
|
Infection de la peau et des tissus mous
|
Klebsiella pneumoniae + Candida albicans
|
Volvulus mésentérique
|
|
Patient 22
|
Infection de la peau et des tissus mous
|
Candida albicans
|
Leucémie aiguë Myéloide
|
|
Patient 23
|
Bactériémie
|
Pseudomonas aeruginosa
|
DR
|
Devenir des patients :
- Sur l'ensemble des patients suivis, 3 sont
décédés en concomitance avec un épisode infectieux
sévère.*
Liste des patients décédés :
*Patiente décédée 1 : de sexe
féminin, âgée de 104 jours (3 mois et demi), intubée
ventilée, admise pour bronchiolite aiguë à VRS
compliquée en Pneumopathie nosocomiale sur Ventilation Mécanique
à Klebsiella pneumoniae BLSE.
*Patient décédé 2 :
prématuré, de sexe masculin, âgé de 5 jours, admis
pour détresse respiratoire scorée à 5 selon
l'échelle de Silverman, sous ventilation mécanique - Sepsis
à Staphylococcus aureus
*Patiente décédée 3 : de sexe
féminin, âgée de 1005 jours (2 ans et 9 mois), en aplasie
fébrile au moment du décès, hospitalisée pour une
Leucémie Aiguë Lymphoblastique II - Avait contracté une
Candidose invasive à Candida Parapsilosis active au moment du
décès et retrouvée dans une hémoculture.
Le nombre de patients décédés
représente 13,04 % des patients infectés.
60
Chapitre III : RESULTATS ET DISCUSSION
Données subsidiaires :

Figure 24 - Consommation en SHA du service de
Pédiatrie durant les mois de Janvier, Février
et Mars selon la
pharmacie du CHU.
Tendances de l'épidémiologie étiologique
:
Dans cette partie on abordera de manière brève
quelques observations pouvant relier des
pathologies avec, différents germes isolés, et les
différentes expositions et pathologies initiales des patients.
Pneumopathies nosocomiales et Ventilation mécanique :
-100 % des patients ayant
développé une pneumopathie nosocomiale étaient sous
ventilation mécanique.
- 57 % d'entre eux étaient intubés
(Ventilation Invasive)
- 43 % étaient sous Ventilation Non
Invasive (CPAP)
50 % des PAVM sont causées par le
Pseudomonas aeruginosa
50 % des PAVM sont causées par les
bactéries du groupe KES (Klebsiella pneumoniae ++ et
Enterobacter cloacae)
- Notons que le Pseudomonas aeruginosa est
retrouvé dans près de 80 % des atteintes de
patients sous VNI (Cpap) ;
Il serait donc judicieux d'inspecter ces appareillages qui sont
fréquemment utilisés en pédiatrie. (Les protocoles de
nettoyage utilisés, le changement des filtres antibactériens, le
changement de la partie consommable).
61
Chapitre III : RESULTATS ET DISCUSSION III.2.
Commentaires et discussion : Commentaires :
Les résultats épidémiologiques
descriptifs rapportés aux contextes ayant jalonné les
différentes phases de l'étude montrent les tendances suivantes
:
Concernant la variation de la prévalence :
La prévalence moyenne des trois unités durant
l'étude était de 26,71 %, elle a évolué de
manière décroissante passant de 32,75 % au premier épisode
de la surveillance, à 27,64 % durant la deuxième phase, pour
finir sur 19,76 % durant le troisième épisode.
Dans le monde, les prévalences des IN en
pédiatrie varient de 2,4 % à plus de 15 %. Cette
prévalence pourrait aller jusqu'à près de 40 % pour les
infections virales des épidémies hivernales. [26]
L'unité ayant enregistré le plus grand taux de
prévalence est l'unité de soins intensifs où le taux de
prévalence a évolué chronologiquement de 56,66 % (Phase
I), en passant par 41,66 % (Phase II), puis 33 % en Phase III.
La prévalence a évolué de manière
décroissante dans les autres unités, excepté un pic
à l'unité Mussy durant l'épisode II.
- Nous retrouvons une tendance relative à la baisse
durant la phase II et qui pourrait vraisemblablement tirer son origine de
l'attention très accrue autour des infections nosocomiales qui
étaient à l'ordre du jour. Nous étions en effet
présents de manière régulière et avions des
latitudes pour faire de la sensibilisation (prise de parole durant les rapports
de garde, les visites, etc.)
- La tendance franche à la baisse durant la phase III
pourrait vraisemblablement tirer son origine du contexte général
de peur suscitée par l'émergence du COVID-19.
En effet, cette dernière a été
menée aux débuts de la crise et dans un contexte de prudence
extrême à tous les niveaux.
En effet, nous avons pu observer un changement notable des
comportements du personnel, une baisse considérable des flux inter et
intra-services (limitation drastique des visites, SAS d'entrée,
vigilance accrue du personnel par rapport aux différents visiteurs et
autres gardes malades), et la diminution de la densité en personnel.
Aussi, l'utilisation des solutions hydroalcooliques a
été considérable tout autant par le personnel de la
santé, les patients eux-mêmes et leurs corollaires.
Les équipements de protections individuelle
(sur-blouses, charlottes, sur-chaussures, gants, masques chirurgicaux) ont
été de plus en plus disponibles et nous avons observé une
rigueur sans précédent dans leur utilisation.
Bien que l'unité ayant enregistré les scores les
plus élevés en prévalence est l'unité de soins
intensifs, l'unité Mussy, qui accueille des patients d'oncologie a
enregistré des prévalences élevées.
L'état des lieux de cette unité montre une
notion de promiscuité et de surcharge (des box avec des lits très
peu espacés), un flux conséquent entre les lits et le transfert
d'objets, aliments, jouets (la présence excessive de jouets est
corrélée avec un plus grand risque d'IN, selon un article
publié dans The Lancet sur une enquête diligentée par Pr
Pitter) entre les gardes malades.
62
Chapitre III : RESULTATS ET DISCUSSION
Il serait peut être judicieux, dans les mesures
correctives, d'avoir une attention particulière à cette
unité qui contient des sujets très prédisposés,
atteints de pathologies cancéreuses et qui sont souvent en aplasies
iatrogènes dues aux chimiothérapies.
Discussion :
Sur l'ensemble des patients hospitalisés aux trois
unités de pédiatrie concernées par l'étude, 91 ont
répondu aux critères d'inclusion.
Une prédominance féminine est retrouvée dans
le panel avec 51,60 %.
L'âge des patients varie de 1 jour à 15 ans avec un
âge moyen de 16 mois.
Concernant les patients infectés :
Le nombre des patients infectés retrouvé est de
23, sur un total de 28 épisodes infectieux enregistrés (5
patients ayant contracté deux infections nosocomiales), ce qui donne un
ratio d'infectés de 0,25 (1 patient infecté pour 3 non
infectés soit 25 % d'infectés)
Ce ratio en pédiatrie varie grandement selon la zone
géographique allant de 1 % dans les pays du nord de l'Europe à
>40 % dans certaines régions d'Asie, Amérique du Sud et
Afrique. [21]
L'âge moyen des patients infectés est de 14 mois
et nous retrouvons 69,56 % des patients (16 patients sur 23) avec un âge
inférieur à 1 an.
Les pathologies cancéreuses, essentiellement des
leucémies, constituent la majorité des motifs d'hospitalisation
des patients infectés (7 patients sur 23), en deuxième position
nous retrouvons les Détresses respiratoires idiopathiques (6 patients
sur 23), suivies des bronchiolites aiguës (4 patients sur 23).
Ceci est dû au fait que l'étude intègre
une unité de cancérologie pédiatrique pour les pathologies
cancéreuses, et que l'un des motifs fréquents d'hospitalisation
en néonatologie est la détresse respiratoire due soit à la
grande prématurité ou la MMH.
Les bronchiolites sont souvent retrouvées en unités
de soins intensifs.
La pathologie cancéreuse est retrouvée comme
étant un facteur de risque d'IN dans la population pédiatrique,
une étude multicentrique prospective publiée en 2008 dans le
BioMed Central sur une population issue de 7 hôpitaux pédiatriques
en Suisse et en Allemagne conclue cela.
Concernant les types d'infections :
Deux types d'infections ont été les plus courantes
:
Les pneumopathies et les bactériémies qui
représentaient respectivement 32,24 % et 25 % des épisodes
infectieux, suivies des infections de la peau et des tissus mous avec 21,42
%
L'infection urinaire est retrouvée en 4ème position
représentant 10,71 % des cas.
Au Maroc, selon l'article Incidence des infections
bactériennes nosocomiales. Hôpital d'enfants Abderrahim Harouchi,
CHU Ibn Rochd, Casablanca, Maroc montrant les résultats d'étude
prospective aussi et dont le recrutement se rapproche de notre étude vu
qu'elle axe la surveillance à la fois une unité de soins
intensifs et une unité de néonatologie (Dans notre étude,
une unité de cancérologie fait aussi parti du panel) on retrouve
des résultats plus ou moins similaires
63
Chapitre III : RESULTATS ET DISCUSSION
Les infections pulmonaires sont aussi majoritaires et
concentrent à elles seules 40 % des infections (32,24 % dans notre
étude), et que les bactériémies / fongémies
représentent 31,4 % des IN contractées (25 % dans notre
étude).
En Europe, les Infections pulmonaires atteignent
jusqu'à 53 % des infections nosocomiales dans les unités de soins
intensifs et les bactériémies vont parfois jusqu'à
représenter 71 % des IN dans les unités de
néonatologie.
En Suisse, les bactériémies représentent
20 % des Infections nosocomiales en pédiatrie ( Pittet 2020).
Les infections de la peau et des tissus mous semblent
être une spécificité à notre étude et dans
aucune étude nous ne retrouvons des taux aussi élevés
(21,42 %).
Une étude prospective publiée en 2006
menée dans l'unité de réanimation néonatale et
pédiatrique de l'hôpital d'enfants de Tunis les
bactériémies sont retrouvées en première position
cumulant (68,2%) des infections suivies des pneumopathies (31,8 %). [22]
Un article intitulé Nosocomial Infections in Pediatric
Intensive Care Units, publié au Indian Journal of Pediatrics[23], cite
une étude Américaine faisant partie du la surveillance nationale
des infections nosocomiales aux USA (NNIS) et qui affirme qu'en unité de
soins intensifs pédiatrique, la tendance générale tend
vers la primauté des Bactériémies primaires avec 28 % des
infections suivies des Infections pulmonaires basses avec 21 % des infections
ensuite des Infections urinaires (15%)
Ce même article parle de résultats parfois
différents où c'est plutôt les infections pulmonaires qui
sont en pôle position, suivies après par les
bactériémies.
L'article soutient que cette tendance fait la
spécificité des IN en pédiatrie par rapport à ces
dernières chez l'adulte où ce sont plutôt les infections
urinaires qui sont les plus communes. [23]
En Espagne, en 2007 et sur un panel de 300 patients issus de 6
Unités de Soins Intensifs, sur les 17 épisodes d'infections
nosocomiales enregistrés, 7 patients ont contracté une
bactériémie et 4 une pneumopathie associée à la
ventilation mécanique. [24]
Une étude multicentrique conduite en Europe
publiée dans le Chicago journals ayant concerné 20 unités
dans 8 pays Européens avec 5 unités de soins intensifs, 7
unités de néonatologie, 8 unités de pédiatrie
générale et 2 unités d'hématologie / oncologie
retrouve aussi 36 % de bactériémies suivies des infections
pulmonaires avec 33 % des infections.
Concernant les micro-organismes isolés
:
Nous retrouvons majoritairement des Bacilles Gram
Négatifs dans 70,98 % des cas. L'étude Tunisienne retrouve un
taux similaire : 68 % de Bacilles Gram Négatifs.
En Turquie, on retrouve une prédominance des bacilles Gram
négatifs avec 79,8 %
64
Chapitre III : RESULTATS ET DISCUSSION
La prédominance des bacilles Gram positifs est
retrouvée dans les pays en voie de développement et en recul aux
pays développés où ce sont plutôt les Cocci Gram
positifs qui émergent (50,4 % en France selon Branger B - Arch
Pédiatr - 2005).
Dans nos résultats, le Pseudomonas aeruginosa
est loin devant avec 22,58 %, suivi de Klebsiella pneumoniae avec
16,13 % puis d' Enterobacter cloacae et Candida albicans avec
tous deux 12,90 %.
En France, chez l'enfant, les micro-organismes responsables de
ces infections sont principalement Staphylococcus epidermidis (20 %),
les entérobactéries (20 %), Staphylococcus aureus (19 %)
et Pseudomonas (10 %). [26]
En Turquie, les germes les plus fréquents sont
Klebsiella spp (28,7%), Pseudomonas aeruginosa (19,1 %),
E.coli (15,9%) et les SCN (9,6%). [27]
En Tunisie, selon une enquête nationale de
prévalence menée en 2005, on retrouve, le Pseudomonas
aeruginosa en première position avec 17,9 %, suivi de
l'Acinetobacter baumannii (12,8%), puis E.coli (10,3%).
Les candidoses sont élevées, cumulant elles seules
plus de 16,13 % des infections.
Cependant, il ne faut pas perdre de vue que 100 % des
Candida spp sont l'apanage de l'unité Mussy seulement.
L'état vétuste et la proximité avec des
travaux ayant lieu à l'étage supérieur (voir état
des lieux des services dans la partie matériel et méthodes)
pourrait être un facteur principal, du moins aggravant de ces
tendances.
Une corrélation est décrite entre l'augmentation
de la mortalité notamment par des agents fongiques dans des structures
de soins liées à des travaux, dans le document intitulé
:
« Infections nosocomiales chez les patients
d'établissements de santé liées aux travaux de
construction » publié en 2001 par la Division des infections
nosocomiales et professionnelles Canadienne.
Le Candida parapsilosis, retrouvé dans une
hémoculture d'une patiente décédé est
retrouvé dans la littérature comme levure nosocomiale par
excellence et qui est souvent retrouvée dans des fongémies
létales. Selon l'article, ce type d'infections sont en augmentation aux
Etats-Unis.
Dans l'étude multicentrique Européenne
publiée au Chicago Journals, les Candida représentent 9 % des
infections avec une fréquence plus élevée dans les
unités de soins intensifs.
L'article INPED burgard 2013 cite trois travaux aux
États-Unis sur les Candidémies nosocomiales relevant
l'augmentation des infections liées à C. albicans et
Candida parapsilosis chez l'enfant.
Ainsi Candida est le deuxième agent
pathogène isolé des hémocultures aux États- Unis et
une candidose sur deux est diagnostiquée chez l'enfant.
Cette augmentation chez l'enfant est liée à la
diffusion de C. parapsilosis en hématologie et
néonatalogie selon ces mêmes articles.
Nous avons retrouvé le C.parapsilosis dans une
candidémie qui a été létale pour la patiente. Les
autres Candida ont surtout causé plutôt des infections de
la peau et des tissus mous.
65
Chapitre III : RESULTATS ET DISCUSSION
50 % des Pneumopathies sont causées par le
Pseudomonas aeruginosa, un taux similaire est retrouvé dans
l'étude Européenne avec le pseudo ayant causé 44 % des
pneumopathies nosocomiales.
Concernant les Bactéries
Multi-résistantes :
Nous avons retrouvé 8 BMR parmi 26 isolats
bactériens ce qui représente 30,76% des bactéries
isolées.
Ce chiffre semble élevé, mais différentes
études établissent une corrélation entre
nosocomialité et fréquences élevées en BMR.
Il serait judicieux de discuter une par une, le ratio BMR/ Non
BMR pour chaque espèce pour une meilleure comparaison avec la
littérature.
Nous avons donc :
-1/3 des Staphylococcus aureus isolés
étant des SARM.
L'enquête de prévalence en 2001 en France qui a
concerné les établissements pédiatriques retrouve un ratio
SARM/Non SARM très proche du notre (21,9 % contre 30 % dans nos
résultats).
Concernant les Entérobactéries productrices de
bêtalactamases à spectre élargi, nous retrouvons les KP
BLSE et les Enterobacter BLSE.
La majorité des Klebsiella pneumoniae
isolées (80%) sont multi-résistantes.
Dans l'étude menée en Tunisie en USI
pédiatrique, qui retrouve les Klebsiella pneumoniae en
pôle position, 85 % des Kp étaient multi-résistantes.
Selon une étude menée en 2009, la
prévalence des Kp BLSE en environnement hospitalier à l'est de
l'Algérie avoisinait les 60%.
La prévalence dépasserait même 80 % selon
une autre étude menée en 2012 à l'ouest de
l'Algérie. [25]
La littérature décrit une tendance à la
hausse des Klebsiella pneumoniae multirésistantes et ce dans
plusieurs zones géographiques.
Pour cette étude, nous déplorons
l'impossibilité de l'étendre sur une période plus
prolongée et de manière longitudinale pour des raisons objectives
(année d'internat), mais nous espérons que cette dernière
puisse être une amorce pour des études futures.
Les IN virales sont à la fois prédominants
(Branger 2013) et largement sous-estimées en particulier dans le cadre
des enquêtes de prévalence. [28]
Cette étude s'est concentrée pour des raisons
objectives sur les agents bactériens et mycosiques.
Comme perspective première, et sur un aspect purement
pratique, nous considérons que ce travail, bien que humble, pourrait
être un facteur déclenchant d'une prise de conscience.
66
Chapitre III : RESULTATS ET DISCUSSION
Sur l'aspect scientifique et académique, nous pensons
qu'un focus sur les infections les plus prévalantes serait
intéressant et que des études par exemple sur les
Bactéries Multi-Résistantes dans les Infections nosocomiales
pulmonaires ou les bactériémies pourrait donner, s'il est bien
conduit, avec un recrutement sur le long terme, des résultats
féconds en connaissance.
« Soulager souvent, guérir parfois,
écouter
toujours. »
Louis Pasteur
Conclusion
69
Conclusion
Les Infections Nosocomiales sont un véritable
problème de santé publique avec des impacts directs et indirects
et intangibles parfois sous-estimées et parfois mortels.
Les prévalences retrouvées ( prévalence
moyenne de 26,71 % ) au sein du service de pédiatrie sont
particulièrement élevées surtout dans l'Unité de
Soins Intensifs, pour des raisons évidentes de fragilité des
patients, de fréquence plus élevées en gestes invasifs et
dispositifs médicaux, et à priori par manque d'une
stratégie de lutte éprouvée, efficace et qui donnant des
retours d'information réguliers. L'idée qu'on a pu avoir de
l'écologie bactérienne du service, le nombre élevé
de Bactéries Multi résistantes (30,76 % des isolats
bactériens) est un élément critique et
méritant une attention particulière.
Documenter cette redondance des BMR est vital dans la prise de
conscience.
L'humain étant le barycentre dans cette
problématique, il est plus qu'urgent de miser sur une politique
d'information entreprenante et créative.
L'émergence du Covid-19 pourrait être un point
d'inflexion dans les pratiques au sein de l'hôpital, nous avons pu avoir
une expérience en temps réel où l'hygiène
était rigoureuse sans avoir à faire d'injonction ; le retour
d'information permet donc de faire prendre conscience qu'il est possible
d'éviter de la souffrance humaine, mais aussi d'économiser
indirectement les surcouts infligés par les IN. Il s'agit donc
d'entretenir la même attitude même en dehors de la crise.
Dans une conjecture économique difficile qui se
profile, il est grand temps d'optimiser les surcouts à tous les
niveaux.
En définitif, l'éradication de ce
phénomène repose sur :
- l'évaluation
- la formation
- la prise de conscience
- l'audit des moyens et des pratiques
- l'évaluation de la résistance aux antibiotiques
et un usage plus rationnel des anti-infectieux
Recommandations et mesures correctives
71
Recommandations et mesures correctives
La maîtrise des Infections Nosocomiales est un
défi majeur à relever par plusieurs maillons, que cela soit le
personnel médical et paramédical, le microbiologiste qui
représente un pivot dans la surveillance et les suggestions de mesures
correctives, ainsi que l'administration de l'hôpital qui se doit
d'être alerte par rapport à cet enjeu de grande importance.
Sur le plan pratique :
- Une lutte efficace commence par une surveillance
efficace :
Que cela soit par des surveillances continues ou discontinues,
d'ordre général ou axées sur une priorité (Site
infectieux dont la fréquence et la gravité sont
inquiétantes, Unités particulièrement contaminées,
surchargées ou insalubres), il est d'une importance capitale de cerner
de plus près ce phénomène.
À la lumière de nos résultats, nous
recommandons une attention particulière par rapport aux sites
pulmonaires, bactériémies et infections de la peau et des tissus
mous.
- Des audits réguliers pour déterminer le
degré d'asepsie et les protocoles de désinfection
utilisés
- Des enquêtes moyennant des prélèvements
sur les respirateurs, appareils de Ventilation Mécanique
(humidificateurs des Cpap par exemple)
- Des audits sur le matériel médical utilisé
(Cathéters, sparadraps, compresses stériles etc.)
- Des audits sur l'usage des antibiotiques et la
fréquence et nature des Bactéries Multirésistantes au sein
de l'hôpital
-Précautions standards et précautions
spécifiques :
Les mesures de précaution standards sont censées
être la norme et une routine pour tout le personnel soignant,
Aussi, il est judicieux, à la lumière de travaux
réalisés au HUG par exemple, d'instaurer la règle
Un praticien de la santé = Un flacon de SHA
à disposition en permanence
Les précautions spécifiques dépendent du
mode de transmission des micro-organismes
* Précautions en cas de transmission
aéroportée (noyaux de gouttelettes < 5 um), par exemple la
tuberculose, varicelle ou rougeole :
- Patients en chambre individuelle avec ventilation
adéquate et si possible une pression négative avec portes
fermées, au moins 6 renouvellements de l'air par heure.
- Port de masques pour le personnel, malades et gardes malades
* Précautions en cas de transmission par gouttelettes
> 5 um Exemples : Méningites bactériennes, VRS,
diphtérie :
- Chambres individuelles pour le patient
- Masque pour le personnel soignant
- Restriction de la circulation pour le patient qui doit porter
un masque chirurgical en cas de nécessité de sortie de sa
chambre.
* Précautions en cas de transmission contact :
- Chambre individuelle pour le patient si possible
- Cohorting (regroupement des patients similaires dans un
même secteur si possible
|
- Transmission de consignes entre équipe du jour et
équipe de nuit en cas de patients porteurs de BMR / BHRe.
- Affichages, pense - bêtes rappelant les
précautions standards.
- Affichages de sensibilisation incitant les visiteurs
à plus de rigueur et d'attention (feuillets pour les parents et
visiteurs, pour le personnel).
- Rappels sur les BMRs, slogans, à ajouter aux feuilles
de résultats rendus par le laboratoire.
|
|
Une hygiène de
l'environnement à l'état de l'art :
- Stérilisation.
- Hygiène générale selon des protocoles
éprouvés.
Figure 25 - Exemples de plaques signalétiques au lit
du patient
72
Recommandations et mesures correctives
-Port de gants pour le personnel entrant dans la chambre, blouses
et sur-blouses pour tout contact
avec le patient, surfaces ou matériel contaminé
- Lavage des mains avant et après contact avec le patient
et en sortant de la chambre
- Restriction des déplacements du patient
- Nettoyage, désinfection et stérilisation
appropriés de l'environnement et du matériel
*Isolement strict (fièvre hémorragique,
Staphylococcus aureus résistant à la Vancomycine, covid-19) :
Ce niveau d'isolement est exigé en cas de risque
d'infection par un agent hautement virulent et potentiellement dangereux
lorsque plusieurs voies sont en cause
- Chambres individuelles dans un secteur d'isolement si
possible
- Port de masque, gants, blouse, coiffe et protection oculaire
pour toute personne entrant dans la
chambre
-Lavage hygiénique des mains à l'entrée et
sortie de la chambre
-Incinération des aiguilles / seringues
-Désinfection rigoureuse des instruments
médicaux
-incinération des excreta , liquides biologiques ,
sécrétion rhinopharyngées
- Désinfection du linge
- Restrictions d'entrée des visiteurs et personnel
-Désinfection quotidienne et désinfection terminale
à la fin du séjour
-Matériel à usage unique
-Transport et manipulation au laboratoire approprié des
échantillons prélevés chez le patient
-Installation de signalétique appropriée
:
L'hôpital Universitaire de Genève, sous l'impulsion
du Pr Pittet, a expérimenté un système de
signalétique.
73
Recommandations et mesures correctives
- Désinfection conforme des dispositifs
médicaux.
- Contrôle rigoureux de l'eau, des conduits
d'aération et de la nourriture.
- Repenser l'architecture, l'agencement des unités et
implémenter au fur et à mesure des matériaux connus pour
leur vectorisation moindre des micro-organismes (par exemple, remplacer les
poignées de porte par des poignées en cuivre antimicrobien comme
il est d'usage dans les pays développés).
Praticiens hygiénistes ; un métier
à part entière :
Dans de nombreux pays développés, il existe
carrément des postes de contrôleurs d'hygiène. Benchmarker
des expériences de pays avancés dans ce terrain-là
s'avère utile.
Par exemple, en France le CLIN table sur la présence
d'au moins un infirmier hygiéniste pour 400 lits.
En cas d'impossibilité de recruter un expert pour
différentes raisons, cette tâche pourrait être
déléguée à une personne qui aura les latitudes pour
interpeller le personnel en cas de dépassements.
Aussi, par exemple, des cellules de crises pourraient
être crées afin de prendre en charge les cas de flambées
des IN ou d'épidémies à l'hôpital.
Le bon usage des antibiotiques :
Après avoir observé une utilisation qui
paraît parfois irrationnelle des anti-infectieux, nous recommandons un
moratoire sur les protocoles utilisés, afin de repenser l'usage
empirique des antibiotique.
La réflexion pourrait intégrer les
équipes de Microbiologie, de Pharmacie Clinique dont l'expertise
pourrait s'avérer précieuse pour cette réflexion
collégiale.
La rédaction de manuels de prescription pourrait aussi
s'avérer précieuse afin d'harmoniser et mieux penser le processus
de prescription et d'administration.
Les principes de désescalade ; de restriction et de
diversification (cycling - mixing) pourraient être envisagées.
Formation du personnel de santé,
éducation des patients et des gardes malades :
Parler de ce problème autour de débats, tables
rondes, cours destinés aux étudiants en sciences
médicales, vulgarisation auprès du grand public, brochures,
vidéos explicatives ...Etc
Toutes ces mesures devraient se juxtaposer à une
volonté sans équivoque de lutte contre les IN et une
sensibilisation efficace, créative et aidant à
l'implémentation des bonnes pratiques.
Prospectus à l'adresse des gardes malades et
visiteurs :
Une documentation digeste , vulgarisée , permet
d'intégrer dans la solution un maillon important qui est celui des
gardes malades. Ce genre de documentation est régulièrement dans
des stratégies de pays avec des stratégies de lutte
multidimensionnelles où la communication n'est pas en reste.
Une stratification des risques selon les patients
(comorbidités, exposition) et aussi selon les services :
Il serait judicieux de développer des matrices jaugeant
le risque, ou bien alors de benchmarker des matrices déjà
existantes.
74
Recommandations et mesures correctives
À titre d'exemple, le guide pratique de la
prévention des infections nosocomiales de l'OMS propose la
stratification suivante :
Tableau 8 - Stratification des IN suivant le risque
infectieux selon guide pratique de lutte contre les infections nosocomiales de
l'OMS.
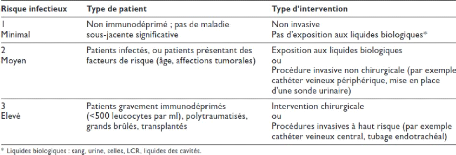
En ce qui concerne la stratification selon le service,
Les services de pédiatrie sont souvent classés
d'office dans les zones à risque sévère et les
unités de soins intensifs et de néonatologie sont classées
comme zones à très haut risque.
Pour revenir à notre étude, nous recommandons
très fortement un découpage du service selon le risque infectieux
et d'intégrer l'unité de cancérologie Mussy de prime abord
dans des zones à très haut risque au même titre que l'USI
et la néonatologie.
Des guidelines pour des types spécifiques
d'infections :
Par exemple, pour les infections urinaires, enlever le sondage
vésical dès que ce dernier n'est plus utile.
- La position demi-assise, le contrôle régulier de
la pression du ballonnet, et les soins de bouche pour les Pneumopathies
Associées à la Ventilation Mécanique.
75
Références Bibliographiques
[1] Rossolini, G. M., D'andrea, M. M., & Mugnaioli, C.
(2008). The spread of CTX-M-type extended-spectrum f3-lactamases. Clinical
Microbiology and Infection, 14, 33-41.
[2] Horan, T. C., Andrus, M., & Dudeck, M. A. (2008).
CDC/NHSN surveillance definition of health care--associated infection and
criteria for specific types of infections in the acute care setting. American
journal of infection control, 36(5), 309-332.
[3] Savey A, Infections nosocomiales, définition, dans
maîtrise des infections nosocomiales de A à Z. 2004, Editions
HEALTH&CO.3. CTIN.
[4] Guide pratique de la Prévention des infections
nosocomiales de l'OMS, 2 ème édition 2008, WHO/CDS/EPH.
2002.12.
[5] : Weinstein, Robert A. "Controlling antimicrobial resistance
in hospitals: infection control and use of antibiotics." Emerging infectious
diseases 7.2 (2001) : 188.
[6] Suman E, Varghese S, Jose J. Gentamicin resistance in
biofilm producing Pseudomonas aeruginosa causing catheter associated urinary
tract infections. Indian J Med Sci 2005 ; 59:214.
[7] National Nosocomial Infection Surveillance (NNIS) system
report : data summary from January 1992 through June 2003.
file://www.cdc.gov/ncidod/dhqp/pdf
(Consulté en Septembre 2020).
[8] A. Bouvet (centre national de référence des
streptocoques, Hôtel-Dieu, université Paris VI) ; Cours (en ligne)
[archive] de bactériologie générale ; «
Streptocoques-entérocoques ». Lien :
http://www.microbes-edu.org/etudiant/streptocoques.html
[9] Festekjian A, Neely M.Incidence and predictors ofinvasive
candidiasis associated with candidaemia in children. Mycoses 2011;54:146-53.
[10] Zaoutis TE, Prasad PA, Localio AR, Coffin SE, Bell LM,
Walsh TJ, et al. Risk factors and predictors for candidemia in pediatric
intensive care unit patients : implications for prevention. Clin Infect Dis
2010;51:e38-45.
[11] : Neu N, Malik M, Lunding A, Whittier S, Alba L, Kubin C,
et al.Epidemiology of candidemia at a Children's hospital, 2002 to 2006.Pediatr
Infect Dis J 2009 ; 28:806-9.
[12] : Verboon-Maciolek MA, Krediet TG, Gerards LJ, et al.
Clinical and epidemiologic characteristics of viral infections in a neonatal
intensive care unit during a 12-year period. Pediatr Infect Dis J 2005 ;
24:901.
[13] : M. Burgard, I. Grall, P. Descamps, J.-R. Zahar, INAPED
Burgard 2013, 4-195-B-10.
[14] : Site internet du Ministère de la Santé de
la Population et de la Réforme Hospitalière DIRECTIVES NATIONALES
PORTANT RENFORCEMENT DES ACTIONS DE LUTTE CONTRE LES INFECTIONS ASSOCIES AUX
SOINS.
Résumé du Séminaire national
d'évaluation sur les urgences et l'hygiène hospitalière
Oran - 28 -29 mars 2013.
76
Lien du PDF :
http://www.sante.dz/rencontres_msprh/Rencontre_UMC_MSPRH/Communications/DGPPS_hyg_h
ospitali%C3%A8re.pdf
[15] : Version électronique du Code la santé
publique Française consultable sur le site officiel :
https://www.legifrance.gouv.fr.
Consulté en Septembre 2020.
Lien du PDF :
https://solidarites-
sante.gouv.fr/IMG/pdf/Bilan_et_propositions_de_reformes_de_la_loi_du_4_mars_2002_relative_a
ux_droits_des_malades_et_a_la_qualite_du_systeme_de_sante.pdf
[16] :
https://www.cdc.gov ; Identifying
Healthcare-associated Infections for NHSN surveillance, Janvier 2020.
Lien Pdf :
https://www.cdc.gov/nhsn/pdfs/pscmanual/2psc_identifyinghais_nhsncurrent.pdf
[17] : CTINILS- Mai 2007, Ministère de la santé,
de la jeunesse et des sports DGS/DHOS. Lien Pdf :
http://nosobase.chu-lyon.fr/recommandations/Ministere_Sante/2006_defIN_ministere.pdf
[18] : Boyce, T. G., Gruber, W. C., & Fisher, R. G.
(2004). Enterobacter. In R. D. Feigin, Cherry, Demmler & Kaplan (Eds.),
Textbook of pediatric infectious diseases (5th ed., pp. 1427- 1431). PA, USA:
Saunders.
[19] : Frédéric Barbut, Catherine Eckert,
Valérie Lalande & Alban le Monnier, Clostridium difficile, Chapitre
58, page 489, Remic 2015, tome 2.
[20] : Dr. José LABARERE, Université Joseph
Fourier de Grenoble, UE7 Santé Société Humanité -
Risques sanitaires, 2011/2012. Lien:
http://unf3s.cerimes.fr/media/paces/Grenoble_1112/labarere_jose/labarere_jose_p11/index.htm
[21] : MCFEE ; R.B 2009 Nosocomial or hospital-acquired
infections ; an overview Dis.Mon 55, 422-438.
[22] : Jaballah, N. Ben, et al. "Epidémiologie des
infections bactériennes nosocomiales dans une unité de
réanimation néonatale et pédiatrique tunisienne."
Médecine et maladies infectieuses 36.7 (2006) : 379-385.
[23] : LODHA, Rakesh, CHANDRA, Uma, NATCHU, Mouli, et al.
Nosocomial infections in pediatric intensive care units. The Indian Journal of
Pediatrics, 2001, vol. 68, no 11, p. 1063-1070.
[24] : García, I. Jordan, et al. "Estudio
multicéntrico nacional sobre la infección nosocomial en la UCIP."
Anales de Pediatría. Vol. 80. No. 1. Elsevier Doyma, 2014.
[25] : Nedjai, S., A. Barguigua, N. Djahmi, L. Jamali, K.
Zerouali, M. Dekhil, and M. Timinouni2012. Prevalence and characterization of
extended spectrum beta-lactamases inKlebsiella-Enterobacter-Serratia group
bacteria, in Algeria. Med.Mal Infect. 42:20-29.
[26] : Albert Faye, Édouard Bingen, Place des
infections nosocomiales en pédiatrie, Volume 15, supplément 1,
Novembre 2012, 10.1684/mtp.2012.0448.
[27] : Balaban, smail, et al. "Nosocomial infections in the
general pediatric wards of a hospital in Turkey." Japanese journal of
infectious diseases 65.4 (2012) : 318-321.
[28]
77
: Hamza, Ridha. "EPIDEMIOLOGIE DES INFECTIONS ASSOCIEES AUX SOINS
HEALTHCARE ASSOCIATED INFECTIONS EPIDEMIOLOGY." Revue Tunisienne
d'Infectiologie-Janvier 4 (2010) : 1-4.
[29] : 2015, Directives Nationales Relatives à
l'Hygiène de l'environnement dans les établissements de
santé publics et privés. Consulté le 14/11/2020, sur le
site de la société Algérienne de Microbiologie Clinique (
SAMIC ) , Lien :
https://www.samic.dz/site/uploads/directives.pdf.
[30] : Intérêt de l'étude de la consommation
des antibiotiques: méthodologie. Journée de formation:
Méthode d'étude de la consommation des antibiotiques.
Présenté par H.Tali-Maamar. Consulté le 14/11/2020. Lien :
http://www.sante.dz/aarn/ipa.pdf.
Annexes
|
Date
|
Traitement 1
|
|
Traitement 2
|
Traitement 3
|
79
Annexes
Les formulaires de recueil de données
:
1) Formulaire physique : Patient
Nom et prénom : ..
Sexe : F M
Age : ..
Date d'Hospitalisation : ..... /..... / .....
Motif : ..
Service :
État de l'immunité :
Exposition du patient :
Intervention chirurgicale Sonde urinaire
Perfusion/ Injections Une antibiothérapie
Un examen invasif (bronchoscopie, gastroscopie, ponction etc...)
Précisez :
Ventilation mécanique Cathétérismes
Précisez quels types:
Autres Précisez : .
Traitements (Antibiotique ou autre)
80
Annexes
Le patient a-t-il présenté d'autres
signes cliniques (que ceux pour lesquels il a été
admis)
Lesquels:
1-
2-
3- ..
4-
5- ..
Date d'apparition :
Site :
Un prélèvement a-t-il été
réalisé ? OUI NON
Date et type du prélèvement :
Site du prélèvement :
Observations / Résultats :
81
Annexes
2) Formulaire numérique pour le logiciel Epidata
3,2 :
Nom: <A >
prenom:<A >
Sexe:# (M=1 F=2)
Age:####
Date de naissance:<dd/mm/yyyy>
Date dadmission a lhopital <dd/mm/yyyy>
Motif admission:<A >
Date dHospitalisation
<dd/mm/yyyy>
Motif hospitalisation:<A >
Service:# (mussy=1, nobecourt rea=2, nobecourt neonat=3)
Etat de limmunite:# (Immunocompetent=1 Immunodeficience
primaire=2 VIH=3 Immunodeficience iatrogene=4 inconnu=9)
Exposition du patient
Intervention chirurgicale:# (oui=1 non=2)
VVP:# (oui=1 non=2)
catheter central:# (oui=1 non=2)
si oui precisez lendroit:<A >
Une
antibiothérapie:# (oui=1 non=2)
Sonde urinaire:# (oui=1 non=2)
Un examen invasif:# (bronchoscopie=1 gastroscopie=2 ponction=3
autre=9)
si autre precisez :<A >
Ventilation mecanique:# (oui=1
non=2)
si oui:# (invasive=1 non anvasive=2)
Portes dentree: # (escarres=1 plaies=2 autre=9)
si Autre, Précisez:<A >
Traitements (Antibiotique
ou autre):# (oui=1 non=2)
traitement 1:<A >
traitement 2:<A >
traitement 3:<A >
traitement 4:<A >
signes cliniques d infection (autres que ceux pour lesquels il a
ete admis):# (oui=1 non=2)
Lesquels:<A >
Date apparition :<dd/mm/yyyy>
Site :<A >
Un prelevement a-t-il ete realise: # (oui=1
non=2) si oui, Date du prélèvement :<dd/mm/yyyy>
type du prélèvement :<A >
Site du prélèvement :<A >
germe isole: # (oui=1 non=2)
si oui, lequel germe1:<A >
germe2:<A >
germe3:<A >
infection nosocomiale confirmee: # (oui=1 non=2)
Annexes

82
Figure 26 - Photos d'infections cutanées
nosocomiales contractées à l'unité Mussy
Les infections cutanées ont été
particulièrement élevées durant cette étude,
surtout à l'unité Mussy. À gauche une infection à
Klebsiella Pneumoniae BLSE, et à droite une infection à
Absidia spp.
83
Annexes
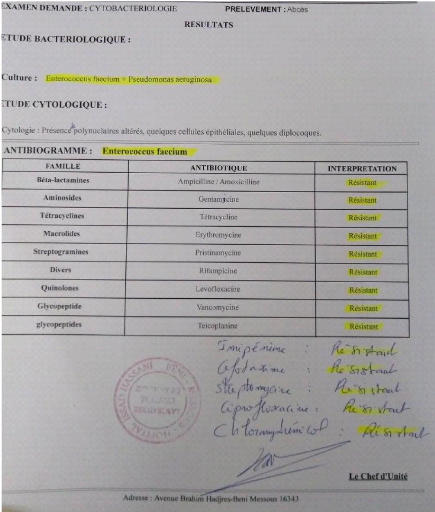
Figure 27 - Enterococcus faecium multirésistant
retrouvé en pédiatrie durant la pré-enquête sur un
prélèvement d'abcès péri-anal.
84
Annexes

Figure 28 - Corrélation consommation en antibiotiques
et résistance [30]
Résumé :
Les infections nosocomiales sont un problème de
santé publique prioritaire au niveau planétaire. La population
pédiatrique est particulièrement prédisposée
à ce type d'infections (immaturité du système
immunitaire), surtout lorsque l'état général est
altéré, ou une comorbidité majeure comme le cancer est
présente.
Quelles mesures peuvent améliorer cette situation dans
un système de santé publique à plusieurs paramètres
et contraintes?
Nous nous sommes intéressés au cas du service de
pédiatrie dans une démarche systématique pour avoir une
vue d'ensemble sur l'écologie bactérienne du service, les
bactéries multi résistantes, et les infections nosocomiales les
plus retrouvées. Nous avons ainsi produit dix recommandations qui,
combinées à une sensibilisation, constituent une démarche
réaliste, simple à adopter, et adaptée à notre
système de santé publique pour aider à endiguer ce
fléau.
Summary :
Nosocomial infections are a priority public health problem at the
planetary level. The pediatric population is particularly predisposed to this
type of infections (immaturity of the immune system), especially when the
general condition is altered, or a major comorbidity such as cancer is present.
What measures can improve this situation in a public health system with several
parameters and constraints?
We were interested in the case of the pediatric department in
a systematic approach to have an overview of the bacterial ecology of the
department, multiresistant bacteria, and the most common nosocomial infections.
We have thus produced ten recommendations which, combined with raising
awareness, constitute a realistic approach, simple to adopt, and adapted to our
public health system to help stem this scourge.
|
|
|
|
|
: ÕÎáã
|
|
äæÖÑÚã
áÇØáÇ
|
.íãáÇÚáÇ
|
ìæÊÓãáÇ
ìáÚ
|
ÉíæáæáÇ
ÊÇÐ ÉãÇÚáÇ
ÉÍÕáÇ
|
ÊáÇßÔã äã
|
)ÊÇíÔÊÓãáÇ
ìæÏÚ( íæÔãáÇ
ÌãÎáÇ ÏÚí
|
|
áËã ßÑÊÔã
ááÇÊÚÇ
|
ÏæÌæ æ
|
ÉãÇÚáÇ
ÉáÇÍáÇ
|
ÑííÛÊ ÏäÚ
ðÉÕÇÎ
)íÚÇäãáÇ
|
ÒÇåÌáÇ
ÌÖä
|
ãÏÚ(
ìæÏÚáÇ äã
ÚæäáÇ ÇÐåá
ÕÇÎ áßÔÈ
|
|
|
|
|
|
.äÇØÑÓáÇ
|
|
|
|
ÏæíÞáÇæ
ÑííÇÚãáÇ äã
ÏíÏÚáÇ Úã
ÉãÇÚáÇ
ÉÍÕáÇ ãÇÙä
í ÚÖæáÇ ÇÐå
äÓÍÊ ä äßãí
íÊáÇ
ÑíÈÇÏÊáÇ íå
Çã
|
|
ÉÏÏÚÊã
|
ÇíÑíÊßÈáÇæ
|
ãÓÞáá
ÉíÑíÊßÈáÇ
ÉÆíÈáÇ ìáÚ
ÉãÇÚ ÉÑÙä
ìáÚ áæÕÍáá
ãÙäã Ìåäã
ááÇÎ äã
áÇØáÇ ÈØ
ãÓÞÈ äíãÊåã
Çäß
|
|
ÇðÌåä
|
íÚæáÇ
|
ÉÏÇíÒ Úã
|
ÈäÌ ìáÅ
ÇðÈäÌ áßÔÊ
ÊÇíÕæÊ ÑÔÚ
ßáÐÈ ÇäÑÏÕ
ÏÞá .ÇðÚæíÔ
ÑËßáÇ
íæÔãáÇ
ÌãÎáÇ ÖÇÑã æ
ÉãæÇÞãáÇ
|
|
|
|
. ÉáÂÇ åÐå
ìáÚ ÁÇÖÞáÇ í
ÉÏÚÇÓãáá
ÇäíÏá
ÉãÇÚáÇ
ÉÍÕáÇ ãÇÙä
Úã åííßÊæ
åÏÇãÊÚÇ
áåÓí
ÇðíÚÞÇæ
|



