Annexes
a
Annexe 01
Partie théorique
Tableau I: Composition d'huiles de soja
génétiquement modifiées (Warner,
2007).

Le tableau ci-dessus tiré du bulletin IBP, numéro
1, 2002 du Canada, montre les modifications possibles par génie
génétique.
Optimisation des paramètres de dégommage
enzymatique
Equivalents de NaOH
Phosphore (ppm)

Ajout de l'enzyme
Ajout d'acide citrique
Ajout du caustique
Temps (heures)
Figure 01: Effet de NaOH sur le
dégommage enzymatique (Münch, 2004).
1,5 mole équivalents relative à l'acide citrique
est l'optimum pour dégommer une huile enzymatiquement
(Münch, 2004).

Phosphore (ppm)
Ajout de l'enzyme
Ajout d'acide citrique
Ajout du caustique
Temps (heures)
Figure 02 : L'effet de température
sur Lecitase Ultra (Münch, 2004).
La température 50 - 55 °C est l'optimum
(Münch, 2004).
Phosphore (ppm)
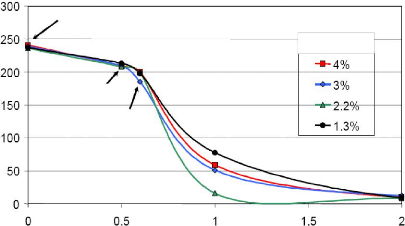
Ajout de l'enzyme
Ajout du caustique
Ajout d'acide citrique
Ajout d'eau
Temps (heures)
Figure 03 : Effet de l'eau sur le
dégommage enzymatique (Münch, 2004).
b
L'optimum d'eau à ajouter est de 2 % (Münch,
2004).

Phosphore (ppm)
Ajout d'acide citrique
Ajout du caustique
Ajout de l'enzyme
c
Temps (heures)
Figure 04 : Effet de la dose de Lecitase
Ultra (Münch, 2004).
Commencer par 50 ppm puis optimiser la dose de l'enzyme à
ajouter (Münch, 2004).
Annexe 02
Matériel et méthodes
Tableau II : Matériel, solutions
et réactifs utilisés au cours des analyses (M.E.,
2001).
|
Matériel
|
Solutions et réactifs
|
|
Balance analytique
|
|
Acétone
|
|
Colorimètre LOVIBOND
|
visuel:
|
Alcool neutralisé
|
|
|
|
Chauffe ballon
|
|
Acide acétique
|
|
Centrifugeuse
|
|
Acide chlorhydrique à 0,01 N
|
|
Dessiccateur
|
|
Acide sulfurique à 20 %
|
|
Etuve
|
|
Bleu de Bromophénol
|
|
Four à moufle
|
|
Chloroforme pùr
|
d
|
Plaque chauffante-
agitatrice
|
Eau distillée
|
|
Spectrophotomètre UV-
visible
|
Empois d'amidon
|
|
Ampoule à décanter
|
Hydroxyde de potassium à 50 %
|
|
Béchers (25ml, 250ml)
|
Hexane
|
|
Ballons à fond plat
|
HCl acétonique
|
|
Burettes graduées (10ml, 25ml)
|
Iodure de potassium
|
|
Barreau magnétique
|
Molybdate de sodium
|
|
Creusets
|
Méthyle orange
|
|
Erlenmayers
|
Oxyde de zinc
|
|
Eprouvettes graduées
|
Phénolphtaléine
|
|
Entonnoir
|
Soude à 0,1 N et 1 N
|
|
Fioles jaugées (50ml, 100ml)
|
Sulfate d'hydrazine
|
|
Papier pH (STUPHAN 4)
|
Thiosulfate de sodium à 0,01N
|
|
Papier filtre
|
|
|
Spatule
|
|
Courbe d'étalonnage de
phosphore
Construire la courbe d'étalonnage de la teneur en
phosphore à l'aide d'une solution mère (1,0967g de
dihydrogénophosphate de potassium (KH2PO4) dans 250 ml d'eau
distillée, cette solution comprend 1mg de phosphore par ml) à
partir de cette solution on prélève 5ml dans une fiole de 500 ml
qu'on ajuste avec de l'eau distillée c'est la solution fille. Cette
solution est à 0,01mg de phosphore par ml.
? Préparation des solutions standards
Pipeter 1ml, 2ml, 4ml, 6ml, 8ml, et 10ml de la solution fille
dans une fiole de 50 ml. Ajouter 8ml de Sulfate d'hydrazine et 2 ml de
Molybdate de sodium, amener à 50 ml avec de l'eau distillée.
Mettre au bain marie bouillant pendant 15 mn, laisser refroidir, lire
l'absorbance à 650 nm et tracer la courbe (M.E.,
2001).
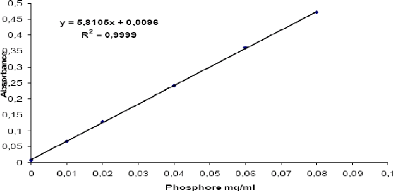
e
Figure 05 : Courbe d'étalonnage de
phosphore (M.E., 2001).
Préparation des solutions (M.E.,
2001)
? Thiosulfate de sodium anhydre à 1 N
Poids moléculaire du thiosulfate de sodium 158,11.
1 N 158,11g
0,1 N X
X=15,811g de Na2S2O3 qsp* 1 litre d'eau
distillée.
0 ,01N, X= 1,581 de Na2S2O3 qsp* 1 litre d'eau
distillée. *qsp : quantité suffisante pour.
? Solution d'amidon à 1%
Prendre 1g de poudre d'amidon compléter à 100 ml
avec de l'eau distillée.
? Solution de phénophtaléine 1%
Prendre 1g et compléter à 100 ml avec de
l'éthanol 95 % (v/v).
? Solution de bleu de Bromophenol à 0,2
%
Prendre 0,2g et compléter à 100 ml avec de
l'acétone.
? Méthyle orange à 1%
Prendre 1g et compléter à 100 ml avec de l'eau
distillée.
| 


