|
Université Sultan Moulay
Slimane
Faculté Polydisciplinaire de Khouribga
Filière de
Sciences de la Vie (SV)
|
|
Année uiversitaire : 2018-2019 N° d'ordre : /
2019
Projet de Fin d'etudes
Essai d'une étude comparée de la
qualité des
eaux brutes et traitées de la source
Ain
Asserdoun (Beni-Mellal) et ceux du barrage
Ait
Massoud (Khouribga)
Présenté en vue d'obtenir la Licence Fondamentale
en :
FilieÌre : Sciences de la Vie (S.V)
Option : Biotechnologie et Microbiologie
Réalisé par : - Mlle. ABOUFARIS HASNAE
- Mlle. CHARRADI NOURA
Encadré par : - Pr. ETTAKI MOHAMMED - Mr.TALBAOUI
RACHID
Soutenu le :08/07/2019 devant le jury :
Faculté Polydisciplinaire de Khouribga Président
Mr.TALBAOUI Rachid ONEE Khouribga Encadrant
Pr.ETTAKI Mohammed Faculté Polydisciplinaire de Khouribga
Encadrant

DEDICACES
Nous dédions ce modeste travail à:
Dieu
Nos chers pères HAMZA et ABDELMAJID
Nos
chères mères FATIMA et FOUZIA, pour
leur éducation,
leur patience, leurs énormes
sacrifices à nous offrir une vie
pleine de joie
et d'amour, leur soutiens et encouragement;
que Dieu les
gardent.
Nos frères et soeurs
Nos ami(e)s
Nos professeurs
à FPK
Les techniciens du laboratoire de L'ONEE
Et à tous
ceux qui nous aiment
Nous dédions ce travail...
La durée du travail : du 01/03/2019 au 31/03/2019.
AVANT PROPOS
Le stage effectué au sein de l'Office National de
L'Electricité et de l'Eau potable)-branche eau- de Khouribga (ONEE) avec
la réalisation du projet de fin des études s'inscrit dans le
cadre de la préparation de notre diplôme de Licence fondamentale
en Sciences de la vie, option : Biotechnologie et microbiologie.. Le choix de
cet établissement est motivé par deux raisons essentielles :
· L'ambition de faire une application élargit sur
la base des études et des compétences acquises pendant trois ans
de formation à la FPK.
· L'importance de l'ONEE au niveau du contrôle de la
qualité des eaux à usage domestique avec la participation
préventive dans la protection de la population contre les maladies
hydriques.
Noms et prénoms des étudiants :
Mlle ABOUFARIS HASNAE & Mlle CHARRADI NOURA
L'intitulé du travail :
Essai d'une étude comparée de la
qualité des eaux brutes et traitées de la
source Ain Asserdoun
(Beni-Mellal) et ceux du barrage Ait Massoud
(Khouribga)
Nom et prénom de l'encadrant à la Faculté
Polydisciplinaire de Khouribga :
Le Professeur Mohammed ETTAKI
Noms et prénoms des encadrants à l'ONEE :
Le
Parrain : M. Rachid TALBAOUI
Mr Zakaria ABBOUZ
Entités où les travaux ont été
réalisés :
Laboratoire des analyses chimiques et bactériologiques
de l'ONEE-Khouribga
Laboratoire des analyses chimiques et
bactériologiques de l'ONEP Ain Asserdoun
Remerciements
Dieu merci pour la santé, la volonté, le courage
et la détermination qui nous ont accompagnés tout au long de la
préparation et l'élaboration de ce travail et qui nous ont permis
d'achever ce modeste travail.
Le présent travail est non seulement le résultat
de notre courage, sacrifice, patience et endurance mais aussi une participation
de plusieurs personnes qui nous sont chères.
Nous exprimons nos profonds remerciements à notre
professeur AHMED BAKRIM responsable pédagogique de la filière
sciences de la vie pour son aide et ses orientations.
Nos sincères et profonds gratitudes sont
exprimées agréablement à Mr. ETTAKI MOHAMMED qui nous a
permis de bénéficier de son encadrement ; Les conseils qu'il nous
a prodigué, la patience, la confiance qu'il nous a
témoignés ont été déterminants dans la
réalisation de notre de projet de fin d'études.
Nous remercions Mr. TALBAOUI RACHID chef de laboratoire
régional de Khouribga. N'oublions pas de remercier très
chaleureusement Mr. ABBOUZ ZAKARYAE pour son accueil, son aide, son attention
et sa gentillesse tout au long du stage, et aussi tous les membres du
laboratoire L'ONEE.
Nos remerciements s'étendent également aux jurys
et à tous nos enseignants durant les années des études.
Enfin, nous tenons à remercier tous ceux qui, de
près ou de loin, ont contribué à la réalisation de
ce travail.
Mots clés : Eutrophisation, eau brute,
eau traitée, paramètres physico-chimiques, paramètres
bactériologiques, Charbon actif, barrage Ait Massoud, Source Aïn
Asserdoune.
Résumé
L'eau est un élément naturel très
abondant sur Terre, présent sous différents états,
état Solide (les glaces polaires), état
Vapeur (atmosphère), état Liquide
(mers, océans) qui grâce à ses
propriétés, le développement et la continuité des
organismes vivants et ainsi leurs fonctions vitales sont
réalisés.
La production de l'eau potable de la ville de
Béni-Mellal est assurée par l'ONEP, qui exploite principalement
les eaux de la source Ain Asserdoune, bien que celle de la ville de Khouribga
soit assurée par l'ONEE qui profite les eaux du barrage Ait Massoud. Ces
eaux subissent premièrement un prétraitement dans le but de
diminuer leurs charges en matière en suspension, ensuite un traitement
assurant l'élimination de la pollution chimique et microbiologique et
l'abaissement de la turbidité pour toute une série de
transformations afin d'obtenir une eau potable destinée à la
consommation humaine.
Pour une bonne santé, l'eau doit être d'une bonne
qualité, et pour sa préservation, plusieurs évaluations du
système de traitement de l'eau ont été
réalisées. Ce travail consiste à un essai d'étude
comparée entre les eaux de Ain Asserdoune (Beni-Mellal) et celles du
barrage Aït Massoud (région Khouribga), grâce à des
analyses physico-chimiques et bactériologiques.
D'après les résultats obtenus des
paramètres physico-chimiques et bactériologiques, on peut
constater que les eaux traitées sont conformes aux normes, ceci est
expliqué par l'efficacité du traitement utilisé.
Contrairement aux eaux brutes, qui sont caractérisées par des
paramètres physico-chimiques et bactériologiques ne
répondant pas aux normes.
Les paramètres organoleptiques (odeur et gout)
concernant l'eau du barrage Aït Massoud, ne sont pas conformes aux normes,
l'inappropriée de ces paramètres est due à un
phénomène qui s'appelle l'Eutrophisation. Le traitement par le
charbon actif granulé améliore la qualité des ces eaux.
Table des matières
Dédicace
Remerciement
Résumé
Liste des figures
Liste des tableaux
Liste des abréviations
Introduction générale 1
Partie I : Bibliographie 4
I. Aperçu général 5
1. Source Ain Asserdoun 5
2. Barrage Ait Massoud 6
II. Description des stations 6
1. Station de traitement de Béni-Mellal 6
2. Station de traitement Ait Massoud 7
3. Traitement des eaux 9
3.1 Prétraitement de l'eau brute 9
3.2 Traitement de l'eau preìtraiteìe (technique de
JART-TEST) 10
III. L'Eutrophisation 13
1. Définition 13
2. Cause 14
3. Milieux touchés 15
4. Les remèdes contre l'eutrophisation 15
Partie II : Matériel et méthodes
17
I. Contrôle de la qualité des eaux 18
1. Analyses physico-chimiques 18
1.1 Mesure de la turbidité 18
1.2 Mesure de la conductivité 18
1.3 Potentiel d'Hydrogène (pH) 19
1.4 L'oxydabiliteì 20
1.5 Titre alcalimétrique complet (TAC) 21
1.6 La dureté calcique (TH-Calcium) 22
1.7 Nitrate 22
1.8 Sulfate 24
1.9 Chlorure 24
2. Analyses bactériologiques/biologiques 25
2.1 Echantillonnages 25
2.2 Bactéries recherchées 25
2.3 Techniques d'analyses 27
a. Filtration sur membrane (Eau Traitée) 27
b. La méthode de NPP (Eau Brute) 29
c. Incorporation en gélose (Eau traitée et brute)
32
Partie III : Résultats et discussions
33
I. Résultats des paramètres physico-chimiques 34
1. La turbidité 34
2. La conductivité 34
3. Le potentiel hydrique (pH) 35
4. L'oxydabiliteì 36
II. Résultats des paramètres organoleptiques 37
III. Résultats des paramètres
bactériologiques 38
Conclusion 40
Références bibliographiques 42
Annexes
Liste des figures
Figure 1 : Station de traitement de
Béni-Mellal 6
Figure 2 : Station de traitement d'Ait
Massoud 8
Figure 3 : Le dégrillage 9
Figure 4 : Le dessablage 9
Figure 5 : Le débourbage 10
Figure 6 : Floculateur pour Jar-Test 11
Figure 7 : Le CAG 12
Figure 8 : L'eutrophisation au niveau de la
rivière Ramapo (New Jersey) 13
Figure 9 : Schéma expliquant le
phénomène de l'eutrophisation 14
Figure 10 : Effet de l'eutrophisation sur la
population aquatique 15
Figure 11 : Turbidimètre 18
Figure 12 : Conductimètre 19
Figure 13 : pH mètre 20
Figure 14 : Le point équivalent
(Oxydabilité) 21
Figure 15 : Le point équivalent (TAC)
21
Figure 16 : Le point équivalent
(TH-Calcium) 22
Figure 17 : Spectrophotomètre 23
Figure 18 : Colonne contenant du cadmium
23
Figure 19 : Point équivalent
(Chlorure) 25
Figure 20 : Bactéries Coliformes
totaux 26
Figure 21 : Bactéries Coliformes
fécaux 26
Figure 22 : Bactéries
entérocoques intestinaux 26
Figure 23 : Bactéries streptocoques
fécaux 27
Figure 24 : Système de filtration sur
membrane 27
Figure 25 : Autoclave 28
Figure 26 : Schéma désignant
l'ensemencement de l'échantillon à 3 différentes
dilutions
recherchant les coliformes totaux et fécaux. 30
Figure 27 : Schéma désignant
l'ensemencement de l'échantillon à 3 différentes
dilutions
recherchant les streptocoques fécaux. 31
Figure 28 : Ensemencement sur gélose
à l'extrait de levure 32
Figure 29 : Mesure de la turbidité de
l'eau brute et l'eau traitée 34
Figure 30 : Mesure de la conductivité
de l'eau brute et l'eau traitée 35
Figure 31 : Mesure de pH de l'eau brute et
l'eau traitée 35
Figure 32 : Mesure de l'oxydabilité de
l'eau brute et l'eau traitée 36
Liste des tableaux
Tableau 1 : Résultats des
paramètres physico-chimiques de l'eau de béni-Mellal 37
Tableau 2 : Résultats des analyses
organoleptiques de l'eau de Khouribga 37
Tableau 3 : Résultats des analyses
bactériologiques des eaux naturelles 38
Tableau 4 : Résultat des analyses
bactériologiques des eaux traitées 38
Tableau 5 : Résultats de la recherche
des micro-organismes révivifiables 39
Liste des abréviations
ONEE : Office Nationale de
l'Electricité et de l'Eau Potable
ONEP : Office National de l'Eau Potable
MES : Matière En Suspension
CTE : Carrière Technologie Equestre
CAG : Charbon Actif Granulé
NTU : Unité de Turbidité
Néphélométrique
TAC: Titre Alcalimétrique Complet
TH-CALCIUM: Dureté Calcique
NPP: Nombre le Plus Probable
UFC: Unité Formant Colonie
EB: Eau Brute
ET: Eau Traité
CT: Coliformes Totaux
ST: Streptocoques Fécaux
Introduction générale
1
Projet de fin d'études
2018/2019
2
Projet de fin d'études
2018/2019
L'eau est une source de vie, a longtemps été
considérée comme une ressource inépuisable. L'accès
durable aux ressources en eau est une préoccupation majeure qui concerne
tous les pays du monde. Mais, la question de cette ressource rare et vitale, se
pose surtout en termes de disponibilité, de qualité de l'eau et
de sa gestion en fonction des priorités des différents secteurs
utilisateurs (domestique, agriculture, industrie et tourisme). Le changement
climatique et la croissance urbaine et démographique ainsi que
l'expansion des activités économiques et agricoles, risquent
d'aggraver la situation du stress hydrique qui frappe déjà
plusieurs pays.
Les eaux destinées à la consommation humaine
(potables) proviennent de différentes sources. On peut citer :
· Les eaux souterraines : Dues à
l'accumulation des infiltrations dans le sol qui varient en fonction de la
porosité et de la structure géologique, elles sont d'excellente
qualité physico-chimique et bactériologique. Les terrains
traversés par l'eau influencent la minéralisation, celle-ci est
faible dans les terrains anciens de type granite et schiste, et
élevée dans les terrains sédimentaires comme les
calcaires. Elles sont exemptes de matières organiques sauf en cas de
pollution. (22)
· Les eaux de surface : Se
répartissent en eaux circulantes (courantes) ou stockées
(stagnantes). Elles se forment à partir, soit de l'émergence des
nappes profondes en sources, soit du rassemblement d'eau de ruissellement.
Elles sont riches en matières en suspension et organiques, ainsi qu'en
plancton. Elles sont très sensibles à la pollution
minérale et organique de type nitrates et pesticides d'origine agricole.
(22)
L'eau on peut le considérer parmi les plus grands et
importants besoins de notre corps, avec les activités qu'on exerce il
perd beaucoup d'eau par jour (entre 2 à 3 litres), donc il doit
récupérer cette perte sans attendre qu'il commence à se
déshydrater et tomber dans des conditions indésirables à
la santé, son usage a des fins alimentaires et d'hygiène
corporelle nécessite un haut niveau de qualité physico-chimique
et microbiologiques.
L'eau distribuée par réseau constitue un des
produits alimentaires les plus contrôlés. Elle doit
répondre aux exigences de qualité imposées par la
législation Marocaine.
Le respect de ces exigences nécessite la plupart de temps
le recours à certains traitements plus ou moins complexes. Divers
facteurs peuvent altérer sa qualité depuis le lieu de
prélèvement jusqu'au robinet : des facteurs naturels ou
anthropiques agissant sur la qualité de
3
Projet de fin d'études
2018/2019
l'eau brute ainsi que des facteurs liés aux installations
nécessaires au transport de l'eau traité.
Malgré son excellente qualité et l'intensité
de contrôles dont elle fait l'objet, de nombreux consommateurs de la
région de Khouribga ont senti un changement de la qualité de
l'eau qu'ils consomment en raison de défauts organoleptiques
attribués à l'eau de robinet ( saveur, odeur) ce qui nous a
amené dans le cadre de l'obtention de Diplôme de Licence Sciences
de la Vie de la Faculté Polydisciplinaire de Khouribga, à faire
une recherche analytique sur la qualité de cette eau en comparaison avec
l'eau de Beni Mellal.
Le présent rapport est organisé de la façon
suivante :
La première partie concerne une étude
bibliographique des zones étudiées : AIN ASSERDOUN (BENI MELLAL)
et AIT MASSOUD (KHOURIBGA) ; La deuxième partie apporte sur les
matériels et méthodes effectuées au sein du laboratoire
;
La troisième partie concerne les résultats et
discussions.
Partie I : Bibliographie
4
Projet de fin d'études
2018/2019
I. Aperçu général :
5
Projet de fin d'études
2018/2019
La région de Béni Mellal-Khénifra
située au centre du Maroc, sa position géographique lui
confère une grande diversité climatique qui varie d'un climat
humide à un climat sub-aride. La pluviométrie moyenne annuelle
connait d'importantes variations (la province de Beni-Mellal en 2012 est de 291
mm de précipitations, ce chiffre qui a diminué par rapport
à l'année 2008 « 460,3 mm », la province de Khouribga
278 mm, alors que la province de Tadla enregistre un taux de 334 mm de
précipitations). (14)
La région de Béni Mellal-Khénifra est
pompé par un cours d'eau principale qui est Oued Oum-Er-Rbia, c'est le
principal cours d'eau du bassin, il prend sa source dans le Moyen Atlas et se
jette dans l'Océan Atlantique à Azemmour. La région
s'étend sur une superficie de 28,374 km2 soit 3,99 % du
territoire national. Cette région compte 2.520.776 habitants dont 49,14
% sont urbains, la densité est de 88,8 habitants au km2. Le
bassin de l'Oum-Er-Rbia englobe d'importantes sources dont les eaux sont
utilisées essentiellement pour l'alimentation en eau potable et
l'irrigation pour cette grande population. (14)
Pour les eaux superficielles et parmi 128 grands barrages qui
sont en service au Maroc, la région de Beni Mellal-Khénifra
compte 15 barrages en plus de 7 systèmes de transfert d'eau. Ces
ouvrages permettent la satisfaction des besoins en eau potable, industrielle et
agricole. Cette infrastructure hydraulique actuelle permet la mobilisation en
moyenne de 3550 millions de mètre cubes, l'irrigation de près de
493 575 ha et la production de d'environ 350 millions de mètres
cubes/an. (14)
Concernant les eaux souterraines, le bassin d'Oum-Er-Rbia est
constitué par un ensemble de nappes phréatiques. On peut citer
les nappes phréatiques de Tadla parmi les principales nappes qui sont
exploitées pour l'alimentation en eau potable et industrielle des
principales villes de bassin Béni-Mellal et Khouribga.
1. Source Ain Asserdoun :
C'est la plus grande source de Beni Mellal qui assure l'eau
potable et l'eau d'irrigation des terres, avec un débit de 2000 litres
par seconde. Ain Asserdoun jaillit des roches calcaires, composé de deux
bassins ; le bassin d'alimentation qui ouvre une surface de 222 km2
et un périmètre de 70 km (Bahzad, 1982) et le bassin de
développement. (15)
2. Barrage Ait Massoud :
Localisé au niveau de la région de Tadla Azilal,
d'une hauteur de 34 m et d'une retenue de
6
Projet de fin d'études
2018/2019
13,2 millions de m3, c'est un ouvrage dont le
volume s'élèvera à 115.000 m3, assurant la
satisfaction des besoins de la ville de Khouribga. Il est équipé
d'une usine qui permettra d'assurer la production de 28 millions de kWh sous
une puissance de 6,4 mW.
Sous le cadre socio-économique, l'usage intensif des
engrais chimique et des pesticides en agriculture, ainsi que les rejets urbains
et industriels, engendrent une augmentation de pollution qui affecte les eaux
souterraines. (16)
II. Description des stations :
1. Station de traitement de Béni-Mellal :
La station de traitement d'eau potable de Béni-Mellal est
située au sud de la ville dont le but d'assurer un écoulement
gravitaire, cette station dernière est alimentée en eau brute
à partir de la source Ain Asserdoun, et équipée pour
assurer une production globale de l'ordre de 260 litres/seconde d'eau potable,
lorsque l'eau brute présente en MES = 2 g/litre, afin de gérer
les besoins de consommateur. (20)

Figure 1 : Station de traitement de
Béni-Mellal
Elle a été réalisée en deux tranches,
décrites ci-après :
La tranche n°1, construite en 1977 par la
société CTE, pour produire un débit de 140 l/s
7
Projet de fin d'études
2018/2019
d'eau potable et qui comprend les ouvrages hydrauliques suivants
:
- 1 ouvrage d'arrivé d'eau brute, équipé
d'un obturateur à disque moyen ;
- 1 canal alimentant cette tranche en eau brute, mais qui est
déjà conditionné en réactifs de traitement
(notamment le chlore et le sulfate d'alumine) ;
- 2 floculateurs ;
- 2 décanteurs statiques ;
- 3 filtres ouverts à lit de sable ; - 1 bâche d'eau
traitée de 60 m3 ;
- 1 réservoir semi enterré de 700 m3
d'eau traitée.
La tranche n°2, construite en 1993 par la
société SOGEA, pour produire un débit de 120 l /s d'eau
potable et qui comprend les ouvrages hydrauliques suivants :
- 1 canal alimentant cette tranche en eau brute, mais qui est
déjà conditionné en réactifs de traitement
(notamment le chlore et le sulfate d'alumine) ;
- 2 floculateurs ;
- 2 décanteurs statiques de type ?longitudinales? ;
- 3 filtres ouverts à lit de sable.
Comme ouvrages hydrauliques celui d'arrivée la
bâche d'eau traitée de 60 m3 ainsi que le
réservoir d'eau traitée de 700 m3 sont communs entre
les deux tranches.
Au niveau de cette station on trouve un laboratoire d'un
équipement moderne qui lui permet de procéder à la
détermination de plusieurs paramètres.
Le laboratoire dispose de 3 salles :
V' Une salle pour les analyses physico-chimiques ;
V' Une salle pour les analyses bactériologiques
;
V' Une laverie pour le nettoyage et la
stérilisation du matériel.
2. Station de traitement Ait Massoud :
La station de traitement Ait Massoud est localisée dans
la région de Tadla Azilal, elle a la
capacité de gérer l'alimentation en eau potable des
populations de la Plaine de Tadla et le
Plateau de Phosphates.

8
Projet de fin d'études
2018/2019
Figure 2 : Station de traitement d'Ait
Massoud
Cette station est composée de plusieurs ouvrages :
V' Ouvrage d'arrivée d'eau brute ;
V' Mélangeur répartiteur ;
V' Débourbeur ;
V' Ouvrage de mélange rapide ;
V' Décanteurs ;
V' Filtres ;
V' Réservoir d'eau traitée 15000 m3 ;
V' Réservoir d'eau industrielle 15000 m3 ;
V' Pompage eau de lavage ;
V' Décanteur eau de lavage ;
V' Bâche de collecte des boues ;
V' Epaississeur ;
V' Lits de séchage ;
V' Bâtiment de réactifs ;
V' Bâtiment de chlore ;
V' Bâtiment d'exploitation ;
9
Projet de fin d'études
2018/2019
y' Poste de transformation ;
y' Station de déminéralisation phase 1 ;
y' Station de déminéralisation phase 2. (23)
3. Traitements des eaux :
Les deux stations (Béni-Mellal et Ait Massoud)
possèdent les mêmes étapes de traitement
pour rendre l'eau potable, ces traitements passent par deux
étapes :
3.1 Prétraitement de l'eau brute :
Le prétraitement de l'eau brute s'effectue quand les
matières en suspension sont comprises entre 2 g/l et 50 g/l. Il comporte
les opérations suivantes :
Ø Le dégrillage :
Le dégrillage permet de protéger les ouvrages
contre l'arrivée de gros objets et de séparer facilement les
matières volumineuses charriées par l'eau brute.

Figure 3 : Le dégrillage
Ø Le dessablage :
Le dessablage a pour but d'éviter le colmatage des canaux
au cours de l'acheminement de l'eau (conservation des particules de
granulométrie supérieure à 200 um).

Figure 4 : Le dessablage
Ø Le débourbage :
10
Projet de fin d'études
2018/2019
Le débourbage permet d'éliminer la majorité
des matières en suspension, d'assurer leur évacuation sous forme
de boues et de fournir à l'étape de décantation principale
une eau acceptable.

Figure 5 : Le débourbage
Ø L'aération :
L'aération a pour but premièrement d'introduire
l'oxygène dans l'eau pour assurer l'oxydation de certains corps
réducteurs tels que le Fer et le Manganèse, deuxièmement
d'éliminer quelques substances volatiles, les gaz en excès (O2,
CO2) et des composés organiques responsables des gouts et odeurs.
(23)
3.2 Traitement de l'eau prétraitée
(technique de JAR-TEST) :
Ce traitement a pour but d'éliminer la pollution chimique
et microbiologique et aussi d'abaisser la turbidité par une série
de transformations afin d'obtenir une eau potable peut être
consommée. Pour effectuer ce traitement on utilise la technique de
JAR-TEST :
Principe : La détermination du taux de
coagulant est effectuée d'un essai expérimental qui consiste
à mettre des doses croissantes de coagulants dont des récipients
contenant la même eau brute. Après quelques instants, on
procède sur l'eau décantée à toutes les mesures
utiles à la qualité de l'eau.
Matériels : - Un floculateur avec six
agitateurs à hélices entrainés par un moteur
électrique à vitesse variable.
- Six béchers de 1 litre.
Réactifs : -Solution du sulfate d'alumine
(coagulant) : Al2(SO4)3 , 18H2O -Solution d'alginate de sodium ou
poly-électrolytes de 1g/l (floculant). (23)

11
Projet de fin d'études
2018/2019
Figure 6 : Floculateur pour Jar-Test
Les principales étapes du traitement sont :
Ø La Pré-chloration :
La pré-chloration consiste à mettre du
chlore gazeux sous forme Cl2 dans l'eau ; elle a pour but d'oxyder les
composés minéraux, d'éliminer les gouts et les odeurs,
inhiber la croissance algale et améliorer la coagulation et la
floculation.
Ø La coagulation-floculation
:
La coagulation : C'est la déstabilisation des
particules colloïdales par élimination de leurs charges
électriques, afin de faciliter leur agglomération.
Les réactifs employés comme coagulants sont :
o Le sulfate d'alumine : Al2(SO4)3 , 18H2O
o Le chlorure ferrique : FeCl3
La floculation : L'agglomérat doit être
d'une taille satisfaisante pour sédimenter dans le bassin, puisque la
taille des flocs déjà formés au cours de la coagulation
n'est pas suffisante, on injecte un floculant accompagné d'une agitation
lente. On utilise comme floculant :
o Les polymères
o L'alginate
Ø
12
Projet de fin d'études
2018/2019
La décantation :
La décantation c'est la sédimentation des
particules solides (flocs) dans un liquide sous l'action de la pesanteur,
basée sur la différence de densité de particules.
Ø La filtration :
C'est la filtration à sables, ce type de filtration
consiste à faire passer l'eau à travers un milieu poreux
constitué d'un matériau granulaire afin d'éliminer les
MES.
Ø La désinfection :
C'est l'état final à la station de traitement, elle
est visant à éliminer les microorganismes pathogènes de
l'eau. Pour les désinfectants on peut citer :
o L'ozone
o Le Dioxyde de chlore
o Le Rayonnement UV (23)
La station de Béni-Mellal possède un traitement
exceptionnel qui est le traitement par charbon actif granulé
(CAG) qui peut être utilisé dans des
procédés de filtration rapide utilisant des filtres à
gravité, de filtration lente utilisant des filtres à sable.

Figure 7 : Le CAG
L'affinage de l'eau au moyen de CAG
améliore la qualité en éliminant :
V' Les composés à l'origine des gouts et des odeurs
V' Les pesticides
V' La couleur
V' Les toxines algales
ü
13
Projet de fin d'études
2018/2019
Les résidus médicamenteux et les résidus de
tous nos produits du quotidien.
Le traitement de l'eau potable nécessite l'utilisation
d'un charbon actif en grain dont la structure poreuse permet l'adsorption de
cette large gamme de composés.
III. L'eutrophisation :
1. Définition :
Eutrophe : du grec Eu : «
bien, vrai », Trophein, Trophus : « nourrir
».
L'eutrophisation est la modification mais aussi la
dégradation d'un milieu aquatique, lié en général
à un apport exagéré de substances nutritives, notamment le
phosphore (que l'on retrouve dans les lessives par exemple) qui augmente la
production d'algues et de plantes aquatiques. (4)

Figure 8 : L'eutrophisation au niveau de la
rivière Ramapo (New Jersey)
En dessous de 4 mg d'oxygène par litre, la vie devient
difficile pour la faune et la flore car les bactéries du milieu
consomment l'oxygène dissous dans l'eau. Pour résoudre ce
phénomène, il suffit de ré-oxygéner les eaux de
couches profondes. Pour cela il est possible de brasser l'eau ou de propulser
régulièrement par des canaux de l'oxygène pour permettre
à la faune de survivre. (4)
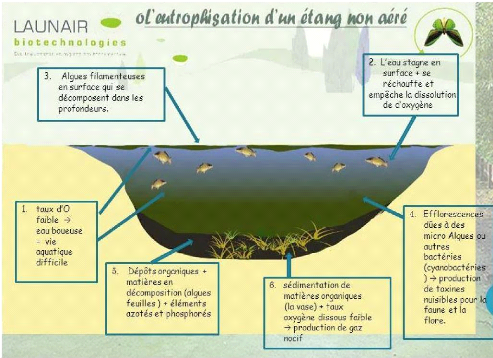
Figure 9 : Schéma expliquant le
phénomène de l'eutrophisation
2. Cause :
L'apparition du phénomène de l'Eutrophisation est
due à des causes Naturelles et Artificielles :
i. Causes Naturelles :
v Températures :
Plus il fait chaud, moins l'oxygène est introduit dans le
milieu ce qui provoque le phénomène d'eutrophisation. Cela
entraine donc le développement d'algues en surface du plan d'eau.
v Luminosité :
La lumière permet la photosynthèse des algues ce
qui favorise leur développement.
v Désoxygénation :
Sans brassage du milieu aquatique, l'oxygène n'est pas
renouvelé. L'eau est eutrophile.
14
Projet de fin d'études
2018/2019
ii. Causes artificielles :
v Les eaux ménagères contenant :
détergents, savons, lessives (...) sont en partie responsables de
l'eutrophisation.
v Les eaux agricoles contenant : fumier, engrais (...)
sont riches en matières organiques azotées dont certains
composés peuvent être solubilisés dans les eaux pluviales
et se retrouvent dans les plans d'eau. (4)
3. Milieux touchés :
L'eutrophisation peut attendre :
- Les eaux douces, saumâtres et salées
- Les milieux marins comme les milieux continentaux
- Les eaux profonds comme les eaux superficielles : dormante
(mares riches en
feuilles mortes ou collectant des eaux usées, des eaux
polluées par des engrais,
étangs, lacs...)

Figure 10 : Effet de l'eutrophisation sur la
population aquatique
- Les cours d'eau de débit faible ou accueillant des
effluants trop riches (issus d'exploitations agricoles, humaines ou
industrielles)
- Les estuaires, golfes, baies et autres étendues
semi-fermées sont particulièrement touchées car elles sont
situées en aval des bassins versants. (4)
4. Les remèdes contre l'eutrophisation
:
Pour combattre ce phénomène, il faut suivre des
remèdes, parmi eux :
- Diminuer l'utilisation de polluants
- Diminution de l'utilisation des engrais en agriculture
15
Projet de fin d'études
2018/2019
- Diminuer l'utilisation de pesticides afin d'éviter
qu'ils ne polluent les eaux
- Remplacer les phosphates des lessives par des agents
anticalcaires sans impact sur l'environnement
- Augmenter les capacités d'infiltration des sols pour
retenir les nutriments et éviter que les eaux ruisselantes (pluies) ne
les entrainent dans les cours d'eaux
- Mise en place de turbines favorisant l'oxygénation des
eaux. (4)
16
Projet de fin d'études
2018/2019
17
Projet de fin d'études
2018/2019
Partie II :Matériel et méthodes
18
Projet de fin d'études
2018/2019
I. Contrôle de la qualité des eaux :
L'eau subit une série d'analyses afin d'assurer une bonne
qualité avant sa distribution au consommateur.
1. Analyses physico-chimiques :
1.1 Mesure de la turbidité :
La turbidité désigne la teneur d'une eau en
particules suspendues qui la troublent. On mesure la turbidité en
unités de turbidité néphalométrique (NTU) à
l'aide d'un turbidimètre qui envoie un rayon de lumière à
travers un échantillon d'eau et mesure la quantité de
lumière qui passe à travers l'eau par rapport à la
quantité de lumière qui est réfléchie par les
particules dans l'eau. On place la cuve remplie par l'échantillon d'eau
dans le turbidimètre et on lise le résultat. (12)

Figure 11 : Turbidimètre
1.2 Mesure de la conductivité :
La plupart des matières dissoutes dans l'eau se trouvent
sous forme d'ions, la mesure de la conductivité permet donc
d'apprécier la quantité de sels dissous dans l'eau
c'est-à-dire sa capacité à conduire le courant grâce
à un appareil électronique qui est le conductimètre en
faisant entrer leur électrode dans un bécher remplie d'eau, et
lisant le résultat à une
température constante de 20 à 25°C. Cette
conductivité, notée ó et exprimée en micro-siemens
par centimètre (uS.cm-1). (23)

Figure 12 : Conductimètre
1.3 Potentiel d'Hydrogène (pH) :
C'est un indicateur de l'acidité ou de l'alcalinité
de l'eau, lié à la nature géologique des terrains
traversés. Les valeurs normales sont comprises entre 6,5 et 8,5.
L'eau qui possède un pH inférieure à 6,5
peut favoriser la corrosion des canalisations et donc la dissolution dans l'eau
potable de métaux comme le plomb et le cadmium.
L'eau qui possède un pH supérieure à 8,5
peut favoriser le risque d'entartage et de mauvaise efficacité du
chlore. La mesure de pH a été réalisée par un
pH-mètre. (23)
19
Projet de fin d'études
2018/2019

20
Projet de fin d'études
2018/2019
Figure 13 : pH mètre
1.4 L'oxydabilité :
L'oxydation des matières organiques et des substances
oxydables est mesurée par le permanganate de potassium (KmnO4)
après 13 minutes en milieu acide à chaud, elle doit être
inférieure ou égale à 5 mg/l en oxygène. Son
augmentation indique une contamination par la matière organique de
l'eau.
v Mode opératoire :
- Prélever 100 ml de l'échantillon à
analyser dans un ballon rodé de 250 ml
- Ajouter 2 ml d'acide sulfurique (H2SO4) concentré
- Ajouter 10 ml de permanganate de potassium (KmnO4) N/100
- Relier le ballon rodé à un
réfrigérant et porter à ébullition pendant
exactement
13 minutes
- Après ces 13 minutes retirer du bain marie et ajouter
10 ml d'oxalate de
sodium (Na2C2O4) N/100
- Titrer après décoloration par le permanganate de
potassium (KmnO4) pendant
que la solution et encore chaude
- Le point équivalent correspond à une couleur
rose persistante pendant environ
30 secondes. (23)

21
Projet de fin d'études
2018/2019
Figure 14 : Le point équivalent
(Oxydabilité)
1.5 Titre alcalimétrique complet (TAC) :
Le TAC correspond à la neutralisation par un acide fort
des ions hydroxydes, carbonates et hydrogénocarbonates en
présence d'un indicateur coloré, c'est-à-dire
neutralisation de toutes les espèces basiques présentes.
v Mode opératoire :
- Introduire 100 ml de l'échantillon dans un erlen de 250
ml
- Ajouter 2 à 3 gouttes de l'indicateur coloré
Hélianthine.
- On obtient une coloration jaune.
- On dose à l'aide de HCl N/10.
- Le point équivalent correspond à un changement
de couleur en orange. (23)

Figure 15 : Le point équivalent
(TAC)
22
Projet de fin d'études
2018/2019
1.6 La dureté calcique (TH-Calcium) :
C'est la détermination de la concentration en ions
calcium.
v Mode opératoire :
- Introduire 100 ml de l'échantillon dans un erlen de 250
ml - Ajouter 5 ml de la solution d'hydroxyde de sodium (NaOH) 2M - Ajouter un
peu d'indicateur Calcon : La solution devient rose. - Titrer à l'aide
d'une solution complexométrique EDTA 0.02M. - Le point équivalent
correspond à un virage au bleu royale. (23)

Figure 16 : Le point équivalent
(TH-Calcium)
1.7 Nitrate :
Les nitrates sont presque quantitativement réduits en
nitrites sur une colonne contenant du cadmium recouvert de noir de cuivre
après traitement au sulfate du cuivre. Les nitrites produits forment
avec l'acide sulfanilique un composé diazoïque lequel couplé
avec N-(1-Naphtyle) éthylènediamine donne une coloration rose
caractéristique dont l'intensité de la coloration, mesurée
à 540 nm, est proportionnelle à la concentration initiale en
nitrates+nitrites présents dans l'échantillon
v Mode opératoire :
- Mettre 1 ml de l'échantillon dans un flacon de 50 ml et
ajouter 49 ml de l'eau
distillé.
- Ajouter 1.25 ml de la solution tampon concentrée.
- Mélanger et percoler l'échantillon à
travers la colonne à un débit de 7 à 10
ml/min.
- Jeter les 25 ml du l'éluât et
récupérer le reste dans le flacon original.
- Ajouter 1 ml de l'acide sulfanilique à la solution
originale et attendre de 2 à 8 minutes.
- Ajouter 1 ml de NED et mélanger la solution.

Figure 17 : Spectrophotomètre
Figure 18 : Colonne contenant du cadmium
- Mesurer l'absorbance de l'échantillon avec un
spectrophotomètre à une longueur d'onde à 540 nm. (23)
23
Projet de fin d'études
2018/2019
24
Projet de fin d'études
2018/2019
1.8 Sulfate :
L'ion sulfate est précipité dans de l'acide
chlorhydrique contenant du chlorure de baryum d'une manière telle qu'il
se forme des cristaux de sulfates de baryum de taille uniforme.
La turbidité ou l'absorbance de la suspension du sulfate
de baryum est mesuré en néphélométrie ou par
transmission au spectrophotomètre à la longueur d'onde 420 nm.
v Mode opératoire :
- Mettre 100 ml de l'échantillon dans un erlen
- Ajouter exactement 5 ml du réactif à l'acide
chlorhydrique, mettre l'agitation.
- Tout en maintenant l'agitation, ajouter une spatule du
chlorure de baryum et agiter à vitesse constante pendant exactement 1
minute.
- Remplir immédiatement la cuve de
spectrophotomètre et mesurer la turbidité après 30
secondes. (23)
1.9 Chlorure :
La teneur en chlorures des eaux naturelles est très
variable. Dans les terrains ne contenant pas en proportion importante de
chlorure de sodium (sel de cuisine), elle peut atteindre 50 à 90 mg/L,
mais ce chiffre peut être très largement dépassé
(jusqu'à 900 mg/L) dans les zones contenant de sel de sodium (cas des
eaux superficielles) ou dans le cas des invasions des eaux marins (cas des eaux
souterraines).
Les chlorures sont dosés, en milieu acide par le nitrate
mercurique en présence de diphénylcarbazone ou
diphénylcarbazide.
v Mode opératoire :
- Mettre 100 ml de l'échantillon dans un erlen
- Ajouter environ 0,5 ml de l'indicateur pH (8 gouttes), puis
agiter
- Ajouter de l'acide nitrique (N/3) goutte à goutte
jusqu'à obtention d'une couleur
jaune foncée, rajouter en plus 2 gouttes d'acide nitrique
N/3
- Titrer au nitrate mercurique jusqu'à apparition de la
première teinte violette.(23)

25
Projet de fin d'études
2018/2019
Figure 19 : Point équivalent
(Chlorure)
2. Analyses bactériologiques/biologiques :
2.1 Echantillonnages :
Les échantillons analysés sont des eaux prises
dans des flacons de 500 ml, prélevées au
niveau de différents points (source Ain Asserdoun, l'ONEP
de Ain Asserdoun, barrage Ait
Massoud et l'ONEE de Khouribga).
Les échantillons doivent être
prélevés dans des récipients stériles afin
d'éviter toute
contamination accidentelle sont transportés au laboratoire
et analysés dans un délai ne
dépassant pas 24 heures.
Avant de commencer le travail préparatoire, il faut tout
d'abord :
- Vérifier la température des salles du
laboratoire.
- Préparer et conserver les milieux déjà
préparés.
- Démarrer le distillateur pour préparer l'eau
distillée.
- Stériliser les matériels du travail par chaleur
(autoclave, flambage).
2.2 Bactéries recherchées :
Les bactéries recherchées dans une eau
destinée à la consommation humaine sont :
· Coliformes totaux :
Les coliformes totaux sont des entérobactéries qui
vivent en général dans l'environnement (sol,
végétation et eau). Ces bactéries sont utilisées
comme indicateur de la qualité microbienne de l'eau. Ce genre
bactérien est en forme de bâtonnets, aérobies ou
anaérobies facultatives, peut résister à une
température de 36°C #177; 2°C.

26
Projet de fin d'études
2018/2019
Figure 20 : Bactéries Coliformes totaux
(5000×)
· Coliformes fécaux :
Les coliformes fécaux sont des thermo
tolérants, sous-groupe des coliformes totaux, capables de fermenter le
lactose à une température de 44°C #177; 2°C. Le
principal genre inclus dans ce groupe est Escherichia coui.

Figure 21 : Bactéries Coliformes
fécaux (21000×)
· Entérocoques intestinaux :
Ce sont des bactéries utilisées comme indicateur
de pollution, capables de résister à une température de
36°C #177; 2°C et dans des conditions environnementales difficiles et
persistent plus longtemps dans l'eau.

Figure 22 : Bactéries
entérocoques intestinaux (10000×)
·
27
Projet de fin d'études
2018/2019
Streptocoques fécaux :
Les streptocoques fécaux sont d'une forme sphérique
ou coccoide. C'est un genre qui constitue un bon indice de contamination
fécale ancienne par contre les coliformes fécaux (contamination
récente). Ils sont capables de croitre à 37°C.

Figure 23 : Bactéries streptocoques
fécaux (30000×)
2.3 Techniques d'analyses :
La situation de l'eau présente un risque de contamination
par des bactéries pathogènes (Coliformes, Escherichia
coui...), pour cette raison on fait des analyses basées sur deux
techniques pour détecter ces micro-organismes présents dans l'eau
traitée et l'eau brute. a. Filtration sur membrane (Eau
Traitée) :
v Principe de la méthode :
On procède à une filtration par un appareil de
filtration sur membrane. La membrane est en esters de cellulose, de
porosité 0.45 um, susceptible de retenir les bactéries (Rodier et
al, 1997). Un échantillon de 100 ml d'eau est filtré sur cette
membrane, cette dernière est déposée à la surface
d'un milieu gélosé. Après incubation, on compte le nombre
de colonies.

Figure 24 : Système de filtration sur
membrane
v Matériel utilisé :
· Matériels de stérilisation (autoclave,
four)
· Système de filtration sur membrane
· Etuve ou enceinte thermo statée 37°C #177;
1
· Gélose au « Tergitol » 7 et «
Slanetz et Bartley » (annexe 4, planche photos 1)
· Matériel de microbiologie : boites de pétri
stériles, pipettes 1 ml (usage unique), flacons stériles.

Figure 25 : Autoclave
v Protocol expérimental :
· Nettoyer le robinet avec un tissu propre,
stériliser à la flamme l'embouchure du robinet et laisser couler
l'eau pendant 1 à 2 min.
· Préparer une zone stérile puis placer
autour du bec Bunsen les boites de pétri avec gélose au Tergitol
7 et les pipettes stériles.
· Placer la membrane stérile sur le
système de filtration.
· Mettre en place la pompe à vide.
· Agiter le flacon vigoureusement.
· Verser 100 ml d'échantillon d'eau et filtrer en
aspirant avec la pompe à
28
Projet de fin d'études
2018/2019
29
Projet de fin d'études
2018/2019
vide.
· En zone stérile, ouvrire le système de
filtration et retirer la membrane avec une pince stérile.
· Mise en culture en déposant la membrane sur la
gélose, les éléments nutritifs de ce dernier traversent la
membrane, ce qui permet le développement des bactéries en
surface.
· Incuber les boites à l'étuve à 37
°C pendant 24 jusqu'à 48h pour la recherche de coliformes. Pour la
recherche de coliformes thermo tolérants, placer les boites à 44
°C pendant 24h.
b. La méthode de NPP (Eau Brute) :
v Principe de la méthode :
La méthode du nombre le plus probable est une estimation
statistique du nombre de micro-organismes qu'on peut trouver dans l'eau d'une
manière aléatoire, elle est applicable sur les eaux brutes ayant
une teneur plus ou moins élevée en MES, elle consiste à
ensemencer trois milieux de culture par dilution, les tubes
ensemencés contiennent un milieu nutritif, milieu Lauryl pour les
coliformes avec introduction de cloche de Durham dans ce dernier, après
incubation on compte le nombre des tubes positifs (dégagement de gaz,
trouble, changement de couleur) pour chaque dilution et on fait la lecture du
NPP correspondant en utilisant la table de Mac Grady. Il s'agit d'une
méthode quantique et non pas énumératif. (23)
v Matériel utilisé :
· 3 tubes contenant 9 ml de diluant (eau
distillée).
· 3 pipettes stériles en plastique de 1 ml.
· Bec bunsen pour garder la stérilité de la
zone de travail.
· 1 vortex.
v Protocole expérimentale :
Ø Coliformes totaux et fécaux :
TEST PRESOMPTIF :
· Stérilisation de la zone de travail
· Ensemencement :
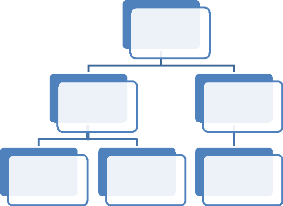
1 ml
0,1 ml
10 ml
Simple
concentration
Double
concentration
Buillon
Lauryl sulfate
de tryptose
30
Projet de fin d'études
2018/2019
Figure 26 : Schéma désignant
l'ensemencement de l'échantillon à 3 différentes
dilutions
recherchant les coliformes totaux et fécaux. (Annexe 4,
planche photos 1).
· Incubation : à 37°C#177; 1°C pendant
48h
· Dénombrer les tubes positifs : trouble + gaz
· Repiquer les tubes positifs sur les milieux confirmatifs
: BEA.
TEST CONFIRMATIF : (annexe 4, planche photos
1)
Coliformes totaux Coliformes fécaux
Ensemencement des tubes positifs
Vert brillant EC medium
Incubation
37°C #177; 1°C/48h 44°C#177; 0,5°C/24h
·
31
Projet de fin d'études
2018/2019
Dénombrement des tubes positifs : trouble + gaz
· Choix du triplet ? lecture-table de Mac Grady? NPP/100
ml.
Ø Streptocoques fécaux :
TEST PRESOMPTIF :
· Stérilisation de la zone de travail
· Ensemencement :

0,1 ml
Simple
concentration
1 ml
Buillon glucosé à l'azide de sodium
Double
concentration
10 ml
Figure 27 : Schéma désignant
l'ensemencement de l'échantillon à 3 différentes
dilutions
recherchant les streptocoques fécaux. (Annexe 4, planche
photos 2).
· Incubation : à 37°C#177; 1°C pendant
48h
· Dénombrer les tubes positifs : trouble et/ou
dépôt
· Repiquer les tubes positifs sur les milieux confirmatifs
: Litsky
TEST CONFIRMATIF :
· Dénombrer les tubes positifs : trouble +
pastille violette éventuellement au fond du tube
· Choix du triplet ? lecture-table de Mac Grady? NPP/100
ml (annexe 3).
32
Projet de fin d'études
2018/2019
c. Incorporation en gélose (Eau traitée
et brute) :
v Principe de la méthode :
Ensemencement en profondeur d'une gélose nutritive non
sélective dans des boites de Pétri, par incorporation d'un ml
d'échantillon initial ou de dilution de celui-ci. (23)
v Matériel utilisé :
· Bain-marie à 47 #177; 1 °C
· Gélose à l'extrait de levure
· Petit matériel stérile à usage
unique : boite de pétri de 90 mm de diamètre, pipettes
individuelles de 2 ml.
v Protocole expérimental :
· Faire fondre au bain-marie la gélose à
l'extrait de levure
· Maintenir la gélose liquide dans un bain-marie
à 47 #177; 1°C
· Ensemencer 1 ml d'échantillon par boite de
Pétri puis ajouter 15 à 20 ml de gélose

Figure 28 : Ensemencement sur gélose
à l'extrait de levure
· Incubation :
? À 22 #177; 2°C/ 68 #177; 4h
? À 36 #177; 2°C/ 44 #177; 4h
· Dénombrement des boites entre 30 et 300 colonies
(nombre de colonies en UFC/ml).
33
Projet de fin d'études
2018/2019
Partie III : Résultats et discussions
34
Projet de fin d'études
2018/2019
I. Résultats des paramètres physico-chimiques
:
1. La turbidité :
La figure suivante illustre les résultats de la
turbidité des eaux de Beni Mellal en comparaison avec les eaux de
Khouribga :
Turbidité (NTU)
|
9 8 7 6
|
|
|
|
|
|
|
|
|
5 4 3 2 1 0
|
|
|
|
|
|
Khouribga Beni Mellal
|
|
|
|
|
|
|
|
|
E.B E.T
Figure 29 : Mesure de la turbidité de
l'eau brute et l'eau traitée
La comparaison entre l'eau de Khouribga et de
Béni-Mellal montre que la turbidité de ce dernier est
inférieure à celle de Khouribga.
La turbidité de l'eau de Béni-Mellal est
conforme aux normes (<5 NTU) avant traitement et après traitement.
Concernant l'eau de Khouribga, la turbidité de l'eau brute est
supérieure à celle de l'eau traitée, ce qui
témoigne de l'efficacité des phases de traitements des eaux dans
la station de traitement (voir annexe 2) (Rodier, et al, 2015).
2. La conductivité :
La figure suivante montre la conductivité pour chacun des
eaux de Beni Mellal en comparaison avec les eaux de Khouribga :
1800
1600
Conductivité
(uS/cm)
1400
1200
1000
800
Khouribga Beni Mellal
600 400 200 0
E.B E.T
35
Projet de fin d'études
2018/2019
Figure 30 : Mesure de la conductivité
de l'eau brute et l'eau traitée
La conductivité de l'eau de Khouribga est
supérieure à celle de Béni-Mellal.
Pour l'eau de Béni-Mellal (Brute et Traitée), sa
conductivité est conforme aux normes (<2700 uS/cm), concernant la
conductivité de l'eau de Khouribga (Brute et Traitée) reste
conforme aux normes (<2700 uS/cm) (voir annexe 1 et 2) (MDCEau, 2015).
|
3. Le potentiel hydrique (pH)
|
:
|
Les résultats de la mesure de pH sont illustrés
dans la figure suivante :
|
pH
|
7,8 7,7 7,6 7,5 7,4
|
|
|
|
|
7,3
7,2
7,1
7
6,9
6,8
|
Khouribga Beni Mellal
|
|
|
|
E.B E.T
Figure 31 : Mesure de pH de l'eau brute et
l'eau traitée
36
Projet de fin d'études
2018/2019
Les valeurs de pH enregistrés pour les échantillons
de Khouribga sont respectivement pour l'eau Brute et l'eau Traitée :
7.66 et 7.52. Les valeurs de pH pour l'eau de Béni- Mellal Brute et
Traitée sont respectivement : 7.3 et 7.1.
Ces valeurs presque neutres peuvent être expliquées
par l'ajout de Sulfate d'Alumine dans l'étape de
pré-chloration.
Généralement, le pH de tous les échantillons
restent conformes aux normes marocaines (6.5 = pH = 8.5) (voir annexe 1).
4. L'oxydabilité :
Les résultats de l'oxydabilité sont
représentés sur la figure ci-dessous :
|
Oxydabilité (mg/l)
|
3,5
3
2,5
|
|
|
|
|
|
|
|
|
2
1,5
1
0,5
0
|
|
Khouribga Beni Mellal
|
|
|
|
|
|
|
|
E.B E.T
Figure 32 : Mesure de l'oxydabilité de
l'eau brute et l'eau traitée
Pour l'eau de Khouribga les résultats montrent que la
valeur de l'oxydabilité de l'eau Brute est supérieure à
celle de l'eau Traitée.
Pour l'eau de Béni-Mellal, la valeur de
l'oxydabilité de l'eau Brute est presque identique à celle de
l'eau Traitée (voir annexe 2).
L'augmentation de l'oxydabilité dans le cas de l'eau Brute
de Khouribga, on peut la considérer comme une indication de
contamination par la matière organique (végétaux en
décomposition, bactéries...).
Tableau 1 : Résultats des
paramètres physico-chimiques de l'eau de Beni Mellal
|
Paramètres
|
Eau brute
|
Eau traitée
|
|
Ammonium (mg/l)
|
0.054
|
0
|
|
Chlorures (mg/l)
|
252.05
|
142
|
|
Dureté (°F)
|
11
|
13.4
|
|
Nitrates (mg/l)
|
0.098
|
0.025
|
|
Nitrites (mg/l)
|
0.056
|
0.045
|
|
Sulfates (mg/l)
|
0.08
|
0.18
|
|
TA (°F)
|
0
|
0
|
|
TAC (°F)
|
23.9
|
22.71
|
|
Température (°C)
|
18.2
|
16
|
Les résultats illustrés dans le tableau
au-dessous montrent une conformité des paramètres
physico-chimiques aux normes marocaines ce qui rend l'eau consommable par
l'être vivant.
II. Résultats des paramètres organoleptiques
:
Tableau 2 : Résultats des
analyses organoleptiques de l'eau de Khouribga
|
Paramètres
|
Eau brute
|
Eau traitée(CAG)
|
|
Seuil de goût
|
1.5
|
0
|
|
Seuil d'odeur
|
0.2
|
0
|
Ce tableau montre les résultats d'analyse organoleptique
des eaux. Après un traitement par le CAG ; Le seuil du gout et de
l'odeur a devenu nul, et dans ce cas-là, la qualité de l'eau de
Khouribga est perfectionnée.
37
Projet de fin d'études
2018/2019
III. Résultats d'analyses bactériologiques
:
Tableau 3 : Résultats des
analyses bactériologiques des eaux naturelles
Nombre des tubes positifs
Test Présomptif Test Confirmatif
|
EAU DE BENI
MELLAL
|
Volume ensemencé (ml)
|
0.1
|
1
|
10
|
0.1
|
1
|
10
|
NPP
|
|
Coliformes totaux
|
2
|
0
|
0
|
1
|
1
|
0
|
9
|
|
Streptocoques fécaux
|
1
|
2
|
0
|
1
|
0
|
0
|
11
|
|
EAU DE
KHOURIBGA
|
Coliformes totaux
|
3
|
2
|
1
|
2
|
2
|
0
|
150
|
|
Streptocoques fécaux
|
2
|
2
|
1
|
2
|
1
|
0
|
28
|
Le nombre le plus probable pour les germes recherchés (CT
et SF) pour l'eau de Béni-
Mellal sont respectivement 9 et 11. Pour l'eau de Khouribga les
germes recherchés (CT et SF) sont 150 et 28 (voir tableau de Mac Grady
sur annexe 3).
Ce résultat montre que l'eau Brute de Khouribga est assez
polluée que l'eau de Béni-Mellal de point de vue
bactériologique à cause des micro-organismes qui
témoignent une contamination fécale.
Tableau 4 : Résultats des
analyses bactériologiques des eaux traitées
|
Bactéries recherchées
|
Nombre de bactéries
trouvées
(UFC/100mL)
|
|
EAU DE BENI
MELLAL
|
Coliformes Totaux
|
0
|
|
Entérocoques Intestinaux
|
0
|
|
Escherichia Coli
|
0
|
|
EAU DE
KHOURIBGA
|
Coliformes Totaux
|
0
|
|
Entérocoques Intestinaux
|
0
|
|
Escherichia Coli
|
0
|
38
Projet de fin d'études
2018/2019
Pour l'eau traitée, on remarque qu'il n'y a aucune
contamination pour les eaux de Khouribga et ainsi que Béni-Mellal. Ces
résultats sont une indication de la potabilité de l'eau.
Tableau 5 : Résultats de la
recherche des micro-organismes révivifiables
Nombre des micro-organismes révivifiables
UFC/100mL
Beni Mellal
Khouribga
Eau Brute
Eau Traitée
2
0
5
0
Le tableau ci-dessus montre qu'il y a une présence des
micro-organismes révivifiables dans l'eau brute des deux villes
(Khouribga et Beni Mellal), le résultat de dénombrement de ces
micro-organismes a donné des valeurs qui n'ont pas
dépassées les normes.
D'après les résultats obtenus on a remarqué
que la qualité des eaux de Khouribga diffère à celle de
Beni Mellal en termes de plusieurs paramètres physico-chimiques tels que
la turbidité, l'oxydabilité, la conductivité,
l'oxygène dissous. Dans le cas de la ville de Beni Mellal ces
paramètres physico-chimiques sont conformes aux normes marocaines, ce
qui signifie que l'eau de Beni Mellal soit brute ou traitée est d'une
excellente qualité ; Ainsi que la qualité
bactériologique.
Ce qui concerne le cas de Khouribga, certains paramètres
ont devenus conformes aux normes marocaines de l'eau potable après
traitement par le charbon actif granulé (CAG) ; Dans le cas de
l'amélioration des paramètres physico-chimiques, la valeur de la
turbidité, la conductivité et l'oxydabilité a connu une
diminution observable grâce à l'influence du CAG.
39
Projet de fin d'études
2018/2019
Conclusion
40
Projet de fin d'études
2018/2019
Pour éviter un risque sanitaire à cause de la
consommation d'une eau poluée, l'eau doit subir un traitement pour la
rendre potable. L'office national de l'eau potable (ONEE), joue un rôle
détérminant dans ce sens, il a pour objet de faire passer l'eau
à travers un ensemble de traitements dans laquelle plusieurs
étapes sont mises en oeuvre pour éliminer d'abord la
matière en suspension à l'aide d'un procédés
physico-chimiques, puis éliminer les micro-organismes par le
procédé de désinfection.
Après le suivi des paramètres physico-chimiques
(turbidité, conductivité, pH, oxydabilité...) au sein de
laboratoire de l'ONEE on a constaté que ces paramètres sont
conformes aux normes pour l'eau de la source d'ain Asserdoune. Pour l'eau du
barrage d'Aït Massoud, ces paramètres sont convenables aux normes
marocaines sauf la turbidité de l'eau brute qui dépasse la norme,
cette dernière après des traitements successives devient conforme
à la norme marocaine.
L'eau de Khouribga montre des paramètres
organoleptiques (odeur, gout) inconvenables aux normes, après un
traitement par l'addition de charbon actif granulé (CAG), elles ont
été améliorés. Ainsi, le seuil de goût
était 1,5 pour l'eau brute, alors qu'après le traitement par le
CAG devient nul. Pour l'odeur, il a été d'une valeur de 0,2 pour
l'eau brute est devenue nul après le même traitement. Nous
recommandons alors le traitement par le CAG les eaux du barrage d'Ait
Massoud.
Pour les paramètres bactériologiques,
l'échantillon d'eau brute du barrage Aït Massoud (150 coliformes
totaux/ 100 ml et 28 streptocoques fécaux/ 100 ml) présentent une
contamination plus grande que les eaux de Ain Asserdoune (9 coliformes totaux/
100 ml et 11 stréptocoques fécaux /100 ml), après un
traitement chimique pour l'élimination des germes pathogènes
suite a un processus de chloration, la charge microbiologique s'annule et
devient conforme à la norme marocaine.
41
Projet de fin d'études
2018/2019
42
Projet de fin d'études
2018/2019
Références bibliographiques
43
Projet de fin d'études
2018/2019
Web graphie :
[1].
https://oceanservice.noaa.gov/facts/eutrophication.html
(Consulté le 5/4/2019)
[2].
https://inra-dam-front-resources-cdn.brainsonic.com/ressources/afile/412485-044a1-resource-expertise-eutrophisation-synthese-148-p.pdf
(Consulté le 5/4/2019)
[3].
http://hmf.enseeiht.fr/travaux/CD0102/travaux/optsee/bei/1/g14/pa0202.htm
(Consulté le 5/4/2019)
[4].
https://slideplayer.fr/slide/5201230/
(Consulté le 10/4/2019)
[5].
https://experteau.com/services/analyse-bacteriologique.php
(Consulté le 17/4/2019)
[6].
https://educalingo.com/fr/dic-fr/enterocoque
(Consulté le 17/4/2019)
[7].
http://id.eaufrance.fr/par/5479
(Consulté le 17/4/2019)
[8].
http://aujourdhui.ma/regions/beni-mellal-vers-lapprovisionnement-en-eau-potable-62030
(Consulté le 18/4/2019)
[9].
https://www.portailsudmaroc.com/actualite/3140/barrages-un-taux-de-remplissage-de-578-au-22-aoucirct-2014
(Consulté le 18/4/2019)
[10].
https://www.aquawal.be/fr/null.html?IDC=502z
(Consulté le 22/4/2019)
[11].
https://docplayer.fr/7421938-Examen-bacteriologique-des-aliments-auto-controle-par-les-professionnels.html
(Consulté 22/4/2019)
[12].
https://www.gov.mb.ca/waterstewardship/odw/public
info/fact sheets/pdf/fr/factsheet turbidity fr.pdf (Consulté le
22/4/2019)
[13].
http://eduterre.ens-
lyon.fr/thematiques/hydro/littoral/investigationlittorale/Fiche%20methode%20conductivite.pf
(Consulté le 24/4/2019)
[14].
https://www.benchaabane.com/Baisse-du-debit-de-Ain-Asserdoun
a1056.html (Consulté le 24/4/2019) [15].
https://www.researchgate.net/publication/331000852_Monitoring_And_Analysis_Of_Wa
ter_Levels_Of_Karst_Springs_Case_Of_The_Spring_Of_Ain_Aserdoun_Atlas_Of_Beni_Me
llal Morocco (Consulté 29/4/2019)
[16].
https://www.researchgate.net/publication/321302143
Correlation entre parametres hydr
ogeochimique_et_geoelectrique_pour_evaluation_de_la_qualite_des_eaux_de_la_nappe_phre
atique_de_la_plaine_de_Tadla-Maroc (Consulté 29/4/2019)
[17].
https://hal.archives-ouvertes.fr/hal-01153495
(Consulté le 29/4/2019)
[18].
https://www.alamyimages.fr/photo-image-algues-resultant-de-leutrophisation-la-riviere-ramapo-nord-de-la-pollution-de-leau-new-jersey-86439139.html
(Consulté le 10/5/2019)
Références bibliographiques :
[19]. Imken F. (2016). Les étapes de
traitement des eaux et contrôle de qualité. PFE, Faculté
des Sciences et Techniques FES, 28 p.
[20]. Fadil F. et E. Harki (2017). Suivi de
l'essai de coagulation-floculation (JAR-TEST) de sources de l'eau d'Ain
Asserdoun. PFE, Faculté des Sciences et Techniques de FES, 38 p.
[21]. Khtayari J. et N. Adssaoui (2018).
Analyses de certains paramètres physico-chimiques et
bactériologiques des eaux brutes et traitées de la ville
Béni-Mellal. PFE licence en SV, Faculté polydisciplinaire de
Khouribga, 36 p.
[22]. Hammouchi S. (2008). Dosage par
spéctrophotomètre des dérivés azotés :
NH4+, NO2-, NO3-. PFE, Faculté des
Sciences et Techniques de FES, 44 p.
[23].Documents et archives de l'ONEE/l'ONEP
44
Projet de fin d'études
2018/2019
| 


