|

REPUBLIC OF CAMEROON
**********
REPUBLIQUE DU CAMEROUN
**********
UNIVERSITE DE YAOUNDE I
**********
THE UNIVERSITY OF YAOUNDE I
**********
FACULTÉ DES SCIENCES
**********
FACULTY OF SCIENCE
**********
CENTRE DE RECHERCHE ET DE FORMATION DOCTORALE
**********
POST GRADUATE RESEARCH AND TRAINING PROGRAMME
**********
SCIENCES, TECHNOLOGIE ET GÉOSCIENCES
SCIENCES, TECHNOLOGY AND GEOSCIENCES
DEPARTEMENT DES SCIENCES DE LA TERRE
DEPARTMENT OF EARTH SCIENCES
LABORATOIRE DE GEOSCIENCES DES
FORMATIONS
SUPERFICIELLES ET APPLICATIONS
LABORATORY
OFGEOSCIENCES OF SUPERFICIAL
FORMATIONS AND APPLICATIONS
Mémoire présenté en vue de
l'obtention du Diplôme de Master en Sciences de la Terre
Spécialité : Géosciences des
Formations Superficielles
Option : Sol, Eau, Sciences
Géotechniques
Par
ABARA A BIABAK INDRICK
Matricule : 15I2572
Licencié ès-Sciences
Sous la co-direction de
Dr. NOA TANG-ONANA Sylvie Désirée Dr.
TCHAKAM KAMTCHUENG Brice
Chargée de cours Chargé de recherche
ENS IRGM
i


ii
Je rends grâce à Dieu qui m'a toujours
donné la santé, la force et les moyens de réaliser
ce travail. En effet, cette recherche a été
très laborieuse, tellement laborieuse que, tout seul,
elle aurait été une mission quasiment
impossible. Qu'il me plaise donc d'exprimer toute ma
gratitude et mes très sincères remerciements
à tous ceux qui y ont apporté leur contribution.
Je remercie les docteurs Noa Tang-Onana Sylvie
Désirée et Tchakam Kamtchueng Brice qui, malgré leurs
nombreuses occupations ont bien voulu superviser ce travail, ils ont pris des
risques énormes pour que ce travail soit réalisé.
Puissiez-vous recevoir ici, l'expression de ma sincère et profonde
gratitude.
J'exprime ma profonde gratitude à tous les enseignants
du Département des Sciences de la Terre et de l'Univers de
l'Université de Yaoundé I pour leurs enseignements et conseils,
je pense particulièrement au Chef de Département des Sciences de
la Terre le Pr. Ndjigui Paul-Désiré ; aux professeurs Nzenti Jean
Paul, Kamgang Pierre, Ndam Ngoupayou Jules Rémy, Yongue Fouateu Rose,
Nkoumbou Charles, Medjo Eko Robert, Njilah Issac Konfor, Tchouankoue Jean
Pierre, Temdjim Robert, Yene Atangana Joseph, Bisso Dieudonné, Nyeck
Brunot, Onana Vincent Laurent, Ganno Sylvestre, Abossolo Angue Monique, Ekomane
Emile ; Les docteurs Mouafo Lucas, Ngo Bidjeck Louise Marie, Temga Jean Pierre,
Ngo Belnoun Rose, Eyong John Takem, Ntsama Atangana Jacqueline, Metang Victor,
Anaba Onana Achille, Elisé Sababa.
Un merci spécial au Chef du quartier Mbalmayo de
Dizangué qui nous a autorisé et permis de travailler en toute
sécurité dans le lac. Un merci incommensurable a notre piroguier
qui par son expérience a su faire preuve de professionnalisme en nous
permettant la navigation dans le lac en toute sécurité. Nous
pensons également à notre guide Raimond, qui non seulement nous a
facilité la tâche dans la communication avec les autorités
locales mais aussi en nous montrant notre chemin tout au long de notre
campagne.
J'exprime une reconnaissance particulière à tous
mes aînés académiques, notamment Ekoa Bessa Armel,
Emmachoua Arrah Justine, Bamagalena Lucien, Onana Léandre, Takam Guy
Bertin, Mbita Arnold et Nsangou Daouda pour leurs encouragements, conseils
continus, aides et disponibilités.
iii
Je remercie tous mes camarades de promotion pour tous ces
moments passés dans la convivialité. Je pense en particulier
à : Ambassa Bela Victorine, Aonsi Kamani Francis, Biami Nya Diane,
Tchinang Mbagang Laetitia, Fopa Keunang Brice, Fankou Fankou William, Nguedong
Leonel ; Takam Larissa ; Tchadji Jordan ; Akoumou Sandrine ; Bile Christian
Sony, Belomo Armel, Bahane Catherine, Ngaisso Sotche Raïssa, Djeufo
Rodrigue, Essomba Leonel, et Ndzengué Séraphine, merci pour vos
encouragements, discussions scientifiques et les suggestions apportées
à ce travail.
Je remercie également ma grande famille, mes oncles,
tantes et soeurs en particulier Awono Olivier, Nyebe Lydie, Belomo Coco, Ndiem
A Biabak Chancelle et Kouna A Biabak Audrey, pour leurs soutiens
inconditionnels, intarissables et perpétuels.
Je remercie mes amis Babaka Armand, Dieuhou Nganso Gabin,
DJidere Sadou Ledoux, Ombolo Nyebe Florent, Batomen Gaitana Fallone, Ntema'a
Guilluamy, Bahoken Loick, Seke Paul, et Djouda Ivanov, pour leurs soutiens
incommensurables.

iv
DEDICACE i
REMERCIEMENTS ii
TABLE DES MATIERES iv
LISTE DES FIGURES vii
LISTE DES TABLEAUX ix
LISTE DES SIGLES ET ACRONYMES x
RESUME xi
ABSTRACT xii
INTRODUCTION GENERALE 1
CHAPITRE I : MILIEU NATUREL 4
I.1. CADRE GEOGRAPHIQUE 5
I.1.1. Localisation de la zone d'étude 5
I.1.2. Climat 5
I.1.3. Géomorphologie 7
I.1.3.1. Orographie 7
I.1.3.2. Hydrographie 8
I.1.4. Végétation 9
I.1.5. Sol 10
I.2. CADRE GÉOLOGIQUE 10
I.3. MILIEU HUMAIN ET ACTIVITE ECONOMIQUE 12
CHAPITRE II : MATERIELS ET METHODES 25
II.1. MATERIELS ET TRAVAUX DE TERRAIN 14
II.1.1. Matériels de terrain 14
II.1.2. Travaux de terrain 14
V
II.1.2.1. Échantillonnage de l'eau 14
II.1.2.2. Étiquetage et conservation des
échantillons 17
III.1.2.3. Mesures sur le terrain 18
II.2. TRAVAUX EN LABORATOIRE 19
II.2.1. Dosage des éléments traces
métalliques (Mn, Fe, Cu, Cd, al) 19
II.2.1.1. Matériels et réactifs 19
III.2.1.2. Méthodologie 20
III.2.2. Cas des éléments majeurs et d'autres
éléments chimiques 20
III.2.2.1. Matériels et réactifs 21
III.2.2.2. Méthodologie 21
II.3. QUALITE ET TRAITEMENT DES DONNEES 22
II.3.1. Qualité des données 22
II.3.1.1. Utilisation d'un échantillon de
référence : ERIL 22
II.3.1.2. Balance ionique 23
II.3.2. Traitement des données 23
II.3.2.1. Méthode hydrochimique 23
II.3.2.2. Analyse Statistique Multivariée (ASM) 24
CHAPITRE III : RESULTATS 38
III.1. NIVEAU DE VARIATION DES PARAMÈTRES
PHYSICO-CHIMIQUES DES
EAUX DU LAC MBOLI ET LES EAUX SOUTERRAINES 27
III.1.1. Paramètres physiques 27
III.1.2. Paramètres chimiques 27
III.1.2.1. Éléments traces métalliques 27
III.1.2.2. Cations majeurs et somme des équivalents
cations (TZ+) 28
III.1.2.3. Anions majeurs et somme des équivalents anions
(TZ-) 28
III.1.2.4. Autres éléments en solutions :
(NH4+, PO43-, F-, OD, SiO2) 28
III.1.2.5. Total des solides dissous (TDS) et la balance ionique
(BI) 29
III.1.2.6. Typologie des eaux 30
CHAPITRE IV : ESSAI D'INTERPRETATION ET DISCUSSION
45
V.1. vi
DISTRIBUTION DES PARAMETRES PHYSICO-CHIMIQUES DANS
LES
EAUX ETUDIEES 34
V.1.1. Paramètres physiques 34
V.1.1.1. pH 34
V.1.1.2. Conductivité électrique 36
V.1.1.3. Température 38
V.1.2. Paramètres chimiques 40
V.1.2.1. Éléments traces métalliques 40
1.2.2. Cations majeurs 43
V.1.2.3. Anions majeurs 45
V.1.2.4. Autres éléments en solutions
(NH4+, PO43-, F-) 47
V.1.2.5. Oxygène dissous 49
V.1.2.6. Total des solides dissous (TDS) 50
V.1.2.7. Facies hydrogéochimiques 51
V.2. ORIGINE DES ÉLÉMENTS CHIMIQUES
PRESENTS DANS LES EAUX DU
LAC ET LES EAUX SOUTERRAINES 53
V.2.1. Analyse statistique multi-variée 53
V.2.1.1. Matrice de corrélation 53
V.2.1.2. Analyse en composantes principales 54
V.2.2. Origines et facteurs environnementaux qui contrôlent
la qualité physico-chimique
des eaux du lac et les eaux souterraines étudiées
57
V.2. APTITUDE DES EAUX ETUDIEES A L'IRRIGATION
59
CONCLUSION GENERALE 62
PERSPECTIVES 62
REFERENCES BIBLIOGRAPHIQUES 69
ANNEXES

vii
Figure 1. Carte de localisation de la zone
d'étude. 6
Figure 2. Courbe ombrothermique de Bagnouls
et Gaussen appliqué aux données
météorologiques de la région
Dizangué (2007-2017). 7
Figure 3. Carte des unités
géomorphologiques de la zone d'étude 8
Figure 4. Carte du réseau
hydrographique de la région du lac Mboli 9
Figure 5. Vue partielle lac Mboli 9
Figure 6. Esquisse géologique de la
zone d'étude extrait de la carte géologique du Sud- Ouest 11
Figure 7. Présentation
l'échantillonneur de Niskin. 16
Figure 8. Échantillonnage d'eau
souterraine : 17
Figure 9. Illustration de l'étiquetage
des échantillons d'un point prélevé dans le lac 18
Figure 10. Application de la mesure des
paramètres physico-chimique 19
Figure 11. Répartition d'ensemble des
éléments chimiques majeurs dans les eaux du lac Mboli,
de la source et du forage 31
Figure 12. Diagramme de piper
représentant le faciès des eaux du lac Mboli de la source et
du
forage. 31
Figure 13. Évolution du pH dans les
colonnes d'eau 35
Figure 14. Variation du pH dans les eaux
souterraines 36
Figure 15. Évolution de la
conductivité électrique dans les colonnes d'eau 37
Figure 16. Variation de la
conductivité dans les eaux souterraines 38
Figure 17. Évolution de la
température dans les colonnes d'eau 39
Figure 18. Variation de la température
dans les eaux souterraines 40
Figure 19. Évolution des ETM dans les
colonnes d'eau 42
Figure 20. Variation des ETM dans les eaux
souterraines 43
Figure 21. Évolution des cations et
TZ+ dans les colonnes d'eau 44
Figure 22. ariation des cations et
TZ+ dans les eaux souterraines 45
viii
Figure 23.volution des anions et
TZ- dans les colonnes d'eau 46
Figure 24. Variation des anions et
TZ- dans les eaux souterraines 47
Figure 25. Évolution d'autres
éléments en solution dans les colonnes d'eau 48
Figure 26. Variation d'autres
éléments en solution- dans les eaux souterraines 48
Figure 27. Évolution oxygène
dissous dans les colonnes d'eau 49
Figure 28. Variation de l'oxygène
dissous dans les eaux souterraines 50
Figure 29. Évolution de la TDS dans
les colonnes d'eau 51
Figure 30. Variation de la TDS dans les eaux
souterraines 51
Figure 31. Proportions des
éléments chimiques majeurs 80
Figure 32. Projection des paramètres
physico-chimiques des eaux du lac, de la source et du
forage sur le plan factoriel F1 - F2 55
Figure 33. Aptitude des eaux du lac, de la
source et du forage à l'irrigation selon le diagramme
de Wilcox. 60
Figure 34. Aptitude des eaux du lac, de la
source et du forage à l'irrigation selon le diagramme
de Riverside. 61

ix
Tableau 1. Données climatiques de
Dizangué couvrant la période de (2007 à 2017). 7
Tableau 2. niveau de variation paramètres
physiques mesurés dans les colonnes d'eau du lac
Mboli. 29
Tableau 3. Niveau du pH et qualité de
l'eau (Anonyme, 2009) 35
Tableau 4. Comparaison des concentrations des
ETM présent dans la colonne des deux stations de
prélèvement dans le lac Mboli aux lignes directrices de l'US EPA
: CMC et CCC
(USEPA, 2006) 43
Tableau 5. matrice de
corrélation entre les paramètres physico-chimiques des eaux du
lac, de la
source et du forage 58

X
ACP : Analyse en Composante Principale
ANOR : Agence des Normes et de la Qualité
BI : Balance Ionique
CCC : Critère de Concentration Continue
CE : Conductivité Electrique
CMC : Critère de Maximum Concentration
ETM : Eléments Traces Métalliques
HSDB : Hazardous Substances Data Bank
LAGE : Laboratoire d'Analyse Géochimique des Eaux
OD : Oxygène dissous
OMS : Organisation Mondiale de la Santé
TDS : Total des Solides Dissous
USEPA : United States Environmental Protection Agency

xi
Les éléments traces métalliques font
partis des polluants les plus dangereux pour l'homme et son environnement. Ces
derniers associés à d'autres paramètres physico-chimiques
ont été étudiés dans les eaux du lac Mboli, ainsi
que les eaux souterraines utilisées comme eau de boisson par les
populations riveraines de ce lac. Cette étude a donc pour but, de
contribuer à une meilleure connaissance des propriétés
physico-chimiques de ces eaux, particulièrement les
éléments traces métalliques. L'approche
méthodologique a consisté à effectuer des travaux sur le
terrain et en laboratoire qui ont permis l'échantillonnage des eaux
ainsi que l'analyse de nombreux paramètres physico-chimiques. Au niveau
du lac, l'échantillonnage est fait dans la colonne d'eau, en raison de
deux échantillons par niveau (à la base, au milieu, et à
la surface). Huit échantillons ont été analysés,
dont 6 dans le lac, un provenant de la source et un du forage. Pour le
traitement des données, la méthode hydrochimique et l'analyse
statistique multivariée ont été utilisées dans le
cadre ce travail. Dans l'ensemble, Ces eaux sont acides à très
faiblement acide (4,34 < pH < 6,84), elles sont très faiblement
minéralisées (27, 21 < CE < 51,22 uS/cm) avec une
température qui oscille de 26,3 à 32,5 °C.
les ETM distribués dans ces eaux sont : Fe, Al, Cu, Mn, Cd. La
classification d'ordre de grandeur décroissant des
éléments majeurs d'après les concentrations moyennes
d'ensemble est la suivante HCO3- > NO3- >
Ca2+ > Mg2+ > Na+ > SO42-
> Cl- > K+. L'observation des proportions de ces
éléments majeurs dans le diagramme de Piper a permis de
visualiser deux faciès à savoir, le faciès chloruré
sulfaté calcique et magnésien qui représente 62,5 % des
eaux et le faciès bicarbonaté calcique 37,5 %. Sur le plan
environnemental, dans le lac, le pH < 5, l'OD < 5 mg/l et les ETM (Al,
Cu, Cd) présents à chaque niveau de la colonne d'eau
dépassant le seuil de l'USEPA présentent un risque toxique pour
les organismes aquatiques. Quant aux eaux souterraines utilisées comme
eau de boisson, la conductivité et l'Al mesurées dans ces eaux ne
respectent pas les normes de l'OMS et ANOR, par contre, seul le pH
relevé au niveau de la source ne respecte pas ces normes. Les
paramètres physico-chimiques présents dans ces eaux ont diverses
origines à savoir, géogénique, anthropique et mixte. Ces
eaux sont excellentes pour une utilisation agricole.
Mots clés : lac Mboli à
Dizangue, éléments traces métalliques, colonne d'eau,
physico-chimique - eau souterraine


Metal trace elements are among the most dangerous pollutants
for humans and their environment. These, combined with other physical and
chemical parameters, have been studied in the waters of Lake Mboli, as well as
groundwater used as drinking water by populations along the lake. This study
aims to contribute to a better knowledge of the physical and chemical
properties of these waters, especially the metal trace elements. The
methodological approach involved field and laboratory work that allowed water
sampling and analysis of many physical and chemical parameters. At the lake
level, sampling is done in the water column, due to two samples per level (at
the base, middle, and surface). Eight samples were analyzed, including 6 in the
lake, one from the source and one from the borehole. For data processing, the
hydrochemical method and multivariate statistical analysis were used in this
work. Overall, these waters are acidic to very low acid (4.34 = pH = 6.84),
they are very low mineralized (27, 21 = CE = 51.22 S/cm) with a temperature
that ranges from 26.3 to 32.5 degrees Celsius. the ETMs distributed in these
waters are Fe, Al, Cu, Mn, Cd. Decreasing order of magnitude classification of
major elements based on the overall average concentrations is the following
HCO3- >NO3- > Ca2+ > Mg2+
> Na+ > SO42- > Cl- >
K+. Observing the proportions of these major elements in the Piper
diagram allowed us to visualize two facies, namely, the calcium sulphate and
Magnesian chlorinated facies, which account for 62.5 % of the water, and the
37.5 % pecic bicarbonate facies. For the lake, the lower pH 5, the OD less than
5 mg/l and the MTEs (Al, Cu, Cd) present at each level of the water column
above the USEPA threshold pose a toxic risk to aquatic organisms. As for
groundwater used as drinking water, conductivity and Al measured in these
waters do not meet WHO and ANOR standards, however, only the pH at the source
does not meet these standards. The physical-chemical parameters present in
these waters have various origins, namely, geogenic, anthropogenic and mixed.
These waters are excellent for agricultural use. For groundwater, they are
generally good for consumption.
Keywords: Lake Mboli at dizangue, metal trace elements, water
column, physico-chemical, groundwater
2
Chaque jour des centaines de tonnes de polluants sont
déversés dans l'environnement. Parmi eux, les
éléments traces métalliques sont considérés
comme des polluants très dangereux de l'environnement aquatique,
à cause de leur rémanence et leur tendance à la
bioaccumulation dans les organismes aquatiques (Harte et al., 1991 ;
Schuurmann et Markert, 1998). La contamination des écosystèmes
aquatiques par les éléments traces métalliques demeure
donc un sérieux problème d'environnement. Cela devient de plus en
plus inquiétant surtout à cause des maladies notées sur
les populations qui y sont exposées (Oumar et al., 2014). Ces
éléments traces métalliques sont présents dans tous
les compartiments de l'écosystème aquatique, eau,
sédiment, faune et flore (Forstner et Wittman, 1983 ; Berg et
al., 2009). Ces dernières années, la pollution par les
métaux lourds est devenue un problème d'actualité qui
préoccupe toutes les régions du monde soucieuses de maintenir
leur patrimoine hydrique à un haut degré de qualité (Ben
bouih et al., 2005).
Les ressources en eau sont rarement stables dans la nature
à cause de plusieurs facteurs environnementaux qui peuvent
altérer sa constitution de base par diffusion, dissolution et hydrolyse,
ou même par simple mélange (Xiao et al., 2012 ; Yao et
al., 2012). La pollution de l'eau est une altération qui rend
son utilisation dangereuse et perturbe l'écosystème aquatique. La
dégradation de la qualité des eaux de surface constitue l'un des
problèmes environnementaux majeurs auquel l'humanité est
confrontée (Madjiki et al., 2013). En ce qui concerne les
études de la pollution des lacs, elles sont le plus souvent
effectuées pour confirmer les dégradations plus ou moins
visibles. Elles apportent ainsi des informations plus précises pour
résoudre ces dégradations observées.
Le lac Mboli, objet du présent travail, est
situé à proximité des plantations d'hévéa et
de palmier à huile. Malgré les activés qui s'y
déroulent, principalement la pêche et l'agriculture, le lac Mboli
ne présente pas visiblement une quelconque dégradation. Cette
approche d'observation ne peut aucunement confirmer de manière
scientifique que ce lac est en santé. En effet, les lac Nyos et Monoun,
sont des lacs ayant aujourd'hui une réputation mondiale à cause
des dégâts qu'ils ont causé. Ces derniers ne
présentaient certainement pas des indices quelconques qui pouvaient
alerter les populations riveraines. C'est après les catastrophes
survenues en 1984 pour le lac Monoun et, 1986 pour le lac Nyos que ces derniers
ont fait et font l'objet de nombreuses études approfondies. Le lac
Mboli, mal connu, est une ressource d'épanouissement
socio-économique des populations environnantes, pourrait être
sujet à une quelconque dégradation.
3
En effet, de manière générale, seule, des
études physico-chimiques permettent de comprendre les
phénomènes qui s'y déroulent et en tirer des conclusions.
Dans le cadre de cette étude, Compte tenu des limites
d'approvisionnement en eau potable dans cette zone, les populations ont recours
aux eaux souterraines pour la consommation et autres travaux ménagers,
une estimation de leur teneur en éléments traces
métalliques est extrêmement importante pour une évaluation
correcte des dangers associés à leur consommation.
La présente étude a pour but principal de
contribuer à une meilleure connaissance de la concentration des ETM,
mais aussi d'autres paramètres physico-chimiques dans les eaux du lac
Mboli et les eaux souterraines utilisées comme eau de boisson par les
populations voisines du lac. Les objectifs spécifiques sont :
- étudier l'évolution physico-chimique des eaux
du lac Mboli dans la colonne d'eau et les eaux souterraines environnantes du
lac utilisées comme eau de boisson ;
- étudier la qualité physico-chimique de ces
eaux (eaux du lac Mboli et les eaux souterraines) ;
- identifier les principales origines des paramètres
physico-chimiques des eaux du lac et les eaux souterraines
étudiées ;
- caractériser ces eaux sur le plan agricole.
Pour atteindre ces objectifs, le présent travail est
subdivisé en quatre chapitres :
- le premier chapitre est axé sur le cadre naturel de la
zone d'étude;
- le deuxième chapitre est basé sur la
présentation des matériels et méthodes utilisés
;
- le troisième chapitre est consacré à la
présentation des résultats obtenus sur le terrain et
en laboratoire ;
- le quatrième chapitre est l'interprétation et la
discussion des principaux résultats obtenus.
|
CHAPITRE I : MILIEU NATUREL
|
11>
|
5
INTRODUCTION
Le présent chapitre a pour objectif de renseigner sur le
cadre géographique, cadre géologie ainsi que le milieu humain et
économiques de la zone d'étude.
I.1. CADRE GEOGRAPHIQUE
I.1.1. Localisation de la zone d'étude
Situé dans le Département de la Sanaga Maritime,
Dizangué se trouve à 13 kilomètres d'Edéa le
chef-lieu du Département. Chef-lieu de l'Arrondissement de même
nom, Dizangué est située dans la partie Sud de la Région
du Littoral. L'arrondissement de Dizangué est limité au sud et
à l'est par l'Arrondissement de Mouanko, au nord par l'arrondissement
d'Edéa II, à l'ouest par l'Arrondissement de Douala
3ème et la Dibamba. Ces coordonnées
géographiques sont 9°41' et 9°50' de longitude Est et entre
4°42' et 4°53' de latitude Nord. Dizangué est marquée
par la présence de nombreux lacs naturels. Le lac Mboli est le
deuxième plus grand lac de la ville, avec une superficie totale de 420
ha. Le lac Mboli se trouve au voisinage des quartiers Mbalmayo et Bikoum qui
sont situés du côté Nord de la ville de Dizangué
(Fig. 1).
I.1.2. Climat
Le climat de Dizangué est une variante océanique
du type guinéen (Suchel, 1988), caractérisée par trois
mois de déficit pluviométrique, deux mois a pluviométrie
moyenne et sept mois très pluvieux. C'est un type régional de
transition entre le régime subéquatorial intérieur et le
régime de mousson de la côte (Suchel, 1972). Il est
caractérisé par l'interaction entre la masse d'air australe
anticyclonique (Sainte Hélène et Indien) et les masses d'air du
flux de mousson. Les deux composantes essentielles du climat sont la
température et la pluviosité. La température
s'élève à 26,5 °C de moyenne annuelle et varie peu
durant l'année (Tab. 1). La pluviosité est également forte
avec 2343 mm d'eau annuelle (Tab. 1). Deux saisons prédominent, Une
longue saison pluvieuse allant de mars à octobre et une baisse
légère de température de juin à septembre qui
marque la période la plus froide de la région. Une saison
sèche bien marquée, de novembre à février (Fig.
2).
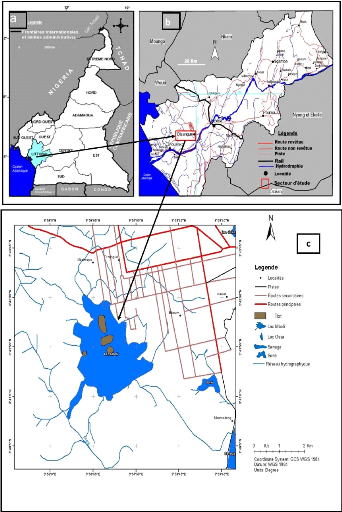
6
g . ( ) g
;
(b) Département de la Sanaga-Maritime dans lequel est
illustré la localité d'étude ; (c) lac Mboli et ses
environs.
7
Tableau 1 : Données climatiques de
Dizangué couvrant la période de (2007 à 2017).
Mois Jan. Fév. Mar. Avr. Mai. Juin. Juil. Aout.
Sept Oct. Nov. Déc. T. Moy.
P(mm) 51 58 119 173 187 236 347 408 390 236 108
30 2343 -
T(°C) 27 28 28 27 27 26 25 25 25 27 27 27 -
26,6
Source : station
météorologique de Douala
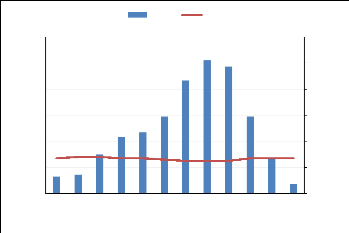
Précipitation (mm)
480
400
240
320
160
80
0
Jan. Fév. Mar. Avr. Mai. Juin. Juil. Aout. Sept Oct. Nov.
Déc.
Mois
P(mm) 2T(°C)
240
200
40
0
80
160
120
Température (°C)
Figure 2. Courbe ombrothermique de Bagnouls et
Gaussen (1957) appliqué aux données météorologiques
de Dizangué (2007-2017).
I.1.3. Géomorphologie I.1.3.1. Orographie
D'après les observations effectuées sur le
terrain, la zone d'étude est assez plate dans l'ensemble. Cependant, on
note à certains endroits des petites élévations. Une
analyse de la carte des unités géomorphologiques (Fig. 3) permet
de subdiviser le site en deux unités en fonction de l'altitude il s'agit
de :
- l'unité morphologique basse comprise
entre 15 - 40 m d'altitude environ, cette partie est représenté
par des bas-fonds marécageux ;
- l'unité morphologique haute comprise
entre 40 -75 m d'altitude environ, représentant les plaines .
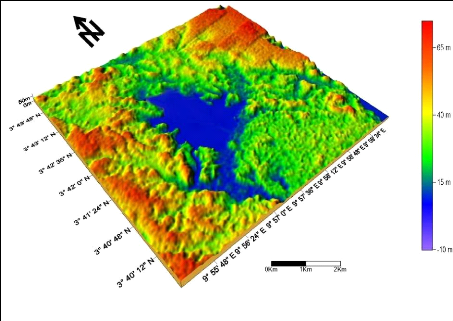
8
Figure 3. Carte des unités morphologiques
de la zone d'étude extrait de la carte SRTM.
I.1.3.2. Hydrographie
Dizangué est entouré de lacs qui domine ainsi
son hydrographie. Il s'agit des lacs : Mboli, Nsipé (I, II, III), Ileka,
Mwembe et le plus important est le lac Ossa. Le fleuve Sanaga serpente la
commune sur une distance de 8 km. On y trouve aussi quelques cours d'eau tels
que la rivière Mbanda, Nsipé, Kwakwa etc. On note aussi la
présence de l'océan Atlantique du côté de
l'île Ndigle.
Le lac Mboli, d'environ 3 m de profondeur moyenne, d'une
superficie totale de 420 ha, a une forme grossièrement rectangulaire
orientée NW-SE. Il contient quelques îles en son sein (Fig. 4).
(Kossoni, 2003).

9
Figure 4. Carte du réseau hydrographique
de la région du lac Mboli extrait de la carte topographique de
Mouanko

Figure 5. Vue partielle lac Mboli.
I.1.4. Végétation
Dans l'arrondissement de Dizangué comme dans tout le
littoral atlantique, la végétation est une forêt dense de
type littoral atlantique. Les espèces caractéristiques sont
Lophira alata et Sacoglottis gabonensis. Lophira alata est
surtout développé sur les interfluves tandis que
10
Sacoglottis gabonensis colonise les thalwegs aux sols
hydromorphes (Letouzey, 1968 ; 1985). Le taxon prédominant est
l'espèce héliophile Lophira alata. Les individus de
cette espèce présentent une très grande
circonférence (220 à 240 cm) donnant de grands ombrages, qui
bloquent le développement des Jeunes plantules. Ce qui implique un
sous-bois clairsemé avec quelques arbustes effilés et peu de
lianes.
La végétation du côté nord du lac
Mboli est constituée principalement d'espèce d'arbre, du genre
hévéa de la famille des euphorbiaceae et du palmier à
huile implantée par la société africaine forestière
et agricole du Cameroun (SAFACAM).
I.1.5. Sol
Les sols de Dizangué sont des sols jaunes
ferrallitiques sur roches sédimentaires (Segalen, 1994). Ils ont une
texture sableuse à sablo-argileuse. Les divers constituants de ces sols
sont la kaolinite, le quartz, la gibbsite, l'hématite, la goethite
(Segalen, 1994). La ferrallitisation est caractérisée par une
hydrolyse totale des minéraux primaires autres que le quartz,
l'élimination de la majeure partie des bases et d'une grande partie de
la silice, la néoformation de kaolinite et d'oxyhydroxydes de fer et
d'aluminium (gibbsite, hématite). Du fait de la pérennité
des climats chauds et humides dans la zone équatoriale, il est admis que
les sols ferrallitiques sont très âgés. La durée
minimale pour qu'un sol soit complétement transformé par
hydrolyse serait de l'ordre de 100 000 ans (Duchaufour,1983).
I.2. CADRE GÉOLOGIQUE
Au Cameroun, les formations géologiques appartiennent
aux grands ensembles géologiques suivant : le craton du Congo, la
couverture du craton, les formations du phanérozoïque et la
chaîne panafricaine. La zone d'étude est regroupée dans le
grand ensemble représenté par la région du SW-Cameroun et
associée au complexe du Nyong (Feybesse et al., 1998 ; Penaye
et al., 2004), la chaîne de l'Oubanguide (Nzenti et
al.,1988 ; Owona et al., 2011b) et la couverture du
crétacé à actuelle correspondant au bassin
sédimentaire côtier Camerounais de Douala-Kribi-Campo (Njike
Ngaha, 1984).
Les formations géologiques de la zone d'étude
(Fig. 6) sont les roches sédimentaires caractéristiques de la
série de Dizangué pour la majeure partie du bassin versant. Elles
sont
11
dominées par des grès ferrugineux à
stratification entrecroisée d'âge paléocène (Njike
Ngaha, 1984).
L'emplacement du lac Mboli comme celui des lacs environnants
est vraisemblablement lié au rejeu des fractures anciennes qui a
créé sur le socle des horsts et des grabens. Ces derniers se
seraient affaissés progressivement en fonction de la surcharge des
sédiments Crétacés et Tertiaires du sous bassin de Douala.
Le rejeu des failles, par accentuation de la subsidence, a donné
naissance à une multitude de petites fractures le long desquelles
coulent les petits cours d'eau. Ces ruisseaux, initialement dirigés vers
l'axe de la Sanaga, auraient été bloqués par
l'accumulation de la basse terrasse alluvionnaire de la Sanaga qui a permis la
retenue des eaux, donnant ainsi naissance au lac du moins dans sa configuration
actuelle (Njiké-Ngaha, 1984 ; Dumont, 1986).

Figure 6. Carte géologique de la zone
d'étude extrait de la carte géologique du Sud- Ouest (Regnoult,
1986).
12
I.3. MILIEU HUMAIN ET ACTIVITE ECONOMIQUE
L'arrondissement de Dizangué est l'une des neuf
communes que compte le Département de la Sanaga Maritime. Sa population
est estimée à 17 086 habitants, parmi lesquelles on compte 8993
hommes contre 8093 femmes suivant le recensement général de la
population de 2005 (PCD Dizangué 2011). Le diagnostic participatif a
relevé un effectif total de la population de la Commune d'environ 32 627
habitants. On rencontre quatre ethnies autochtones, Pongo, Ndonga, Yakalak et
Malimba. La population est étendue sur deux cantons (Ndonga et Yakalak)
et 32 villages. Sur le plan religieux, on y retrouve le christianisme et
l'islam (PCD Dizangué 2011). Les principales activités
économiques de la ville de Dizangué sont concentrées sur
les activités menées par les sociétés SAFACAM et
SOCAPALM possédant des hectares de plantation de palmiers à huile
et de l'hévéas. Néanmoins, on note aussi la
présence du secteur informel etc(PCD Dizangué 2011).
CONCLUSION
La zone d'étude est située dans la région
du littoral Cameroun, précisément dans le département de
la Sanaga maritime, arrondissement de Dizangué. Elle est
caractérisée par un climat de variante océanique du type
guinéen, caractérisée par trois mois de
pluviométrie faible et sept mois très pluvieux. Le relief de la
zone est assez plat, l'hydrographie est dominée par la présence
de nombreux lacs dont les plus importants sont le lac Mboli et le lac Ossa. On
note également la présence de certaines rivières et celle
du fleuve Sanaga. Les sols de la zone d'étude sont des sols
ferrallitiques jaunes développés sur roches sédimentaires.
La végétation de la zone d'étude est une forêt dense
de type littoral atlantique. Le substratum est constitué de roches
sédimentaires, caractéristiques de la série de
Dizangué. Pour la majeure partie du bassin versant, ce sont de
grès ferrugineux à stratification entrecroisée d'âge
Paléocène. Les matériels et méthodes
utilisés seront présenté dans le chapitre
subséquent.
|
CHAPITRE II : MATERIELS ET
METHODES
|
I,>
|
|
14
INTRODUCTION
Les travaux ont été menés tant sur le
terrain qu'en laboratoire. Au préalable, une synthèse des travaux
antérieurs déjà réalisés dans la zone
d'étude et ses environs ainsi ceux réalisés dans les
autres sites mais dans le même contexte (hydrochimie, hydrologie,
pollution) a été effectué, ajouter à cela une
précampagne de terrain a permis de circonscrire le site d'étude.
Dans ce chapitre il est question de présenter les matériels
utilisés ainsi que les approches méthodologiques qui ont permis
l'obtention des résultats dans le cadre de cette étude.
II.1. MATERIELS ET TRAVAUX DE TERRAIN
II.1.1. Matériels de terrain
Le matériel utilisé lors de la réalisation
des travaux sur le terrain comprend :
- un récepteur GPS (système de
localisation par satellite) de marque Garmin modèle
64S qui a permis de prendre les coordonnées
géographiques des sites de prélèvement
des différents échantillons ;
- une carte de la zone d'étude pour le
repérage des secteurs ;
- un échantillonneur de Niskin d'une
contenance de 1,7 l pour prélever l'eau dans le lac ;
- une pirogue artisanale pour les
déplacements dans le lac ;
- des bouteilles de contenance 0,5 l pour
échantillonner l'eau ;
- une glacière pour la bonne conservation
des échantillons ;
- du ruban adhésif pour
l'étiquetage des échantillons ;
- un appareil photo numérique pour la
prise des photographies ;
- un stylo et un carnet de terrain pour
consigner toutes les notes prises sur le terrain ;
- un marqueur pour la codification des
échantillons ;
- une sonde multiparamètre
professionnelle de marque YST pour la mesure des
paramètres physiques de l'eau sur le terrain.
II.1.2. Travaux de terrain
II.1.2.1. Échantillonnage de l'eau
Les échantillons obtenus sont issus du lac Mboli, d'un
forage et d'une source. Le forage et la source sont situés non loin du
lac, précisément dans le quartier jouxtant le lac (Mbalmayo). Il
s'agit d'un échantillonnage d'eau de surface (lac Mboli) et d'eau
souterraine (source et
15
forage). L'échantillonnage s'est effectué le 21
mars 2020 car à cette période, la pluviométrie
n'était pas encore assez élevée, ce qui nous a permis la
bonne navigation dans le lac. Les bouteilles utilisées sont de type
polyéthylène de 500 ml préalablement lavées avec
l'eau déminéralisée.
L'échantillonnage au niveau du lac s'effectue dans la
colonne d'eau. Dans le cadre de ce travail, deux stations (1 et 2) ont
été choisis représentant les zones les plus profondes du
lac Mboli. La station 1 a une profondeur de 3,40 mètres, la station 2,
une profondeur de 2,65 mètres. Avant le prélèvement, la
profondeur maximale de chaque station a été
déterminée au préalable, car le prélèvement
est fait de façon verticale. Cette profondeur est obtenue à
partir du dispositif de prélèvement possédant une corde
graduée. Après avoir déterminé la profondeur, les
niveaux de prélèvements dans la colonne d'eau ont
été choisis. Dans cette étude, pour chaque profondeur
maximale de la colonne d'eau, trois prélèvements ont
été effectués, c'est à dire au fond du lac, au
milieu et à la surface. La bouteille de Niskin (Fig. 7) est le
dispositif utilisé pour le prélèvement de l'eau à
une profondeur précise (Issa, 2014 ; Gouin et al., 2016). Celle
utilisée à une longueur d'un mètre, avec un volume de 1,7
l. Il possède une corde permettant de déterminer la profondeur
à laquelle le prélèvement est
effectué. il s'agit d'un
cylindre, ouvert aux deux extrémités et muni d'un système
de fermeture automatique au contact du « messager » afin
d'emprisonner le volume d'eau qui sera remonté à bord de la
pirogue. Dans cette étude, les prélèvements ont
été effectués en respectant un écartement d'un
mètre de la surface vers la profondeur. Pour charger de l'eau dans les
bouteilles, le robinet fixé sur l'échantillonneur de Niskin est
utilisé pour éviter toute contamination externe. Après
avoir remonté l'échantillonneur de Niskin remplie d'eau de la
profondeur de prélèvement prédéfinie, il faut au
préalable rincer les bouteilles au moins trois fois avant le remplissage
définitif. Le prélèvement à la surface se fait
à la main par immersion directe des bouteilles plastiques à une
certaine profondeur (Ndam Ngoupayou, 1997). La profondeur a été
estimée à environ dix centimètres. A ce niveau aussi, le
rinçage de la bouteille est fait trois fois de manière
consécutive avant le remplissage définitif. La colonne d'eau de
chaque station de prélèvement possède six
échantillons dont deux à la base, deux au milieu et deux à
la surface. Dans le lac, douze échantillons ont été
récoltés correspondant à deux points de
prélèvements, respectivement six pour chaque point et deux pour
chaque niveau de profondeur.
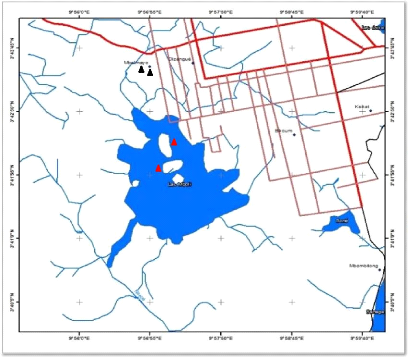

Point d'échantillonnage au niveau du lac Mboli
Point d'échantillonnage au niveau des eaux souterraines
Figure 7. Carte d'échantillonnage de la
zone d'étude
a b c d

16
Figure 8. Présentation
l'échantillonneur de Niskin : (a) vue d'ensemble d'une bouteille de
Niskin, (b) vue d'une ouverture d'entrée d'eau, (c) introduction d'une
bouteille de Niskin dans l'eau pour un prélèvement, (d) Niskin
fermé à l'aide d'un messager.
17
En ce qui concerne les eaux souterraines, deux
échantillons ont été prélevés au niveau du
forage et deux au niveau de la source. Le prélèvement se fait en
respectant la procédure suivante : tout d'abord rincer trois fois (de
manière énergétique) la bouteille de
prélèvement et son bouchon avec de l'eau à
échantillonner, ensuite remplir la bouteille lentement sans barbotage,
en fin boucher la bouteille avec précaution, mais vivement de
façon à ne pas emprisonner de bulles d'air.
Figure 8. Échantillonnage d'eau
souterraine : (a) échantillonnage au forage, (b) échantillonnage
à la
source.
II.1.2.2. Étiquetage et conservation des
échantillons
Pour ce qui est de l'étiquetage, la désignation
des échantillons est une opération délicate, qui doit
être réalisée avec le plus grand soin. Afin de pouvoir
identifier les différents échantillons par le laboratoire
d'analyse et après analyse, les différents échantillons
ont été codifiés. Sur chaque échantillon, a
été inscrit sur le ruban adhésif, un code qui correspond
à sa localisation précise (Fg. 9). Pour les échantillons
prélevés dans le lac Mboli, le sigle LMB signifie lac Mboli les
lettres (b, m, et s) placées en indice signifient respectivement, base,
milieu et surface tandis que les chiffres 1 et 2 correspondent à chaque
station de prélèvement qui représente une la colonne
d'eau. Pour les échantillons issus des eaux souterraines, la
codification est plus simplifiée. Pour le forage, le code utilisé
est MF qui signifie Mbalmayo forage. Pour ce qui est de l'étiquetage de
la source, nous avons pris la lettre S pour la codifier.

LMBm 1 LMBb 1
18
Figure 9. Illustration de l'étiquetage
des échantillons d'une colonne d'eau du lac.
Les eaux superficielles, en particulier si elles sont
chargées en matières dissoutes issues d'eaux résiduaires,
sont susceptibles de subir des transformations plus ou moins prononcées
et rapides d'origine physique (température, pression, absorption,
adsorption, évaporation), physico-chimiques (précipitation,
évasion de gaz dissous) et biologiques' (autoépuration, fixation
photosynthèse), entre le moment du prélèvement et
l'analyse. Raison pour laquelle les échantillons ont été
conservés dans une glacière tapissée de glaçons.
III.1.2.3. Mesures sur le terrain
De nombreux paramètres concernant la nature physique et
chimique des points d'échantillonnage ont été
mesurés in-situ. Ces derniers ont été obtenus à
l'aide d'une sonde multiparamètres de marque YSI. Il s'agit notamment de
:
- la température ; - l'oxygène dissous ; - la
conductivité ; - le pH.

a
b
Figure 10. Application de la mesure des
paramètres physico-chimique : (a) multiparamètres de marque YSI,
(b) mesure des paramètres dans la source.
II.2. TRAVAUX EN LABORATOIRE
Les échantillons ont été conservés
dans une glacière pendant le transport du terrain jusqu'au Laboratoire
d'Analyse Géochimique des Eaux à Nkolbisson où ils ont
été stockés dans un réfrigérateur à
4° C avant d'être analyser.
II.2.1. Dosage des éléments traces
métalliques (Mn, Fe, Cu, Cd, al)
II.2.1.1. Matériels et réactifs
Pour la détermination des ETM les matériels et
réactifs suivants ont été utilisés :
- spectromètre d'absorption atomique par flamme
(ContrAA300) ;
- 08 fioles de 100 ml, 08 fioles de 50 ml, une pipette
graduée pour chaque élément ;
- tubes pour étalons d'analyses et échantillons,
;
- solution de dilution HNO3 1 % (blanc et
référence), ;
- solution de rinçage HNO3 0.1 % ;
- solutions Mères à 1000 ppm de chaque
élément ;
- solution de Laboratoire ERIL ;
- eau Ultra pure pour préparation des solutions ;
- purificateur d'eau (MilliQ) ;
19
- béchers.
20
III.2.1.2. Méthodologie
La méthodologie consiste à préparer une
solution de dilution 1 % de HNO3, qui est obtenue en plaçant 1 ml de
HNO3 à 65 % (à l'aide d'une micro pipette graduée à
1 ml) dans une fiole de 100 ml et on complète la fiole jusqu'au trait de
jauge avec de l'eau ultra pure. Ensuite, la Préparation d'une solution
fille à 100 ppm (solution intermédiaire) est
obtenue Prélevant 10 ml de solution mère de Fe (ou tout
élément) à 1000 ppm et l'introduire dans une fiole de
100ml, complétez jusqu'au trait de jauge avec la solution de dilution 1
% HNO3, puis une solution intermédiaire est préparée elle
aussi à partir d'une solution mère de 1000 ppm par
prélèvement de 10 ml qu'on dilue dans une fiole de 100 ml avec
l'acide Nitrique 1 %. La préparation des étalons de travail
(gamme étalon) pour chaque élément à doser est
obtenue en préparant une gamme d'étalons à
différentes concentrations, il est important de passer par une solution
intermédiaire de concentration égale à 100 ppm (en
fonction du type de métal). Les quantités prélevées
dans cette solution pour la préparation et les concentrations des
étalons de chaque métal dépendront de chacun. Afin
d'éviter d'éventuelle interférence due à la
matrice, chaque étalon (S1, S2, S3 et S4) est préparé par
un mélange de concentration des différents
éléments. L'étalonnage et la calibration de la
méthode d'analyse consistent à comparer la concentration des
échantillons à tester avec celle d'une solution dont on connait
la concentration avec précision et par la suite de comparer les
résultats des échantillons tester avec celles obtenus par un
autre laboratoire sur le même aliquote et le même équipement
(LAGE Nkolbison). Avant de faire des analyses, : les échantillons
conditionnés à 1 % HNO3 sont préparés de la
même manière que les étalons. Ainsi, cette étape
prendra en compte le domaine de linéarité qui correspond à
la zone de mesure où le signal enregistré par l'appareil est
directement proportionnel à la quantité ou à la
concentration de substance mesurée. En d'autres termes, seul le
résultat de dosage se trouvant dans le domaine de
linéarité peut être validé (dans l'intervalle de la
gamme étalon). L'analyse est effectuée à l'aide d'un
spectromètre d'absorption atomique par flamme.
III.2.2. Cas des éléments majeurs et d'autres
éléments chimiques
La technique retenue pour l'analyse des anions
(HCO3-, Cl-, SO42- ; NO3-), les
cations (Ca2+, K+, Mg2+, Na+) et
d'autres éléments chimiques (F-, NH4+,
PO43- , Al 3+) est celle par chromatographie ionique
à phase liquide selon la norme ISO 103041.
21
III.2.2.1. Matériels et réactifs
Plusieurs matériels et réactifs ont
été utilisés pour l'analyse des éléments
majeurs et d'autres éléments chimiques. Il s'agit :
- des fioles jaugées de 1000 ml pour préparation
des éluant Cations et Anions ;
- des pipettes graduées de 10 ml et 1 ml de classe A ;
- une balance électronique de précision de marque
Mettler (#177; 0.0001)
- des piluliers en polyéthylène de 60 ml pour les
dilutions ;
- deux Passeurs automatiques de marque Dionex AS-AP
- deux Chromatographes Ioniques (ICS 1100) et ICS 90 de Dionex
;
- un purificateur d'eau de marque Milli-Q ;
- un Ordinateur possédant un logiciel de pilotage des
Passeurs et des Chromatographes, Chroméléon 6.80 ;
- une solution acide, H2SO4 (22 mM) pour les cations ;
- une solution alcaline ((Na2C03 (2.7 mM) + NaHCO3 (0,3 mM) ; -
l'eau ultra pure.
III.2.2.2. Méthodologie
Le principe de la chromatographie ionique à phase
liquide est basé sur la séparation d'espèces dans un
mélange par partage entre une phase mobile (gaz ou liquide) et une phase
stationnaire (liquide ou solide). Chaque soluté injecté sur la
colonne est soumis à deux effets antagonistes qui sont : un effet
d'entrainement par la phase mobile dans laquelle il est soluble et un effet de
rétention par phase stationnaire avec laquelle il interagit. Ainsi, la
séparation et le temps de migration des composés à
éluer seront donc fonction des différences affinités des
phases mobile et stationnaire. S'agissant du mode opératoire, les
concentrations des anions et des cations ont été
déterminées respectivement, à l'aide des systèmes
de chromatographie ionique en phase liquide de model respectif ICS1100 et ICS90
opérant à température ambiante avec pour précision
des mesures 5 %. Tous les échantillons étaient filtrés sur
papier filtre (0,45 um) avant injection dans le système de
chromatographie par un passeur automatique de marque DIONEX AS-AP. Les
échantillons ayant une conductivité élevée ont
été dilués de manière appropriée avec de
l'eau distillée avant d'être analysés. Les anions
F-, Cl -, NO3 -, PO43- et SO42-
22
ont été séparés dans une colonne
de chromatographie model IonPAC AS12A (4 x 200 mm) muni d'une colonne de garde
model AG12A (4 × 50 mm) et détectés après suppression
de la conductivité anionique par un suppresseur anionique IonPAC ASRS300
(4 mm) auto-régénérant. Les anions ont été
élués à l'aide du mélange d'éluant ((Na2CO3
(2.7 mM) + NaHCO3 (0,3 mM)) à un débit de 1 ml/min. Un volume
d'échantillon de 100 ìl était injecté par un
passeur automatique et analysé pour 15 minutes. Les cations
Na+, NH4+, K+, Mg2+ et
Ca2+ ont été séparés dans une colonne de
chromatographie model IonPac CS12A Ion PAC (4 x 250 mm) avec une colonne de
garde de marque IonPac CG-12A IonPac et détecté après
suppression de la conductivité anionique par un suppresseur cationique
IonPac CSRS300 (4 mm) auto-régénérant. Les cations
étaient élués avec H2SO4 (22 mM) à un débit
de 1 ml/minute. Le volume d'injection était de 100 ìl, alors que
le temps d'exécution était fixé à 15 minutes. Sa
limite de détection est de 0,1 méq/l et sa
reproductibilité varie de 1 à 3 % (SOM, LAGE
2012). Les échantillons et les étalons sont placés dans un
passeur automatique et les valeurs sont transmises sur un écran
d'ordinateur où chaque pic correspond à un élément
majeur.
II.3. QUALITE ET TRAITEMENT DES DONNEES
Avant de traiter et d'interpréter les données
physico-chimiques des échantillons d'eau issus des différentes
stations (eaux souterraines et eaux de surfaces) à l'aide des logiciels
Microsoft Excel et Word, il faut analyser la fiabilité des
résultats de ces analyses.
II.3.1. Qualité des données
II.3.1.1. Utilisation d'un échantillon de
référence : ERIL
Cette méthode de fiabilité des résultats
concerne les ETM. En effet, le laboratoire a préparé un
échantillon témoin nommé ERIL. L'ERIL est composé
de la moyenne des échantillons qui ont été reçus
par le laboratoire en vue d'une analyse. Il s'agit des eaux en provenance des
régions de : l'Est, du Sud et centre du Cameroun et auquel on a
ajouté 10 ml de HNO3 pour 1000 ml d'échantillon
(conditionnement).
Il s'agit de comparer la concentration des échantillons
à tester avec celle d'une solution dont on connait la concentration avec
précision et par la suite de comparer les résultats des
échantillons tester avec celles obtenus par un autre laboratoire sur le
même aliquote et le même équipement.
23
II.3.1.2. Balance ionique
La méthode utilisée pour vérifier la
fiabilité des résultats obtenus des éléments
majeurs es. Il faut rappeler qu'en théorie, une eau naturelle est
électriquement neutre. De ce fait, la somme (en équivalents
chimiques) des cations devrait être égale à celle des
anions (en équivalents chimiques) (Mahamane et Guel, 2015).
Equation 1: [Ca2+] + [Na+] +
[Mg2+] + [K+] = [Cl-] + [HCO3-] +
[SO42-] + [NO3-]
En réalité, cette égalité est
rarement obtenue. De façon générale, la différence
est attribuée aux incertitudes, à la présence de certains
ions non dosés ou à d'éventuelles erreurs d'analyse.
Ainsi, une certaine marge de déséquilibre entre anions et cations
est admise. Elle est exprimée sous forme d'un écart relatif par
la formule :
-
+
TZ-TZ
- × 100
BI= +
TZ + TZ
Le calcul de la balance ionique permet
généralement de vérifier la fiabilité des
résultats des analyses chimiques. Cependant, les incertitudes sur les
résultats, variables selon les techniques d'analyse, peuvent expliquer
les erreurs parfois élevées sur les balances ioniques, à
cause de la présence éventuelle d'anions organiques non pris en
compte dans les calculs. D'une manière générale, une
analyse chimique des eaux n'est considérée comme
représentative et acceptable que lorsque la balance ionique est
inférieure ou égale à 10 % (Kouassi et al., 2013).
II.3.2. Traitement des données
Les données physico-chimiques sont saisies et
traitées à l'aide des logiciels Microsoft Excel et Word. Par la
suite, les données physico-chimiques sont traitées et
analysées à partir d'une combinaison des méthodes
hydrochimiques et de statistiques multivariées. L'utilisation de ces
méthodes permet de connaître les principaux facteurs
environnementaux à l'origine de la qualité physico-chimiques des
eaux ainsi que leurs aptitudes.
II.3.2.1. Méthode hydrochimique
L'étude du chimisme des eaux a pour objectif
d'identifier les faciès des eaux et l'origine des principaux
éléments chimiques ; il se réalise par l'exploitation des
rapports caractéristiques qui sont considérés comme des
indicateurs de la qualité de l'eau. Le Diagramme de Piper (1994) est
l'une des représentations les plus classiques pour comparer les
compositions chimiques des eaux naturelles. Il permet une représentation
des cations et anions sur deux triangles spécifiques dont les
côtés témoignent des teneurs relatives de chacun des ions
majeurs par rapport au total
24
des ions. La position relative d'un résultat analytique
sur chacun de ces triangles permet de préciser en premier lieu la
dominance cationique et anionique. A ces deux triangles, est associé un
losange sur lequel est reportée l'intersection des deux lignes issues
des points identifiés sur chaque triangle. Ce point d'intersection
représente l'analyse globale de l'échantillon. Cette position
permet de préciser le faciès de l'eau naturelle concernée.
Cette étude a été possible grâce au logiciel
DIAGRAMME (Simler, 2005) version 6.61. Ce même logiciel a permis dans le
cadre de cette étude, de faire une analyse des données
physicochimiques des eaux afin de mettre en évidence leurs aptitudes
à l'irrigation au travers les digrammes de Wilcox (1948) et de Richards
(1954).
II.3.2.2. Analyse Statistique Multivariée (ASM)
L'analyse statistique Multivariée est une
méthode qui a pour but de faciliter la visualisation des données,
de révéler leurs structures sous-jacentes et d'extraire certaines
variables importantes (Gournay, 2012 ; Glèlè Kakai et
al., 2016).
Cette méthode est couramment utilisée dans les
domaines des sciences de l'eau et donne des résultats très
satisfaisants (Yao et al., 2012 ; Mfonka et al., 2015 ;
Kanohin et al., 2017)
II existe plusieurs étapes et/ou techniques dans la
chaine d'analyse hydrochimique par la méthode d'Analyse Statistique
Multivariée (ASM). Il s'agit notamment de la matrice de
corrélation (MC), l'Analyse en Composante Principale (ACP), et la
Classification Ascendante Hiérarchique (CAH). Dans le présent
travail, seule la matrice de corrélation (MC) et l'Analyse en Composante
Principale (ACP) ont été utilisées. Pour faciliter ce type
d'analyse, les ASM sont réalisées à l'aide du logiciel
XLSTAT 2020 mis à disposition sur le site
w.vw.xlstat.com et logiciel Excel
version 2019.
Pour ce qui est de la matrice de corrélation, elle est
obtenue à partir des coefficients calculés sur plusieurs
variables prises deux à deux et qui permet de noter des associations
entre variables qui peuvent montrer la cohérence globale de l'ensemble
de données (Guler et al., 2002 ; Everitt et Horthorn, 2011).
L'analyse en composantes principales (ACP) est une
méthode d'analyse multi-variée permettant l'étude
simultanée d'un grand nombre de variables dont l'information totale ne
peut pas être visualisée à cause d'un espace à plus
de trois dimensions. Cette méthode permettrait de préciser les
relations entre les variables et les phénomènes à
l'origine de ces relations. (Mfonka et al., 2015 ; Kanohin et
al., 2017). La réduction des données est
effectuée en transformant les données en un nouvel ensemble de
variables (composantes principale) dérivées
25
des combinaisons linéaires des variables d'origine et
classées de telle sorte que les premières composantes principales
(typiquement deux ou trois) soient responsables de la plupart des variations de
données originales (Mfonka et al., 2015 ; Kanohin et
al., 2017).
CONCLUSION
Plusieurs matériels et méthodes ont
été utilisés pour les prélèvements et les
analyses des échantillons. Les travaux effectués sur le terrain
ont permis l'échantillonnage des eaux ainsi que l'analyse in-situ de
nombreux paramètres obtenus par une sonde multiparamètre. Seize
échantillons ont été obtenus en raison de douze dans le
lac, deux dans la source et deux au forage. Les travaux en laboratoire, ont
été réalisés en fonction de la catégorie
d'élément. Huit échantillons ont été
analysés, dont six dans le lac, un provenant de la source et un du
forage. Les éléments traces métalliques ont
été obtenus par spectrométrie d'absorption atomique par
flamme et les éléments majeurs (cationiques et anioniques) par
chromatographie ionique à phase liquide. Pour le traitement des
données, la méthode hydrochimique à partir du logiciel
diagramme de Simler et l'analyse statistique multivariée (les logiciels
XLSTAT et Excel) ont été utilisées dans le cadre ce
travail. Les résultats obtenus dans cette étude seront
présentés au chapitre suivant.
|
CHAPITRE III : RESULTATS
|
I,>
|
27
INTRODUCTION
Plusieurs résultats ont été obtenus
à la suite des différents travaux et des relevés
effectués sur le terrain, ainsi que ceux effectués en
laboratoire. De ce fait, dans le présent chapitre, il sera question de
présenter les résultats qui se rapportent aux
caractéristiques physico-chimiques des eaux du lac Mboli et les eaux
souterraines (forage et source) du quartier jouxtant le lac.
III.1. NIVEAU DE VARIATION DES PARAMÈTRES
PHYSICO-CHIMIQUES DES
EAUX DU LAC MBOLI ET LES EAUX SOUTERRAINES
III.1.1. Paramètres physiques
Plusieurs paramètres physiques sont pris en comptes
dans le milieu, notamment le pH, la conductivité et la
température (Tab. 2).
Le pH des eaux du lac, de la source et du forage varie dans
l'ensemble entre 4,34 et 6,84, ce sont des eaux acides à faiblement
acides. La valeur moyenne du pH de ces eaux est de 5,96. La température
de ces varie entre 26,3 et 32,5 °C pour une valeur moyenne de
30,31°C. La conductivité quant à elle varie entre 6,5 et
51,22 uS/cm dans l'ensemble. Elle a une valeur moyenne de 32,81uS/cm. Dans
l'ensemble, ces eaux sont faiblement minéralisées (Detay,
1993).
III.1.2. Paramètres chimiques
Les paramètres chimiques renseignent sur la
qualité chimique des eaux. Ceux considérés dans le cadre
de cette étude sont les éléments traces
métalliques, les cations et anions majeurs, la somme des
équivalents cations (TZ+) et anions (TZ-), SiO4,
l'oxygène dissout, et d'autres éléments en solution tels
que le Cl-, F-, NH4+, PO42- ainsi
que le total des solides dissous (TDS), la balance ionique (BI) et le facies
hydrochimiques (tableau 2).
III.1.2.1. Éléments traces
métalliques
Les ETM obtenus après analyse dans les eaux du lac
Mboli, de la source et du forage sont le Mn, Fe, Cu, Cd, et l'Al. La
concentration d'ensemble de Mn dans ces eaux varie de 0,002 à 0,008 mg/l
avec une concentration moyenne de 0,01 mg/l. Les eaux du lac Mboli de la source
et forage présentent une concentration de Fe variant entre 0,024 et
0,337 mg/l, la concentration moyenne d'ensemble dans ces eaux est de 0,20 mg/l.
En ce qui concerne le Cu, sa concentration d'ensemble varie entre 0,030 et
0,094 mg/l, avec une concentration moyenne
28
de 0,03mg/l. quant au Cd, il a une concentration d'ensemble
variant entre 0,002 et 0,004 mg/l dans ces eaux. Sa concentration moyenne est
de 0,002 mg/l. pour le Al présent dans ces eaux, sa teneur d'ensemble
varie entre 0,101 et 1,553 mg/l, pour une contraction moyenne de 0,34 mg/l.
III.1.2.2. Cations majeurs et somme des équivalents
cations (TZ+)
Les concentrations d'ensemble en alcalino-terreux
(ca2+ et Mg2+) dans les eaux du lac Mboli, de la source
et du forage varient respectivement entre 0,165 et 49,78 mg/l et entre 0,21 et
20,827 mg/l, pour des moyennes respectives 12,33 et 4,33mg/l. Pour ce qui est
des concentrations en alcalins (Na+ et K+) dans ces eaux,
elles varient respectivement entre 0,181 et 20,827 mg/l et entre 0,048 et 2,597
mg/l, avec des teneurs moyennes respectives de 3,40 et 0,64 mg/l.
En ce qui concerne la somme des équivalents cations
(TZ+) de ces eaux, elle varie dans l'ensemble entre 0,064 et 4,941
méq/l, pour une moyenne de 0,137 méq/l.
III.1.2.3. Anions majeurs et somme des équivalents
anions (TZ-)
Les concentrations d'ensemble du Cl- et du
HCO3- dans les eaux du lac Mboli, de la source et du forage
oscillent respectivement entre 0,02 et 13,576 mg/l et entre 0,49 et 65,368
mg/l, pour des moyennes respectives de 1,95 et 41,4 mg/l. Pour ce qui est des
concentrations du NO3- et du SO42- dans
ces eaux, elles oscillent respectivement entre 1,311 et 39,927 mg/l et entre
0,486 et 0,894 mg/l, avec des teneurs moyennes respectives de 12,55 et 2,59
mg/l. La somme des équivalents anions (TZ-) de ces eaux,
varie dans l'ensemble entre 0,056 et 4,032 méq/l, pour une valeur
moyenne 0,99 méq/l.
III.1.2.4. Autres éléments en solutions :
(NH4+, PO43-, F-, OD, SiO2)
La teneur du NH4+ d'ensemble dans les eaux du lac,
de la source et du forage varie entre 0,018 et 1,812 mg/l, pour une teneur
moyenne de 0,33 mg/l. La teneur PO43- présent dans ces eaux
est comprise entre 0,005 et 4,351 mg/l pour une concentration moyenne de 1,07
mg/l. le F- quant à lui oscille entre 0,001 et 0,025 mg/l, pour une
concentration moyenne 0,01 mg/l dans ces eaux. La concentration d'ensemble en
oxygène dissous contenue dans ces eaux varie entre 2,56 et 6,16 mg/l,
pour une teneur moyenne de 4,80 mg/l. La teneur d'ensemble de silice de ces
eaux est comprise entre 0,004 et 0,894 mg/l, pour une concentration moyenne de
0,634 mg/l.
29
III.1.2.5. Total des Solides Dissous (TDS) et Balance
Ionique (BI)
Le total des solides dissous (TDS) d'ensemble des eaux du lac
Mboli, de la source et du forage est comprise entre 4,306 et 323,338 mg/l, pour
une moyenne de 79,833 mg/l, tandis que La balance ionique (BI) de ces eaux
présente des valeurs acceptables dans l'ensemble des
échantillons. En effet, tous ces échantillons présentent
des valeurs = 10 %. Dans l'ensemble, la balance ionique oscille entre -8 et 1 0
%, pour une moyenne 2 %.
Tableau 2. Niveau de variation des
paramètres physiques mesurés dans les colonnes d'eau du lac Mboli
et les eaux souterraines.
|
Paramètres
|
Unités
|
NE
|
Min
|
Max
|
Moy
|
Médiane
|
Ecart-type
|
|
pH
|
-
|
8
|
4,340
|
6,840
|
5,960
|
6,460
|
0,950
|
|
T
|
° C
|
8
|
26,300
|
32,500
|
30,310
|
30,950
|
2,300
|
|
CE
|
uS/cm
|
8
|
27,210
|
51,220
|
32,810
|
27,440
|
10,090
|
|
OD
|
mg/l
|
8
|
2,560
|
6,160
|
4,800
|
5,290
|
1,320
|
|
Ca2+
|
mg/l
|
8
|
0,1650
|
49,780
|
12,330
|
6,590
|
16,570
|
|
Mg2+
|
mg/l
|
8
|
0,210
|
20,827
|
4,330
|
1,870
|
6,880
|
|
Na+
|
mg/l
|
8
|
0,181
|
15,432
|
3,400
|
0,750
|
5,430
|
|
K+
|
mg/l
|
8
|
0,048
|
2,597
|
0,640
|
0,270
|
0,850
|
|
NH4+
|
mg/l
|
8
|
0,018
|
1,812
|
0,330
|
0,090
|
0,610
|
|
TZ+
|
méq/l
|
8
|
0,064
|
4,941
|
0,137
|
0,570
|
1,620
|
|
PO43-
|
mg/l
|
8
|
0,005
|
4,351
|
1,070
|
0,470
|
1,520
|
|
F-
|
mg/l
|
8
|
0,001
|
0,025
|
0,010
|
0,010
|
0,010
|
|
Cl-
|
mg/l
|
8
|
0,020
|
13,576
|
1,950
|
0,150
|
4,710
|
|
NO3-
|
mg/l
|
8
|
1,311
|
39,927
|
12,550
|
9,150
|
13,500
|
|
SO42-
|
mg/l
|
8
|
0,004
|
9,151
|
2,590
|
1,870
|
2,970
|
|
HCO3-
|
mg/l
|
8
|
0,490
|
65,368
|
41,400
|
7,870
|
64,760
|
|
TZ-
|
méq/l
|
8
|
0,056
|
4,030
|
0,990
|
0,600
|
1,310
|
|
SiO2
|
mg/l
|
8
|
0,486
|
0,894
|
41,40
|
7,870
|
64,760
|
|
TDS
|
mg/l
|
8
|
4,306
|
323,338
|
79,83
|
47,630
|
105,160
|
|
BI
|
%
|
8
|
-8,000
|
10,000
|
2,000
|
6,000
|
7,000
|
|
Mn
|
mg/l
|
8
|
0,002
|
0,008
|
0,010
|
0,010
|
0,000
|
|
Fe
|
mg/l
|
8
|
0,024
|
0,337
|
0,200
|
0,210
|
0,11
|
|
Cu
|
mg/l
|
8
|
0,030
|
0,094
|
0,030
|
0,020
|
0,04
|
|
Cd
|
mg/l
|
8
|
0,002
|
0,004
|
0,002
|
0,002
|
0,001
|
|
Al
|
mg/l
|
8
|
0,101
|
1,553
|
0,340
|
0,170
|
0,53
|
Légende : CE= conductivité
électrique ; OD=oxygène dissous ; BI=balance ionique TDS=
total des solides dissous ; NE=nombre d'échantillons ;
Min=minimum ; Max=maximum ; Moy=moyenne.
3%
Ca+ Mg2+ Na+ K+ Cl- NO3 SO42- HCO3-
16%
3%
1%
4%
52%
5%
16%
30
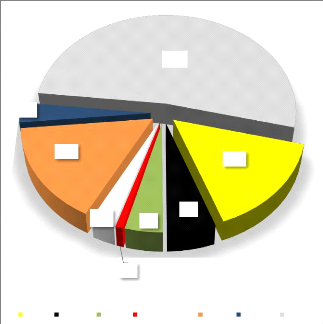
III.1.2.6. Typologie des eaux
Les eaux du lac Mboli, de la source et du forage
présentent de manière générale des
différentiations quantitatives entre les éléments majeurs
cationiques et anioniques. La méthode de camembert nous permet de
visualiser les proportions en pourcentage des éléments majeurs
présents dans ces eaux. La classification d'ordre de grandeur
décroissant de ces éléments d'après les
concentrations moyennes d'ensemble est la suivante (Fig. 11) :
HCO3- >NO3- > Ca2+
> Mg2+ > Na+ > SO42- >
Cl- > K+
Les différentes concentrations des
éléments chimiques majeurs des eaux du lac de la source et du
forage sont reportées sur le diagramme de Piper (1994). Ce diagramme a
permis de mettre en évidence les différents facies hydrochimiques
de ces eaux. De ce fait, il en ressort deux faciès hydrochimiques (Fig.
12) :
- le faciès chloruré et sulfaté calcique et
magnésien qui représente 62,5 % des eaux ; - le faciès
bicarbonaté calcique et magnésien qui représente 37,5 %
des eaux
31
Figure 11. Répartition d'ensemble des
éléments chimiques majeurs dans les eaux du lac Mboli, de la
source et du forage.
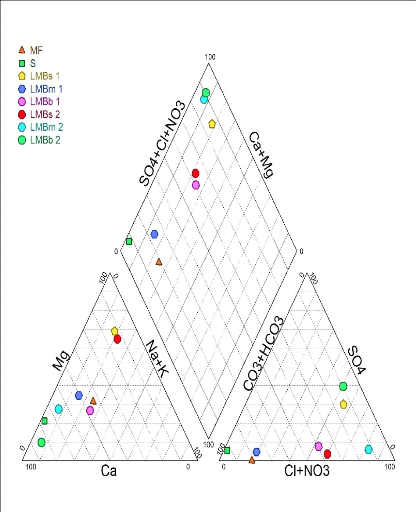
Figure 12. Diagramme de piper (1944)
représentant le faciès des eaux du lac Mboli de la source et du
forage.
32
CONCLUSION
Sur le plan physique, les eaux du lac Mboli,
de la source et du forage sont dans l'ensemble acides à faiblement
acides ; la température moyenne de ces eaux est de 29,58 °C ;
d'après les valeurs de leurs conductivités, elles sont dans
l'ensemble faiblement minéralisées. Sur le plan chimique, les
eaux du lac Mboli, de la source et du forage dans l'ensemble renferme plusieurs
éléments traces métalliques (Mn, Fe, Cu, Cd, et le Al) ;
les concentrations des éléments majeurs reportées sur le
diagramme de piper révèlent deux principaux facies (le
faciès chloruré et sulfaté calcique et magnésien,
le faciès bicarbonaté calcique et magnésien). Chapitre
subséquent se propose d'interpréter et discuter les
résultats.
CHAPITRE IV : INTERPRETATION ET
DISCUSSION
34
INTRODUCTION
Les études décrites dans ce chapitre se
proposent d'interpréter et discuter les résultats obtenus
à partir des analyses physico-chimiques des échantillons d'eau.
Il est donc question de manière générale, de donner une
signification aux résultats obtenus. Pour cela, les variations
quantitatives, la méthode hydrochimique d'analyse statistique
multivariée ont été utilisés.
V.1. DISTRIBUTION DES PARAMETRES PHYSICO-CHIMIQUES DANS
LES EAUX ETUDIEES
Il est question de montrer comment est distribué les
paramètres physico-chimiques des eaux du lac, de la source et du forage.
Pour ce qui est du lac, le paramètre profondeur sera pris en compte.
V.1.1. Paramètres physiques
V.1.1.1. pH
Le pH mesure l'alcalinité et l'acidité d'un
milieu, c'est-à-dire de la concentration en ions d'hydrogène
(H+). L'échelle des pH s'étend en pratique de 0
(très acide) à 14 (très alcalin), la valeur médiane
7 correspond à une solution neutre à 25° C. Le pH des eaux
naturelles est lié à la nature des terrains traversés. La
mesure est importante, car le pH régit un grand nombre
d'équilibres physico-chimiques (Ngaram, 2011).
Les échantillons d'eau obtenus des deux stations de
prélèvement dans le lac Mboli montrent que la colonne d'eau issue
de la station 1 a un pH acide à faiblement acide (4,96 à 6,84).
La valeur acide se trouve à la base de la colonne (LMBb1), tandis que
les valeurs faiblement acides se trouvent respectivement au milieu et à
la surface de la colonne d'eau (LMBm1, LMBs1). Au niveau de la station 2,
l'évolution du pH est pratiquement la même que dans la colonne
d'eau de la station 1, c'est-à-dire acide à faiblement acide
(5,30 à 6,62), avec à la base un pH acide (LMBb2), au milieu et
à la surface des valeurs de pH faiblement acides (LMBm2,
LMBs2). Le caractère acide pourrait provenir du type
lithologique sous-jacente (grès ferrugineux) d'une part, et d'autre part
de la décomposition des matières organiques et la présence
de CO2 d'origine atmosphérique. Le caractère acide pourrait aussi
provenir d'une précipitation des hydroxydes qui génère une
acidité du milieu et consomme les ions et les métaux (Miramond et
al., 2006). L'acidité plus élevée à la
base des colonnes d'eau montre une minéralisation importante des
particules organiques qui provoque l'abaissement du pH (Alayat
35
et al. (2013) par rapport au milieu et à la
surface des colonnes d'eau (Fig. 13). Le pH est un facteur important dans le
système biologique, chimique de l'environnement aquatique (Ngaram,
2011), il influe alors sur le développement de la vie aquatique.
D'après les valeurs obtenues des deux colonnes d'eau, seule le fond de
chaque colonne pourrait rencontrer des difficultés de
développement de la vie aquatique (Tab. 3. De plus, les faibles valeurs
de pH affectent de façon indirecte la santé humaine puisqu'elles
favorisent la dissolution des métaux lourds qui peuvent avoir des
conséquences défavorables sur des personnes (Sorlini et
al., 2013). Par ailleurs, les travaux de Alayat et al. (2013)
dans le lac Oubeira en Algérie ont montré que le pH est basique
et reste constant dans toute la colonne d'eau (8-9), cette alcalinité
est due aux populations phytoplanctoniques et en partie à la
précipitation de carbonates, notamment de la calcite à partir des
bicarbonates. Par contre les travaux réalisés par Issa (2014)
dans le lac Nyos au Cameroun ont montré que le pH dans ces eaux est
acide (5,9 en moyenne), avec des valeurs plus faibles au fond de la colonne
d'eau. L'acidité le lac Nyos est due à la dissolution du CO2
(H2CO3).

Station 1
pH
0 2 4 6 8
Profondeur (cm)
0 50 100 150 200 250 300 350 400
Station 2
pH
0 2 4 6 8
Profondeur (cm)
200
250
300
100
150
50
0
Figure 13. Évolution du pH dans les
colonnes d'eau.
Tableau 3. Niveau du pH et qualité de
l'eau (Anonyme, 2009)
|
pH < 5
|
- Impropre à une vie aquatique normale, ruisseaux des
régions granitiques, issus de tourbières ou à cours
forestier,
|
|
5 < pH < 6
|
- Peu favorables à la vie aquatique, cours d'eau à
substrat acide,
|
|
6 < pH < 8
|
- Situations les plus favorables à la vie aquatique,
|
|
8 < pH < 9
|
- Eaux closes ou assimilées, développements
végétaux importants, situation favorable à la vie
aquatique,
|
|
pH > 9
|
- Eaux peu favorables à la vie aquatique ou valeurs
passagères dues à la photosynthèse.
|
36
En ce qui concerne la variation spatiale du pH au niveau des
eaux souterraines (forage et source), il est nettement plus bas dans les eaux
de la source qu'au forage (Fig. 14). Dans l'ensemble, ces eaux sont acides.
Seul le pH mesuré dans les eaux du forage se trouve à une valeur
acceptable par les normes de l'OMS et ANOR (6,5-8,5 et 6,5-9). Sur la plan
naturel, l'acidité au niveau de la source ne de devrait pas être
différente de celle du forage du fait qu'ils ont la même nature
lithologique. En effet, la qualité physico-chimique des eaux
souterraines peu profondes dépend bien souvent de l'activité
humaine, tant agricole que domestique, (Close et al., 1989 ; Hassoun et al.,
2006), du type de végétation recouvrant le sol (Mahendrappa,
1989). Cette diminution du pH dans la source serait donc due à des
apports supplémentaires en eaux acides (CRE, 2009), notamment les eaux
de pluies acides, les eaux de ruissellement chargées de matières
organiques en décomposition, car la source est exposée à
toute pollution de par son ouverture directe avec l'atmosphère. La
valeur moyenne du pH de ces eaux est supérieure à celle obtenu
par Messolo (2020) dans les eaux souterraines de la localité de Nkozoa,
par contre elle est inférieure à celle obtenue par Emmachoua
(2018) dans le bassin versant de Makenéné.
Echantillons
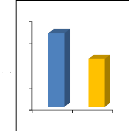
pH
8
MF1 S
6
4
2
0
Figure 14. Variation du pH dans les eaux
souterraines. V.1.1.2. Conductivité
électrique
La conductivité désigne la
propriété qu'a une solution à conduire le courant
électrique. Cette mesure permet d'évaluer rapidement le
degré de minéralisation d'une eau, c'est-à-dire la
quantité de substances dissoutes ionisées qui y sont
présentes (Madjiki et al., 2013).
En ce qui concerne le lac Mboli, les valeurs de
conductivités mesurées au niveau des deux colonnes d'eau sont
inférieures à 100 ìS/cm. Ces eaux ont une très
faible minéralisation (Detay 1993). Ces conductivités montrent
une minéralisation insuffisante des eaux dans les colonnes (Nisbet et
Vernaux, 1970). Les deux stations de mesure ont pratiquement la même
évolution dans la colonne d'eau (Fig. 15). D'une
façon générale, les résultats montrent que la
conductivité est constante de la base de la colonne jusqu'à la
surface pour les deux stations de mesure. Il y'a donc une
homogénéité de la conductivité dans la colonne. Ces
faibles conductivités électriques des eaux dans le lac seraient
à mettre en relation avec la composition minéralogique des roches
drainées dans le lac (grès) et une dilution par les eaux de pluie
car l'échantillonnage de ces eaux a été effectué en
période pluvieuse (mars 2020). Par ailleurs, ces valeurs de
conductivité sont de même ordre de grandeur que celles
mesurées par Ngafack (2014) dans le lac Ossa situé dans la
même localité, mais par contre elles sont inférieures
à celles obtenues par madjiki et al (2013) dans lac municipal
d'Ebolowa (Sud-Cameroun) situé en zone métamorphique. Ces
remarquent montrent que la signature chimique des eaux dépend
étroitement de la formation géologique qu'elle draine (Andre et
al., 2005 ; Xing et al., 2013).
Station 1
conductivité (ìS/cm)
27,3 27,4 27,5 27,6 27,7

Profondeur (cm)
200
250
300
350
400
100
150
50
0
Station 2
conductivité (ìS/cm)
27,1 27,2 27,3 27,4 27,5
|
Profondeur (cm)
|
0 50 100 150 200 250 300
|
|
37
Figure 15. Évolution de la
conductivité électrique dans les colonnes d'eau.
Pour ce qui est des eaux souterraines (source et forage), la
conductivité est plus basse dans les eaux source que ceux du forage avec
une différence de 4,32 uS/cm. Dans l'ensemble ces conductivités
sont inférieures à 100 uS/cm (Fig. 16). Ce qui traduit une
minéralisation très faible de ces eaux (Detay, 1993). Ces faibles
conductivités seraient liées à la force ionique qui
découle des formations traversées par ces eaux (Loukman et
al., 2017). Les valeurs de conductivités mesurées dans
les eaux de la source et du forage sont inférieures aux valeurs
recommandées par l'OMS et l'ANOR pour les eaux de boisson
(respectivement 1500 et 1000 uS/cm). Ces conductivités sont de
même ordre de grandeur que celles obtenues par Ngounou (2018) dans les
eaux des rivières de Garoua Sambé (Est Cameroun) par contre elles
sont inférieures aux valeurs obtenues par Ngouh et al. (2020)
dans les eaux de l'aquifère à nappe libre du bassin versant du
Nkié (Yaoundé-Cameroun).
Echantillons

Conductivité (uS/cm)
20
MF1 S
55
50
45
40
35
30
25
38
Figure 16. Variation de la conductivité
dans les eaux souterraines. V.1.1.3. Température
La température est l'un des facteurs qui
contrôlent l'essentiel des activités biologiques et
écologiques des êtres vivants. La température de l'eau est
un élément essentiel dans le fonctionnement des systèmes
aquifères (Brooke et Colby, 1980). Elle joue un rôle important par
exemple en ce qui concerne la solubilité des sels et des gaz dont, entre
autres, l'oxygène nécessaire à l'équilibre de la
vie aquatique (IBGE, 2005). C'est un paramètre qui dépend des
facteurs climatologiques (Ben Charrada, 1992) mais aussi de la géologie
et des activités qui se déroulent sur le plan d'eau.
Les températures mesurées dans les profils
verticaux de chaque station de prélèvement du lac Mboli, montrent
que pour ce qui est de la station 1, la température varie peu dans la
colonne d'eau (Fig. 17). La valeur la plus basse dans cette station se trouve
à la base de la colonne d'eau (LMBb1) tandis qu'on note une
température constante du milieu jusqu'à la surface de la colonne
d'eau (LMBm1, LMBs1). La variation thermique dans cette station est d'amplitude
2,6° C. Il est donc difficile de parler de stratification thermique dans
cette colonne d'eau, néanmoins s'il fallait considérer cette
légère variation on dira qu'il y'a stratification thermique entre
les couches supérieures de mesure et le fond de la colonne d'eau. Cette
stratification thermique serait alors due à un réchauffement par
les rayons solaires des eaux de la surface par rapport aux eaux de profondeurs.
En ce qui concerne la station 2 on note de légères
disparités de température entre les niveaux de mesure dans la
colonne d'eau. La valeur
la plus importante est celle mesurée en surface (,
LMBs2) et la valeur la plus basse est celle obtenue au milieu de la
colonne d'eau (LMBm2). Cette différence de température est de
l'ordre de 1,5° C. Jean-René et Daniel (1994) expliquent que les
variations de la température des eaux ont pour origine les milieux
frontaliers. En effet, la profondeur moyenne (3 m) du lac Mboli, le brassage
des eaux dû aux vents, aux activités de pêche, de navigation
sur le plan d'eau du lac, crée un fort hydrodynamisme qui favorise le
mélange des couches d'eau de surface et des couches d'eaux
sous-jacentes, d'où les faibles disparités de température
observée dans la colonne d'eau. En outre, les rayons du soleil
traversent la faible épaisseur d'eau et la réchauffe de
façon homogène (Séraphin et al., 2008 ;
Jean-René et Daniel, 1994). Ces résultats sont pratiquement de
même ordre que ceux obtenus par Nziéleu et al. (2016) ;
Ngafack (2014), respectivement dans le complexe du lac Ossa (littoral Cameroun)
à la même période, et sont supérieures à ceux
obtenus par Oumar et al. (2014) dans les lacs Birni et Dang
(région de l'Adamaoua, Cameroun).
Station 1
Température (° C)
30,5 31 31,5 32 32,5

Profondeur (cm)
200
250
300
350
400
100
150
50
0
Station 2
Température (° C)
30,5 31 31,5 32 32,5 33
|
Profondeur (cm)
|
0 50 100 150 200 250 300
|
|
39
Figure 17. Évolution de la
température dans les colonnes d'eau.
En ce qui concerne les eaux souterraines, la
température varie peu, la valeur la plus grande se trouve au niveau de
la source avec une différence de 0,9° C avec la valeur
mesurée dans les eaux du forage (Fig. 18). L'OMS n'a recommandée
aucune valeur pour la température de l'eau de boisson. Par ailleurs,
L'eau froide est généralement plus appréciée que
l'eau chaude
40
et la température aura un impact sur
l'acceptabilité d'un certain nombre de constituants inorganiques et de
contaminants chimiques qui peuvent affecter le goût. Une
température élevée de l'eau stimule la croissance des
micro-organismes et peut accroître les problèmes liés au
goût, à l'odeur, à la coloration et à la corrosion
(OMS, 2017). Ces valeurs de température sont supérieures aux
valeurs obtenues par Ngouh et al. (2020) dans les eaux de
l'aquifère à nappe libre du bassin versant du Nkié
(Yaoundé-Cameroun) ; Yaka et al. (2020) dans les eaux
souterraines de quelques quartiers de Yaoundé VII (centre Cameroun).
Températures (°C)
30
25
20
15
10
Echantillons
MF1 S
Figure 18. Variation de la température
dans les eaux souterraines. V.1.2. Paramètres
chimiques
V.1.2.1. Éléments traces
métalliques
Dans le lac, en ce qui concerne la colonne d'eau du point
d'échantillonnage de la station 1, le Mn est présent dans toute
la colonne d'eau, avec une évolution en dents de scie (Fig. 19). La plus
faible valeur de Mn est enregistrée à la base de la colonne d'eau
et la plus forte au milieu. Quant à La concentration de Fe, elle est
nettement plus élevée que celle du Mn, on note une
évolution de Fe qui décroit de la surface jusqu'au fond de la
colonne d'eau. Par contre le Cu n'est que présent à la surface et
le Cd à la surface et à la base à des concentration
relativement faibles par rapport aux autres ETM, tant dis que l'Al est
présent au milieu et au fond de la colonne d'eau. En moyenne, La
distribution quantitative des teneurs en métaux dans la colonne d'eau
est de l'ordre suivant : Fe > Al > Cu > Mn > Cd. Pour ce qui est de
la colonne d'eau du point d'échantillonnage de la station 2 (Fig. 19),
le Mn est aussi présent dans toute la colonne
41
d'eau, avec des valeurs qui décroient du fond
jusqu'à la surface, on note néanmoins de légères
disparités à chaque niveau de la colonne d'eau. Pour le Fe, la
concentration la plus forte est relevée à la base et la
concentration plus faible milieu de la colonne d'eau. Quant au Cu et le Al,
leur présence n'est que marquée au fond de la colonne d'eau
à une teneur faible pour le Cu mais forte pour le Al. Le Cd par contre
est relevé en très faible quantité dans l'ensemble de la
colonne d'eau. En moyenne, La distribution quantitative des teneurs en
métaux dans cette colonne d'eau est de l'ordre suivant : Al > Fe >
Cu > Mn > Cd.
De manière générale, le comportement des
ETM dans les deux stations de mesure sont pratiquement les mêmes, avec
une prédominance de Fe et Al. On note l'absence de certains ETM (Al, Cu,
Cd) soit à la surface, au milieu ou à la base de la colonne
d'eau. Afin d'évaluer le risque associé à la
présence des contaminants métalliques dans la colonne d'eau, les
concentrations mesurées ont été comparées aux
critères de l'agence américaine de la protection de
l'environnement (USEPA, United States Environmental Protection Agency) en
fonction du critère maximum concentration (CMC) et le critère de
concentration continue (CCC). Le CMC représente la concentration
maximale d'une substance à laquelle les organismes aquatiques peuvent
être exposés brièvement sans être gravement
touchés, tandis que le CCC représente la concentration la plus
élevée d'une substance ne produisant aucun effet néfaste
sur les organismes aquatiques y étant exposés quotidiennement
pendant toute leur vie (USEPA, 2006). Certains ETM se trouvent à des
concentrations supérieures aux teneurs fixées par l'USEPA pour le
CMC et le CCC dans certains compartiments de la colonne. La colonne d'eau issue
de la station 1 montre que, la teneur de Al (au milieu et base), Cd (à
la base) sont supérieures au seuil de CCC, tandis que la concentration
de Cu (à la surface) dépasse les teneurs seuils de CMC et CCC
(tableau 4). Pour ce qui est de la station 2, les concentrations de Al et de Cu
(à base) dépassent les teneurs seuils de CMC et CCC tant dis que
la teneur de Cu au milieu de la colonne d'eau est supérieure au seuil
CCC (Tab. 4). Cela montre que les ETM présents à chaque niveau de
la colonne d'eau (surface, milieu, base) dépassant le seuil CMC et de
CCC présentent un risque toxique pour les organismes aquatiques.
Par ailleurs ces ETM ont été retrouvés
dans les eaux de nombreux lac africains à des concentrations variables,
il s'agit notamment du lac Mariout en Égypte (Saad, 1985), le lac George
en Ouganda (Bugenyi, 1982) et le lac McIlwaine au Zimbabwe (Greichus et
al., 1978a).

Profondeur (cm)
200
250
300
100
150
50
0
Mn Fe Cu Cd Al
0 500 1000 1500 2000
Station 2

Profondeur (cm)
200
250
300
350
400
100
150
50
0
Mn Fe Cu Cd Al
0 100 200 300 400
Station 1
42
Figure 19. Évolution des ETM dans les
colonnes d'eau.
Tableau 4. Comparaison des concentrations des
ETM présent dans la colonne des deux stations de
prélèvement dans le lac Mboli aux lignes directrices de l'USEPA :
CMC et CCC (USEPA, 2006)

|
ETM (ug/l)
|
Al
|
Cd
|
Cu
|
Fe
|
Mn
|
|
USEPA
|
CMC
|
750
|
4,3
|
13
|
-
|
-
|
|
CCC
|
87
|
2,2
|
9
|
1000
|
-
|
|
LMBs 1
|
0
|
2
|
30
|
287
|
7
|
|
LMBm 1
|
101
|
0
|
-
|
223
|
8
|
LMBm 2
LMBb 2
LMBs 2
1553
-
-
2
2
3
53
-
-
337
192
24
5
7
8
LMBb 1
232
4
-
58
2
Station 1
Station 2
Pour ce qui concerne les eaux souterraines, le comportement
des ETM est sensiblement le même ou présente de faibles
disparités quantitatives pour certains éléments. La
concentration de Mn mesurée dans les eaux du forage est identique
à celle mesurée dans la source. La teneur de Fe dépasse
largement celle de la source avec une différence de 73 ug/l, tandis que
la concentration de Cu dans la source est supérieure à celle
obtenue au forage avec une différence de 16ug/l. On n'observe presque
pas de disparité entre la concentration de Cd obtenue au forage et celle
mesurée dans la source, on note juste une petite différence de 1
ug/l. La teneur de Al dans les eaux souterraines se trouve en quantité
largement supérieure par rapport aux autres
43
ETM, sa concentration au forage est deux fois
supérieure celle obtenue dans la source. L'ordre d'abondance est : Al
> Fe > Cu > Mn > Cd (Fig. 20). Seule la concentration de Al se
trouve supérieure à la norme de l'OMS qui recommande une
concentration de Al pour les eaux de boisson inférieure à 200
ug/l (OMS 2011). Cela pourrait être dû aux phénomènes
d'hydrolyse de la roche riche en Al. Ces résultats sont
inférieurs à ceux obtenus par Tohouri et al. (2016) dans
les eaux de surface de la région de Bonoua (Sud-Est de la Côte
d'Ivoire), par contre ils sont supérieurs aux résultats obtenus
par Mbé (2020) dans les eaux souterraines de Nkozoa (Yaoundé,
Centre Cameroun), excepté le Mn.
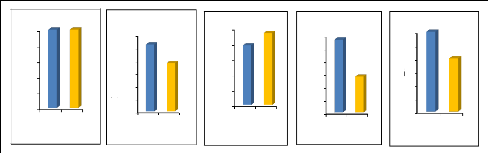
Mn (ug/l)
4
2
5
3
0
1
MF1 S
Échantillons
MF1 S Échantillons
300
250
200
Fe (ug/l)
150
100
50
0
MF1 s
Échantillons
Cu (ug/l)
100 80
60 40
20
0
MF1 s Échantillons
Al (ug/l)
400
200
600
500
300
100
0
MF1 s Échantillons
Cd (ug/l)
2,5
0,5
,5
2
3
0
1
Figure 20. Variation des ETM dans les eaux
souterraines. 1.2.2. Cations majeurs
Pour ce qui est des eaux du lac, les cations majeurs et la
TZ+ ont une évolution hétérogène dans la
colonne d'eau dans l'ensemble (Fig. 21). Pour la station 1, on constate que les
teneurs des cations majeurs Ca2+, Mg2+, Na+,
K+ et TZ+ au milieu de la colonne d'eau sont toutes
supérieures aux concentrations mesurées à la surface et la
base. On note des concentrations de Ca2+, Mg2+ et
Na+ au milieu, largement supérieures par rapport à la
surface et à la base de la colonne d'eau, tandis que les teneurs de
K+ et TZ+ obtenues au milieu sont faiblement
supérieures aux teneurs obtenues à la surface et à la base
de la colonne d'eau. La station 2 quant à elle, présente le
même comportement dans la colonne d'eau que la précédente.
Les teneurs les plus élevées des cations majeurs
(Ca2+, Mg2+, Na+, K+) et
TZ+ se trouvent toutes au milieu de la colonne d'eau.
Néanmoins on constate qu'ils se trouvent dans l'ensemble à des
faibles concentrations par rapport aux autres. Le Ca2+ au milieu
enregistre la concentration la plus élevée des cations, tandis
que TZ+ est inférieur à 1 méq/l dans toute la
colonne d'eau. Les concentrations des cations majeurs et TZ+
obtenues dans les deux stations d'échantillonnage du lac Mboli sont
largement inférieures à ceux obtenues par Emmachoua (2017) dans
les eaux du bassin versant de Makénéné
(Centre-Cameroun).
Au niveau des eaux souterraines, les cations majeurs et
TZ+ dans l'ensemble présentent des concentrations faibles
à l'exception du Ca2+ qui est largement supérieur aux
autres (Fig. 22). La teneur la plus élevée de Ca2+ est
rencontrée au niveau des eaux de la source, par contre celles de
Mg2+ et Na+ sont rencontrées des eaux du forage.
La teneur de K+ au niveau de la source comme au forage est
inférieur à 1mg/l. TZ+ quant à lui est
sensiblement égale dans les eaux de source et du forage. La
concentration des cations dans les eaux souterraines se trouvent a des teneurs
acceptables par les normes de l'OMS et ANOR. Les résultats obtenus dans
ces eaux sont dans l'ensemble similaire à ceux abstenus par Ngouh et
al. (2020) dans les eaux de source du bassin versant du Nkié
(Yaoundé-Cameroun).
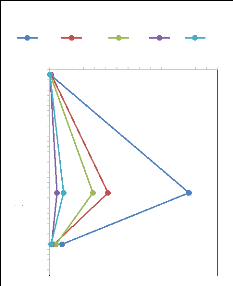
Profondeur (cm)
400
300
350
200
250
100
150
50
0
Ca2+ Mg2+ Na+ K+ TZ+
0 20 40 60
Station 1
(En jig/l)

Profondeur (cm)
200
250
300
100
150
50
0
Ca2+ Mg2+ Na+ K+ TZ+
0 2 4 6 8 10
Station 2
(En jig/l)
44
Figure 21. Évolution des cations et
TZ+ dans les colonnes d'eau.

Mg2+ (mg/l)
4
6
2
0
Na+ (mg/l)
4
8
6
2
0
K+ (mg/l)
0,8
0,6
0,4
0,2
0
1
TZ+ (méq/l)
1,38
1,36
1,34
1,32
1,28
1,26
1,4
1,3
25
20
Ca2+ (mg/l)
15
10
5
0
MF1 S
Échantillons
MF1 S Échantillons
MF1 S
Échantillons
MF1 S
Échantillons
MF1 S Échantillons
45
Figure 22. Variation des cations et
TZ+ dans les eaux souterraines.
V.1.2.3. Anions majeurs
Pour les eaux du lac, l'évolution des anions et
TZ- dans la colonne d'eau de la station 1 est sensiblement la
même pour tous les éléments (Fig. 23). Les concentrations
les plus élevées se situent au milieu de la colonne d'eau. On
note néanmoins la concentration de HCO3- au milieu, largement
supérieure par rapport aux autres anions (Cl-,
NO3-, SO42-). La TZ- est très faible
à la surface et à la base. Dans l'ensemble, les concentrations
les plus basses sont rencontrées à la surface de la colonne
d'eau. Au niveau de la station 2, l'évolution des anions et
TZ- dans la colonne d'eau est pratiquement la même que dans la
station 1 (Fig. 24). Les concentrations les plus importantes sont
rencontrées au milieu de la colonne d'eau à l'exception du
SO42- dont la concentration la plus élevée se situe
à la base de la colonne d'eau. La concentration d'ensemble la plus
élevée est celle du NO3- au milieu de la colonne
d'eau. La teneur en Cl- est inférieure à 1 mg/l, il en
est de même pour la TZ- qui n'atteint pas 1 méq/l dans
toute la colonne d'eau. Dans l'ensemble, ces résultats sont largement
inférieurs à ceux obtenus par Emmachoua (2017) dans les eaux du
bassin versant de Makénéné (Centre-Cameroun).
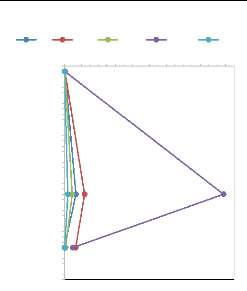
Profondeur (cm)
Cl- NO3- SO42- HCO3- TZ-
200
250
300
350
400
100
150
50
0
0 50 100 150 200
Station 1
(En mg/l)
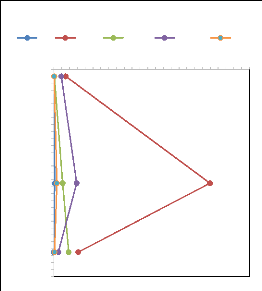
Profondeur (cm)
300
200
250
100
150
50
Cl- NO3- SO42- HCO3- TZ-
0
0 10 20 30 40 50
Station 2
(En mg/l)
46
Figure 23. Évolution des anions et
TZ- dans les colonnes d'eau.
Au niveau des eaux souterraines, les teneurs des anions sont
faibles et présentent un comportement dissemblable. La concentration de
Cl- est très faible, avec des valeurs n'atteignant pas 1 mg/l
à la source et au forage. Le NO3- à une teneur plus
élevée au forage. Le SO42- tant à disparaitre
au niveau du forage, tandis qu'au niveau de la source on rencontre une
concentration moyenne. Le HCO3- est l'anion majeur
prédominant de ces eaux, on y rencontre des concentrations largement
supérieures par rapport aux autres anions, néanmoins la
concentration la plus élevée se situe au niveau de la source.
Quant à la TZ-, les concentrations sont sensiblement
égales (Fig. 24). Les anions majeurs présents dans ces eaux se
trouvent à des concentrations acceptables par la norme de l'OMS et ANOR
pour les eaux de boisson. Ces résultats sont dans l'ensemble similaire
à ceux obtenus par Mfonka et al. (2015) dans les eaux du bassin
versant du Nchi dans le plateau Bamoun (Ouest Cameroun).

NO3- (mg/l)
15
10
5
0
CL- (mg/l)
0,8
0,6
0,4
0,2
0
1
HCO3- (mg/l)
66
64
62
60
58
56
54
TZ- (méq/l)
1,19
1,18
1,17
1,16
1,15
1,14
MF1 S
Échantillons
MF1 S Échantillons
MF1 S
Échantillons
4
3
2
1
SO42- (mg/l)
0
MF1 S
Échantillons
MF1 S
Échantillons
47
Figure 24. Variation des anions et
TZ- dans les eaux souterraines V.1.2.4. Autres
éléments en solutions (NH4+, PO43-,
F-)
En ce qui concerne les eaux du lac, la concentration de
NH4+ et de PO43- dans la station 1 est faible dans
l'ensemble par rapport aux autres, on rencontre les valeurs les plus
importantes dans la colonne d'eau respectivement au milieu et à la
surface, tant dis que les teneurs les plus basses sont observées
respectivement à la base de la colonne d'eau. Les concentrations
F- et SiO2 dans l'ensemble de la colonne d'eau sont
inférieures à 1 mg/l (Fig. 25). La distribution dans la station 2
montre que le NH4+, PO43-, F- et le SiO2 sont dans
l'ensemble faibles, dans la colonne d'eau, ils sont présents en traces
dans ces eaux à l'exception de la teneur de
PO43-rencontrée au milieu (Fig. 25). Les concentrations de
NH4+, PO43- et F- dans la colonne d'eau sont
dans l'ensemble similaires aux teneurs obtenues par Emmachoua (2017) dans les
eaux du bassin versant de Makénéné (Centre-Cameroun).
Cependant, on note des disparités entre la teneur de NH4+
dans la colonne d'eau du lac Mboli et les eaux du bassin versant de
Makénéné qui possède des concentrations largement
supérieures. Les teneurs de SiO2 dans la colonne d'eau sont largement
inférieures à celles obtenues par Mfonka et al. (2015)
dans les eaux du bassin versant du Nchi dans le plateau Bamoun (Ouest
Cameroun).
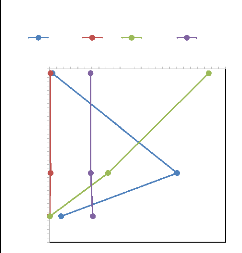
400
300
350
Profondeur (cm) 200
250
100
150
50
0
0 0,5 1 1,5 2 2,5
NH4+ F- PO43- SiO2
Station 1
(En mg/l)

Profondeur (cm)
200
250
300
100
150
50
0
NH4+ PO43- 0,001 SiO2
0 1 2 3 4 5
Station 2
(En mg/l)
48
Figure 25. Évolution d'autres
éléments en solution dans les colonnes d'eau.
Dans les eaux souterraines, les concentrations de
NH4+, PO43- F- et SiO2 sont relativement très
faible par rapport à d'autres paramètres chimiques mesurés
dans ces eaux. On les observe dans ces eaux pour l'ensemble sous forme de
trace. Par ailleurs, ils sont tous présents dans les eaux souterraines
à l'exception du F- au niveau de la source. Les plus fortes
concentrations sont rencontrées au forage (Fig. 26). Cependant, Les
concentrations NH4+, PO43-et F-
reconcentrées dans ces eaux se trouvent à des valeurs acceptables
par la norme de l'OMS. Par ailleurs, ces teneurs sont similaires à
celles obtenues par Emmachoua (2017) dans les eaux du bassin versant de
Makénéné (Centre-Cameroun).
|
NH4+ (mg/l)
|
0,4 0,3 0,2 0,1 0
|
|
MF1 S
Échantillons
|
PO43- (mg/l)
|
0,5 0,4 0,3 0,2 0,1 0
|
|
MF1 S
Échantillons
|
0,02
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F- (mg/l)
|
0,015
0,01
0,005
|
|
|
|
|
|
|
|
0
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
MF1 S
|
Échantillons
|
SiO2 (mg/l)
|
0,8 0,6 0,4 0,2 0
|
|
MF1 S
Échantillons
Figure 26. Variation d'autres
éléments en solution- dans les eaux souterraines.
49
V.1.2.5. Oxygène dissous
L'oxygène dissous est la quantité
d'oxygène présent en solution dans l'eau à une
température donnée. Dans le lac, la teneur en oxygène
dissous est un paramètre fondamental de la vie aquatique. Ainsi, la
concentration de l'oxygène dans l'eau est contrôlée par
plusieurs processus biologiques et chimiques, dont la photosynthèse et
la respiration. Pour la station 1, la teneur en oxygène dissous dans
l'ensemble varie peu dans la colonne d'eau. Les valeurs obtenues à la
surface et au milieu son pratiquement les mêmes tandis que la
concentration obtenue au fond de la colonne d'eau diminue
légèrement par rapport aux autres niveaux (Fig. 27). Pour ce qui
est de la station 2, la concentration en oxygène dissous dans l'ensemble
diminue légèrement par rapport à la station 1. Cependant,
le même comportement est observé dans la colonne d'eau. On note
des teneurs sensiblement égales à la surface et au milieu mais
par contre on observe une diminution à la base par rapport aux autres
niveaux de la colonne d'eau (Fig. 27). Les teneurs en oxygène dissous
d'une manière générale se maintiennent à des
valeurs supérieures à 5 mg/l, à l'exception de la base de
la colonne d'eau de la station 2, ce qui est bon pour
l'écosystème (Monkolo et al., 1993). Les valeurs
d'oxygène dissous obtenus dans les deux stations du lac Mboli sont dans
l'ensemble supérieurs à ceux obtenus par Madjiki et al.,
2013 dans les eaux du lac municipal d'Ebolowa (Sud-Cameroun).

Station 2
(En mg/l)
Station 2
(En mg/l)
O dissous
5,6 5,7 5,8 5,9 6 6,1 6,2
Profondeur (cm)
200
250
400
300
350
100
150
50
0
O dissous
0 2 4 6
Profondeur (cm)
200
250
300
100
150
50
0
Figure 27. Évolution oxygène
dissous dans les colonnes d'eau.
50
Dans les eaux souterraines, la teneur en oxygène
dissous est faible. La teneur la plus élevée est
rencontrée au niveau de la source (Fig. 28). Du fait de l'absence de vie
aquatique dans ces eaux ces teneurs sont négligeables. Cependant, un
appauvrissement en oxygène dissous des approvisionnements en eau peut
stimuler la réduction microbienne des nitrates en nitrites et des
sulfates en sulfures. Il peut également entraîner une augmentation
de la concentration de fer ferreux en solution avec, par la suite, un
changement de coloration au robinet quand l'eau est aérée. Aucune
valeur guide reposant sur des arguments sanitaires n'est recommandée.
Par ailleurs, des niveaux très élevés d'oxygène
dissous peuvent stimuler la corrosion des tuyaux métalliques (OMS,
2017).
MF1 S Échantillons
OD (mg/l)
4
0
3
2
1
Figure 28. Variation de l'oxygène dissous
dans les eaux souterraines. V.1.2.6. Total des solides dissous
(TDS)
Dans les eaux du lac, on observe une évolution de la
TDS en dents de scie dans la colonne d'eau au niveau de la station 1 et 2. pour
la station 1, le pic est rencontré au milieu tandis que la teneur la
plus faible se situe à la surface. Pour ce qui est de la station 2, les
teneurs de TDS dans la colonne d'eau, sont dans l'ensemble inférieures
à celles obtenues au niveau de la station 1. La concentration la plus
forte se situe au milieu tandis que la concentration la plus faible se situe
à la base (Fig. 29). Cette évolution en dents de scie de la TDS
au niveau des deux stations montre
l'hétérogénéité des phénomènes
de minéralisation dans la colonne d'eau. Le niveau de la colonne d'eau
ayant une TDS élevée montre qui s'y déroule les
phénomènes de minéralisation plus important par rapport
aux autres niveaux de la colonne d'eau. En moyenne, la TDS de ces eaux est
largement supérieures à celle obtenue par Messolo (2020) dans les
eaux de l'étang de Nkozoa (Centre Cameroun).
Profondeur (cm) 0 50 100 150 200 250 300 350 400
0 200 400
Station 1
TDS
Station 2
TDS
0 50 100
|
Profondeur (cm)
|
0 50 100 150 200 250 300
|
|
51
Figure 29. Évolution de la TDS dans les
colonnes d'eau.
Pour les eaux souterraines, on observe juste une
légère différence entre la source et le forage.
Néanmoins, la teneur la plus élevée est rencontrée
au niveau du forage (Fig. 30). Par ailleurs ces teneurs sont dans l'ensemble
inférieures à celles obtenues par Yaka et al. (2020)
dans les eaux souterraines de quelques quartiers de Yaoundé VII
(Cameroun), par contre elles sont supérieures aux teneurs obtenues par
Messolo (2020) dans les eaux souterraines de Nkozoa (Centre Cameroun).
MF1 S
Échantillons
TDS (mg/l)
99
98
97
96
95
94
93
92
Figure 30. Variation de la TDS dans les eaux
souterraines. V.1.2.7. Facies hydrogéochimiques
Pour les deux stations de prélèvements des eaux
dans la colonne d'eau associé aux échantillons des eaux
souterraines, on constate dans l'ensemble que, les pourcentages de
NO3-et le HCO3- sont les plus élevés (Fig.
31). L'observation des proportions de ces éléments
52
majeurs et le diagramme de Piper (Fig. 12) nous a permis de
visualiser les différents faciès hydrogéochimiques
auxquels appartient chaque échantillon d'eau. Il en ressort que :
- le faciès chloruré et sulfaté calcique
et magnésien qui est le plus représenté de ces eaux est
rencontré uniquement au niveau des deux stations de
prélèvements des eaux du lac Mboli à l'exception de
l'échantillon (LMBm 1) de la station 1 ;
- le faciès bicarbonaté calcique et
magnésien est rencontré au niveau des eaux souterraines mais
aussi dans l'échantillon issu du lac (LMBm 1)
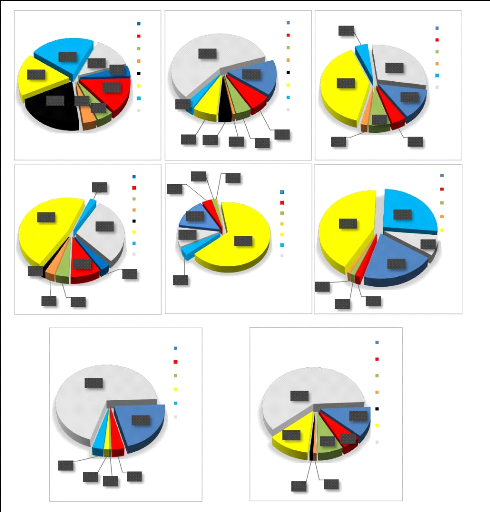
17%
1%
47%
LMBs 2 Ca
3% 4%
20%
3%
22%
LMBs 1 Ca
Mg Na
10%
4%
1%
70%
13%
5%
2%
30%
15%
1%
4%
S
3%
4%
21%
Mg Na K Cl NO3 SO4 HCO3
Cl NO3 SO4 HCO3
K
4%
4%
Ca
Mg
Na
NO3
HCO3
SO4
3%
10%
7% 4%
14%
1% 1%
58%
LMBm 1 Ca
Mg Na
1%
66%
15%
5%
LMBm 2
7%
Ca Mg Na K NO3 SO4 HCO3
12%
Cl NO3 SO4 HCO3
K
60%
1%
1%
MF Ca
8%
1%
2%
1%
40%
4%
43%
5%
13%
1%
7%
LMBb 1
LMBb 2 Ca
Mg Na
Mg Na
NO3
K
Cl-
HCO3
29%
20%
26%
13%
5%
8%
Ca Mg Na K
SO4 HCO3
NO3
K
Figure 31. Proportions des
éléments chimiques majeurs
53
V.2. ORIGINE DES ÉLÉMENTS CHIMIQUES
PRESENTS DANS LES EAUX DU LAC ET LES EAUX SOUTERRAINES
V.2.1. Analyse statistique multi-variée
Pour apporter des explications sur le fonctionnement
hydrogéochimique des eaux étudiées ainsi que la
connaissance des principales origines des paramètres physico-chimiques,
l'analyse statistique multi-variée a été
effectuée.
V.2.1.1. Matrice de corrélation
La matrice de corrélation présentée dans le
tableau 5 avec un niveau de signification Alpha = 0,05 est appliquée au
21variables notamment : pH, T, CE, OD, Ca2+, Mg2+,
Na+, K+, NH4+, PO43-,
F-, SiO2, HCO3- Cl-, NO3-,
SO42-, Fe, Al, Cu, Mn, Cd.
La matrice de corrélation met en évidence de
bonne corrélation entre plusieurs ions. C'est le cas observé
entre :
- les ions Ca2+ et les ions Mg2+ (0,96),
K+ (0,88), Na+ (0,87), NH4+ (0,91),
HCO3- (0,98),
Cl- (0,91), SO42- (0,87) ;
- les ions Mg2+ et les ions K+ (0,96),
Na+ (0,96), NH4+ (0,99), HCO3- (0,97),
Cl- (0,97),
SO42- (0,84) ;
- les ions Na+ et les ions K+ (0,98),
NH4+ (0,96), HCO3- (0,92), Cl- (0,91) ;
- les ions K+ et les ions NH4+ (0,98),
HCO3- (0,89), Cl- (0,94) ;
- les ions NH4+ et les ions (0,98), HCO3-
(0,93), Cl- (0,99), SO42- (0,83);
- les ions Cl- et les ions SO42- (0,87),
HCO3- (0,92) ;
- les ions PO43- et les ions F- (0,81) ;
- les ions SO42- et les ions HCO3- (0,81)
;
- le SiO2 et Al (0,88) ;
- la CE et le Cu (0,85) ;
- la température et l'oxygène dissous (0,85).
De même, on rencontre des corrélations moyennes
entre certains ions. C'est le cas observé entre :
- les ions Na+ et les ions SO42- (0,70) ; -
les ions K+ et les ions SO42- (0,74) ; - les ions
PO43-et les ions NO3- (0,76).
54
Ces différentes corrélation
inter-éléments traduisent ainsi leurs origines communes et de
l'influence de chaque paramètre dans la minéralisation de ces
eaux. C'est ainsi qu'un élément peut avoir plusieurs origines. Il
pourrait provenir de l'action humaine mais pourrait aussi avoir des origines
géogéniques d'après ces différentes
corrélations.
V.2.1.2. Analyse en composantes principales
L'analyse des variables de l'ACP dans le plan factoriel F1- F2
est présentée par la figure 32. Elle montre que ce plan factoriel
représente 63,45% de la variance exprimée. Le facteur F1 est le
plus important, avec 41,61% de l'inertie totale, le facteur F2
représente 21,70% de la variance exprimée. Ce graphe met en
exergue trois grands regroupements des paramètres étudiés
dans les points d'eau :
- le groupement entouré du cercle noir, qui prend en
compte les ETM (Fe, Cu, Al), le SiO2 et la conductivité
électrique (CE). Ce groupement se situe du côté positif du
facteur F2. Ce groupement met en évidence les apports de source
anthropique (l'érosion mécanique, lessivage des sols)
- le groupement entouré du cercle rouge, qui prend en
compte uniquement les paramètres chimiques (Ca2+,
Mg2+, Na+, K+, NH4+-,
HCO3-, Cl-, SO42-). Ce groupement se situe du
côté positif du facteur F1. Ce dernier met en évidence en
bonne partie une minéralisation des eaux liée au contact
eau-roche (hydrolyse des minéraux).
- le groupement entouré du cercle jaune, qui prend en
compte les paramètres physiques pH, température, et les
paramètres chimiques PO43-, F-, NO3- et
l'oxygène dissous. Ce groupement se situe du côté
négatif du facteur F2. C'est un groupement d'éléments
chimique associé à certains indicateurs de la qualité des
eaux. Ce dernier plus diffus traduit une origine mixte (anthropique,
atmosphérique, biogénique).
Par ailleurs, deux éléments ne font pas partis
des groupements sus cités, notamment le Mn et Cd. Leurs positions
rendent ainsi difficile leurs interprétations.

F2 (21,70 %)
-0,25
-0,75
0,75
0,25
-0,5
0,5
-1
0
1
-1 -0,75 -0,5 -0,25 0 0,25 0,5 0,75 1
F1 (41,61 %)
Variables (axes F1 et F2 : 63,45 %)
Cd
Cu
Al
CE
SiO2
Fe
PO43-
T
F-
pH
OD
NO3-
Mn
SO42-
K+
Na+
Mg2+
HCO3-
Cl-
NH4+
Ca2+
55
Figure 32. Projection des paramètres
physico-chimiques des eaux du lac, de la source et du forage sur le plan
factoriel F1 - F2.
56
Tableau 5. Matrice de corrélation entre
les paramètres physico-chimiques des eaux du lac, de la source et du
forage
|
Variables
|
pH
|
T
|
CE
|
OD
|
Ca2+
|
Mg2+
|
Na+
|
K+
|
NH4+ PO43-
|
F-
|
Cl-
|
NO3-
|
SO42- HCO3-
|
SiO2
|
Mn
|
Fe
|
Cu
|
Cd
|
Al
|
|
pH
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T
|
0,38
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CE
|
-0,23
|
- 0,96
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OD
|
0,29
|
0,83
|
-0,81
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ca2+
|
0,07
|
- 0,07
|
0,13
|
0,15
|
1,00
|
|
|
|
|
|
|
|
|
N = 8
|
|
|
|
|
|
|
|
Mg2+
|
0,28
|
0,07
|
0,01
|
0,25
|
0,96
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Na+
|
0,36
|
- 0,04
|
0,10
|
0,13
|
0,88
|
0,96
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K+
|
0,36
|
0,11
|
-0,06
|
0,29
|
0,87
|
0,96
|
0,98
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH4+
|
0,35
|
0,18
|
-0,11
|
0,32
|
0,91
|
0,99
|
0,96
|
0,98
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
|
PO43-
|
0,42
|
0,25
|
-0,32
|
0,35
|
-0,10
|
-0,08
|
-0,14
|
-0,10
|
-0,08
|
1,00
|
|
|
|
|
|
|
|
|
|
|
|
F-
|
0,64
|
- 0,04
|
0,02
|
0,11
|
0,23
|
0,30
|
0,35
|
0,33
|
0,29
|
0,81
|
1,00
|
|
|
|
|
|
|
|
|
|
|
Cl-
|
0,35
|
0,27
|
-0,19
|
0,40
|
0,91
|
0,97
|
0,91
|
0,94
|
0,99
|
- 0,05
|
0,26
|
1,00
|
|
|
|
|
|
|
|
|
|
NO3-
|
0,26
|
0,12
|
-0,24
|
0,28
|
0,35
|
0,37
|
0,36
|
0,42
|
0,38
|
0,68
|
0,76
|
0,33
|
1,00
|
|
|
|
|
|
|
|
|
SO42-
|
-0,05
|
0,25
|
-0,25
|
0,31
|
0,87
|
0,84
|
0,70
|
0,74
|
0,83
|
-0,03
|
0,09
|
0,87
|
0,34
|
1,00
|
|
|
|
|
|
|
|
HCO3-
|
0,14
|
- 0,11
|
0,19
|
0,10
|
0,98
|
0,97
|
0,92
|
0,89
|
0,93
|
-0,20
|
0,19
|
0,92
|
0,24
|
0,81 1,00
|
|
|
|
|
|
|
|
SiO2
|
0,05
|
- 0,10
|
0,02
|
-0,51
|
- 0,25
|
-0,17
|
0,00
|
-0,05
|
-0,09
|
-0,22
|
-0,05
|
-0,14
|
-0,12
|
-0,06 -0,20
|
1,00
|
|
|
|
|
|
|
Mn
|
0,41
|
0,33
|
-0,27
|
0,09
|
0,32
|
0,35
|
0,24
|
0,22
|
0,35
|
0,44
|
0,42
|
0,43
|
0,23
|
0,53 0,28
|
0,24
|
1,00
|
|
|
|
|
|
Fe
|
0,18
|
-0,06
|
0,18
|
-0,37
|
0,02
|
0,07
|
0,11
|
0,01
|
0,09
|
-0,38
|
-0,23
|
0,13
|
-0,63
|
0,10 0,13
|
0,56
|
0,49
|
1,00
|
|
|
|
|
Cu
|
-0,41
|
-0,83
|
0,85
|
-0,84
|
- 0,03
|
-0,18
|
-0,15
|
-0,31
|
-0,30
|
-0,34
|
-0,20
|
-0,31
|
-0,49
|
-0,18 0,01
|
0,24
|
-0,01
|
0,50
|
1,00
|
|
|
|
Cd
|
-0,30
|
-0,33
|
0,16
|
-0,24
|
- 0,70
|
-0,71
|
-0,56
|
- 0,55
|
-0,70
|
0,09
|
-0,03
|
-0,78
|
0,05
|
-0,75 -0,71
|
0,11
|
-0,71
|
-0,50
|
0,05
|
1,00
|
|
|
Al
|
-0,36
|
-0,22
|
0,11
|
-0,60
|
- 0,17
|
-0,20
|
-0,13
|
- 0,18
|
-0,17
|
- 0,33
|
-0,30
|
-0,19
|
-0,24
|
0,09 -0,16
|
0,88
|
0,25
|
0,56
|
0,46
|
0,03
|
1,00
|
Les valeurs en rouge sont significativement différentes de
0 à un niveau de signification alpha = 0,05 ; N = nombre
d'échantillon
57
V.2.2. Origines et facteurs environnementaux qui
contrôlent la qualité physico-chimique des eaux du lac et les eaux
souterraines étudiées
Le facies hydrochimique (à partir du digramme de piper,
1994) et l'analyse multi-variée (à partir de la matrice de
corrélation et de l'analyse en composante principale), nous ont permis
à partir des résultats obtenus, de déterminer les
principales origines des paramètres physico-chimiques des eaux du lac et
les eaux souterraines étudiées. Il en ressort trois principales
origines à savoir :
- l'origine géogénique (lithologie et
pédologie)
- l'origine anthropique (activités
socio-économiques et agricoles pratiquées au niveau du site
d'étude)
- l'origine mixte (biogénique, anthropique,
atmosphérique).
En effet, la plupart des éléments
présents dans ces eaux proviennent en partis de la roche (grès
ferrugineux) et des sols (sols ferralitique) qui sont drainés.
En ce qui concerne des ETM (Al, Fe, Cu, Cd, Mn), Ils sont
présents dans la croute terrestre à des faibles concentrations et
sont libérés par l'altération et l'érosion des
roches (Elder, 1988). Le Fe et Al prédominant dans ces eaux, est
dû au fait que la lithologie de la zone qui est dominée par les
grès ferrugineux (roche sédimentaire détritique
constituée essentiellement de quartz, feldspath et d'oxyde de fer). De
manière générale, la présence des ETM dans ces eaux
pourraient être dû aux phénomènes d'érosion
des sols, lessivage des terrains et altération des roches.
Pour les cations majeurs (Ca2+, Mg2+,
Na+, K+), les bicarbonates (HCO3-) et la
silice (SiO2), leur origine est liée à l'interaction de l'eau
chargée d'agent actif (comme le CO2) et la roche. En effet, les
minéraux de feldspaths (orthose, albite, anorthite, microcline) et
ferromagnésiens (pyroxène, olivine, amphiboles) de la roche sont
attaqués par hydrolyse et libèrent ainsi les cations majeurs
(Ca2+, Mg2+, Na+, K+), les
bicarbonates (HCO3-) et la silice selon les équations
à l'annexe 3. Cependant, en absence des roches carbonatées, tous
les bicarbonates (HCO3-) rencontrés sont d'origine
atmosphérique (Mfonka et al., 2015). Par ailleurs, le
K+ pourrait provenir des apports biogéniques et du
pluviolessivage des sols (Mfonka et al., 2015), mais aussi des
activités anthropiques notamment l'utilisation des engrais chimiques
(chlorure de potassium) à des fin agricoles (Emmachoua, 2017). Le
K+ est le cation majeur ayant la concentration la plus faible dans
l'ensemble. Sa faible teneur est
58
vraisemblablement liée à sa faible
mobilité géochimique (Wirmvem et al., 2013a) et son
absoption par les plantes (Emmachoua, 2017).
Dans l'ensemble, les nitrates (NO3-) font partis
des éléments chimiques qui prédominent dans ces eaux. Ils
constituent le stade final de l'oxydation de l'azote et représente la
forme d'azote au degré d'oxydation le plus élevé
présent dans l'eau (Ngounou, 2018). Leur origine dans ces eaux pourrait
provenir l'application d'engrais, les eaux usées, les décharges
rejetées directement dans les eaux de surface (Yao, 2009), les eaux de
ruissellement, le lessivage des terres par les précipitations et
l'oxydation de l'azote mais également de l'oxydation des nitrites par
les bactéries de la nitrification suite à l'infiltration des eaux
usées (Mfonka et al., 2015).
En ce qui concerne les ions chlorures (Cl-)
présents dans les eaux étudiées, la géologie de la
région met en évidence l'absence de roches évaporites
(halite). Leurs présences dans ces eaux pourraient donc être dus
aux activités anthropiques des populations locales, notamment par
l'utilisation des pesticides, des insecticides et des engrais chimique
(chlorure de potassium) lors des activités agricoles et des rejets
humains et animaux (Aboudi et al., 2014 ; Rakotondrabe et
al., 2017b).
Les ions ammonium (NH4+) sont des indicateurs de
pollution de l'eau par les rejets organiques d'origines agricole, domestique ou
industriel. Leur présence dans les eaux étudiées seraient
dues à la décomposition incomplète de la matière
organique et du lessivage des sols (Emmachoua, 2017). Leur présence dans
les eaux pourrait aussi s'expliquer par Les déjections animales
(Audouin, 1991) mais aussi par l'utilisation de certaines gammes de
fertilisants synthétiques (Bateman et al., 2007).
Les sulfates quant à eux peuvent provenir de
l'oxydation des minéraux sulfurés formant le socle cristallin,
mais également de l'oxydation d'espèces sulfurées dans les
eaux météoriques formant des précipitations acides
(Ollagnier et al., 2007) ainsi que l'utilisation d'engrais chimique et
de lessive.
Pour ce qui est des fluorures, ils proviendraient de l'hydrolyse
des minéraux ferromagnésien tels que la biotite mais aussi des
apports atmosphériques par les pluies et la lixiviation des sols
ferralitiques.
Le phosphate est l'un des éléments majeurs qui
contribue à la prolifération d'algues et d'autres
végétaux sur les cours d'eaux lorsqu'ils sont en concentration
excessive. En effet c'est la forme sous laquelle le phosphore peut être
assimilé par les êtres vivants en particulier les
59
végétaux. Leurs origines dans les eaux
étudiées seraient liées à l'érosion et le
lessivage des sols mais également par les activités anthropiques
et les lessives.
V.2. APTITUDE DES EAUX ETUDIEES A L'IRRIGATION
L'agriculture est l'activité dominante de la
localité soumis à notre étude, raison pour laquelle nous
avons fait une étude sur la qualité des eaux du lac Mboli, de la
source et du forage pour évaluer leurs aptitudes à l'irrigation.
L'irrigation avec des eaux riches en sels peut entraîner la fixation de
sodium par le complexe adsorbant du sol, donc un processus de salinisation,
avec ses conséquences éventuelles pour les
propriétés du sol : tendance à la dispersion des argiles,
à la dégradation de la structure, à la perte de
perméabilité et à l'asphyxie des plantes (Gouaidia et
al., 2012). A cet effet, les résultats des analyses
physico-chimiques ont été projetés sur les digrammes de
Wilcox (1948) et de Riverside ou Richard (1954) pour appréhender le
risque de salinisation et de sodisation des sols. Ces diagrammes ont
été effectués grâce au logiciel DIAGRAMME (Simler,
2005) version 6.61.
Pour ce qui est du digramme de Wilcox, il basé sur la
teneur en Na+ dans l'eau exprimé en pourcentage et la
conductivité. Ce pourcentage de Na+ est obtenu à
partir de la formule suivante :
[????+]+[K+]
%????= [??????+]+[??????+]+[????+]+[K+] ×
??????
En ce qui concerne le digramme de Riverside, il utilise les
valeurs des conductivités des différentes eaux et le SAR
(Sodium Absorption Ratio). Dans ce cas, le risque est d'autant plus grand
que la conductivité et le SAR sont élevés
(Gouaidia et al., 2012). Le SAR est obtenu d'après la
formule suivante :
????
D'après la classification de Wilcox (figure 33), les
eaux étudiées sont excellentes dans l'ensemble. La classification
de Riverside (Figure 34) montre aussi que ces eaux sont appropriées
à l'irrigation du fait de leurs pouvoirs absorbants et
conductivités faibles (C0S1). Ces deux classifications montrent en
effet, la qualité excellente de l'eau de lac, de la source et du forage
pour l'irrigation.
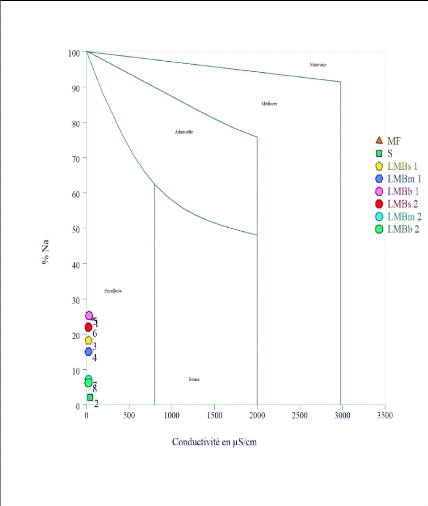
60
Figure 33 : Aptitude des eaux du lac, de la
source et du forage à l'irrigation selon le diagramme de
Wilcox.

C0S1
C0S3
C0S2
S3
S1
S2
C3S3
C3S1
C3S2
C4S2
C4S3
C4S1
C5S2
C5S3
C5S1
C6S1
61
Figure 34 : Aptitude des eaux du lac, de la
source et du forage à l'irrigation selon le diagramme de Riverside.
62
CONCLUSION
Les résultats d'analyses physico-chimiques des eaux du
lac Mboli, de la source et du forage ont montré dans l'ensemble un
comportement similaire. Ces eaux sont très faiblement
minéralisées sans exception. Spécifiquement, dans le lac,
la signature physico-chimique observée dans la colonne d'eau des deux
stations de prélèvement du lac Mboli, montre pour la majeure
partie des paramètres mesurés, ont+ une évolution à
caractère hétérogène le long des deux profils
verticaux à l'exception de quelques paramètres tels que la
conductivité et la température qui présentent de
légères disparités pour leurs évolutions dans la
colonne d'eau. Sur le plan environnemental, le pH obtenu à la base des
colonnes d'eau peut provoquer des difficultés de développement de
la vie aquatique. La teneur en oxygène dissous dans la colonne d'eau se
maintient à des valeurs supérieures à 5 mg/l, à
l'exception de la base de la colonne d'eau au niveau de la station 2, ce qui
est bon pour l'écosystème. Les ETM (Al, Cu, Cd) présents
à chaque niveau de la colonne d'eau (surface, milieu, base)
dépassant le seuil CMC et de CCC présentent un risque toxique
pour les organismes aquatiques. Pour ce qui est des eaux souterraines (source
et forage) utilisées comme eau de boisson, la conductivité
mesurée dans ces eaux ne respecte pas les normes de l'OMS et ANOR, par
contre, seul le pH mesuré au niveau de la source ne respecte pas les
normes. Quant aux paramètres chimiques, seul l'Al se trouve à des
teneurs supérieures à celle recommandée par l'OMS. En ce
qui concerne l'origine des paramètres mesurés, il en ressort dans
l'ensemble plusieurs origines à savoir, l'origine
géogénique (lithologie et pédologie), l'origine
anthropique (activités socio-économiques et agricoles
pratiquées au niveau du site d'étude) et l'origine mixte
(biogénique, anthropique, atmosphérique). Pour l'aptitude de ces
eaux à l'irrigation, les diagrammes de Wilcox et de Riverside nous ont
montré que ces eaux sont excellentes pour une utilisation agricole. Cela
est dû en partis à leur faible minéralisation.
64
Le lac Mboli situé dans l'arrondissement de
Dizangué, est l'objet principal de notre étude. Il était
question dans le cadre de ce travail de contribuer à une meilleure
connaissance de la concentration en éléments traces
métalliques, mais aussi d'autres paramètres physico-chimiques
présents dans la colonne d'eau des stations d'échantillonnages du
lac Mboli et d'évaluer la qualité des eaux souterraines
utilisées comme eau de boisson par les populations voisines du lac. Cet
objectif a été atteint à partir des observations et
travaux faits sur le terrain et les analyses effectuées en laboratoire.
Pour ce qui est de l'approche méthodologique, il a été
question dans le cadre de ce travail, d'effectuer des travaux sur le terrain
qui ont permis l'échantillonnage des eaux ainsi que l'analyse in-situ de
nombreux paramètres obtenus par une sonde multiparamètre. Seize
échantillons ont été obtenus en raison de douze dans le
lac, deux dans la source et deux au forage. Les travaux en laboratoire ont
été réalisés en fonction de la catégorie
d'éléments. Huit échantillons ont été
analysés, dont 6 dans le lac, un provenant de la source et un du forage.
Les éléments traces métalliques (Fe, Al, Cu, Mn, Cd) ont
été obtenus par spectrométrie d'absorption atomique par
flamme et les éléments majeurs et d'autres éléments
chimiques (HCO3-, Cl-, SO42- ;
NO3-, Ca2+, K+, Mg2+,
Na+, F-, NH4+, PO43- , Al
3+) par chromatographie ionique à phase liquide. Pour le
traitement des données, la méthode hydrochimique à partir
du logiciel diagramme de Simler et l'analyse statistique multivariée (le
logiciel XLSTAT et Excel) ont été utilisées dans le cadre
de ce travail. Les résultats d'analyses des eaux du lac et les eaux
souterraines nous ont permis d'avoir leurs signatures physico-chimiques. Dans
l'ensemble, ces eaux sont acides faiblement acide (4,34 = pH = 6,84), elles
sont très faiblement minéralisées (27, 21 = CE = 51,22
uS/cm ; 0,064 = TZ+ = 4,941 méq/l ; 0,056 = TZ- =
4,03 méq/l) avec une température qui oscille de 26,3 à
32,5 °C. La classification d'ordre de grandeur
décroissant des éléments majeurs d'après les
concentrations moyennes d'ensemble est la suivante HCO3- >
NO3- > Ca2+ > Mg2+ > Na+
> SO42- > Cl- > K+. L'observation des
proportions de ces éléments majeurs dans le diagramme de Piper
nous a permis de visualiser deux faciès à savoir le faciès
chloruré et sulfaté calcique et magnésien qui
représente 62,5% des eaux et le faciès bicarbonaté
calcique et magnésien qui représente 37,5% des eaux. Pour les
colonnes d'eau du lac, la distribution des paramètres physico-chimiques
n'est pas homogène le long des profils verticaux a l'exception de la
conductivité et la température qui présentent de
légères disparités pour leurs évolutions dans la
colonne d'eau. Le pH inférieur à 5 mg/l, la teneur en
oxygène dissous inférieure à 5 mg/l et les ETM (Al, Cu,
Cd) présents à chaque niveau de la colonne d'eau (surface,
milieu, base) dépassant le seuil CMC et de CCC présentent un
risque toxique pour les organismes aquatiques. Pour ce qui est des eaux
souterraines utilisées comme eau de boisson, la conductivité
mesurée dans ces eaux ne respecte pas les normes de
65
l'OMS et ANOR, par contre, seul le pH relevé au niveau
de la source ne respecte pas ces normes. Quant aux paramètres chimiques,
seul le Al se trouve à des teneurs supérieures à celle
recommandée par l'OMS. Dans l'ensemble les eaux souterraines
étudiée, sont bonnes pour la consommation d'après leurs
signatures physico-chimiques. La matrice de corrélation et l'Analyse en
Composante Principale nous ont permis de connaitre les relations et les
différentes origines des éléments présent dans ces
eaux à savoir, géogénique (lithologie et
pédologie), anthropique (activités socio-économiques et
agricoles pratiquées au niveau du site d'étude) et mixte
(biogénique, anthropique, atmosphérique). Pour l'aptitude de ces
eaux à l'irrigation, les diagrammes de Wilcox et de Riverside nous ont
montré que ces eaux sont excellentes pour une utilisation agricole. Cela
est dû en partis à leur faible minéralisation

66
A l'issue de la présente étude, les perspectives
formulées sont les suivantes :
- augmenter la surface d'investigation au niveau du lac qui
permettra de faire une étude complète du lac Mboli;
- faire une étude des paramètres
physico-chimique spatio-temporelle en prenant compte des paramètres
biologiques et d'autres éléments traces métalliques dans
le lac Mboli et les eaux souterraines pour mieux évaluer de façon
complète ces eaux;
- évaluer la pollution du lac en prenant en compte des
sédiments qui sont un lieu de stockage permanent des ETM.
REFERENCES BIBLIOGRAPHIQUES
70
Aboudi, A., Tabiyaoui, H., El Hamichi, F., Benaabidate, L.,
Labrach, A., 2014. Etude de la qualité physico-chimique et contamination
métallique des eaux de surface du bassin versant de Guigou, Maroc.
European Scientific journal 10, 1857 - 7881.
Abdel Salam, G. M., Liégeois, L., Stern, R. J., 2002.
The Saharan Metacraton. Journal of African Earth Sciences 34, 119 -
136.
Andre, L., Franceschi, M., Pouchan, P., Atteia, O., 2005.
Using geochemical data and modelling to enhance the understanding of
groundwater flow in a regional deep aquifer, Aquitaine Basin, south-west of
France. Journal of Hydrology 305, 40 - 62.
Anonyme, 2009. Pollution des eaux.
Alayat, H., El Khattabi, J., Lamouroux, C., 2013.
Évolution spatiale des caractéristiques physico-chimiques des
eaux du lac Oubeira impose par les conditions sévères de la
sècheresse (Extreme NE Algerien). European Scientific Journal
9, 1857 - 7881.
Audoin, L., 1991. Rôle de l'azote et phosphore dans la
pollution animale. Scientific and technical review of the office
international 10, 629 - 654.
Ball, E., Bard, JP., Soba, D., 1984. Tectonique tangentielle
dans la catazone panafricaine du Cameroun : Les gneiss de Yaoundé.
Journal of African Earth Sciences 2, 91 - 95.
Bagnouls, F., Gaussen, H., 1957. Les climats biologiques et
leur classification. Annexe Géographie XXVI, 193 - 220 p.
Bateman, A.S., Kelly S.D., 2007. Fertilizer nitrogen isotope
signatures. Isotopes in environmental and health studies 43, 237 -
247.
Ben Bouih, H., Nassali, H., Leblans, M., Srhiri, A., 2005.
Contamination en métaux traces des sédiments du lac Fouarat
(Maroc), Afrique Science 1, 109 - 125.
Ben, C., 1992. Le lac de Tunis après les
aménagements. Paramètres physico-chimiques de l'eau et relation
avec la croissance des macroalgues. Marine life 1, 29 - 44.
Berg, L.R., Raven, P.H., Hassenzahl, D.M., 2009.
Environnement. Editeur De Boek, 687 p. Boyce, F.M., 2006. Les Lacs.
Encyclopédie Canadienne,11 p.
Brooke, L.T., Colby, P.J., 1980. Development and survival of
embryos of lake herring at different constant oxygen concentrations and
temperatures. Progressive Fish-Culturist 42, 3 - 9.
71
Bugenyi, F.W.B., 1982. Copper pollution studies in Lakes
George and Edward, Uganda: the distribution of Cu, Cd, and Fe in the water and
sediments. Environment Pollutant 3, 129 - 38.
Close, M.E., Hodgson, L.R., Todgre, G., 1989. Field evaluation
of fluorescent whitening agents and sodium tripolyphosphate as indicator of
septic tank contamination in domestic wells. New Zealand Journal Marine
Freshis Ressource 23, 563 - 568.
CRE, 2009. Conseil régional de l'environnementale des
Laurentides. Le pH. 3 p.
Detay, M., 1993. Forage d'eau (réalisation, entretien
et minéralisation). Edition. Masson, Paris, 280 p.
Duchaufour, P., 1983. Pédologie. Tome 1 :
pédogenèse et classification. Masson, Paris, 477 p.
Elder, J. F., 1988. Metal Biogeochemistry in Surface Water
system- A review of Principles and Concepts. United States Geological
Survey, 50 p.
Emmachoua Arrah, J. L., 2017. Qualité physico-chimique
et bactériologique des eaux du bassin versant de
Makénéné (Centre-Cameroun). Mémoire master II
Université Yaoundé I, 78 p.
Everitt, B. S., Horthon, T., 2011. An introduction to applied
multivariate Analysis with. Springer, New York. ISBN, 978 - 4419.
Feybesse, J.L., Johan, V., Triboulet, T, C., Guerrot, C.,
Mayaga-moi<OLO, F., Bouchot, V., Eko N'dong, J., 1998. The West Central
African belt: a model of 2.5 - 2.0 Ga accretion and two-phase orogenic
evolution. Precambrian Research 87, 161 - 216.
Forstner, U., Wittmann, G.T.W., 1983. Metal Pollution in
Aquatic Environment. Springer Verlag, Berlin, Heidelberg, New York, Tokyo,
486 p.
Glèlè Kakai, R., Salako, V. K., Padoumou, E.A.,
Lykke, M., 2016. Méthode statistiques multi-variées
utilisées en écologie. Annales des sciences agronomiques
spécial projet Undersert-UE, 139 - 157 p.
Gouaidia, L., Omar, G., Abderahmane, B., Mohamed, L., Claude, M.,
2012. Évaluation de la salinité des eaux souterraines
utilisées en irrigation et risques de dégradation des sols :
exemple de la plaine de Meskiana (NordEst Algérien).
Physiologie-géographie 6, 141 - 160.
Gouin, C. A., Aka, N., Adiaffi, B., Bamba, S.B., Soro, N.,
2016. Pollution saisonnière des sédiments de lagune par des
métaux lourds (Cu, Pb et Zn) en zone tropicale humide : cas de
72
la lagune Mondoukou (Sud-Est de la Côte d'Ivoire).
International Journal of Biological and Chemistry Sciences 10,
835 - 845.
Gournay, A., 2012. Analyse statistiques multi-variées.
Notes de cours Université de Neuchatel. 76 p.
Greichus, Y.A., Greichus A., Draayer H. A., 1978. Insecticides,
polychlorinate biphenyls and metals in African lake ecosystems. II. Lake
McIlwaine, Rhodesia. Bulletin of Environment Contamination Toxicology
19, 44 - 53.
Guler, C., Thyne, G.D., McCray, J.E., Turner, K.A., 2002.
Evaluation of graphical and multivariate statistical methods for classification
of water chemistry data. hydrogeology journal 10, 455 - 477.
Harte, J., Holdren, C., Schneider, R., Shirley, C., 1991. Toxics
A to Z, A Guide to Everyday Pollution Hazards. Oxford, England: University
of California Press, 478 p.
Hassoune, E.M., Bouzidi, A., Koulali, Y., Hadarbach, D., 2006.
Effets des rejets liquides domestiques et industriels sur la qualité des
eaux souterraines au nord de la ville de Settat (Maroc). Bulletin de
l'Institut Scientifique, Rabat, section Sciences de la Vie 28, 61 - 71.
IBGE, 2005. Institut bruxellois pour la gestion de
l'environnement, l'eau à Bruxelles, 16 p.
Issa, 2014. Géochemical charactérization of
volcanic lakes: implication for volcanic hazards monitoring/surveillance along
the Cameroon volcanic line. Mémoire thèse de doctorat
Université Toyama (Japon), 227 p.
Jean-René, D., Daniel, G., 1994. Hydroclimat et
Hydrochimie. Environnement et Ressources Aquatiques de Côte d'Ivoire
2, 59 - 90 p
Kanohin, F., Ossey, Y., B., Dibi, B., Bonny, A. C., 2017.
Caractérisation physico-chimique et bactériologique des eaux
souterraines de Bingerville. International Journal of Biological and
Chemistry Sciences 11, 2495 - 2509.
Kossoni, A., 2003. Processus sédimentaires du lac Ossa
(Dizangué, Sud-ouest Cameroun) et évolution
paléoclimatique holocène. Thèse de doctorat.
Université de Perpignan, 237 p.
Kouassi, A.M., Mamadou, A., Ahoussi, K.E., Biemi, J., 2013.
Simulation de la conductivité électrique des eaux souterraines en
relation avec leurs propriétés géologiques : cas de la
Côte d'Ivoire. Revue Ivoirienne, Science Technologique 22, 138 -
166.
73
Letouzey, R., 1985. Notice de la carte
phytogéographique du Cameroun au 1/500.000. Institut de Recherche
Agricol de Yaoundé et Institut de Cartographie Internationale.
Végétation, Toulouse, 240 p.
Letouzey, R., 1968. Étude phytogéographique du
Cameroun. Lecl1evalier, Paris, 508 p.
Loukman, B., Nakolendousse, S., Nour, A.M., Nguinambaye, M.M.,
2017. Caractérisation hydrochimique de la nappe de Yao et ses environs :
relations entre eaux de surface (lac-Fitri) et eaux souterraines.
International Journal of Biological Chemical and Sciences 11, 1336 -
1349.
Madjiki, A.G., Annie-Claude, P., Ngoupayou, N.J.R., Akoa, A.,
2013. Caractérisation hydrologique, morpho-métrique et
physicochimique d'un hydrosystème urbain : le lac municipal d'Ebolowa
(Sud-Cameroun). Afrique Science 9, 122 - 134.
Mahendrappa, M.K., 1989. Impact of forest on water chemistry.
Water, Air and Soil Pollution 46, 61 - 72.
Mbé, G. A. S., 2020. Distribution des
éléments traces métalliques dans les eaux souterraines de
Nkozoa, (Yaoundé, Centre Cameroun). Mémoire master II,
Université Yaoundé I, 60 p.
Messolo, J. M., 2020. Hydrochimie et évaluation de la
qualité des eaux souterraines de la localité Nkozoa,
Yaoundé. Mémoire master II, Université Yaoundé
I, 86 p
Mfonka, Z., Ndam, N. J. R., Ndjigui, P. D., Zammouri, M.,
Kpoumie, A., Rasolomanana, E., 2015. Hydrochimie et potabilité des eaux
du bassin versant du Nchi dans le plateau Bamoun (Ouest Cameroun).
International Journal of Biological and Chemical Sciences 9, 2200 -
2218 p.
Miramond, N., Miau, D., Brochard, F., 2006. Diagnostic du
phénomène drainage minier acide sur des mines d'or primaire
à Guyane française : évaluation des risques
associés, rapport GEM Impact DIREN, Guyane française.
Monkolo, J., Laraque, A., Olivry, J.C., Briquet, J.P., 1993.
Transport en solution et en suspension par le fleuve Congo (Zaïre) et ses
principaux affluents de la rive droite. Journal des sciences hydrologiques
38, 133 - 145 p.
Ndam, N. J.R., 1997. Bilans hydrogéologiques sous
forêt tropicale humide en Afrique du bassin expérimental de
Nsimi-Zoételé aux réseaux hydrographyques du Nyong et de
la Sanaga (Sude-Cameroun). Thèse université de paris IV,
214 p.
74
Ngaram, N., 2011. Contribution à l'étude
analytique des polluants (en particulier de type métaux lourds) dans les
eaux du fleuve Chari lors de sa traversée de la ville de N'Djamena.
Chimie analytique. Université Claude Bernard - Lyon I.
Français, 166 p.
Ngafack, P.R., 2014. Prédiction saisonnière de
présence du lamantin d'Afrique (trichechus senegalensis link, 1795) en
fonction des caractéristiques physico-chimiques de l'eau : cas du lac
Ossa, Cameroun. Mémoire de master II, Université Dschang,
88 p.
Ngouh, A. N., Amidou, K., Etame, N. G., Aloysious, K. L.,
Ndjeng, E., Ndam, N.J.R., 2020 Caractérisation Hydrodynamique et
Qualité des eaux de l'aquifère à nappe libre du bassin
Njike Ngaha, P.R., 1984. Contribution à l'étude
géologique, stratigraphique et structurale de la bordure du bassin
Atlantique au Cameroun. Thèse, Université de Yaoundé
I, 131 p.
Nisbet, M., Vernaux, J., 1970. «Composantes chimiques des
eaux courantes. Discussion et proposition des classes en tant que base
d'interprétation des analyses chimiques. Annals Limnologie 6,
161 - 190.
Nziéleu Tchapgnouo J. G., Zébazé Togouet
S. H., Foto Menbohan S., Njiné Thomas and Bernadette Pinel-Alloul.,
2016. Baseline Information on the Metallic Pollution of Sediments of the Lakes
of the Ossa Complex, Dizangue, Cameroon. British Journal of Applied Science
et Technology, 14 (6), 1-14.
Nzenti, J.P., Barbey, P., Macaudière, J., Soba, D.,
1988. Origin and evolution of the late Precambrian highgrade Yaoundé
gneisses (Cameroon). Precamb Research 38, 91 - 109.
OMS, 2011. Guidelines for Drinking-water Quality. World Health
Organization, Fourth Edition; Genève, Suisse, 541 p.
OMS, 2017. Directives de la qualité pour l'eau de
boisson : 4e édition intégrant le premier additif, 539
p.
Oumar, B., Ekengele, N.L., Ondoa, B.A.D., 2014.
Évaluation du niveau de pollution par les métaux lourds des lacs
Bini et Dang, Région de l'Adamaoua, Cameroun. Afrique Science
10, 184 - 198.
Owona, S., Mvondo, O. J., Ratschbascher, L., MbolaNdzana,
S.P., Tchoua, M.F., Ekodeck, G.E., 2011. The geometry of the Archean, Paleo and
Neoproterozoic tectonics in the Southwest Cameroon. Compte Rendu de
Géosciences 343, 312 - 322.
75
Penaye, J., Toteu, S.F., Tchameni, R., Van Schmus, W.R.,
Tchakounté, J., Ganwa, A., Minyem, D., Nsifa, E.N., 2004. The 2.1 Ga
West Central African Belt in Cameroon: extension and evolution. Journal of
African Earth Sciences 39, 159 - 164.
Piper, A.M., 1994. A graphic procedure in the geochemical
interpretation of water analyses. Americain Geophysical Union, Transcript
25, 914 - 923.
PCD de Dizangue., 2011.Plan communal de développement de
Dizangue, 163 p
Rakotondrabe, F., Ndam, N. J.R., Mfonka, M., Rasolomanana, H.E.,
Nyangono, A.A.J., Ako Ako, A., 2017. Water quality assessment in
Bétaré-Oya gold mining area (East-Cameroon): Multivariate
Statistical Analysis approach. Science of the Total Environment 611,
831 - 844.
Richards, L.A., 1954. Sous la direction de - Diagnosis and
improvement of saline and alkali soils. US Department of Agriculture,
Agricultural Handbook, Washington (USA), 160 p.
Schuurmann, G., Markert, B., 1998. Ecotoxicology, Ecological
Fundamentals, Chemical Exposure, and Biological Effects. John Wiley,
900 p.
Saad, M.A.H., 1985. Influence of pollution on Lake Mariut, Egypt.
Revue International d'Océanographie médicale 79, 33 -
77.
Salard-Cheboldaeff, M., 1977. Paléopalynologie du
bassin sédimentaire Littoral du Cameroun dans ses rapports avec la
stratigraphie et la paléoécologie. Thèse d'Etat.
Science National Université Pierre et Marie Curie. Paris,
262 p.
Séraphin, K. K., Marcel, A.K., Antoinette, A. A.,
Dongui, B. K., Dago, G., 2008. Variations saisonnières des
paramètres abiotiques des eaux d'une lagune tropicale : la lagune de
Grand-Lahou, Côte d'Ivoire. European Journal of Scientific
Research, 21(3), 376-393.
Simler., 2005. Diagrammes software. http ://
wwwlha.univ-arvignon.fr/LHA
Logiciels.htm
Sorlini, S., Palazzini, D., Sieliechi, J.M., Ngassoum, M.B.,
2013. Assessment of Physical-Chemical Drinking Water Quality in the Logone
Valley (ChadCameroon). Sustainability 5, 3060 - 3076.
Sparks, D.L., 1998. Environmental soil chemistry. Academic
Press, 267 p.
Suchel, J.B. (1988). Les climats du cameroun. Thèse,
Université de Bourgogne, 1177 p.
Suchel, J.B., 1972. La répartition des pluies et des
régimes pluviométriques au Cameroun. Géographie
Tropical CEGET, Bordeaux 5, 287 p.
76
Tchameni, R., Nsifa, E.N., 1998. Revues des données
géochronologiques sur la partie nord-ouest du craton du Congo (groupe du
Ntem), Sud Cameroun. Press University of Yaoundé I. 351 -
359.
Tohouri, P., Soro, G., Ahoussi, K. E., Adja Miessan, G., Ake,
G. E., Biemi, J., 2016. pollution by trace metals of the surface water of
bonoua area in high water time (southeast of ivory coast). Larhyss Journal,
ISSN 43, 1112 - 3680.
USEPA, 2006. Environmental Protection Agency, National
recommended water quality criteria. Office of Water, 2 - 47.
Wilcox, L.V., 1948. The quality of water for agricultural use.
US Department of Agriculture, Technical Bulletin 962, 40 p.
Wirmvem, M.J., Takeshi., Fantong, W. Y., Ayonghe, S. N.,
Suila, J. Y., Asobo, N. E., Tanyileke, G., Joseph, V. H., 2013. Hydrochemistry
of shallow groundwater and surface water in the Ndop plain, west Cameroon.
African Journal of Environnemental Science and Technology 7, 518 -
530.
Xiao, J., Zhang-Dong, J., Ding, H., Wang, J., Zhang, F., 2012.
Geochemistry and solute sources of surface waters of the Tarim River Basin in
the extreme arid region, NW Tibetan Plateau. Journal of Asian Earth
Sciences 55, 162 - 173.
Xing, L., Guo, H., Zhan, Y., 2013. Groundwater hydrochemical
characteristics and processes along flow paths in the North China Plain.
Journal of Asian Earth Sciences 71, 250 - 264.
Yaka, M.A., Tiemeni, A., Zing, Z.B., Nenkam, J.T. L. L.,
Aboubakar, A., Nzeket, A.B., Tcholong, F. B. H., Mfopou, M. Y. C., 2020.
Qualité physico-chimique et bactériologique des eaux souterraines
et risques sanitaires dans quelques quartiers de Yaoundé VII, Cameroun.
International Journal of Biological and Chemical Sciences 14, 1902 -
1920.
Yao, T.K., 2009. Hydrodynamisme dans les aquifères de
socle cristallin et cristallophyllien du Sud-Ouest de la Côte d'Ivoire :
cas du Département de Soubré. Apports de la
télédétection, de la géomorphologie et de
l'hydrogéochimie. Thèse de Doctorat en cotutelle,
Conservatoire national des Arts et Métiers, France et Université
de. Cocody, Côte d'Ivoire, 265 p.
Yao, T.K., Oga, M.S., Fouché, O., Baka, D., Pernelle,
C., Biemi, J., 2012. Évaluation de la potabilité chimique des
eaux souterraines dans un bassin versant tropical : cas du Sud-Ouest de la
Côte d'Ivoire. International of Journal Biological and Chemical
Sciences 6, 7069 - 7086.
ANNEXES
xvi
Annexe 1. Résultat complet d'analyse des eaux du
lac et les eaux souterraines étudiées
|
Libele
|
Unités
|
MF
|
S
|
LMBs 1
|
LMBm 1
|
LMBb 1
|
LMBs 2
|
LMBm 2
|
LMBb 2
|
|
pH
|
-
|
6,67
|
4,34
|
6,84
|
6,57
|
4,96
|
6,62
|
6,35
|
5,3
|
|
T
|
°C
|
26,3
|
27,2
|
32
|
32
|
30,6
|
32,5
|
30,9
|
31
|
|
CE
|
uS/cm
|
51,22
|
46,9
|
27,45
|
27,38
|
27,61
|
27,21
|
27,31
|
27,43
|
|
OD
|
mg/l
|
2,56
|
3,68
|
6,04
|
6,16
|
5,7
|
5,18
|
5,39
|
3,72
|
|
Ca2+
|
mg/l
|
12,194
|
20,184
|
0,165
|
49,78
|
4,41
|
0,206
|
8,76
|
2,98
|
|
Mg2+
|
mg/l
|
5,339
|
3,369
|
0,54
|
20,827
|
1,499
|
0,609
|
2,239
|
0,21
|
|
Na+
|
mg/l
|
7,361
|
0,617
|
0,181
|
15,432
|
2,277
|
0,273
|
0,891
|
0,187
|
|
K+
|
mg/l
|
0,965
|
0,048
|
0,151
|
2,597
|
0,672
|
0,202
|
0,345
|
0,118
|
|
NH4+
|
mg/l
|
0,385
|
0,018
|
0,04
|
1,812
|
0,164
|
0,07
|
0,11
|
0,043
|
|
PO43-
|
méq/l
|
0,493
|
0,05
|
2,263
|
0,83
|
0,005
|
0,109
|
4,351
|
0,443
|
|
F-
|
mg/l
|
0,017
|
0
|
0,012
|
0,014
|
0,001
|
0,001
|
0,025
|
0,002
|
|
Cl-
|
mg/l
|
0,944
|
0,02
|
0,736
|
13,576
|
0,01
|
0,082
|
0,225
|
0,023
|
|
NO3-
|
mg/l
|
12,044
|
1,311
|
0,65
|
23,831
|
13,349
|
3,061
|
39,927
|
6,264
|
|
SO42-
|
mg/l
|
0,004
|
3,043
|
0,81
|
9,151
|
1,486
|
0,152
|
2,25
|
3,819
|
|
HCO3-
|
mg/l
|
58,95
|
65,368
|
0,49
|
187,56
|
9,882
|
1,932
|
5,856
|
1,159
|
|
SiO2
|
mg/l
|
0,764
|
0,486
|
0,583
|
0,584
|
0,613
|
0,585
|
0,563
|
0,894
|
|
Mn
|
méq/l
|
0,005
|
0,005
|
0,007
|
0,008
|
0,002
|
0,005
|
0,007
|
0,008
|
|
Fe
|
mg/l
|
0,262
|
0,189
|
0,287
|
0,223
|
0,058
|
0,192
|
0,024
|
0,337
|
|
Cu
|
mg/l
|
0,078
|
0,094
|
0,03
|
-
|
-
|
-
|
-
|
0,053
|
|
Cd
|
mg/l
|
0,003
|
0,002
|
0,002
|
-
|
0,004
|
0,002
|
0,003
|
0,002
|
|
Al
|
mg/l
|
0,567
|
0,28
|
-
|
0,101
|
0,232
|
-
|
-
|
1,553
|
|
TZ-
|
mg/l
|
1,187
|
1,157
|
0,056
|
4,032
|
0,409
|
0,087
|
0,793
|
0,2
|
|
TZ+
|
mg/l
|
1,394
|
1,315
|
0,064
|
4,941
|
0,46
|
0,077
|
0,67
|
0,177
|
|
TDS
|
mg/l
|
98,565
|
94,445
|
4,306
|
323,338
|
34,198
|
7,1
|
61,057
|
15,654
|
|
BI
|
%
|
8
|
6
|
7
|
10
|
6
|
-6
|
-8
|
-6
|
Annexe 2. Relation entre la conductivité
électrique et la minéralisation
|
Conductivité électrique (uS/cm)
|
Minéralisation
|
|
< 100
|
Très faible
|
|
100 à 200
|
Faible
|
|
200 à 400
|
Peu accentuée
|
|
400 à 600
|
Moyenne
|
|
600à 1000
|
Importante
|
|
> 1000
|
Excessive
|
Annexe 3. Quelques équations de mise en solution
des éléments chimiques majeurs
Au cours de l'hydrolyse des minéraux primaires, les
bicarbonates, les cations majeurs et la silice sont libérés
suivant l'équation :
Minéraux primaires + CO2 + H2O ? HCO3-+
minéraux secondaires + cations + silice
- Hydrolyse de l'orthose en montmorillonite
xvii
2KAlSi3O8 + 3H2O + 2CO2 ? Al2Si4O10 (OH)2 +
2HCO3- + 2K+ 2SiO2
- Hydrolyse de l'albite en kaolinite
2NaAlSi3O8 + 2CO2 + 3H2O ? Al2Si2O5 (OH) 4 + 2Na+
+ 2HCO3- + 4SiO2
- Hydrolyse de l'anorthite en kaolinite
CaAl2Si2O8 + 2CO2+3H2O ? Al2Si2O5 (OH)4 +
2HCO3- + Ca2+
- Hydrolyse de l'olivine
MgSiO4 + 2CO2 + H2O ?Mg2+
2HCO3- + SiO2
Annexe 5. Caractères
d'essentialité et de toxicité de quelques éléments
traces. FC : faible concentration (Lamprea, 2009)
|
Elément
|
Symbol
|
Indispensable FC Toxique FC
|
Commentaires
|
|
|
Plantes
|
Animaux
|
Hommes
|
Plantes
|
Animaux
|
Hommes
|
|
|
Arsenic
|
As
|
Non
|
Oui
|
Non
|
Oui
|
Oui
|
Oui
|
Phytotoxique, carcinogénique
|
|
Cadmium
|
Cd
|
Non
|
Non
|
Non
|
Oui
|
Oui
|
Oui
|
Phytotoxique,
bioaccumulation et
carcinogénique
|
|
Cobalt
|
Co
|
Non
|
Non
|
Non
|
Oui
|
Oui
|
Oui
|
Relatv. Phytotoxique,
carcinogénique
|
|
Chrome
|
Cr
|
Non
|
Non
|
Non
|
Oui
|
Non
|
Oui
|
Cr+6 : toxique, mobile dans le sol, Cr+3
Peu toxique pour
mammifères
|
|
Cuivre
|
Cu
|
Oui
|
Oui
|
Oui
|
Oui
|
Non
|
Non
|
Immobile dans le sol, peu toxique
|
|
Fer
|
Fe
|
Oui
|
Oui
|
Oui
|
Non
|
Non
|
Oui
|
Phytotoxique à pH acide, maladie par déficience
|
|
Mercure
|
Hg
|
Non
|
Non
|
Non
|
Non
|
Oui
|
Oui
|
Toxique,
bioaccumulation
|
|
Nickel
|
Ni
|
Oui
|
Oui
|
Oui
|
Non
|
Oui
|
Oui
|
Très mobile dans le sol et plantes,
carcinogénique
|
|
Plomb
|
Pb
|
Non
|
Non
|
Non
|
Oui
|
Oui
|
Oui
|
Peu phytotoxique
Immobile dans le sol,
saturnisme
|
|
Sélénium
|
Se
|
Oui
|
Oui
|
Oui
|
Oui
|
< 4ppm
|
|
Maladies par
déficience
|
|
Etain
|
Sn
|
Non
|
Oui
|
Oui
|
Non
|
Oui
|
Oui
|
Relativement non toxique
|
|
Zinc
|
Zn
|
Oui
|
Oui
|
Oui
|
Oui
|
Non
|
Non
|
Facilement complexé dans le
sol, peu toxique
mammifères
|
xviii
Annexe 5. Sources industrielles et agricoles des
métaux présents dans l'environnement (Biney et al.,
1995).
|
Utilisations
|
Métaux
|
|
Batteries et autres appareils électriques
|
Cd, Hg, Pb, Zn, Mn, Ni,
|
|
Pigments et peintures
|
Ti, Cd, Hg, Pb, Zn, Mn, Sn, Cr, Al,
As, Cu, Fe
|
|
Alliages et soudures
|
Cd, As, Pb, Zn, Mn, Sn, Ni,
Cu
|
|
Biocides (pesticides, herbicides, conservateurs)
|
As, Hg, Pb, Cu, Sn, Zn, Mn
|
|
Agents de catalyse
|
Ni, Hg, Pb, Cu, Sn
|
|
Verre
|
As, Sn, Mn
|
|
Engrais
|
Cd, Hg, Pb, Al, As, Cr,
Cu, Mn, Ni, Zn
|
|
Matières plastiques
|
Cd, Sn, Pb
|
|
Produits dentaires et cosmétiques
|
Sn, Hg
|
|
Textiles
|
Cr, Fe, Al
|
|
Raffineries
|
Ni, V, Pb, Fe, Mn, Zn
|
|
Carburants
|
Ni, Hg, Cu, Fe,
Mn, Pb, Cd
|
Annexe 6. Critère de qualité de
l'eau destinée à la consommation humaine de quelques
paramètres physico-chimiques d'après L'ANOR et l'OMS
|
Paramètres
|
Normes ANOR
|
Normes OMS
|
|
Température (°C)
|
-
|
-
|
|
pH
|
6,5-9
|
6,5 à 8,5
|
|
C.E (uS/cm)
|
1000
|
1500
|
|
Chlorures Cl- (mg/l)
|
= 200
|
250
|
|
Sulfates (SO4)2- (mg/l)
|
= 250
|
250
|
|
Nitrates NO3- (mg/l)
|
= 50
|
50
|
|
Calcium Ca2+ (mg/l)
|
-
|
500
|
|
Magnésium Mg2+ (mg/l)
|
= 50
|
125
|
|
Sodium Na+ (mg/l)
|
= 150
|
200
|
|
Potassium K+ (mg/l)
|
= 12
|
Non mentionné
|
|
Bicarbonates HCO3- (mg/l)
|
-
|
125-130
|
|
Ammonium NH4+ (mg/l)
|
= 0,5
|
0,5
|
|
Phosphates PO43- (mg/l)
|
0
|
5
|
|
Fluorure F- (mg/l)
|
-
|
1,5
|
xix
Annexe 7. Concentrations de quelques
éléments traces métallique définissant les limites
de qualité d'une eau potable (OMS)
|
Éléments Traces
Métalliques
|
Norme OMS
|
|
Zn (ug/L)
|
< 5000
|
|
Cu (ug/L)
|
< 1000
|
|
Pb (ug/L)
|
< 50
|
|
Cd (ug/L)
|
< 5
|
|
Mn (ug/L)
|
< 50
|
|
Al (ug/L)
|
< 200
|
|
Fe (ug/L)
|
< 300
|
|
|



