INTRODUCTION GENERALE :
Certaines maladies d'origine infectieuse sont
méconnues de la population ; bien quelles soient à l'origine
de maladies graves ou de malformations, cela est du en grande partie au manque
d'information concernant les causes de ces maladies et malformations.
Des enfants morts nés, ou ayant une malformation, des
avortements spontanés sont enregistrés et les causes
imputées souvent à des facteurs qui n'ont aucune relation avec la
science (la croyance, le destin, le mektoub...etc)
Pour les raisons invoquées ci-dessus, il nous a
semblé judicieux de porter notre choix entre autre sur le
thème : le suivie sérologique de la toxoplasmose
chez la femme enceinte.
La toxoplasmose est une maladie parasitaire, cette maladie est
sans aucune gravité lorsqu'elle est contractée en dehors d'une
grossesse ; elle varie essentiellement en fonction du niveau
d'hygiène de la population et des habitudes alimentaires, sa
prévalence et très hétérogène selon les
pays, en Europe, sa prévalence s'étend entre 20 à 85%.Aux
Etats Unis, elle est plus faible, elle se situe de 12 à41%. Dans les
autres pays, elle peut varier de 18 à 65%.
Dans le cadre d'une approche académique de ce
thème, il peut être posé la problématique
suivante :
Quels sont les facteurs déclenchants de cette
maladie ?
Quel est le pourcentage de population touché par cette
maladie ?
A quel niveau du corps humain cette maladie se déclare
t-elle ? Pourquoi la contrôle t-on lors d'une grossesse ?
Existe-t-il des moyens pour la dépister ?
Les infrastructures sanitaires disposent t-elles des moyens
adéquats ?
Quels sont les remèdes qui peuvent réduire
efficacement le risque de contraction de cette maladie ?
Pour tenter de répondre aux questions posées
dans la problématique nous proposons de traiter ce thème à
travers un plan de travail qui comporte en l'occurrence un aperçu
théorique (grossesse et généralités sur la
toxoplasmose) et une partie expérimentale dont laquelle nous
examinerons la sérologie de la femme enceinte.
Dans le chapitre I, il sera abordé des questions ayant
trait à la grossesse, son diagnostic biologique, transfert de
l'immunité maternel ainsi que les infections maternofeotales ;
compte tenu du fait qu'il s'agisse d'éléments constituant un
terrain privilégié pour le déclenchement de cette
maladie, tandis que le 2ème chapitre sera consacré à
l'étude de la maladie proprement dite :la
toxoplasmose, la toxoplasmose congénitale,sa
fréquence,l'agent pathogène, son cycle de vie , le mode
d'infection ,l'évolution du risque foetal, les conséquences de
l'infection , les marqueurs de l'infection , ainsi que la prévention et
le traitement.
Et enfin la partie pratique ou expérimentale où
nous essayerons d'examiner la sérologie de la toxoplasmose chez un
certain nombre de femmes enceintes basant sur la recherche d'avidité des
anticorps IgG et IgM antitoxoplasmiques.
CHAPITRE I : LA GROSSESSE
1-1.DEFINITION :
La grossesse (ou gestation) est l'état
physiologique de la femme enceinte du jour de la fécondation
jusqu'à l'accouchement (SHADE, 2001).
La grossesse dure environ 39 semaines, elle se divise en trois
périodes de trois mois chacune, communément appelées
trimestres, mais pour des raisons de conventions internationales, on parle en
semaines d'aménorrhée (à partir du premier jour des
dernières règles), ou en mois de grossesse (ELIA,
1989).
Le tableau n°1 présente la correspondance pratique
entre semaines d'aménorrhée et mois de grossesse.
1-2.DIAGNOSTIC BIOLOGIQUE DE LA GROSSESSE :
Depuis la publication de ZONDEK et ASCHEIME en 1927, le
diagnostic précoce de la grossesse peut être établi avec
certitude par des examens biologiques, ces examens ont pour base la recherche
de l'hormone humain gonadotrophine chorionique (HCG) dans les urines ou le
sérum de la femme (MERGER et al., 1995).
Tab. n°1 : Correspondance pratique
entre mois de grossesse
et semaines
d'aménorrhée (Edwige, 1994).
|
Mois
|
Semaines d'aménorrhée
|
Semaine de grossesse
|
|
1
|
6
|
4
|
|
2
|
10
|
8
|
|
3
|
15
|
13
|
|
4
|
19
|
17
|
|
5
|
24
|
22
|
|
6
|
28
|
26
|
|
7
|
32
|
30
|
|
8
|
36
|
34
|
|
9
|
41
|
39
|
1-3. DEVELOPPEMENT DE L'EMBRYON :
Tout commence simplement par la fusion d'un spermatozoïde
et d'un ovule formant ainsi une cellule d'un dixième de
millimètre au poids insignifiant (figure n°1).
L'ovule roule lentement à la surface de la muqueuse de
la trompe de faloppe, il achève la maturation qui le rend apte à
être fécondé par un spermatozoïde (figure n°2).
De cette cellule originelle naîtront des milliards
d'autres cellules, chacune ayant une fonction bien précise et
irremplaçable (figure n°3).
Les cellules de la périphérie de l'oeuf
fécondé s'ancrent dans la paroi de l'utérus maternel, et
vont former ce qui plus tard deviendra le placenta, les cellules au centre de
l'oeuf vont constituer le bouton embryonnaire qui donnera l'embryon et le
bébé.
Trois semaines après la fécondation, l'embryon
humain mesure à peine 2mm, ses cellules se différencient et
suivent munitieusement le programme préétabli par les
gènes contenus dans les chromosomes.
La semaine suivante, l'esquisse d'un être humain se
dessine avec une ébauche de coeur en son centre, de cerveau à son
extrémité supérieur et de coccyx à l'autre
extrémité (figure n°4).
Le cerveau est bien individualisé dés la fin du
deuxième mois, on distingue alors les hémisphères
cérébraux à travers la peau transparente du crâne,
la tête grossit beaucoup ,les lèvres épaisses et le nez
aplati (figure n°5) .
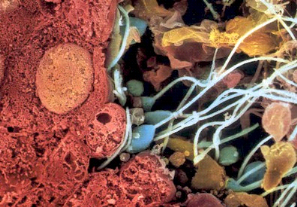
Fig. n°1 : Fusion d'un
spermatozoïde et d'un ovule
(POLGE, 1984).
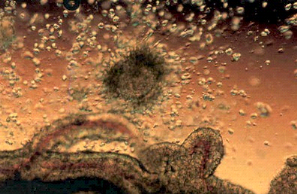
Fig. n°2 : Maturation de l'ovule
pour être apte à la
fécondation (POLGE, 1984).
Au début du troisième mois de grossesse
débute la période foetale, le foetus est bien installé
dans le sac amniotique nageant dans le liquide amniotique et relié
à sa mère par le cordon ombilical (figure n°6).
Dés le quatrième mois ,la future maman commence
à sentir son bébé bouger, au cinquième mois le
foetus prend du poids , ses mouvements pas ordonnés
témoignent de sa vitalité , à la fin de ce mois le futur
bébé pèse 500g pour 25cm .
Au cours du septième mois, un enduit blanchâtre
recouvre sa peau, il bouge beaucoup et ses paupières sont ouvertes, il
commence à se trouver à l'étroit, son sommeil de 16
à 20 heures par jour, ne suit pas forcément le rythme de sa
mère, son coeur bat au rythme de 120 à 160 battements par
minute.
Quarante et une semaines et trois jours ; c'est le terme
théorique de la grossesse, et enfin vient l'accouchement
(POLGE ,1984).
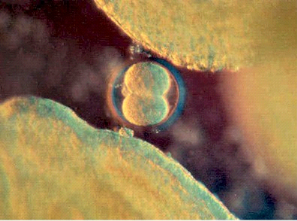
Fig.n°3 : Division de
l'oeuf après fécondation
(POLGE,
1984).
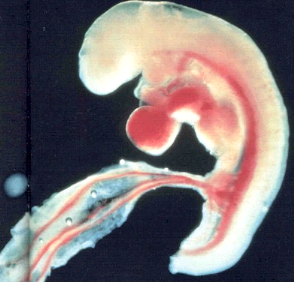
Fig.n° 4 : L'esquisse d'un
être humain se dessine
(POLGE,
1984).
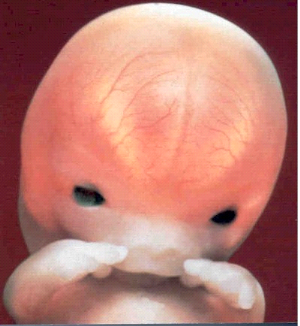
Fig.n° 5 :
Le cerveau est bien individualisé
dés la fin du
2éme mois (POLGE ,1984).
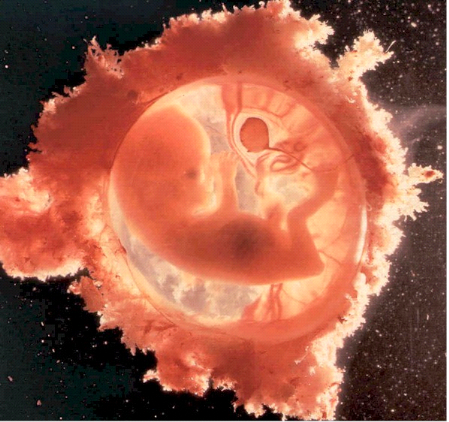
Fig.n°6: La
période foetale (POLGE, 1984).
1.4-TRANSFERT PASSIF DE L'IMMUNITE MATERNELLE :
Il s'agit d'un transfert passif des anticorps entre la
mère et le foetus,c'est le placenta et l'utérus qui assure le
rôle de barrière pour protéger le foetus contre les
infections (et qui empêche le foetus de subir le phénomène
du rejet) ,de ce fait les capacités de défense du foetus contre
l'infection sont faible d'où un risque important de mortalité et
d'avortement lors d'infection d'une femme enceinte .
La transmission des anticorps maternels au foetus
présente un avantage et un inconvénient :
l'avantage est d'assurer une protection immédiate efficace contre
les différents antigènes.
L'inconvénient est que l'immunité
adaptée à l'environnement maternel ne protége pas le
foetus contre les antigènes que la mère n'a pas
rencontrés, cela veut dire que le foetus peut être au contact aux
antigènes contre lesquels, il n'a pas reçu d'anticorps, donc
l'immunité et les principaux mécanismes d'immunité sont
efficaces dés la naissance (DELPHINE ,2002).
1.5-INFECTIONS MATERNOFOETALES :
Plusieurs infections contractées pendant la grossesse
sont susceptibles de contaminer le foetus par voie transplacentaire, notamment
les infections parasitaires, puisque chez la femme enceinte des parasites
passent communément dans le sang, la plupart du temps sans dommage, il
arrive que ces infections touchent le placenta sans aller plus loin, mais elles
peuvent aussi atteindre le foetus et avoir des conséquences gravissimes.
Parmi ces infections, il convient de citer « la
toxoplasmose » qui est une maladie parasitaire dont l'agent
pathogène est un parasite nommé toxoplasma gondii; par
sa fréquence et le poids de ses conséquences prend une dimension
socio-économique considérable (PECHERE et al.,
1982).
CHAPITRE II : LA TOXOPLASMOSE
2.1-HISTORIQUE :
C'est en 1908 que NICOLLE et MANCEAUX découvrirent la
toxoplasmose chez de nombreux mammifères sauvages entre autres chez un
rongeur appelé : Ctenodactylus gondii à la
suite d'une épidémie de laboratoire à l'institut pasteur
de Tunis, ils isolèrent un protozoaire de forme arquée, c'est
ainsi qu'ils nommèrent le parasite : toxoplasma gondii,
l'origine du mot est grecque : toxon « arc » et
plasma « forme », mais ce n'est qu'en 1923 que JANKU
décela le premier cas humain, en 1937-1938 WOLF et COWEN firent les
premières expérimentations.
Au début, on pensait se trouver en présence
d'autant d'espèces de toxoplasmes différents mais en 1939 SABIN a
montré qu'il s'agisse d'une seule et même espèce :
Toxoplasma gondii, c'est encore lui en collaboration avec FELDMAN qui
découvrirent et mirent au point un test immunologique le DYE TEST qui
permet le diagnostic sérologique de cette parasitose (GOLVAN,
1983).
2.2-QU'EST CE QUE LA TOXOPLASMOSE ?
La toxoplasmose est une zoonose (Maladie infectieuse
atteignant l'animal mais également transmissible à l'homme)
(BOUREE ,1989).
Cette maladie parasitaire cosmopolite est due à un
protozoaire intracellulaire : toxoplasma gondii.
Sur le plan clinique, elle existe sous trois formes : la
toxoplasmose acquise habituellement bénigne et très souvent
inapparente, la toxoplasmose de l'immunodéprimé que ce soit dans
le cadre des sidéens ou dans le cadre des transplantés et
gréffés, et la toxoplasmose qui survient au cours de la grossesse
et qui est transmissible au foetus et responsable de foetopathies graves
dite : toxoplasmose congénitale
(AMBROISE ,1998).
2.2.1-PREVALENCE DE LA TOXOPLASMOSE :
La toxoplasmose est ubiquitaire, elle peut atteindre 85% de la
population (ELIA, 1989), sa prévalence est très
hétérogène selon les pays, elle varie essentiellement en
fonction du niveau d'hygiène de la population et des habitudes
alimentaires (FORTIER et AJANA, 1993).
2.2.2-Agent pathogène :
a- Morphologie et biologie du parasite :
Toxoplasma gondii est un protozoaire, parasite
intracellulaire obligatoire, c'est un pathogène très
répandu chez l'homme.
Le parasite dont l'hote définitif est le chat, est
disséminé dans la nature et infecte de nombreux autres
mammifères (AMBROISE ,1998).
Il se présente sous trois formes
évolutives : forme végétative, kyste et oocyste.
1) LA Forme végétative :
Elle a une forme d'arc et mesure de 5 à 10 ì m
sur 1 à 3 ì m, encore appelée
tachyzoîte, ce terme vient du grec tachus (rapide) pour
évoquer la rapidité de sa division dans les cellules qui
l'hébergent. Une extrémité est plus arrondie que l'autre,
le pôle extérieur près duquel est
généralement situé le noyau. L'extrémité
antérieure présente un appareil de pénétration ou
complexe apical (Figure n° 7).
Les formes végétatives sont rapidement
détruites par l'acide chlorhydrique gastrique. Leur ingestion ne peut
donc pas entraîner la contamination
(AMBROISE ,1998).
2) KYSTE :
Sphérique ou ovoïde, il mesure 50 à 200
ì m, il résulte d'une série de multiplication
asexuée d'une forme végétative qui arrive progressivement
à coloniser tout l'intérieur d'une cellule hôte
entourée par une membrane
épaisse et résistante (Figure
n° 8) , les kystes contiennent plusieurs centaines
à plusieurs milliers de formes végétatives. Un kyste de
100 um contient 2 à 3000 bradyzoïtes (parasite ne
se divisant que très peu, du grec bradus-lent). Lors de conditions
favorables, les bradyzoïtes se transforment en tachyzoïtes qui vont
se déplacer et coloniser les cellules de l'hôte.
Les kystes sont particulièrement abondants dans les
tissus pauvres en anticorps (tissu nerveux).
Dans les tissus, les kystes restent très longtemps
vivants.
Les kystes sont des formes de résistance et de
dissémination. Ils ne sont pas détruits par des
températures inférieures à 45 c°, ni par l'acide
chlorhydrique gastrique. C'est cette résistance particulière qui
rend possible le principal mode de contamination humaine par ingestion de
viande, contenant des kystes de toxoplasmes, consommée crue ou saignante
(AMBROISE, 1998).
3) oocyste :
Ovoïde (14x9 ì m), également forme de
résistance et de contamination, il est issu d'une multiplication
sexuée. Après maturation, il contient deux sporocystes renfermant
chacun 4 sporozoïtes (Figure n° 9).
Les oocystes sont capables de demeurer infestant au moins un
an dans le sol humide. Ils ne sont pas détruits par l'acide
chlorhydrique gastrique
et sont responsables de la contamination des herbivores et,
chez l'homme, d'un mode d'infestation accessoire (au moins en France) par
ingestion de fruits ou de crudités souillées (AMBROISE,
1998).
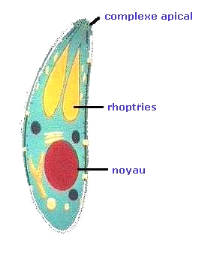
Fig.n° 7: Toxoplasma gondii
Forme tachyzoîte (AMBROISE ,1993).

Fig. n° 8: Toxoplasma gondii
forme kystique (AMBROISE, 1993).

Fig. n°9 : Toxoplasma gondii
forme oocyste (AMBROISE ,1993).
b- Cycle de vie du toxoplasme :
Il correspond à deux modalités
différentes produisant chacune un stade infestant particulier (Figure
n°10).
1) Cycle Asexué,
incomplet :
Il fait intervenir uniquement des hôtes
intermédiaires (homme, animaux omnivores ou carnivores). La
contamination est liée à l'ingestion des kystes contenus dans la
chair d'animaux aussi bien carnivores qu'herbivores. Les kystes libèrent
les toxoplasmes qui se reproduisent rapidement par multiplication
asexuée. Ils donnent naissance à des kystes intracellulaires qui
permettent la poursuite du cycle par carnivorisme (AMBROISE,
1998).
2) Cycle complet :
Il se déroule successivement chez un hôte
intermédiaire (généralement un oiseau ou un petit
mammifère), puis chez l'hôte définitif, le chat, ce dernier
s'infeste en ingérant des kystes contenus dans ses proies. Les formes
végétatives libérées par les kystes
pénètrent dans les cellules de l'intestin grêle du chat
où elles se reproduisent par multiplication asexuée
(schizogonie).
Des éléments sexués apparaissent ensuite,
males ou femelles également situés dans les cellules de
l'intestin grêle. La fécondation (gamogonie) aboutit à la
formation d'un oeuf particulier, l'oocyste est rejeté dans le milieu
extérieur avec les féces du chat.
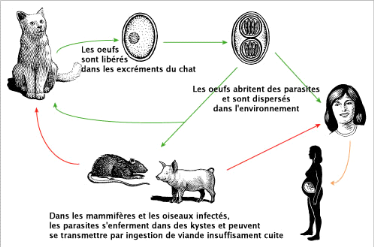
Fig. n° 10 : cycle de vie de la
toxoplasma gondii (AMBROISE, 1993).
Cet oocyste n'est pas infestant et plusieurs jours sont
indispensables pour permettre sa maturation (sporogonie). Il rend possible la
contamination des
herbivores. Il intervient également dans la
contamination des omnivores (AMBROISE, 1998).
c- Mode de contamination :
L'homme se contamine par l'alimentation (ingestion de
kystes) :
-En mangeant de la viande qui n'est pas assez cuite.
-En buvant du lait non pasteurisé qui renferme le
parasite toxoplasma gondii
- En consommant des légumes et fruits souillés
par la terre.
-L'homme se contamine par contact avec le chat (ingestion
d'oocystes).Après avoir été avalés par un sujet,
les oocystes éclatent dans les intestins et se propagent à tout
l'organisme par voie du courant sanguin.
-Il est déjà arrivé que la toxoplasmose
soit transmise par transfusion sanguine et par transplantation d'organe.
-La transmission du parasite de personne à personne
ne peut se produire que chez la femme enceinte à son enfant par voie du
placenta (Figure n°11). (EDWIGE, 1994).
Transplacentaire
Ingestion des viandes
Ingestion des fruits et végétaux
contaminés
Mode
d'infection
Source d'infection
Stade parasitaire
Oocyste
Tachyzoite
Kyste tissulaire
Environnement
Sol, végétaux, fruit, eau.
Liquide biologique
Tissus, organe :
Muscle, coeur, foie, rein, poumons.

Fig. n°11 : Sources et mode
d'infection humaine par toxoplasma gondii
(EVANS, 1992).
2.2.3-SYMPTOMATOLOGIE :
1) l'infection aigue :
Les symptômes sont une grosse fatigue, de la
fièvre, l'augmentation du volume des ganglions et des douleurs
musculaires, Dans 80% des cas, il s'agit d'une forme inapparente car le patient
n'a pas de fièvre, mais seulement une augmentation du volume des
ganglions pendant une huitaine de jours, il ne s'en souviendra souvent pas.
2) Les formes
symptomatiques :
Ces formes touchent les personnes
immunodéprimées comme les sidéens, le parasite va alors se
produire dans tous les organes : cerveau, oeil, coeur.
3) Les formes
congénitales :
Elles correspondent à l'infection du foetus durant la
grossesse, cela suppose que la mère a fait une toxoplasmose aigue, ou
une première infection qui ne sera pas visible en dehors de la
sérologie systématique .L'infection peut
être grave et provoquer l'avortement, la mort du foetus ou une naissance
prématurée (AMBROISE ,1998).
2.3-TOXOPLASMOSE ET GROSSESSE :
Chez la femme enceinte, la toxoplasmose peut être
caractérisée par certains symptômes se manifestant
généralement par un gonflement des ganglions
éventuellement accompagné d'une fièvre, maux de gorge ou
de tête, fatigue et des douleurs musculaires, mais elle peut bien passer
complètement inaperçue ; de ce fait ne peut pas être
diagnostiquer en
dehors de la sérologie, mais la transmission de cette
infection au foetus est à l'origine de lourdes conséquences,
cette transmission s'effectue en
moyenne 4 à 8 semaines après la colonisation du
placenta (DESMONTS ,2004).
Les femmes séropositives avant d'être enceintes
ne transmettent qu'exceptionnellement le parasite à leur enfant, celles
qui sont séronégatives sont susceptibles d'être
infectées durant leur grossesse
(THULIEZ ,1993).
2.3.1-TOXOPLASMOSE
CONGENITALE :
La toxoplasmose congénitale est due à la
transmission maternofoetale du protozoaire toxoplasma gondii
après primo-infection maternelle (ROMAND et
THULIEZ, 2003).
Elle succède au passage du toxoplasme à travers
le placenta dont laquelle la contamination se fait in utero (GOLVAN,
1983).
2.3.2-FREQUENCE DE LA TOXOPLASMOSE
CONGENITALE :
Elle est estimée de 1 à 3 pour 1000 grossesses,
soit 700 à 3000 cas par an (VIGOT, 1981).
Elle dépend de plusieurs facteurs :
-La date de survenance de l'infection maternelle.
- La virulence de la souche parasitaire.
-L'importance de l'inoculum.
-La qualité de la réponse immunitaire de la
mère (ROMAND et THULLIEZ, 2003).
2.3.3-EVOLUTION DU RISQUE FOETAL :
La toxoplasmose congénitale est très souvent
grave, surtout au cours du premier trimestre de la grossesse, par contre plus
la grossesse avance plus
la transmission est fréquente , mais elle est moins
grave (Figure n°11) (BOUREE, 1989).
Schématiquement, le risque peut évoluer de la
façon suivante :
-Pendant le premier trimestre de grossesse, le placenta est de
taille très réduite et laisse rarement passer les toxoplasmes, si
la mère se contamine à ce moment, les risques de transmission au
foetus sont minimes.
Au contraire, après le troisième mois, la
barrière placentaire est moins efficace et la contamination du foetus
est facilitée.
Mais, la gravité des lésions suit pratiquement
un schéma inverse du précédent :
La contamination pendant le premier trimestre de la gestation
est responsable des lésions les plus graves, au contraire, les
contaminations tardives ne provoque généralement que des formes
dégradées, retardées ou même absolument inapparentes
à la naissance (AMBROISE-THOMAS, 1998).
% d'atteinte foetale « atteinte
sévère et d'enfants morts nés
parmi les infections
congénitales »
41%
14%
1er trimestre
8%
29%
2éme trimestre
0%
59%
3éme trimestre
Taux de transmission
Fig. n°12: Fréquence de la
transmission transplacentaire de toxoplasmes et sévérité
de l'infection congénitale (
www.biomérieux.com ).
Le risque d'infection foetale croît
régulièrement du début à la fin de la grossesse,
passant progressivement de 1% en période périconceptionnelle
à 20% autour de la 20e semaine pour atteindre 75% à 90% au
voisinage du terme (Tableau n°2) :
-Si la contamination se fait au moment de la conception de
l'enfant, le risque de transmission au bébé est très
faible, mais la gravité de l'atteinte est importante.
-Si la contamination se fait avant la 16ème
semaine d'aménorrhée, le risque de transmission est important, et
la gravité de l'atteinte est maximale (lésions s'accompagnant de
destructions cérébrales, hydrocéphalie ...etc.)
- Si la contamination se fait après la
16ème semaine d'aménorrhée, le risque de
transmission est maximal, mais la gravité de l'atteinte est d'autant
plus faible que l'on se rapproche du terme.
- La période la plus dangereuse se situe entre la
10ème et la 16ème semaine
d'aménorrhée qui correspond aux 2ème et
3ème mois de grossesse
(THULLIEZ et DESMONTS, 1988).
Tab. n°2 : Fréquence des
infections foetales en fonction du terme de la
contamination maternelle (THULLIEZ
et DESMONTS, 1988).
|
epoque de l'infection maternelle
|
risque FOETAL de transmission
|
risque foetal de gravité
« si transmission »
|
|
Antérieur à la
conception
|
-nul
-sauf si déficit immunitaire
|
-nul
-sauf si déficit immunitaire
|
|
Préconceptionelle
|
Faible environ 1%
|
Risque maximal
|
|
Avant la 16éme semaine
d'aménorrhée
|
Important :
-mère traitée 5%
-Non traité 15%
|
Risque maximal
|
|
Après la 16éme semaine
d'aménorrhée
|
Maximal :
-20% entre 16et 26 semaines d'aménorrhée.
- plus de 90% à terme
|
D'autant moindre que l'infection est plus proche a terme
|
2-3-4) CONSEQUENCE DE LA TOXOPLASMOSE
CONGENITALE :
Elles sont multiples (figure n°12) :
a) La forme majeure :
Encéphalomyélite toxoplasmique, elle s'observe dés la
naissance et correspond à une contamination maternelle puis à
une transmission au foetus survenue au tout début de la grossesse.
Elle est caractérisée par quatre groupes de
signes.
1) Aspect et volume du
crâne :
Macrocéphalie avec hydrocéphalie externe,
bombement des fontanelles, augmentation du périmètre
crânien dés la naissance est supérieur à la normale,
mais surtout augmente ultérieurement plus vite que la normale.
2) Signes neurologiques
variés :
-Des convulsions généralisées.
-Des troubles du tonus avec soit hypotonus ou hypotonus.
-Des modifications des réflexes.
-Des troubles végétatifs (déglutition,
irrégularité respiratoire ;
déséquilibre thermique).
3) Calcification
intracrânienne :
Presque pathognomoniques.
4) Signes oculaires :
-Microphtalmie, strabisme, nystagmus décelés
à l'inspection du visage.
-Choriorétinite pigmentaire maculaire unie ou
bilatérale et associée à des signes
d'évolution récente et des traces de foyers cicatrisés.
b) Les formes
viscérales :
Correspondent généralement à des
contaminations in utero plus tardives, caractérisées soit
par :
-Un ictère néonatal avec
hépato-splénomégalie et hémorragies muqueuses.
- Une atteinte digestive aigue à type
d'oesophagite ou de colite ulcéro-hémorragique. Ces formes sont
à la limite des possibilités thérapeutiques.
c) Les formes dégradées ou
retardées :
Elles sont reconnues dés la naissance ou ne sont
dépistées quelque fois qu'après plusieurs
années.
Elles comportent l'un des signes suivants :
-Retard psychomoteur.
-Périmètre crânien augmentant plus
rapidement que la normale.
-Crises convulsives.
-Apparition souvent tardive d'un foyer de
Choriorétinite pigmentaire à tendance récidive.
d) Les formes inapparentes ou infra-clinique
à la naissance :
Ont uniquement une traduction sérologique, il est
important de les dépister très précocement et de les
traiter afin d'éviter une éventuelle décompensation avec
passage à la forme retardée et dégradée.
Ces formes inapparentes sont les plus nombreuses et,
actuellement représentent environ 80% des toxoplasmoses
congénitales.
e) Enfin, la toxoplasmose congénitale
peut être responsable d'avortement ou de prématurité
(AMBROISE-THOMAS ,1998).
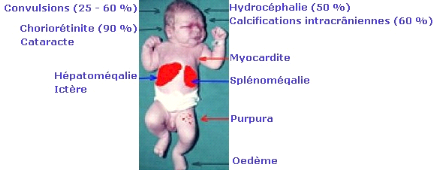
4) Signes oculaires :
-Microphtalmie, strabisme, nystagmus décelés
à l'inspection du visage.
-Choriorétinite pigmentaire maculaire uni ou
bilatérale et associe des signes d'évolution récente et
des traces de foyers cicatrisés.
Fig. n°13: Toxoplasmose
congénitale (AMBROISE, 1993).
2.3.5 -MARQUEURS DE L'INFECTION :
Une femme enceinte qui n'a jamais contractée la
toxoplasmose est dépourvue des marqueurs sérologiques pour
cette infection.
L'infection par toxoplasma gondii provoque une
réaction humorale très riche avec des anticorps persistant durant
toute la vie de l'individu (Figure n° 13).
Les tests habituellement pratiqués permettent de mettre
en évidence des immunoglobulines Ig de type G et M.
-Au jour zéro où se développe
l'épisode infectieux, des anticorps spécifiques apparaissent dans
le sang, ce sont tout d'abord des IgM qui sont les marqueurs
de l'infection active et qui vont persister en moyenne 6 mois.
-Chez 80 % des malades, on trouve également des
IgA longtemps utilisé pour dater l'infection toxoplasmique, ce
marqueur est tombé en désuétude avec l'apparition des
tests d'avidité.
-Enfin, les IgG montent très
rapidement pour atteindre un plateau et décroître par la suite,
ils resteront cependant positifs à vie (DEROUIN et THULLIEZ,
1993).
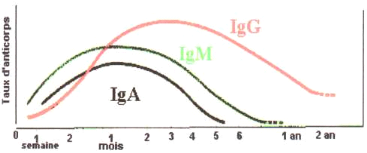
Fig. n°14: Courbe
sérologique chez la femme enceinte
(AMBROISE, 1998).
2.3.6-DIAGNOSTIC BIOLOGIQUE DE LA TOXOPLASMOSE :
Le diagnostic doit être constant chez toute femme
enceinte en début de grossesse, et mieux, avant la
procréation.
Il est sérologique et doit comprendre la recherche des
IgG et celle des IgM (MERGER et al.,
1995).
Celle des IgG se fait par réaction
d'agglutination directe ou par réaction d'immunofluorescence indirecte
donnant une limite de positivité a 10UI/ml.Les IgG
spécifiques n'apparaissent que 12à 15 jours après
l'infection, avec un taux maximum vers les 2 mois , puis une
décroissance
jusqu'à un taux faible qui persiste
définitivement.
La recherche des IgM se fait par
immunofluorescence (test de REMINGTON), celles-ci ne s'observent qu'au
début de la maladie et disparaissent au delà de 2à 4
mois.
-Si le taux d'IgG est compris entre 10 et
300 UI/ml et le test de REMINGTON négatif, la femme est immunisée
et n'a pas besoin d'être surveillée.
-Si le taux d'IgG est inférieur
à 10 UI/ml et le test de REMINGTON négatif, la femme est
exposée à la toxoplasmose, ce qui impose une surveillance
mensuelle pendant toute la grossesse. Une contamination se traduira par
séroconversion.
-Si le taux d'IgG est supérieur
à 300UI/ml, la femme est atteinte de toxoplasmose évolutive,
très récente si le test de REMINTON est positif (MERGER
et al., 1995).
2.3.7-PREVENTIONS:
La prévention ne concerne que les femmes
séronégatives au cours de leur grossesse (absence de vaccination)
(AMBROISE, 1998).
Il y a des règles
hygiéno-diététiques à suivre telles que :
-Eviter les contacts avec les chats et leur litière.
-Lavez vous les mains soigneusement après avoir
manipulé de la viande saignante, ou de la terre potentiellement
souillée, ou bien porter des gants en cas de manipulation.
-Si vous avez un chat à la maison, faites le examiner
et éventuellement traiter par votre vétérinaire.
-Lavez soigneusement les fruits et les légumes,
privilégier les légumes cuits, éviter la consommation des
crudités.
-Bien cuire la viande, éviter la consommation de viande
fumée ou grillée, préférez le poisson et la
volaille en cas de repas en dehors du domicile
(EDWIGE ,1994).
-Chez toutes les femmes, un examen sérologique est
obligatoire avant la grossesse ou lors de l'examen prénuptial, en
l'absence d'immunité, il sera refait dés que le diagnostic de
grossesse est posé, et répété tous les mois afin de
dépister une séroconversion dont la découverte trop
tardive est cause de la plupart des échecs (MERGER et
al., 1995).
-A titre de prévention, un suivi systématique
est effectué en France, depuis 1978, chez les femmes non
immunisées contre la toxoplasmose tout au long de leur grossesse
(BOUGNOUX et HUBERT, 1990).
2.3.8-TRAITEMENT :
Les femmes enceintes qui ne sont pas immunisées
contre la toxoplasmose sont donc contrôlées tous les mois (une
prise de sang suffit) afin de vérifier qu'il n'y a aucune atteinte.
Cela permet si elles contractent la toxoplasmose de prendre
des mesures immédiates afin de diminuer au maximum le risque de passage
du parasite au foetus grâce à un traitement et d'essayer
d'éviter ainsi toute atteinte grave (AMBROISE, 1998)
Dés que le diagnostic d'infection maternelle est
établi ou fortement suspecté : Spiramycine jusqu'à
l'accouchement.
Si une infection foetale est démontrée ou
fortement suspectée : Pyriméthamine + sulfamides + acide
folinique, en remplacement de la Spiramycine (tableau N°3) (ROMAND
et THULLIEZ, 2003).
-Dans le cas où le foetus a été
contaminé, il existe plusieurs hypothèses selon la gravité
de l'atteinte :
-Soit l'atteinte est grave, il existe des lésions
cérébrales importantes visibles à l'échographie et
il peut être nécessaire d'interrompre la grossesse.
-Soit il n'existe pas des lésions échographiques
et le cas est alors discuté avec les médecins, un traitement
intensif médicamenteux est possible avec une surveillance
rapprochée par échographie.
Tout dépendra donc du terme où la toxoplasmose
a été contractée (AMBROISE,
1998).
Tab.n°3 : Traitement
anténatal (ROMAND et THULLIRZ, 2003).
|
Indications
|
Médicaments
|
Posologie
|
Durée
|
|
Infection maternelle en cours de grossesse
|
Spiramycine
(Rovamycine®)
|
3 g / jour
|
Jusqu'à l'accouchement
|
|
Infection foetale ou infection maternelle tardive
|
Pyriméthamine
(Malocide®)
Sulfadiazine
(Adiazine®)
Acide folinique
(Lederfoline®)
|
50 mg / jour
3 g / jour
50 mg / semaine
|
Jusqu'à l'accouchement
|
CHAPITRE III : MATERIELS ET METHODES
1- PROBLEMATIQUE :
Durant la grossesse, la femme est sujette à de
nombreuses infections, parmi les plus importantes, nous nous sommes
intéressées à la toxoplasmose congénitale,
qui est responsable de foetopathies graves, d'avortement et de
prématurité. Les manifestations cliniques de la
toxoplasmose congénitale peuvent être
particulièrement graves lorsque la contamination foetale a lieu au cours
du premier trimestre de la grossesse, et il est fréquent que les femmes
enceintes viennent au laboratoire pour effectuer une sérologie
toxoplasmique sans connaître leur statut immunitaire antérieur,
ainsi devant plusieurs cas clinique pouvant faire craindre une
séroconversion précoce chez les femmes enceintes.
2- L'OBJECTIF:
Le but voulu à travers notre étude pratique est
de réaliser un suivi sérologique concernant la recherche des
immunoglobulines IgG et IgM
antitoxoplasmiques chez un certain nombre de femme enceinte.
Autrement dit l'objectif de cette sérologie est d'aider
à la détermination du statut immunitaire.
3- POPULATION ETUDIEE :
Notre étude a été réalisée
au niveau du laboratoire d'analyse médical à Mostaganem durant
une période de 04 mois Janvier- Avril 2006.
La population concernée se compose de 100 femmes
enceintes dont l'age varie entre 17 et 36 ans. Notre échantillon est
réparti comme suite :
(63 immunisées, 37 non immunisées)
4-PRELEVEMENT SANGUIN :
Le prélèvement sanguin se fait chez les malades
de préférence à jeun, au niveau de la veine superficielle
du pli du coude.
Le sang est ensuite recueilli dans des tubes secs.
5- ANALYSE SEROLOGIQUE :
La quantité du sang prélevée est
centrifugée à 5000 tours/ min pendant 5 min, et le dosage
sérologique se fait sur le sérum.
6- LA TECHNIQUE UTILISEE :
Le test sérologique a été
réalisé en technique ELFA (Enzyme linked
fluorescent Assay), sur un automate Mini Vidas
(figure n°16 ) permettant la
mesure d'avidité des IgG et IgM
antitoxoplasmiques, nos résultats sont exprimées en unités
internationales par ml (UI/ml).
6.1-DOSAGE DES IgM :
Principe :
-Le principe du dosage associe la méthode
immunoenzymatique par immunocapture à une détection finale en
fluorescence (ELFA).
-Le cône à usage unique sert à la fois de
phase solide et de système de pipetage.Les autres réactifs de la
réaction immunologique sont prêts à l'emploi et pré
répartis dans la cartouche (Tableau n°4).
-Toutes les étapes du test sont réalisées
automatiquement par l'instrument.
Elles sont constituées d'une succession de cycle
d'aspiration/refoulement du milieu réactionnel.
Tableau n° 04: Description de la cartouche
des IgM (FORTIER et al., 1990)
|
Puits
|
réactifs
|
|
1
|
Puits échantillon
|
|
2
|
Diluant sérum : Tampon TRIS (50mmol/l) PH 7,4 +
stabilisants protéiques et chimiques + azoture de sodium 0,9 g/l (300 u
l)
|
|
3
|
Tampon de prélavage : TRIS (50mmol/l) PH 7,4 +
stabilisants protéiques et chimiques + azoture de sodium 0,9 g/l (600 u
l)
|
|
4-5-7-8
|
Tampon de lavage : TRIS (50mmol/l) PH 7,4 + stabilisants
protéiques et chimiques + azoture de sodium 0,9 g/l (600 u l)
|
|
6
|
Conjugué : immuncomplexe (antigène
toxoplasmique souche RH Sabin - anticorps monoclonal de souris anti-P30)
marqué a la phosphatase alcaline + azoture de sodium 0,9 g/l +
gentamycine 0,02 % (400 u l)
|
|
9
|
Puits vide
|
|
10
|
Cuvette de lecture avec substrat : 4-Méthyl -
ombélliferyl phosphate (0,6 mmol/l) + diéthanolamine (DEA*)
(0 ,62mol/l soit 6 ,6 % PH 9,2) + azoture de sodium 1 g/l (300
ul)
|
-Après une étape de dilution du sérum,
les IgM sont capturées par l'Ac poly clonal
présent sur la paroi du cône.
Les IgM anti-toxoplasmiques sont
détectées spécifiquement par de l'antigène
toxoplasmique inactivé, lui même révélé par
anticorps anti-toxoplasmique conjugué à la phosphatase
alcaline.
-Lors de l'étape finale de révélation, le
substrat(4-Méthyl-Ombelliferyl phosphate) est aspiré puis
refoulé dans le cône ; l'enzyme du conjugué catalyse
la réaction d'hydrolyse de ce substrat en un produit
4-Méthyl-Ombélliferone) dont la fluorescence émise est
mesurée a 450 nm. La valeur de signal de fluorescence est
proportionnelle à la concentration d'anticorps présents dans
l'échantillon.
-A la fin du test, un indice est calculé
automatiquement par l'instrument par rapport au standard S1
mémorisé (Tableau n°5), puis imprimé (FORTIER
et al., 1990).
Tab.n°5: Normes utilisés pour le
dosage des IgM (FORTIER et al., 1990) :
|
Indice
|
Interprétation
|
|
i < 0.56
|
Négatif
|
|
0.55 = i = 0.65
|
Equivoque
|
|
i =0.65
|
positif
|
6.2-DOSAGE DES IgG :
Principe :
-Le principe du dosage associe la méthode
immunoenzymatique par immunocapture à une détection finale en
fluorescence (ELFA).
-Le cône à usage unique sert à la fois de
phase solide et de système de pipetage. Les autres réactifs de la
réaction immunologique sont prêts à l'emploi et pré
répartis dans la cartouche (Tableau n°6).
-Toutes les étapes du test sont réalisées
automatiquement par l'instrument.
Elles sont constituées d'une succession de cycle
d'aspiration/refoulement du milieu réactionnel.
-Dans une première étape l'échantillon
est dilué, puis aspiré et refoulé à
l'intérieur du cône .les anticorps anti-T.gondii présents
dans l'échantillon vont se fixer aux antigènes T.gondii
fixées à l'intérieur du cône.
-Des étapes de lavage éliminent les composés
non fixés .au cour de la seconde étape des IgG monoclonales
(souris) anti-IgG humaines conjuguées à la phosphatase alcaline
sont aspirées et refoulées à l'intérieur du
cône et vont se lier aux IgG humaines fixées sur
l'antigène.
-Lors de l'étape finale de révélation, le
substrat (4-méthyl-ombelliferyl phosphate) est aspiré puis
refoulé dans le cône ; l'enzyme du conjugué
catalyse la réaction d'hydrolyse de ce substrat en un produit
(4-méthyl-ombelliferone)
dont la fluorescence émise est mesurée à 450
nm .la valeur du signal de fluorescence est proportionnelle à la
concentration de l'anticorps Présent dans l'échantillon.
-A la fin du test, les résultats sont calculés
automatiquement par l'instrument par rapport à une courbe de calibration
mémorisée, puis imprimés et sont interprétés
dans le tableau n°7 (FORTIER et al., 1990).
Tab. n° 6 : Description de la
cartouche des IgG(FORTIER et al.,1990) :
|
Puits
|
réactifs
|
|
1
|
Puits échantillon
|
|
2
|
Diluant sérum : tampon TRIS (50mmol/l) PH 7 ,4
+stabilisants protéiques et chimiques+azoture de sodium 0,9g/l
(600ul)
|
|
3
|
Tampon de prélavage : TRIS (80mmol/l) pH 7,4
+stabilisants protéiques et chimiques+azoture de sodium 0,9g/l
(600ul)
|
|
4-5-7-8
|
Tapon de lavage : TRIS (50mmol /l) pH 7,4+ stabilisants
protéiques et chimiques +azoture de sodium 0,9g/l(400ul)
|
|
6
|
Conjugué : anticorps monoclonal anti-IgG humaines
(souris) marqué à la phosphatase alcaline + azoture de sodium 0,9
g/l (400ul)
|
|
9
|
Diluant sérum : tampon TRIS (50mmol/l) pH7,4 +
stabilisants protéiques et chimiques + azoture de sodium 0,9g/l
(400ul)
|
|
10
|
Cuvette de lecture avec substrats : 4- méthyl-
ombelliferyl
Phosphate (0,6mmol/l) +diéthanolamine (DEA*) (0,62 mol / l
soit 6,6%, PH 9,2) + azoture de sodium 1g/l (300ul)
|
Tab.n°7 : Normes utilisés pour
le dosage des IgG (FORTIER et al., 1990) :
|
Titre (UI/ml)
|
Interprétation
|
|
< 4
|
Négatif
|
|
4 = TITRE =8
|
Equivoque
|
|
= 8
|
Positif
|

Fig. n°16 : La photo de L'appareil mini
VIDAS (BIOMERIEUX).
CHAPITRE IV : RESULTATS ET DISCUSSION
1-RESULTATS ET INTERPRETATION
Les femmes qui présentent une sérologie : IgG
+ IgM - sont considérées comme
immunisées, celles qui présentent une sérologie IgG
- IgM + considérées comme non
immunisées.
Sur une étude d'échantillon
réalisées chez 100 femmes enceintes qui a nécessité
un relevé de résultat de 04 mois, on a constaté que :
- les femmes dont l'age est inférieur à 20
ans : 9% des femmes sont immunisées et 12% non
immunisées.
- Celles dont l'age varie entre 20 et 30 ans : 36% sont
immunisées et 15% non immunisées.
- Celles de plus de 30 ans : 18% sont immunisées
et 10% non immunisées.
L'interprétation des résultats est
illustrée dans le tableau ci-dessus :
Tab. n°8 : Pourcentage de
l'immunisation des femmes enceintes en fonction de l'age.
|
Age (ans)
|
% des femmes
|
Positive (immunisées)
|
Négative (non immunisées
|
|
<20
|
21
|
9
|
12
|
|
20-30
|
51
|
36
|
15
|
|
>30
|
28
|
18
|
10
|
|
total
|
100
|
63
|
37
|
Il ressort de notre étude pratique que 37% des femmes
enceintes sont non immunisées , et 63% immunisées.
Prévalence %
10
18
15
36
9
12
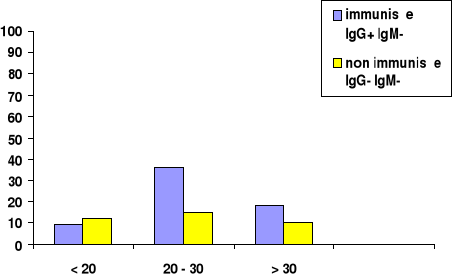
Tranches d'âge par ans
Figure n°15: prévalence de la
toxoplasmose chez 100 femmes enceintes en fonction de l'age.
-On remarqué que la majorité des gestantes qui
se sont présentées pour le dépistage, leur age se
située entre 20 et 30 ans « 51 femmes ».
-Quelques femmes se présentent après le
3ème mois de gestation parfois même deux ou trois
semaines avant l'accouchement.
2- DISCUSSION :
Les résultats obtenus montrent que la variation
de la prévalence de la
toxoplasmose chez les femmes enceintes en fonction de l'age
est non significative.
-Nos résultats se rapproche avec des résultats
d'une étude réalisée au Congo (Non immunisées 40%,
immunisées 60%). (MAKUWA et al., 1992).
Les femmes séropositives n'ont aucune crainte
d'infection congénitale, puisque la maladie confère une
immunité durable. Par contre Celles qui sont séronégatives
sont susceptibles d'être contaminées pendant leur grossesse.
L'affirmation d'une toxoplasmose congénitale
nécessite d'étudier un second prélèvement
concernant les femmes séronégatives, mais cette affirmation n'a
pas pus être établie dans le cadre de notre travail cela est due
en grande partie au manque d'information concernant les conséquences de
cette infection, au coût élevé de ce test.
Donc l'immunisation des femmes enceintes dépend
probablement de plusieurs facteurs comme :
Les préférences alimentaires (niveau de cuisson
des viandes et fréquence de consommation de crudités), le contact
avec les chats, le niveau d'hygiène et les activités
quotidiennes (activités agricoles, activités de jardinage, chat
au domicile et entretien d'une litière de chat, hygiène de
cuisine, manipulations de poubelles, séjour en dehors du domicile).
Les conditions de contamination sont donc largement
réunies.
-les femmes qui se sont présentées après
le 3ème mois de gestation sont mal informées et
ignorent les conséquences que cette maladie peut
engendrées ; car ce test doit être effectuer lors de l'examen
prénuptial , ou lors de la déclaration de la grossesse pour en
épargner les conséquences.
-la toxoplasmose ne peut être décelée lors
d'un questionnaire médical, car certains symptômes peuvent
être confendus à ceux de la grippe, de ce fait la maladie peut
passer complètement inaperçue ; donc seul la
sérologie s'avère efficace.
Conclusion :
Au terme de notre expérimentation à travers les
résultats obtenus sur les 100 femmes enceintes, concernant la recherche
de l'avidité des IgG et IgM
antitoxoplasmique.
On a remarqué que 63% des femmes sont immunisées
et 37% immunisées.
De notre étude, il ressort que la détermination
de l'avidité des IgG et IgM
antitoxoplasmique par la méthode ELFA avec l'utilisation d'un
automate mini VIDAS est fiable et facile à mettre en
oeuvre.
Le test sérologique doit être effectuer
précocement ou lors de la déclaration de la grossesse, afin
d'éviter une éventuelle séroconversion ainsi qu'une
transmission foetale qui est responsable de lourdes conséquences
(avortement , prématurité, malformation........).
Pour éviter les risques de la toxoplasmose
congénitale, la femme enceinte séronégative doit suivre
certaines recommandation afin d'en épargner les risques à son
foetus :
-Il est conseillé de consommer la viande bien cuite
pour éviter l'ingestion possible de kystes de toxoplasma
gondii.
De la même façon une hygiène alimentaire
stricte est recommandée (lavage des fruits et légumes) afin
d'éviter l'ingestion d'oocystes de toxoplasma
gondii.
Enfin tout contact avec le chat est
déconseillé.
Malgré le coût élevé de ce test, le
coût global pour la femme reste moins élevé.
Références bibliographiques
· AMBROISE.T, (1998) :
Parasitologie Mycologie, P : 141, 142,145, 146, 147, 148, 149.
· BOUGNOUX M.-E., HUBERT
B.(1990 ):Toxoplasmose congénitale : bilan de la
prévention primaire en France, p: 13-14.).
· DEROUIN.F, THULLIEZ.P, (1993) :
Diagnostic biologique de la toxoplasmose, P : 33.
· DESMONTS.G, (2004) :
Encyclopédie universelle, P : 145
· EDWIGE.A, (1994) : Attendre mon
enfant aujourd'hui, P : 41, 187, 188.
· ELIA.D, (1989) : Les 1000
réponses sur la femme et son corps, P : 188, 200.
· EVAN.R, (1992) : cycle de vie et
infection toxoplasmique, p : 14.
· FORTIER.B, AJANA.F, (1993) :
Toxoplasme et Toxoplasmose encyclopédie médicale, P :
330.
· FORTIER.B, AJANA.F, CAMUS.D,
(1990) : prévention, diagnostic et suivi de la toxoplasmose
congénitale, p : 156, 157, 158, 159,160.
· GOLVAN.J-.Y, (1983) :
Eléments de parasitologie médicale, P : 320, 321, 328.
· MERGER.R, LEVY.J, MELCHIOR.J, (1995):
Précis D'obstétrique, P : 18, 468, 469.
· MAKUWA.M, LECKO.M, NSIMBA .B,BAKOUETELLA.J,
LOUNANA.K
(1992) : Toxoplasmose et la femme enceinte au
Congo
· PATRICE.B, (1989) : Dictionnaire
de parasitologie, P : 111.
· PECHERE.J.C, (1982) : Les
infections, P : 252
· POLGE.R-H, (1984) : Atlas en
couleur de la vie avant la naissance, P : 35, 40, 41, 67, 208.
· PROUST.J, (1981) : Maladie
infectieuses, P : 182
· ROMAND.S, THULLIEZ.P, (2003) :
Revue française des laboratoires, P : 61,64.
· SCHADE.J, (2001) :
Encyclopédie médecine et santé, P : 256..
· THUILLIEZ.P, (1988) :
Toxoplasmose et grossesse , P : 37.
· THIMOSSAT.P, (1992) :
Médecine d'Afrique noire, P : 39.
· TOMAN.M,
(2002) : Immunologie et immunopathologie, P
326
· www.biomérieux.com.
DICTIONNAIRE :
§ Choriorétinite :
OEdème localisé dans la région maculaire, d'aspect
pseudo-kystique aboutissant à un décollement de la
rétine.
§ déglutition : Acte
réflexe par lequel le bol alimentaire passe de la bouche dans
l'oesophage, puis l'estomac.
§ Hydrocéphalie : Augmentation
du volume du liquide céphalo- rachidien, entraînant, chez l'enfant
une augmentation du volume de la boite crânienne et une insuffisance du
développement intellectuel.
§ Ictère : Coloration jaune de
la peau, due à la présence dans le sang et dans les tissus,
notamment dans la peau, de pigments biliaires (Jaunisse).
§ Macrocéphalie : Augmentation
du volume du crâne.
§ Méningo- encéphalite :
Inflammation simultanée de l'encéphale et des
méninges.
§ Myélite : Inflammation de la
moelle épinière.
§ Microphtalmie : Anomalie
congénitale consistant en une diminution des différents
diamètres de l'oeil.
§ Nystagmus : Mouvement oscillatoires
et quelque fois rotation des globes oculaires, ces mouvements sont
involontaires, sarcadés, horizontaux, verticaux, ils sont
congénitaux ou symptomatiques d'une lésion des centre nerveux.
§ Oesophagite : Inflammation de
l'oesophage (première partie du tube digestif).
§ Purpura : Petites hémorragies
due à la rupture des capillaires dans l'épaisseur du derme et
provoquant l'apparition de taches rougeâtres sur la peau
§ Splénomégalie :
Augmentation du volume de la rate.
§ Tonus : Contraction partielle et
permanente de certains muscles
-Hypertonie : Augmentation
de la tonicité musculaire.
-Hypotonie : Diminution de la
tonicité musculaire.
| 


