REPUBLIQUE DE
GUINEE
Travail -Justice -Solidarité

251658240Université Gamal Abdel Nasser de
Conakry
Faculté des Sciences
Département de Chimie
Master de Chimie Biologie Appliquée :
MACBA
Technologies et Qualité des Produits
Industriels
« Détermination de quelques
paramètres physico-chimiques et microbiologiques des eaux de puits de la
commune urbaine de Mamou »
Mémoire présenté et soutenu à
Conakry, le 12/08/2015
Par
DIALLO Alhassane Diami
Pour obtenir le grade de Master ès Sciences
Président : Dr
Abdoulaye KEITA, MC UGANC
Rapporteur : Dr
Aboubacar DIALLO, UGANC
Membres : Pr Mamadou
SOW, UGANC
Dr Aboubacar SANGARE, UGANC
Consultant: Dr Mamadou Bailo
DIALLO, MC UGANC
Co-consultant: Dr Cellou KANTE, MC
IST-MAMOU
DEDICACE
Je dédie ce mémoire à :
Ø Feu Professeur Saidouba BALDE
Ø Feu Dr Mody Oury DIALLO
Ø Feu père Amadou DIALLO
Ø Au personnel du MACBA
Remerciements
A DIEU, le clément et
Miséricordieux
Pour m'avoir donné la santé et la force de
parachever mes études de l'école primaire jusqu'à ce
stade, le Tout Puissant, Maitre de l'univers, c'est en toi que je place ma
confiance et c'est en toi que je trouve mon soutien.
A mon Père Feu Amadou
DIALLO
Toi, sans le quel je ne saurais atteindre mes objectifs, je ne
sais comment te remercier pour tout ce que tu as fait pour moi, Papa. Je
profite encore de tous tes conseils qui me font suivre le chemin du travail
bienfait. Que DIEU te donne le paradis comme récompense.
A ma Mère Diami NIANG
Femme forte ! Toi qui m'as mis sur la voie de
l'humanité et de la détermination, tu es ma force, et ce travail
est le résultat de tes sacrifices, de tes prières, de tes
conseils, de tes efforts inlassables et quotidiens dans le seul but de voir
tes enfants devenir des personnes respectueuses et respectables. Puissent ton
courage et ta détermination nous servent d'exemples. Merci Maman, que
DIEU te prête vie aussi longtemps et te donne le paradis comme
récompense.
A mes oncles et Tantes
Vous m'avez toujours guidé vers le chemin de
l'honnêteté, la réussite et la dignité humaine.
Malgré la distance qui nous sépare et les multiples
difficultés quotidiennes, vous avez toujours répondus à
mes appels.
Cette réussite est aussi la votre et merci pour tout.
Que DIEU vous prête vie aussi longtemps.
A mes
frères et Soeurs
Boubacar, Fatoumata Binta, Kadiatou et
Aminata
Mon affection pour vous est sans limite, votre soutien, vos
encouragements mais surtout vos prières m'ont guidé
jusqu'à ce résultat qu'il vous importe de savourer à sa
juste valeur. Qu'Allah le tout puissant nous donne longue vie pour que nous
puissions bâtir une famille merveilleuse. Ce travail est le notre, qu'il
soit l'un des éléments fédérateurs de nos liens
familiaux.
Qu'Allah bénisse chacun de nous.
A mes amis
Nous avons traversé de longues
épreuves ensemble. Sachez que les moments passés à vos
cotés ont été les meilleurs. Vous êtes comme des
frères et soeurs pour moi, merci pour vos soutiens et vos conseils.
Puisse cette amitié qui nous lie dure à jamais. Qu'Allah vous
protège vous et vos familles.
Ce travail est le notre que DIEU nous donne la chance de savourer
cette réussite et bien d'autres à jamais.
A ma Femme
Nènè Mariama DIALLO
Ce travail est ton oeuvre car tu n'as ménagé aucun
effort sur le chemin de ma réussite. Ce travail est la
consécration de tes énormes sacrifices et le témoignage
de ma vive reconnaissance et ma profonde affection. Je suis fier de toi et
j'ose espérer un avenir meilleur entre nous, que DIEU nous donne longue
vie, santé et d'enfants, et nous accorde le paradis.
A mes enfants
Tiguidanké et
Abdoul Gadirou
Vous représentez bien plus que vous ne le croyez pour
moi. Merci de m'avoir soutenu, supporté et encouragé, ce travail
est le votre.
Aux membres du Jury
Vous nous faites un grand honneur et un réel plaisir en
acceptant de diriger ce travail malgré vos multiples occupations.
Cher maitre nous avons été touchés par votre
simplicité et votre disponibilité. Votre ouverture d'esprit et
surtout l'intérêt que vous portez à la science font de vous
une source intarissable à la quelle tout étudiant devrait
s'abreuver. Nous garderons toujours le souvenir de votre bienveillance.
Veuillez recevoir ici, cher maitre, l'expression de notre profonde
reconnaissance.
A mes consultants
Dr Mamadou Bailo DIALLO et Dr Cellou KANTE
Vous avez contribué à l'amélioration de ce
travail malgré vos multiples occupations. Sachez que votre humanisme et
vos remarquables connaissances scientifiques, font de cette thèse une
oeuvre consommable. Sachez enfin que vous êtes pour nous des
modèles pour les générations futures.
Au Directeur Général de
l'IST-Mamou
Dr Cellou KANTE, qui m'a offert l'opportunité de
m'inscrire au MACBA en sa qualité de Directeur Général
ainsi que pour sa disponibilité.
Malgré vos multiples responsabilités et votre temps
précieux, vous n'avez pas hésité à m'aider tant sur
le plan scientifique que moral.
Vous m'avez accepté et vous m'avez facilité les
démarches pour l'élaboration de ce mémoire, qui va
couronner mes études de master. Sachez que vos facilités de
contact et votre disponibilité font de vous un homme admirable, un
exemple pour vos collaborateurs. Vous êtes de ceux dont la Guinée
a besoin pour se construire. Je vous dis merci et que DIEU vous comble de
bonheur.
A Dr Mamadou Foula BARRY, M. Kaba KOUROUMA et M.
Boubacar SOW
Pour les aides intellectuelles et morales. Vous m'avez soutenu,
encouragé et épaulé tout au long de ces années de
recherche. Je vous témoigne mon affection la plus sincère.
Aux collègues de la Deuxième promotion du
groupe de formation doctorale MACBA
Mon séjour parmi vous s'est déroulé dans une
ambiance amicale et les discussions que j'ai eues avec vous ont
été très fructueuses.
Ma gratitude pour votre compréhension, votre soutien et
vos multiples sollicitudes durant ces années passées ensemble.
A mes maitres des différents cursus scolaires et
universitaires.
Chers maitres, vous avez toujours su trouver un temps pour ma
formation malgré les vicissitudes de l'histoire. Je garde de vous, le
souvenir d'hommes ouverts, disponibles, aimables. Je suis fier d'avoir
travaillé avec vous pendant ces années d'études.
A la République de Guinée
Tu m'as vu naitre et grandir, et tu as fait de moi un homme
Diplômé. Que DIEU t'accorde paix, unité et
développement.
En fin mes sincères remerciements vont à l'endroit
de tous ceux qui ont de près ou de loin contribué de façon
anonyme ou non à ma formation et à l'élaboration du
présent travail.
Abréviation et sigles
|
SEG
|
Société des Eaux de Guinée
|
|
MES
|
Matières en Suspension
|
|
OMS
|
Organisation Mondiale de la Santé
|
|
Cl-
|
Ion chlore
|
|
ONU
|
Organisation des Nations Unies
|
|
OMD
|
Objectif du Millénaire pour le Développement
|
|
CRD
|
Commune Rurale de Développement
|
|
pH
|
Potentiel d'hydrogène
|
|
°C
|
Degrés Celsius
|
|
mg/l
|
Milligramme par litre
|
|
TDS
|
Solides Totaux Dissous
|
|
uS/cm
|
Micro siemens par centimètre
|
|
UGANC
|
Université Gamal Abdel Nasser de Conakry
|
|
IST-Mamou
|
Institut Supérieur de Technologies de Mamou
|
|
MaCBA
|
Master Chimie-Biologie Appliquées
|
|
NTU
|
Nephelometric Turbidity Unit
|
|
DRASS
|
Direction Régionale des Affaires Sanitaires et Sociales
|
|
A 1
|
Puits N° 1 de Abattoir
|
|
A 2
|
Puits N° 2 de Abattoir
|
|
A 3
|
Puits N° 3 de Abattoir
|
|
L 1
|
Puits N° 1 de Loppe
|
|
L 2
|
Puits N° 2 de Loppe
|
|
L 3
|
Puits N° 3 de Loppe
|
|
K 1
|
Puits N° 1 de Kimbely
|
|
K 2
|
Puits N° 2 de Kimbely
|
|
K 3
|
Puits N° 3 de Kimbely
|
|
T 1
|
Puits N° 1 de Télico
|
|
T 2
|
Puits N° 2 de Télico
|
|
T 3
|
Puits N° 3 de Télico
|
|
P 1
|
Puits N° 1 de poudrière
|
|
P 2
|
Puits N° 2 de poudrière
|
|
P 3
|
Puits N° 3 de poudrière
|
|
CNRS
|
Centre National de Recherche Scientifique ( France)
|
Liste des tableaux
|
Tableau
|
Titres
|
Page
|
|
1
|
les principales maladies d'origine hydrique et leurs agents
pathogènes
|
7
|
|
2
|
Classification des eaux en fonction de leur turbidité
|
11
|
|
3
|
Conductivité des eaux des nappes souterraines
|
13
|
|
4
|
Influence des activités humaines et impact sur la
santé des différents niveaux de nitrates dans l'eau
|
16
|
|
5
|
Normes de l'OMS pour l'eau potable
|
24
|
|
6
|
Résultats de quelques travaux similaires effectués
en Guinée et en Afrique
|
25
|
|
7
|
Récapitulatif des paramètres d'analyses pour
quelques éléments à l'aide du spectrophotomètre DR
2800
|
45
|
|
8
|
Variation du pH des eaux de puits pour Juin et Novembre 2014
|
50
|
|
9
|
Conductivité des eaux de puits pour Juin et Novembre
2014
|
52
|
|
10
|
Matières en suspension des eaux de puits en Juin et en
Novembre 2014
|
55
|
|
11
|
Turbidité des eaux de puits en Juin et en Novembre 2014
|
57
|
|
12
|
Nitrites dans les eaux de puits en juin et en Novembre 2014
|
59
|
|
13
|
Nitrates dans les eaux de puits en Juin et en Novembre 2014
|
62
|
|
14
|
Variation des Phosphates dans les eaux de puits en juin et en
Novembre 2014
|
65
|
|
15
|
Fer total dans les eaux de puits en juin et en Novembre 2014
|
67
|
|
16
|
Coliformes Totaux dans les eaux de puits en juin et en Novembre
2014
|
70
|
|
17
|
Escherichia Coli dans les eaux de puits en juin et en Novembre
2014
|
72
|
|
18
|
Récapitulatif des résultats d'analyses des eaux de
puits de la commune urbaine de Mamou pour Juin 2014
|
75
|
|
19
|
Récapitulatif des résultats d'analyses des eaux de
puits de la commune urbaine de Mamou pour Novembre 2014
|
76
|
Liste des figures
|
Figure
|
Titre
|
Page
|
|
1
|
Cycle de l'eau
|
5
|
|
2
|
Histogramme de la Variation du pH suivant les mois de juin
et novembre 2014
|
51
|
|
3
|
Histogramme de la Variation de la conductivité suivant
les mois de juin et novembre 2014
|
54
|
|
4
|
Histogramme de la Variation des MES suivant les mois de juin
et novembre 2014
|
56
|
|
5
|
Histogramme de la Variation de la turbidité suivant
les mois de juin et novembre 2014
|
58
|
|
6
|
Histogramme de la Variation du taux de nitrites suivant les
mois de juin et novembre 2014
|
61
|
|
7
|
Histogramme de la Variation du taux de nitrates suivant les
mois de juin et novembre 2014
|
64
|
|
8
|
Histogramme de la Variation du taux de phosphates suivant les
mois de juin et novembre 2014
|
66
|
|
9
|
Histogramme de la Variation du taux de fer suivant les mois
de juin et novembre 2014
|
69
|
|
10
|
Histogramme de la Variation du taux de coliformes Totaux
suivant les mois de juin et novembre 2014
|
71
|
|
11
|
Histogramme de la Variation du taux de E. coli suivant les
mois de juin et novembre 2014
|
73
|
Résumé
Summary
Résumé
L'eau des puits est d'une importance capitale dans la
plupart des régions du monde surtout pour les pays en voie de
développement notamment l'Afrique sub-saharienne. Toutefois, cette
ressource qui était jadis de bonne qualité, se trouve
actuellement menacée par diverses sources de contamination et pourtant
elle constitue un élément incontournable pour le
développement économique.
Il convient donc de connaitre et de suivre la
qualité de cette ressource.
Ainsi dans le but d'évaluer la qualité
physico-chimique et microbiologique de ces eaux de puits, des analyses
physico-chimiques et microbiologiques ont été effectuées
sur quatre vingt dix (90) échantillons d'eau.
L'analyse descriptive des paramètres
physico-chimiques a montré que :
- 22.22% des puits étudiés en juin 2014 et
20% en novembre 2014 ont un pH ne répondant pas aux normes de
potabilité de l'OMS ;
- Les eaux de deux (2) puits sur les trois (3) de
Poudrière ont une conductivité dépassant la norme alors
que le troisième (3ème) puits a connu une augmentation
de la conductivité sur la période d'étude.
- La turbidité des eaux de puits des quartiers
Abattoir, kimbely et Loppè ont connu une forte augmentation sur la
période d'étude en dépassant les normes de l'OMS alors que
les eaux des puits de Télico et deux (2) puits de poudrière
répondent aux normes ; mais la forte augmentation de la
turbidité durant l'étude (de 1.00 à 6.00 NTU en juin et de
4.66 à 14.33 NTU en novembre) dénote un fort risque de pollution
microbiologique.
- les MES (de 3 à 13.66 mg/l), le fer (de 0.01
à 1.0mg/l) répondent aux normes de potabilité.
- Les eaux de 26.67% des puits étudiés sont
polluées par les nitrites et 53.37% des puits par les nitrates avec une
forte augmentation en novembre.
- Par contre les eaux de 40% des puits
étudiés en juin 2014 et 20% en novembre sont polluées par
les phosphates.
L'analyse microbiologique montre que presque tous les
puits étudiés sont souillés par les germes de
contaminations microbiens notamment les coliformes totaux et Escherichia
coli.
Dans l'ensemble, les eaux de ces puits ne sont pas bonnes
pour la boisson en l'état.
Summary
Well water is of paramount importance in most parts of the
world especially in developing countries, particularly in sub-Saharan Africa.
However, this resource was once good, is currently threatened by various
sources of contamination and yet it is an essential element for economic
development.
It is therefore necessary to know and monitor the quality of
this resource.
Thus, in order to evaluate the physico-chemical and
microbiological quality of well water, physico-chemical and microbiological
analyzes were performed on ninety (90) water samples.
Descriptive analysis
of the physico-chemical parameters showed that:
- 22.22% of the wells
surveyed in June 2014 and 20% in November 2014 have a pH not meeting the WHO
drinking water standards;
- The waters of two (2) wells on the three (3)
Powder have a conductivity exceeding the standard while the third (3rd) wells
has increased the conductivity of the study period.
- The turbidity of the
well water of Abattoir neighborhoods kimbely and envelope have increased
sharply over the study period exceeding the WHO standards while Telico water
wells and two (2) Powder wells meet the standards; but the sharp increase in
turbidity during the study (from 1.00 to 6.00 NTU in June and 4.66 to 14.33 NTU
November) indicates a high risk of microbiological contamination.
- TSS
(from 3 to 13.66 mg / L), iron (0.01 to 1.0mg / l) meet the standards for
potable water.
- The waters of 26.67% of the studied wells are polluted by
nitrites and 53.37% of the wells with nitrates with a strong increase in
November.
- By the waters against 40% of the wells surveyed in June 2014 and
20% in November are polluted with phosphates.
Microbiological analysis shows
that almost all studied wells are contaminated by the germs of microbial
contamination including total coliforms and Escherichia coli.
Overall, the
waters of these wells are not good for drinking but are of acceptable quality
for domestic use (laundry, kitchen, ...).
Table des matières
|
Pages
|
|
Dédicace
|
I
|
|
Remerciements
|
Ii
|
|
Abréviation et sigles
|
Iii
|
|
Liste des tableaux
|
Iv
|
|
Liste des figures
|
V
|
|
Résume
|
Vi
|
|
Summary
|
Vii
|
|
Introduction
|
1
|
|
Première partie
|
|
Chapitre I : Revue Bibliographique sur les eaux
souterraines
|
5
|
|
1- Cycle de l'eau
|
5
|
|
2- Les maladies d'origines hydriques
|
6
|
|
3- Principaux descripteurs de la qualité de
l'eau
|
9
|
|
3-1- les paramètres organoleptiques
|
9
|
|
3-2. les paramètres physiques
|
10
|
|
3-2-1.la température
|
10
|
|
3-2-2. la turbidité
|
10
|
|
3-3. les paramètres physico-chimiques
|
11
|
|
3-3-1. le pH
|
11
|
|
3-3-2. la conductivité
|
12
|
|
3-3-3. les Matières en suspension MES
|
14
|
|
3-3-4. les nitrates et nitrites
|
15
|
|
3-3-5. le fer
|
17
|
|
3-3-6. les phosphates
|
18
|
|
3-4. les paramètres microbiologiques
|
21
|
|
4- Pollution des eaux souterraines
|
26
|
|
4-1. les effets sur l'homme et l'environnement
|
26
|
|
4-2. Différentes sources de pollution des eaux
souterraines
|
28
|
|
4-3. Types de polluants
|
30
|
|
4-3-1. les polluants physiques
|
30
|
|
4-3-2. Les polluants chimiques
|
31
|
|
4-3-3. les polluants organiques
|
32
|
|
4-3-4. La pollution microbiologique
|
33
|
|
Deuxième partie
|
|
Chapitre II : Matériel et Méthode de
travail
|
|
|
II-1. Présentation de la zone d'étude
|
35
|
|
II-2. Matériel de Travail
|
40
|
|
II-2-1. Matériel de Terrain
|
40
|
|
II-2-2. Matériel de Laboratoire
|
40
|
|
II-3. Méthode de travail
|
41
|
|
II-3-1. Echantillonnage
|
41
|
|
II-3-2. Mode Opératoire
|
42
|
|
II-3-2-1. Détermination du pH
|
42
|
|
II-3-2-2. Détermination de la Turbidité
|
42
|
|
II-3-2-3. Détermination de la
conductivité
|
43
|
|
II-3-2-4. Détermination des MES
|
43
|
|
II-3-2-5. Détermination des nitrites, nitrates, fer
total et phosphates
|
44
|
|
II-3-2-6. Recherche des coliformes totaux et E. coli
|
45
|
|
Chapitre III. Résultats et Discussions
|
50
|
|
III-1. Résultats de la détermination des
paramètres physico-chimiques.
|
50
|
|
III-2. Résultats de l'analyse microbiologique
|
70
|
|
Conclusion et suggestions
|
77
|
|
Annexe
|
80
|
|
Référence et Bibliographie
|
83
|
Introduction
Introduction
De toutes les substances nécessaires à la vie,
l'eau est de loin la plus importante. Elle est indispensable par son rôle
dans les processus métaboliques et représente 70 à 75% du
poids des êtres vivants et elle couvre les trois quarts de la surface du
globe terrestre.
De nos jours, disposer d'eau potable en permanence à
domicile est un confort auquel les Guinéens et, de façon
générale les pays en voie de développement ne sont pas
habitués.
Chaque année, en effet, dans ces pays en voie de
développement, des millions de personnes sont privées de l'eau
qui leur serait nécessaire et meurent encore pour avoir consommé
de l'eau non potable
Ainsi en tant que ressource cardinale pour la vie et à
l'épanouissement de l'homme sur terre, l'eau est aujourd'hui au centre
des préoccupations des pouvoirs publics pour sa gestion durable.
Avec le développement technologique, les pouvoirs
publics se sont proposé d'assurer à la collectivité une
distribution optimale des ressources en eau moyennant une contribution
financière des consommateurs.
C'est ainsi que surgissent dans presque toutes les
localités du monde des réseaux d'adduction d'eau pour une
distribution privée ou publique de l'eau potable.
En Guinée, la distribution de l'eau potable est
assurée par la Société d'Exploitation des eaux de
Guinée (SEG), une société étatique d'exploitation
des eaux naturelles destinées à la consommation humaine.
Cependant, si pour certains Guinéens le problème
de l'accès à l'eau potable ne se pose que sommairement, pour
d'autres (les habitants de l'intérieur par exemple) en revanche, le
problème de la qualité de l'eau s'ajoute aux difficultés
d'approvisionnement en eau potable qu'on y rencontre.
La Commune urbaine de Mamou, s'alimente en eau potable
domestique pour l'essentiel grâce au réseau de distribution de la
SEG.
Après plusieurs tentatives d'amélioration de la
distribution suite à une demande sans cesse croissante résultant
de l'augmentation de la population et l'insuffisance de l'offre, les
populations font de plus en plus recours aux eaux des puits traditionnels.
Comme conséquences de ce fait, on observe ces
dernières années une recrudescence des maladies hydriques et
essentiellement le choléra et la fièvre typhoïde.
En effet d'après les statistiques du ministère
en charge de la santé à travers le bulletin hebdomadaire de la
Division Prévention et Lutte contre le cholera au 13 Aout 2013, 150
personnes ont étés touchées par l'épidémie
en 2013 en Guinée à travers 3 localités dont Mamou qui a
enregistré à elle seule 89 cas dont 4 décès.
Cet état de fait pourrait être lié
à la qualité de l'eau de consommation et à une
insalubrité.
Disposer d'eau de bonne qualité améliore
considérablement la santé humaine. Elle apporte à
l'organisme certains éléments dont il a besoin pour son
fonctionnement.
En Afrique subsaharienne, 42% de la population n'a toujours
pas accès à des sources de bonne qualité (CNRS, France
2012).
L'ONU a bien compris le danger potentiel que représente
cette boisson d'eau non potable, ce qui l'a amené à fixer comme
objectif à atteindre avant 2015 : Réduire de
moitié le pourcentage de la population qui n'a pas accès de
façon durable à un approvisionnement en eau de boisson
salubre (OMD, OBJECTIF 7, CIBLES 10).
Mais à la fin de cette décennie, l'objectif
n'était pas atteint. Les maladies hydriques font de nombreuses victimes
au sein de la population qui continue de consommer les eaux de faible
qualité.
C'est ainsi que le pari est loin d'être gagné
puisque pour atteindre cet objectif important, 260.000 personnes à
travers le monde par jour doivent encore obtenir l'accès à des
sources d'eau de bonne qualité (OMS, 2002).
Cette étude s'intéresse à la pollution de
l'eau de puits traditionnel. Elle nous permettra de dégager certaines
causes de la pollution des eaux, de faire des propositions permettant à
nos populations d'observer des attitudes garantissant la qualité de
l'eau de consommation. Nous espérons que les résultats issus de
ce travail permettront de sensibiliser les décideurs pour une meilleure
application des normes de protection des puits en vue de la réduction de
l'incidence des maladies notamment celles hydriques comme le cholera.
En effet, à Mamou, tous les ménages n'ont pas
accès à l'eau de la SEG (1300 abonnés sur une population
urbaine de près de 100 000 habitants) et ceux qui sont
abonnés n'ont pas d'eau tous les jours. Ce qui amène la plupart
des habitants à utiliser pour la plupart les eaux de puits
traditionnels. Cependant on observe un manque d'hygiène et
d'assainissement autour de ces puits. Les déchets sont mal
gérés. Les tas d'ordures se trouvent parfois à
proximité des puits. Les eaux usées sont jetées un peu
partout. Les latrines sont construites sans respecter une distance minimale de
15m requise. De même les eaux sont stockées dans des
matériels mal entretenus. Ces différentes conditions
d'hygiène et d'assainissement sont des sources probables de
contamination. L'eau peut être non seulement souillée à la
source mais également lors du stockage et de l'usage.
Le véritable problème que pose ce travail de
recherche est d'évaluer la qualité de ces eaux de puits.
Pour aborder cette étude, nous nous sommes fixés
les objectifs suivants :
Objectif général :
Etudier quelques paramètres physico-chimiques et
microbiologiques des eaux de puits de certains quartiers de la commune
urbaine de Mamou.
Objectifs spécifiques :
- Déterminer le pH, la conductivité, les MES,
les nitrites, les Nitrates, les phosphates, la Turbidité, les coliformes
Fécaux et Escherichia Coli.
- déterminer quelques éléments (les
nitrites et nitrates ; les coliformes totaux ; Escherichia Coli,)
présentant un risque pour la santé :
- évaluer les impacts de la consommation de ces eaux
sur la santé Humaine et l'environnement.
- proposer des mesures permettant l'utilisation à
moindre risque de ces eaux.
Première partie
Chapitre I : Revue Bibliographique sur les eaux
souterraines
Composée de deux (2) atomes d'hydrogènes et d'un
atome d'oxygène, l'eau est indispensable à la vie de tout
être vivant et est le seul composé présent à
l'état naturel sous trois (3) phases : liquide, solide et
gazeux.
Le caractère banal de l'eau qui nous environne fait
parfois oublier que ce liquide qui nous est si familier s'avère en
réalité le fluide le plus indispensable à la vie.
L'histoire de l'eau se confond avec celle de l'humanité
et tout développement industriel s'est construit en partenariat avec
l'eau.
L'eau est partout et constitue la base de la vie. En effet,
les premières formes de vie se sont développées dans les
océans et, encore aujourd'hui plus de la moitié des
espèces animales et végétales vivent dans l'eau. Par
ailleurs comme toutes les autres composantes de l'environnement, l'eau ne peut
pas être considérée isolement. Dans le cas d'une
rivière, d'un fleuve, d'un océan et même d'un puits, son
état dépend en grande partie des activités humaines ayant
lieu sur le territoire environnant. [1]
1. Cycle de l'eau :
L'eau sous ses différents états
suit dans la nature un vaste cycle que résume le schéma
de la Figure 1.

· Les précipitations : la
vapeur d'eau atmosphérique se condense en nuages qui engendrent des
précipitations sous forme de pluie, de neige ou de grêle. Les
précipitations, qui constituent l'origine de presque toutes nos
réserves en eau douce, sont variables d'une région à une
autre suivant le climat et le relief qui sont des facteurs essentiels.
· Le ruissellement : parvenue sur
le sol, une partie des précipitations s'écoule à sa
surface vers le réseau hydrographique et les étendues d'eu libre
(lacs, mers), c'est le ruissellement de surface.
· L'infiltration : une partie des
précipitations pénètre dans le sol et le sous-sol
où elle alimente les eaux souterraines constituant le stock d'eau du sol
et les réserves des nappes aquifères.
· L'évapotranspiration :
c'est la somme des pertes par transformation de l'eau en vapeur. On distingue
deux (2) composantes : l'une constituée par le retour direct de
l'eau dans l'atmosphère (phénomène physique) et l'autre
constituée par la transpiration des plantes. [1]
2. Les maladies d'origine hydrique.
L'eau est indissociable de la vie et en particulier de celle
des populations humaines dont elle a influencé l'histoire et conditionne
le développement. Elle est aussi un des principaux vecteurs des
maladies, par l'intermédiaire des germes infectieux, et par voie de
conséquence de la mortalité humaine. Le risque microbiologique
est ainsi le paramètre à prendre en compte en matière
d'alimentation en eau potable. Il est d'ailleurs, après l'accès
à la ressource, un des principaux facteurs d'inégalité
« nord-sud ».
Les maladies d'origine hydrique sont des infections
essentiellement dues à des bactéries, des virus et des
protozoaires. Les plus anciennes infections connues sont les fièvres
typhoïdes, les dysenteries bacillaires et le cholera (Voir Tableau
N°1). Or de nos jours dans les pays en voie de
développement ces infections sont encore d'actualités et
constituent un problème de santé publique contrairement aux pays
développés. [2]
Tableau 1 : les principales maladies d'origine
hydrique et leurs agents pathogènes d'après C. Haslay et H.
Leclerc. 1993
|
Maladies
|
Agents
|
|
Origine bactérienne
|
|
Fièvres typhoïdes et paratyphoïdes
|
Salmonella typhi, salmonella paratyphi A et B
|
|
Dysenteries bacillaires
|
Shigella
|
|
Cholera
|
Vibrio cholérae
|
|
Gastro-entérites et diarrhées
|
Escherichia coli entérotoxinogène
|
|
Campilobacter jejuni /coli
|
|
Yersinia enterocolitia
|
|
Salmonella SP
|
|
Shigella SP
|
|
Legionella pneumophila
|
|
Origine virale
|
|
Hépatite A et E
|
Virus hépatite A et E
|
|
Poliomyélite
|
Virus poliomyélitique
|
|
Gastro-entérites aigues et diarrhées
|
Virus de Norwalk
|
|
Rotavirus
|
|
Astrovirus
|
|
Calicivirus
|
|
Coronavirus
|
|
Entérovirus
|
|
Adénovirus
|
|
Réovirus
|
|
Origine parasitaire
|
|
Dysenteries amibiennes
|
Entamoeba histolytica
|
|
Gastro-entérites
|
Giardia lamblia
|
|
Cryptosporidium
|
La notion d'indicateur.
Il est actuellement difficile de rechercher
systématiquement tous les germes pathogènes susceptibles
d'être présents dans l'eau, étant donné leur
variété et l'irrégularité de leur
présence ; ainsi que la diversité et le coût des
analyses qu'il convient de mettre en oeuvre pour les détecter.
Néanmoins, comme l'origine de la plupart des
microorganismes pathogènes véhiculés par l'eau est
fécale, le principe de contrôle de la qualité de l'eau
repose sur la démonstration que l'eau distribuée ou
consommée ne contient pas de germes provenant de contaminations
fécales. Pour cela, on recherche des indicateurs de contamination
fécale, appelés aussi germes test ou germes témoins de
contamination fécale. On parle également d'indicateurs de
traitement qui permettent d'évaluer l'efficacité des
différents traitements de potabilisation mis en oeuvre vis-à-vis
des différents germes.
Ces indicateurs doivent répondre à des exigences
de nature :
Ø Epidémiologique : il
doit exister une relation entre un indicateur et l'apparition d'infection dans
une population ;
Ø Ecologique : il doit être
spécifique d'une contamination fécale :
systématiquement rencontré lorsqu'il ya présence des
fèces d'animaux à sang chaud et toujours absent dans les milieux
non pollués. Il doit être sensible pour être mis en
évidence dans l'eau lorsque des pathogènes sont présents,
et ce, en grand nombre ;
Ø Bactériologique : il ne
doit pas se multiplier dans l'eau ;
Ø Technique : il doit être
facile et rapide à détecter, et ce, à moindre coût.
[3]
3. Principaux descripteurs de la qualité des
eaux souterraines.
Les principaux descripteurs de la qualité d'une eau
sont entre autres les paramètres organoleptiques, physiques,
physico-chimiques et ceux microbiologiques.
3-1- Les paramètres organoleptiques
Ce sont les caractéristiques qui peuvent être
observées et appréciées par les organes de sens. Ce sont
la couleur, la saveur et l'odeur.
La couleur est un paramètre à la fois
organoleptique et physique, elle témoigne de la présence dans
l'eau de particules, de substances minérales ou organiques
colloïdales dissoutes, résultant de la décomposition
partielle par les microbes du sol des déchets animaux et
végétaux.
L'eau pure en petite quantité est incolore, mais les
grandes étendues reflètent la couleur bleue du ciel. Les autres
teintes témoignent de l'existence d'additions différentes :
de composés chimiques (fer, magnésium, etc.), de matières
colloïdales et d'autres matières décantable, de pollutions
techniques (industrielles) et urbaines.
L'eau potable doit être incolore. Une eau colorée
parait suspecte au consommateur qui peut craindre une contamination.
Les colloïdes et les matières en suspension sont
responsables de la coloration et de la turbidité de l'eau. La coloration
d'une eau peut être « vraie » ou
« apparente ». Elle est dite vraie lorsqu'elle est due aux
seules substances en suspension, elle est dite apparente lorsque les substances
en suspension y ajoutent leur propre coloration. [4]
La couleur de l'eau est un paramètre lié au
confort et à l'agrément du consommateur. Elle n'a pas d'influence
directe sur la santé humaine, cependant, elle limite la
pénétration des rayons UV, nécessaire à la
désinfection et une consommation importante du chlore pour l'oxydation.
[5]
Actuellement des appareils spéciaux (photo
colorimètres) sont utilisés pour la mesure de la couleur
3-2- Les paramètres physiques :
3-2-1- La Température
La température de l'eau est un facteur important dans
la production biologique. Ceci vient du fait qu'elle affecte les
propriétés physiques et chimiques de celle-ci ; en
particulier sa densité, sa viscosité et la vitesse des
réactions chimiques et biochimiques. [6]
La variation de la température de l'eau dépend
largement de son origine et de la profondeur de la source. La
température de l'eau n'a pas d'influence directe sur la santé.
Elle peut avoir des effets secondaires à travers l'efficacité du
traitement, de chloration.
L'OMS ne donne pas de valeur guide concernant la valeur de la
température. Pratiquement la température peut être
responsable d'une modification de la densité, d'une réduction de
la viscosité, d'une augmentation de la tension de valeur saturante
à la surface, d'une diminution de la solubilité des gaz.
L'augmentation de la température favorise aussi
l'autoépuration et accroit la vitesse de sédimentation. Elle peut
favoriser la mortalité de certaines espèces et le
développement d'autres.
3-2-2- La Turbidité :
La turbidité est une mesure de la
propriété optique de l'eau qui résulte de la dispersion et
de l'absorption de la lumière par les particules des matières en
suspension, présentes dans l'échantillon.
Elle permet de préciser les informations visuelles de
la couleur de l'eau. La turbidité est causée par les particules
en suspension dans l'eau (débris organiques, argiles, organismes
microscopiques...). Les désagréments causés par une
turbidité auprès des usagers est relative: certaines populations
habituées à consommer une eau très colorée
n'apprécient pas les qualités d'une eau très claire.
Cependant, une turbidité forte peut permettre à des
micro-organismes de se fixer sur les particules en suspension: la
qualité bactériologique d'une eau turbide est donc suspecte.
Pour les eaux des puits traditionnels de la commune de Matoto
(Conakry), la turbidité varie de 0,79 à 6,19 NTU.
[7]
En fonction de la turbidité, on peut classer les eaux
en eau incolore, incolore ou légèrement colorée
(Voir Tableau N° 2)
Elle se mesure sur le terrain à l'aide d'un tube
plastic transparent. Unités: 1 NTU (Nephelometric Turbidity Unit) = 1
JTU (Jackson TU) = 1 FTU (Formazin TU).
Tableau N° 2: Classification des eaux en fonction
de leur turbidité
|
NTU < 5
|
eau incolore
|
|
5 < NTU < 30
|
eau légèrement colorée
|
|
NTU > 50
|
eau colorée
|
|
NTU > 200
|
eau de surface "Africaine"
|
La turbidité de l'eau ne présente pas de risque
sur la santé chez les humains, mais lorsqu'elle est importante, elle
peut diminuer l'efficacité de désinfection et
générer des risques microbiologiques.
Les eaux turbides limitent la pénétration des
rayons lumineux nécessaires à la photosynthèse et la
pénétration des rayons UV qui jouent un rôle important en
limitant la population microbienne de certains pathogènes. [8]
3-3- Les paramètres physico-chimiques
3-3-1- pH
Le pH est un paramètre chimique caractérisant
l'acidité ou la basicité d'un milieu. Il résulte de la
composition ionique de l'eau, et essentiellement de la présence des
carbonates issus de l'échange de dioxyde de carbone à l'interface
air-eau, ainsi que de la dissolution du calcaire. [8]
Le pH dépend aussi de l'origine des eaux, de la nature
géologique du substrat et du bassin versant traversé.
Dans la plupart des eaux naturelles, le pH est compris habituellement
entre 6 et 8,5 alors que dans les eaux tièdes, celui-ci est compris
entre 5 et 9. [9]
Les eaux des puits traditionnels de la commune de Matoto
(Conakry), ont un pH compris entre 6,60 et 7,38 ; celui des eaux de puits
de la commune urbaine de coyah se situe entre 6,03 et 6,39
[10], alors que celui des puits des environs de la
décharge de Hamdanllaye ont un pH variant de 6,62 à 8,65 [11].
Le pH diminue en présence des teneurs
élevées en matière organique et augmente lorsque
l'évaporation est importante. [12]
3-3-2-La conductivité
La conductivité mesure la capacité de l'eau
à conduire le courant entre deux électrodes métalliques
(Platine) de 1 cm2 de surface et séparée l'une de
l'autre de 1 cm. Elle est l'inverse de la résistivité
électrique et a pour unité le micro siemens par centimètre
(us/cm). La conductivité donne une idée de la
minéralisation d'une eau et est à ce titre un bon marqueur de
l'origine d'une eau. En effet, la mesure de la conductivité permet
d'apprécier la quantité de sels dissous dans l'eau, donc de sa
minéralisation.
La conductivité est également fonction de la
température de l'eau, elle est plus importante lorsque la
température augmente. Les résultats doivent donc être
présentés pour une conductivité équivalente
à 20 ou 25°C. Les appareils de mesure utilisés sur le
terrain font généralement la conversion automatiquement. [13]
Les eaux souterraines ont une minéralisation et une
composition ionique variables selon la géologie des terrains en contact
avec l'eau, la minéralisation augmentant généralement avec
la profondeur. [14]
En effet, les eaux des puits traditionnels de la commune de
Matoto (Conakry) ont une conductivité comprise entre 245,95 et
253,05us/cm à 25°C alors celle des puits aux environs de la
décharge de Hamdanllaye (Conakry) est comprise entre 319,66 et 480,66
us/cm à 25°C.
En fonction de la conductivité, on peut classer les
eaux. (Voir Tableau N°3)
Tableau 3 : Conductivité des eaux des
nappes souterraines
|
Type d'eau
|
Conductivité en S/cm
|
|
Eaux très peu minéralisées (socles
granitiques, gneissiques ou schisteux)
|
< 25
|
|
Eaux peu minéralisées (grès)
|
50 à 100
|
|
Eaux du jurassique et du crétacé
|
200 à 700
|
|
Eaux minéralisées du trias
|
1000 à 1 500
|
|
Eaux accompagnant les gites pétrolières
|
>10 000
|
Comme la température, des contrastes de
conductivité mesurés sur un milieu permettent de mettre en
évidence des pollutions, des zones de mélange ou
d'infiltration....
La conductivité permet d'évaluer rapidement mais
très approximativement la minéralisation globale de l'eau et d'en
suivre l'évolution. Dans le cas du contrôle de qualité,
l'intérêt de cette mesure réside en une série de
mesures ou d'enregistrements qui permettront de déceler les variations
de composition pouvant signaler des arrivées d'eau susceptibles
d'êtres polluées.
Par exemple une enquête du ministère de la
santé réalisée en France en 1981 a montré
qu'environ 2% de la population reçoit une eau dont la
conductivité électrique est supérieure à 1000 uS/cm
et que près de 90% de la population reçoit une eau dont la
conductivité est comprise entre 200 et 1000 uS/cm.
3-3-3- Les Matières en Suspension (MES) :
La teneur et la composition minérale ou organique des
matières en suspension dans les eaux sont très variables.
Cependant des teneurs élevées en MES peuvent empêcher la
pénétration de la lumière, diminuer l'oxygène
dissous et limiter alors le développement de la vie aquatique et
créer des déséquilibres entre diverses espèces.
Elles peuvent être responsables de l'asphyxie des poissons
par colmatage des branchies.
Elles peuvent aussi interférer sur la
qualité d'une eau par des phénomènes d'adsorption
notamment de certains éléments toxiques, et de ce fait être
une voie de pénétration des substances toxiques plus ou moins
concentrées dans l'organisme. Ainsi les MES rentrent
systématiquement en compte dans un bilan de pollution.
Ces analyses des MES permettent donc de connaître la
quantité de matière non dissoutes, quelles soient organiques ou
minérales, présentes dans un échantillon.
Cette analyse peut être faite soit par la
spectrophotométrie (utilisation d'un spectrophotomètre), soit par
l'analyse gravimétrique.
Cette dernière consiste à faire passer sur une
membrane filtrante qui aura été préalablement pesée
P1, une quantité connue d'effluent à analyser.
Après passage à l'étuve à
110°C, la membrane est à nouveau pesée. La différence
entre les deux (2) poids représentera la quantité de
matières retenues sur la membrane filtrante, puis séchée
lors du séjour en étuve ; se sont les MES, elles s'expriment en
mg/l.
Sur une eau domestique, les teneurs de matières en
suspension sont normalement de 200 mg/l ; pour la nappe phréatique
du plateau de MEKNES (Maroc) cette teneur pour les puits en milieu rural varie
de 10 à 100 mg/l. [15]
3-3-4-les nitrates et nitrites
Les nitrates et les nitrites sont des ions présents de
façon naturelle dans l'environnement. Ils sont le résultat d'une
nitrification de l'ion ammonium présent dans l'eau et le sol, qui est
oxydé en nitrites par les bactéries du genre Nitrosomonas, puis
en nitrates par les bactéries du genre Nitrobacter. Les nitrates sont
très solubles dans l'eau ; ils migrent donc aisément dans la
nappe phréatique lorsque les niveaux excèdent les besoins de la
végétation. [
La toxicité des nitrates résulte de leur
réduction en nitrites et de la formation de méthémoglobine
d'une part et de leur contribution possible à la synthèse
endogène de composés N-nitrosés d'autre part.
Pour les eaux souterraines de la nappe phréatique de
la région de MEKNES (Maroc), la teneur en nitrates oscillent de 1,05
à 6,75mg/l [15], alors que celui des eaux des puits traditionnels de la
commune de Matoto (Conakry) est compris entre 0,00 et 0,0066 mg/l.
a- Sources
La présence des nitrates dans l'eau de consommation est
principalement attribuable aux activités humaines.
L'utilisation de fertilisants synthétiques et de
fumier, associée aux cultures et à l'élevage, favorise
l'apparition de nitrates dans l'eau. Les installations septiques
déficientes, de même que la décomposition de la
matière végétale et animale, peuvent aussi être une
source de nitrates dans l'eau.
Le risque de contamination est plus important si le sol
recouvrant la nappe d'eau est vulnérable (sablonneux par exemple) et si
la nappe est peu profonde (puits de surface). [16]
Tableau N° 4 : Influence des
activités humaines et impact sur la santé des différents
niveaux de nitrates dans l'eau. [12]
|
Concentration de nitrates dans l'eau potable
(mg/l)
|
C<0,2
|
0,21=C< 3,0
|
3,1=C<10
|
C>10
|
|
Influence des activités humaines
|
Non
|
Possible mais impact mineur
|
Certaine mais avec impact modéré
|
Certaine avec impact majeur
|
|
Impact sur la santé
|
Non
|
Non
|
Non démontré
|
Possible
|
b- Impact sur la santé.
La méthémoglobinémie du nourrisson est le
seul effet sur la santé qui a été associé de
façon non équivoque à une exposition excessive aux
nitrates par l'eau de consommation. Elle survient principalement chez les
enfants de moins de trois (3) mois exposés à des concentrations
de nitrates qui excèdent 20 mg-N/l.
La méthémoglobinémie résulte de la
réduction des nitrates en nitrites par les microorganismes du
système digestif, suivie de l'oxydation par les nitrites du fer ferreux
de l'hémoglobine en fer ferrique, qui engendre la
méthémoglobine. Cette dernière contrairement à
l'hémoglobine, est incapable de fixer l'oxygène, ce qui contribue
à réduire le transport de l'oxygène des poumons vers les
tissus.
Les nourrissons de moins de trois (3) mois nourris au biberon
de même que les femmes enceintes sont considérés comme
étant des sous groupes de la population particulièrement
vulnérables à la présence de nitrates et de nitrites dans
l'eau potable. [17]
Les nourrissons sont sensibles aux nitrates du fait que leur
hémoglobine est facilement oxydable et que l'activité de la
méthémoglobine- réductase est faible.
Les eaux des puits traditionnels de la commune urbaine de
coyah ont un taux de nitrites compris entre 0,024 et 0,358
mg/l ; celui des eaux de puits de la
commune de Matoto varie de 0,043 à 0,572 mg/l alors que celui de la
nappe phréatique de la région de MEKNES (Maroc) est compris entre
0,012 et 0,080 mg/l.
3-3-5 Le fer
Le fer est un élément assez abondant dans les
roches sous formes de silicates, d'oxydes et hydroxydes, de carbonates et de
sulfures. Le fer est soluble à l'état d'ion Fe++ (ion
ferreux) mais insoluble à l'état Fe+++ (ion ferrique).
Les nappes captives isolées des échanges avec la surface sont en
conditions réductrices : leur eau est ferrugineuse. Ce fer dissous
précipite en milieu oxydant, en particulier au niveau des sources et
à la sortie des conduites. La présence de fer dans l'eau peut
favoriser la prolifération de certaines souches de bactéries qui
précipitent le fer où corrodent les canalisations.
L'existence dans l'eau du fer ferrique dissous exige un pH
bas, ce qui n'est pas caractéristique pour toutes les eaux naturelles.
C'est pourquoi la majeure partie de tout ce fer ferrique se trouve à
l'état colloïdal, ou en suspension finement dispersée. En
présence de l'oxygène de l'air, le fer bivalent contenu dans les
eaux s'oxyde en fer ferrique ; une eau contenant 50mg/l de fer ferreux
 parait claire et incolore. Laissée au repos à l'air
libre, elle devient trouble et il se précipite au fond du
récipient un dépôt rougeâtre de rouille. [18] parait claire et incolore. Laissée au repos à l'air
libre, elle devient trouble et il se précipite au fond du
récipient un dépôt rougeâtre de rouille. [18]

Dans la région de MEKNES (Maroc), la teneur en fer pour
les eaux souterraines est comprise entre 0,032 et 0,280 mg/l.
Les concentrations élevées de fer
confèrent un goût désagréable et peuvent donner des
dépôts dans les tuyaux et diminuer ainsi leur section vive.
L'excès de fer peut provoquer des taches ou ternir la coloration des
vêtements. Il semble que la consommation prolongée d'une eau
contenant un excès de fer peut provoquer des maladies hépatiques
et augmenter le risque d'infarctus. C'est pourquoi les normes d'eau potable
limitent le taux de fer à 0,3 mg/l. [19]
3-3-6 Les phosphates
Les phosphates sont des composés phosphorés.
Dans la nature, le phosphore (P) est généralement présent
sous forme de molécules de phosphates. Parmi les phosphates
présents dans l'eau, on distingue couramment :
- les ortho phosphates (H2PO4-,
HPO42-, PO43-), qui sont des sels
minéraux de l'acide phosphorique (H3PO4). Cette
forme, parfois notée o-P, est également appelée lors de la
mesure des concentrations dans les eaux « phosphore réactif »
;
Ø les polyphosphates (ou phosphates condensés),
qui correspondent à des molécules plus complexes de phosphates
minéraux. On parle également de « phosphore hydrolysable
» dans l'acide ;
Ø les phosphates organiques, qui correspondent
à des molécules de phosphates associées à des
molécules à bases carbonées, comme dans la matière
organique vivante ou morte (animaux, végétaux, microorganismes,
etc.).
Dans l'eau, les phosphates inorganiques (ortho phosphates et
polyphosphates) et les phosphates organiques peuvent se retrouver sous formes
dissoutes et/ou particulaires (associés aux particules en suspension, de
sédiment, ou de sol).
Lors de la détermination des concentrations en
phosphates dans une matrice quelconque (eau, sol, aliment), suivant les cas, la
teneur en phosphates est exprimée en grammes de PO4, de
P2O5 ou de P par litre.
Ainsi : 1 g.L-1 de PO4 = 0,747
g.L-1 de P2O5 = 0,326 g.L-1 de
P.
Sources de phosphate
Contrairement à l'azote, les composés gazeux du
phosphore sont presque inexistants dans l'atmosphère. Il n'existe donc
pas de réservoir atmosphérique important de phosphore.
Le phosphore est naturellement présent dans certaines
roches (ignées ou sédimentaires). Le lessivage de celles-ci par
les processus naturels d'érosion conduit à sa solubilisation dans
les milieux aquatiques. En absence d'intervention humaine, les eaux de surfaces
contiennent cependant très peu de phosphates.
Les phosphates sont moins aisément lessivables que les
nitrates. Ils s'adsorbent aisément aux particules de sol, de
sédiment et aux particules en suspension pour former des complexes
organiques ou minéraux. Par conséquent lors de l'infiltration de
l'eau dans les sols, une fraction des phosphates initialement dissous dans
l'eau sera retenue par les particules de sol.
Une partie est généralement
entraînée et contamine les eaux superficielles et les nappes
phréatiques.
L'urine et les fèces excrétées par les
animaux et les hommes constituent également une source de phosphore. Si
cette source peut être considérée comme naturelle,
l'élevage (troupeaux, aquaculture) constitue une pollution
supplémentaire. Les agglomérations urbaines conduisent à
des concentrations ponctuelles des rejets.
Les rejets d'eaux domestiques constituent
généralement la principale source de pollution des eaux par les
phosphates. En France, les rejets de phosphore sont estimés à
environ 70 000 tonnes par an, dont 51 % d'origine urbaine. A
proximité des grands centres urbains, cette part est beaucoup plus
importante. L'usage de tripolyphosphates de sodium (TPPS) comme additifs dans
les lessives textiles et les produits pour lave-vaisselle constitue une autre
source de contamination des eaux par les phosphates. Cette source de pollution
a été réglementée dans divers pays (Etats-Unis,
Japon, certains pays Européens) et est en cours de diminution effective.
Dans les pays où la production agricole intensive est
particulièrement développée, l'utilisation d'engrais
phosphatés peut constituer la principale source artificielle
d'enrichissement des eaux en phosphore. La fertilisation des terres agricoles
est à la source d'une pollution diffuse des eaux. En 1997, la
Société Française de Chimie estimait la consommation
mondiale de fertilisants phosphatés à 32 000 000 tonnes par an.
En 1999, les consommations Française et Européenne étaient
respectivement de 966 000 et 3 467 000 tonnes par an (UE, 2002). Le phosphore
utilisé comme engrais est principalement dispersé sous forme de
superphosphates (ortho phosphates solubles), et est donc fortement bio
disponible.
Les autres usages industriels du phosphore (chimie de
synthèse, photographie, lithographie, etc.) constituent des sources
ponctuelles moins importantes de contamination des eaux.
Il est enfin important de noter que le phosphore
utilisé comme fertilisant est épandu sur les sols et est par
conséquent susceptible d'être en partie assimilé par les
végétaux ou fixé sur les particules de sol.
Effets connus sur l'environnement
Comme l'azote, le phosphore est un constituant essentiel de la
matière organique et est un nutriment indispensable pour les organismes
vivants. Cependant il doit être considéré comme un polluant
lorsqu'il est présent à de fortes concentrations dans
l'environnement. Les rejets de phosphore dans les écosystèmes
aquatiques constituent l'un des plus sérieux problèmes
environnementaux car ils contribuent à accélérer
l'eutrophisation de ces milieux. Dans les eaux douces, ce sont cependant les
apports de phosphore qui sont généralement à l'origine
d'un disfonctionnement des écosystèmes. Dans les eaux naturelles,
le ratio entre les quantités d'N et de P disponibles est
généralement supérieur à 16. Par conséquent,
même en cas de pollution du milieu par l'azote, si aucun apport de P
n'est réalisé, les algues ne pourront pas se développer.
La pollution des eaux par le phosphore est donc très souvent à
l'origine de développements algaux importants et conduit à la
dystrophisation (eutrophisation accélérée) des lacs et
rivières.
Effets connus sur la santé humaine
Si les composés phosphorés utilisés
à hautes concentrations dans l'industrie (phosphore blanc qui est par
exemple un constituant de la mort-aux-rats, P rouge, P noir, etc.) peuvent
avoir des effets très toxiques sur l'homme, les concentrations
normalement observées dans l'eau ou dans l'habitat semblent ne pas
présenter de risque direct pour la santé humaine. C'est surtout
par l'intermédiaire des nombreuses perturbations des
écosystèmes aquatiques qui sont imputables aux pollutions par les
phosphates que cet élément a des répercussions sur
l'être humain.
3-4- Les paramètres microbiologiques
L'eau destinée à la consommation humaine peut
contenir des microorganismes pathogènes, agents d'infections humaines
redoutables. Ce sont des bactéries, des virus, voire des champignons,
des protozoaires, des algues. Cette eau doit être potable,
c'est-à-dire incapable de nuire à la santé des
consommateurs, donc exempte de ces agents pathogènes.
La grande majorité de ces microorganismes nocifs
diffuse dans l'environnement aquatique, par l'intermédiaire des
souillures fécales humaines ou animales. La mise en évidence de
ces contaminations fécales est à la base même de l'analyse
bactériologique de l'eau de consommation.
Elle consiste à rechercher et à dénombrer
certaines espèces, ou certains groupe de bactéries les plus
représentatives d'une telle contamination et dont la présence ne
constitue pas un risque pour la santé ; on les appelle
indicateurs de contaminations fécale.
Ainsi E. coli est un indicateur de contamination
fécale ; sa présence laisse planer un risque ; celui de
la présence de bactéries ou de virus pathogènes d'origine
fécale (Salmonella, Shigella, Enterovirus, etc....). Certains
microorganismes comme les Bacillus, les Candida ont été
proposés comme indicateurs de traitement. Les tests auxquels sont
habituellement soumises les eaux de consommation sont :
a- Le dénombrement des bactéries
b- La recherche et le dénombrement des coliformes
c- La recherche et le dénombrement des streptocoques
fécaux
d- La recherche et le dénombrement des spores de
clostridium.
· Dénombrement des
bactéries.
Le dénombrement des bactéries se fait par
comptage de colonies, après inoculation d'une quantité
définie de l'échantillon, dans un milieu de culture
gélosé ou à la surface de ce milieu. Parmi les
bactéries cultivant sur gélose dans les conditions
décrites, on a coutume de distinguer deux (2) catégories
fondamentales sur le plan de l'hygiène : les germes saprophytes,
qui se développent à 20°C et les germes dits
« pathogènes », qui se multiplient à
37°C. cette distinction provient du fait qu'à 20°C on favorise
le développement des germes spécifiques de l'eau et qu'à
37°C on sélectionne les microorganismes provenant de l'homme et
des animaux à sang chaud, de leurs sécrétions, de leurs
flores naturelles et en particulier des matières fécales.[20]
· Dénombrement des coliformes.
Actuellement on peut distinguer deux (2) catégories
de coliformes, d'origine et d'habitat différents. La
première est celle des coliformes d'origine fécale qui comprend
les espèces genres Citrobacter ; Levinea, .... Rencontrées
habituellement dans les matières fécales humaines et
animales ; les eaux usées et les eaux polluées (de surface
et souterraine). La seconde correspond à des espèces nouvelles
comme Serratia fonticola, Bautiauxella agrestis qui, au contraire proviennent
uniquement des eaux d'alimentation (potables) et de sols incultes. Elles sont
très fréquentes dans les eaux de distribution et sont le plus
souvent confondues avec les espèces indicatrices d'une pollution. [5]
Les coliformes fécaux, ou coliformes thermo
tolérants, sont un sous-groupe des coliformes totaux capables de
fermenter le lactose à une température de 44,5°C.
L'espèce la plus fréquemment associée à ce groupe
bactérien est l'Escherichia coli (E. coli) et, dans une moindre mesure,
certaines espèces des genres Citrobacter, Enterobacter et
Klebsiella.
La bactérie E. coli représente
toutefois 80 à 90 % des coliformes thermo tolérants
détectés. [20]
L'intérêt de la détection de ces
coliformes, à titre d'organismes indicateurs, réside dans le fait
que leur survie dans l'environnement est généralement
équivalente à celle des bactéries pathogènes et que
leur densité est généralement proportionnelle au
degré de pollution produite par les matières fécales.
Par ailleurs, puisque les coliformes fécaux ne
prolifèrent habituellement pas dans un réseau de distribution,
ils sont utiles pour vérifier son étanchéité,
permettant de détecter une contamination fécale découlant
par exemple d'infiltrations d'eau polluée dans les canalisations. Ils
sont aussi de bons indicateurs de l'efficacité du traitement de l'eau,
mais comme leur nombre est moins élevé que celui des coliformes
totaux, ces derniers leur sont préférables pour cette
fonction. [21]
· Dénombrement des streptocoques
fécaux.
La classification générale des streptocoques
fécaux a été modifiée dans les années 80 par
la création d'un nouveau genre, Enterococcus. Dans ce contexte,
plusieurs espèces appartenant antérieurement au genre
Streptococcus ont été transférées vers le
genre Enterococcus, ce dernier correspondant, grosso modo, aux
streptocoques du groupe sérologique D de la classification de
Lancefield. [21]
Les streptocoques du groupe D susceptibles de contaminer les
eaux d'approvisionnement, ils sont plutôt typiques des déjections
animales, comme Streptococcus bovis, S. equinus, S.
gallolyticus et S. alactolyticus. Ces espèces colonisent le
bétail, les chevaux et la volaille bien qu'elles peuvent parfois
être présentes chez l'humain, en particulier S. bovis
et elles n'ont pas été transférées dans le
genre Enterococcus. Cette nomenclature, basée sur des modifications
à la classification bactérienne, peuvent engendrer une certaine
confusion d'autant plus que certains documents récents utilisent
toujours le terme Streptococcus pour décrire des espèces du
genre Enterococcus; c'est le cas du Standard Methods for the Examination
of Water and Wastewater.
Des études menées aux États-Unis ont
démontré leur utilité pour mettre en évidence une
contamination fécale de l'eau souterraine.
Cet intérêt
à l'égard des entérocoques s'expliquerait par le fait que,
comparativement aux coliformes (incluant Escherichia coli), ils sont plus
résistants à des conditions environnementales difficiles et
persistent plus longtemps dans l'eau; de telles conditions sont typiques des
eaux souterraines où la température est
généralement plus froide et qui sont pauvres en
éléments nutritifs. [22]
Tableau N°5 : NORMES DE L'OMS POUR L'EAU
DE BOISSON
|
N°
|
Paramètres
|
Concentration minimale en mg/l
|
|
Analyses physico-chimiques
|
|
1
|
pH
|
6.5-8.5
|
|
2
|
Turbidité
|
<5 NTU
|
|
3
|
Chlorures
|
200
|
|
4
|
Sulfates
|
200
|
|
5
|
Nitrites
|
=0.1
|
|
6
|
Nitrates
|
=50
|
|
7
|
Magnésium
|
50
|
|
8
|
Calcium
|
75
|
|
9
|
Sodium
|
500
|
|
10
|
Fer
|
=0.3
|
|
11
|
Fluor
|
1
|
|
12
|
Phosphates
|
=0.05
|
|
13
|
Conductivité
|
<400 uS/cm à 20°C
|
|
Analyses microbiologiques
|
|
14
|
Coliformes Totaux
|
0/100ml
|
|
15
|
Coliformes fécaux
|
0/100 ml
|
|
16
|
Streptocoques fécaux
|
0/100ml
|
|
17
|
E. coli
|
0/100ml
|
4. Les acquis (Travaux antérieurs)
Certains résultats de travaux antérieurs portant
sur les eaux de puits en Guinée et en Afrique sont consignés dans
les tableaux ci-dessous.
Tableau N° 6 : résultats de quelques
travaux similaires effectués en Guinée et en Afrique.
|
Lieu
|
|
 NTU NTU
|
 us/cm us/cm
|
 mg/L mg/L
|
 mg/L mg/L
|
 mg/L mg/L
|
 mg/L mg/L
|
|
|
référence
|
|
Eaux de puits de Ratoma
|
5.43
|
2.10
|
400
|
0.018
|
70.37
|
-
|
-
|
-
|
-
|
N'famara camara juin 12
|
|
Eaux de puits de Matoto
|
7.17
|
2.25
|
245.22
|
0.168
|
0.0025
|
-
|
-
|
-
|
-
|
Maimouna Diallo juin 12
|
|
Eaux de puits de Coyah
|
6.98
|
1.39
|
272.63
|
0.157
|
0.0025
|
-
|
-
|
-
|
-
|
Salma Balde 04/12
|
|
Eaux de puits de Mali-Labe Tougué
|
7.25
|
4.94
|
318.25
|
-
|
-
|
-
|
0.23
|
-
|
-
|
Aminata Sylla juin 12
|
|
Eaux de puits de Daar-Salam 2
|
5.71
|
-
|
-
|
0.277
|
-
|
-
|
-
|
-
|
-
|
Aissata Magassouba et al 06/12
|
|
Eaux de puits Décharge hamdallaye
|
7.11
|
-
|
283.66
|
0.062
|
-
|
-
|
-
|
-
|
-
|
Aminata Traoré et al. 06/12
|
|
Eaux de puits de Pobè (Bénin)
|
5.83
|
-
|
236.62
|
0.072
|
45.3
|
0.75
|
-
|
-
|
-
|
Moissou LAGNIKA et al 31/07/14
|
|
Eaux de puits du plateau de MEKNES (Maroc)
|
6.70
|
|
|
5
|
28
|
|
1.5
|
|
|
BELGHITI. L et al 10/13
|
5. Pollution des eaux souterraines.
La pollution de l'eau est la modification des
propriétés physiques, chimiques et biologiques susceptible de
provoquer un effet sur la santé des êtres vivants.
Les eaux souterraines ont pendant longtemps été
synonymes « d'eau propre », c'est-à-dire
répondant naturellement aux normes de potabilité. Cela est
malheureusement inexact dans l'absolu, car bon nombre d'eaux des nappes sont
à présent contaminées par des éléments
indésirables, voire toxiques à des concentrations
dépassant largement les normes, et doivent par la suite être
traitées avant consommation. [23]
Les eaux souterraines sont encore plus fragiles que les eaux
superficielles : situées dans un milieu plus confiné, les
nappes se renouvellent beaucoup moins vite que les eaux superficielles (en
particulier les nappes profondes).Leur dégradation est donc
quasi-irréversible
L'eau d'un puits peut être contaminée par des
bactéries et des substances chimiques. Les sources de contamination les
plus fréquentes sont : l'infiltration des effluents provenant d'une
installation septique, de leurs proximités à l'eau de mer, de
fumier, de produits de voiries ainsi que des substances chimiques dissoutes
présentes naturellement dans la nappe phréatique telle que les
nitrites, le calcium, le soufre et les nitrates ou le fer. [24]
5.1. Les effets sur l'homme et l'environnement.
· Matières en suspension :
Les matières en suspension provoquent une augmentation de
la turbidité préjudiciable à la photosynthèse,
à la respiration des poissons et colmatant les milieux aquatiques. Les
particules peuvent transporter différentes formes de pollution
(organiques, métalliques,...)
· Pollution organique : La pollution
organique provoque l'asphyxie du milieu par consommation de l'oxygène
dissous et augmente la toxicité de la charge organique faiblement
biodégradable.
· Azote, Phosphore :
La présence de ces éléments dans l'eau
entraine l'eutrophisation des milieux aquatiques par excès de
matières nutritives pour les végétaux (algues) et
conduisant à l'asphyxie des milieux. Toxicité de l'ammoniaque et
des nitrites pour la faune aquatique.
Les nitrates peuvent engendrer chez
les nourrissons un empoisonnement du sang par blocage de l'hémoglobine
interdisant le transport de l'oxygène.
· Métaux :
La
majorité des éléments métalliques est indispensable
à la vie animale et végétale
(oligo-éléments).Cependant, à des doses importantes, ils
peuvent se révéler très nocifs. La pollution
métallique des milieux aquatiques pose un problème particulier
car non biodégradable. Elle a tendance à se concentrer dans les
organismes vivants (bioaccumulation ou bioamplification).
Les effets
toxicologiques varient suivant le métal et sa forme chimique : les
composés organiques sont généralement plus toxiques. De
façon générale, les troubles les plus fréquents
sont d'ordre respiratoire, digestif, nerveux ou cutané. Certains
métaux sont également considérés comme
cancérigènes : Arsenic, Nickel, Chrome VI.
· Substances très dangereuses pour les
milieux aquatiques :
Les insecticides sont
généralement les pesticides les plus toxiques. Ce sont des
polluants organiques persistants subissant trois types de
phénomènes (transformation, rétention, transport) selon
leurs propriétés physico-chimiques.
Ils s'adsorbent sur les
matières en suspension et s'accumulent dans certains compartiments
(sédiments, matières organiques, chaîne alimentaire) Selon
leurs formes et propriétés chimiques, ces substances
présentent des effets toxiques, mutagènes et
cancérogènes. [24]
5-2 Différentes sources de pollution des eaux
souterraines.
Les différentes sources de pollution des eaux
souterraines peuvent être d'origine:
a- Naturel: Les eaux souterraines contiennent
quelques impuretés, même si elles ne sont pas affectées par
les activités humaines. Les types et les concentrations
d'impuretés naturelles dépendent de la nature du matériel
géologique par lequel les eaux souterraines se déplacent, et de
la qualité de l'eau de recharge. Les eaux souterraines se
déplaçant à travers les roches et les sols
sédimentaires, peuvent absorber un éventail de composés
tels que le magnésium, le calcium, et les chlorures. Certaines couches
aquifères ont des concentrations naturelles élevées en
constituants dissous tels que l'arsenic, le bore, et le sélénium.
L'effet de ces sources normales de contamination sur la qualité d'eaux
souterraines dépend du type du contaminant et de ses concentrations.
b- Agricole: Les pesticides, les engrais, les
herbicides et les déchets animaliers sont des sources agricoles de
contamination des eaux souterraines. Les sources agricoles de contamination
sont nombreuses et variées: débordement des engrais et des
pesticides pendant la manipulation, écoulement du chargement et lavage
des pulvérisateurs de pesticide ou de tout autre équipement
d'application, utilisation de produit chimique...
c- Industriel: La pollution des eaux
souterraines se produit quand l'eau utilisée dans l'industrie est
retournée au cycle hydrologique.
L'activité économique
moderne exige le transport et le stockage de la matière employée
dans la fabrication, le traitement, et la construction. Certaines entreprises,
habituellement sans accès aux réseaux d'égouts, se servent
dans les eaux souterraines peu profondes. Elles emploient des fosses ou des
puisards secs, ou envoient l'eau usagée dans les réservoirs
septiques. Tout ceci peut mener à la contamination des sources
souterraines d'eau potable. Les fosses et les puisards secs provoquent
l'infiltration des déchets directement dans le sol. Les autres sources
industrielles de contamination incluent: le nettoyage des réservoirs ou
la pulvérisation d'équipement sur la terre, l'évacuation
de déchets dans les systèmes septiques ou les puits secs, et le
stockage de matériaux dangereux dans des secteurs découverts ou
dans les secteurs qui n'ont pas des garnitures avec des drains ou des bassins
de captation.
d- Résidentiel: Les systèmes
résidentiels d'eau usagée peuvent être une source de
différents types de contaminants, y compris des bactéries, des
virus, des nitrates, et des composés organiques. Les puits
utilisés pour l'évacuation des eaux domestiques usagées
(les systèmes septiques, puisards, puits de drainage pour
l'écoulement de précipitations exceptionnelles, puits de recharge
d'eaux souterraines) sont particulièrement concernés par la
qualité des eaux souterraines s'ils sont placés près des
puits d'eau potable. Le stockage incorrect ou l'évacuation de produits
chimiques ménagers tels que les peintures, les détergents
synthétiques, les dissolvants, les huiles, les médicaments, les
désinfectants, les produits chimiques de piscine, les pesticides, les
batteries, l'essence et le carburant diesel peut mener à la
contamination des eaux souterraines. De même, les déchets
vidés ou enterrés dans la terre peuvent souiller les sols et
s'écouler dans les eaux souterraines. [24]
5-3 Principaux types de polluants.
Un polluant est un agent physique, une substance
minérale ou biologique, issus de l'activité humaine provoquant,
sous une intensité ou une concentration anormales, une
dégradation de la qualité de l'eau naturelle.
Le nombre de polluant est considérable. En 1977 une
société Américaine de chimie a dénombré plus
de 4 millions de substances chimiques polluant dont 70 000 suspects
d'actions cancérigène.
Les polluants peuvent êtres classés, selon leur
nature, en quatre (4) grandes catégories : physiques, chimiques,
organiques et bactériologiques. Il est nécessaire, en premier
lieu, d'en dresser un catalogue fixant la nature, leur dose néfaste et
leur toxicité.
5-3-1 les polluants physiques :
Les trois principaux agents physiques de la pollution
sont : la chaleur, le transport des matières solides en suspension
et la radioactivité.
La chaleur, par élévation de température
de l'eau, surtout de surface, provoque des effets écologiques sur la vie
aquatique (développement de micro-organismes comme les algues).
Elle diminue la solubilité de l'oxygène,
déficit renforcé par l'accroissement de l'activité
biologique qui en consomme.
Les matières solides en suspension sont introduites par
les précipitations et les eaux de surface. Certaines particules,
très petites de l'ordre de micron, peuvent ainsi être
traitées.
La radioactivité est potentiellement la plus dangereuse
des polluants physiques. C'est pourquoi tous les rejets sont
sévèrement réglementés et contrôlés.
[24]
5-3-2 les polluants chimiques.
L'eau, par son pouvoir dissolvant élevé,
dissout les substances rejetées par l'activité humaine.
Les polluants chimiques sont nombreux et d'origines
diverses :
Ø Les sels minéraux dissous
Ø Métaux lourds, pesticides et détergents
constituent les micros polluants
· Sels minéraux dissous.
Les plus nocifs sont les composés de l'azote :
nitrates (NO3-) et nitrites (NO2-).
Ils provoquent des troubles graves des jeunes vertébrés par
dégradation de l'hémoglobine du sang et production de
méthémoglobine toxique (méthémoglobinémie
des nourrissons). Ils peuvent provoquer l'hypertension et sont
précurseurs de nitrosamines cancérigènes. Non
présents dans les formations géologiques ou très rares,
les nitrates sont essentiellement d'origine agricole, toutefois leur
présence dans l'eau montre que cette pollution n'est toujours pas
liée à des causes récentes. [24]
· Métaux lourds.
Les pollutions engendrées par la présence de
métaux dans les eaux souterraines sont dues généralement
aux activités industrielles par rejets d'effluents et par lessivage de
produits stockés sur un sol.
Certains de ces métaux peuvent
être toxiques (cadmium, chrome, mercure, plomb...), D'autres
éléments sont considérés comme indésirables
et peuvent présenter des inconvénients au consommateur d'ordre
organoleptique : goût, saveur, coloration. C'est le cas pour le cuivre,
le zinc, le fer, le manganèse, l'aluminium.
5-2-3 Les polluants organiques :
L'eau est le vecteur des microorganismes, pathogènes ou
non. Le pouvoir auto épurateur du sol est très efficace.
Pratiquement l'eau en est dépourvue dans les conditions naturelles. On
peut citer par exemple :
· Les détergents
Ce sont des substances utilisées pour les diverses
opérations de nettoyage. Un détergent est un produit complexe
contenant un ou plusieurs agents de surface et des composés
minéraux (carbonates, phosphates, polyphosphates, perborates), souvent
associés à des matières organiques améliorantes
(carboxyméthyl-cellulose, alkanolamides), à des enzymes
hydrolysants et à des séquestrant (dérives de l'acide
éthylène diamine tétracétique et de l'acide
mitriloacétique). La biodégradabilité de ces substances
est très variable. Les détergents sont rares dans les eaux
souterraines, sauf dans les zones suburbaines, en liaison avec les puisards
recevant les eaux usées et dans certaines nappes alluviales en relation
étroite avec un cours d'eau pollué. Ces détergents sont
peu toxiques mais ils facilitent par leur pouvoir mouillant la dispersion et le
transfert d'autres polluants comme les pesticides. [24]
· Les pesticides
Les produits phytosanitaires sont apportés dans
l'environnement par les grandes cultures, par le maraîchage agricole, par
le traitement des forêts, par le traitement sur plans d'eau, par les
traitements en zone urbaine (espaces verts, jardins, trottoirs, rues), par
certains rejets industriels de conditionnement ou de fabrication, par le
traitement des routes et des voies de chemin de fer. Ils comprennent:
· des substances minérales (soufre, sulfate de
cuivre, arséniates de plomb et de calcium) ;
· des composés organo-chlorés agissant comme
insecticides (lindane, aldrine, dieldrine, heptachlore...) ou herbicides
(dérivés chlorés de phénoxyacides)
· des composés organophosphorés
utilisés comme insecticides (parathion, malathion...) ;
· d'autres composés organiques ou
organométalliques à groupements fonctionnels variés
(dérivés de l'urée, triazines, carbamates...)
employées comme herbicides, insecticides ou fongicides.
Une étude sur la teneur en pesticides e été
effectuée par la DDASS entre 1992 et le 1996 sur 911 captages d'eau
souterraine de Picardie: 27 % contenaient des traces de triazines.
[24]
5-2-4 La pollution microbiologique.
De nombreux microorganismes, virus, bactéries et
protozoaires, voire des champignons et des algues sont présents dans
l'eau. Les conditions anaérobies généralement
rencontrées dans les eaux souterraines en limitent cependant la
diversité. Les bactéries, virus et autres agents
pathogènes rencontrés dans les eaux souterraines proviennent de
fosses septiques, des décharges, des épandages d'eaux
usées, de l'élevage, de matières fermentées, de
cimetières, du rejet d'eaux superficielles. Ces pollutions peuvent
être aussi dues à des fuites de canalisations et d'égouts
ou à l'infiltration d'eaux superficielles.
La grande majorité de ces microorganismes nocifs,
susceptibles d'engendrer des infections humaines redoutables, diffuse dans
l'environnement hydrique par l'intermédiaire de souillures
fécales humaines ou animales. Les pollutions microbiologiques se
rencontrent surtout dans les aquifères à
perméabilité de fissure (craie, massifs calcaires), dans lesquels
la fonction épuratrice du sous-sol ne peut s'exercer et dans lesquels la
matière organique est dégradée partiellement. Les
émergences de type karstique avec des circulations souterraines rapides
sont par conséquence très vulnérables à cette
pollution. Dans les aquifères à porosité inter granulaire,
une contamination bactérienne implique une source proche de pollution
(puisard, défaut d'étanchéité du captage, rejet de
station d'épuration, décharges,...).
D'après une
étude réalisée par la D.R.A.S.S. à partir des
données des années 1994, 1995 et 1996, la situation en Picardie
(France) n'apparaît pas totalement satisfaisante. Près de 95% de
la population a reçu une eau de qualité microbiologique
acceptable et aucune eau de mauvaise qualité n'a été
distribuée. Mais pour plus de 5,5% de la population régionale,
répartis dans 169 unités de distribution, l'eau a subi des
contaminations passagères plus ou moins fréquentes.
[24]
Deuxième partie
Chapitre II : Matériel et méthode de
travail
II-1 Présentation de la zone d'étude
Selon le découpage administratif, la préfecture
de Mamou est la capitale de la Région Administrative dont elle compte au
total 13 sous préfectures plus (+) la commune urbaine que sont :
(Timbo, Porédaka, Dounet, Boulliwel, Tolo, Konkouré,
Saramoussaya, Gongoré, Soyah, Ourékaba, Niagara, Kégneko,
Téguéréya.).
Elle couvre une superficie de 8 000 km2et est
limitée au Sud par la SIERRA LEONE ; au Nord par les
préfectures de Tougué et de Dalaba ; à l'Est par les
préfectures de Faranah et Dabola et à l'Ouest par celle de
Kindia. Voir carte en annexe
Son unité géomorphologique est
caractérisée par des hauts plateaux du Foutah Djallon dont les
sols demeurent : des « bowés » (sols
latéritiques), sols peu différenciés sur cuirasse
ferrugineuse, ferralitiques non différenciés dont la couleur
dominante reste jaune beige.
Les peuls, les dialonkés, et une minorité des
malinkés, soussou, de kissiens et de Toma sont les principales ethnies
de la préfecture.
Les activités économiques les plus
pratiquées sont : l'artisanat, la production des fruits et
légumes, l'élevage extensif et une partie de la production
agricole dont : le fonio, le taro, la patate douce, l'arachide, le mais,
le manioc et peu de riz.
Aussi, c'est une région à position
géographique privilégiée, de carrefour entre les
différentes régions du pays et entre les pays frontaliers du nord
et du sud. [25]
II-1-2 LA COMMUNE URBAINE DE MAMOU :
II-1-2-a CADRE GEOGRAPHIQUE
Dans la deuxième moitié du 19ème
siècle le sud du Foutah Djallon, la sous-province de Telico était
devenue une très importante étape des caravanes en
direction et en provenance des côtes. Le flux des hommes et des
produits qu'entraînèrent ces voies donnèrent
à la paroisse de Telico les dimensions d'un important marché
régionale. En 1908 le chemin de fer Conakry-Niger traversa la sous
province de Telico ; et à 4km de la province, il fut crée
une gare qui donna naissance à la ville de Mamou.
En1917 la capitale du foutah théocratique fut
transférée à Mamou sous le nom de cercle de
Mamou.
Du 02 octobre 1958 au 03 avril 1984, Mamou centre
fut érigé en arrondissement puis en sous-préfecture de
1984 à 1991.
En 1991, la sous-préfecture centrale
de Mamou devient une commune urbaine et elle est située à 266 km
de Conakry.
Elle est limitée au Nord par la Commune Rurale de
Développement (CRD) de Boulliwel et de Tolo, au Nord Est par celle de
Dounet, au Sud est par celle de Soyah, à l'Ouest par celle de
Konkouré et est située en plein coeur de la guinée sur la
Nationale/Internationale Conakry - Kindia - Kankan - Faranah et Labé,
d'où son nom ville carrefour le plus caractéristique du
résumé physionomique de l'ensemble des ethnies de la
Guinée. Elle compte vingt huit (28) quartiers.
Les températures les plus élevées
étant observées en mars - avril 37 et 38°c, alors que les
plus basses se notent en décembre 11°c.
Les vents dominants sont l'harmattan et la mousson. Il existe
des forêts classées à Tyéwel, Sèrè,
Koumi, Diarabaka et Tambassa. [25]
II-1-2-b Principales activités
économiques
Longtemps considéré comme ville carrefour, Mamou
reste incontestablement le centre d'échange le plus accessible de la
Guinée. Le chef-lieu est entrain de devenir une véritable plaque
tournante des échanges entre l'est du pays et le nord de la Basse
Guinée. On note, par exemple, que la très grande partie des
activités commerciales de cette préfecture se déroule dans
l'informel. Malgré cet état de fait, l'agriculture reste de loin
la branche d'activité la plus importante de la préfecture de
Mamou. Elle couvre près de 87% de la population. Encore pratiquée
de manière extensive sur brûlis, l'agriculture est surtout
orientée vers les cultures vivrières. On note cependant une
certaine spécialisation pour les différentes
sous-préfectures, par exemple Timbo et Porédaka qui
détiennent 25% des superficies en fonio, 30% du maïs, 37% en
manioc, 36% en arachide et 33% en patate douce. Les sous-préfectures de
Dounet, Timbo Konkouré et la commune urbaine fournissent l'essentiel de
la production maraîchère (tomate, piment etc.).
L'artisanat constitue la deuxième activité
économique de cette préfecture. Il comprend la fabrication des
objets usuels et d'ornement: cotonnades, outils, canaris, sandales et bijoux.
Le travail artisanal est organisé essentiellement sur la base de la
division traditionnelle de la société. Certaines familles sont
spécialisées dans les activités artisanales
données, c'est ainsi qu'on distingue de familles de forgerons, de
tisserands, de potiers et de cordonniers. Ce secteur est très
répandu dans la vie quotidienne comme activité, une vingtaine de
métiers y sont exercés. Pour les métiers féminins,
c'est exclusivement la teinture, la saponification et la broderie; les
métiers typiquement masculins sont la cordonnerie, le tissage, la forge
et la menuiserie. [25]
II-1-2-C. Hydrographie
Trois cours d'eau sont les plus importants : les fleuves
Bafing, Kaba et Konkouré avec de nombreux affluents, qui pour la plupart
tarissent en saison sèche.
Il existe trois hauts bassins qui sont le
Bafing, la Kaba et le Konkouré.
- Le bassin de Bafing est situé au nord de la ville de
Mamou, ou le Bafing prend sa source ; ce même fleuve est
dénommé fleuve Sénégal en dehors de la
Guinée. Il draine ses eaux du sud vers le nord traversant ainsi le Fouta
Djallon, région montagneuse.
- Le bassin de la Kaba, situé dans la partie sud-est de
la préfecture, draine ses eaux en Sierra Leone où il est
appelé « Little Castle ». Il a pour affluent
principal le Mamouwol qui prend sa source à l'ouest de la ville de
Mamou.
- Le bassin de Konkouré est situé au sud-ouest
de la ville de Mamou et draine ses eaux dans la préfecture de Kindia.
II-1-2-d Sites touristiques
Grâce non seulement à son potentiel naturel
caractérisé par un relief accidenté et dominé par
des chaînes montagneuses du Fouta Djallon, avec des pics du Mont Loura
(1558 m) au nord et le Mont Diaguissa (1425 m) au sud, mais aussi son
histoire riche et mouvementée, la préfecture de Mamou
possède de sites intéressants notamment les suivants:
· Timbo: Cette CRD située
à 55 km de Mamou sur la route Mamou-Dabola est l'ancienne capitale
du Fouta théocratique. D'importants sites touristiques marquent
l'histoire du Fouta Djallon dont surtout la première mosquée de
Timbo, construite en 1625; Talansan, village situé à 5 km de
Timbo, où a eu lieu la première bataille de Karamoko Alpha, 1er
Almamy du Fouta Djallon; le mausolée de Karamoko Alpha; Tata de Timbo,
la plus vieille clôture du Fouta Djallon, construite en 1790 par le
père d'Almamy Bocar Biro; la plaine de Petel Djaga,
célèbre champ de bataille entre Almamy Bocar Biro, roi de Timbo,
et les troupes françaises; Gnagara, où se trouve la tombe de
l'Almamy Bocar Biro. Le mausolée de Bocar Biro est à
Fétoré, celui de Karamoko Alpha à Timbo. Au village de
Timbo se trouvent aussi les neuf stèles de pierre représentant
les neuf (9) diwés du Fouta théocratique.
· Ourékaba: Dans cette CRD,
située à 65 km de Mamou sur la nationale Mamou-Faranah et
à 15 km de Ouré-kaba Centre, se trouve un parc naturel
où l'on peut rencontrer des différentes sortes d'animaux
sauvages, par exemple des lions, panthères, hyènes, girafes et
antilopes. A 25 km de cette CRD, dans le district de Yomaya et à
3 km de la frontière Guinée-Sierra Léone, se trouve
une grotte naturelle lieu de refuge des guerriers en temps colonial. Cette
grotte peut abriter 2000 personnes. Elle est actuellement
fréquentée pour des prières de bénédictions,
surtout des femmes en recherche d'enfants ou d'époux.
· Le Bafing: Situé dans la CRD de
Tolo, à 25 km de Mamou sur la nationale Mamou-Dalaba, ce site
fluvial comprend un barrage hydro-agricole aménagé. Il est
régulièrement fréquenté par les populations pour
les jeux de natation et d'autres loisirs divers. La source du fleuve
Sénégal, à 2 km du Bafing, et les réserves
forestières adjointes sont aussi fréquentées par des
touristes.
· Les chutes de Konkouré:
Situé à 17 km de Mamou sur la route Mamou-Kindia, dans la
CRD de Konkouré, ce site donne la source du fleuve Konkouré par
une chute en forme de voile d'une trentaine de mètres de haut dans une
forêt dense tombant d'une falaise de 50 m en plusieurs paliers au
milieu de grands arbres. On peut aussi descendre au pied de la chute, tout au
moins en saison sèche, en partant sur la droite à travers les
arbres en arrivant sur le site. Il n'existe pas vraiment de chemin et la pente
est un peu raide. Donnant naissance au fleuve de Garafiri, cette source est
fréquentée en toute période. [25]
II-2 Matériel de travail
Le matériel suivant a été utilisé
pour réaliser la présente étude :
II-2-1. Matériel de terrain
· Une glacière ;
· Des marqueurs ;
· Des flacons de 1,50 l;
· Des gangs en latex ;
· Un pH mètre HANA HI : 1832
· Un conductimètre HANA LF 330
· Un turbidimètre Hach 2100p
II-2-2. Matériel de laboratoire
· Un pH mètre HANA HI : 1832
· Un turbidimètre Hach 2100p
· Un conductimètre HANA LF 330
· Un spectrophotomètre DR 2800
· Un thermomètre à 0.5°C
· Un microscope binoculaire
· Stérilisateur à rayons ultraviolets
· Boîtes de Pétri d'environ 49 mm x 9 mm
· Membranes filtrantes stériles quadrillées de
porosité de 0,45 ìm et de 47 mm de diamètre
· Pincettes en acier inoxydable à bouts plats
· Pipettes stériles de 10,0 ml et 1,0 ml de type TD
· Thermomètre permettant une lecture à 0,5
°C
· Tubes à essais de 16 mm x 125 mm avec bouchons
· Fil à boucle
· stéréoscope
· Autoclave
· Incubateur dont la température est ajustée
à 35 °C #177; 0,5 °C
· Balance analytique avec une précision de 0,0001 g
· Rampe de filtration avec entonnoirs et supports de filtres
· pH-mètre
· Plaque chauffante agitatrice avec barre magnétique
· Réfrigérateur maintenant une
température entre 1 °C et 4 °C
· Pompe à vide
· Hygromètre
· Flacons laveurs pour l'eau de rinçage
· Bouteilles de 150 ml avec bouchon
· Lampe à ultraviolets d'une longueur d'onde de 365
nm et d'une puissance de 4 ou 6 W
· Chambre d'observation à rayons ultraviolets
· Disque de filtration de 0,2 ìm monté sur une
seringue jetable de 10 ml
II-3 Méthode de travail
II-3-1 Echantillonnage
Deux campagnes de prélèvement des eaux de puits
traditionnel ont été effectuées durant la période
Juin 2014 et Novembre 2014 au niveau de certains puits traditionnels de la
commune urbaine de Mamou.
Ces puits ont été choisis de manière
à avoir une image d'ensemble de la qualité des eaux de puits de
la commune urbaine. Nous avons effectué au total quatre vingt dix (90)
prélèvements pour l'analyse physico-chimique et
bactériologique des eaux repartis comme suit : quarante cinq (45)
prélèvements durant Juin 2014 et quarante cinq (45)
prélèvements durant Novembre 2014.
Ainsi sur les vingt huit (28) quartiers que compte la commune
urbaine, nous avons effectué des prélèvements au niveau de
cinq (5) quartiers choisis en fonction de la densité de population, des
activités pratiquées, du taux de desserte en eau de la SEG et de
leur géographie.
Dans chaque quartier nous avons choisis trois (3) puits
à prélever en fonction de la fréquentation.
Et au niveau de chaque puits nous avons effectué les
prélèvements de 1,50 litres à différentes heures
7heures ; 9heures et 11 heures. On obtient ainsi trois (3)
échantillons pour chaque puits.
Ces échantillons sont ensuite étiquetés
et placés dans une glacière qui a été
transportée au laboratoire pour les analyses. [26]
II-3-2- Mode opératoire :
II-3-2-1 Détermination du pH
Appareillage : pH mètre HANA HI :
1832
Protocole :
-Rincer l'électrode du pH mettre avec de l'eau
distillée puis avec l'échantillon d'eau à analyser au
moins trois fois.
-Ensuite mettre une quantité représentative de
l'échantillon d'eau à analyser dans un bécher, y plonger
l'électrode du PH mettre.
-Enfin, presser la touche ON/OFF de l'appareil
qui affichera la valeur du ph de l'échantillon et sa température,
lire et noté la valeur correspondante.
II-3-2-2 Détermination de la
Turbidité
Appareillage : Turbidimètre Hach
2100p
Protocole
Ø Essuyer la cuvette avec un tissu doux sans peluches
pour retirer les gouttes d'eau et les traces de doigts.
Ø Prélever un échantillon
représentatif dans un récipient propre. Remplir une cuvette
jusqu'au trait (environ 15 ml) en prenant soin de manipuler la cuvette par la
partie supérieure. Boucher la cuvette.
Ø Appliquer un léger film d'huile silicone.
Essuyer avec un tissu doux pour obtenir un film uniforme sur toute la
surface.
Ø Presser 0/1. L'appareil s'allume. Placer l'appareil
sur une surface plane stable. Ne pas tenir l'appareil à la main pour
effectuer les mesures.
Ø Placer la cuvette dans le puits de mesure de
l'appareil avec le losange ou la marque d'orientation aligné avec le
repère à l'avant du puits de mesure. Fermer le capot.
Ø Presser la touche RANGE pour choisir le mode manuel
ou automatique de sélection de gammes L'affichage indique AUTO RNG
lorsque l'appareil est en mode de sélection automatique de gamme.
Ø Choisir le mode d'intégration du signal en
pressant la touche SIGNAL AVERAGE. L'affichage indique SIG AVG. lorsque le mode
d'intégration du signal est actif. Utiliser le mode d'intégration
du signal si l'échantillon donne un signal instable.
Ø Presser READ, l'affichage indique NTU puis la
turbidité en NTU. Noter la turbidité lorsque le symbole de lampe
s'éteint.
II-3-2-3 Détermination de la
Conductivité
Appareillage : conductimètre HANA LF
330
Protocole
- Rincer l'électrode avec de l'eau distillée ou
de l'eau déminéralisée au moins trois (3) fois ; puis
avec l'échantillon d'eau à analyser.
Introduire une quantité représentative
d'échantillon d'eau à analyser dans un bécher après
agitation.
Plonger l'électrode dans l'échantillon.
Enfin, presser la touche ON/OFF pour allumer puis la touche de
recherche « X » pour afficher la valeur de la
conductivité de l'échantillon exprimé en uS/cm.
II-3-2-4 Détermination des matières en
suspension : MES
Appareillage : Spectrophotomètre DR
2800
Protocole :
Ø Appuyer sur Programmes
enregistrés
Ø Remplir une cuve carrée de 1" jusqu'au trait
de 10 ml avec l'échantillon
Ø Essuyer l'extérieur du blanc (cuve) et
l'introduire dans le compartiment de cuve en dirigeant le trait de remplissage
vers la droite.
Ø Appuyé sur le programme MES.
II-3-2-5 Détermination des nitrites, des
nitrates, du fer total, des phosphates.
Appareillage : Spectrophotomètre DR
2800
Protocole :
Ø Appuyer sur Programmes
enregistrés
Ø Sélectionner le programme d'analyse. Par
exemple : 371N Nitrite LR PP
Ø Remplir une cuve carrée de 1" jusqu'au trait
de 10 ml avec l'échantillon.
Préparation de l'échantillon
:
Ø Transférer le contenu d'une pochette de
réactif dans la cuve ronde. Agiter pour homogénéiser
jusqu'à dissolution de la poudre. Une coloration se développera
en présence de l'élément cherché.
Ø Appuyer sur l'icône représentant la
minuterie. Appuyer sur OK. Une période de
réaction.
Préparation du blanc :
Ø Remplir une autre cuve carrée de 1" jusqu'au
trait de 10 ml avec l'échantillon.
Ø Essuyer l'extérieur du blanc (cuve) et
l'introduire dans le compartiment de cuve en dirigeant le trait de remplissage
vers la droite.
Ø Sélectionner sur l'écran :
Zéro Indication à l'écran : 0,000
mg/l
Ø Essuyer l'extérieur de la cuve contenant
l'échantillon préparé et l'introduire dans le compartiment
de cuve en dirigeant le trait de remplissage vers la droite.
Sélectionner sur l'écran : Mesurer
Les résultats sont indiqués
en mg/l
Tableau N° 7 : Récapitulatif des
paramètres d'analyses pour quelques éléments à
l'aide du spectrophotomètre DR 2800
|
N°
|
Elément Cherché
|
Réactif
|
Temps de réaction (mn)
|
Longueur d'onde, nm
|
N° Programme
|
|
1
|
Fer total
|
ferroZine
|
3
|
562
|
265 Fer Ferro Ver
|
|
2
|
Phosphates
|
Phos Ver3
|
2
|
880
|
490
|
|
3
|
Nitrites
|
NitriVer 3
|
20
|
507
|
371N Nitrite LR PP
|
|
4
|
Nitrates
|
Nitra Ver 5
|
1
|
400
|
353 Nitrate MR PP
|
II-3-2-6 Recherche et dénombrement
simultanés des coliformes totaux et d'Escherichia coli dans l'eau
potable avec le milieu de culture MI : méthode par filtration sur
membrane
Appareillage
· Stérilisateur à rayons ultraviolets
· Boîtes de Pétri d'environ 49 mm x 9 mm
· Membranes filtrantes stériles quadrillées de
porosité de 0,45 ìm et de 47 mm de diamètre
· Pincettes en acier inoxydable à bouts plats
· Pipettes stériles de 10,0 ml et 1,0 ml de type TD
· Thermomètre permettant une lecture à 0,5
°C
· Tubes à essais de 16 mm x 125 mm avec bouchons
· Fil à boucle
· stéréoscope
· Autoclave
· Incubateur dont la température est ajustée
à 35 °C #177; 0,5 °C
· Balance analytique avec une précision de 0,0001 g
· Rampe de filtration avec entonnoirs et supports de filtres
· pH-mètre
· Plaque chauffante agitatrice avec barre magnétique
· Réfrigérateur maintenant une
température entre 1 °C et 4 °C
· Pompe à vide
· Hygromètre
· Flacons laveurs pour l'eau de rinçage
· Bouteilles de 150 ml avec bouchon
· Lampe à ultraviolets d'une longueur d'onde de 365
nm et d'une puissance de 4 ou 6 W
· Chambre d'observation à rayons ultraviolets
· . Disque de filtration de 0,2 ìm monté sur
une seringue jetable de 10 ml
Protocole
Tous les échantillons d'eau ou les échantillons
très liquides doivent être homogénéisés en
agitant vigoureusement les bouteilles d'un mouvement vertical.
Les échantillons soupçonnés d'être
plus contaminés (eaux brutes, eaux de puits de surface, captage de
source, etc.) doivent être traités de façon à
obtenir, pour un volume donné d'échantillon, entre 20 et 80
colonies cibles sur la membrane et ainsi permettre une lecture juste et rapide
du nombre de colonies. Pour l'eau potable, un volume d'échantillon de
100 ml doit être vérifié, mais il peut être
réparti en plusieurs volumes plus faibles sur plusieurs membranes.
Des dilutions en série peuvent aussi être
effectuées de la façon suivante :
· en conditions aseptiques, pipetter 10 ml
d'échantillon dans 90 ml d'eau tamponnée de dilution (1 : 10) ou
encore 10 ml de la dilution 1 : 10 d'un échantillon solide dans 90 ml
d'eau tamponnée de dilution (1 : 100);
· bien agiter la bouteille d'eau tamponnée de
dilution afin d'homogénéiser son contenu;
· répéter cette opération
jusqu'à l'obtention de la dilution désirée (1 : 100, 1 : 1
000, 1 : 10 000, etc.);
changer de pipette entre chaque dilution.
ANALYSE DE L'ÉCHANTILLON
· Placer les entonnoirs et les supports dans le
stérilisateur à rayons ultraviolets pendant 2 minutes.
· Mettre les supports et les entonnoirs sur la rampe de
filtration.
Mettre en fonction l'appareil à vide.
· Prendre une membrane filtrante stérile
près du bord à l'aide d'une pincette stérilisée par
flambage à l'alcool et la déposer ensuite sur le support de
filtre.
· Placer l'entonnoir sur le support et le fixer
fermement.
· Verser 100 ml de l'échantillon pour l'eau
potable ou le volume approprié pour les cas particuliers. Pour les
volumes de 10 ml ou moins, introduire de 20 à 30 ml d'eau
tamponnée de rinçage dans l'entonnoir de filtration.
Ensuite, prélever à l'aide d'une pipette stérile le volume
d'échantillon désiré. Laisser couler l'échantillon
en appuyant le bout de la pipette sur l'épaulement interne de
l'entonnoir. Enlever la dernière goutte de la pipette à l'aide de
la poire.
· Faire le vide pour filtrer l'échantillon.
· Rincer au moins deux fois la paroi intérieure de
l'entonnoir avec environ 20 ml à 30 ml d'eau tamponnée de
rinçage stérile (utiliser un flacon laveur). Rincer davantage
s'il y a possibilité de forte contamination.
Retirer l'entonnoir et déposer la membrane filtrante
à l'aide d'une pince stérile sur une gélose MI.
NB - Déposer la membrane en la
déroulant pour obtenir un contact étroit avec la gélose.
La présence de bulles d'air est signalée par des taches
blanches.
· Inscrire sur la boîte de Pétri le
numéro de l'échantillon et le volume filtré.
· placer les boîtes de Pétri en position
inversée dans un incubateur à 35 °C #177; 0,5 °C
pendant 24 heures #177; 2 heures le plus tôt possible après la
filtration. L'inversion des boîtes de Pétri empêche la
condensation sur les membranes.
OBSERVATION DES RÉSULTATS
· Après la période d'incubation, sortir et
ranger les boîtes de Pétri par ordre de numéro
d'échantillon. L'observation des membranes s'effectue le plus tôt
possible après leur sortie de l'incubateur.
· Choisir les membranes sur lesquelles il y a entre 20 et
80 colonies cibles et au maximum de 200 colonies de toutes sortes.
· Observer d'abord les boîtes de Pétri avec un
éclairage normal pour vérifier la présence de colonies
d'E. coli.
· Les colonies d'E. coli sont bleues sous un
éclairage normal.
· Les colonies d'E. coli peuvent être
visibles et dénombrables malgré la présence d'un tapis de
croissance ou de > 200 colonies atypiques ou > 200 colonies de coliformes
totaux. Cependant, lorsque la membrane est très chargée en
colonies, l'absence de colonies bleues typiques d'E. coli ne garantit
pas l'absence de cette bactérie.
· Avec un éclairage normal, dénombrer les
colonies de toutes sortes.
· Observer ensuite les boîtes de Pétri avec un
éclairage fluorescent à 365 nm pour vérifier la
présence de coliformes totaux. Effectuer cette observation dans
l'obscurité lorsque la fluorescence n'est pas nette.
· Les colonies de coliformes totaux sont fluorescentes.
· Les colonies bleues (E. coli) sont aussi des
coliformes totaux.
· Le nombre de coliformes totaux est la somme des colonies
bleues (fluorescentes ou non) et des colonies fluorescentes (non bleues).
- Un résultat positif apparaissant avant une durée
d'incubation de 24 heures est valide.
- Les résultats négatifs ne sont définitifs
qu'après une période d'incubation de 24 heures.
- Un résultat négatif après 24 heures est
valide.
Si la lecture est difficile, effectuer les observations à
l'aide d'un stéréoscope aux grossissements de 10 X à 15 X.
Placer la lampe à un angle minimum de 80° avec le plan de la lame
de microscope. Ne pas vérifier la fluorescence avec le
stéréomicroscope.
Inscrire sur la feuille de travail le nombre de colonies
bleues, de colonies fluorescentes et de colonies atypiques (non bleues et non
fluorescentes) correspondant au volume d'eau filtrée et reporter le
résultat par 100 ml.
Chapitre III : Résultats et Discussion
III-1 Résultats de la Détermination des
paramètres physico-chimiques
III-1-1 Le pH des eaux en fonction des mois
Tableau 8. pH des eaux de puits en Juin et Novembre
2014
|
Quartier
|
Puits N°
|
H. Echant
|
pH Juin
|
Moyenne
|
Ecart-type
|
pH Novem
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
6.70
|
6.70
|
0.00
|
6.70
|
6.70
|
0.06
|
|
9H
|
6.70
|
6.71
|
|
11H
|
6.70
|
6.70
|
|
2
|
7H
|
6.60
|
6.60
|
0.01
|
6.60
|
6.61
|
0.06
|
|
9H
|
6.61
|
6.61
|
|
11H
|
6.60
|
6.50
|
|
3
|
7H
|
6.30
|
6.30
|
0.01
|
6.50
|
6.50
|
0.06
|
|
9H
|
6.31
|
6.51
|
|
11H
|
6.30
|
6.50
|
|
LOPPE
|
1
|
7H
|
5.90
|
5.90
|
0.20
|
5.80
|
5.83
|
0.06
|
|
9H
|
6.10
|
5.90
|
|
11H
|
5.70
|
5.80
|
|
2
|
7H
|
6.30
|
6.23
|
0.06
|
6.20
|
6.13
|
0.12
|
|
9H
|
6.20
|
6.20
|
|
11H
|
6.20
|
6.00
|
|
3
|
7H
|
7.40
|
7.33
|
0.06
|
7.40
|
7.40
|
0.00
|
|
9H
|
7.30
|
7.40
|
|
11H
|
7.30
|
7.40
|
|
KIMBELY
|
1
|
7H
|
6.90
|
6.90
|
0.00
|
6.80
|
6.90
|
0.12
|
|
9H
|
6.90
|
6.80
|
|
11H
|
6.90
|
7.00
|
|
2
|
7H
|
6.80
|
6.80
|
0.00
|
6.85
|
6.87
|
0.03
|
|
9H
|
6.80
|
6.85
|
|
11H
|
6.80
|
6.90
|
|
3
|
7H
|
6.70
|
6.73
|
0.06
|
6.60
|
6.67
|
0.06
|
|
9H
|
6.80
|
6.60
|
|
11H
|
6.70
|
6.70
|
|
TELICO
|
1
|
7H
|
6.60
|
6.60
|
0.00
|
6.60
|
6.60
|
0.00
|
|
9H
|
6.60
|
6.60
|
|
11H
|
6.60
|
6.60
|
|
2
|
7H
|
7.70
|
7.70
|
0.00
|
7.60
|
7.63
|
0.06
|
|
9H
|
7.70
|
7.70
|
|
11H
|
7.70
|
7.60
|
|
3
|
7H
|
6.80
|
6.83
|
0.06
|
6.90
|
6.83
|
0.06
|
|
9H
|
6.90
|
6.80
|
|
11H
|
6.80
|
6.80
|
|
POUDRIERE
|
1
|
7H
|
7.00
|
7.00
|
0.00
|
7.10
|
7.10
|
0.00
|
|
9H
|
7.00
|
7.10
|
|
11H
|
7.00
|
7.10
|
|
2
|
7H
|
6.50
|
6.47
|
0.06
|
7.50
|
7.50
|
0.00
|
|
9H
|
6.50
|
7.50
|
|
11H
|
6.40
|
7.50
|
|
3
|
7H
|
7.40
|
7.40
|
0.06
|
6.45
|
6.46
|
0.01
|
|
9H
|
7.40
|
6.45
|
|
11H
|
7.41
|
6.47
|
Figure N°2 : Histogramme de la Variation du pH
suivant les mois de Juin et de Novembre 2014

Dans le tableau N°7 nous remarquons qu'en juin 2014, les
valeurs du pH déterminé sur les échantillons des eaux de
puits des quartiers : Abattoir (puits N°1 et N°2), Loppe (puits
N°3), les trois (3) puits de Kimbely, les trois (3) de Telico et les puits
N°1 et 3 de Poudrière sont conformes aux normes de l'OMS
(6,5-8.5).
Par contre :
Le puits N°3 d'Abattoir, les puits
N°1 et 2 de Loppè et le puits N°2 de Poudrière sont
inferieurs aux normes de l'OMS (6,5 à 8,5).
Au mois de Novembre 2014, nous avons observé une
légère variation du pH comme le montre la figure N°2
Cet état de fait serait dû à la
présence du gaz carbonique (CO2) produit lors de la
décomposition des matières organiques au niveau du sol par les
bactéries.
D'après le tableau N° 7, 22.22% des puits
étudiés (soit 10 puits/45) ont un pH en dessous de la normale
(6.5-8.5), ce qui pourrait avoir pour conséquence le risque de corrosion
du ciment ou des métaux.
Toute fois la consommation de ces eaux par la population ne
pourrait pas constituer un risque pour la santé humaine.
III-1-2 La conductivité
Tableau 9. Conductivité en uS/cm des eaux des
puits à 25°C en Juin et Novembre 2014
|
Quartier
|
Puits N°
|
H. Echant
|
Cond Juin
|
Moyenne
|
Ecart-type
|
Cond Nov
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
116
|
115
|
1
|
118
|
121
|
3
|
|
9H
|
115
|
124
|
|
11H
|
114
|
120
|
|
2
|
7H
|
221
|
220
|
1
|
220
|
222
|
2
|
|
9H
|
220
|
224
|
|
11H
|
220
|
222
|
|
3
|
7H
|
165
|
165
|
0
|
171
|
178
|
6
|
|
9H
|
165
|
183
|
|
11H
|
165
|
180
|
|
LOPPE
|
1
|
7H
|
295
|
295
|
1
|
320
|
327
|
6
|
|
9H
|
294
|
331
|
|
11H
|
295
|
330
|
|
2
|
7H
|
265
|
265
|
1
|
260
|
274
|
13
|
|
9H
|
264
|
286
|
|
11H
|
266
|
276
|
|
3
|
7H
|
289
|
290
|
1
|
337
|
340
|
3
|
|
9H
|
291
|
343
|
|
11H
|
291
|
340
|
|
KIMBELY
|
1
|
7H
|
198
|
198
|
0
|
220
|
222
|
2
|
|
9H
|
198
|
224
|
|
11H
|
198
|
222
|
|
2
|
7H
|
301
|
300
|
1
|
360
|
380
|
20
|
|
9H
|
300
|
400
|
|
11H
|
300
|
380
|
|
3
|
7H
|
150
|
151
|
1
|
182
|
185
|
2
|
|
9H
|
152
|
186
|
|
11H
|
151
|
185
|
|
TELICO
|
1
|
7H
|
100
|
100
|
1
|
110
|
112
|
2
|
|
9H
|
100
|
114
|
|
11H
|
101
|
112
|
|
2
|
7H
|
179
|
180
|
1
|
215
|
220
|
9
|
|
9H
|
181
|
230
|
|
11H
|
180
|
215
|
|
3
|
7H
|
145
|
145
|
0
|
190
|
194
|
5
|
|
9H
|
145
|
200
|
|
11H
|
145
|
198
|
|
POUDRIERE
|
1
|
7H
|
99
|
99
|
1
|
100,8
|
112
|
11
|
|
9H
|
100
|
122,8
|
|
11H
|
98
|
111,8
|
|
2
|
7H
|
244
|
245
|
1,00
|
997
|
998
|
2
|
|
9H
|
246
|
1000
|
|
11H
|
245
|
997
|
|
3
|
7H
|
849
|
852
|
3,00
|
290
|
300
|
10
|
|
9H
|
855
|
310
|
|
11H
|
852
|
299
|
Figure N°3 : HISTOGRAMME DE LA VARIATION DE LA
CONDUCTIVITE POUR JUIN ET NOVEMBRE 2014
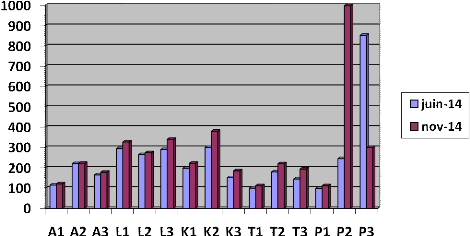 De manière générale la conductivité
a subi une croissance sur la période d'étude au niveau de la
plupart des quartiers (sauf le puits N°3 de Poudrière) entrainant
donc une croissance de la minéralisation. Mais cette croissance pourrait
être due à l'arrivée dans ces puits d'eaux usées.
Cette infiltration d'eaux usées c'est accentuée au niveau du
puits N°2 de Poudrière alors qu'elle a décrue pour le puits
N° 3 de Poudrière. Cependant la décroissance de la
conductivité au niveau du puits N°3 de Poudrière pourrait
être liée au déménagement des occupants des lieux et
l'absence de nouveaux occupants en Novembre 2014. De manière générale la conductivité
a subi une croissance sur la période d'étude au niveau de la
plupart des quartiers (sauf le puits N°3 de Poudrière) entrainant
donc une croissance de la minéralisation. Mais cette croissance pourrait
être due à l'arrivée dans ces puits d'eaux usées.
Cette infiltration d'eaux usées c'est accentuée au niveau du
puits N°2 de Poudrière alors qu'elle a décrue pour le puits
N° 3 de Poudrière. Cependant la décroissance de la
conductivité au niveau du puits N°3 de Poudrière pourrait
être liée au déménagement des occupants des lieux et
l'absence de nouveaux occupants en Novembre 2014.
La valeur la plus élevée est observée au
niveau du puits 2 de Poudrière. Cette minéralisation
élevée serait surtout due au fait que les richesses
précieuses en eaux souterraines sont confrontées à des
menaces de pollution liées essentiellement aux activités
humaines.
Ainsi durant notre étude nous avons constaté
qu'en juin 2014 toutes les eaux analysées répondaient aux normes
de l'OMS mais qu'en novembre 2014, la conductivité des eaux de puits de
la poudrière a dépassé les normes suite à
l'infiltration d'eaux usées.
III-1-3-Les Matières en Suspension (MES)
Tableau 10 : Matières en suspension (MES)
en mg/l dans les eaux des puits en Juin et novembre 2014
|
Quartier
|
Puits N°
|
H. Echant
|
MES Juin
|
Moyenne
|
Ecart-type
|
MES Novem
|
Moyenne
|
Ecart-type
|
|
Abattoir
|
1
|
7H
|
20
|
22
|
2
|
4
|
5
|
1
|
|
9H
|
24
|
6
|
|
11H
|
22
|
5
|
|
2
|
7H
|
6
|
7
|
2
|
0
|
0
|
0
|
|
9H
|
7
|
0
|
|
11H
|
9
|
0
|
|
3
|
7H
|
9
|
9
|
0
|
7
|
7
|
1
|
|
9H
|
9
|
8
|
|
11H
|
9
|
6
|
|
Loppè
|
1
|
7H
|
6
|
6
|
0
|
3
|
3
|
0
|
|
9H
|
6
|
3
|
|
11H
|
6
|
3
|
|
2
|
7H
|
11
|
12
|
1
|
10
|
9
|
1
|
|
9H
|
13
|
9
|
|
11H
|
12
|
8
|
|
3
|
7H
|
28
|
28
|
2
|
26
|
25
|
1
|
|
9H
|
30
|
24
|
|
11H
|
26
|
25
|
|
Kimbély
|
1
|
7H
|
7
|
7
|
0
|
5
|
5
|
0
|
|
9H
|
7
|
5
|
|
11H
|
7
|
5
|
|
2
|
7H
|
5
|
5
|
1
|
0
|
0
|
0
|
|
9H
|
6
|
0
|
|
11H
|
4
|
0
|
|
3
|
7H
|
37
|
29
|
4
|
18
|
16
|
2
|
|
9H
|
31
|
14
|
|
11H
|
29
|
16
|
|
Télico
|
1
|
7H
|
10
|
6
|
3
|
0
|
0
|
0
|
|
9H
|
4
|
0
|
|
11H
|
4
|
0
|
|
2
|
7H
|
18
|
18
|
0
|
10
|
10
|
0
|
|
9H
|
18
|
10
|
|
11H
|
18
|
10
|
|
3
|
7H
|
2
|
2
|
0
|
0
|
0
|
0
|
|
9H
|
2
|
0
|
|
11H
|
2
|
0
|
|
Poudrière
|
1
|
7H
|
8
|
6
|
2
|
2
|
2
|
0
|
|
9H
|
6
|
2
|
|
11H
|
4
|
2
|
|
2
|
7H
|
8
|
8
|
0
|
10
|
10
|
2
|
|
9H
|
8
|
8
|
|
11H
|
8
|
12
|
|
3
|
7H
|
16
|
16
|
0
|
0
|
0
|
0
|
|
9H
|
16
|
0
|
|
11H
|
16
|
0
|
Figure N°4 : HISTOGRAMME DE LA VARIATION DES
MES EN JUIN ET NOVEMBRE 2014
 Nous constatons que les MES sont plus élevées en
juin qu'à novembre. Cela serait due au fait qu'en saison sèche
les puits sont plus utilisés qu'en novembre ; entrainant ainsi une
surexploitation de ces puits et par conséquent d'un apport de
matériaux de toute sorte allant des chaussures des personnes aux
débris apportés par le vent. Nous constatons que les MES sont plus élevées en
juin qu'à novembre. Cela serait due au fait qu'en saison sèche
les puits sont plus utilisés qu'en novembre ; entrainant ainsi une
surexploitation de ces puits et par conséquent d'un apport de
matériaux de toute sorte allant des chaussures des personnes aux
débris apportés par le vent.
L'abondance des matières en suspension dans l'eau favorise
la réduction de la luminosité et abaisse la production biologique
du fait, en particulier, d'une chute de l'oxygène dissous
consécutive à une réduction des phénomènes
de photosynthèse. [26]
La consommation de ces eaux ne constitue pas un risque pour la
santé du point vue MES.
II-1-4-La turbidité
Tableau N°11 : Turbidité en NTU dans
les eaux des puits en Juin et novembre 2014
|
Quartier
|
Puits N°
|
H. Echant
|
Turb Juin
|
Moyenne
|
Ecart-type
|
Turb Nov
|
Moyenne
|
Ecart-type
|
|
Abattoir
|
1
|
7H
|
14
|
12
|
2
|
25
|
29
|
5
|
|
9H
|
12
|
34
|
|
11H
|
10
|
29
|
|
2
|
7H
|
2
|
2
|
0
|
7
|
8
|
1
|
|
9H
|
2
|
8
|
|
11H
|
2
|
9
|
|
3
|
7H
|
1
|
1
|
0
|
7
|
6
|
1
|
|
9H
|
1
|
6
|
|
11H
|
1
|
5
|
|
Loppè
|
1
|
7H
|
5
|
5
|
0
|
8
|
8
|
0
|
|
9H
|
5
|
8
|
|
11H
|
5
|
8
|
|
2
|
7H
|
3
|
3
|
0
|
9
|
8
|
1
|
|
9H
|
3
|
8
|
|
11H
|
3
|
7
|
|
3
|
7H
|
9
|
10
|
1
|
6
|
6
|
0
|
|
9H
|
10
|
6
|
|
11H
|
11
|
6
|
|
Kimbely
|
1
|
7H
|
0
|
0
|
0
|
4
|
4
|
1
|
|
9H
|
0
|
5
|
|
11H
|
0
|
3
|
|
2
|
7H
|
0
|
0
|
0
|
5
|
4
|
1
|
|
9H
|
0
|
4
|
|
11H
|
0
|
3
|
|
3
|
7H
|
5
|
5
|
1
|
8
|
9
|
1
|
|
9H
|
6
|
10
|
|
11H
|
4
|
9
|
|
Télico
|
1
|
7H
|
0
|
0
|
0
|
3
|
3
|
0
|
|
9H
|
0
|
3
|
|
11H
|
0
|
3
|
|
2
|
7H
|
3
|
3
|
0
|
0
|
0
|
0
|
|
9H
|
3
|
0
|
|
11H
|
3
|
0
|
|
3
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
Poudrière
|
1
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
2
|
7H
|
7
|
7
|
1
|
8
|
8
|
0
|
|
9H
|
6
|
8
|
|
11H
|
8
|
8
|
|
3
|
7H
|
0
|
0
|
0
|
16
|
15
|
1
|
|
9H
|
0
|
15
|
|
11H
|
0
|
14
|
Figure N°5 : HISTOGRAMME DE LA VARIATION DE LA
TURBIDITE POUR JUIN ET NOVEMBRE 2014

Au niveau des eaux étudiées, la turbidité
est croissante pendant la période d'étude pour les quartiers
Abattoir (puits N°1 ; 2 ; et 3), kimbely (puits 3), Loppe et
Poudrière en dépassant les normes de l'OMS. Cet état de
fait pourrait être dû à l'infiltration d'eaux usées.
Ces eaux deviennent ainsi impropre à la boisson car suspectes à
la pollution microbiologique.
Cet état de fait serait dû à la
proximité de ces puits sur le trajet des eaux de ruissellement ou par
usage abusif des puits.
Par contre nous observons un abaissement de la
turbidité pour Telico et le puits N°1 de Poudrière.
La faiblesse de la turbidité et des MES font que les
propriétaires de ces puits assimilent la qualité de leur eaux
à celle de la SEG.
III-1-5-Les nitrites
Tableau 12. Les nitrites en mg/l dans les eaux des puits
en juin et Novembre 2014
|
Quartier
|
Puits N°
|
H. Echant
|
NO2- Juin
|
Moyenne
|
Ecart-type
|
NO2- Novem
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
0,090
|
0,090
|
0,000
|
0,013
|
0,013
|
0,000
|
|
9H
|
0,090
|
0,013
|
|
11H
|
0,090
|
0,013
|
|
2
|
7H
|
0,035
|
0,036
|
0,000
|
0,056
|
0,056
|
0,000
|
|
9H
|
0,037
|
0,056
|
|
11H
|
0,036
|
0,056
|
|
3
|
7H
|
0,046
|
0,045
|
0,000
|
0,056
|
0,056
|
0,000
|
|
9H
|
0,045
|
0,056
|
|
11H
|
0,044
|
0,056
|
|
LOPPE
|
1
|
7H
|
0,200
|
0,200
|
0,00
|
0,270
|
0,260
|
0,020
|
|
9H
|
0,200
|
0,270
|
|
11H
|
0,200
|
0,240
|
|
2
|
7H
|
0,340
|
0,330
|
0,010
|
0,449
|
0,449
|
0,000
|
|
9H
|
0,330
|
0,449
|
|
11H
|
0,320
|
0,449
|
|
3
|
7H
|
0,010
|
0,010
|
0,000
|
0,013
|
0,013
|
0,000
|
|
9H
|
0,010
|
0,012
|
|
11H
|
0,010
|
0,014
|
|
KIMBELY
|
1
|
7H
|
0,020
|
0,020
|
0,000
|
0,030
|
0,030
|
0,000
|
|
9H
|
0,020
|
0,030
|
|
11H
|
0,020
|
0,030
|
|
2
|
7H
|
0,020
|
0,020
|
0,000
|
0,030
|
0,030
|
0,000
|
|
9H
|
0,020
|
0,030
|
|
11H
|
0,020
|
0,030
|
|
3
|
7H
|
0,370
|
0,370
|
0,010
|
0,420
|
0,440
|
0,020
|
|
9H
|
0,380
|
0,440
|
|
11H
|
0,360
|
0,460
|
|
TELICO
|
1
|
7H
|
0,004
|
0,004
|
0,000
|
0,007
|
0,007
|
0,000
|
|
9H
|
0,004
|
0,007
|
|
11H
|
0,004
|
0,007
|
|
2
|
7H
|
0,018
|
0,017
|
0,000
|
0,026
|
0,026
|
0,000
|
|
9H
|
0,016
|
0,026
|
|
11H
|
0,017
|
0,026
|
|
3
|
7H
|
0,050
|
0,060
|
0,010
|
0,077
|
0,079
|
0,000
|
|
9H
|
0,060
|
0,079
|
|
11H
|
0,070
|
0,081
|
|
POUDRIERE
|
1
|
7H
|
0,010
|
0,010
|
0,000
|
0,013
|
0,013
|
0,000
|
|
9H
|
0,010
|
0,013
|
|
11H
|
0,010
|
0,013
|
|
2
|
7H
|
0,002
|
0,002
|
0,000
|
0,380
|
0,370
|
0,010
|
|
9H
|
0,002
|
0,370
|
|
11H
|
0,002
|
0,360
|
|
3
|
7H
|
0,300
|
0,300
|
0,000
|
0,003
|
0,003
|
0,000
|
|
9H
|
0,300
|
0,003
|
|
11H
|
0,300
|
0,003
|
Figure N°6 : HISTOGRAMME DE LA VARIATION DES
NITRITES POUR JUIN ET NOVEMBRE 2014
 Au cours de cette étude, nous avons remarqué
qu'au niveau des puits N°1 de Abattoir et N°3 de Poudrière, le
taux de nitrites a connu une très grande chute. Ceci pourrait être
dû au réaménagement (faire le linge loin des puits,
nettoyage interne et externe des puits) effectue par les occupants des lieux. Au cours de cette étude, nous avons remarqué
qu'au niveau des puits N°1 de Abattoir et N°3 de Poudrière, le
taux de nitrites a connu une très grande chute. Ceci pourrait être
dû au réaménagement (faire le linge loin des puits,
nettoyage interne et externe des puits) effectue par les occupants des lieux.
Un accroissement modéré des nitrites s'observe
au niveau des puits N°2 ; 3 de Abattoir, du puits N°3 de
Loppè ; des puits N°1 et 2 de kimbely ; des puits
N°1, 2 et 3 de Télico et du puits N°1 de Poudrière.
Cela serait dû au maintient des habitudes comportementales des
populations vis-à- vis des puits.
Aussi, au niveau des puits N° 1 et 2 de Loppè,
N°3 de Kimbely et N°2 de Poudière, le taux de nitrites a connu
une très forte croissance dû a l'accentuation des pratiques
domestiques favorisant la pollution de ces eaux.
Ainsi, au cours de notre étude, nous avons
constaté que 12 puits sur 45 (soit 26.67%) ont un taux de nitrites
supérieur à la norme de l'OMS. Ce qui pourrait être
lié aux activités humaines et aux mauvaises pratiques agricoles.
Par conséquent, ces eaux sont considérée comme suspectes
car un taux élevé en nitrites est souvent associé à
une détérioration de la qualité microbiologique.
Comme la présence de nitrites dans le sang
empêche l'hémoglobine de fixer convenablement l'oxygène et
entraîne ainsi des risques de méthémoglobinémie
aiguë, la consommation de ces eaux comme eaux de boisson n'est par
conséquent pas recommandé. En outre, les nitrites sont
très toxiques pour les poissons et souvent mortels.
III-1-6 Les nitrates
Tableau 13. Variation des nitrates en mg/l dans les
eaux des puits en juin et en Novembre 2014.
|
Quartier
|
Puits N°
|
H. Echant
|
NO3- Juin
|
Moyenne
|
Ecart-type
|
NO3- Novem
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
29,67
|
29,68
|
0,01
|
35,17
|
35,17
|
0,00
|
|
9H
|
29,69
|
35,17
|
|
11H
|
29,68
|
35,17
|
|
2
|
7H
|
98,58
|
98,59
|
0,01
|
105,50
|
105,60
|
0,10
|
|
9H
|
98,60
|
105,60
|
|
11H
|
98,59
|
105,70
|
|
3
|
7H
|
150,24
|
150,26
|
0,02
|
192,28
|
192,28
|
0,00
|
|
9H
|
150,27
|
192,28
|
|
11H
|
150,27
|
192,28
|
|
LOPPE
|
1
|
7H
|
199,32
|
199,32
|
0,01
|
217,36
|
217,36
|
0,00
|
|
9H
|
199,33
|
217,36
|
|
11H
|
199,31
|
217,36
|
|
2
|
7H
|
105,20
|
105,20
|
0,00
|
172,00
|
172,00
|
0,00
|
|
9H
|
105,20
|
172,00
|
|
11H
|
105,20
|
172,00
|
|
3
|
7H
|
1,58
|
1,59
|
0,01
|
2,65
|
2,64
|
0,01
|
|
9H
|
1,60
|
2,64
|
|
11H
|
1,59
|
2,63
|
|
KIMBELY
|
1
|
7H
|
79,35
|
79,35
|
0,00
|
97,24
|
97,24
|
0,00
|
|
9H
|
79,35
|
97,24
|
|
11H
|
79,35
|
97,24
|
|
2
|
7H
|
296,64
|
296,64
|
0,00
|
370,50
|
370,50
|
0,00
|
|
9H
|
296,64
|
370,50
|
|
11H
|
296,64
|
370,50
|
|
3
|
7H
|
102,52
|
102,53
|
0,01
|
167,85
|
167,85
|
0,00
|
|
9H
|
102,54
|
167,85
|
|
11H
|
102,53
|
167,85
|
|
TELICO
|
1
|
7H
|
6,80
|
6,80
|
0,00
|
8,80
|
8,80
|
0,00
|
|
9H
|
6,80
|
8,80
|
|
11H
|
6,80
|
8,80
|
|
2
|
7H
|
4,66
|
4,67
|
0,01
|
7,92
|
7,92
|
0,00
|
|
9H
|
4,67
|
7,92
|
|
11H
|
4,68
|
7,92
|
|
3
|
7H
|
78,20
|
78,21
|
0,01
|
84,47
|
84,48
|
0,01
|
|
9H
|
78,22
|
84,48
|
|
11H
|
78,21
|
84,49
|
|
POUDRIERE
|
1
|
7H
|
32,58
|
32,58
|
0,00
|
47,60
|
47,60
|
0,00
|
|
9H
|
32,58
|
47,60
|
|
11H
|
32,58
|
47,60
|
|
2
|
7H
|
49,67
|
49,68
|
0,01
|
6,60
|
6,60
|
0,00
|
|
9H
|
49,69
|
6,60
|
|
11H
|
49,68
|
6,60
|
|
3
|
7H
|
4,10
|
4,10
|
0,00
|
52,80
|
52,80
|
0,00
|
|
9H
|
4,10
|
52,80
|
|
11H
|
4,10
|
52,80
|
Figure N°7 : Histogramme de la Variation du
taux de nitrates suivant les mois de Juin et de Novembre 2014
 Nous observons d'après la figure N°7 que le puits N°1
de Abattoir, N°3 de Loppe, N° 1 et N°2 de Telico ainsi que les
trois (3) puits de la Poudrière sont dans les normes de l'OMS durant la
période d'étude mais tout les autres ne répondent pas aux
normes de l'OMS. Nous observons d'après la figure N°7 que le puits N°1
de Abattoir, N°3 de Loppe, N° 1 et N°2 de Telico ainsi que les
trois (3) puits de la Poudrière sont dans les normes de l'OMS durant la
période d'étude mais tout les autres ne répondent pas aux
normes de l'OMS.
L'accroissement du taux de nitrates dans ces eaux pour les
puits N° 1 ; N°2 de Abattoir, N°1 ; 2 et 3 de Telico,
N° 1 de Loppe et même N°1 de kimbely est moindre ce qui traduit
une incidence modérée de la pollution domestique. Par contre, la
forte croissance du taux de nitrates pour le puits N° 2 de Loppe, N°
3 de Abattoir ; N° 2 et 3 de kimbely et N° 3 de Poudrière
prouve à suffisance l'impact de la pollution domestique.
D'après le tableau N°12, 24 puits sur les 45
(soit 53.37%) ne répondent pas aux normes de l'OMS.
En effet, on observe au niveau de certains de ces puits de la
présence des poubelles et des eaux usées domestiques.
Les nitrates sont naturellement présents mais en faible
quantité dans les sols. Ils constituent aujourd'hui le principal
indicateur d'une dégradation des ressources en eau [27]. L'augmentation
des teneurs constatées est notamment le résultat
d'activités humaines.
Par conséquent la consommation de cette eau en eau de
boisson devrait être interdite aux femmes enceintes et aux nourrissons
pour prévenir la méthémoglobinémie.
III-1-6- Les Phosphates
Tableau 14. Variation des Phosphates en mg/l dans
les eaux des puits en Juin et novembre 2014
|
Quartier
|
Puits N°
|
H. Echant
|
Phosp Juin
|
Moyenne
|
Ecart-type
|
Phosp Novem
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
0,62
|
0,62
|
0,00
|
0,70
|
0,70
|
0,00
|
|
9H
|
0,62
|
0,70
|
|
11H
|
0,62
|
0,70
|
|
2
|
7H
|
1,80
|
1,80
|
0,00
|
2,10
|
2,10
|
0,00
|
|
9H
|
1,80
|
2,10
|
|
11H
|
1,80
|
2,10
|
|
3
|
7H
|
0,48
|
0,49
|
0,01
|
0,55
|
0,54
|
0,01
|
|
9H
|
0,50
|
0,54
|
|
11H
|
0,49
|
0,53
|
|
LOPPE
|
1
|
7H
|
0,01
|
0,01
|
0,00
|
0,02
|
0,02
|
0,00
|
|
9H
|
0,01
|
0,02
|
|
11H
|
0,01
|
0,02
|
|
2
|
7H
|
0,03
|
0,03
|
0,00
|
0,05
|
0,05
|
0,00
|
|
9H
|
0,03
|
0,05
|
|
11H
|
0,03
|
0,05
|
|
3
|
7H
|
0,98
|
0,98
|
0,01
|
1,16
|
1,14
|
0,02
|
|
9H
|
0,97
|
1,13
|
|
11H
|
0,99
|
1,13
|
|
KIMBELY
|
1
|
7H
|
0,01
|
0,01
|
0,00
|
0,06
|
0,06
|
0,00
|
|
9H
|
0,01
|
0,06
|
|
11H
|
0,01
|
0,06
|
|
2
|
7H
|
0,03
|
0,03
|
0,00
|
0,05
|
0,05
|
0,00
|
|
9H
|
0,03
|
0,05
|
|
11H
|
0,03
|
0,05
|
|
3
|
7H
|
0,40
|
0,40
|
0,00
|
0,60
|
0,60
|
0,00
|
|
9H
|
0,40
|
0,60
|
|
11H
|
0,40
|
0,60
|
|
TELICO
|
1
|
7H
|
0,11
|
0,11
|
0,00
|
0,18
|
0,18
|
0,01
|
|
9H
|
0,11
|
0,19
|
|
11H
|
0,11
|
0,17
|
|
2
|
7H
|
0,18
|
0,19
|
0,01
|
0,22
|
0,22
|
0,00
|
|
9H
|
0,20
|
0,22
|
|
11H
|
0,19
|
0,22
|
|
3
|
7H
|
0,01
|
0,01
|
0,00
|
0,02
|
0,02
|
0,00
|
|
9H
|
0,01
|
0,02
|
|
11H
|
0,01
|
0,02
|
|
POUDRIERE
|
1
|
7H
|
3,65
|
3,64
|
0,01
|
4,95
|
4,94
|
0,01
|
|
9H
|
3,63
|
4,93
|
|
11H
|
3,64
|
4,94
|
|
2
|
7H
|
0,01
|
0,01
|
0,00
|
4,97
|
4,98
|
0,02
|
|
9H
|
0,01
|
5,00
|
|
11H
|
0,01
|
4,97
|
|
3
|
7H
|
3,90
|
3,90
|
0,00
|
0,02
|
0,02
|
0,00
|
|
9H
|
3,90
|
0,02
|
|
11H
|
3,90
|
0,02
|
Figure N°8 : Histogramme de la Variation du
taux de phosphates suivant les mois de Juin et de Novembre 2014
 Nous avons observé un accroissement modéré du taux
de phosphates au niveau des puits N°1 ; 2 et 3 de Abattoir,
N°1 ; 2 et 3 de Loppe ; N°1 ; 2 et 3 de Kimbely, et
des trois (3) puits de Telico. Ceci serait dû au maintient des habitudes
comportementales des populations vis-à- vis des puits. Nous avons observé un accroissement modéré du taux
de phosphates au niveau des puits N°1 ; 2 et 3 de Abattoir,
N°1 ; 2 et 3 de Loppe ; N°1 ; 2 et 3 de Kimbely, et
des trois (3) puits de Telico. Ceci serait dû au maintient des habitudes
comportementales des populations vis-à- vis des puits.
Nous observons aussi une très forte croissance du taux
de phosphates au niveau du puits N°2 de Poudrière, une très
forte chute de ce taux au niveau du puits N°3 et une forte augmentation au
niveau du puits N°1 alors que trop de phosphates peuvent provoquer des
problèmes de santé, tels que l'ostéoporose ou des
problèmes de reins. Au total, nous avons constaté que 60% des
puits étudié en juin (soit 27 puits sur 45) et 60% des puits
étudié en novembre (soit 27 puits sur 45) sont pollués par
les phosphates.
III-1-7 Le fer total
Tableau 15. Fer total en mg/l dans les eaux des puits
en Juin et novembre 2014
|
Quartier
|
Puits N°
|
H. Echant
|
Fer Juin
|
Moyenne
|
Ecart-type
|
Fer Novem
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
0,05
|
0,05
|
0,00
|
0,06
|
0,06
|
0,00
|
|
9H
|
0,05
|
0,06
|
|
11H
|
0,05
|
0,06
|
|
2
|
7H
|
0,09
|
0,09
|
0,00
|
0,09
|
0,09
|
0,00
|
|
9H
|
0,09
|
0,09
|
|
11H
|
0,09
|
0,09
|
|
3
|
7H
|
0,04
|
0,04
|
0,00
|
0,05
|
0,05
|
0,00
|
|
9H
|
0,04
|
0,05
|
|
11H
|
0,04
|
0,05
|
|
LOPPE
|
1
|
7H
|
0,04
|
0,04
|
0,00
|
0,04
|
0,04
|
0,00
|
|
9H
|
0,04
|
0,04
|
|
11H
|
0,04
|
0,04
|
|
2
|
7H
|
0,05
|
0,05
|
0,00
|
0,05
|
0,05
|
0,00
|
|
9H
|
0,05
|
0,05
|
|
11H
|
0,05
|
0,05
|
|
3
|
7H
|
0,02
|
0,02
|
0,00
|
0,02
|
0,02
|
0,00
|
|
9H
|
0,02
|
0,02
|
|
11H
|
0,02
|
0,02
|
|
KIMBELY
|
1
|
7H
|
0,03
|
0,03
|
0,00
|
0,03
|
0,03
|
0,00
|
|
9H
|
0,03
|
0,03
|
|
11H
|
0,03
|
0,03
|
|
2
|
7H
|
0,02
|
0,02
|
0,00
|
0,02
|
0,02
|
0,00
|
|
9H
|
0,02
|
0,02
|
|
11H
|
0,02
|
0,02
|
|
3
|
7H
|
0,02
|
0,02
|
0,00
|
0,03
|
0,03
|
0,00
|
|
9H
|
0,02
|
0,03
|
|
11H
|
0,02
|
0,03
|
|
TELICO
|
1
|
7H
|
0,04
|
0,04
|
0,00
|
0,04
|
0,04
|
0,00
|
|
9H
|
0,04
|
0,04
|
|
11H
|
0,04
|
0,04
|
|
2
|
7H
|
0,04
|
0,04
|
0,01
|
0,04
|
0,04
|
0,00
|
|
9H
|
0,03
|
0,04
|
|
11H
|
0,05
|
0,04
|
|
3
|
7H
|
0,01
|
0,01
|
0,00
|
0,01
|
0,01
|
0,00
|
|
9H
|
0,01
|
0,01
|
|
11H
|
0,01
|
0,01
|
|
POUDRIERE
|
1
|
7H
|
0,10
|
0,10
|
0,00
|
0,10
|
0,10
|
0,00
|
|
9H
|
0,10
|
0,10
|
|
11H
|
0,10
|
0,10
|
|
2
|
7H
|
0,99
|
1,00
|
0,01
|
0,99
|
0,98
|
0,01
|
|
9H
|
1,01
|
0,97
|
|
11H
|
1,00
|
0,98
|
|
3
|
7H
|
0,05
|
0,05
|
0,00
|
0,04
|
0,04
|
0,00
|
|
9H
|
0,05
|
0,04
|
|
11H
|
0,05
|
0,04
|
Figure N°9 : Histogramme de la variation du
taux de fer pour juin et novembre 2014

La présence du fer dans l'eau peut favoriser la
prolifération de certaines souches de bactéries qui
précipitent le fer et corrodent les canalisations.
Nous constatons au niveau de la figure N°9, pratiquement
une stabilité de la teneur en fer sur la période d'études
sauf pour le quartier Poudrière. Ceci pourrait être dû
à la présence dans le quartier de garages mécaniques.
Ainsi, au cours de notre étude, nous avons
constaté que 93.33% des puits étudiés au cours de chacune
des campagnes ont un taux de fer dans les normes de l'OMS (soit =0,3 mg/l)
La consommation de ces eaux ne présente pas de danger
du point de vu fer total.
III-2 Résultats de l'analyse
microbiologique :
Tableau 16 : Coliformes Totaux dans les eaux des
puits pour Juin et Novembre 2014.
|
Quartier
|
Puits N°
|
H. Echant
|
CT- Juin/100ml
|
Moyenne
|
Ecart-type
|
CT Nov/100ml
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
40
|
38
|
2
|
62
|
60
|
2
|
|
9H
|
37
|
60
|
|
11H
|
37
|
58
|
|
2
|
7H
|
50
|
50
|
2
|
60
|
58
|
3
|
|
9H
|
52
|
60
|
|
11H
|
48
|
54
|
|
3
|
7H
|
39
|
39
|
1
|
36
|
35
|
2
|
|
9H
|
38
|
36
|
|
11H
|
40
|
33
|
|
LOPPE
|
1
|
7H
|
45
|
45
|
3
|
52
|
51
|
1
|
|
9H
|
48
|
51
|
|
11H
|
42
|
50
|
|
2
|
7H
|
29
|
30
|
2
|
55
|
53
|
2
|
|
9H
|
32
|
52
|
|
11H
|
29
|
52
|
|
3
|
7H
|
18
|
20
|
3
|
17
|
15
|
2
|
|
9H
|
18
|
15
|
|
11H
|
24
|
13
|
|
KIMBELY
|
1
|
7H
|
16
|
19
|
3
|
10
|
10
|
0
|
|
9H
|
19
|
10
|
|
11H
|
22
|
10
|
|
2
|
7H
|
30
|
32
|
2
|
48
|
48
|
1
|
|
9H
|
34
|
47
|
|
11H
|
32
|
49
|
|
3
|
7H
|
50
|
48
|
4
|
48
|
45
|
3
|
|
9H
|
51
|
42
|
|
11H
|
43
|
45
|
|
TELICO
|
1
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
2
|
7H
|
8
|
8
|
0
|
5
|
5
|
0
|
|
9H
|
8
|
5
|
|
11H
|
8
|
5
|
|
3
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
POUDRIERE
|
1
|
7H
|
2
|
2
|
0
|
2
|
2
|
0
|
|
9H
|
2
|
2
|
|
11H
|
2
|
2
|
|
2
|
7H
|
32
|
29
|
3
|
0
|
0
|
0
|
|
9H
|
28
|
0
|
|
11H
|
27
|
0
|
|
3
|
7H
|
32
|
32
|
2
|
42
|
40
|
2
|
|
9H
|
30
|
40
|
|
11H
|
34
|
38
|
Figure N° 10 : HISTOGRAMME DE LA VARIATION DU
TAUX DE COLIFORMES TOTAUX POUR JUIN ET NOVEMBRE 2014
 Nous observons qu'au niveau des puits N°1 ; 2 de
Abattoir ; des puits N° 1 et 2 de Loppe ; des puits N°1 et
2 de Kimbely ; et du puits N°3 de Poudrière une augmentation
du taux de coliformes totaux du fait de l'utilisation accrue des puits en
novembre et du taux de desserte très faible en eaux de la SEG au niveau
de ces quartiers. Nous observons qu'au niveau des puits N°1 ; 2 de
Abattoir ; des puits N° 1 et 2 de Loppe ; des puits N°1 et
2 de Kimbely ; et du puits N°3 de Poudrière une augmentation
du taux de coliformes totaux du fait de l'utilisation accrue des puits en
novembre et du taux de desserte très faible en eaux de la SEG au niveau
de ces quartiers.
La chute ou la décroissance observée au niveau
des puits N° 3 de Abattoir, N°3 de Loppe ; N°3 de
kimbely ; N°2 de Telico et N° 2 de poudrière serait
dû au fait que les populations voisines de ces puits ont plus
accès à l'eau de la SEG.
Tableau N°17 : Escherichia Coli dans les
eaux des puits pour Juin et Novembre 2014.
|
Quartier
|
Puits N°
|
H. Echant
|
E.coli Juin
|
Moyenne
|
Ecart-type
|
E.coli Novem
|
Moyenne
|
Ecart-type
|
|
ABATTOIR
|
1
|
7H
|
26
|
26
|
1
|
48
|
49
|
1
|
|
9H
|
27
|
50
|
|
11H
|
25
|
49
|
|
2
|
7H
|
48
|
48
|
0
|
48
|
48
|
0
|
|
9H
|
48
|
48
|
|
11H
|
48
|
48
|
|
3
|
7H
|
22
|
20
|
2
|
0
|
0
|
0
|
|
9H
|
19
|
0
|
|
11H
|
19
|
0
|
|
LOPPE
|
1
|
7H
|
25
|
25
|
1
|
47
|
47
|
0
|
|
9H
|
24
|
47
|
|
11H
|
26
|
47
|
|
2
|
7H
|
3
|
3
|
0
|
3
|
3
|
0
|
|
9H
|
3
|
3
|
|
11H
|
3
|
3
|
|
3
|
7H
|
14
|
12
|
2
|
10
|
10
|
0
|
|
9H
|
10
|
10
|
|
11H
|
12
|
10
|
|
KIMBELY
|
1
|
7H
|
8
|
8
|
0
|
5
|
5
|
0
|
|
9H
|
8
|
5
|
|
11H
|
8
|
5
|
|
2
|
7H
|
29
|
29
|
1
|
40
|
40
|
1
|
|
9H
|
28
|
41
|
|
11H
|
30
|
39
|
|
3
|
7H
|
21
|
22
|
1
|
22
|
22
|
1
|
|
9H
|
22
|
23
|
|
11H
|
23
|
21
|
|
TELICO
|
1
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
2
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
3
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
POUDRIERE
|
1
|
7H
|
0
|
0
|
0
|
0
|
0
|
0
|
|
9H
|
0
|
0
|
|
11H
|
0
|
0
|
|
2
|
7H
|
13
|
13
|
1
|
0
|
0
|
0
|
|
9H
|
14
|
0
|
|
11H
|
12
|
0
|
|
3
|
7H
|
10
|
11
|
1
|
15
|
15
|
0
|
|
9H
|
11
|
15
|
|
11H
|
12
|
15
|
Figure N° 11 : HISTOGRAMME DE LA VARIATION
DU TAUX DE E. COLI POUR JUIN ET NOVEMBRE 2014
 D'après la figure N°10, nous observons trois (3)
tendances : D'après la figure N°10, nous observons trois (3)
tendances :
- Une augmentation au niveau du puits N° 1 de
abattoir ; du puits N° 1 de Loppe ; du N° 2 de Kimbely et
du N°3 de poudrière. Cet accroissement serait dû au maintient
des habitudes et comportements domestiques.
- Une décroissance au niveau des puits N°3 de
loppe ; N°1 de kimbely et même une chute du taux au niveau du
puits N° 3 de Abattoir ; N°2 de Poudrière ; dû
au fait que ces puits sont moins utilisés en novembre qu'en juin.
- Une stabilité au niveau des puits N° 1, 2, 3 de
Telico et N°1 de Poudrière.
La forte augmentation en Coliformes et E. coli pourrait
être expliqué par une pollution fécale d'origine animale ou
Humaine (fosse septique, élevage de bétail, utilisations des
déchets des animaux comme fertilisant pour les terres agricoles
avoisinant les puits).
Par conséquent, ces eaux de puits ne sont
recommandées pour la boisson en l'état mais peuvent l'être
sous certaines conditions dont entre autres faire bouillir l'eau et la
refroidir ou l'utilisation du Sur' eau.
Conclusion et suggestions
Cette étude réalisée sur la
détermination de quelques paramètres physico-chimiques et
microbiologiques des eaux des puits de la commune urbaine de Mamou a abouti aux
résultats ci-après :
Ø Au total, nous avons étudié les eaux
des puits traditionnels de cinq (5) quartiers de la commune urbaine choisis en
fonction de la population, des activités pratiquées, du taux de
desserte en eaux de la SEG et de la géographie ; pour un total de
quatre vingt dix (90) échantillons repartis en deux (2) lots dont
quarante cinq (45) en juin et quarante cinq (45) autres en novembre 2014.
Ø L'analyse physico-chimique nous a montré
que le pH (de 6,45 à 7,03), la conductivité (de 166.66
à 469,6), les MES (de 3 à 13.66 mg/l) et le fer total,
répondent aux normes de potabilité des eaux pour la plupart des
puits ; mais un pH souvent bas peut présenter un problème de
solubilisation des différents métaux toxiques (plomb, cadmium,
mercure).
Ø L'accroissement de la turbidité entre les deux
périodes (de 1.00 à 6.00NTU en juin et de 4.66 à 14.33NTU
en novembre) montre un fort risque de pollution microbiologique ;
Ø les eaux de Loppe, Kimbely et Poudrière sont
polluées par les nitrites du fait essentiellement des activités
humaines dont le rejet des eaux usées domestiques et des installations
sceptiques avoisinantes ;
Ø la pollution par les nitrates des eaux des puits
des quartiers Abattoir, Loppe et Kimbely est le résultat des
activités humaines notamment les pratiques agricoles. La consommation de
ces eaux devrait être interdite aux femmes enceintes et aux
nourrissons.
Ø Les résultats des analyses microbiologiques
montrent que presque tous les puits étudiés sont
souillés par les germes de contaminations microbiennes. La plupart des
différents puits échantillonnés présentent une
forte contamination par les germes recherchés (coliformes totaux, E.
coli) presque toutes les concentrations enregistrées sont
supérieures aux normes de l'OMS. En effet, les forts taux en coliformes
totaux et en E. coli enregistrés au niveau de la plupart des puits
peuvent être attribués aux mauvaises conditions d'hygiène
enregistrées dans la zone d'étude.
Ø La pollution microbiologique des eaux de puits est
très inquiétante car elle pourrait signifier une
insalubrité des eaux souterraines de la commune urbaine de Mamou.
Ø Les résultats montrent bien l'impact des
rejets d'eaux usées domestiques, le dépôt d'ordure
ménagères.
Ø La présence très élevée
des germes indicateurs de la contamination fécale, ainsi que la
présence d'autres germes responsables d'infections transmises par l'eau
pour la plupart des puits étudiés, constituent sans doute une
menace pour les habitants qui tirent l'eau nécessaire à la
majeure partie de leurs besoins à partir de ces puits.
Ø La contamination bactérienne des eaux de puits
pourrait être augmentée par des pollutions ponctuelles suite
à une mauvaise conception des latrines, une mauvaise évacuation
des eaux usées domestiques et en présence d'ordures à
coté des puits.
Ø En somme, les eaux des puits de la commune urbaine de
Mamou sont impropres à la boisson mais sont de qualité acceptable
pour l'usage domestique (cuisine, linge et autre nettoyage) ;
Ø Cependant les études doivent se poursuivre
pour surveiller l'évolution de la pollution des eaux de ces puits.
Ø Vu la forte teneur de certains éléments
(Coliformes Totaux, E. coli, nitrites, nitrates, phosphates,...) si rien n'est
fait le risque d'élévation de leurs teneurs est prévisible
et pour éviter la possibilité de tout risque sanitaire nous
suggérons :
Ø A la population,
· vu la densité démographique et
l'insalubrité qui règnent près de certains de ces puits,
d'établir un programme de nettoyage interne et externes de ces
puits,
· De supprimer les points de dépôt des
ordures prés des puits et d'effectuer la lessive loin de ces puits.
· L'utilisation du SUR `eau ou du Chlore à
l'échelle familiale dans le cadre de la boisson.
Ø Aux autorités,
· de renforcer la sensibilisation sur les
conséquences sur la santé de la boisson de ces eaux sans
traitement préalable ainsi que des règles d'hygiène.
· L'extension du réseau d'eau potable
· La conception d'un réseau d'assainissement pour
l'évacuation des déchets
· La protection des points d'eaux.
ANNEXE
Annexe
I carte de Mamou

III- photos lors de l'échantillonnage
 
 
Loppè
Loppè
 
Un puits de kimbely
Télico

REFERENCES ET BIBLIOGRAPHIE
REFERENCE ET BIBLIOGRAPHIE
[1] Contrôle des eaux de consommation humaine : Jean
Claude BOEGLIN 2005
[2] Production et traitement des eaux destinées à
l'alimentation : Emmanuel JESTIN. 2010
[3] Cours de microbiologie Générale : Alpha
Oumar DIALLO UGANC MaCBA Avril 2013
[4] Cours de chimie et microbiologie de l'eau : Dr Bley
Nimbalo GUEMOU UGANC-Mai 2005
[5] Etude de la qualité physico-chimique et
bactériologique des eaux de la nappe plio-quaternaire dans la region de
MEKNES (Maroc) : BELGHETI M.L, CHAHLAOUI A., BENGOUMI D., EL MOUSTAINE R.
larhyss journal ISSN 1112-3680 N°14 juin 2013, pp 21-36
[6] www. Google. Fr- Traitement de l'eau CNRS- France
consulté le 24/04/2014
[7] Détermination de quelques paramètres
physico-chimiques dans les eaux de puits de la commune de Matoto
(Conakry) : Maimouna DIALLO juin/2012 UNGANC
[8] Effet des conditions climatiques et anthropiques sur la
variation de la qualité de certains puits en milieu rural, cas de la
nappe phreatique du plateau de MEKNES (MAROC) : BELGHETI M.L, CHAHLAOUI
A., BENGOUMI D., EL MOUSTAINE R. Science Lib Editions Mersenne : vol 5
N° 131004 ISSN 2111-4706 du 04/10/2013
[9] Haut Commissariat aux Eaux et Forets et à la Lutte
Contre la Désertification HCEFLCD- MAROC 2007
[10] Détermination de quelques paramètres
physico-chimiques dans les eaux de puits de la commune de Coyah : BALDE
Salma Avril/2012 UGANC
[11] Evaluation de quelques paramètres physico-chimiques
des eaux de puits des environs de la décharge de Hamdanllaye
(Conakry) : Adama Guilavogui et Aminata TRAORE juin 2012 UGANC.
[12] Haut Commissariat aux Eaux et Forets et à la Lutte
Contre la Désertification HCEFLCD- MAROC 2006
[13] WWW. Google.fr Santé Canada ; santé de
l'environnement et du milieu de travail ; les chlorures consulté le
22/10/2014 à 2h36'
[14]- Nitrates et nitrites : groupe scientifique de l'eau,
Institut National de santé publique du Québec juillet 2013
[15] Effet des conditions climatiques et Anthropiques sur la
variation de la qualité des eaux de certains puits en milieu
rural ; cas de la nappe phréatique du plateau de MEKNES
(Maroc) : BELGHITI. L et al Scienceslib editions Mersenne Vol 5 N°
131004 du 04-10-2013 ISSN 2111-4706
[16]- california Environmental Protection Agency, 2011 ;
santé Canada 2012
[17]- Google, qualité et pollution des eaux
souterraines ; Jacques BEAUCHAMP, Université de Picardie Jules
Verne consulté le 29/09/2014 à 3h53'
[18]- GRASSHOFF.K Determinations of nitrate in sea water
analysis 1976
[19]- Google, prévention des risques : pollution,
qualité de l'environnement et santé- Ministère de
l'écologie, du développement durable et de l'énergie-
France. Consulté le 01/11/2014 à 23h49'
[20]- Google, sources de pollution des eaux souterraines, water
Treatment Solutions, LENNTECH consulté le 11/09/2014 à 22h58'
[21] - Cours de pollution et traitement des eaux
usées : Dr Mamadou Bailo DIALLO, UGANC PhD, MC mars 2013
[22]- Pollution des eaux souterraines-ALPHA-AWWA-WEF, 1998
[23]- Google, Encyclopedia of Food Sciences and Nutrition,
Second Edition 2003 4136-4141 Nitrates and Nitrites consulté le
01/11/2014 à 3h29'
[24]- Google, Pollution et Dépollution des nappes d'eau
souterraine, Jacques BEAUCHAMP, Université de Picardie Jules
Verne ; consulté le 24/11/2014 à 6h48'
[25]-
www.foutapedia.com: Mamou
consulté le 20/10/14 à 23h45'
-[26] Google : Guide pratique : Echantillonnage des
eaux souterraines. Office fédéral de l'environnement, des forets
et du paysage. CANADA consulté le 24/11/2014 à 16h58'.
[27] Pollution physico-chimique et microbiologique de l'eau des
puits de la commune urbaine d'Abomey-calavi au Benin en 2009 : C. DEGBEY
et al. Int.J.Biol.chim.Sci 4(6) : 2257-2271 Décembre 2010 ISSN
1991-8631.
|
|



