|

Accès aux Traitements :
De l'engagement des firmes pharmaceutiques
aux revendications des activistes.
Mémoire
Diplôme Universitaire SIDA
Eddy Basset

Sommaire
1 - Introduction 1
2 - Le VIH infection planétaire .3
3 - Les firmes engagées dans le VIH .7
4 - Ce que les laboratoires 13
5 - Histoire chronologique de l'accès aux
antirétroviraux 27
6 - Accès universel : les avancées 39
7 - Obstacles à l'accès universel 48
8 - Des initiatives encourageantes 64
9 - Conclusion 72
10 - Résumé 74
11 - Références bibliographiques 75
12 - Remerciements 76

1 - Introduction
« In AIDS we trust ,> dans le texte « dans le
SIDA nous prospérons ,> est une formule détournée de la
célèbre devise « In God we trust ,> qui figure sur les
fameux billets verts. Je trouve qu'elle illustre parfaitement ce sujet car, il
est évident que c'est le regard négatif que posent la plupart des
gens sur les firmes pharmaceutiques (souvent d'ailleurs entretenu par les
médias) qui selon eux « s'engraissent ,> sur la souffrance du
monde. Je travaille dans l'industrie pharmaceutique depuis 1986. Tout d'abord
chez Wellcome dans le cadre du lancement de l'AZT. Puis chez GlaxoWellcome et
enfin GlaxoSmithKline. J'ai pu ainsi présenter les différents
antirétroviraux de ce grand groupe britannique et côtoyer le
milieu VIH en France. Depuis 2001, je travaille pour la « biotech ,>
californienne Gilead Sciences, toujours dans ce domaine, ce qui me permet
d'avoir suivi une partie de l'histoire du VIH. Mais avant d'être un
représentant d'une compagnie pharmaceutique, je suis avant tout un
citoyen du Monde. Dans mon cercle d'amis le VIH aussi s'est invité. De
ce fait, je ne suis pas indifférent aux critiques qui sont
formulées à l'encontre des laboratoires, surtout en
matière de politique d'accès aux antirétroviraux pour les
pays à faibles revenus. Encore moins, lorsqu'il s'agit du groupe pour
lequel je travaille. Pour autant, mon but n'est pas d'être l'avocat
aveugle et inféodé de l'industrie, mais de tenter d'être
objectif. J'ai souhaité aborder les différents aspects, des
laboratoires qui travaillent dans le VIH et qui annoncent des « access
program ,>, aux critiques des activistes en passant par des exemples de
certains gouvernements qui illustrent malheureusement que les
responsabilités sont partagées. L'Afrique du Sud, l'Inde, mais
aussi des pays comme la Chine ou la Russie démontrent que l'accès
aux traitements ne dépend pas seulement des laboratoires, mais aussi
d'une véritable volonté des gouvernements. 840 millions de
personnes endurent la faim. 300 000 enfants meurent chaque jour de maladies qui
peuvent être évitées. Les raisons ne sont pas seulement
liées à l'absence de traitements. Rappelons que 1 milliard de
personnes n'ont pas accès à l'eau. C'est ce que le Professeur
Fauci disait déjà il y a quelques années en ces termes :
«si prendre une trithérapie consistait à boire un verre
d'eau n'oublions pas qu'actuellement dans le Monde nombreux sont ceux qui n'y
ont pas accès,>. A travers ce mémoire, l'occasion m'est
offerte de faire le point sur ce sujet particulièrement sensible et
néanmoins complexe. « L'activisme ,> dans ce mémoire
n'est vu qu'au travers du prisme : bataille pour les antirétroviraux et
plus particulièrement affrontement avec les laboratoires. Aussi
Dominique Blanc (TRT5) à raison de rappeler que l'activisme est bien
plus grand : bataille pour les droits, soutien, interactions avec les
structures nationales et internationales, information et prévention
auprès des publics vulnérables et des personnes touchées
par le VIH. Un regret : j'aurais aimé rencontrer plus d'acteurs tant au
sein des firmes que des associations de patients pour confronter les positions
des uns et des autres, mais mon éloignement géographique et mon
manque de temps libre ne m'ont pas permis de le faire. Je le regrette, et
à défaut, je propose bien modestement une synthèse sur ce
sujet qui n'en demeure pas moins passionnant et pleinement d'actualité
J'espère que ce travail contribuera à une meilleure connaissance
de ce qui reste un des enjeux majeur du millénaire.
« Quand les historiens étudieront notre
époque,
ils verront que notre civilisation a
dépensé
des millions de dollars pour éduquer les
gens
à propos du fléau du virus VIH et du
SIDA,
qui a déjà emporté 25 millions
de vies
et pourrait infecter encore 100*
millions
de personnes dans les 8 années à
venir.
Mais ils ne trouveront pas
civilisée
notre incapacité à traiter 95
%
des gens touchés par la mala
die.
Alors même que la
médecine
permet de transformer le SIDA
d'une sentence de mort en une maladie chronique
(...),
cette rétention de traitements
apparaîtra
aux historiens futurs aussi
moyenâgeuse
que la saignée ».
* 3 à 4 millions par an feraient 25 à
40 millions dans les 8 prochaines années
Bill Clinton. New York Times 2002

06/06 f
2 - Le VIH infection planétaire

Adultes et enfants vivant avec le VIH, estimations
2005

Amériquedu Nord
1,3 million
[770 000 - 2,1 millions]
Caraïbes 330 000
[240 000
Amérique latine ,1,6 illi million
[1,2 - ,2,4 mill millions]
-420 00]000]
Afrique du Nord & Moyen-Orient
440 000
Europe occidentale
et centrale
720
000
[550 000 -950 000]
[250 000
Afrique subsaharienne
24,5 lmillions
[21,6 -,27,4 millions]
-720 000]
Europe orientale & Asie centrale , 1,5
million
,[1,0 --,2,3 il
millions]
Asie du Sud & du Sud-Est , 7,6 ili
millions
[5,1 -11,7 millions]
Asie de l'Est 680 000
[420 000 -1,1 million]
Océanie 78 000
[48 000
-170 000]000]
Total : 38,6 (33,4 - 46,0) millions
3
L'OMS (Organisation Mondiale de la Santé) et l'Onusida
(programme commun des Nations unies sur le VIH/sida) publient chaque
année un rapport épidémiologique de suivi du sida dans le
monde, intitulé le Point sur l'épidémie de sida.
Celui de novembre 2005 estime à environ 40,3 millions le nombre de
personnes vivant avec le VIH ou un sida déclaré, dont 17,5
millions de femmes et 2,3 millions d'enfants et de jeunes de moins de 15 ans.
Le nombre de personnes nouvellement infectées en 2003- 2004 est
d'environ 4,9 millions : ce chiffre annuel de nouvelles infections est stable
depuis 2001, signe d'une difficulté à mettre en place des moyens
de prévention efficaces ou signe que l'on atteint un plateau dans le
développement de l'épidémie. Ces chiffres manquent
toutefois de précision, étant donné le décalage
entre la réalité de l'épidémie et les
déclarations officielles, en particulier dans les pays où le
système sanitaire est déficient. La face visible de
l'épidémie est représentée par le sida
déclaré, mais la séropositivité passe souvent
inaperçue -- en effet, il s'écoule en moyenne une dizaine
d'années entre la contamination et la maladie effective. L'OMS et
l'ONUSIDA considèrent que, dans le monde, moins de 10 % des personnes
séropositives chez lesquelles le sida n'est pas encore
déclaré sont au courant de leur séropositivité (un
peu moins de 50 % en France). Ainsi, le nombre total de cas dans le monde est
considéré par l'OMS et l'ONUSIDA comme compris entre un minimum
de 34,5 millions et un maximum de 45,3 millions de personnes, le chiffre de
40,3 millions étant une moyenne.

La situation est dramatique en Afrique subsaharienne : entre
23,8 et 28,9 millions de personnes sont touchées -- soit plus des deux
tiers des cas de la planète, et près d'un million de cas de plus
qu'en 2003. Selon la Banque Mondiale, le nombre de décès dus au
sida en Afrique dépassera bientôt le nombre de victimes - 20
millions - de l'épidémie de peste qui a ravagé l'Europe de
1347 à 1351. A la différence près qu'à cette
époque on ne savait pas faire face au drame. Les moyens de
dépistage et de traitement y font défaut et les politiques de
prévention sont difficiles à évaluer. Les statistiques
révèlent, pour première conséquence, une chute
considérable (environ quinze ans) de l'espérance de vie dans
l'ensemble de l'Afrique subsaharienne. Le mode de transmission y est
essentiellement hétérosexuel, les femmes étant plus
vulnérables que les hommes, et la maladie frappe de plein fouet les
jeunes adultes et les enfants (transmission de la mère à l'enfant
au cours de la grossesse).
La situation est aussi très préoccupante en Asie
du Sud et du Sud-Est (7,4 millions de personnes). En Inde et en Chine, le sang
contaminé est un réservoir identifié. Gravité de la
situation également en Amérique latine et Caraïbes (2,1
millions). L'épidémie de sida est également très
importante en Asie de l'Est (870 000 personnes vivent avec le VIH) -- c'est
l'une des régions du monde qui a enregistré l'une des plus fortes
progressions de l'épidémie (environ 50 % de cas de plus en 2004
qu'en 2002). L'activité du commerce sexuel et la consommation croissante
de drogues injectables sont les facteurs principaux auxquels cette situation
est imputable. Dans les pays d'Europe de l'Est et d'Asie centrale,
l'épidémie a également explosé au cours des
dernières années, essentiellement chez les consommateurs de
drogues injectables ; aujourd'hui, environ 1,6 million de personnes sont
infectées. Mais les données collectées se situent
probablement bien en deçà des chiffres réels, en raison
des déficiences des réseaux de surveillance
épidémiologique dans la plupart de ces pays. Il en va de
même pour les pays d'Afrique du Nord et du Moyen-Orient -- régions
pour lesquelles le rapport 2005 fait état d'un nombre total de personnes
vivant avec le VIH compris entre 230 000 et 1,4 million (en moyenne 510
000).
En Europe occidentale, quelque 720 000 personnes sont
infectées ; en Amérique du Nord, probablement 1,2 million. Dans
tous les pays à revenu élevé, l'OMS et l'ONUSIDA notent
d'une part une baisse de la mortalité en raison de l'accès aux
traitements, mais d'autre part un relâchement de la vigilance de la
population sexuellement active (homosexuelle comme
hétérosexuelle) vis-à-vis du sida, et s'inquiètent
de la très
probable reprise de vitesse de l'épidémie
à court terme si l'accent n'est pas à nouveau mis rapidement sur
la prévention. Autre point de préoccupation, en Europe de
l'Ouest, et aux USA des cas de résistance du virus aux traitements
antiviraux ont été signalés chez des patients nouvellement
infectés.
Selon les estimations de l'OMS et l'ONUSIDA, 750 000 enfants
seraient morts du sida en 2005. Plus de 15 millions d'enfants sont orphelins du
fait du décès d'au moins un de leurs parents à cause du
VIH. Ces chiffres ont considérablement augmenté depuis les
années 90, pour plusieurs raisons dont les trois principales sont sans
doute :
- une prise de conscience tardive.
- le « fossé » préventif entre les
pays développés, ou le taux de transmission mère enfant
est d'environ 1% grâce à la prophylaxie médicamenteuse et
à l'éviction de l'allaitement maternel, et les pays du Sud,
où ce taux est compris entre environ 2 à 6 % là ou les
programmes de prévention de la transmission mère enfant (PTME)
sont fonctionnels et optimaux, et 25 à 40 % là ou il n'y a pas de
programme incluant la grossesse, l'accouchement et l'allaitement donc pas de
traitement antirétroviraux.
- à l'échelle mondiale, seulement 9 % des femmes
enceintes ont accès à un dépistage du VIH, incontournable
pour toute possibilité de prévention. Le fossé est encore
plus large au plan curatif : alors que l'accès au traitement progresse
pour les adultes, les centres de prise en charge sont encore peu nombreux pour
les enfants (au Lesotho par exemple, il n'y a qu'un seul pédiatre pour
l'ensemble du pays !), pour lesquels les obstacles sont divers, incluant
l'absence de formes pédiatriques accessibles des
antirétroviraux.


06/06 f
3 - Les firmes engagées dans le VIH / SIDA
5 juin 1981 sous le titre « cas de pneumocystose - Los
Angeles » à la page 2 du volume 30, fascicule 21, un numéro
du MMWR (Mortality Morbidity Weekly Report) qui deviendra historique pour avoir
été le premier au monde à parler d'une maladie que
l'humanité allait bientôt découvrir avec terreur sous le
nom de SIDA.

25 ans d'infection VIH

50 45 40 35 30 25 20 15 10 5
0

4 In Africa, a heterosexual AIDS epide,,ic is
revealed
5 The first HIV antibody test beco,,es
available
6 Global Network of People living with HIV/AIDS (GNP+)
(then International Steering Co,,,,ittee of People Living with HIV/AIDS)
founded
8 The first therapy for AIDS -
1 2 3456
7
8
9
10
11
12
13
nfection Infection
VIH
e saharienne
Orphelins en Afrique Sub-
14
15
16
9 In 1991 -1993, HIV prevalence in young pregnant
wo,,en in Uganda and in young ,,en in Thailand begins to decrease, the first
,,ajor downturns in the epide,,ic in developing countries
10 Highly Active Antiretroviral Treat,,ent
launched
11 Scientists develop the first treat,,ent regi,,en to
reduce ,,other-to-child trans,,ission of HIV
12 UNAIDS is created
13 Brazil beco,,es the first developing country to
provide antiretroviral therapy through its public health syste,,
14 The UN General Asse,,bly Special Session on HIV/AIDS.
Global Fund to fight AIDS, Tuberculosis and Malaria launched
15 WHO and UNAIDS launch the '3 x 5' initiative with the
goal of reaching 3 ,,illion people in developing world with ART by
2005
16 Global Coalition on Wo,,en and AIDS
launched
1980 1985 1990 1995 2000 2005
Quatre ans après qu'un médecin de Los Angeles
eut diagnostiqué le premier cas de l'épidémie, deux ans
après que des biologistes de l'Institut Pasteur de Paris eurent
découvert le rétrovirus responsable du SIDA, des fonctionnaires
de la santé publique et des chercheurs de l'industrie pharmaceutique se
réunissaient pour jeter les bases d'un protocole clinique en vue de
l'expérimentation de la première arme inventée contre le
fléau mortel - l'AZT.
Aucun produit n'avait encore été testé
avec succès contre une maladie aussi complexe et dont on savait si peu
de choses. Ensuite, en raison des nombreuses inconnues concernant l'AZT
lui-même. Son mode d'action n'avait pu être totalement
élucidé et ses effets toxiques n'avaient été
mesurés que pendant quelques courtes semaines sur des animaux. L'AZT
(utilisé en vain dès 1964 pour leurrer des cellules
cancéreuses et casser le mécanisme de leur reproduction
anarchique) n'était pas un produit très courant : il fallait une
matière première aussi rare que du sperme de hareng pour obtenir
la thymidine qui en était l'un des composants.
L'histoire tragique du SIDA ne devra pas oublier que les
premiers milligrammes d'AZT administrés à des humains eurent pour
receveurs ses trois principaux inventeurs, à commencer par le vice
président du laboratoire Wellcome en personne. Comme il n'existait ni
comprimés ni gélules, il avait été contraint de
dissoudre dans un jus de fruit la poudre de sperme de hareng. L'essai clinique
sur 21 malades qui suivra épuisera, jusqu'au dernier gramme le stock
d'AZT constitué au printemps précédent par l'achat de
toutes les réserves mondiales de sperme de hareng. Les chimistes de
Wellcome n'avaient pas encore réussi à reproduire en laboratoire
la fameuse substance contenue à l'état naturel dans la semence de
ce poisson de mer (la synthèse de la thymidine était d'une grande
complexité). A l'automne 85, la mise à disposition de 50
kilogrammes de sperme de hareng et surtout, l'imminente synthèse de la
thymidine par les chimistes de Wellcome permettaient d'envisager une production
massive d'AZT en vue de sa mise rapide sur le marché. Ce sera le cas
deux ans plus tard.
Le médicament devait pourtant faire l'objet de
critiques à commencer par son prix jugé exorbitant, voire
scandaleux. Aux Etats-Unis, ou 18 millions de citoyens ne
bénéficiaient d'aucune protection sociale, la moitié des
victimes du SIDA n'avaient pas les moyens de s'offrir un traitement dont le
coût annuel s'élevait à 6500 dollars soit près de 40
000 francs. Au cours de l'été 89, des activistes
s'enchaînèrent aux balcons de la bourse de Wall Street pour
dénoncer les bénéfices spectaculaires du laboratoire
Wellcome dont les actions connaissaient des hausses jugées immorales en
raison du contexte dramatique de l'épidémie. L'un des
pères de l'AZT dû comparaître devant une commission du
congrès « pour y subir le feu roulant de questions parfois hostiles
» et expliquer que le prix du médicament se justifiait par
l'importance des investissements qu'avaient nécessités sa mise au
point et son expérimentation continue sur des milliers de malades.

L'annonce que le laboratoire allait distribuer gratuitement
l'AZT aux enfants atteints par le SIDA ne fit pas taire toutes les
polémiques. Au printemps 86 Wellcome décida de débuter un
essai avec 281 patients. 144 sous AZT et 137 sous placebo. Immédiatement
les 10 000 américains victimes de l'épidémie partirent en
croisade contre Wellcome pour un arrêt immédiat de cet essai et la
distribution immédiate de l'AZT à tous les malades, soutenu par
un battage médiatique. On reprochait même à Wellcome que si
il n'était pas en mesure ou ne voulait pas fabriquer suffisamment d'AZT,
il fallait que le gouvernement fédéral signe des contrats avec
d'autres laboratoires et distribue gratuitement le médicament.
Dès 96 les revendications pour les pays du Sud seront les
mêmes.
Le monopole de Wellcome n'aura duré que cinq ans avant
que d'autres laboratoires pharmaceutiques se lancent également dans
l'aventure et décident de capter ce nouveau marché : Bristol
Meyer Squib, ROCHE, Merck Sharp Dohm & Chibret, Boehringer Ingelheim,
Abbott rejoints plus récemment par les « biotechs » Gilead et
Tibotec. En 2007 l'arsenal thérapeutique s'est considérablement
renforcé avec vingt quatre antirétroviraux commercialisés
et trois en cours d'enregistrement.

Refining Antiretroviral Regimens:
Complications métaboliques chez les patients
infectés par le VIH
1987 19881989 1990 199119921993 1994 1995 1996 1997 1998 1999
2000 2001 2002 2003 2004 2005 2006
25
20
15
10
5
0
ZDV
ddC d4T
ddI
SQV 3TC
RTV IDV NVP
NFV DLV
EFV ABC
APV
LPV/ RTV
TDF
ATV FPV ENF FTC
DRV
TPV
Year
Figure does not include fixed-dose combinations.
clnicaoptions.com/hiv
Timeline of ARV Development
AIDS 1 st reported
ddI
ddC d4T
3TC, SQV
RTV, IDV, NVP
NFV, DLV, COM , SQV-gc
EFV, ABC
APV
LPV/RTV, ddI-EC, ZDV/3TC/ABC
TDF
EFV-600, 3TC-300, d4T-XR
T-20, NFV 625, ATV, FTC, FPV ABC/3TC, TDF/FTC, ddI generc SQV
500, TPV, ZDV generic , LPV/RTV tabs
DRV, TDF/FTC/EFV
clinicaloptions.com/hiv
ZDV
Refli Reformulations Cofli Coformulations
En 2007, les cliniciens des pays industrialisés
bénéficient de molécules dont les différents modes
d'actions permettent d'agir sur cinq étapes du cycle de
réplication du virus VIH : les inhibiteurs d'entrée (au compte
goutte car aucun n'a d'AMM), les inhibiteurs de fusion (un seul disponible),
les inhibiteurs de la reverse transcriptase, les inhibiteurs de
l'intégrase (un seul en cours d'enregistrement), et les inhibiteurs de
la protéase. Les régimes de première ligne de traitement
(source 2003 - 2005) dans le Monde sont particulièrement inégaux
en fonction des continents :
· Amérique du Nord : 59
· Amérique du Sud : 11
· Europe de l'Ouest : 47
· Asie : 3
· Afrique de l'Est : 3
· Sud de l'Afrique : 3


Schémas Première Ligne:
nouvelles recommandations
OMS Toronto Août 2006
ZDV or d4T*
TDF or ABC
3TC ou FTC
NVP
EFZ
En France, les cliniciens disposent de recommandations de
traitement depuis 1996 (Rapport Dormont devenu en 1999 le Rapport Delfraissy et
enfin en 2006 le Rapport Yeni). Ces recommandations sont revues et
adaptées tous les deux ans en fonction des nouvelles connaissances et
des avancées thérapeutiques.

Associations à utiliser de préférence
En Afrique les cliniciens disposent de recommandations seulement
depuis 2003 réactualisées par l'OMS en 2006. Les options
thérapeutiques sont bien plus limitées.


Number of people on antiretroviral therapy
in -
lowand middle-income ,countries, -20022005
North Africa and the Middle East Europe and Central Asia
East, South and South-East Asia Latin America and the
Caribbean Sub-Saharan Africa


1400
1200
1000
800
600
400
200
0
People
receiving therapy
(thousands)
End Mid- End Mid- End
Mid- End
2002 2003 2003 2004 2004 2005 2005
Source: WHO/UNAIDS (2005). Progress on global access to HIV
antiretroviral therapy: An update on «3 by 5.»
06/06 f
4 - Ce que les laboratoires annoncent en terme de
programmes d'accès aux traitements
Au regard du début de l'épidémie et des
dates de commercialisations des premières molécules actives, ce
qui retient l'attention, c'est que l'engagement de l'industrie pharmaceutique
dans les pays en voie de développement ou à faible revenus est
décalé dans le temps. Le premier à s'être
engagé dans un (( access program >> institutionnalisé est
Wellcome (GSK) en 1992 avec ((Positive action>> soit 15 ans après
le début de l'épidémie et 5 ans après la
commercialisation de L'AZT. BMS emboîtera le pas dès 1999. A ce
jour, tous les laboratoires proposent un (( access program >>. En plein
ATU (autorisation temporaire d'utilisation) TIBOTEC annonce déjà
que sa deuxième molécule TMC125 sera disponible à travers
son programme d'accès aux traitements.
Il paraît évident qu'en 2007 aucun laboratoire
pharmaceutique ne semble pouvoir se dispenser de son (( access program
>>. Sans remettre en cause ce qui a été fait, est-ce
à la hauteur des attentes des pays du Sud ou au moins à la
hauteur de leurs possibilités financières. Act Up à ce
propos n'hésitait pas à communiquer les ventes des
différents groupes pharmaceutiques.
Laboratoire
|
Chiffre d'affaire
2000
|
Bénéfices
2000
|
Bénéfices
2002
|
Médicament
|
Ventes
2000
|
Ventes 2003
|
Glaxo-SmithKline
|
26 000
|
4 750 6 600 Retrovir 86,4 60,5
|
|
|
|
|
Epivir
|
430,5
|
311
|
|
|
|
|
Combivir
|
818
|
1168
|
|
|
Ziagen 210 427,4
|
|
|
|
|
Trizivir
|
28,8
|
294
|
|
|
|
|
Agénérase
|
89
|
209
|
|
|
|
|
Total
|
1 656
|
2 515
|
ROCHE
|
29 600
|
6 500 10 200 Viracept 423 325
|
Merck & C°
|
40 000
|
6 900
|
8 000
|
Crixivan
|
560
|
520
|
BMS
|
21 700
|
4 700
|
5 200
|
Zérit
|
618
|
838
|
|
|
Videx 183 309
|
Abbott
|
13 700
|
2 800
|
3 400
|
Norvir
|
123
|
105
|
|
|
|
|
Kaletra
|
31
|
300
|
Roche
|
16 600
|
Invirase 198 169
|
Boehringer
|
|
Ingelheim
|
|
Viramune
|
199
|
260
|
|
|
Act Up allait même plus loin en mettant en
parallèles les bénéfices des laboratoires et le PIB
(Produit Intérieur Brut) de certains pays particulièrement
touchés par le VIH/SIDA.
Publication mars 2001 dans Action 72
« L'industrie pharmaceutique est la plus rentable au
monde, et l'une des plus riches. Pour mieux comprendre le rapport de force qui
existe entre cette industrie et les gouvernements africains, il suffit de
comparer le poids économique de ces entreprises avec celui des Etats qui
tentent de lutter contre leur pouvoir absolu. Les bénéfices 2000
de Merck, toutes pathologies confondues, sont équivalents au produit
intérieur brut (PIB) du Congo (7 milliards de $).Les
bénéfices 2000 de ROCHE sont équivalents au PIB de
l'Ethiopie (6,5 milliards de $). Ceux de BMS équivalent au PIB du Gabon.
Ceux d'Abbott au PIB du Mali. L'Ouganda, un des premiers pays à avoir
mis en place un accès aux traitements contre le sida, a un PIB
équivalent aux bénéfices prévus en 2002 pour
Glaxo-Smithkline (6,3 milliards de $). Le Sénégal, qui vient de
négocier une réduction de prix avec les grandes compagnies
pharmaceutiques, a un PIB équivalent aux bénéfices 2000 de
Glaxo-Smithkline (4,8 milliards de $).Le fossé est encore plus criant
quand on voit que les ventes 2000 du médicament
Zérit® (d4T), produit par BMS, sont équivalentes
au PIB du Cap Vert, celles du Videx® (ddI, produit par BMS) au
PIB des Comores, celles de Combivir® (combinaison d'AZT et de
3TC en un seul médicament produit par GlaxoSmithkline) au PIB du
Lesotho. Pour finir, les ventes totales de médicaments anti-VIH de
Glaxo-Smithkline sont équivalentes au PIB du Tchad (1,6 milliard de $)
>>.
N'est-ce pas aussi un moyen comme un autre de communication
permettant de redorer le blason. Un prétexte pour se donner « bonne
conscience >>. La mode actuellement est au commerce équitable. Des
sociétés comme McDonald, Accor, Nestlé embrassent ce
nouveau courant pour « re-lifter >> leur image très
malmenée et parfois même faire oublier leur politique salariale
fortement décriée. Est-on dans la même stratégie en
ce qui concerne « l'access program >> ?
L'ONUSIDA, l'Organisation Mondiale de la Santé,
l'UNICEF, l'UNFPA, la Banque Mondiale et des laboratoires de recherche
pharmaceutique (Boehringer-Ingelheim, Bristol-Myers Squibb, F. Hoffmann-La
Roche et GlaxoSmithKline, et plus tard Abbott Laboratories et Gilead Sciences)
créent en mai 2000 Accelerating Access Initiative (AAI) L'objectif
commun consistait à trouver des moyens d'élargir l'accès
tout en garantissant une utilisation rationnelle, abordable, sûre et
efficace des médicaments destinés aux maladies liées au
VIH/SIDA. Alors justement, que font les laboratoires.

L'américain Abbott a opté pour un « fond
» sous couvert de la création en 1951 d'une société
Illinoise à but non lucratif et philanthropique. Son budget, programmes
humanitaires et d'assistance aux patients, actions sociales et dons de
médicaments aux malades du SIDA, totalise plus de 300 millions de
dollars (contre 225 millions de dollars en 2003). Son programme d'assistance
aux patients (PAP) délivre un accès gratuit à la
médecine à des individus à faibles revenus sans assurance
médicale ou aide gouvernementale. Ainsi, en août 2005 des milliers
de patients Illinois ont bénéficié du partenariat de
sociétés, fondations et institutions. Depuis son lancement en
avril, ce programme a été délivré à 600 000
personnes.
Depuis 2001, Abbott procure ses antirétroviraux
à prix coûtant (500 dollars par patient et par an) en Afrique et
dans les pays en développement. Kaletra est disponible à hauteur
de 1000 dollars par an dans plus de 40 pays aux revenus faibles ou
intermédiaires.
Toujours dès 2001, Abbott a contribué à
l'ouverture d'une clinique pédiatrique en Roumanie permettant une baisse
spectaculaire de la mortalité dans ce centre de 90 % en 3 ans. Depuis,
d'autres expériences de ce type se sont mises en place en Afrique comme
au Malawi. Depuis 2001, plus de 600 000 enfants et leurs familles ont
bénéficiés des services d'Abbott.
En 2002, Abbott et le gouvernement de Tanzanie ont
formé un partenariat public-privé unique. Il est soutenu par
l'organisation Axos - spécialisée dans l'encadrement des
systèmes de santé à l'attention des pays en
développement. Cette initiative à pour objectif de moderniser le
système de santé, des équipes soignantes aux patients.
En plus d`un hôpital de référence dans la
capitale, 80 hôpitaux ou centres de soins en milieu rural ont
été incorporé dans ce projet ce qui représente un
investissement de 44 millions de dollars.
Abbott a investi 100 millions de dollars sur les cinq
dernières années à des programmes d'accès aux
antirétroviraux en Afrique et autres soutiens aux malades et à
leurs familles.

Bristol Meyer Squib / BMS
En juin 2005, BMS annonce la création d'un corps
spécial de pédiatres, en vue de l'envoie de 250 médecins
en Afrique afin de traiter quelques 80 000 enfants atteints du SIDA dans les 5
années à venir. A cette opération s'ajoute la construction
de quatre nouveaux « centres d'excellence » ou cliniques pour enfants
atteints du VIH pour un montant total de 40 millions de dollars. En
parallèle, BMS annonce la réduction des prix des formulations
pédiatriques de ses médicaments anti-VIH dans les pays moins
développés, afin d'accroître l'accès aux
traitements.
Ce dernier programme s'inscrit aussi dans la
continuité des opérations engagées en Afrique de l'Ouest
autour d'un plan d'actions humanitaires à cinq ans, mis en place par BMS
et par sa fondation en 1999 et dénommé « Sécuriser le
futur ». Pour la petite histoire, cette initiative aurait vu le jour suite
à un dîner de charité où Kofi Ahnan - marié
tout comme le PDG de BMS à une suédoise - lui aurait
manifesté son exaspération quant à l'absence d'implication
de ce géant pharmaceutique en Afrique. Doté d'une enveloppe
initiale d'environ 100 millions de dollars, passée à 150 millions
de dollars en 2005, ce plan vise à bâtir toute une série
d'opérations innovantes et reproductibles en matière de prise en
charge des mères et des enfants atteints du SIDA dans une dizaine de
pays du continent noir. Il faut noter que c'est le programme le plus important
après celui de la Fondation Mélinda & Bill Gates. Les
programmes incluent entre autres, l'éducation du public à la
prévention, la formation de médecins et autres personnels
médicaux, des stratégies de soins basées sur les domiciles
des malades, des interventions pour porter secours aux orphelins et autres
enfants vulnérables, la recherche clinique et enfin les soins
médicaux. Au fil des années, cette initiative, la première
et la plus vaste de ce style émanant d'un groupe pharmaceutique,
basée sur un partenariat public-privé, s'est élargie
à de nouveaux pays de l'Afrique du Sud.

Gilead Sciences

Depuis 2003, Gilead se préoccupe également de
l'accès de ses molécules dans 107 pays émergents et a
ainsi contribué à la mise sous traitement de plus de 50 000
patients années pour un montant de plus de 250 millions de dollars. Il
s'est également investi dans plus de 20 essais qui ont concernés
plus de 10 000 patients en Asie, en Afrique et en Amérique Latine. Ces
essais concernent des évaluations thérapeutiques et de la
recherche dans les domaines de la prévention des accidents d'exposition
au virus VIH, la prévention de la transmission materno-foetale et les
gels vaginaux microbicides contenant du Tenofovir. A ce propos, en
décembre 2006, Gilead a passé un accord avec l'International
Partnership for Microbicides (IPM) et Conrad pour le développement, la
fabrication et en cas d'efficacité démontrée, la
distribution pour les pays à faibles ressources d'un microbicide
contenant du Ténofovir. Gilead a octroyé ses droits
d'exploitation du TDF, mais néanmoins il a provisoirement
contribué à la fabrication en vue des essais qui se mettent en
place dans l'attente d'un relais par un fabricant de
génériques.

Sa politique de prix est basée sur le poids
économique de chaque pays et sur leur possibilité de paiement.
Comme les autres firmes, Gilead a segmenté la planète en
différentes catégories en fonction de leurs ressources. La base
de cette politique de prix repose aussi sur le GNI ou Gross National Income per
Capital. Les pays à faibles revenus sont ceux dont le GNI est < 825
dollars, et ainsi de suite. Revenus moyens 826 - 2999 dollars, revenus
supérieurs 3000 - 10065 dollars et enfin hauts revenus 10066 dollars et
plus.
Gilead souligne que la propriété intellectuelle
est importante pour la viabilité d'un développement continu des
médicaments et devrait être utilisée de façon
responsable et appropriée. Si Gilead ne finance pas la protection
intellectuelle pour bloquer la fabrication des génériques ou leur
distribution dans les pays les moins développés, il
s'appuie sur elle pour protéger les marchés ou
il pense devoir bénéficier d'un retour sur investissement en
matière de recherche et développement. Pour Gilead, la
reconnaissance de la propriété intellectuelle ainsi qu'une
politique tarifaire responsable basée sur la capacité relative
d'un pays à payer ses médicaments permet de poursuivre
l'innovation médicale dans le domaine du VIH et au-delà.
La distribution du Viread et du Truvada dans les pays du Sud
à faible revenus est donc orchestrée par des laboratoires
génériques indiens (ils sont au nombre de 11) à qui Gilead
a offert une licence non exclusive pour un transfert de technologie et leur
permettre ainsi d'exporter Tenofovir dans 95 pays incluant la Thaïlande
à prix réduit. Pour l'Afrique subsaharienne c'est le laboratoire
sud africain Aspen Pharmacare qui depuis 2005 en est responsable. Pour les pays
à revenus moyens, supérieurs et élevés, c'est
Gilead ou ses partenaires qui se charge de la distribution. La combinaison TDF
+ FTC + EFV « Atripla » sera intégrée dans l'access
program de MSD.
Gilead Access Program Timeline
October
2001
Viread
approved
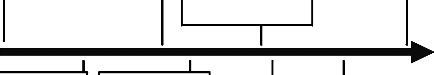
July 2004
37% reduction;
$0.82
per day
March 2005
Program expanded
to
97
countries;
Manufacturing
established
in Bahamas to
meet
increased demand
August 2006
First Indian
generics
licenses announced
April 2003
|
|
August 2004
|
|
|
August 2005
|
Gilead Access
|
|
Truvada added to
|
|
|
Truvada and Viread
|
Program begins;
|
|
Program; $0.99
|
|
|
prices reduced;
|
No-profit pricing;
|
|
per day
|
|
|
$0.87 and $0.57 per day
|
68 countries;
|
|
|
|
|
|
$1.30 per day
|
|
|
|
|
|
|
|
Aspen
|
|
|
partnership
|
|
|
announced
|
6
|
|
TIbotec / Johnson & Johnson / Janssen Cilag
Depuis 2000, Tibotec travaille avec Johnson & Johnson et
a déjà vendu à prix coûtant ou donné a 1.6
millions de patients des traitements à base de Miconazole nitrate 10 mg
pour le traitement des candidoses oropharyngées. En mars 2004,
l'International Partnership for Microbicides (IPM) a annoncé un accord
avec Tibotec - première collaboration dans le domaine des microbicides
entre une Major compagnie et un partenaire public/privé comme IPM. A
travers cet accord, Tibotec accorde gratuitement à IPM la licence pour
développer, produire et distribuer le TMC120 dans les pays à
faibles ressources. Approuvé par la FDA en juin 2006, la nouvelle
antiprotéase TMC1 14 est disponible pour les patients en échec
virologique aux USA et depuis peu en Europe. Tibotec a annoncé un
accès du TMC114 à prix réduit pour 100 pays. Des
autorisations pour les transferts de technologies et les licences sont à
l'étude.

Boehringer Ingelheim
Propose un programme pour la prévention de la
transmission mère enfant du VIH1. Cette initiative PMTCT (Prevention of
Mother-to-Child Transmission of HIV1) a débuté en 2000. Elle
comptabilise 150 programmes à travers 58 pays dans le Monde (Afrique,
Asie, Amérique Latine et Europe de l'Est). Au total plus de 75 000
couples mères et enfants ont été pris en charge
gratuitement.
Boeringher est associé dans le cadre du programme PTMTC
à Abbott. Ce dernier fournit un test rapide de dépistage du VIH1
et VIH2 baptisé « Determine » (plus de 65 millions de tests
distribués) alors que Boeringher lui dispense son antirétroviral
Viramune (Névira pine).
GlaxoSmithKline / GSK
GSK, s'est engagé dans la lutte contre le SIDA en
améliorant l'accès aux médicaments par une politique de
réduction des prix, par des donations et des participations à
tous les programmes des Nations Unies en matière d'accès aux
soins.

Positive Action est le programme
international à long terme de GlaxoSmithKline pour s'investir aux
côtés des séropositifs. Fondé en 1992, en
partenariat avec les associations de lutte contre le sida et des personnes
touchées, ce programme vise à soutenir la lutte contre le sida en
favorisant l'information, les soins et les initiatives de proximité.
Positive Action ne se limite pas à apporter un soutien
financier à des projets individuels. Il s'agit bien plutôt de
travailler en étroite collaboration avec les populations touchées
par l'infection à VIH et le sida pour s'assurer que les ressources
soient employées de façon productive et pour maximiser l'impact
collectif contre l'épidémie. Pour mettre en place une
réponse réellement efficace et mondiale au défi
posé par le VIH et le sida, ce programme comprend des partenariats d'un
genre nouveau entre toutes les parties en présence : des Etats à
la société civile, notamment les individus, les associations de
patients, les réseaux de personnes séropositives, les organismes
internationaux et le secteur privé. Dans les pays en
développement, Positive Action permet aux populations
locales d'optimiser leur réponse face à l'épidémie
en leur fournissant une information fiable, en partageant les
expériences et les savoirs entre les différentes organisations et
en donnant aux populations touchées par l'infection à VIH et le
sida les moyens de s'impliquer de façon dynamique dans les projets de
santé publique.
En Juin 2005, GSK a initié un partenariat Public /
Privé avec l'organisation AIDS Vaccine Initiative pour le
développement d'un vaccin contre le VIH. GSK et l'Institut Pasteur ont
annoncé une collaboration européenne sur cette
thématique.
GSK soutient 28 essais cliniques de partenariat dans les pays
en voie de développement et en Afrique impliquant plus de 18 000
patients. Quatre essais cliniques pédiatriques dans les pays en voie de
développement qui inclut 2400 enfants, notamment dans le cadre de la
prévention de la transmission mère/enfant par le VIH.
En parallèle de Positive Action, GSK France a
créé la Fondation GSK en 1998. Elle a pour mission
d'améliorer l'accès et la qualité des soins en Afrique
essentiellement. Depuis huit ans, elle a initié et soutenu 68 programmes
à travers 13 pays et a apporté une aide directement à des
équipes de soins d'un budget global de 4,9 millions d'euros.
Roche
Il n'existe pas de fondation, Roche privilégiant une
approche intégrée au développement même de son
groupe au plan international.
Ce laboratoire ne prévoit pas de renforcement ou de
dépôt de Brevets pour ses antirétroviraux dans les pays les
moins développés et en Afrique sub-saharienne, ni d'action contre
la vente de génériques de leurs propres antirétroviraux.
De même, sur ses traitements contre la malaria, le groupe Bâlois
renonce à ses brevets dans ces deux zones géographiques
(Bangladesh, Haïti, Afrique du Sud... soit 64 pays). En matière de
prix sur ces pays, Roche, comme d'autres membres de l'AAI a adopté une
politique de (( bénéfice zéro » pour les livraisons
directes depuis Bâle vers l'Afrique sub-saharienne et les pays les moins
développés. Se reposant sur les analyses de coûts
réalisées par MSF, les antirétroviraux de Roche sont
accessibles à des prix équivalents ou inférieurs à
ceux des versions génériques dans les pays en
développement (Inde, Vietnam... soit
9 pays) ou moyennement développés
(Brésil, Chine... soit 46 pays). Roche adapte sa politique de brevet et
de prix en fonction de la capacité de chaque pays pouvant ou non
contribuer à l'effort en terme d'accès aux soins et aux
médicaments. En résumé 64 % des pays sont concernés
par la politique de prix coûtant. Pour le reste 87 %
bénéficient d'un prix réduit et les 13 % restant paient le
prix standard. Pour aider à renforcer les capacités de production
dans les pays en développement dont l'Afrique sub-saharienne, Roche a
aussi lancé une nouvelle initiative en 2006 - (( the AIDS Technology
Transfer Initiative » - pour accompagner les fabricants locaux de
génériques à travers une expertise technique devant
conduire à la réalisation d'une copie de leur antiprotéase
Invirase.

Merck Sharp Dohme & Chibret / MSD
En 1997, Merck a lancé un effort de collaboration avec
le gouvernement roumain visant à fournir un accès aux soins
à des milliers d'enfants et d'adultes vivant avec le VIH/SIDA en
Roumanie, le pays d'Europe où l'on compte presque 60 % des cas de SIDA
pédiatrique. Aujourd'hui, le pourcentage de personnes soignées en
Roumanie peut être comparé à celui de n'importe quel pays
de l'Europe de l'Ouest ou des États-Unis, et un nouvel espoir est
né pour des milliers d'enfants et d'adolescents.
Depuis juillet 2000, MSD a développé et mis en
oeuvre le programme ACHAP (African Comprehensive HIV/AIDS Partnerships -
Partenariats globaux de lutte contre le VIH/SIDA en Afrique), partenariat
public-privé novateur qui s'inscrit dans la lutte contre le VIH/SIDA.
Avec le soutien financier de la Fondation Bill & Melinda Gates et en
étroite collaboration avec le gouvernement du Botswana, une
stratégie pointue a été élaborée, ciblant
les principales interventions dans le domaine de la prévention, des
soins et du traitement. L'ACHAP a notamment proposé des modèles
visant à atténuer l'impact à long terme de
l'épidémie, et initié des projets d'amélioration
des mécanismes de coordination et de l'allocation des ressources au
niveau du pays, des régions et des communautés.
En 2004, presque quatre ans plus tard, la réponse du
Botswana à l'épidémie de VIH est de plus en plus
considérée par les pays en voie de développement, les
communautés et les institutions de financement comme un modèle
d'excellence, en matière de développement et d'application d'une
stratégie globale de lutte contre le VIH/SIDA. Des programmes comme
l'accès aux ARV dans le secteur public, l'instauration d'un test de
dépistage du VIH en routine, l'introduction de cours sur la
sexualité et sur les relations hommes / femmes à l'école,
ainsi que les modèles d'administration de soins aux orphelins,
axés sur la communauté, les programmes sur le lieu de travail et
les efforts de mobilisation du secteur privé sont devenus autant
d'exemples à suivre pour les pays confrontés à la
même crise.
Au début de l'année 2001, MSD a personnellement
décidé de fournir ses traitements VIH/SIDA sans faire de profits
aux pays les plus pauvres et dans ceux les plus touchés par
l'épidémie de VIH/SIDA.
De nombreux pays en voie de développement sont
confrontés à un problème grave : la désertion
continue de leurs professionnels de santé vers des pays
développés, attirés par des salaires plus
élevés, de meilleures conditions de travail et des
opportunités de carrière. Il ne faut pas oublier également
tous les personnels soignants qui sont morts du sida au chevet de leurs
malades.
Depuis 1990, le continent africain déplore chaque
année le départ de 20 000 personnes. Pour compenser cette
désertion des compétences, l'Afrique dépense 4 milliards
de dollars par an pour employer des expatriés non africains venus
remplacer les
professionnels ayant émigré. Que faire pour
juguler la fuite des cerveaux de ce vaste continent dépourvu de
moyens?
Une approche est en train de naître de
l'expérience de MSD de la gestion du VIH/SIDA. Depuis 1996, lorsqu'il
s'est avéré que la trithérapie pouvait prolonger la
durée de vie de patients atteints du SIDA dans les pays occidentaux, de
nombreux médecins exerçant dans des pays en voie de
développement ont pris conscience qu'ils avaient besoin d'être
formés au VIH/SIDA s'ils voulaient prescrire correctement ces
traitements complexes.
Entre 1998 et 2005, l'unité VIH de MSD a
financé la formation clinique européenne de plus de 110
médecins africains venus de 24 pays, sur les 2 200 médecins ayant
reçu une formation grâce au soutien de Merck lors d'ateliers
locaux, de conférences scientifiques régionales et
internationales, et de préceptorats cliniques. D'une durée
variant d'une semaine à un mois, ces sessions de formation auraient
été impossibles sans la volonté d'experts européens
du VIH. Pratiquant dans des hôpitaux belges, anglais et français,
ils ont partagé leur expérience avec leurs confrères
originaires du continent le plus durement frappé. Les participants
étaient aussi bien des responsables de programmes nationaux africains
sur le SIDA que de médecins traitants spécialisés dans le
VIH qui, par la suite, ont assuré la formation de milliers d'autres
prestataires de soins de santé, une fois de retour dans leur pays
d'origine. Nombre de ces spécialistes du VIH sont devenus des
médecins de référence dans des hôpitaux locaux ou
des experts du VIH au sein d'organisations internationales de renom.





1994
2007
26
5 - Chronologie de l'accès au traitement
antirétroviral
1994
Dans le cadre de l'Organisation Mondiale de la santé
mise en place des accords ADPIC sur la propriété intellectuelle
(Aspects de Droits de Propriété Intellectuelle relatifs au
Commerce : TRIPS en anglais).
Peter Piot, directeur exécutif de l'ONUSIDA, le
signalait dans son discours à la Commission Européenne le 28
septembre 2000 : « le contrat actuel, par lequel, nous avons
accepté des prix élevés en échange de traitements
innovants et de meilleur qualité, a fonctionné pour le
bénéfice de tous dans les pays riches. Quoi qu'il en soit,
aujourd'hui, en particulier à cause du SIDA, ce contrat est à
remettre en question, puisqu'il exclut des millions de gens de l'accès
à ces mêmes produits ». Les accords internationaux ont en
effet servi avant tout les intérêts des laboratoires
pharmaceutiques. Ils ont ainsi imposé une protection organisée de
leur monopole : un respect des brevets sur 20 ans, au lieu de 10, dans tous les
Etats membres de l'OMC. De fait ils en restreignent l'accès aux seuls
malades solvables. L'article « spécial 301 » de la loi
américaine sur le commerce introduit en 1988 a été
utilisé contre plus de 30 pays, afin d'assurer la protection des
intérêts des compagnies américaines et de pouvoir exercer
des sanctions commerciales sur les pays dont les lois sur la
propriété intellectuelle les desservent. L'Inde, le
Brésil, l'Argentine, l'Egypte, le Ghana ont été les
premières cibles.
1996
A partir de 1996, d'importantes avancées de la
recherche fondamentale et clinique bouleversent la prise en charge
médicale de l'infection par le VIH. De nouveaux concepts
physiopathologiques et la mise à disposition de tests biologiques de la
charge virale plasmatique, montrent qu'il existe une intense activité de
réplication virale tout au long de l'infection à VIH, dont
l'importance est prédictive de l'évolution vers le SIDA. Ils
fournissent un instrument permettant de suivre au plus près
l'évolution de l'infection et les effets des traitements.
L'introduction des multithérapies
antirétrovirales, associant aux inhibiteurs
nucléosidiques de la transcriptase inverse la nouvelle
classe thérapeutique des inhibiteurs de protéase, puis celle des
inhibiteurs non nucléosidiques, rendent la charge virale
indétectable chez une proportion importante de patients traités.
Cela se traduit par une diminution spectaculaire de l'incidence des infections
opportunistes (les laboratoires qui commercialisaient des antiviraux actifs sur
le CMV se rappellent encore de la chute vertigineuse de leurs ventes) et de la
mortalité. Par voie de conséquence, le nombre d'hospitalisations
dues à l'infection par le VIH dans les pays industrialisés,
où l'accès aux traitements est possible à large
échelle, diminue considérablement.
L'annonce de l'efficacité des multi-thérapies
antirétrovirales utilisant les antiprotéases en juillet 96 lors
de la XI° Conférence Internationale de Vancouver (Canada) suscite
chez certains groupes associatifs, responsables de santé publique, et
scientifiques, une prise de conscience militante en faveur de la diffusion de
ces progrès thérapeutiques en Afrique. 95 % des patients
infectés par le VIH qui vivent dans les pays en voie de
développement n'ont pas accès à ces progrès. C'est
moralement intolérable que le plus grand nombre ne puisse pas disposer
de traitements antirétroviraux à l'efficacité
démontrée. Tout doit être mis en oeuvre afin d'essayer de
rationaliser la prise en charge, et de proposer des programmes favorisants
l'accès aux médicaments actifs contre le VIH, y compris en
Afrique Sub-saharienne. Cependant le prix élevé sur le
marché international limite de dramatiquement l'accessibilité de
ces traitements, particulièrement dans les pays ou la demande et le
besoin sont les plus importants au regard des moyens économiques et
financiers dont disposent les Etats et les ménages. En 1996, ceci
relève du défi face au scepticisme international qui
considère cette proposition comme irréaliste.
1997
En Afrique, cet engagement pour l'accès aux
traitements débouche notamment sur l'organisation d'une consultation
scientifique internationale à Dakar en septembre 97. Cette consultation
permet de définir les pré-requis à la diffusion de
traitements antirétroviraux, et de préciser les protocoles
thérapeutiques optimaux. Par la suite, au cours de la conférence
internationale sur le SIDA et les MST d'Abidjan en décembre 97 un appui
politique est apporté à cette démarche en annonçant
la mise en oeuvre du programme de traitements dans plusieurs pays africains.
Cette annonce est loin d'accueillir l'assentiment général.
Quelques mois auparavant, en juin l'ONUSIDA annonce son
initiative d'accès aux antirétroviraux dans quatre sites pilotes
: Ouganda, Côte d'Ivoire, Chili et Vietnam. Celleci débutera
officiellement en novembre de la même année.
1998
GSK et 38 autres laboratoires pharmaceutiques saisissent la
Haute Cour de justice de Pretoria. Ces laboratoires s'opposent au gouvernement
Sud Africain qui souhaite importer des médicaments
génériques contre le SIDA. Les laboratoires sont sûrs de
leur bon droit. La loi Sud Africaine de 1997 sur le médicament donne au
ministre de la santé de larges prérogatives pour recourir
à des importations parallèles, des licences obligatoires et une
substitution par les génériques. Or cette loi, selon les
compagnies pharmaceutiques porte atteinte aux droits d'exclusivité
conférés à leurs médicaments grâce aux
brevets. Le droit des brevets doit donc l'emporter et la loi, dont
l'application est bloquée depuis le dépôt de la plainte en
1998, doit être modifiée. D'ailleurs, à la fin des
années 90, en opposition au gouvernement sud Africain, le gouvernement
américain et
la commission européenne, entre autres, ont pris
position pour le respect du droit de propriété intellectuelle et
ont exercé des pressions sur le gouvernement Sud Africain afin qu'il
modifie sa loi.
2000
Les objectifs du millénaire sont fixés par les
Nations Unies.
Mai : création de l'initiative «
Accelerating Access » par l'ONUSIDA en partenariat avec plusieurs agences
des Nations Unies (la Banque Mondiale, l'OMS, le FNUAP, l'UNICEF) et cinq
compagnies pharmaceutiques. A partir de 2001 cette initiative se poursuivra
sous l'égide de l'OMS.
2001
Février : Le laboratoire
générique indien Cipla propose une trithérapie pour 600
dollars par an aux gouvernements du Sud.
Avril : Les compagnies pharmaceutiques
retirent leur plainte contre le gouvernement Sud Africain sans que celui-ci ait
transigé sur la loi incriminée, ce qui met un terme à 3
ans de procédures judiciaires et de guerre d'intox face aux ONG. A
l'arrivée une rédition sans conditions. Cette affaire a
été particulièrement catastrophique pour GSK.
Deuxième groupe pharmaceutique du monde et leader dans le traitement du
SIDA. GSK a cédé sur presque tout - une réduction
drastique du prix des traitements et l'attribution de licences de fabrication
de génériques. Sa puissance financière (30 milliards de
dollars de chiffre d'affaire et 10 milliards de profits) comme les accords
internationaux sur la protection des brevets que le groupe invoquait n'ont pas
pesé lourd. Pis, la pression sur les prix s'est étendue aux USA
son premier marché.
GSK ainsi que les autres entreprises pharmaceutiques ont cru
que la bataille se mènerait sur un terrain strictement juridique. La loi
Sud Africaine revenait à mettre en péril le business model de
cette industrie : amortir sur 10 ou 15 ans des frais de recherche colossaux
grâce à la vente des médicaments dont ils sont issus,
même si leurs coûts de productions sont ensuite très
faibles. Pour les laboratoires, les brevets représentent le carburant de
l'innovation. C'est le sens des accords internationaux adoptés en 1994
dans le cadre de l'OMC, argumentait GSK. Et c'est pourquoi l'entreprise avait,
au départ, le soutien de l'administration américaine et la
commission européenne.
Malheureusement pour les firmes le contentieux s'est vite
orienté vers un thème éthique « la santé
contre le profit ». En effet, des ONG sud africaines, dont TAC (Treatment
Action Campaign) se sont mobilisées contre cette plainte, et ont
attiré l'attention sur le coût humain du non accès, pour
les malades, à des médicaments vitaux : 400 000 morts de SIDA
depuis que la loi de 1997 est bloquée. Le président charismatique
de TAC Zackie Achmat séropositif n'hésita pas à mettre sa
vie en péril en refusant de prendre le
moindre traitement tant que celui-ci n'est pas accessible
à tous ses compatriotes. TAC réclame donc, au nom des malades, le
droit d'être (( amicus curiae >> ((( amie de la Cour >>) dans
le procès. Le procès s'ouvrira sur l'étude de la
requête de TAC que la Haute Cour accepte. Les malades sont donc parties
civiles dans ce procès. C'est la nature même du procès que
la haute cour a ainsi modifiée. La bataille ne va plus reposer sur les
seuls arguments juridiques : la loi de 1997 est-elle ou non conforme aux
engagements internationaux de l'Afrique du Sud sur la propriété
intellectuelle ? Les données humaines vont désormais être
prises en compte : le droit des brevets peut-il prévaloir sur le
traitement des malades ? TAC demande alors aux compagnies pharmaceutiques de
justifier le prix de leurs médicaments. Rappelons que le contexte sud
africain au moment du procès est le suivant : En 2000 cinq millions de
personnes étaient infectées soit 20 % de la population. Le
problème ne fera que s'aggraver. Les autorités sanitaires du pays
prévoient que 7,5 millions de personnes pourraient être
contaminées en 2010 dont 50 % des 15-29 ans. Dans ce contexte invoquer
la protection des brevets paraissait maladroit, sinon cynique. D'autant que
pour GSK, l'Afrique du Sud ne présentait que 1 % des ventes de
médicaments contre le SIDA (2 milliards de dollars par an).
Le laboratoire britannique ne l'a pas compris. Surtout, il a
sous estimé la puissance des ONG (Organisations Non Gouvernementales)
qui menaient campagne contre lui dont l'OXFAM. Avec un budget de 400 millions
de dollars, un réseau de 3000 partenaires dans 100 pays et une
équipe d'experts de haut niveau, cet organisme basé à
Oxford (UK) est parmi les plus puissants au monde. Face à GSK, OXFAM a
opté pour une attaque très ciblée, lancée
début 2001 et baptisée (( cut of costs >>. Objectif :
obtenir une baisse de 90 % du prix du traitement contre le SIDA, alors de 10
000 dollars par an, un montant inaccessible pour les Sud Africains. Entre
autres (( bombes médiatiques >>, OXFAM a relevé que GSK
appliquait dans certains pays en développement des tarifs jusqu'à
20 % plus élevés qu'aux USA, cette information a laminé la
défense du laboratoire. En avril 2001 l'ONG des (( french
doctors>> MSF lancera une pétition sur le thème (( la
protection des vies humaines passe avant celle des brevets >>. Celle-ci
recueillera 270 000 signatures dans plus de 130 pays.
Les protestations de Kofi Ahnan, secrétaire
général de l'ONU et la position du parlement européen
conduirent un abandon du procès et fit perdre à GSK les rares
soutiens qui lui restaient. La cohésion entre les firmes s'était
déjà sérieusement fissurée. Cinq d'entre eux, parmi
les plus importants, avaient décidé de faire cavaliers seuls en
prenant leurs propres avocats. Ces cinq laboratoires demandèrent
à retirer leurs plaintes et demandèrent à leurs
confrères d'en faire autant. Au final 37 sur 39 le feront.
Le 19 avril la plainte est retiré, la loi Sud
Africaine n'est pas modifiée et les frais de justice seront payés
par l'industrie pharmaceutique. Pourtant cette victoire n'a, au fond, rien de
bien anormal : dans sa loi, l'Afrique du Sud ne fait qu'interpréter et
utiliser les clauses de sauvegarde prévues par l'accord ADPIC pour la
santé publique. Pour rappel
l'accord sur les ADPIC prévoit la possibilité
pour les états, souverains, de passer outre le droit des brevets en cas
de besoin (licences obligatoires). La déclaration de DOHA en 2001 a
rappelé ce droit. Un amendement (12/05) permet en théorie aux
pays qui ne peuvent produire d'importer des génériques.
Novembre : Signature des accords de DOHA. Un
laboratoire détenteur d'un brevet prêt à négocier
avec un pays tiers peut céder une autorisation de production locale en
échange de royalties : il s'agit alors de licence volontaire. Si le
laboratoire n'est pas prêt à négocier, un Etat souverain,
peut décider de faire fabriquer une copie d'un produit dont il a besoin
par une industrie locale : c'est ce que l'on appelle une licence obligatoire.
Cette disposition permet également à un pays ne disposant pas de
capacités de production propre d'importer des copies de traitement.
Cela étant, sous la pression de gouvernements du Nord,
eux-mêmes guidés par les compagnies pharmaceutiques, l'Afrique
francophone - a adopté les accords de Bangui qui stipulent que le
recours aux licences obligatoires est interdit dans les pays signataires.
Autrement dit ces pays ont adopté une législation encore plus
contraignante que les accord (ADPIC) qui cantonnaient déjà la
santé des populations à des dispositions exceptionnelles.

2003
Décembre : Séance historique
à New-York. L'OMS et l'ONUSIDA lancent la stratégie 3 by 5 «
3 millions de traitements antirétroviraux d'ici 2005. 400 000 personnes
bénéficient d'un traitement ARV dans les pays à ressources
faibles ou intermédiaires. En 2006, près de 700 000 personnes
sont mises sous traitement pour la première fois. En décembre
2006 près de 2 015 000 personnes vivant avec le VIH
bénéficieront d'un traitement dans les pays à faibles
ressources ou intermédiaires soit 28 % des 7,1 millions de personnes qui
en auraient besoin.
2005
Janvier : L'Inde a dû mettre sa
législation sur les brevets en conformité avec les règles
de l'OMC sur la propriété intellectuelle qu'elle a rejoint. Le
pays délivre désormais des brevets pour 20 ans sur les nouveaux
produits et procédés pharmaceutiques ce qui restreint
considérablement la possibilité de produire des
génériques à prix abordables.
Mars : La Food and Drug Administration (FDA)
a donné, pour la première fois, un accord à titre d'essai
à une compagnie pharmaceutique étrangère - ASPEN
PHARMACARE, pour la production d'une version générique de
médicaments anti-VIH.
Le produit concerné est une trithérapie vendue
en pack, comprenant deux types de comprimés, l'un de Lamivudine /
Zidovudine et l'autre de Névirapine, à prendre chacun deux fois
par jours après une phase d'initiation de deux semaines de Nevirapine.
Le comprimé de la combinaison Lamivudine / Zidovudine à la dose
fixe est une copie du produit déjà approuvé par la FDA
et commercialisé par GSK, Combivir. Le comprimé de
Névirapine est quant à lui une version de Viramune produit par
Boeringher. L'accord spécifique donné par la FDA, fait de sorte
que même si les brevets et l'exclusivité protègent le
marché américain du produit d'ASPEN, il doit répondre aux
standards américains de qualité, de sécurité et
d'efficacité. Il permet surtout à l'administration et aux
organisations humanitaires américaines d'acheter ces médicaments
génériques à moindre coût pour les redistribuer aux
quatorze pays d'Afrique et des Caraïbes plus particulièrement
concernés par le plan américain d'aide d'urgence contre le
SIDA
Septembre : L'assemblée
générale de l'ONU puis le sommet des chefs d'Etats du G8 à
Gleneagles en juillet adoptent l'objectif (( d'accès universel >>
aux traitements du VIH/SIDA, et aussi définitivement clôturent le
débat international qui faisait rage depuis plus de 5 ans entre les
économistes sur le bien fondé de la diffusion massive des mu
ltithérapies antirétrovi rales.
2006
XVI° Conférence Internationale à Toronto
et surtout deux conférences (( satellites >> à Toronto en
août et à Harvard en septembre entérinent un tournant
majeur dans les recherches sur l'économie du SIDA dans les pays en
développement. Même si elle n'atteint pas l'objectif
proclamé fin 2005 (à cette date le chiffre s'établissait
à 1,3 millions) l'initiative (( 3 by 5 >> de l'OMS cristallise des
progrès significatifs (le nombre de personnes sous traitement a
triplé en deux ans.
Septembre : Dans la foulée de la
Conférence de Paris, la France propose de créer une
facilité internationale d'achat de médicaments : UNITAID.
Alimentée par des prélèvements de solidarité, elle
permettra d'augmenter l'offre et de faire baisser les prix des
médicaments.
2007
La firme pharmaceutique suisse Novartis s'attaque à la
loi indienne sur les brevets votée par les parlementaires en 2005. Dans
cette loi qui essaie de concilier respect du droit de propriété
intellectuelle et impératif de santé publique, le gouvernement
indien a inclus dans sa loi (le Patent Act) une clause (article 3D)
prévoyant que ne sont brevetables que les médicaments
réellement nouveaux et innovants. Cet article vise à contourner
la pratique courante des entreprises pharmaceutiques qui consiste à
apporter des modifications mineures à des molécules existantes
pour obtenir un nouveau brevet. C'est cette loi que Novartis attaque devant les
tribunaux. Si le laboratoire obtient gain de cause, un médicament
développé et commercialisé dans les pays riches et
susceptible, au terme d'une période de 20 ans, de tomber dans le domaine
public pourra, moyennent des changements mineurs être de nouveau
protégé par un brevet... de 20 ans !
C'est ce type de prolongation de la protection qu'offre les
brevets que Novartis a tenté d'obtenir pour son anticancéreux
Glivec et que permettrait l'abrogation de l'article 3D. L'Inde a rejeté
la demande de brevet en janvier 2006 car ce médicament étant une
nouvelle formulation d'un médicament déjà existant. Dans
d'autres pays ou Novartis a obtenu un brevet, le Glivec est vendu 2600 dollars
par patient et par mois. En Inde la version générique du Glivec
est disponible à moins de 200 dollars par patient et par mois. Novartis
tente aujourd'hui d'annuler cette décision afin de vendre ce
médicament au même prix en Inde que dans les autres pays.
Depuis que la loi indienne a été changée
en 2005, près de 10 000 demandes de brevet sont en attente d'examen. Si
l'Inde accorde des brevets de la même manière que les pays
développés cela signera l'impossibilité de produire des
génériques de médicaments récemment
développés et commercialisés dans les pays riches. Il est
évident que les prix de plusieurs médicaments monteraient en
flèche. Cela aura un impact très lourd sur les malades qui
dépendent des génériques particulièrement les
personnes vivant avec le VIH.
Le budget antirétroviral pèse lourd sur le
budget d'une famille. Un traite ment générique coûte entre
23 à 24 dollars par mois. Ce coût est déjà
énorme dans un pays ou 80 % de la population vit avec moins de 2 dollars
/ jour (moins de 1 dollar en Afrique). IL pourrait s'élever à 340
dollars par mois. Lorsque la charge virale augmente, il faut se procurer un ou
deux inhibiteurs de la protéase par mois ce qui fait 115 dollars de plus
car ce ne sont pas des génériques.
Si Novartis l'emporte, le prix des médicaments contre
le Sida pourrait devenir 20 à 50 fois plus cher car de plus en plus de
malades ont recours aux médicaments de deuxième ligne. Etant
donné que l'Inde est aujourd'hui le principal fabriquant mondial de
médicaments contre le sida, l'impact serait ressenti au niveau
international.

Janvier : En conformité avec les
règles de l'OMC, le gouvernement thaïlandais a décidé
en janvier dernier d'émettre des licences obligatoires sur plusieurs
médicaments utilisés dans les trithérapies, dont le
Kalétra® (ou Aluvia - produit phare du laboratoire
Abbott. La réaction ne s'est pas fait attendre : Abbott a publiquement
condamné cette mesure, et annoncé par voie de presse dans la
foulée qu'il retirait ses demandes d'autorisation de mise sur le
marché (AMM), présentes et à venir, pour tous ses
produits. Sans AMM, impossible pour le pays de produire ou d'importer une
version, même générique, du médicament, puisqu'il
n'aura pas pu être évalué. Abbott prive donc les
Thaïlandais de ses nouveaux médicaments, notamment,
l'Aluvia®, une version thermo-stable du
Kaletra®, résistante à chaleur.
En Thaïlande, jusqu'en 1992 les brevets n'étaient
accordés que sur les procédés industriels de fabrication,
et non sur les produits eux-mêmes. Aussi les médicaments en
eux-mêmes n'étaient pas sous brevet, et si tant est qu'un autre
procédé de fabrication existe, rien ne s'opposait
légalement à la production de copie. C'est pourquoi l'AZT, la D4T
et la DDI qui ont été brevetés avant 1992 existent en
version copiée dans ce pays.
Mars : Abbott annonçait ses mesures
de rétorsion contre la licence obligatoire émise sur le Kaletra
par la Thaïlande : retrait des demandes d'AMM de 7 produits (antibiotique,
traitement contre l'insuffisance rénale chronique, hypertension
artérielle, thrombose...) et boycott du marché thaïlandais
(refus d'y enregistrer ses produits à venir).

La Thaïlande se retrouve donc au coeur de la plus grande
bataille des brevets jamais menée. C'est ainsi qu'il faut
interpréter la décision (en deux temps) du laboratoire
américain Abbott. : abaisser, le 10 avril, le prix d'un de ses
médicaments antisida le Kaletra , à 1 000 dollars par an et par
malade dans 40 pays, dont la Thaïlande. Proposer à Bangkok, le 23
avril, la nouvelle formule de son Kaletra (l'Aluvia, qui n'a pas besoin
d'être réfrigéré) à prix
((cassé)). Qu'est-ce qui a donc poussé l'un des fleurons
du plus rentable des business à lâcher du lest sur un
((blockbuster)) qui lui rapporte 1,1 milliard de dollars dans 118 pays
?
La nouvelle junte au pouvoir à Bangkok depuis
septembre 2006 (actionnaire du laboratoire générique GPOvir) est
à l'origine d'une initiative sans précédent. Ce qu'aucun
gouvernement n'avait, jusque-là, osé faire. Pas même le
Brésil, pourtant en pointe pour faciliter l'accès aux traitements
à plus de 50 % de ses patients : promulguer une succession de lois
(((licence obligatoire>>) pour permettre l'importation ou la production
d'un générique, alors que les médicaments ((de
marque>> sont toujours protégés par des brevets. D'autres
pays l'avaient précédé dans la production de copies
à bas prix (la Malaisie et le Mozambique, par exemple). Mais la
Thaïlande a fait plus fort en s'octroyant trois licences obligatoires.
D'abord, en novembre 2006 sur l'Efavirenz (un autre antirétroviral de
l'américain MSD). Puis, en janvier 2007, sur le Plavix (du
français Sanofi-Aventis), un anticoagulant destiné aux maladies
cardio-vasculaires. Et sur le fameux Kaletra d'Abbott, un traitement de
((deuxième intention>> administré aux malades du sida qui
développent des résistances. Contrairement aux
antirétroviraux de première génération, accessibles
à 150 dollars par an et par patient, le Kaletra se monnayait, lui,
à 3 700 dollars !
La réaction d'Abbott a été d'une rare
virulence. La firme de Chicago a décidé de retirer sept nouveaux
médicaments en passe d'être enregistrés dans le pays, dont
le fameux Aluvia. Prudemment, Abbott avait d'abord proposé, en
février, de diviser par trois le prix de son Kaletra...
Pour bien comprendre l'ampleur de la bataille et la virulence
des coups échangés, il faut jeter un oeil sur l'analyse des
alliés de l'industrie, tel l'American Enterprise Institute (AEI), vent
debout contre ceux ((qui veulent démonter les droits de
propriété intellectuelle)).
La junte de Bangkok serait ainsi coupable à ses yeux,
((avec l'aval des ONG)), de ne consacrer que 3,3 % de son budget à la
santé, contre 7,6 % pour le Brésil, par exemple. Et risque, par
sa ((politique anti-brevet)), de mettre en ((danger)) les investissements
étrangers en Thaïlande, note Roger Bate de l'AIE, dans une
récente analyse.
Pas évident. Une étude publiée le 10
avril rappelle que le lancement de nouvelles générations de
molécules antisida rapportera 10,6 milliards de dollars contre 7,5
milliards en 2005. Par ailleurs, le business du médicament affiche une
santé insolente avec une expansion de 7 % l'an passé, à
693 milliards de dollars. ((Les pays émergents, qui représentent
17 % du marché mondial, vont connaître un boom de 30 % l'an
prochain)), note un autre rapport. L'Afrique, grande oubliée, ne
pèse que 1,3 % des ventes mondiales.
Les médicaments au Nord, les malades au Sud. C'est
peut-être ce qui a poussé des actionnaires chrétiens
d'Abbott, The Interfaith Coalition on Corporate Responsibility, à
dénoncer une position ((non éthique)) de leur groupe. Et
pressé la Fondation Clinton, rejointe par 22 sénateurs
américains, à fustiger l'attitude d'Abbott envers Bangkok. Le
groupe américain se devait donc de reprendre la main à la veille
de son assemblée générale. Et de ne pas perdre la guerre
de l'image, à l'instar du fiasco de 39 laboratoires contre le
gouvernement sud-africain en 2001. C'est ce qu'il a fait, avec la
bénédiction de l'OMS, qui se félicite de voir la firme
proposer son Kaletra à un prix ((moins cher que les
génériques.)) Adoubant au passage la stratégie d'Abbott :
céder sur le prix plutôt que de lâcher sur les brevets, et
tenter de conserver une rente, une situation de monopole sur les
médicaments. Que va faire la Thaïlande ? S'affranchir des brevets
au motif qu' ((il devient indispensable que l'humanité formule un
nouveau mode de pensée si elle veut survivre)), invoque le
ministère de la Santé citant Einstein ? Ou retirer sa licence
obligatoire, victime ((d'une prise d'otage de ses malades du sida)) par Abbott,
comme le dénonce Médecins sans frontières ? Son choix
risque de faire jurisprudence...
Mai : Le gouvernement brésilien
refuse les offres de MSD qui proposait une réduction de 30 % du prix de
son antirétroviral Efavirenz et décide l'importation d'un
générique...
Juin : Une plainte a été
déposée par la firme pharmaceutique Abbott contre Act Up-Paris, a
annoncé l'association. Cette plainte fait suite à une action
menée le 26 avril, la veille de l'Assemblée
générale des actionnaires du groupe. Act Up-Paris et des
associations de malades thaïlandaises appelaient à un
((netstrike»: il s'agissait de se connecter de manière
répétée sur le site internet de la firme ((pour le
ralentir ou le saturer». La firme pharmaceutique a porté plainte
contre Act Up-Paris pour entrave au fonctionnement d'un système de
traitement automatisé de données et détention ou mise
à disposition des outils qui permettent le blocage d'un système.
Act Up risquerait ((70.000 euros d'amende et des dommages et
intérêts»....


6 - Accès universel : les avancées

« 3 by 5 »
Les tendances mondiales encourageantes se poursuivent dans
l'extension de l'accès au traitement antirétroviraux.
En Afrique Sub-saharienne en 2006, on estime que plus de 1,3
million de personnes suivent un traitement antirétroviral, ce qui
représente une couverture de 28 % alors qu'il y a trois ans, on
dénombrait 100 000 patients sous traitement et une couverture d'à
peine 2 %. 67 % des personnes sous traitement antirétroviral dans les
pays aux faibles revenus (PRF) ou intermédiaires (PRI) vivent en Afrique
Sub-saharienne - alors qu'elles n'étaient que 25 % à la fin 2003.
Cependant, il faut faire attention aux critères relatifs aux «
besoins » qui sont critiquables. Les patients qui
bénéficient d'un traitement sont à un stade avancé
de la maladie et ont soit des signes cliniques soit un bilan immunitaire
très altéré (< 200 CD4 / mm3). En France, il est
possible de débuter un traitement en dessous de 350 CD4 / mm3.
En Asie de l'Est, du Sud et du Sud Est, 280 000 personnes sont
désormais sous traitement, avec une couverture évaluée
à 19 % soit quatre fois plus que fin 2003, date à laquelle 70 000
personnes suivaient un traitement. Bien que l'Asie représente 21 % des
besoins totaux en traitement, 14 % seulement des patients sous traitement dans
les PRF ou PRI vivent dans cette région.
En Amérique Latine et dans les Caraïbes, le nombre
de patients sous traitement atteint progressivement les 355 000 personnes,
contre 210 000 fin 2003. Même s'il existe des variations
considérables entre pays, la couverture globale de 72 % semble
s'approcher de l'accès universel.
Les pays d'Europe Orientale et d'Asie Centrale ont
enregistré des progrès importants, avec 35 000 personnes qui
suivent maintenant un traitement, contre 15 000 fin 2003. La couverture de
cette région est estimée à 15 % des patients qui ont
besoin d'un traitement.
La région de l'Afrique du Nord et du Moyen-Orient est
celle qui atteint la couverture la plus faible, 6 % avec seulement 5000
personnes sous traitement fin 2006 contre 77 000 qui en auraient besoin.
A la fin 2006, le Plan d'urgence du président des
Etats-Unis d'Amérique pour l'aide à la lutte contre le SIDA
finançait des programmes traitant 987 000 personnes. Les
programmes financés par le Fond Mondial de lutte
contre le SIDA, la tuberculose et le paludisme traitaient 77 000 personnes.
Toutefois, selon les calculs du Plan d'urgence et du Fond Mondial, quelques 492
000 personnes suivaient un traitement dans le cadre de programmes
financés conjointement par les deux initiatives. Au total, celles-ci
venaient donc en aide à 1 265 000 individus.
Sur les 2,3 millions d'enfants (âgés de 0 - 14
ans) vivant avec le VIH en 2006 (dont presque 90 % en Afrique Sub-saharienne)
environ 780 000 avaient besoin d'un traitement antirétroviral. On estime
que fin 2006, près de 115 500 enfants avaient accès au
traitement, ce qui représente un taux de couverture de 15 %. Par
conséquent , si l'on compare ces chiffres aux estimations de l'UNICEF
pour 2005 qui étaient de quelque 75 000 enfants sous traitement, le
nombre d'enfants suivant une thérapie antirétrovirale dans le
monde a enregistré une hausse de 50 % en 2006. Néanmoins la
couverture du traitement antirétrovirale est estimée à 28
% dans les PRF ou PRI.

Prix des antirétroviraux de 1ère
ligne
Le GPRM (Global Price Reporting Mechanism) est un
système mondial d'information sur les médicaments
antirétroviraux établi par l'OMS en 2004 qui rassemble
des données concernant les prix des transactions sur
les antirétroviraux achetés dans les pays en
développement.
Dans les pays à faibles revenus ou
intermédiaires, le prix de la de la plupart des médicaments de
1° intention avait diminué de 37 % à 53 % entre 2003 et
2006, et de 10 à 20 % entre 2005 et 2006. Cette baisse a sensiblement
contribué à élargir l'accès au traitement,
même si les prix demeurent élevés dans la plupart des pays
d'Europe Orientale et d'Amérique Latine.
En 2006, le prix moyen du traitement de première
intention (pré sélectionné par l'OMS) dans les pays
à faibles revenus allait, par patient et par an, de 123 dollars à
493 dollars. La baisse des prix des médicaments enregistrée entre
2004 et 2006 est attribuable à l'expansion des programmes de traitement,
à la forte concurrence entre le nombre croissant de produits pré
sélectionnés par l'OMS et aux négociations avec les
fabricants de génériques.
Dans les pays aux revenus intermédiaires, le prix
moyen du traitement de 1° intention a diminué très nettement
et il est maintenant plus proche des prix pratiqués dans les pays
à faibles revenus. En 2006, le prix moyen pour un traitement de 1°
intention allait de 145 dollars, par personne et par an, pour le schéma
le meilleur marché (D4T + 3TC + NVP) à 623 dollars pour le
schéma le plus coûteux.


Le programme national anti-sida lancé par ce pays au
début des années 90 a très vite buté sur un
problème de coût : sur les 500 millions de dollars
consacrés au programme, les 3 / 5èmes sont destinés
à l'approvisionnement en médicaments.
Un laboratoire brésilien, Far-Manguinhos, a
été mandaté pour produire à bas prix des
traitements. Résultat, sur les 600 000 séropositifs que compte le
pays, plus d'un quart se voient fournir gratuitement les traitements qui les
maintiennent en vie. Les admissions en hôpital dues au Sida ont
diminué de 80 % depuis 1996. Et le nombre de séropositifs et la
mortalité liée au Sida est deux fois inférieur aux
prévisions faites au début des années 90.
En cassant le brevet d'un médicament d'un laboratoire
multinational, le gouvernement brésilien a pris début mai une
décision inédite et sujette à polémique. La
nécessité d'assurer la viabilité financière du
programme public de soins destiné aux patients atteints du sida a
conduit le président Luiz Inacio Lula Da Silva à signer un
décret qui permet de contourner le brevet détenu par le
laboratoire américain MSD sur le médicament Efavirenz (sustiva ou
Stocrin), utilisé dans le VIH. Cette mesure inédite autorise pour
une période indéterminée l'importation d'un
générique puis, dans un second temps, la fabrication du
médicament dans le pays.
MSD à fait savoir qu'elle avait proposé «
différentes formules » au gouvernement, allant même
jusqu'à négocier une réduction de 30 % du prix actuel de
vente du médicament au Brésil. En réponse, le
Brésil souhaite que MSD lui vende le médicament au prix ou la
firme le vend en Thaïlande, soit 0,65 dollar l'unité. Selon le
directeur de communication chez MSD, la différence entre le prix de
l'Efavirenz dans les deux pays résulte d'accords internationaux fixant
des prix distincts en fonction de l'indice de développement humain (IDH)
et de l'incidence de la maladie sur la population.
Le gouvernement, qui est l'unique acquéreur du
médicament au Brésil, estime qu'il économisera 30 millions
de dollars par an avec les génériques, un montant qui pourra
être réinvesti dans le traitement de 200 000 personnes atteintes
du sida.
A partir de septembre, le ministère de la santé
distribuera dans le réseau public le générique produit par
des laboratoires indiens. Il achètera chaque pilule de
l'antirétroviral pour 0,45 dollar, un prix largement inférieur
à celui de 1,65 dollar accordé actuellement par MSD. Le
ministère versera au laboratoire, à titre de royalties, 1,5 % de
la valeur totale d'achat des génériques, un prix conforme, selon
le gouvernement, aux accords commerciaux internationaux et qui tempère
quelque peu selon lui le fait qu'il ait cassé le
brevet. Le gouvernement a déjà menacé
à plusieurs reprises les laboratoires multinationaux de leur imposer un
brevet obligatoire (et donc d'autoriser l'importation et la fabrication de
génériques). En 2001 le ministre José Serra avait
annoncé un arrêté qui faisait du brevet de
l'antirétroviral Nelfinavir, des laboratoires suisses Roche, un brevet
d'utilité publique. Son successeur, Humberto Costa, avait fait de
même avec le médicament Kaletra, des laboratoires Abbott, en 2005.
Les deux laboratoires avaient ensuite réussi à négocier la
réduction des prix.

Les génériques

Le prix d'un médicament n'est pas lié au brevet
selon le LEEM, il est lié à l'investissement nécessaire
à sa recherche et à son développement, et au processus de
fabrication qui est parfois complexe à mettre en oeuvre (notamment pour
les médicaments de biotechnologies). De 10 000 molécules
identifiées, à 10 qui feront l'objet d'un dépôt de
brevet, et une qui parviendra à passer toutes les étapes de tests
et d'essais cliniques, le chemin de l'innovation au malade est long (12 ans en
moyenne), complexe et onéreux. La recherche nécessite des efforts
renouvelés d'investissement à moyen et long terme. La mise au
point d'une nouvelle molécule représente un investissement
d'environ 800 millions d'euros, ce coût a été
multiplié par 10 en 20 ans.
Pour les associations, ces fameux 800 millions d'euros sont
très contestés : d'abord parce qu'ils recouvrent des sommes qui
ne sont pas détaillées dans certains cas et dont
l'évaluation reste obscure. Ensuite parce que des sommes énormes
sont investis dans le marketing dont on ne parle pas. Enfin, il ne faut pas
oublier que pour que les retours sur investissement des actionnaires soient
maximaux les sociétés ((gonflent » le prix de la recherche
et développement.
Mais pour qu'un médicament soit commercialisé,
il ne faut pas seulement que le marché soit important (les 3/4 de la
population sont concernés), il faut aussi qu'il rapporte de l'argent.
Beaucoup d'argent. Le plus rapidement possible. Comme le constatait le Docteur
Gro Harlem Brundtland, directrice générale de l'OMS : (( plus
d'un milliard de personnes abordent le XXI° siècle sans avoir
profité de la révolution sanitaire. De fait le 4/5eme des
dépenses mondiales de santé sert à 1/5eme de la
population. En ce qui concerne le sida, le constat est plus accablant
encore.
L'industrie du médicament est le secteur
économique qui consacre, sur ses fonds propres, le budget le plus
important à la recherche et au développement (certes, mais qui
fait le plus de bénéfices), devant l'aéronautique, le
spatial ou l'automobile. 99% de l'investissement consacré en France
à la recherche sur le médicament est financée par les
entreprises privées. Le prix des médicaments est le reflet des
coûts de la recherche conduite par les entreprises. Il faut
préciser que sur leur chiffre d'affaire la plupart des laboratoires
consacrent presque autant de fonds à la publicité et à la
promotion qu'à la recherche soit moins de 15 %.




Cipla société créée en 1935 avec
son siège à Bombay et ses 22 usines à travers le pays est
le numéro 1 du médicament dans un pays aux 2000 laboratoires - et
fer de lance de la fourniture d'antirétroviraux contre le sida à
prix cassé. Le laboratoire indien innove à partir de l'existant.
Il est le premier à avoir lancé le premier
générique de l'AZT en 1993.
La revue scientifique The Lancet en juillet 2004 a
publié une étude qui a validé scientifiq uement
l'efficacité de la trithérapie génériq ue associant
trois anti rétrovi raux calqués sur les médicaments de
trois multinationales différentes dans un même
comprimé. C'est justement le précurseur
Triomune commercialisé en 1992 qui a notamment servi de base à
l'étude. Cipla proposa en 2001 à MSF une trithérapie pour
600 dollars par an alors que les grands groupes pharmaceutiques plafonnaient
à 10400 dollars. Preuve que l'industrie pharmaceutique indienne ne s'est
pas contentée de copier des molécules. Avec Triomune, elle a
innové en proposant la première trithérapie «
combinaison fixe », c'est-à-dire la synthèse de trois
molécules de laboratoires différents (et concurrents) en un seul
comprimé. 6 ans avant Gilead et sa fixe dose Atripla contenant ses
molécules TDF + FTC associées à celle de MSD / BMS
Efavirenz. Quand les géants de la pharmacie dépensent en moyenne
15 % de leur budget en recherche et développement, Cipla n'y consacre
que 3 %. C'est 12 millions de dollars comparés aux 7 milliards de
Pfizer. Impossible de nourrir de grandes ambitions quand le budget annuel de
Cipla (400 millions de dollars) s'avère de deux fois inférieur au
coût officiel de la mise en vente d'un nouveau médicament.
Quatrième producteur de médicaments au Monde en
2004, l'Inde exporte quand même 6,5 milliards de dollars, mais c'est
moins que le blockbuster Lipitor de Pfizer un hypolipémiant qui
pèse 8 milliards de dollars. Depuis 2005, et en vertu des accords de
l'OMC, l'Inde doit maintenant attendre 20 ans que les nouveaux
médicaments ne tombent dans le domaine public et puissent être
copiés. Ceci conduit à une inquiétude sur la fabrication
de génériques pour les produits de 2° et 3° ligne de
traitement sortis récemment, et l'accès pour des pays à
ces traitements. L'Inde, le Brésil (et la Thaïlande) sont en crise
à cause de ça. Il est à craindre que ce problème va
s'étendre sur l'ensemble du globe. Encore faut-il que les laboratoires
ne trouvent pas des stratagèmes pour prolonger la protection de leurs
produits. L'exemple de Novartis et Sanofi Avantis et son bras de fer qui
l'oppose à l'Inde en sont un exemple criant. En attendant Cipla pourrait
se voir copier sa Triomune par des grands laboratoires du Nord. Le monde
à l'envers. La firme Cipla a donc déposé un brevet pour
court-circuiter les velléités des multinationales.
Il est acquis que grâce aux génériques
des milliers de patients ont pu être mis sous traitement. Ne soyons pas
pour autant naïfs. Ces sociétés convoitent les parts de
marchés de leurs concurrents occidentaux oubliant de faciliter
l'accès dans leur propre pays (en Inde par exemple). D'autre part, comme
le montre le graphique ci-contre, ces sociétés font elles aussi
de jolis bénéfices grâce au sida et sont pour certaines
cotées en bourse comme Aspen Pharmacare. Ciplan rend
régulièrement des comptes à ses actionnaires. Les
activistes proposent d'ailleurs un boycott des sociétés
génériques qui ont des actionnaires au profit de celles qui n'en
ont pas.


7 - Les obstacles à l'accès
universel
Lors de l'assemblée du millénaire que les
Nations Unis ont tenue en 2000 des objectifs pour le développement ont
été adoptés. La communauté internationale a
décidé qu'il fallait en fixer 8 pour 2015 :
· Réduire de moitié l'extrême
pauvreté et la faim
· Promouvoir l'égalité des femmes
· Assurer l'éducation primaire pour tous
· Réduire de 2/3 le taux de mortalité des
enfants de moins de cinq ans
· Rédu ire de 3/4 le taux de mortalité
maternelle
· Assurer un environnement durable
· Mettre en place un partenariat mondial pour le
développement
· Stopper la propagation du VIH / sida et du paludisme
Selon la Banque Mondiale ou le Programme des Nations Unies
pour le développement (PNUD) aucun des pays ou la prévalence du
VIH est élevée n'atteindra ces objectifs. L'Afrique subsaharienne
est si pauvre, si affligée par des maladies contagieuses de toutes
sortes, si limitée en capacité humaine et si dépourvue
d'infrastructures qu'il est vraisemblable qu'aucun pays de la région n'y
arrivera.
Le sommet du G8 tenu en juillet 2005 n'a d'ailleurs pas fait
grand-chose pour améliorer la situation, car malgré les
déclarations de bonne intention consistant à fixer à 0,7 %
du PNB le chiffre correspondant au niveau légitime de l'aide
étrangère des pays industrialisés, aucun pays ne l'a
atteint, exception faite la Norvège, le Danemark, la Hollande et le
Luxembourg. On est en droit de se demander pourquoi ces pays à
l'économie plus petite y sont parvenus, au contraire de pays riches
à l'économie florissante. Dans l'optique du 0,7 %, Tony Blair a
demandé que l'aide à l'Afrique soit doublée d'ici 2010,
qu'elle passe donc de 25 milliards de dollars à 50 milliards de dollars.
C'est peine perdue. Les Etats-Unis et le Japon sont loin du compte. L'aide de
ce pays se chiffre à 0,18 % du PNB et, parmi les nations
industrialisées, seuls les Etats-Unis font moins bien que lui. L'ONUSIDA
a récemment rendu public un rapport décisif dans lequel elle
indique que, en 2008, soit deux ans avant cette échéance, la
lutte contre le VIH/sida exigera à elle seule 22 milliards de dollars
par année, pour les pays d'Afrique surtout.
Ce qui ressort d'emblée, c'est que la cible
fixée par le G8 est inacceptable parce qu'elle n'est pas assez
élevée. Où est l'argent pour combattre la pauvreté,
la fa im, le paludisme, la tuberculose et d'autres maladies, sans parler de la
mortalité infantile et maternelle ? C'est de 50 milliards de dollars de
plus par année d'ici 2010 qu'il faut. Ce qui correspond tout simplement
au 0,7 % du PNB à laquelle tous les gouvernements occidentaux sont
théoriquement tenus. Les Etats-Unis ont promis des miettes en
s'engageant à doubler leur aide à l'Afrique, qui passerait de 3
milliards aujourd'hui à 6 milliards en 2010, au lieu des 16 milliards
qui constitueraient leur juste part.
Pour rappel en 2005 les dépenses militaires mondiales
ont franchit le cap de mille milliards de dollars par année. Par rapport
au besoin de 50 milliards de dollars d'aide à l'Afrique, le rapport est
de vingt contre un.
Tout au long des années 80 et 90, la question de la
dette africaine a fait l'objet d'incessants débats dans le cadre des
conférences internationales. Tout le monde savait que de nombreux pays
africains consacraient plus d'argent au remboursement de dettes
bilatérales et multilatérales qu'à la santé ou
à l'éducation, voire aux deux réunis.
En juillet 2005 le G8 a annulé des dettes de 40
milliards pour 18 pays. Le gouvernement de la Zambie a annoncé qu'une
part des économies servira à l'achat d'antirétroviraux et
des médicaments plus récents contre le paludisme. Malgré
cette « ristourne >> les 200 milliards de dollars que doit toujours
l'Afrique hypothèquent l'avenir du continent.
Au sein de l'Union européenne, chaque vache a droit
à deux dollars de subvention par jour ; pendant ce temps, de quatre
à cinq cents millions d'africains disposent de moins d'un dollar par
jour pour vivre.

« 3 by 5 »
L'expansion de la maladie continue à augmenter. A ce
terme ce sont donc dix, vingt millions de malades à mettre sous
traitement. L'initiative « 3 by 5 >> est une stratégie
à court terme qui a surtout eu pour mérite de lancer le
processus. Mais ce n'est en aucun cas un objectif final, car aucune projection
dans l'avenir n'a réellement été faite. Il y a un manque
criant de vision politique à long terme.
De plus, les critères d'accès sont discutables, et
une absence d'évaluation de l'accès au suivi biologique et para
clinique indispensable à des soins au long cours de qualité...
D'autre part « 3 by 5 >> n'a pas tenu ses
promesses et a abusivement augmenté les chiffres (par exemple, en
incluant les chiffres du Brésil, alors que les malades étaient
déjà sous traitement grâce au gouvernement). Toute fois, il
a montré qu'être ambitieux pour les pays du Sud était
possible et réalisable.

Prix des médicaments de 2ème
ligne
Le prix moyen des schémas thérapeutiques de
2° intention reste insupportable dans les pays à revenu faible ou
intermédiaire, ou peu ou pas de médicaments
génériques pré qualifié par l'OMS sont
disponibles.
En 2006 une association DDI + ABC + Lopinavir-Ritonavir, le
schéma le plus couramment utilisé coûtait en moyenne 1698
dollars dans les pays à faibles revenus et 4735 dollars dans les pays
aux revenus intermédiaires. L'association TDF+ ABC + Lopinavir
-Ritonavir coûte en moyenne 1572 dollars par personne et par an dans les
pays à faibles revenus et 4698 dollars par personne et par an dans les
pays aux revenus intermédiaires. Les prix réellement
pratiqués pour les schémas de 2° intention varient beaucoup
d'un pays à l'autre. Ainsi l'association Tenofovir + Abacavir +
LopinavirRitonavir coûte en moyenne 1600 dollars par personne et par an
en Afrique du Sud contre 7613 dollars en El Salvador.

Les brevets
Début 2000, une année de traitement coûte
environ 12 000 dollars par personne, une somme élevée, mais que
les systèmes de santé des pays riches peuvent assumer. Pas les
pays les plus pauvres, sans infrastructures sanitaires. Cependant les firmes
pharmaceutiques s'affirment incapables de baisser leurs tarifs, par crainte de
ne plus pouvoir amortir leurs investissements (l'exemple récent d'Abbott
en Thaïlande en fait douter).
Salué comme un quasi-miracle au Nord,
l'avènement des trithérapies ajoute une inégalité
de plus à la mondialisation et il devient insupportable de voir des pays
entiers dévastés par l'épidémie alors même
que les traitements existent.
Les solutions à ce drame existent pourtant. Il est
évident que la copie peut permettre d'endiguer ce fléau. En Inde,
où les brevets sur les médicaments n'existaient pas, les
sociétés Cipla et Ranbaxy étaient capables de produire des
trithérapies à coût très faible. Mais encore faut-il
pouvoir les acheminer aux populations concernées. En l'occurrence, la
règle est simple : il est impossible de distribuer une copie de
médicament encore sous
brevet dans un pays reconnaissant ces mêmes brevets. En
théorie, cette limitation ne devrait pas poser de problèmes car
les pays les plus pauvres, ne disposant pas d'industrie pharmaceutique, n'ont
aucune raison de légiférer dans ce domaine. L'Inde, par exemple,
a montré que les pays en voie de développement savaient se
prémunir en refusant l'accord des brevets sur les médicaments,
encourageant ainsi une industrie de copie à bas prix. En théorie,
il ne devrait donc pas y avoir d'obstacles à l'acheminement de clones
peu onéreux de trithérapies vers les pays les plus touchés
par la maladie, Afrique Noire en tête.
Malheureusement, alors que l'épidémie du Sida
explose, de façon concomitante se met en place un chantier international
crucial : en 1994 les membres de l'Organisation Mondiale du Commerce (OMC) ont
posé les bases d'un accord sur les Aspects de droits de
propriété intellectuelle qui touchent au commerce (ADPIC). Ce
traité vise à établir un seuil minimum de protection des
droits de propriété intellectuelle dans le monde entier, dans
tous les secteurs. Dans le cas des médicaments, tous les pays doivent se
conformer à la même norme et octroyer un monopole de 20 ans sur
toute nouvelle molécule. Voilà les nations le plus pauvres
sommées de se conformer aux mêmes critères que les pays
riches. Voilà le Botswana, dont 35 % des 1,6 millions d'habitants sont
séropositifs, tenu de reconnaître les brevets sur les
médicaments, et de se priver de l'accès à des copies de
traitements à prix réduit alors même qu'il ne peut financer
le coût des molécules originales. C'est à peine si un
délai de grâce a été accordé à
certaines nations pour transposer l'accord dans leurs législations
nationales : si les pays développés ont dû
obtempérer dès 1996, certains pays en développement
(l'Inde par exemple avait jusqu'en 2005) et les pays les moins avancés
jusqu'en 2016.
La crise du Sida révèle l'absurdité d'un
tel traité international. Comme s'il s'agissait d'accepter de rayer de
la carte des populations entières au nom d'un brevet tout puissant. Le
brevet s'érige en principe de toute chose, et la santé est
subordonnée à son fonctionnement harmonisé sur toute la
planète. C'est là une évidente perversion de la
propriété i ntellectuel le censée promouvoi r les
avancées technolog iq ues et scientifiques. Qui pourrait soutenir que
les brevets existent pour donner à des entreprises un pouvoir de vie ou
de mort sur des populations entières ?
Sous la pression de l'opinion publique, des associations et
des pays les plus pauvres, l'OMC s'emploie désormais à amender
cet accord scélérat. Ce sera la « déclaration de Doha
» de novembre 2001, où les membres de l'Organisation affirment la
prééminence du droit à la santé sur le droit du
commerce et confirment le rôle fondamental des licences obligatoires : en
cas d'urgence sanitaire, les états peuvent recourir à cet outil
pour autoriser un laboratoire à copier une molécule pourtant
couverte par le brevet. C'est la stratégie adoptée, avec
succès, notamment par le Brésil. Cependant cette
expérience n'est pas exportable, car il impose la présence sur le
territoire d'une industrie pharmaceutique capable de produire des
médicaments. Or la majorité des pays les plus touchés par
l'épidémie de Sida n'en dispose pas. Dans cette situation, la
licence
obligatoire - par essence limitée au pays qui
l'édicte - n'est d'aucune utilité et l'importation des copies en
provenance de pays tiers reste alors la seule voie possible.
Au moment de la déclaration de Doha, les états
membres de l'OMC avaient bien conscience de cet écueil, mais ils avaient
laissé à une négociation ultérieure le soin de
régler ce point pourtant essentiel. Pendant deux ans, les Etats-Unis
poussés par des laboratoires pharmaceutiques feront obstacle à
tout arrangement et refuseront de signer un accord autorisant l'import-export
de copies à bas prix en cas de nécessité sanitaire. Tous
les prétextes seront invoqués : crainte de voir des copies
destinées à des pays pauvres revenir en contrebande dans les pays
riches ; risque de laisser des pays en développement dotés d'une
industrie pharmaceutiques dupliquer des molécules de confort, comme le
Viagra ; inquiétude de perdre le marché des riches vivant dans
les pays pauvres. A force d'entêtement, l'industrie pharmaceutique a fini
par démontrer l'inverse de ce qu'elle prônait, la preuve
étant faite que ce n'était pas les médicaments de demain
que les laboratoires défendaient, mais bien leurs marchés
d'aujourd'hui.
En août 2003, à quelques jours du début
du sommet de l'OMC à Cancun, au Mexique, les Etats-Unis ont dû
enfin accepter un mécanisme de licence obligatoire internationale,
permettant aux pays ne disposant pas de capacités de productions
pharmaceutiques d'importer des copies de molécules en provenance de pays
tiers à prix bradés.
A cette logique industrielle, les industriels ajoutent un
paramètre pour justifier leur incessante demande de protection
supplémentaire : les coûts de recherche et développement
s'envolent depuis plusieurs années, conséquence de la
complexité scientifique croissante du domaine. En 1975, il fallait en
moyenne 138 millions de dollars pour mettre sur le marché un nouveau
traitement ; en 2000, 802 millions, soit une augmentation de près de 500
%. . .(les chiffres étant communiqués par les laboratoires
eux-mêmes). A l'OMC, au congrès américain ou au
ministère de la santé à Paris, ce sont les données
fournies par l'industrie qui servent de référence. C'est pourtant
la clef de toute politique de santé publique : sans évaluation
honnête des dépenses en recherche et développement, il est
impossible de déterminer si un prix est abusif ou légitime, s'il
faut ou non durcir le régime de protection dont
bénéficient les médicaments.
Entre 1975 et 1999, sur 1400 nouveaux médicaments
commercialisés, seuls 13 concernaient les maladies tropicales
infectieuses qui sont pourtant la principale cause de mortalité et de
morbid ité dans le Sud.
L'industrie renvoie de son côté la
responsabilité de l'injustice en terme d'accès au traitement sur
les gouvernements, notamment du Sud, incapables d'offrir à leurs
populations une sécurité sociale digne de ce nom. L'argument est
juste, mais l'hypocrisie des Etats du Nord, incapables de brider les efets
dévastateurs d'un brevet tout puissant dans un domaine aussi sensible
que la santé est tout aussi honteux.
La responsabilité de certains
gouvernements
Si les groupes pharmaceutiques ont une responsabilité
écrasante, certains gouvernements ne doivent pas être
dédouanés. Lorsque l'on parle de difficulté d'accès
aux traitements, il est inconcevable de ne pas évoquer la
responsabilité de nombreux gouvernements à travers le Monde en
terme de manque de volonté politique pour l'accès au plus grand
nombre, la gratuité, le recours aux génériques le cas
échéant. Responsabilité également en terme de
discrimination vis-à-vis de certains patients : usagers de drogues,
homosexuels, prostituées. Responsabilité en terme de message de
prévention. Responsabilité en imposant des taxes aux
molécules originelles proposées à l'origine à prix
coûtant. Juste quelques exemples pour illustrer cet aspect.
Les habitants souffrent d'un double fléau. Les pays
donateurs n'aiment pas le président Mugabe donc ne le soutiennent pas.
D'autre part la situation se détériore à cause d'une
politique gouvernementale catastrophique.
Le taux de prévalence se situe autour de 25 %. A cause
de l'instabilité du pays, la lutte efficace contre la pandémie
est impossible. En 2005 Robert Mugabe aura ordonné le rasage des
bidonvilles zimbabwéens entraînant un déplacement massif de
la population, mais aussi perturbé le traitement d'un grand nombre de
personnes infectées par le VIH.
Malgré des structures hospitalières qui n'ont
rien à envier aux pays les plus riches et qui sont exhibées aux
visiteurs occidentaux comme l'hôpital de Shanghai construit lors de
l'épisode du SRAS, il est manifeste que le nombre de cas de sida est
très largement sous estimé comme ce fût le cas dans les
plus belles heures de l'Union Soviétique et que l'ensemble de la
population n'a pas accès aux traitements. Un manque de transparence et
de reconnaissance d'une très grave affaire de sang contaminé
aggrave la confusion (le gouvernement chinois mettant toute la
responsabilité sur les usagers de drogues...).
Le Swaziland

Le Swaziland est un tout petit Etat enclavé dans
l'Afrique du Sud. Il a une population d'environ 1,1 million d'habitants et une
dette extérieure de 145 millions de dollars. C'est l'un des pays les
plus pauvres d'Afrique, donc du monde, et l'un des plus touchés par la
pandémie du sida. L'année dernière, le pays a
été frappé par une grande sécheresse qui a conduit
le gouvernement à décréter l'état de «
désastre national ». 350 000 personnes, soit environ le tiers de la
population du pays, survivent grâce à l'aide alimentaire.
Rien de tout cela n'a empêché le roi de ce pays,
Mswati III, âgé d'une trentaine d'années, dernier monarque
absolu du continent, de construire des palais pour ses dix épouses et
deux fiancées, pour un coût global de 14 millions de dollars. Il a
célébré ensuite son anniversaire pour près d'un
million de dollars. Et s'est offert un avion à 45 millions de dollars
(« pourquoi la reine d'Angleterre aurait un avion et lui n'en aurait pas ?
»), mais il a dû y renoncer devant le tollé que cela a
soulevé chez les bailleurs de fonds qui font vivre son pays.
Mais Mswati III aime voyager. On dira que c'est normal pour
un roi qui aime son pays et travaille pour le bonheur de son peuple. Cette
année, il a déjà été en Malaisie, à
Singapour, en Arabie saoudite, et il vient de rentrer d'un voyage en Ouganda et
au Kenya. Ces voyages ont coûté 610 000 dollars (plus de 300
millions de francs CFA) aux contribuables du Swaziland, soit huit fois plus que
ce qui était prévu dans le budget. Mais ce montant n'inclut pas
le coût de la location des avions qu'il utilise pour voyager. Mswati III
ne voyage jamais sans une trentaine de personnes autour de lui. Parce que la
tradition de son pays veut que le roi voyage toujours entouré de
guerriers et de membres de sa famille.


L'Afrique du Sud
Un pays ou la lenteur de la mise en oeuvre des programmes de
traitement pour les sudafricains vivant avec le sida est préoccupant :
plus de 6 millions de personnes infectées,

soit le nombre absolu de cas le plus élevé au
monde. Au moins 900
sud africains meurent chaque jour du SIDA. L'Afrique du Sud
aurait
besoin d'une véritable stratégie pour lutter contre
cette épidémie qui
dévore ses enfants : de leaders qui parlent du SIDA,
informent sur
comment se protéger et comment ne pas se contaminer ;
d'un
gouvernement qui donne des traitements à tous ceux qui en
ont
besoin et qui soit prêt à
créer un véritable leadership pour lutter
contre le SIDA. Un appui sur les associations dont Treatment
Action Campaign (TAC) et de son leader charismatique Zackie Achmat qui fournit
depuis 1998 un travail incessant pour obtenir un accès
généralisé aux ARV, et à des prix abord ables.
A la place de cela, les propos délirants tenus par son
ministre de la santé Manto Tshabalala y sont pour quelque chose. L'ail,
l'huile d'olive et les patates douces seraient plus importants que les
antirétroviraux ! Le Président lui-même fait du
négationnisme. Thabo Mbeki soutient que les malades souffrent des effets
secondaires des antirétroviraux et non du SIDA ! Cette politique a
pesé dans la non atteinte des objectif de « 3 by 5 » et c'est
cette politique qui tue en Afrique du Sud. Pourtant l'Afrique du Sud est riche
et capable de produire. Le transfert de technologie des grandes firmes
pharmaceutiques comme BMS, Gilead... se fait en direction de l'Afrique du Sud
justement. Tous recourent aux services du laboratoire Aspen Pharmacare.


La Russie
L'accès aux traitements, malgré l'aide du Fonds
Mondial reste limité. En 2005 seulement 5 % des patients
nécessitant un traitement avaient accès aux
antirétroviraux. Taux plus faible que dans certains pays en voie de
développement comme la Zambie (27 %), le Malawie (20 %) ou l'Ouganda (51
%). La pérennité du système n'est pas assurée.
Surtout si les programmes d'accès aux traitements donnent la
priorité aux personnes dites « stables » donc surtout pas aux
travailleurs du sexe ou aux usagers de drogues.
Les dirigeants russes poursuivent l'éradication
d'opposants politiques par le biais de méthodes d'un autre âge
comme l'empoisonnement, et mènent une politique répressive en
Tchétchénie. Difficile de croire que ces mêmes dirigeants
puissent d'un autre côté avoir de la compassion pour les victimes
du sida et vouloir aider les toxicomanes particulièrement touchés
dans ce pays.
La situation en Inde est pathétique. Alors que ce pays
est le plus touché dans le monde (5,1 millions de personnes
infectées) et que les plus grands fabricants de médicaments
génériques sont indiens, le VIH continue de faucher
énergiquement des millions de vies et les séropositifs ne
reçoivent pas de traitements. Les activistes indiens rappellent en effet
qu'en Inde, 500 000 personnes ont besoin d'un traitement contre le SIDA mais
n'ont pas les moyens pour le payer. La promesse formulée il y a un an
par le gouvernement indien de traiter 100 000 malades dans les zones les plus
affectées n'a toujours pas été ten ue.
Manifestement le gouvernement indien - à l'inverse du
Brésil - a privilégié le développement industriel
au détriment du développement du système de santé.
Le générique est souvent cité comme la solution pour que
le plus grand nombre ait accès aux traitements. La situation en Inde met
un bémol à cette démonstration. La situation risque
même de s'aggraver avec sa nouvelle loi sur les accords de
propriété intellectuelle, le gouvernement indien étant en
train de réduire considérablement la possibilité de
produire des copies génériques de médicaments. Le
gouvernement indien défend sur la scène internationale
l'idée d'un accès universel aux traitements alors qu'il ne
l'assure même pas pour son pays. Précisons que l'Inde sera
dès 2015 la troisième puissance économique après
les Etats-Unis et la Chine devançant le Japon

La défaillance du système de
santé
Les guerres, les déplacements de population, ont dans
certains pays fait voler en éclat les systèmes de santé ;
ailleurs, les politiques prônées par le Fonds Monétaire
International (FMI) et la Banque Mondiale, avec leurs exigences de
réductions drastiques des dépenses publiques, ont conduit
à un résultat à peu près identique. L'état
des routes, l'impossibilité de se déplacer faute de moyens de
transports, les centaines de kilomètres qui séparent les patients
du premier centre de soin, l'absence de structure, le manque de médecins
contribuent aussi à un non accès au traitement. Les conditions de
vie d'un séropositif Sud africain est atroce, rythmée à la
fois par la stigmatisation, la peur et la pauvreté.
Le Burundi par exemple compte environs 400 médecins
mais parmi eux la moitié exerce en dehors du pays. En France il y en a
110 (source MSF)! Face à cette pénurie, la stratégie est
d'impliquer le personnel paramédical dans la prescription
d'antirétroviraux. Sans compter ceux qui sont « aspirés
» par le organisations mondiales : ONUSIDA, OMS...
En mai 2007, MSF lançait un cri d'alarme à
l'attention des donateurs et des gouvernements pour qu'ils offrent des
salaires, des budgets et des formations, et aussi pour qu'ils revoient les
règles restrictives de finances qui bloquent l'expansion du personnel
soignant dans chaque pays de la région. En attendant, les listes
d'attente de traitement en Afrique Australe elles augmentent en raison d'un
manque de personnel soignant. L'année 2000 marque le début du
programme de MSF en Afrique du Sud dans la banlieue noire pauvre de Khayelitsha
(500 000 habitants) et depuis 2001, 7262 adultes et enfants ont
été traités. Cependant aujourd'hui, les cliniques sont
saturées. Entre mai et décembre 2006, le déclenchement
mensuel d'antirétroviraux dans les cliniques de cette province du Cap a
chuté de 60 %. Sans davantage de personnel, les listes d'attentes se
développeront. 400 patients qualifiés pour une mise sous
traitement attendent. Les autorités de santé estiment qu'il
faudrait 466 infirmières qualifiées d'ici 2010. Actuellement il
n'y en a que 71.
Au Mozambique la situation est la même. MSF rapporte
dans la région de Maputo une chute de 30 % des mises sous traitement
entre 2005-2006. Dans la zone de Malavane, des patients doivent attendrent
jusqu'à deux mois pour commencer un traitement en raison du manque de
médecins et d'infirmières - et nombreux sont ceux qui sont morts
dans l'attente. L'objectif du Mozambique pour 2007 est de fournir des
antirétroviraux pour 95 000 personnes, mais le manque de ressources
humaines est identifié comme obstacle principal pour réaliser ces
plans. Le ministère de la santé a calculé que le
personnel additionnel suivant serait nécessaire : 130
médecins, 125 « techniciens de médecine », 380
infirmières et 200 aides infirmières, ainsi que 90 postes en
pharmacies et 29 personnels de laboratoires.
Le Lesotho compte 89 médecins pour une population de
1,8 millions d'habitants. MSF a délégué les soins VIH
autant que faire se peut aux infirmières, mais dans tout le pays 54 %
des postes d'infirmières sont actuellement vides - laissant le travail
à des aides infirmières ayant seulement deux ans
d'expérience. 80 % des médecins exerçant au Lesotho
proviennent d'autre pays africains dans l'attente d'obtenir un travail en
Afrique du Sud ou ils peuvent gagner d'avantage.
Idem dans la zone de Thyolo au Malawi ou MSF traite 7000
patients VIH. Ce chiffre devrait passer à 10000 vers la fin de
l'année, mais le programme est dans l'impasse par manque de personnel
soignant. Un aide médical peut voir jusqu'à 200 patients par jour
ce qui ne permet pas d'assurer des soins de qualité.
Selon différentes projections, il manquerait en
Afrique subsaharienne un million de
professionnels de santé, alors
que 20 000 émigrent chaque année.
La limite législative :
Il est important de parler de lois également qui vont
très certainement limiter le dépistage et donc la mise sous
traitement. Des lois qui condamnent à la peine capitale une personne
connaissant son statut et contaminant son partenaire (Burundi) ou
l'emprisonnement des homosexuels (Côte d'Ivoire). Globalement, dans la
plupart du territo ire sub-saharien, l'homosexualité est un sujet tabou
de discussion publique. Le statut légal de l'homosexualité y est
assez vague, c'est souvent les préjugés locaux qui prennent le
dessus pour interpréter la loi arbitrairement. La majorité des
pays de l'Afrique
occidentale et orientale ont criminalisés
l'homosexualité. Dans l'Afrique méditerranéenne, les
dispositions législatives criminalisant sur l'homosexualité sont
en grande partie basées sur la Charia.

La limite culturelle :
Egalement les messages peu lucides des églises ou des
guérisseurs et autres marabouts catastrophiques en terme de
prévention.
La limite financière :
Enfin, les firmes pour la plupart proposent maintenant des
antirétroviraux à prix coûtant. Il est regrettable de
constater que de nombreux pays en voie de développement en profitent au
passage pour imposer des taxes (parfois jusqu'à + de 40 %) qui
réduisent les efforts faits en amont. Tous les pays receveurs devraient
abandonner cette politique. C'est ce que tente d'obtenir le réseau
RESAPSI en Afrique.
En Europe, les médicaments ARV sont
généralement commercialisés 1 an après que la FDA
(Found & Drug Administration) ait donné son feu vert pour le
marché Nord américain. L'Agence Européenne (EMEA) accorde
souvent l'autorisation avec des indications plus limitée (patients en
échec d'une première ligne). Lorsque l'AMM européenne est
enfin obtenue, chaque pays du Vieux Continent dispose d'une date de
commercialisation différente. Cela va du lendemain pour l'Angleterre
à deux mois pour la France, voire plus pour d'autres pays
européens. On comprend aisément que dans des pays en
développement où les structures administratives sont moins bien
structurées pour des raisons diverses les délais soient bien plus
longs. Comme le souligne Gilead, entre le dépôt d'enregistrement
de ses molécules et la commercialisation locale, il s'écoule
entre 3 mois à 3 ans. Cela ne contribue pas à la mise à
disposition rapide du traitement aux patients fût il a prix
coûtant.
Registrations in Access Program Countries
20
71
6
17
51
29
Approved Submitted
To be filed

Viread
Truvada
8
97 Access Countries
Ces déficiences illustrent que le coût du
médicament n'est pas le seul frein à l'accès universel.
N'oublions pas que dans le VIH, l'adhérence au traitement doit
être exceptionnelle et atteindre plus de 95 % pour être pleinement
efficace et limiter l'émergence de mutations qui hypothèqueraient
le traitement en cours et certaines options ultérieures.
Dans les pays industrialisés, des structures
spécifiques (les CISIH en France) ont été crées
pour offrir au patient une prise en charge optimale et
spécialisée. Des collaborations muti-disciplinaires sont
reconnues comme capitale. Des consultations infirmières ont
été développées pour soutenir les patients et
renforcer l'adhérence. Toutes ces structures n'existent pas dans de
nombreux pays.
L'accès aux bilans immuno-virologiques, examens
biologiques, pharmacologiques, complémentaires (Scanner,
radiographies...) est indispensable, mais trop onéreux ou tout
simplement inexistante dans certains pays.
En plus des antirétroviraux et de la continuité
d'accès, la rupture des stocks de médicaments est dramatique dans
certains pays du Sud.

La transmission mère enfant
|
|
|
Il me paraît important d'aborder cet aspect. La
transmission du VIH se fait aussi dans le cadre de la grossesse surtout durant
le troisième trimestre avec un risque maximal pendant la
délivrance et dans une moindre mesure in utero. Dans le meilleur des
cas, les protocoles à base de Névirapine (Viramune) peuvent
permettre de limiter cette transmission du VIH de la mère à
l'enfant, mais cette molécule à barrière
génétique faible (jamais utilisée en monothérapie
dans les pays industrialisés pour cette raison) - génère
des mutations (15 à 67 %) dans le cadre des essais
réalisés dans les pays en voie de développement. Cela est
d'autant plus dramatique lorsque l'on sait que lorsque la mère ou les
enfants auront besoin d'un traitement, la trithérapie accessible pour 80
% des patients est la «Triomune » fixe dose contenant de la 3TC + D4T
mais aussi et surtout de la Névirapine. Il est clair que dans ce
contexte de mutations acquises à la Viramune lors du protocole de
prévention de la transmission de la mère à l'enfant le
traitement ne sera que partiellement actif et reposera seulement sur la
bithérapie 3TC + D4T. Dans le meilleur des cas, malgré la
présence d'une prévention antirétrovirale, rappelons que
l'allaitement maternel est responsable d'un taux de transmission de VIH
majoré (36,7 % dans une étude Kenya / Jama en 2000). Ce dernier
est néanmoins difficile à proscrire pour des raisons culturelles,
sanitaires et économiques, ainsi que des risques de discriminations
envers la mère infectée. Cet exemple illustre là encore
les limites et le fait que malgré un traitement efficace disponible
d'autres facteurs contribuent à rendre la prise en charge du VIH - qui
doit être globale - difficile dans tous les pays et davantage dans
certains. Si les femmes étaient traitées en trithérapie
pendant la grossesse, l'accouchement et l'allaitement, on ne se poserait plus
de problèmes...

Impossible de ne pas évoquer le rôle des
médias en terme d'obstacle à la compréhension lorsque l'on
aborde ce sujet. Le rôle de la presse est bien sûr indispensable et
il ne s'agit nullement ici de le remettre en cause. Nous sommes tous
attachés à la liberté de la presse. Flle attire
l'attention sur des évènements qui pourraient rester dans l'ombre
ou passer sous silence : l'exemple récent du bras de fer qui oppose
certaines firmes comme Abbott, MSD ou Novartis au Brésil, à la
Thaïlande ou à l'Inde. Flle se devait de couvrir l'actualité
qu'était le procès de Pretoria. Néanmoins l'article
proposé et tiré de l'International Herald Tribune paru en marge
de la Conférence sur les Rétrovirus et les Infections
Opportunistes : CROI 2007 (l'évènement annuel de portée
mondial de la communauté médicale et scientifique) est assez
symptomatique et démonstratif du rôle «
délétère » que peut avoir la presse et la
responsabilité qu'est la sienne dans l'entretien de cette vision
simpliste qu'il y a les bons (les patients), les méchants (les
laboratoires) et les redresseurs de torts (les activistes). Que les entreprises
du médicament en général fassent des
bénéfices (parfois conséquents) est tout à fait
normal comme toute entreprise commerciale. Les sociétés qui
fabriquent et commercialisent des scanners, des IRM font aussi des
bénéfices. Si leurs produits étaient plus accessibles, les
dépistages des cancers seraient dispensés de façon plus
précoce et répétée. Le dépistage est tout
aussi important que les médicaments. Qu'au sein de la
spécialité VIH les bénéfices soient importants,
c'est un fait (qui en doutait) mais pas plus qu'en cancérologie. De
nombreux médecins et chercheurs ont jalousé et reproché
à leurs confrères sidénologues de bénéficier
de plus de moyens dans la lutte contre le VIH. Mais les avancées ont eu
des retombées importantes dans d'autres spécialités.
D'autre part ce n'est pas tant le trop du VIH mais le pas assez d'autres
spécialité qui étaient dommageables. Je ne pense pas que
ce soit intellectuellement honnête d'opposer systématiquement les
bénéfices des laboratoires au problème de l'accès.
Mettre en avant leurs résultats sur le marché de la bourse est
facile. Les fabricants de génériques font aussi des
bénéfices. Le problème est donc bien plus compliqué
que cela. Il n'en demeure pas moins que les laboratoires doivent poursuivre
leurs efforts ou passer par des relais. C'est ce que font déjà
certains laboratoires lorsqu'ils ne sont pas implantés sur certains
continents. Ils soumettent la promotion de leurs molécules à
d'autres laboratoires (concurrents sur le marché des pays du Nord). La
presse devrait être plus didactique et pédagogique et
présenter ce sujet sous différents angles et non pas toujours
dans le même sens. J'ai été surpris de constater que de
nombreux médecins dans le VIH ou mêmes certains membres
d'associations n'aient qu'une connaissance très limitée de ce
sujet sans connaître tous les facteurs qui limitent l'accès aux
traitements. Par contre que l'industrie se fasse beaucoup d'argent et
défende bec et ongles ses brevets est bien ancré dans les esprits
(et pas vraiment faux).
Les associations quant à elles trouvent que les
médias soulignent et saluent trop souvent « la bonne santé
des laboratoires », félicitent l'industrie pharmaceutique de ses
bons résultats. Par ailleurs, très peu de journaux mettent en
avant le vécu des malades, le travail des associations et leurs
avancées. La plupart du temps, les médias sont à
l'affût de « scoops » en matière de traitement et de
vaccin, mal compris et qui créent des ravages chez les patients
infectés par le VIH.

WHAT (RED) IS
(RED) was created by Bono and Bobby Shriver, Chairman of DATA
to raise awareness and money for The Global Fund by teaming up with the world's
most iconic brands to produce (PRODUCT)RED branded products. A
percentage of each (PRODUCT)RED product sold is given to The Global
Fund. The money helps women and children affected by HIV/AIDS in Africa.
What's the meaning of the parentheses or brackets? Well, we
call them "the embrace." Each company that becomes (RED) places its logo in
this embrace and is then elevated to the power of red. Thus the name --
(PRODUCT)RED.
You, the consumer, can take your purchase to the power of
(RED) simply by upgrading your choice. Thus the proposition:
(YOU)RED. Be embraced, take your own fine self to the power of
(RED). What better way to become a good-looking samaritan?!
HOW (RED) WORKS

8 - Les initiatives prometteuses

Unitaid, des médicaments pour tous. Le 1er juillet
2006, la France a été le premier pays à mettre en place
une «contribution internationale de solidarité» sur les
billets d'avion. Son produit alimente Unitaid, un mécanisme
destiné à faciliter l'accès aux médicaments pour
les populations des pays les plus pauvres. Pour assurer un financement durable
des programmes de santé publique, la France et le Brésil,
rejoints par le Royaume-Uni, la Norvège et le Chili, ont pris
l'initiative de créer une facilité internationale d'achats de
médicaments, Unitaid. L'objectif est de fournir aux pays en
développement, à des coûts bien plus faibles que dans les
nations développées, des moyens de lutte contre le sida, la
tuberculose et le paludisme dans les rég ions les plus pauvres. Ce
programme repose, pour l'essentiel, sur un mode de financement innovant, stable
et prévisible : une contribution de solidarité sur les billets
d'avion, que la plupart des pays participant à Unitaid se sont
engagés à mettre en oeuvre. Une contribution variable selon la
destination
En France, elle s'applique à tous les vols au
départ des aéroports français, mais elle varie selon la
destination et la classe de voyage. Ainsi, pour les vols nationaux et
européens, les passagers paient 1 € en classe Economique et 10
€ en Première ou en classe Affaires. Pour les long-courriers, ils
s'acquittent d'un supplément de 4 € en classe Economique et de 40
€ en Première ou en Affaires. Outre les membres fondateurs,
Madagascar, Maurice, Chypre, la Corée du Sud, l'Espagne ou la Pologne
ont déjà rejoint le projet. Et, à ce jour, 24 autres pays
ont déjà engagé les procédures pour contribuer
à ce fonds de solidarité.
Grâce à ce soutien international, le budget
d'Unitaid devrait dépasser 300 millions d'euros dès 2007, et
continuer à progresser très régulièrement par la
suite. Selon Bruxelles, il devrait générer 560 millions d'euros
par an. Les premières actions sur le terrain Unitaid, qui s'appuie sur
l'Organisation mondiale de la santé (OMS), a décidé de se
concentrer dans un premier temps sur les traitements destinés aux plus
jeunes. A l'heure actuelle, peu de médicaments sont accessibles aux
enfants malades du SIDA. Selon les sept organisations formant le mouvement
mondial pour l'enfance, cette absence de soins signifie que la plupart d'entre
eux sont condamnés à mourir avant l'âge de 5 ans. Une
série d'interventions prioritaires ont déjà
été identifiées : des formulations pédiatriques
contre le sida (pour traiter 100 000 enfants en 2007) et la tuberculose (pour
en soigner 150 000 en 2007) ; des antirétroviraux de deuxième
génération pour aider les patients infectés par le sida
qui ont développé des résistances aux
thérapeutiques de base ; de nouvelles formes de médicaments
contre le paludisme à base d'artémisinine ; des traitements
contre la tuberculose multi et ultra résistante.
Cette initiative Unitaid a déjà permis
d'engager 50 millions de dollars pour les antirétroviraux
pédiatriques et 55 millions de dollars pour les antirétroviraux
de seconde ligne dans les pays du Sud.
Ce dispositif doit être la première étape
vers une fiscalité internationale. Mais il faut rester vigilant sur
plusieurs points. Les Etats européens doivent poursuivre leurs efforts
pour porter leur aide publique au développement à 0,7 % de leur
richesse nationale (PNB), comme ils s'y sont engagés - sans
intégrer cette nouvelle contribution dans leurs calculs. Par ailleurs,
l'ONU évalue à 50 milliards de dollars les financements
nécessaires pour éradiquer la grande pauvreté. Avec cete
taxe européenne, on est encore loin du compte...

Des modèles de délivrance des
antirétroviraux sont indispensables aujourd'hui pour mettre des malades
sous traitement à grande échelle et pour imaginer des
réponses politiques plus globales. Pour l'instant ce sont
essentiellement des cliniciens qui ont démarré des programmes de
traitement en se souciant de la relation médecin patient.
En mars 2002, un Groupement d'intérêt public
(GIP) est créé à l'initiative de Bernard Kouchner par les
ministères français chargés de la Santé et de la
Coopération afin de piloter l'initiative Esther. Il est doté d'un
budget de 16 millions d'euros pour 3 ans.
Le réseau ESTHER "Ensemble pour une Solidarité
Thérapeutique Hospitalière En Réseau" (Esther) en Europe a
été constitué en avril 2002 par un engagement commun de
quatre pays (Espagne, France, Italie et Luxembourg). Son assise
européenne a été renforcée en 2004 par l'inclusion
de 4 pays supplémentaires : Allemagne, Autriche, Belgique et Portugal.
La Grèce a rejoint en septembre 2006 le réseau Esther. Ce
programme a reçu le soutien de Kofi Ahnan, secrétaire
général de l'Organisation des Nations Unies. L'organisation
Mondiale de la santé et l'ONUSIDA y sont associées.
Le noyau européen initial (dont la France) a
développé des projets dans 30 pays situés en Afrique
Subsaharienne, Afrique du Nord, Amérique Centrale et du Sud et Asie du
Sud Est. 92 jumelages hospitaliers sont répertoriés alors que les
jumelages associatifs débutent, tout particulièrement à
partir de la France. Les activités des pays européens membre
d'ESTHER sont multiples. Elles s'articulent autour de jumelages hospitaliers
puis associatifs et contribuent à une prise en charge globale et de
qualité des personnes vivant avec le VIH : formation des professionnels
(médicaux, paramédicaux, médicotechniques, sociaux...),
prévention de la transmission mère enfant (PTME) et prise en
charge des femmes et des enfants, équipements selon le niveau du
système de santé,
approvisionnement temporaire en antirétroviraux (stock
tampon pour éviter les ruptures de stock), actions d'accompagnement et
de soutien psychosocial des personnes vivant avec le VIH, développement
de partenariats multiformes intégrant la société civile.
Des activités d'appui technique et de soutien aux pays pour le
renforcement des capacités institutionnelles complètent la
démarche de façon transversale sous forme de compagnonnage.
L'initiative européenne ESTHER présente un fort
potentiel pour contribuer au passage à l'échelle en terme de
soins et de traitements des personnes vivant avec le VIH. Les pays membres en
Europe se sont engagés à lancer rapidement de nouveaux projets
dans des pays supplémentaires en Amérique Latine, en Afrique
subsaharienne et en Asie. L'Europe de l'Est et les Balkans sont
également des zones d'intervention envisagées par plusieurs pays
membres d'ESTHER en Europe. Le rôle grandissant et la reconnaissance
d'ESTHER sur la scène internationale s'illustrent par la multiplication
des demandes des pays du Sud et les partenariats établis avec des
acteurs multilatéraux tels que l'OMS (protocole d'accord) et le Fonds
Mondial (déclaration commune). L'initiative ESTHER est aujourd'hui en
capacité d'apporter une réponse d'envergure aux défis
posés par le VIH/SIDA dans les pays à ressources
limités.
Si les pays pauvres ne peuvent s'offrir les
médicaments, autant les leur fournir à un prix très bas -
et gagner ainsi un peu d'argent - plutôt que de se priver d'un
marché même ridicule en comparaison de ceux des pays riches.
Généralement les laboratoires préfèrent vendre des
médicaments plus chers à une population limitée mais
solvable, que fournir l'ensemble de la population à un prix très
bas. Dernièrement le laboratoire Sanofi a manifestement
décidé de rompre avec ce dogme et annoncé
dernièrement que son nouveau traitement contre le paludisme, ASAQ,
serait bientôt disponible en Afrique subsaharienne.
Dans son communiqué, Sanofi-Aventis rappelle que le
paludisme ampute environ 25% des revenus des ménages en Afrique et tue
3.000 enfants chaque jour. Le groupe assure que plusieurs dizaines de millions
de personnes pourraient bénéficier de son nouveau traitement
chaque année.
Le médicament a été
développé dans le cadre du projet FACT (combinaisons à
dose fixe à base d'artémisinine), géré par la
fondation DNDi (Initiative pour les médicaments contre les maladies
négligées). Sanofi-Aventis est responsable depuis 2004 du
codéveloppement, de la production industrielle, de l'enregistrement et
de la distribution à
l'échelle mondiale du médicament. Cette
nouvelle co-formulation sera moins chère que les autres combinaisons
existantes contenant des dérivés de l'artémisinine
puisqu'elle associe deux principes actifs largement connus et utilisés
aujourd'hui en monothérapie et en co-blister.
Par ailleurs, cette combinaison ne fait l'objet d'aucun
brevet. D'après les évaluations de volume faites par l'OMS pour
les prochaines années et dans le cadre de la stratégie à
prix coûtant de Sanofi-Aventis, on envisage à terme un prix cible
inférieur à 1 dollar pour l'adulte et 0,5 dollar pour l'enfant.
Cet objectif ne sera atteint que si les organisations internationales mettent
en place les aides financières en faveur des pays pour leur permettre de
conduire le changement indispensable dans le traitement du paludisme et ainsi
stabilisent les marchés de matières premières. Ce prix
diminuera ainsi très sensiblement l'impact budgétaire du
traitement de la malaria au niveau international.
Il faut toute fois nuancer la politique d'accès aux
traitements de Sanofi-Aventis, car en parallèle de cette initiative sur
le paludisme, ce groupe aux côtés du géant Abbott est
opposé au gouvernement Thaïlandais qui souhaite importer d'Inde des
génériques moins onéreux du Kaletra et du Plavix !
Le RESAPSI (Réseau Africain des Praticiens Assurant la
prise en charge médicale des personnes vivant avec le SIDA) a
été créé à Dakar (Sénégal) le
6 septembre 2003. Il regroupe des praticiens d'Afrique et d'Europe intervenant
dans la pris en charge médicale des patients africains vivant avec le
VIH/SIDA. Il est né dans un contexte ou l'accès aux soins et aux
antirétroviraux en Afrique est plus important, mais ou l'essoufflement
des schémas (limités) des premières lignes se fait
ressentir. Conjugué à la toxicité à long terme des
multithérapies, la disponibilité limité des
antirétroviraux de secondes lignes.
Il soumet des recommandations à l'attention des
membres du réseau, mais également aux gouvernements, à
l'OMS, aux bailleurs de fonds, ainsi qu'aux laboratoires pharmaceutiques. Ce
réseau est une initiative particulièrement intéressante
car elle regroupe de nombreux pays à forte endémie VIH et elle
essaie d'agir auprès des firmes pour qu'elles réduisent
significativement le prix des nouvelles molécules (Tenofovir, Abacavir,
FTC, protéases boostées, Combinaisons Fixes doses. Assurent la
disponibilité de la forme sèche du Kaletra (ou Aluvia) dans les
pays africain (Kaletra Meltrex disponible depuis 2006 dans les pays
industrialisés). Développent une formulation du Ritonavir ne
nécessitant pas une conservation réfrigérée.
Assurent l'enregistrement des médicaments VIH/SIDA auprès des
autorités pharmaceutiques et médicales des pays.
D'autre part, ce qui est important c'est que RESAPSI n'oublie
pas que le problème de l'accès aux traitements ne repose pas
exclusivement sur les compagnies pharmaceutiques. Il demande aux gouvernements
des pays membres du RESAPSI d'exonérer les médicaments,
réactifs de droits de douane et de taxes. De mettre en place un
processus d'allègement de l'enregistrement des médicaments.
D'appuyer la formation sur les bonnes pratiques et de renforcer le suivi et
l'évaluation des antirétroviraux. Assurer la disponibilité
des tests CD4. Promouvoir les tests pour la sérologie VHB et VHC, la
gratuité du suivi biologique, l'accès au diagnostic biologique
précoce du VIH chez l'enfant. Assurer la disponibilité des formes
pédiatriques. Enfin de renforcer les moyens de diagnostic et de
traitement des infections opportunistes.

Fondation
La Fondation Bill & Melinda Gates est une fondation
américaine humaniste philanthropique créée en janvier
2000. Son but est d'apporter à la population mondiale des innovations en
matière de santé et d'acquisition de connaissances. En 2006, Bill
Gates a décidé de consacrer 95 % de sa fortune à la lutte
contre les maladies et l'analphabétisme dans les pays du Sud. Sa
fondation a déjà dépensé 9,26 milliards de dollars,
en particulier pour vacciner 55 millions d'enfants. La fondation est
financée par Bill et Melinda Gates à hauteur de 28,8 milliards de
dollars par an. Ses dons annuels sont supérieurs aux dépenses de
l'Organisation mondiale de la santé.
Depuis sa création en 2002, l'initiative de Clinton a
été chargée par UNITAID de réaliser des prix
inférieurs de traitements de deuxième ligne et des
antirétroviraux à usage pédiatrique, principalement en
travaillant avec des fabricants génériques indiens - Cipla et
Matrix - pour identifier des améliorations économiques de
procédé de productions.
En pédiatrie à travers le soutien d'UNITAID en
novembre 2006, ce sont 12 000 enfants supplémentaires qui ont eu
accès à une prise en charge thérapeutique. La Fondation
Clinton a déjà obtenue quatre baisses de prix consécutives
sur les antirétroviraux en 4 ans.
En mai dernier, Clinton a pesé de tout son poids et
obtenu une réduction des prix des antirétroviraux de seconde
ligne de 25 % dans les pays à faibles revenus et de 50 % dans ceux
à revenus moyens comme la Thaïlande et le Brésil.
La Fondation Clinton commencera à acquérir ces
médicaments dès juillet 2007 et ce, grâce notamment
à la taxe sur les billets d'avions.
Bill Clinton s'en est récemment pris aux compagnies
pharmaceutiques qui refusent de mettre à disposition leurs brevets pour
permettre de fabriquer des produits génériques accessibles aux
pays du Sud. (( Aucune compagnie ne mourra jamais du prix élevé
des médicaments anti-SIDA dans les pays à revenus moyens, mais
les patients eux peuvent en mourir ». (( Je crois en la
propriété intellectuelle (...) mais cela ne doit pas
empêcher de fournir des médicaments essentiels et sauvant des vies
à ceux qui en ont besoin dans les pays à faibles et moyens
revenus.
Concrètement dès juillet 2007, un
générique de Tenofovir devrait être proposé par la
Fondation Clinton à 149 dollars par an. Gilead le propose lui à
207 dollars dans les pays à faibles revenus et 360 dollars pour les pays
aux revenus moyens. L'OMS recommande de la 3TC ou de la FTC et juge ces deux
composants interchangeables. Une fixe dose contenant du Tenofovir et de la 3TC
sera donc disponible pour un coût annuel de
179 dollars par an. De même, une fixe dose, proche de
l'original Truvada (Tenofovir + FTC) à 225 dollars. Le prix Gilead pour
les pays à faibles revenus étant de 319 dollars et 552 dollars
pour les pays aux revenus moyens. Enfin Atripla une autre fixe dose contenant
du Tenofovir + FTC et Efavirenz est disponible depuis juillet 2006 aux USA et
est attendue en Europe d'ici la fin de l'année. Un
générique Tenofovir + 3TC + Efavirenz coûtera 339 dollars
dans les pays à faibles et moyens revenus - ce qui reste
inférieur au prix pratiqué par le programme d'accès aux
traitements de Gilead pour le seul Tenofovir.
Mais ce n'est pas tout. Le Kaletra (Aluvia) sera
proposé à 695 dollars par an - un prix plus élevé
que celui qu'Abbott fixe pour les pays de l'Afrique sub-saharienne, mais
toujours sensiblement meilleur marché que 1000 dollars - coût
demandé par le groupe américain aux pays à revenus moyens
comme le Brésil ou la Thaïlande. D'autres réductions
importantes incluent les comprimés meilleurs marchés incluant AZT
+ 3TC (Combivir) : 129 dollars par an comparé aux 180 dollars
facturés l'année dernière aux pays à faibles
revenus. Abacavir (Ziagen) sera disponible pour 331 dollars par an au lieu d'un
prix moyen de 750 à 800 dollars par an actuellement. Enfin la Didanosine
(Videx) a chuté vertigineusement de 1096 dollars à 248 dollars
par an !
(( Quand nous avons entrepris ce travail au sein de notre
Fondation, il y a cinq ans, nous avons fait une promesse aux gens souffrant du
SIDA : une fois que vous serez sous traitement, nous veillerons à ce que
les médicaments arrivent ». Manifestement Bill Clinton est en passe
de tenir ses promesses.

![]()
9 - Conclusion
Au départ le prix des médicaments était
l'obstacle affiché. Puis les prix ont baissé de façon
très significative et devraient continuer dès juillet sous
l'impulsion de Bill Clinton. Ces baisses de coût n'ont pas pour autant
mis en péril les compagnies pharmaceutiques. Les ventes de
médicaments pour le SIDA vont atteindrent le chiffre de 10 milliards de
dollars en 2015. En effet, le lancement de nouvelles molécules et
l'augmentation du nombre de patients diagnostiqués pour le VIH vont
permettrent d'atteindre cette somme.

Malgré la pression qui s'exerce sur les fabricants de
devoir baisser le prix de leurs produits pour les pays en développement,
les ventes dans les pays du Nord restent très lucratives et
florissantes. Une société de recherche indépendante
Datamonitor a analysé les changements qui vont s'opérer dans les
10 prochaines années dans le marché VIH/SIDA du fait de
l'arrivée de nouvelles molécules ayant des nouveaux
mécanismes d'activité et les prochaines générations
d'antirétroviraux déjà disponibles. Les ventes se sont
élevées significativement en 2005 - atteignant 7,1 milliards de
dollars profitant surtout à des compagnies détenant des
molécules prometteuses comme MSD, Pfizer, Gilead et Johnson &
Johnson. Le marché global pour l'ensemble des compagnies pharmaceutiques
a augmenté de 7 % l'année dernière pour atteindre la somme
de 643 milliards de dollars.
Même si elle n'a pas atteint l'objectif proclamé
dans les pays en développement à l'échéance de fin
2005 (à cette date, le chiffre s'établissait à 1,3
millions), l'initiative « 3 by 5 » de l'OMS a cristallisé des
progrès significatifs (le nombre de personnes sous traitement a
triplé en deux ans). Même si il subsiste un manque important par
rapport aux besoins de financement qui seraient nécessaires à une
« reprise adéquate » face à l'épidémie et
même si les financements des 3 principaux bailleurs de fonds au plan
international pour les programmes SIDA dans les pays en développement ne
sont pas assurés de leur pérennité après 2008, les
ressources financières disponibles ont connu une augmentation sans
précédent dans l'histoire de l'aide au développement pour
la santé : elles sont passées de moins de 1 milliard de dollar en
2001 à plus de 8 milliards en 2005.
La principale question porte plutôt sur le manque de
ressources humaines pour inclure, traiter et suivre des milliers de malades.
Là des solutions sont à trouver. Mais il sera difficile
d'appliquer des réponses globales car des problèmes de chaque
pays sont spécifiq ues.

![]()
10 - Résumé

ASPEN
Générique
Afrique
du
Sud
2
2
6
Multinationale
Brési l
Afrique
3
5
CIPLA
Générique
INDE
4
6
Far-Manghinos
Générique
Brésil
1 : La compagnie pharmaceutique propose son
antirétroviral à prix coûtant à travers son
Programme d'accès aux traitements.
2 : Transfert de technologie pour permettre
la production locale sous certaines conditions de générique.
3 : Certains laboratoires demandent à
l'Inde suite à son adhésion à l'OMC de respecter le
délai de 20 ans (fin de brevet) pour produire des
génériques.
4 : Certains laboratoires essaient de
contraindre l'Inde à abandonner sa « patent act » lui
permettant de produire des génériques sans tenir compte des
nouvelles formes galéniques apportées par un laboratoire dans le
but de prolonger le brevet.
5 : Production et exportation de
génériques vers d'autres pays : licence obligatoire.
6 : Production et utilisation locale de
génériques : licence volontaire.
11 - Références bibliographiques
· Plus grand que l'amour : Dominique Lapierre. Robert
Laffont 1990.
· Prise en charge médicale des personnes
infectées par le VIH : recommandations du groupe d'expert. Flammarion
2006.
· Contre la montre : Stephen Lewis. Léméac /
Actes Sud. 2007
· L'initiative sénégalaise d'accès aux
médicaments antirétroviraux : analyses économiques et
comportementales et médicales. Collection sciences sociales et sida
ANRS. 2004
· L'accès aux traitements du VIH/sida en Côte
d'Ivoire : évaluation de l'initiative ONUSIDA. Collection sciences
sociales et sida ANRS. 2001
· Industrie pharmaceutique entreprises citoyennes : Jean
Jacques Christofari. Mensuel Prescription santé 2005.
· Le monde merveilleux des laboratoires. Act UP. Action 72.
2001
· Glaxo : ce qu'il en coûte de mépriser les
ONG. Mensuel Management 2006
· Le point sur l'épidémie de sida. Rapport
ONUSIDA / OMS 2006.
· 35 ans de combat dans le monde. Emmanuelle Cosse &
Gaëlle Krikorian. Cahier n°3 Têtu+ 2006-2007
· Atelier International sur l'évaluation des
stratégies antirétrovirales en Afrique: recommandations de Saly -
Sénégal: Professeur Papa Salif Sow. Intervention IMEA 2006
· Du bon usage de la piraterie. Florent Latrive. Exils
2004
· Accelerating Access Initiative: UNAIDS. Progress report
2002
· Les firmes pharmaceutiques organisent l'apartheid
sanitaire: Martine Bulard. Le Monde Diplomatique 2000.
· Du rififi en pharmacie. Mensuel 852 Courrier
International 2007
· Accords de libre échange et
génériques : Gaëlle Krikorian. Congrès Francophones
2007.
· Pricing guide sources and prides of selected medicines
and diagnostics for people living with HIV/AIDS: Unicef/UNAIDS/WHO/MSF 2005.
· Les virus ennemis utiles: dossier pour la Science. Avril
/ juin 2007
·
www.fondation-gsk.org
·
www.positiveaction.com
·
www.tibotec.com
·
www.securethefuture.com
·
www.PMTCTdonations.org
·
www.esther.fr
·
www.gatesfondation.org
·
www.clintonfoundation.org
·
www.resapsi.org
·
www.dndi.org
·
www.accesstohivcare.org
· www.carefarica.info
· www.hiv@msd.info
·
www.actupparis.org
·
www.msf.fr
·
www.gileadaccess.org
·
www.joinred.com
·
www.unitaid.eu
·
www.frontaids.org
·
www.tac.org.za
·
www.inpplus.net
·
www.aspenpharma.com
·
www.aidsmap.com
12 - Remerciements
Je tiens à remercier Monsieur le Professeur
Hervé Gallais qui m'a offert la possibilité de participer au
Diplôme Universitaire SIDA dont il est à l'origine : une aubaine
pour un autodidacte. D'autre part, de m'avoir permis d'exercer mon
métier au sein de son service dans des conditions exceptionnelles durant
dix ans. Il m'a manifesté une très grande confiance et
accordé une certaine liberté d'action me permettant
d'entreprendre des projets riches scientifiquement et humainement parlant.
Merci également à Dominique Blanc du TRT5 pour
sa relecture, ses idées, son soutien ainsi que sa sympathie à mon
égard alors que je représente quand même « le diable
». Tous les cliniciens (ils existent, je les ai rencontré !) avec
qui il est possible d'échanger et qui dépassent les à
priori réducteurs selon lesquels les délégués
médicaux ne sont là que pour pousser à la prescription et
se faire de l'argent (sale ?).
Je tiens aussi à remercier les rares membres de
l'industrie qui ont eu le courage de répondre spontanément
à mes questions comme Benoît Gallet. Merci à
l'équipe Gilead Sciences pour sa confiance et la prise en charge
financière de mon D.U. SIDA. Merci à Patrick Philibert pour la
coupure de presse de l'International Herald Tribune.
Une pensée pour Danielle Nommay, Sébastien Gallice,
Isabelle Ravaux, ma maman et Olivia ma compagne pour la relecture de ce
travail.
Merci plus particulièrement à Act Up,
Médecins Sans Frontières, Gaëlle Krikorian, Dominique
Lapierre, Jean Paul Moatti, Stephen Lewis.

Contact :
ebasset@gilead.com
![]()
Je dédie ce mémoire à Pascale.
Jeune
maman emportée par le VIH en 1994 avant l'arrivée des
trithérapies.
![]()
| 


