CHAPITRE II
Hydrates de gaz
Les hydrates sont des structures cristallines qui peuvent se
former lorsqu'on met des hydrocarbures et de l'eau en contact dans certaines
conditions de pression et de température. Ils se forment pratiquement
avec les hydrocarbures suivants : méthane, éthane, propane,
butane et également avec le gaz carbonique CO2 et
l'hydrogène sulfuré H2S.
Section 1 : Nature
Un certain nombre d'études ont été
consacrées à la détermination de la composition des
hydrates sans qu'un accord soit intervenu entre les différents auteurs.
Il est admis cependant que les hydrates seraient des inclusions de
molécules de gaz dans les espaces laissés libres dans un
empilement dodécaédrique de molécules d'eau sans liaisons
chimiques entre le gaz et l'eau. Ce sont des solides de couleur blanche qui
peuvent revêtir différents aspects (neige, givre, cristaux ou
arborescences).
La densité des hydrates est d'environ 0,98 de sorte que
leur première apparition se traduit par une fine pellicule à
l'interface eau-gaz permettant d'ailleurs d'effectuer les mesures
expérimentales de conditions de formation en cellule. La réaction
de formation est exothermique.
Dans le cas du bouchage d'une tuyauterie par des hydrates,
l'adhérence aux parois et la dureté du bloc d'hydrates est telle
qu'aucun moyen mécanique normal de débouchage ne peut être
mis en oeuvre.
Section 2 : Conditions de formation
Le phénomène de formation d'hydrates constitue
le problème majeur dans la production et le transport du gaz naturel. Il
y a formation d'hydrates lorsque les conditions suivantes sont
simultanément réalisées :
13

|
Optimisation d'un procédé de déshydratation
de gaz naturel
|
|
2. 1 - Présence d'eau liquide
Un gaz naturel saturé ou non en eau ne donne pas lieu
à la formation d'hydrates. Celle-ci ne peut intervenir qu'en
présence d'eau liquide par exemple libérée par le gaz au
cours d'un changement des conditions de pression ou de température.
2. 2 - Présence d'hydrocarbures légers
Seuls les quatre premiers hydrocarbures (méthane,
éthane, propane, butane) sont susceptibles de former des hydrates en
présence d'eau liquide. D'autres corps tels que le gaz carbonique ou
l'hydrogène sulfuré peuvent également former des hydrates
avec l'eau.
2. 3 - Réalisation de certaines conditions (P,
T)
En plus des conditions précédentes, pour que des
hydrates puissent se former, il faut, pour un gaz donné, que la pression
soit suffisamment élevée et la température suffisamment
basse. La formation des hydrates est favorisée par un certain nombre de
facteurs :
> Tourbillons ;
> Vitesse du gaz ;
> Coude, orifice, changement de diamètre ;
> Phénomène auto amplifié ;
> Haute pression ;
> Basse température.
Pour un gaz naturel donné, en présence d'eau
liquide, les hydrates se forment à une certaine température pour
une pression donnée.
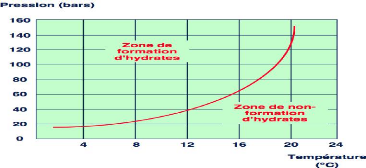
Figure 1.1 : Courbe de formation d'hydrates (source :
Les hydrates, IFP Training, 2007)
14

|
Optimisation d'un procédé de déshydratation
de gaz naturel
|
|
Une des méthodes pour tracer la courbe de formation
d'hydrates est l'utilisation des abaques de Katz. En effet, comme nous pouvons
le voir sur la figure 1.1 précédente, les conditions de formation
d'hydrates dans un domaine (P, T) sont définies par une courbe
séparant le plan en 2 zones. La zone à gauche de la courbe
où il y a formation d'hydrates (hautes pressions, basses
températures). La zone à droite de la courbe où il n'y a
pas de formation d'hydrates (basses pressions, hautes températures).
Notons que le début de formation d'un bouchon
d'hydrates augmente la perte de charge dans la conduite, donc
créé une détente supplémentaire du gaz, ce qui a
pour effet de le refroidir et donc d'entretenir et d'accélérer la
formation des hydrates.
| 


