Introduction
Chapitre I : Généralités
Chapitre II : Matériel et méthodes
Chapitre III : Résultats
Chapitre IV : Discussion
Conclusion
Recommandations
Références
Table de matières
Annexes
iv
SIGLES ET ABREVIATIONS
ABR : Antibiorésistance
ANC : Acide nalidixique et de colistine
APAB : Acide para-amino-benzoïque
BMR : Bactérie multirésistante
BORSA : Borderline Staphylocoque aureus
CDC: Centers for Disease Control and Prevention
CLSI: Clinical and Laboratory Standards Institute
CUDG : Centre Universitaire de Diagnostic au Graben
DHFS : Dihydrofolique acide synthétase
ECDC : Centre Européen de Prévention et de
Contrôle des Maladies
GS : Gélose au sang
IC : Intervalle de confiance
ISO: Infection du site opératoire
KTG : Kanamycine-Tobramycine-Gentamicine
LCR : Liquide céphalo-rachidien
LPV : Leucocidine de Panton et Valentine
MLS : Macrolides-Lincosamides - Streptogramine
MODSA : Modified Staphylocoque aureus
OMS : Organisation Mondiale de la Santé
OR: Odds Ratio
ORL: Oto-Rhino-Larynologie
PBP : Pencilln binding proteins
RDC : République Démocratique du Congo
SARM : Staphylocoque aureus résistantes
à la méthicilline
SASM : Staphylocoque aureus sensibles à la
méthicilline
THF : Acide tétrahydrofolique
V
TSI : Triple Sugar Iron
VRSA : Staphylocoque aureus résistant à la
vancomycine VP : Voges-Proskauer
VW : Von Willbrand
vi
LISTE DES FIGURES
Figure 1 : Amas de Staphylocoque après coloration de Gram
Figure 2 : Ordinogramme des cultures effectuées
LISTE DES TABLEAUX
Tableau I : Facteurs socio-démographiques de SARM
Tableau II : Type d'échantillon et origine de SARM
Tableau IV : Sensibilité de S. aureus et de SARM aux
antibiotiques
Tableau V : Antibiosensibilité des SARM par rapport
à l'origine de l'échantillon
vii
RESUME
Introduction : Le Staphylococcus aureus
résistant à la méthicilline (SARM)
constitue mondialement un problème de santé
publique. La prévalence des infections à ce germe,
hospitalière et communautaire, augmente de façon
régulière; et leur traitement devenu difficile à cause de
l'émergence des souches multi résistantes. L'objectif de ce
travail est de rechercher phénotypiquement le SARM dans les
échantillons cliniques reçus au Centre Universitaire de
Diagnostic du Graben. Le but est de contribuer à l'amélioration
de la prise en charge des infections liées à ces germes et la
surveillance de leur émergence.
Méthodologie : L'étude est
prospective longitudinale, allant du 1er Septembre 2018 au 31 Décembre
2018. Notre échantillon était164 souches de S. aureus.
L'identification de SARM a été faite par des méthodes
phénotypiques. La sensibilité aux antibiotiques a
été faite par la méthode de diffusion de disque. L'analyse
des données a été faite par le logiciel SPSS version 22.
P-value <0.05 était considéré significatif.
Résultat : Sur 164 souches de S. aureus,
102 (62,2%) cas de SARM ont été isolés. Le SARM concerne
les hommes d'âge variant entre 25 à 40 ans, souvent acquis en
communauté et fréquemment dans les sécrétions de la
sphère urogénital. Les non SARM sont plus sensibles à la
plupart d'antibiotiques. Les SARM expriment un taux de résistance plus
élevé. La sensibilité de SARM aux antibiotiques ne
dépend pas de l'origine de l'échantillon. 100% des SARM
étaient résistants à l'oxacilline, la cloxacilline, la
meropèneme et la cotrimoxazole ; 97,2 ; 96,8 et 89,9% respectivement
pour la clarythromycine, l'azythromycine et la ceftriaxone. Les souches ont
exprimé la résistance la plus faible à la vancomycine et
l'augmentin.
Conclusion : La prévalence de SARM est
élevée dans notre milieu, et il présente la
résistance à la quasi-totalité des antibiotiques
utilisés localement.
Mots clés : SARM, phénotypes,
antibiogramme
VIII
ABSTRACT
Background: Methicillin-resistant Staphylococcus
aureus (MRSA) is a public health problem throughout the world. The prevalence
of MRSA infections, both in hospitals and community is increasing; and their
treatment has become difficult due to the multi drugs resistant strains. The
objective of our study is to search phenotypically the MRSA in clinical
specimens isolated at the Centre Universitaire de diagnostic au Graben. The
final target is to contribute to the improvement of the management of
infections linked to these germs and the surveillance of their emergence.
Methodology: It's a cross-sectional and
prospective study carried out from September 1st, 2018 to December 31, 2018.
Our sample was constituted with 164 strains of S.aureus.
Identification of MRSA strains was made through phenotypic method, the
antibiotic susceptibility patterns of strains was done by disk diffusion
method. Data was analyzed by SPSS version 22. P -value of <0.05 was
considered as significant.
Results: Out of 164 examined samples, 102
(62,2%) of them were MRSA. The MRSA concerns more men with 25 to 40 years old,
often acquired in community and frequently isolated in the secretions of the
urogenital tract. The non MRSA strains are more susceptible to almost
antibiotics; the MRSA expresses a high rate of resistance. The susceptibility
of MRSA to the antibiotics is independent to its hospital and community
acquirement. The susceptibility antibiotics showed that 100% of MRSA were
resistant to oxacillin, cloxacillin, meropenem and cotrimoxazol; 97,2; 96,8 and
89,9% respectively for clarythromycin, azythromycin and ceftriaxone. The
strains expressed the lowest resistance was observed to vancomycin.
Conclusion: Our study has reported a relatively
high prevalence of MRSA in our country; and they present a resistance to the
quasi-totality of antibiotics used locally.
Key words: Phenotypics, MRSA, antibiogramme,
CUD.
1
INTRODUCTION
Le Staphylococcus aureus est une bactérie
pyogène. Son caractère ubiquitaire, sa virulence et sa
remarquable capacité de survie dans un environnement défavorable
ou même hostile expliquent sa grande fréquence en pathologie
communautaire et nosocomiale. S. aureus est responsable d'une grande
variété d'affections de gravité variable parfois
bénignes comme les infections cutanées et muqueuses, ou
sévères comme l'endocardite et la septicémie. Bien qu'il
soit virulent, S. aureus n'infecte pas forcement son hôte mais
le colonise [1].
La prévalence des infections staphylococciques,
nosocomiales et communautaires augmente de façon
régulière. Le traitement de ces infections est devenu de plus en
plus difficile à cause de l'émergence des souches multi
résistantes. Ce phénomène est observé aussi bien
à l'hôpital que dans la ville.
Les souches de S. aureus de phénotype sauvage
sont sensibles aux pénicillines (Penicillin G, Penicillin M, Penicillin
A), à la céfalotine, à la céfoxitine, au
moxalactam, à la céfotaxime, aux macrolides, lincosamides et
streptogramines, aux aminosides, aux tétracyclines, aux
fluoroquinolones, au chloramphénicol, aux rifamycines, aux sulfamides et
à la triméthoprime, à l'acide fusidique, à la
fosfomycine et aux glycopeptides. S. aureus a une résistance
naturelle à l'acide nalidixique, aux polymyxines, à
l'aztréonam et aux 5-nitro-imidazolés [2-5].
En effet, dès 1950, c'est-à-dire dix ans
après la découverte de la pénicilline, les
Staphylococcus aureus deviennent un problème
thérapeutique majeur par l'acquisition de la résistance
plasmidique à la pénicilline. Peu après l'introduction de
la méthicilline en 1959, apparaissent des souches de S. aureus
résistantes à la méthicilline (SARM) [6]. La
résistance à la méthicilline est liée à
l'acquisition d'une autre protéine liant la pénicilline, la PLP2a
ou PLP2', présentant peu d'affinité pour les
béta-lactamines. La production de PLP2a est codée par le
gène chromosomique mecA dont l'origine reste encore inconnue [7].
Les SARM présentent également une
résistance à d'autres antibiotiques. Les SARM sont aussi
résistants aux bêta-lactamines, à la tétracycline,
au chloramphénicol et aux macrolides [8]. Par la suite, ces souches sont
devenues résistantes à la gentamicine [9]. La plupart des SARM
isolés dans le monde expriment des phénotypes de multi
résistance, une caractéristique qui, jusqu'en 1995, s'appliquait
seulement aux SARM acquis dans les hôpitaux [6].
2
La diffusion des SARM concerne aujourd'hui tous les types
d'établissements de soins, mais tend également à
déborder de plus en plus sur le milieu communautaire. Il est reconnu que
les SARM ne remplacent pas les souches sensibles mais s'y ajoutent ; par
conséquent, il y a une augmentation globale du nombre d'infections
[10].
Les études antérieures ont montré que le
SARM constituait un problème mondial [11-13] et constitue un
problème majeur de santé publique [14]. D'après une
étude coordonnée par un économiste britannique, environ
700 000 personnes décéderaient chaque année à cause
des résistances aux antimicrobiens (antibiotiques, antiviraux,
antifongiques et antiparasitaires). Si les tendances se confirment dans les
années à venir, ce nombre pourrait atteindre 10 millions de
décès dans le monde en 2050 [15]. Les infections
résistantes feraient alors plus de morts que le cancer (8,2 millions).
D'après Wakefield et al. [16], les SARM prolongent la
durée d'hospitalisation dans 71% de cas, augmentent le coût des
examens (33%) et celui des antibiotiques (43%) en comparaison avec les patients
ayant présenté une infection aux souches des Staphylocoque
aureus sensibles à la méthicilline (SASM).
D'après les données du Centre Européen de
Prévention et de Contrôle des Maladies (ECDC), 33 000 personnes
décèdent chaque année de suites d'une infection à
bactérie multirésistante (BMR) dans les pays de l'Union
Européenne [17]. Alors qu'aux Etats Unis d'Amérique, les centres
pour le contrôle et la prévention des maladies (Centers for
Disease Control and Prevention (CDC)) cité par Leaper et al.
[18] estiment que chaque année, 2 millions d'américains sont
victimes d'infections provoquées par une BMR et que 23 000 en
meurent.
En France, les résultats des enquêtes nationales
de prévalence de 1996, 2001 et 2006 montrent que les BMR occupent une
place importante. Le Staphylococcus aureus représentait en 2006
un cinquième de l'ensemble des bactéries responsable des
infections, y compris des bactériémies, et un tiers des
bactéries responsables des infections du site opératoire (ISO).
Par contre, l'ensemble des entérobactéries représentait
40% des bactéries, responsables de bactériémies, deux
tiers des infections urinaires et un quart des ISO. SARM était alors la
plus fréquente des BMR (environ 13% de l'ensemble des bactéries),
suivi par les entérobactéries résistantes à la
céfotaxime (5%) [19-21].
Au Québec comme au Canada, le système de
surveillance des infections montre que le taux de prévalence de SARM est
passé de 16,6% en 2000 à 48% en 2003 dans les centres
hospitaliers de courtes durées et que 82% des cas de SARM seraient des
bactériémies dont la mortalité moyenne est de 30% des cas
[22].
3
La résistance aux antibiotiques dans la région
Africaine constitue un domaine qui n'est pas bien documenté dans les
rapports de l'Organisation Mondiale de la Santé (OMS). Les
données ne sont rassemblées que dans un nombre limité de
pays. Une résistance importante est constatée pour plusieurs
bactéries qui se sont propagées dans les communautés et
dans les hôpitaux. La prédominance des SARM a été
déterminée dans huit pays africains entre 1996 et 1997 et a
été relativement élevée au Nigeria, au Kenya et au
Cameroun (21 à 30%) et inférieur à 10% en Tunisie et en
Algérie [23].
En Afrique de l'Ouest, la menace est inquiétante
concernant le SARM avec une prévalence qui est supérieure
à 30% [24]. Une étude mauritanienne a montré que
l'activité de la pénicilline G sur les souches de
Staphylococcus aureus isolées dans la région de Nouakchott
est quasi nulle et le taux de SARM communautaire est important, atteignant
jusqu'à 34% [25].
Le travail de Vlieghe et al. concernant
l'étude systématique de la littérature publiée sur
la résistance bactérienne en Afrique centrale entre 1955 et 2008,
a montré de taux de résistance élevés dans presque
tous les pathogènes. Ils ont également constaté la
multi-résistance de Shigella et de Salmonella spp.
ainsi que l'émergence de SARM [26]. Les conclusions de Vlieghe
et al. montrent que la région d'Afrique Centrale n'est pas
exclue de la tendance mondiale d'antibiorésistance croissante et a donc
besoin d'une surveillance urgente basée sur la microbiologie pour
fournir les données claires sur l'antibiorésistance (ABR).
En République Démocratique du Congo (RDC), les
recherches de Nyembwe et al. sur la prévalence de SARM à
Kinshasa ont montré un taux élevé de SARM dans le milieu
hospitalier mais aussi, elles ont montré l'existence du portage sain a
une fréquence élevée chez les soignants [27].
L'usage irrationnel d'antibiotiques a déjà
été démontré à l'Est de la RDC.
Les
antibiotiques comme amoxicilline-acide clavulanique, penicilline,
amoxicilline, ciprofloxacine, erythromycine et doxycycline sont beaucoup
utilisés abusivement dans le milieu académique pour le traitement
des infections urinaires et respiratoires [28-29]. Ce qui favoriserait
l'accroissement des BMR.
Cependant, au Nord-Kivu, la plupart des structures sanitaires
manquent la capacité d'identifier microbiologiquement des agents de
maladies infectieuses, y compris les infections bactériennes
envahissantes. Butembo n'est donc pas loin de cette triste
réalité d'ABR. Bunduki et al. ont démontré
que S. aureus est le germes fréquemment isolé des
urocultures [30] et hémocultures [31], respectivement avec une
fréquence de 47,0% et 39,9%. Ce germe
4
était résistant aux antibiotiques les plus
couramment utilisés, sauf pour les quinolones comme la ciprofloxacine
pour laquelle il était sensible. Mais aucune étude publiée
n'a analysée les caractéristiques phénotypiques et
génotypiques de S. auresus résistants à la
méthiciline.
Malgré l'importance du problème d'ABR et de
conséquences sanitaires et économiques qui en découlent,
rares sont les pays d'Afrique qui disposent de programme et plan nationaux de
surveillance et de lutte contre la résistance comme le recommande l'OMS
[32]. Le niveau de la recherche sur la résistance aux antibiotiques dans
ces pays reste encore trop faible. En RDC, aucune étude n'a
été effectuée sur les caractéristiques
phénotypique et génotypique d'antibiorésistance de
bactéries.
Les SARM sont l'une des BMR faisant l'objet de la plupart des
programmes nationaux en raison de leur fréquence élevée,
leur potentiel pathogène se traduisant par une morbi-mortalité et
des surcoûts économiques associé à leur
caractère commensal qui expose au risque de diffusion, et de leur
caractère clonal ou du caractère aisément
transférable des mécanismes de résistance impliqués
[16,19-21,24,33].
Un point important est de connaître les
phénotypes des souches SARM chez les patients qui nécessitent un
traitement adéquat comme c'est le cas de ceux qui souffrent de
bactériémies [31] et d'infections nosocomiales et d'autres
infections liées à ces germes. En effet, les traitements
empiriques administrés chez ces patients pourraient ne pas être
efficaces vis-à-vis des SARM. Vu l'importance du problème
lié aux SARM, son étude phénotypique serait important dans
le milieu démuni comme le nôtre.
Ainsi, l'objectif de ce travail est de rechercher
phénotypiquement le S. aureus
méthicillino-résistant dans les échantillons
cliniques reçus au Centre Universitaire de Diagnostic au Graben en vue
de contribuer à l'amélioration de la prise en charge des
infections liées à ces germes et la surveillance de leur
émergence.
Les objectifs spécifiques sont :
- Déterminer la prévalence des souches de S.
aureus résistantes à la méthicilline ;
- Étudier la sensibilité de SARM aux antibiotiques
couramment utilisés ;
- Comparer la sensibilité aux antibiotiques des SARM
d'origine hospitalière à celle
d'origine communautaires.
L'intérêt de ce travail se résume par le
fait que les SARM est une cause de morbidité et mortalité tant
dans les pays développés que dans les pays en voie de
développement, en milieu hospitalier comme dans les communautés
et avec une élévation du coût des soins médicaux. La
connaissance de la sensibilité de SARM aux différents
antibiotiques servira de guide pour le clinicien lors du traitement.
5
Les résultats de cette étude serviront des
données locales sur les SARM, leur surveillance
épidémiologique, et orienteront les mesures préventives et
hygiéniques à mettre en place dans la politique locale de lutte
contre l'antibiorésistance.
6
CHAPITRE I : GENERALITES SUR LES
STAPHYLOCOQUES
AUREUS METHICILLINO-RESISTANTS
I.1. Staphylococcus aureus
I.1.1. Historique
Observés par Pasteur en 1879 dans un pus de furoncle, les
staphylocoques
doivent leur nom à Ogston (1881) qui les a mis en
évidence dans des abcès aigus et chroniques [34]. Trente-cinq
espèces sont actuellement répertoriées dans le genre
Staphylococcus [35].
I.1.2. Habitat
S. aureus est un commensal de la peau et des muqueuses
de l'homme et des
animaux à sang froid. Le site de colonisation de S.
aureus est préférentiellement la muqueuse nasale, la peau,
les zones humides (aisselles, aines, périnée) et les mains.
Trente à cinquante pourcent des adultes sains sont
colonisés avec 10 à 20% de porteurs chroniques[2].
I.1.3. Caractères bactériologiques a)
Morphologie
Ce sont des cocci à Gram positif, isolés ou
groupés en diplocoques, en courtes chaînettes ou en amas, ayant la
forme de grappe de raisin, immobiles, non sporulés mais parfois
encapsulés. Ils mesurent 0,8 à 1 ìm de diamètre.
b) Caractères culturaux
S. aureus se cultive facilement sur tous les milieux
usuels, et aussi sur des milieux riches en NaCl à des conditions de pH
et de température variables. Sur gélose Columbia
additionnée de sang de mouton (5%) d'acide nalidixique et de colistine
(ANC), les colonies sont lisses, brillantes, bombées et rondes.
En milieu liquide (hémoculture), il produit dans le
bouillon un trouble homogène. Certaines souches sont pigmentées
en jaune doré ; d'où, le nom d'aureus. Le pH varie de 5,6
à 8,1 ; l'optimum est de 7,5.
La température optimale de croissance est de 37°C.
Mais, la culture est possible de 10 à 45°C. S. aureus est
une bactérie aéro-anaérobie facultative,
c'est-à-dire qu'il est capable de se développer à la
surface de la peau, en aérobiose et aussi dans les tissus mal
oxygénés [36].
7
I.1.4. Substances biologiquement actives
a) Le génome
Le génome du S. aureus est constitué
d'un chromosome circulaire d'environ 2800 paires de bases. Les gènes de
virulence et de résistance aux antibiotiques sont retrouvés
à la fois sur le chromosome et sur des éléments
extra-chromosomiques. Cela permet ainsi leur transfert d'une bactérie
à l'autre dans la même espèce et dans les espèces
différentes.
b) La paroi
Elle est formée de peptidoglycane, des acides
teichoïques et lipoteichoïques. Les acides teichoïques sont des
polymères linéaires du ribitol phosphate liés de
façon covalente au peptidoglycane. Ces composants possèdent des
effets biologiques démontrés in vitro. Ils ont une
activité endotoxin-like stimulant la sécrétion de
cytokines par les cellules lympho-monocytaires, l'activation du
complément, et l'agrégation plaquettaire.
Les acides téichoïques sont les récepteurs
des bactériophages et donnent naissance à des anticorps que l'on
retrouve dans le sérum du malade (lysotypie des staphylocoques).
c) La capsule
La capsule polysaccharidique est impliquée dans le
phénomène d'adhérence et permet également une
meilleure résistance des souches à la phagocytose et à
l'opsonisation. d) Les protéines de surface
Plusieurs de ces protéines de surface jouent un
rôle dans la capacité des staphylocoques à coloniser les
tissus. S. aureus se fixe aux cellules et à la matrice
extracellulaire par l'intermédiaire de ces protéines de surface
dénommées adhésines.
La protéine A inhibe l'opsonophagocytose grâce
à sa capacité de fixation au fragment Fc des immunoglobulines.
Elle se lie au facteur de Von Willbrand (VW) et au fragment Fab (partie
variable) des immunoglobulines.
e) Les toxines
? Hémolysines ou staphylolysines
Plusieurs ont été décrites (alpha,
bêta, gamma, delta). Elles ont une action cytolytique sur les plaquettes
et les globules rouges. L'alpha-toxine est une toxine à action
membranaire. Après liaison au récepteur membranaire, elle forme
des pores d'où peuvent s'échapper des cations et des petites
molécules. Elle a un effet vasoconstricteur et nécrotique sur la
peau. Son poids moléculaire est de 33 kDa.
8
? Superantigènes
Ce sont des toxines pyrogènes qui se lient au complexe
majeur d'histocompatibilité de type II et causent une
prolifération majeure des lymphocytes T avec production de cytokines. Ce
sont :
? Les entérotoxines
Il en existe sept : A, B, C 1, C 2, C 3, D et E. Elles sont
responsables du choc toxique staphylococcique, de toxi-infection alimentaire et
d'entérocolite aiguë pseudomembraneuse. Elles résistent aux
protéases du tube digestif et partiellement à la chaleur. Leur
origine est chromosomique.
? Toxine du choc toxique staphylococcique ou TSST1
D'origine chromosomique, elle induit la synthèse
d'anticorps dont la fréquence augmente avec l'âge. On la trouve
dans 20 % des souches S. aureus.
? Exfoliatines
Ce sont des toxines épidermolytiques A et B. Elles sont
responsables d'érythème et de clivage de l'épiderme,
causant l'épidermolyse bulleuse staphylococcique (A et B responsables
d'infections néonatales : syndrome de Ritter, impétigo
bulleux)
? Leucocidine de Panton et Valentine (LPV)
Ce sont des protéines à deux composants non
associés mais agissant en synergie sur les membranes cellulaires. Ces
toxines ont des cellules cibles telles que les polynucléaires, les
monocytes, et les macrophages, et sur lesquelles elles se fixent et provoquent
la formation des canaux membranaires laissant passer les cations divalents.
La LPV constituée d'un composant de classe S et d'un
composant de classe F est dermonécrotique et leucotoxique [4].
f) Les enzymes
Les staphylocoques produisent de nombreuses enzymes comme les
protéases, lipases, hyalurodinases qui lysent les tissus et peuvent
faciliter l'extension de l'infection aux tissus adjacents.
? La coagulase libre
S. aureus fabrique une exoenzyme capable de coaguler
en quelques heures le plasma humain citraté ou hépariné.
La coagulase est une protéine extracellulaire qui se lie à la
prothrombine de l'hôte et forme un complexe appelé
staphylothrombine. La thrombine activée transforme donc le
fibrinogène en fibrine. C'est la base du test de la coagulase en tube.
C'est un marqueur classique de l'identification de S. aureus.
9
· La coagulase liée ou clumping factor
C'est une protéine constituant la paroi, elle fixe le
fibrinogène et entraîne l'agglutination des staphylocoques.
· La fibrinolysine ou staphylokinase
Elle active le plasminogène en plasmine et contribue
à la dislocation du caillot et à la formation de microembols
bactériens responsables des métastases septiques.
· La désoxyribonucléique thermostable
C'est une nucléase ayant des propriétés
endo et exonucléasiques et elle est active sur les ADN et les ARN. Elle
est produite par la plupart des souches de S. aureus.
· Les bêta-lactamases
Elles inactivent la pénicilline. Les PBP (pencilln
binding proteins) sont situées dans la membrane cytoplasmique, leur
modification confère une résistance aux pénicillines A et
M et aux céphalosporines.
I.1.5. Pouvoir pathogène
S. aureus est responsable d'infections suppuratives
superficielles et profondes ainsi que des syndromes liés à
l'action des toxines.
a) Les infections suppuratives
Les infections à S. aureus les plus
fréquentes sont les infections cutanéo-muqueuses telles que les
folliculites, les furoncles, les anthrax, le panaris, les cellulites ou les
sinusites et les otites. Il s'agit le plus souvent d'auto-infestation. Ces
infections se compliquent parfois par extension loco-régionale ou par
diffusion hématogène de la bactérie. S. aureus
peut alors être responsable de septicémies, d'endocardites,
de pneumopathies, d'ostéomyélites, d'arthrites, de
méningites ou d'infections urinaires.
b) Les infections d'origine toxinique
· Syndromes cutanés staphylococciques
Le syndrome de la peau ébouillantée chez les
jeunes enfants est provoqué par la diffusion d'exfoliatines de
même que le syndrome de Ritter observé chez les
nouveaux-nés. Quant à l'impétigo bulleux, il est induit
par productions d'exfoliatines au sein même des lésions
cutanées.
· Choc toxique staphylococcique
Ce syndrome est provoqué par la diffusion dans
l'organisme du TSST-1 et ou des entérotoxines. Ce même syndrome a
été décrit en pédiatrie comme étant une
complication d'infections suppuratives staphylococciques. Il est
caractérisé par une fièvre à 39°C, une
10
hypotension artérielle, une érythrodermie
scarlatiniforme, une desquamation diffuse, des diarrhées, une
céphalée et une atteinte multiviscérale.
? Intoxications alimentaires
Elles sont provoquées par l'ingestion
d'entérotoxines thermostables. L'intoxication est
caractérisée par une incubation courte d'une à six heures
après l'ingestion, on a des crampes abdominales douloureuses, des
nausées, des diarrhées, des vomissements, absence de
fièvre et parfois, on a des collapsus cardiovasculaires.
I.1. 6. Diagnostic bactériologique des
infections à S. aureus
a) Le prélèvement
Le résultat des examens bactériologiques
dépend pour une grande part des conditions de prélèvement
et de transport de l'échantillon. Les prélèvements doivent
être effectués en principe avant l'administration
d'antibiotiques.
Ainsi, les modalités pour un bon
prélèvement sont :
? Pour les lésions cutanéo-muqueuses : on
désinfecte au préalable la zone à prélever, puis on
procède par aspiration douce à l'aide d'une aiguille
stérile surmontée d'une seringue stérile.
? Pour les urines, les sécrétions vaginales et
autres liquides, le prélèvement se fait dans un étui
stérile pour éviter toute contamination. L'acheminement au
laboratoire du produit pathologique doit être fait le plus rapide
possible.
b) Diagnostic direct
Les produits pathologiques sont systématiquement
examinés au microscope optique, à l'état frais
après étalement entre lame et lamelle ou à l'aide d'une
cellule de Malassez. Ensuite, on procède à la coloration de Gram
qui nous montre des cocci à Gram positif, le plus souvent groupés
en amas ou en diplocoques (Fig. n° 1).
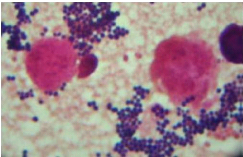
Fig 1 : Amas de Staphylocoque après coloration de Gram
11
La culture se fait généralement sur milieu
sélectif notamment sur gélose Columbia additionnée au sang
de mouton (5%) d'acide nalidixique et de colistine et incubée à
37°C pendant 24 à 48 heures sous dioxyde de carbone ou en
anaérobiose. S. aureus pousse également sur milieu de
CHAPMAN. Pour obtenir des cultures pures, il faut réensemencer les
germes prédominants lorsque la première culture
révèle un caractère impur.
L'identification de S. aureus repose sur les
caractères suivants : présence d'un pigment
caroténoïde, d'une coagulase, d'une protéine A, d'une
hémolysine alpha, la réduction des nitrates, la fermentation du
mannitol, la présence de l'acétoïne, d'une phosphatase et la
sensibilité à la novobiocine[37-39].
c) Diagnostic indirect
Ce diagnostic repose sur la recherche des antistaphylolysines
alpha et les anticorps anti-acide teichoïques dans le sérum
[40].
I.2. Les antibiotiques
I.2.1. Définition
En 1942, WAKSMAN définit un antibiotique comme
étant un dérivé produit
par métabolisme de micro-organisme, possédant
une activité antibactérienne à faible concentration et
n'ayant pas de toxicité sur l'hôte. Il est aussi défini
comme une substance d'origine biologique ou synthétique, agissant
spécifiquement sur une étape essentielle du métabolisme
des bactéries [38].
I.2.2. Les différentes classes
d'antibiotiques
a) Les bêta-lactamines
Ce sont des antibiotiques dont la structure de base est le cycle
bêta-lactame et
trois groupes sont individualisés dans cette classe. Les
pénicillines et les céphalosporines
feront l'objet de notre étude.
? Mécanisme d'action
Les bêta-lactamines agissent par inhibition de la
dernière étape de la synthèse
du peptidoglycane de la paroi bactérienne.
? Mécanismes de résistance
Ils existent plusieurs mécanismes.
? Modification de la cible :
La résistance est due à la présence de
protéine de liaison à la pénicilline
additionnelle la PLP 2a qui a une très faible
affinité pour l'ensemble des bêta-lactamines.
Cette résistance peut être soit homogène
soit hétérogène. La production de ces PLP anormales
12
est codée par un gène chromosomique mec A qui
appartient à un fragment additionnel d'ADN intégré
à celui des SARM.
+ Production de bêta-lactamase : souches BORSA (borderline
S. aureus)
Cette résistance est due à une
sécrétion importante de bêta-lactamase. Ce sont notamment
des souches qui n'ont pas de résistance intrinsèque,
c'est-à-dire ni PLP 2a, ni gène mec A et il y a restauration in
vitro si l'oxacilline est associée à un inhibiteur de
bêta-lactamase.
+ Production de méthicillinase
Quelques souches semblent produire une méthicillinase
capable d'hydrolyser la méthicilline, en absence de gène mec
A.
+ Modification des PLP autre que la PLP 2a (souches MODSA :
modified S. aureus)
Les souches résistantes à bas niveau à
l'oxacilline et non productrices de bêta-lactamase présentent une
modification d'affinité de leurs PLP, normales vis-à-vis des
bêta-lactamines.
? Phénotypes de résistance
On distingue trois phénotypes de résistance aux
bêta-lactamines chez S. aureus, selon que les souches sont sensibles ou
résistantes à la méthicilline.
+ Peni S- méti S : Ce sont des souches sensibles
à la pénicilline G et à la méthicilline
sensible.
+ Peni R-méti S : Ces souches sont productrices d'une
pénicillinase plasmidique qui hydrolyse la pénicilline G, V, les
amino, carboxy et uréidopénicillines. Mais ces souches restent
sensibles aux céphalosporines et aux inhibiteurs de
bêta-lactamase.
+ Péni R-méti R : En plus de la
pénicillinase, les SARM produisent une PLP 2a ayant peu
d'affinité pour la méthicilline. Ce type de résistance est
chromosomique inductible et est croisée à toutes les
bêta-lactamines.
La recherche de la résistance s'est faite par la
méthode de disques. Ainsi la diminution du diamètre d'inhibition
< à 20 mm ou la présence de colonies autour du disque
(même si le diamètre reste = 20 mm) montre une résistance
à l'oxacilline. Il faut rajouter un disque de céfoxitine qui est
un meilleur substrat pour l'expression de la résistance à
l'oxacilline. Le phénotype oxacilline sensible et céfoxitine
résistant ne sont pas possibles. En Europe, les SARM représentent
25 à 30 % des souches de S. aureus et 40 à 60 % en Afrique.
13
b) Les aminosides
· Mécanisme d'action
Bactériostatiques à faible dose et très
bactéricides à forte dose, les aminosides se fixent sur des sites
divers de la sous-unité 30 S des ribosomes bactériens et
perturbent la lecture du code génétique de même que la
synthèse protéique. Il en résulte des protéines
anormales pour la bactérie, ce qui entraîne sa mort.
· Mécanismes de résistance
Plusieurs mécanismes interviennent dans l'apparition de
résistances.
- Réductionde la fixation sur la surface cellulaire,
- Dégradation de la molécule d'aminoside par trois
types d'enzymes : phosphotransférases,
acétyltransférases,
adényltransférases.Ces enzymes sont généralement
codées par des
plasmides et le transfert de résistances'effectue par
conjugaison.
- Mutation ribosomale
· Phénotypes de résistance.
Sept phénotypes de résistance ont
été décrits chez Staphylococcus aureus : -
Phénotype S : il correspond à la résistance isolée
à la streptomycine.
- Phénotype KNm : résistance à la fois
à la kanamycine et à la néomycine (paromomycine et
framycétine).
- Phénotype KTG (Kanamycine-Tobramycine-Gentamicine) :
il confère une résistance totale à ces trois
molécules et une résistance partielle à l'amikacine et
à la nétilmicine, soit une résistance à tous les
aminosides utilisable en pratique clinique.
- Phénotype KT : ce phénotype confère une
résistance totale à la kanamycine et à la tobramycine et
une résistance partielle à la néomycine.
- Phénotype S+KNm : il confère une
résistance à la streptomycine, à la kanamycine, à
la néomycicne et une résistance partielle à
l'amikacine.
- Phénotype S+KTG : Il confère une
résistance à la streptomycine, à la kanamycine, à
la tobramycine, à la gentamicine et une résistance partielle
à la nétilmicine.
- Phénotype S+KNm+KTG:Il confère une
résistance à la totalité des aminosides. Toutefois la
résistance pour l'amikacine et la nétilmicine n'est que
partielle.
· Fréquence de résistance.
Plus de 90 % des souches résistantes à
l'oxacilline sont résistantes à la streptomycine, à la
kanamycine, à la gentamicine et à la tobramycine. La
résistance à la gentamicine et à la tobramycine doit
être considérée comme croisée à la
nétilmicine et à
14
l'amikacine quel que soit le résultat de l'antibiogramme
en raison du mécanisme commun de résistance.
c) Macrolides, Lincosamides et Streptogramines
(MLS)
· Mécanisme d'action
Les MLS inhibent la synthèse des protéines en se
fixant au niveau de la sous unité 50 S du ribosome bactérien et
cette fixation empêche celle du chloramphénicol (antagonistes).
Les MLS sont des antibiotiques bactériostatiques.
· Mécanisme de résistance
De nombreux déterminants sont impliqués dans la
résistance aux MLS, leur conférant ainsi une résistance
par altération de la cible ribosomale (ARNr 23 S). Cette
résistance est soit inductible, soit constitutive.
· Phénotypes de résistance
- Phénotype sensible: souche sensible à tous les
MLS
- Phénotype MLSB : Constitutif : souche résistante
à tous les macrolides (M), aux
lincosamides (L) et aux streptogramines B : résistance
MLSB
Inductible : souche résistante à
l'érythromycine, sensible aux autres macrolides, aux
lincosamides et aux streptogramines.
- Phénotype LSA : souche sensible aux macrolides,
résistante aux lincosamides (L) et à
lastreptogramine A.
- Phénotype L : souche résistante uniquement
à la lincomycine.
- Phénotype MLSB + SA : résistance aux macrolides,
lincosamides et aux streptogramines A
et B
- Phénotype SA : souche résistante aux
Streptogramines A. Cette résistance est due à
unmécanisme d'efflux et à
l'acétyltransférase.
· Fréquence
En France, les souches de staphylocoques résistantes aux
macrolides ont une résistance de type MLSB dans 89% des cas,
constitutive en général chez les SARM et inductible chez les
SASM. Une résistance par efflux est observée dans 2 % des cas
[40]. d) Quinolones : Ciprofloxacine
· Mécanisme d'action
Il s'agit d'une inhibition de l'ADN-gyrase bactérienne,
enzyme indispensable à la synthèse de l'ADN pour sa
transcription. Elle a un effet bactéricide.
· Mécanisme de résistance
15
La résistance bactérienne est de type
chromosomique et non plasmidique. Cette résistance est associée
à celle des pénicillines M. S. aureus a aussi une
résistance naturelle à l'acide nalidixique.
e) Phénicolés :
Chloramphénicol
? Mécanisme d'action
Le chloramphénicol est un antibiotique
bactériostatique agissant par inhibition de la synthèse des
protéines bactériennes au niveau de la sous unité 50 S.
? Mécanisme de résistance
Le mécanisme de résistance est plasmidique, mais
il existe une résistance chromosomique.
f) Tétracyclines
? Mécanisme d'action
Les tétracyclines ont une action
bactériostatique par inhibition de la synthèse protéique
bactérienne. Elles se lient à la sub-unité 30 S des
ribosomes bactériens (et secondairement à la fraction 50 S) et
inhibent l'enzyme de liaison de l'aminocyl-transférase-RNA au
ribosome.
? Mécanisme de résistance
La résistance est souvent plasmidique et
transférable. Ceci s'explique par la sécrétion d'une
protéine qui empêche la pénétration
intrabactérienne de l'antibiotique.
g) Sulfamides et Triméthoprime
? Mécanisme d'action
Les sulfamides sont bactériostatiques. Leur
mécanisme d'action est fondé sur l'inhibition de la
synthèse par la bactérie, de l'acide folique nécessaire
à l'édification de ses bases puriques et pyrimidiques (donc de
son ADN). La membrane bactérienne étant imperméable
à l'acide folique, la bactérie doit en effet édifier son
acide folique de ses trois constituants élémentaires : acide
para-amino-benzoïque (APAB), acide glutamique, ptéridine. Elle en
réalise l'assemblage grâce à une enzyme, la dihydrofolique
acide synthétase (DHFS), c'est celle-ci qui est inhibée par les
sulfamides.
Le triméthoprime se fixe sur une autre enzyme, la
dihydrofolate réductase (DHFR) et empêche la formation de l'acide
tétrahydrofolique (THF) nécessaire à la synthèse de
l'ADN à partir des précurseurs, grâce en particulier
à une enzyme, la thymidine synthétase. En présence de
triméthoprime et pour échapper à l'action de celui-ci, les
bactéries sont
16
capables d'effectuer la synthèse de l'ADN directement
à partir de la thymidine lorsque celle-ci est présente dans le
milieu.
L'effet inhibiteur de la DHFR est complémentaire à
celui de DHFS et explique la parfaite synergie entre sulfamide et
triméthoprime.
? Mécanisme de résistance
Les souches résistantes sont capables soit de surmonter
l'effet inhibiteur par une synthèse accrue d'APAB ou soit de
synthétiser une dihydrofolique acide synthétase et une
dihydrofolate réductase présentant une affinité moindre
pour leurs antagonistes respectifs.
h) Acide fusidique
? Mécanisme d'action
L'acide fusidique agit sur la synthèse protéique en
inhibant le facteur d'élongation, ce qui bloque la traduction de l'ARN
messager au niveau de la sous-unité 50 S du ribosome.
? Mécanisme de résistance
Chez S. aureus, la résistance à l'acide fusidique
est due à une mutation chromosomique, ce qui justifie l'emploi de cet
antibiotique en association. L'incidence est de 1 à 2% en France.
i) Fosfomycine
? Mode d'action
C'est un antibiotique bactéricide qui agit en inhibant la
synthèse de la paroi bactérienne, mais de façon
différente de celle des bêta-lactamines alors il peut y avoir une
association entre les deux molécules.
En effet, la fosfomycine inhibe la pyruvyl-transférase,
enzyme intervenant dans la première étape de la synthèse
du peptidoglycane.
? Mécanisme de résistance
La fosfomycine n'induit pas de résistance plasmidique mais
une résistance chromosomique est d'apparition fréquente et
rapide. Donc, il faut éviter de l'utiliser au long cours, en
monothérapie [39].
17
CHAPITRE II : MATERIEL ET METHODES
II.1. Cadre de l'étude
Notre étude a été effectuée au
Centre Universitaire de Diagnostic du Graben (CUDG) à Butembo. Il
organise en son sein les services suivants : microbiologie, hématologie,
parasitologie, immuno-sérologie, biochimie, hormonologie,
anatomo-cyto-pathologie, physico-chimie et bromatologie, contrôle
pharmaceutique et l'unité de production d'eau distillée et autres
réactifs.
Les objectifs poursuivis par le CUDG sont :
- Servir d'outil pédagogique et de recherche aux
professeurs et étudiants de l'Université Catholique du Graben et
ceux des autres institutions de l'enseignement supérieur et
universitaire de la place en vue d'une formation pratique ;
- Contribuer à la résolution de grands
problèmes sanitaires du milieu en élevant le niveau technique du
diagnostic qui demeure rudimentaire ;
- Effectuer les surveillances épidémiologiques,
qualitatives, toxicologiques grâce aux analyses des aliments, des
boissons et des médicaments afin de contribuer à la
prévention ;
- Servir d'outil précieux aux médecins
grâce aux analyses biomédicales.
II.2. Matériel
La population d'étude est constituée des
patients qui se sont présentés au CUDG et/ou ceux dont un
échantillon a été envoyé au CUDG pour des analyses
microbiologiques (culture) après suspicion d'une infection
bactérienne invasive. Ces patients étaient de tout âge,
sans distinction de sexe ni du type d'échantillon prélevé
pour la culture (sang, urines, pus, sécrétions respiratoires,
frottis vaginal, selles,...).
II.3. Méthodes
Nous avons procédé à une étude
prospective transversale allant du 1er Septembre 2018 au 31
Décembre 2018.
Ont été inclus dans cette étude, tous les
patients chez qui le germe S. aureus a été isolé
de l'échantillon prélevé. Les échantillons
cliniques humains concernés par cette étude étaient le
sang, les urines, le selles, les secrétions purulentes de la peau/plaie,
oreilles-nasopharynx-larynx, frottis vaginal et urétral, liquide
céphalo-rachidien(LCR), etc.
18
Ont été exclus de notre étude tous les
patients dont le germe isolé était autre que le S.
aureus, ceux dont le germe isolé était des souches de
staphylocoques à coagulase négative, ceux dont les
paramètres n'étaient pas complets et ceux dont les
résultats n'étaient pas disponibles pendant la période de
notre étude.
Notre échantillon était exhaustif et non
probabiliste, incluant tous les patients ayant réuni les critères
d'inclusion. Pour des raisons pratiques d'accessibilité et de
coût, la technique de sélection par convenance a été
utilisée pour les analyses des échantillons
prélevés.
La collecte des données a été faite
à l'aide d'une fiche de collecte de données, reprise en annexe
n°1. Un numéro était attribué à chaque patient
pour conserver l'anonymat. Les données sociodémographiques des
patients dont les échantillons prélevés ont répondu
à nos critères d'inclusion étaient trouvées dans le
registre du service de microbiologie du CUDG. Les variables d'étude
étaient constituées de : sexe, âge, adresse, type de
produit biologique prélevé, origine de l'échantillon, type
d'examen microbiologique réalisé, résultats de la culture
et de la coloration Gram de SARM
Analyses bactériologiques
Le prélèvement est une étape essentielle
du diagnostic car, c'est de sa qualité que dépend l'analyse
bactériologique. Les prélèvements provenant de divers
produits pathologiques (sang, urine, pus, LCR, frottis vaginal, frottis
urétral, selles, secrétions diverses,...) ont été
effectuées selon la technique appropriée à chaque
prélèvement. Ensuite, les souches de germes ont été
isolées et identifiées.
On procèdait directement à une recherche de
germes et cela en déchargeant en stries condensées
l'écouvillon de prélèvement sur toute la surface de la
boite gélosée. Trois types de milieux de culture ont
été utilisés : la gélose Chapman, gélose au
sang (GS), gélose de Mac-Conkey et incubés pendant 18 à 24
h à 37°C.
La purification des souches était basée sur les
caractères culturaux et la coloration de Gram. A partir des colonies
isolées sur les différents milieux (Chapman, GS, Mac-Conkey), on
procèdait directement à la coloration de Gram. Ensuite, les
colonies étaient sélectionnées : cocci à Gram
positif et bacilles à Gram négatifs. Le germe de candida qui
était isolé était confirmé par la croissance sur le
milieu de Sabouraud. La purification se faisait en poursuivant le repiquage sur
le même type de milieu jusqu'à l'obtention d'un isolat pure
présentant les mêmes caractéristiques que celui obtenu en
premier isolement. La dernière culture pure était faite sur
gélose nutritive pour faire l'objet d'autres tests.
19
La conservation de courte durée des isolats
purifiés était réalisée par ensemencement sur
gélose nutritive inclinée par l'anse de platine. Après
incubation à 37°C pendant 24 heures, les tubes étaient
conservés au réfrigérateur à 4°C. Les tubes
étaient stockés à la température ambiante.
Après la coloration Gram et les caractéristiques
de la colonie, les germes isolés étaient identifiés
à partir d'autres techniques standard de la microbiologie : les
propriétés biochimiques incluant la catalase, la coagulase (libre
ou liée), la production d'ADNase, la croissance sur le disque d'agar de
mannitol salé et l'activité hémolytique sur le disque
d'agar. Pour les germes Gram-négatif, le Triple Sugar Iron (TSI), la
motilité, l'indole, l'utilisation du citrate, l'uréase, l'oxydase
et la production de sulfure d'hydrogène, l'épreuve de
Voges-Proskauer (VP) étaient utilisés.
La sensibilité aux antibiotiques testée pour
tous les germes isolés était faite à l'aide de la
méthode de diffusion de disque de Kirby-Bauer sur le milieu de
Mueller-Hinton (oxoid) conformément aux recommandations du Clinical and
Laboratory Standards Institute (CLSI, 2017) [43]. L'interprétation des
souches (sensibles, intermédiaires ou résistantes) se faisait
selon les diamètres critiques recommandés par le CLSI.
Les antibiotiques dont la sensibilité était
testée sont les suivants :
- Les bêta-lactamines : oxacilline (1jig),
amoxicilline-acide clavulanique (20+10jig), cefotaxime (30 jig), ceftriaxone
(30 jig), méropenème (10 jig),
- Un glycopetide : vancomycine (30 jig),
- Les aminosides : gentamicine (10 jig), Amikacine (30
jig), neomycine (30 jig), spectinomycine (100 jig),
- Un phénicolé : chloramphénicol (30
jig),
- Une tétracycline : doxycycline (30 jig),
- Les macrolides: érythromycine (15 jig),azithromycine
(15 jig), clarithromycine (15 jig),
- Un lincosamide : clindamycine (2 jig),
- Les fluoroquinolones systémiques : ciprofloxacin (5 jig)
et levofloxacin (5 jig),
- Un sulfamidé : co-trimoxazole(200 jig+5 jig)
La suspicion de la résistance à la
méthicilline étaient effectuée par la méthode de
diffusion, d'une part du disque de céfoxitine 30 jig où un
diamètre d'inhibition autour du disque de moins de 27 mm et la
présence de colonies dans la zone d'inhibition témoignaient
20
de la présence d'un SARM, et d'autre part, par le
disque d'oxacilline 5 mg où la présence d'une souche ayant un
diamètre < 20 mm était considérée comme SARM.
? Saisie et analyses des données
La saisie et l'analyse des données ont
été effectuées à l'aide du logiciel SSPS Version
22.
Les liens entre les différentes variables ont
été examinés à travers les tableaux
bi-variés en utilisant les tests de signification tels que les Odds
Ratio (OR), les intervalles de confiance (IC) et le P-value. Le seuil
de signification était fixé à 95%. L'association
était dite significative si l'OR était supérieur à
1 et quand l'intervalle de confiance ne contenait pas 1. Elle était
aussi significative si P était inférieur à 0,05. L'OR a
été utilisé pour déterminer le niveau de risque
attribuable à un facteur F dans l'exposition de la population à
un germe antibiorésistant. Cette association était
qualifiée de significative quand l'intervalle de confiance ne contenait
pas 1.
| 


