II.2.3. Le dosimètre thermoluminescent
La thermoluminescence (TL) est l?émission de
lumière observée autour de températures bien
définies (pic) quand on réchauffe un solide cristallisé
dit phosphore, qui a subit au préalable une irradiation ionisante
provenant de rayonnement naturel ou artificiel. Cette émission
thermostimulée est connue depuis fort longtemps, vraisemblablement
depuis la préhistoire, mais c?est Sir Robert Boyle qui le premier en fit
la description scientifique. En 1663, il décrivit une (étrange et
pâle lueur) émise par un diamant qu?il avait chauffé dans
l?obscurité. Ce n?est qu?en 1945 que sera développée par
J.T. Randall et H.F. Wilkins la première théorie permettant
d?expliquer l?émission lumineuse lors du chauffage. [SFPM
N°18-00]
Le domaine d?application de la TL est vaste allant de la
physique du solide à la dosimétrie des rayonnements ionisants.
Dans le cadre de notre étude nous nous sommes intéressés
seulement à la propriété dosimétrique des
détecteurs thermoluminescents (TLD).
La dosimétrie par thermoluminescence reste et restera
encore pendant de nombreuses années une technique de choix pour la
dosimétrie en radiothérapie. [HAB05]
Les TLD sont utilisés en routine pour la
vérification de la dose délivrée lors des traitements par
irradiation corporelle totale. Ils sont également utilisés dans
différents programmes postaux pour des audits de qualité externe,
permettant de contrôler la dose délivrée par les
accélérateurs dans les conditions de références et
de non références.
II.2.3.1. Généralités sur le
cristal
a) Le cristal parfait
Le cristal parfait est un solide dont la structure est
constituée de molécules ou d?atomes dans un réseau
périodique. Le réseau est obtenu par translations dans toutes les
directions d?une unité de base. Cette unité de base est le plus
petit volume cristallin du réseau et est appelée maille
élémentaire. Chaque élément de la maille est
associé à un site bien défini autour duquel il peut
effectuer des mouvements de vibration.
La théorie des bandes décrit la structure
électronique d?un cristal. Cette théorie stipule que la
périodicité d?un réseau cristallin est à l?origine
d?un diagramme énergétique comportant des bandes
d?énergies permises et accessibles aux porteurs de charges et des bandes
d?énergies interdites. La dernière bande d?énergie permise
est appelée la bande de conduction (BC).
La bande de valence (BV) est l?avant dernière bande
d?énergie permise. Les électrons de valence des atomes sont
situés dans cette bande. Les deux bandes sont séparées par
une bande interdite aux électrons (BI) d?énergie Eg,
également appelée gap. L?énergie Eg est une
grandeur caractéristique du matériau (figure II.8) et
représente l?énergie nécessaire à un
électron de valence pour accéder à la bande de
conduction.
b) Le cristal réel
Le cristal réel est un réseau d?atomes, dont la
périodicité est perturbée ou rompue par des
défauts. Si la perturbation est localisée au niveau d?un atome ou
d?une maille élémentaire, on parle de défauts ponctuels.
Lorsque les perturbations sont étendues au sein du réseau, on
parle de défauts étendus S. Il existe plusieurs types de
défauts ponctuels comme la lacune, les atomes interstitiels ou encore
les impuretés chimiques. La lacune correspond à l?absence d?un
atome sur un site normalement occupé. Les atomes interstitiels sont des
atomes positionnés entre les atomes du réseau. La présence
d?impuretés chimiques se rapporte à la présence d?atomes
étrangers au réseau cristallin, en position interstitielle ou en
substitution. Dans
le cas d?un cristal avec plusieurs types d?atomes, le
remplacement d?un atome par un atome d?un autre type dans le réseau est
appelé défaut anti-site. La figure montre les différents
types de défauts ponctuels que l?on peut trouver dans un réseau
cristallin constitué de deux types d?atomes A et B.
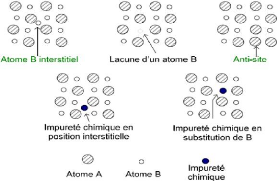
Figure II. 6. Différents défauts ponctuels
dans un réseau cristallin
Les associations de défauts ponctuels dans un
réseau cristallin sont possibles (Figure II.7). Dans le cas
d?un cristal ionique on peut ainsi trouver l?association d?une lacune
anionique et d?une lacune cationique. Cette association est
connue sous le nom de défaut de Schottky. Le défaut de
Frenkel correspond au déplacement d?une espèce du réseau
cristallin de son site vers une position interstitielle. Il s?agit donc d?une
association d?une espèce cristalline en position interstitielle et de la
lacune associée. Les défauts ponctuels confèrent au
cristal des propriétés spécifiques comme la couleur du
cristal ou encore la conduction du courant électrique.
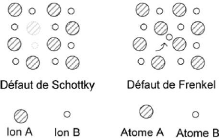
Figure II. 7. Exemples d'associations de défauts
ponctuels: défaut de Schottky
(Lacune de 2 ions) et
défaut de Frenkel (déplacement d'un ion)
Parmi les défauts étendus on distingue les
défauts de volume et de surface comme les joints de grains. Ces derniers
peuvent être définis comme la juxtaposition de deux grains. Des
erreurs d?empilement d?atomes ou de plans modifient la
périodicité du réseau cristallin au niveau d?au moins une
chaîne d?atomes. Ainsi la rupture d?un plan atomique est appelée
dislocation.
Les perturbations induites par les défauts introduisent
des changements dans les niveaux d?énergie permis d?un cristal. Dans
certains cas, la perturbation est suffisamment importante pour produire un
état électronique localisé dans la bande interdite. Ces
niveaux électroniques sont appelés pièges. Si un niveau
possède une section efficace de capture des électrons très
supérieure à celle des trous, se>>st, ce niveau est
appelé piège à électrons. Dans le cas contraire, le
niveau est appelé piège à trous. Certains de ces
pièges peuvent être le siège de recombinaisons
électron-trou, on dit alors qu?il s?agit d?un centre de recombinaison.
Les pièges à électrons sont des niveaux donneurs
d?électrons à la bande de conduction. Ces niveaux donneurs sont
situés en dessous de la bande de conduction, tandis que les
pièges à trous sont proches de la bande de valence. Les
pièges à trous sont également appelés niveaux
accepteurs d?électrons. Dans le diagramme de bandes d?énergie,
les pièges suffisamment éloignés des bandes de conduction
ou de valence ne sont pas perturbés par la température ambiante
et sont appelés pièges métastables. Les pièges
situés près du niveau de Fermi sont caractérisés
par une section efficace de capture des électrons très proche de
celle des trous (se ~ st) et sont donc en général des centres de
recombinaison. Cependant, selon la température, les pièges
à électrons (trous) suffisamment éloignés de la
bande de conduction (valence) peuvent devenir des centres de recombinaisons.
Le schéma de bande de la (figure II.8) montre le cas
d?un isolant ayant un piège à électrons situé
à une énergie E sous le bas de la bande de conduction,
un piège à trous situé à une énergie
Ep au-dessus du haut de la bande de valence et deux centres de
recombinaison situés de part et d?autre du niveau de Fermi
caractérisé par Ef.

Figure II. 8. Schéma de bandes d'un cristal
réel
L?énergie E (Ep) correspond à
l?énergie nécessaire à apporter au cristal pour
dépiéger un électron (un trou) d?un piège à
électron (trou) vers la bande de conduction (valence). Cette
énergie est appelée énergie d?activation du piège
ou profondeur du piège.
| 


