|
Page | I
Epigraphe
«La pollution de la planète n'est qu'un
reflet extérieur d'une pollution, celle des millions d'individus
inconscients qui ne prennent pas la responsabilité de leur vie
intérieure»
Anonyme 2012
Gabin KANDJI
Page | II
Dédicace
Je dédie ce travail à :
Mon très cher papa CEMA MULIMA pour tous
ses efforts qu'il ne cesse jamais de manifester à mon égard,
malgré les multiples difficultés rencontrées. Que la
grâce et bénédiction vous soit accorder sur cette terre.
Ma mère marie KAJ MUNUNG pour m'avoir
gardé et pour tout son amour qu'elle n'a cessé de manifester. A
papa MIJI MWALINIKA, Victoire MUTETE,
DOULIN MIJI, Ethé KAYAKEZ.
Mon beau-frère NAWEZI Alger et son
épouse Mélina KAYAKEZ, mon grand frère
Patrick MWANGALA, Padou KANA pour leurs soutien financiers,
matériels que mon Dieu vous le rend au centuple.
Le pasteur Salomon KAFUKU et maman
Esther MWADI
Ma famille biologique sous le lien de CEMA et
MARIE, Gauthier MANYIK, Clitonne
MANSONJ, Yvon LUPANDDA, Jacquie KASAU
et ThéThé SONY.
Gabin KANDJI
Page | III
Remerciement
Ce travail de fin de premier cycle n'aurait jamais pu voir le
jour sans le soutien que j'ai reçu de la part de nombreuses personnes.
C'est avec un grand plaisir que je tiens donc à remercier :
Tout d'abord, Mon âme bénis l'Eternel Dieu pour
sa miséricorde, sa bonté ainsi que, pour la faveur
imméritée dont nous bénéficions auprès de
lui.
Comment exprimer ma profonde gratitude envers le Directeur de
ce travail l'ingénieur SAWALEWA Alain qui m'a si
formidablement encadré, soutenu et éclairé de ses
lumières pendant le moment de rédaction de ce travail, de ces
conseils précieux, Son encadrement consiste en un savant qui m'a permis
de vraiment d'achever ce travail. Ainsi qu'une disponibilité à
toute épreuve (toujours prêt à répondre aux
interrogations de tout genre).
Ma reconnaissance s'adresse au corps professoral de la
faculté des sciences agronomiques, au doyen Dr. MUTUNDA
Stanislas, le vice doyen Ir TSHALA joseph, la
secrétaire MAVUNGU Eliane et tous les assistants de la
faculté d'agronomie, trouvent l'expression de notre reconnaissance pour
tous les efforts consentis pour le développement de la faculté et
pour notre formation.
Ma reconnaissance va également au beau frère
NAWEZI MBUYA Alger et sa femme KAYAKEZ Mélina ; le pasteur KAFUKU
Salomon et sa chère épouse MWADI Esther, et mon grand
frère MWANGALA Patrick.
Je remercie très chaleureusement tous mes compagnons de
lutte : Aaron KAULU, Mechack TSHIFUNGA, Cédric MAKONGA, Popaul MUKENDI,
Blaise KATSHABA, Nadège MUSOZ, Pierre MUTOMB, Guy MOTA, Maxime NGOIE,
Patrick KASIL, Olivier NAWEJI, Christian MULUNDA, Giresse LUKUNGA, Bonheur
MWANABUTE, Israël KAFUKU, Jean Paul TSHALA, Ir Alain KITABALA, Pascal
IPANG, Jean KAJIMOTO. Enfin, merci à tous ceux qui ont rendu possible ce
travail et a toutes mes connaissances même s'ils ne se retrouvent pas
dans cette petite liste, ils sont dans mes pensées.
Page | IV
Résume
Un essai de phytostabilisation a été
réalisé dans le cadre de ce travail pour définir les
possibilités d'utilisation de Microchloa altéra en
revégétalisation des sols contaminés par les rejets
métallurgiques des usines de cuivre à Kolwezi. Cet essai avait
pour objectif général d'évaluer les effets
résiduels des amendements organiques et calcaires utilisés en
2014, afin de réduire la dispersion des éléments traces
dans l'environnement.
Pour y parvenir, un essai a été installé
suivant un dispositif en tiroir (SPLIT PLOT) composant 2 campagnes, 3 doses
d'amendement calcaire (0 t.ha-1, 10 t.ha-1 et 20
t.ha-1) et 3 d'amendement organique (0 t.ha-1, 45
t.ha-1 et 225 t.ha-1) répétées six
fois. Pour évaluer les effets de ces traitements sur le comportement de
M. altéra une série d'observation ont été
faites a différent stade de croissance.
Cependant, la tendance générale des
résultats obtenus montrent qu'une diminution sur tous les
paramètres observés au cours de la deuxième campagne. Par
ailleurs, bien qu'une diminution des résultats observés, l'apport
de 20 t.ha-1 des calcaires et 225 t.ha-1 de la
matière organique qui a donné les meilleurs résultats quel
que soit la campagne peuvent être recommandable. Les résultats
obtenus en première année sont expliqués par le fait que
les amendements organiques et calcaires auraient amélioré le
statut nutritionnel, ce qui expliquerait leurs effets hautement significatifs
sur la production des épis et hampes florales.
Mots clés : effets résiduels, amendement
organique et calcaire, M altéra, rejets métallurgiques,
campagne, UCK.
Page | V
Abstracts
A phytostabilisation test was conducted as part of this work
to define the possibilities of using Microchloa altera in revegetation
of soil contaminated with metal discharges from factories in Kolwezi copper.
This test was general objective to evaluate the residual effects of organic
amendments and limestone used in 2014 to reduce the dispersion of trace
elements in the environment. To achieve this, a test was installed following a
drawer device (SPLIT PLOT) component 2 campaigns, 3 doses of liming (0 t.ha-1,
10 and 20 t ha-1 t ha-1) and 3 organic amendments (0 t.ha-1, 45 t ha-1 and 225
t ha-1) repeated six times. To assess the effects of these treatments on the
behavior of Mr. altered a series of observations were made in different growth
stage. However, the general tangency of the results show a reduction on all
parameters observed during the second campaign. Furthermore, although a
decrease in results is observed for the intake of 20 t ha-1 of limestone and
225 t ha-1 of organic matter that has given the best results regardless of the
campaign can recommendable. The results obtained in the first year are
explained by the fact limestone and organic amendments would have improved the
nutritional status, which would explain their highly significant effects on the
production of corn and flower stalks.
Keywords: residual effects, organic soil and
limestone, M altered, metallurgical waste, country, UCK.
Page | VI
Sommaire
Epigraphe I
Dédicace II
Remerciement III
Résume IV
Abstracts V
Sommaire VI
Liste des tableaux VIII
Liste des figures et photos IX
Liste des abréviations X
Introduction 1
Chapitre 1. La revue de la littérature sur les
métaux lourds 3
1.1. Les métaux lourds 3
1.1.1. Définition des métaux lourds 3
1.1.2. Origine des métaux lourds 3
1.1.3. Formes et localisation des métaux dans le sol 5
Les métaux lourds existent dans six compartiments
différents du sol. 5
1.1.4. Mobilité, biodisponibilité et
toxicité des métaux lourds 5
1.1.5. Impact des métaux lourds dans l'environnement 9
1.1.6. Les teneurs en éléments métalliques
dans les végétaux 10
1.2. Réhabilitation des sols pollués en
métaux lourds 11
1.2.1. Phytostabilisation 12
1.2.2. Les plantes 13
1.2.3. Les amendements 14
a) Les amendements calcaires 15
b) matière organique 15
1.2.4. Mécanismes de résistance 16
1.2.5. Importance d'un couvert végétal 16
Chapitre 2. Milieu, matériel et méthode 18
2.1. Milieu 18
2.1.1. Aperçu géographique 18
2.1.2. Présentation de la zone d'étude 18
2.1.2.1. L'origine des bassins à rejets 19
2.2. Matériels 20
Page | VII
2.2.1. Matériel biologique 20
2.2.1.1. Microchloa altera 21
2. La Morphologie de Microchloa altera 21
2.2.2. Les amendements 22
2.3. Méthodes 23
2.3.1. Traitements et dispositif expérimental 23
2.3.2. Observations 25
2.3.3. Analyse des données 25
Chapitre 3. Présentation des résultats 26
3.1. Arrières-effets du calcaire et de la matière
organique sur le comportement de M. altéra planté
à
l'UCK 26
3.1 Influence des amendements calcaire et organique sur la
reprise au cours de deux campagnes 27
3.2 Influence des amendements calcaire et organique sur la survie
au 90ème jour au cours de deux
campagnes 27
3.3 Influence des amendements calcaire et organique sur le
paramètre diamètre au collet au cours deux
campagnes 28
3.4 Influence des amendements calcaire et organique la longueur
de hampe et le nombre de hampe au
cours deux campagnes 28
Chapitre 4. Discussion des résultats 29
Conclusion 31
Références bibliographiques 32
Annexe 36
Page | VIII
Liste des tableaux
Tableau 1. Toxicité des ETM sur les consommateurs 8
Tableau 2. Moyennes et écart types des paramètres
végétatifs et de productions de M altéra 26
Page | IX
Liste des figures et photos
Figure 1. Différentes formes et localisations des
éléments traces dans les sols (Baize, 1997) 5
Figure 2. Concentration en métaux lourds dans le sol :
le résultat de la biodisponibilité (Meerts, 2010) 7
Figure 3. Le cheminement des métaux lourds dans
l'environnement (Bert et Deram, 1999) 9
Figure 4: Localisation du site expérimental de l'usine
à cuivre de Kolwezi. (Google earth, Image satellitaire)
19
Figure 5 : Le plan du dispositif expérimental sur le
bassin à rejets métallurgiques de l'UCK 24
Photo 1: Le bassin des rejets métallurgiques d'UCK
(kandji Décembre 2015) 20
Photo 2: La touffe de Microchloa altéra sur un
sol pollué à l'UCK, faisant semblant de se sécher pendant
la
saison sèche 21
Page | X
Liste des abréviations
B : bore
Ca : calcium
Cd: cadmium
Cl: chlore
Co: cobalt
Cr : chrome
Cu : cuivre
F : fluor
Fe: fer
Hg: mercure
I: iode
K : potassium
Mg : magnésium
Mn : manganèse
Mo : molybdène
Na : sodium
N : azote
Ni : nickel
P : phosphore
Pb : plomb
Se : sélénium
Si : silicium
V : vanadium
Zn : zinc
CEC : Capacité d'Echange Cationique
DI : Diamètre
Eh : potentiel d'oxydo-réduction
ETM : Eléments Trace
Métalliques
FB : facteur de bioconcentration
KZC : concentrateur de Kolwezi
LH : Longueur des Hampes
NH : Nombre des Hampes
pH : Potentiel d'Hydrogène
TFC : Travail de Fin de Cycle
U.Z.K : usine de zinc de Kolwezi
Page | 1
Introduction
Le problème de sols pollués est aujourd'hui
très préoccupant pour les pays émergents. Les
métaux lourds tels que le Plomb, le Cadmium, le Cuivre, le Zinc et le
Mercure ne peuvent pas être biodégradés et donc persistent
dans l'environnement pendant de longues périodes. De plus ils sont
continuellement rajoutés dans les sols par des activités
minières telles que : l'extraction des boues d'épuration dans les
industries métallurgiques.
Cette accumulation des métaux lourds dans
l'écosystème peut avoir des effets néfastes sur la
santé des êtres humains et des animaux (Wang et al.,
2003). A l'échelle microscopique, les métaux lourds ont aussi des
effets négatifs sur la population bactérienne, ce qui n'est pas
sans conséquence sur le fonctionnement de l'écosystème
(Probha et al., 2007).
Différents procédés de
réhabilitation de sols contaminés existent, mais la
phytostabilisation parait comme la moins coûteuse et la plus
adaptée (Mpundu, 2010 ; Ngoy, 2010). L'utilisation des amendements dans
la phytostabilisation permet d'améliorer les propriétés
des sols contenant des niveaux toxiques d'ETM, de produits pétroliers
ayant des valeurs extrêmes de pH (Mulaji, 2010). L'ajout du compost
à de sols contaminés au Plomb a permis de réduire les
formes disponibles de Plomb et de Cuivre au niveau des sols amendés
(Charland et al., 2001).
Une autre technique de la phytoremédiation est la
phytostabilisation qui cherche à confiner la pollution à l'aide
d'espèces végétales tolérantes aux milieux
pollués et dont la couverture stabiliserait les couches des sols,
limitant ainsi la dispersion des métaux lourds par ruissellement, par
percolation et par le vent (Salt et al., 1998).
Dans cette partie du travail, nous nous sommes
intéressés à une espèce de plante tolérante
aux métaux et sur son potentiel en tant qu'outil de stabilisation des
sols et qui permettrait de restaurer les sites étudiés. Cette
espèce est Michlocoa altéra.
Ce travail poursuit comme objectif général,
l'installation d'une couverture végétale permanente sur les
rejets métallurgiques de l'usine à cuivre de Kolwezi (UCK), afin
de réduire la dispersion des éléments traces dans
l'environnement à travers l'érosion hydrique ou
éolienne.
Page | 2
Objectifs spécifiques :
> Installer une couverture végétale sur les
rejets pour la stabilité des éléments traces
métalliques
> Déterminer l'influencé des amendements de la
chaux et du compost sur la performance de Microchoa altéra
Les hypothèses retenues pour cette étude sont :
> Microchloa altéra se comporterait
favorablement sur les rejets métallurgiques issus des traitements
hydrométallurgiques de l'usine à cuivre de Kolwezi (UCK).
> L'utilisation des amendements pourrait améliorer les
propriétés des sols pour une influence positive sur la
performance de la culture
Outre l'introduction et la conclusion, ce travail s'articule en
quatre chapitres :
+ Le premier présente la revue de la littérature
+ Le deuxième illustre le milieu d'étude, les
matériels et méthodes
+ Le troisième fait la présentation des
résultats + Et le quatrième fait la discussion des
résultats.
Page | 3
Chapitre 1. La revue de la littérature sur
les
métaux lourds
1.1. Les métaux lourds
1.1.1. Définition des métaux
lourds
La définition du terme «
métaux lourds » varie selon les auteurs
mais communément, nous rassemblons sous cette appellation les
éléments d'une densité supérieure à 5g/cm3
que nous pouvons retrouver dans l'eau, l'air et le sol. Parmi les métaux
lourds, nous retrouvons des éléments majeurs et des
éléments traces, c'est-à-dire des éléments
dont la concentration dans la croute terrestre est pour chacun d'entre eux
inférieure à 1%. Dans le présent travail, nous utiliserons
de manière indifférenciée les termes métaux lourds
et les éléments traces métalliques. Parmi les
métaux lourds, on cite classiquement le Cd, Cr, Co, Cu, Sn, Fe, Mn, Hg,
Mo, Ni, Pb, Zn ainsi que trois autres éléments, le B, As et Se
qui ne sont cependant pas des métaux par leur structure atomique (Impens
et al, 1991). Certains métaux sont dit «
essentiels à la vie » (Fe, Mn, Zn, Cu,
Mo, Ni, Co...), ce sont les oligo-éléments, tandis que d'autres
sont dits « non nécessaires
»
(Cd, Hg, Pb...) (Bert et Deram, 1999). Dans les deux cas, en
concentrations trop importantes, ceux-ci deviennent toxiques pour la
biosphère (Bliefert et Perraud, 2001).
1.1.2. Origine des métaux lourds
La présence de métaux lourds dans les sols peut
être d'origine naturelle ou anthropique. L'origine naturelle de
métaux lourds est fonction du fond pédo-géochimique local
et des apports de poussières et aérosols libérés
dans l'atmosphère par l'activité volcanique, les embruns marins,
etc. La composition chimique de la roche-mère va influencer la richesse
future du sol en métaux. A cela, s'ajoute les sources anthropiques qui
sont, quant à elles, liées à l'exploitation et au
traitement des minéraux, à la fabrication et l'utilisation
d'engrais et de pesticides, à l'industrie chimique, aux décharges
et a l'incinération de déchets ménagers et industriels,
etc. L'accomplissement des cycles biogéochimiques des métaux dans
les sols et les plantes modifie la forme chimique des éléments
traces métalliques et participe à leur évolution dans les
sols. Enfin, les transferts pédologiques verticaux et latéraux
vont entrainer le lessivage des métaux vers les horizons profonds et les
nappes
Page | 4
phréatiques. Ainsi, les métaux se trouvent
disperses dans les différents horizons du sol (Bert et Deram, 1999 ;
Baize, 1997). Nous pouvons distinguer deux types des contaminations suit aux
apports à métaux lourds :
? « Les contaminations locales », qui touchent une
aire relativement faible et sont dues à une ou plusieurs source (s) bien
identifiée (s) et souvent très proches (quelques mètres
à quelques kilomètres). Il s'agit généralement
d'apports massifs, souvent associés aux exploitations minières,
aux installations industrielles et à d'autres installations, tant en
cour exploitation qu'après leur fermeture (Pereira et Sonnet, 2007).
? Les « contaminations diffuses », qui affectent
tous les sols, plus ou moins faiblement mais de manière
généralisée. Ce type de contamination résulte
principalement des dépôts atmosphériques qui ne peuvent pas
être liés à une ou plusieurs source (s) ponctuelle (s)
indispensable (s) et des pratiques agricoles et horticoles (épandages
d'engrais, d'amendements, de boues de stations d'épuration, traitements
phytosanitaires, etc.). Ce type de contamination ne peut être totalement
évité : elle est la conséquence d'apports involontaire
(émissions atmosphériques industrielles, par exemple) ou
d'impuretés indésirables dans les apports volontaires (ETM dans
les engrais minéraux, par exemple) (Pereira et Sonnet, 2007).
Page | 5
1.1.3. Formes et localisation des métaux dans le
sol
Les métaux lourds existent dans six compartiments
différents du sol.
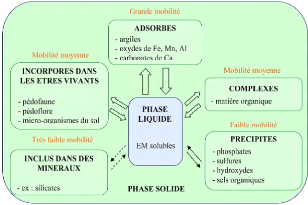
Figure 1. Différentes formes et
localisations des éléments traces dans les sols (Baize, 1997)
La solution du sol peut être le lien de fixation
à une phase solide, c'est le phénomène de sorption tandis
que l'influence des facteurs externes peut mener à ce que les
métaux repassent en solution, c'est le phénomène de
désorption (Baize, 2007). Les métaux lourds sous formes
associées à la phase liquide (solution du sol avec ses
élément solubles) qui, bien que minoritaires, sont les plus
importants puisqu'ils sont les plus biodisponibles (Pereira et Sonnet,
2007).
1.1.4. Mobilité, biodisponibilité et
toxicité des métaux lourds
Les métaux lourds ont tendances à passer d'une
forme à l'autre et leur répartition dans les différents
compartiments du sol évolue dans le temps. On appelle spéciation,
l'ensemble des espèces chimiques sous lesquelles les
éléments traces métalliques se présentent dans le
sol. Selon la spéciation, les liaisons qui se forment entre les
métaux lourds et autres composés seront différentes,
influençant la mobilité et donc la toxicité de ceux-ci.
Quatre facteurs influencent le comportement prévisible des métaux
lourds dans les sols : l'héritage minéralogique, les processus
pédologiques, la dynamique propre de l'élément chimique et
le fonctionnement actuel des sols (Baize, 1997).
Page | 6
Sans un minimum de mobilité ou biodisponibilité,
les métaux lourds, disséminés dans l'atmosphère
puis de manière non homogène dans le sol, peuvent y rester de
nombreuses années étant donné leur persistance,
c'est-à-dire leur faible capacité de dégradation par voie
biologique ou chimique. La mobilité d'un élément trace
métallique constitue l'aptitude d'un élément à
passer dans de compartiment du sol ou il est de moins en moins
énergétiquement retenu, avec comme compartiment ultime la phase
liquide ou dans certains cas, l'atmosphère du sol (Juste, 1988).
Il existe des multiples paramètres influençant
la mobilité des métaux dans les sols dont les plus importants
sont (Colinet, 2003) :
? Le pH : à pH faible, la solubilité de la
plupart des métaux est plus élevée (Alloway, 1995);
? Le potentiel redox (Eh) : en condition réduites, la
mobilité des métaux lourds est fortement liée au pH
puisqu'il augmente quand celui-ci diminue (Alloway, 1995) ;
? La quantité et la composition de la matière
organique, les métaux peuvent être
complexés. Ils forment alors un complexe
organométallique et sont immobilisés. Malgré
l'immobilisation, il peut y avoir un phénomène de
l'immobilisation, c'est-à- dire la précipitation
simultanée d'un agent chimique en conjonction avec la matière
organique (Kabata-Pendias et Pendias, 2001) ;
? La capacité d'échange ionique : les
métaux lourds ont une grande affinité avec la fraction argileuse
du sol ainsi qu'avec d'autres phases minérales comme les oxydes de Fer,
d'Aluminium, de Manganèse ou les Phosphates, les Carbonates
etc. la présence de ces
éléments favorise l'immobilisation des métaux lourds. En
effet, ils possèdent une charge électronégative qui leur
permet de contracter des laissons réversible avec, notamment, les
cations métalliques qui restent échangeable. La capacité
d'échange ionique minérale joue un rôle plus important dans
la fixation que la matière organique (Alloway, 1995 ; Impens et al,
1991).
D'autre facteur influencent la mobilité de
métaux lourds dans les sols. La température peut avoir un effet
direct sur les équilibre physico-chimique (solubilisation,
cinétique d'échange...) et un effet indirect lié aux
conséquences de l'activité microbiologique. Les micro-organismes
sont capables d'accumuler des éléments trace métalliques
dans leurs tissus, de modifier le pH, de libérer des ions...
(Kabata-Pendias et Pendias, 2001).
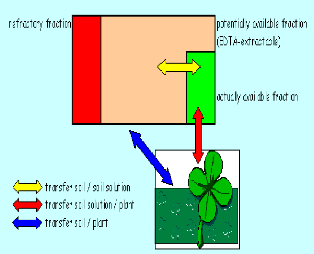
Figure 2. Concentration en métaux lourds
dans le sol : le résultat de la biodisponibilité (Meerts,
2010)
Page | 7
La biodisponibilité représente la
capacité d'un élément trace métallique à
passer d'un compartiment du sol quel qu'il soit vers une bactérie, un
animal ou végétal vivant dans ce dernier (Juste, 1988).
Les quantités des métaux lourds absorbés
par les plantes sont fonction de nombreux facteurs. Premièrement, il y a
les facteurs liés au sol, tels que les matériaux parental, le
type de pédogénèse, le pH, la matière organique,...
; Deuxièmement, l'absorption et le transfert du polluant est fonction de
la plante (espèce, cultivar, morphologie racinaire, types
d'exsudats...).
La plante peut produire des exsudats racinaires susceptibles
d'entrer en interaction avec les métaux lourds ou de provoquer le
développement d'une flore microbienne entrant en compétition avec
le végétal pour l'absorption des certains éléments
ou favorisant l'absorption de ces éléments via la production de
ligans organiques ; Troisièmement, les caractéristiques de
l'environnement physique comme la température, l'humidité, etc.
jouent également un rôle ; Enfin, l'absorption est fonction de
l'environnement microbien ainsi que des éléments eux-mêmes
et de leurs inter actions (Colinet, 2003 ; Juste, 1988).
Page | 8
Tableau 1. Toxicité des ETM sur les
consommateurs
Cadmium (Cd) Cuivre (Cu) Cobalt (Co) Plomb (Pb) Zinc
(Zn)
Elément
|
Toxicité aigue
|
Pneumonie, troubles hépato-digestifs (vomissements,
diarrhées)
|
Troubles rénaux, du système nerveux et du
système cardio-vasculaire
|
Troubles digestifs (vomissements)
|
Anémie, néphropathie (avec comme
conséquence
élévation de
l'azotémie,
protéinurie...)
|
Trouble gastrointestinal, atteinte du système digestif
supérieur, irritation des muqueuses respiratoires
|
|
Syndrome
|
Douleurs
|
Douleurs gastro-
|
|
Effet goitrogène, fibrose
|
schizophrénique, troubles
|
abdominales,
coliques, troubles
|
intestinales,
altération des
|
|
pulmonaire, troubles gastro-intestinaux, dyspnée, perte de
poids et atteinte cardiaque
|
hépatiques
|
nerveux (convulsion, néphrite hématurique,
saturnisme)
|
réponses immunitaires, induit la carence en cuivre
|
|
Toxicité
Chronique
|
Troubles respiratoires (bronchite, emphysème...), troubles
rénaux (albuminurie), anémie, troubles nerveux
|
Références
A, D, F, G, H C, E, F C, D, F
Référence
A. Apao (1989) in Useni (2009)
B. Ari et al. (1991) in Useni (2009)
C. Boudene (2000) in Useni (2009)
D. Buchet et al. (1983) in Useni (2009)
E. Pennington et Jones (1987) in Useni (2009)
F. Razeyre (1991) in Useni (2009)
G. André (2003) in Useni (2009)
H. Miquel (2001) in Useni (2009)
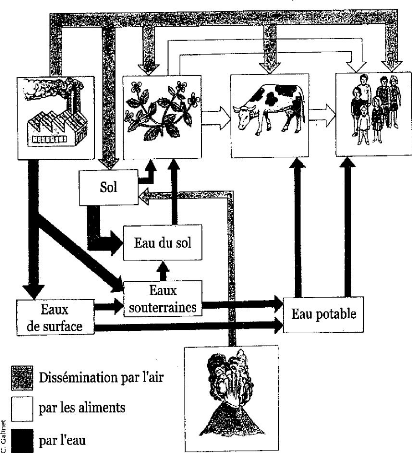
Figure 3. Le cheminement des métaux
lourds dans l'environnement (Bert et Deram, 1999)
Page | 9
1.1.5. Impact des métaux lourds dans
l'environnement
L'accumulation des métaux lourds dans les sols, l'eau,
constitue une menace. Le fait qu'ils puissent remonter la chaine trophique
représente un danger pour les écosystèmes et pour la
santé des organismes vivants et peut avoir des conséquences
sociales, environnementales et économiques caractéristiques.
Page | 10
« Les trop fortes teneurs en métaux lourds
diminuent la densité, la biodiversité et l'activité de la
microflore et de la microfaune du sol » (Bert et Deram, 1999).
Toutefois, la perte de biodiversité de la microflore et
de la microfaune est discutable. En effet, nous verrons que des écotypes
végétaux se développent spécifiquement sur des
sites métallifères.
« L'aération du sol est moins bonne, la
minéralisation de la matière organique est plus lent. A long
terme, le fonctionnement de l'écosystème sol est réduit
ainsi que sa fertilité. La nutrition est le métabolisme des
plantes sont perturbés. Certaines espèces
végétales, non tolérantes disparaissent, ce qui entraine
des changements dans la composition des communautés
végétales » (Bert et Deram, 1999).
« Les animaux peuvent être contaminés par
contact avec la peau, par inhalation de poussières toxiques et par
ingestion de l'eau et d'aliment pollués. La dispersion des métaux
constitue un danger par la faune sauvage, le bétail et l'homme, qui se
situe en bout de chaine alimentaire. Dans certaines zones très
contaminées à l'alimentation humaine sont interdites » (Bert
et Deram, 1999).
1.1.6. Les teneurs en éléments
métalliques dans les végétaux
Les éléments nécessaires pour assurer la
croissance et le développement de la plante sont dits essentiels. Ils
sont traditionnellement subdivisés en trois catégories: les
macroéléments ou éléments de base,
éléments secondaire et les micro- ou
oligo-éléments. Ce classement est le reflet des concentrations
relatives de ces éléments dans les tissus végétaux
(FERTIAL, 2010). Les macroéléments (exprimés en % de
matière sèche) comprennent l'N (1 à 3%), le K (2 à
4%), et le P (0,1 à 0,5%).
Les éléments secondaires : le Ca (1 à
2%), le Mg (0,1 à 0,7%), et le S (0,1 à 0,6%). Les
micro-éléments comprennent des éléments qui sont
classés ici par concentration décroissante : Fe, Mn, Zn, Cu, B,
Ni, Co, Mo. Les autres contaminants métalliques ne sont pas essentiels
pour la plante (Tremel-Schaub et Feix, 2005). Nous pouvons constater que les
teneurs normalement retrouvées chez les plantes ainsi que leurs teneurs
observées lors de contamination des sols varient
considérablement. Ces teneurs dépendent de l'espèce
végétale, de la variété mais aussi l'âge.
Voici quelques caractéristiques particulières de
phytodisponibilité de métaux d'après (Tremel-Schaub et
Feix, 2005).
Page | 11
> Le Zn : Comme pour la plupart des
éléments métalliques, la phytodisponibilité du Zn
dépend surtout du pH. Le Zn se concentre surtout dans les racines mais
est également présent dans les parties aériennes. Le
chaulage, un apport d'argile, de Fe ou de P diminuent le transfert du Zn vers
les plantes.
> Le Cu : il voit sa phytodisponibilité
diminuer avec le chaulage ou avec l'apport des matières organiques. Le
Zn ralentit l'absorption du Cu. Le Cu a tendance à s'accumuler dans les
racines, son insolubilisation est aussi obtenue par la précipitation
avec les phosphates, la formation de complexes de sphère interne
(adsorption) ou de sphère externe (échange d'ions) avec la phase
solide et l'augmentation du pH.
> Le Cd : Il est très phytodisponible et
peut s'accumuler à la fois dans les racines et dans les parties
aériennes. Sa biodisponibilité est plus importante pour des pH
acides et elle peut diminuer si on ajoute de la chaux, du Cu ou du Zn au
sol.
> Le Co : La disponibilité du Co
dépend des oxydes de Mn qui fixent le Co.
> Le Pb : La biodisponibilité du Pb est
également dépendante du pH, il est fixé par les oxydes de
Fer et d'Aluminium.
1.2. Réhabilitation des sols pollués en
métaux lourds
La phytoremédiation est définie comme
étant l'utilisation de plantes et de techniques culturales
appropriées pour éliminer, contenir ou rendre inoffensifs les
contaminants environnementaux présents dans sols et les eaux (Cunningham
& Ow, 1996). Elle présente des avantages économiques et
environnementaux qui justifient son utilisation dans le traitement des sites
contaminés. En particulier, son utilisation dans le traitement des sols
contaminés par les métaux lourds a pour objectif de
développer des techniques moins coûteuses et compatibles avec les
normes environnementales (Ensley, 2000). Les techniques de
phytoremédiation des métaux lourds peuvent être
divisées en trois groupes :
> La phytoextraction: c'est l'utilisation
des plantes accumulatrices pour extraire les métaux lourds des sols
contaminé;
> La rhyzofiltration: cette technique
utilise les racines des plantes accumulatrices pour absorber et diminuer la
quantité des métaux dans les effluents et eaux
polluées;
Page | 12
? La phytostabilisation:
c'est l'utilisation des plantes tolérantes pour réduire
la mobilité (et donc la biodisponibilité) des métaux
lourds, diminuant ainsi leur lessivage ainsi que le transport par le vent. Pour
cette dernière technique, il est souvent nécessaire d'utiliser
des amendements pour améliorer les conditions d'installation de la
culture.
Parmi ces trois techniques, la phytostabilisation peut
être la mieux appropriée et la plus raisonnable pour la
restauration des sites contaminés par les activités
minières. En effet, un programme de phytoextraction serait utopique car
: d'une part les contaminations des sols sont généralement de
nature polymétalliques, bien que le cuivre soit l'élément
le plus abondant, alors que les espèces hyperaccumulatirices le sont
généralement pour un métal, deux à la limite ;
d'autre part les teneurs en métaux étant trop
élevées et la biomasse des plantes faible, il faudrait des
milliers d'années pour décontaminer les sols.
1.2.1. Phytostabilisation
La phytostabilisation est une technique de
Phytoremédiation qui n'a pas vocation à « nettoyer »
les sols, mais à immobiliser et séquestrer les contaminants dans
un sol pollué grâce aux plantes. Cette technique a pour fonction
de stabiliser la couverture végétale sur des terrains
pollués qui n'en n'ont pas ou peu, d'améliorer la
biodiversité, de réduire la fonction métallique facilement
assimilable par les plantes et de limiter l'accumulation des métaux par
celles-ci (Ineris, 2010).
La phytostabilisation consiste en l'utilisation des
capacités de la plante à absorber les contaminants et à
stabiliser le sol via le système racinaire, protégeant ainsi le
sol de l'érosion par le vent et l'eau et réduisant les
percolations d'eau à travers les sols. Les plantes vont immobiliser les
contaminants dans la zone racinaire par l'exsudation des composés
chimiques, par l'inhibition des protéines de transport dans les
membranes racinaires et par le stockage des contaminants dans les vacuoles des
cellules racinaires (Bert et Deram, 1999 ; Anonyme, 2009).
Selon Impens et al. (1991), le recolonisation
végétale s'effectue en deux phases dont l'ordre d'application
varie en fonction des circonstances.
« 1ère phase : le semis
d'espèces herbacées, et parfois d'espèces ligneuses, en
choisissant des espèces adaptées (tolérantes) au (x)
métal (aux) présent (s), soit un ensemble d'espèces
relevant de la végétation typique de la région. Les
principes étant défavorisés la colonisation naturelle
du
Page | 13
site et d'accélérer le processus de colonisation
en fertilisant le sol et en l'amendant. Sur terrain acide, un chaulage sera
souvent favorable ».
« 2ième phase : consiste à planter des
espèces ligneuses. On apportera ou non dans le trou de plantation un sol
seul riche en fertilisants et amendement organiques. Si cette tâche est
souvent difficile dans les sites miniers et les friches industrielles,
l'opération est plus facile à réaliser dans les terrains
contaminés ».
La culture des végétaux tolérants aux
métaux peut donc être précédée de
l'incorporation d'amendements au sol tel que (Ademe, 2010) :
? Des minéraux phosphatés ;
? Des amendements calciques ;
? Des alimino-silicates pur ou associés ;
? Des oxydes ou hydroxydes de Fe, Al, Mn ;
? Divers substrats organiques.
Les amendements changent la forme chimique de contaminants
dans le sol et permettent la diminution de leur disponibilité et donc de
leur toxicité, c'est ce que l'on appelle « les techniques
d'inactivation ». Le choix de l'amendement ainsi que du couvert
végétal et réalisé de manière à ce
que l'effet d'immobilisation soit durable (Ademe, 2010 ; Dechamp et Meerts,
2003).
1.2.2. Les plantes
Les plantes utilisées en phytostabilisation doivent
évidemment être tolérantes aux métaux lourds
présents dans le sol. Elles devraient, de préférence, ne
pas accumuler les métaux dans leurs parties aériennes car
celles-ci peuvent être consommées par des animaux ou les humains ;
elles doivent également supporter les autres conditions du sol (pH bas,
salinité, structure défavorable, sécheresse) qui peuvent
limiter la croissance des plantes dans les zones à remédier ;
avoir un développement rapide pour établir un couvert
végétal dans un bref délai, avoir un système
racinaire extensif et un port denses. De plus, les plantes doivent être
faciles à établir et à entretenir, et avoir relativement
une longue vie ou être apte à se propager d'elles-mêmes
(Zhou & Wong, 2001 ; Kiikliä, 2002).
Page | 14
Pour être un bon candidat à la phytostabilisation,
une plante doit (Meetrs et Deram, 1999) :
? Tolérer les métaux du site à
remédier ;
? Tolérer les conditions de culture de ce site ;
? Accumuler préférentiellement dans ses racines
pour éviter la pénétration des contaminants dans des
niveaux trophiques plus élevés ;
? Induire une importante couverture végétale ;
? Avoir des nombreuses racines moyennement profondes, qui
stabilisent bien le sol.
Le type de plante et d'amendement choisi varie en fonction des
caractéristiques du sol contaminé.
1.2.3. Les amendements
Les amendements utilisés en phytostabilisation doivent
inactiver le métal rapidement après incorporation dans le sol,
prévenant ainsi le lessivage et le prélèvement par les
plantes et réduisant la biodisponibilité. De plus, l'amendement
ne doit pas être cher, il doit être facile à manier et
à appliquer, sans danger pour les manipulateurs, compatible et non
toxique pour la plante choisie en revégétation, disponible ou
facile à produire et ne doit pas causer d'impact environnemental
supplémentaire au site. Parmi les amendements utilisés, de bons
résultats sur la mobilité du cuivre ont été obtenus
avec la chaux et la matière organique (Zhou & Wong, 2001 ;
Kiikliä, 2002).
L'amendement est l'apport d'un produit fertilisant ou d'un
matériau destiné à améliorer la qualité des
sols (en termes de structure et d'acidité).
Les amendements utilisés en phytostabilisation doivent
inactiver le métal rapidement après incorporation dans le sol,
prévenant ainsi le lessivage et le prélèvement par les
plantes et réduisant la biodisponibilité (Berti & Cunningham,
2000 ; Kumpiene et al, 2008 ; Madejon et al, 2006 ; Mench et
al, 2006). De plus, l'amendement ne doit pas être cher, il doit
être facile à manier et à appliquer, sans danger pour les
manipulateurs, compatible et non toxique pour la plante choisie en
revégétalisation, disponible ou facile à produire et ne
doit pas causer d'impact environnemental supplémentaire au site
(Kumpiene et al., 2008).
Page | 15
a) Les amendements calcaires
Les amendements calcaires sont épandus dans le but de
stimuler l'activité biologique du sol et participer même
très partiellement, à l'un ou l'autre des grands cycles
biogéochimiques du Carbone, de l'Azote, du Phosphore ou du Soufre. Les
principaux efforts de fertilisation que l'on met en oeuvre sont les amendements
calcaires et magnésiens dont le but est de favoriser l'activité
des bactéries du sol et en consolidant les complexes argilo-humiques.
Les sols, les plantes et les animaux ont besoin de calcium et
de Magnésium. On rappellera que les amendements calcaires jouent un
rôle physique, un rôle chimique et un rôle biologique. Le
Calcium joue un rôle physique, car il rend la structure des sols plus
meuble et plus stable. Celle-ci favorise la perméabilité à
l'eau et à l'air. Elle facilite le travail du sol et la
pénétration des racines.
Le Calcium agit aussi sur la structure et la stabilité
en favorisant l'humification et la stabilisation du complexe argilo-humique. Le
Calcium joue un rôle chimique dans la mesure où il
régularise le pH des sols et favorise les échanges d'ions. On
n'oubliera pas le rôle du Calcium dans la fixation réversible du
Phosphore.
Enfin, le Calcium joue un rôle sur l'activité
biologique dans les sols, sur tout en créant des conditions
préférentielles aux micro-organismes du sol (mobilité des
bases échangeables, pH ou légèrement acide, bonne
aération, humidité moyenne, chimie du fer et de l'alumine dans le
sol, etc.). La teneur en Calcium dans les sols varie constamment. Ce facteur
essentiel voudrait qu'on le mesure fréquemment et qu'on le maintienne
à un niveau acceptable par rapport aux types de sols auxquels on a
à faire, c'est-à-dire qu'il y a toujours lieu de distinguer les
sols calcaires, toujours riches en Calcium actif, les sols non calcaires, mais
bien pourvus en Calcium échangeable, le plus souvent sur terrains
siliceux et acides. Cela écrit, on se doit de rappeler que les
phénomènes naturels et permanant. Ces phénomènes
sont liés, par exemple, aux exportations de matière organique
depuis les agrosystèmes (récolte ou résidus de
récoltes), au lessivage, inéluctable en région
océanique et à l'addition d'engrais, surtout sous forme
soluble.
b) Matière organique
La matière organique du sol (MO) joue un rôle
similaire à celui de la fraction argileuse du sol en affectant la
concentration de métaux dans la plante, puisque la MO est un
contributeur majeur aux charges négatives dont dépend le pH du
sol, lequel permet une augmentation de la capacité du sol
Page | 16
de retenir les cations métalliques
(Représenté par la CEC). L'addition de la MO au sol sous forme de
compost peut par conséquent marquer la réduction du
prélèvement de cations métalliques par les plantes (Farfel
et al. 2005; Jones et al.1987).L'addition de la MO au sol permet de
réduire l'accumulation de l'arsenic par les plantes sur sol
contaminé (Cao et Ma, 2004). Cependant, il a été aussi
noté que la grande concentration de la MO dissoute dans le sol peut
conduire à une augmentation potentielle de la lixiviation de cations
métalliques, due à leur complexassions par la MO dissoute
(Sauvé et al., 2000). C'est particulièrement important
pour le cuivre.
1.2.4. Mécanismes de résistance
Face au stress déclenchée par une
biodisponibilité excessive en métaux lourds, les plantes peuvent
mettre en place deux mécanismes de résistance de nature
différente mais non exclusifs (Verkleij et Schat, 1990 ; Hopkins, 2003).
Certaines plantes choisissent la formule de l'évitement :
capacité
d'un organisme à éviter une absorption
importante de métaux. D'autres pratiquent la tolérance, ce qui
correspond à :
« La capacité d'une plante à survivre et
à se reproduire sur des sites toxiques ou hostiles, pour la plupart des
autres plantes, parce que le sol contient des quantités
élevées d'un ou plusieurs métaux. » (Baker et
Macnair, 1994 dans Bert et Deram, 1999).
La distinction qui est faite dans la littérature entre
la résistance par l'exclusion et la résistance par la
tolérance n'est pas toujours claire. Verkleij et Schat (1990)
considèrent que les mécanismes de la tolérance pourraient
faire partie des mécanismes d'évitements tandis que Baker et
Walker (1990) classent les mécanismes d'exclusion parmi les
stratégies de tolérance des plantes aux métaux.
En fonction du facteur de transfert sol-plante des
éléments traces métalliques, les plantes peuvent
être classées en quatre groupes : les excluantes, les
indicatrices, les accumulatrices et les hyperaccumulatrices.
1.2.5. Importance d'un couvert
végétal
L'implantation d'un couvert végétal de plantes
tolérantes permet de diminuer la dispersion de contaminants par
érosion éolienne et par lessivage. Les plantes tolérantes
vont aussi absorber dans une certaine mesure les contaminants créant
ainsi une zone d'exposition plus faible pour les autres.
Page | 17
L'implantation de végétaux agit aussi de
façon indirecte car leur canopée fournit un abri contre le vent
et l'ensoleillement souvent élevés dans ces sites et leur
litière est source de matière organique (Mench et al.
2005). Dans le cas de la phytostabilisation, un cortège assemblant
des espèces ligneuses et herbacées est conseillé. Les
arbres permettent de maintenir un flux d'eau vers la surface limitant le
lessivage et les herbacées limitent l'érosion éolienne et
la dispersion vers les écosystèmes adjacents grâce à
leur système racinaire très dense (Pilon-Smits, 2005). Cet
assemblage permet d'améliorer des propriétés du sol comme
la fertilité ou la capacité d'échange cationique,
d'augmenter la quantité de microorganismes et de diminuer
l'érosion. L'implantation de légumineuses capables de fixer
l'azote atmosphérique est bénéfique pour
l'écosystème (Guo et al. 2004). En effet, elles
permettent d'enrichir le sol en nutriments et l'utilisation combinée
d'annuelles et de pérennes permet de garantir un apport continu de
matière organique au sol.
Page | 18
Chapitre 2. Milieu, matériel et
méthode
2.1. Milieu
2.1.1. Aperçu géographique
Kolwezi est le milieu qui a servie d'étude pour ce
travail; Il est le chef-lieu de la Province de Lualaba, en République
Démocratique du Congo. Il est juché sur le plateau de Manika
à 1460 mètres d'altitude. Ses coordonnées
géographiques sont situé entre 26°27' longitude Est et
10°11' latitude Sud. Sa localisation sur les riches gisements miniers du
Cooper belt lui a valu la réputation de «poumon
économique» de la République Démocratique du Congo
(Dibwe, 2005; in Fwamba et al 2011).
La province du Lualaba couvre une superficie de 121 308
Km2, elle est bornée au Nord par la Province du Haut-Lomami ;
au Sud-Est par la République de la Zambie et la Province du Haut-Katanga
; au Sud-Ouest par l'Angola. La ville de Kolwezi est baignée par le
fleuve Lualaba, les lacs de retenue de Kando, de N'zilo, de Dikolongo et les
principales rivières : Pande, Dikulwe, Dipeta, Kalule- Nord, Kalule-Sud,
Mukuleshi, Lufupa, Ludi et Musonoie. Avec une superficie de 213 Km2,
répartie comme suit la commune de Dilala 154 km2 et la
commune de Manika 59 km2.
Le climat est tropical de type CW6 selon la classification de
Koppen (1930), avec alternance de deux saisons : la saison sèche qui va
du moins d'avril au moins d'octobre et la saison des pluies du mois de novembre
au moins de mars. La variation de la température est entre 18 et
20° C. Le sol est argilo-sablonneux avec un sous-sol riche en gisements
miniers (cuivre, cobalt, or, uranium et radium), sa végétation
est une savane boisée traversée par des rivières et des
ruisseaux.
2.1.2. Présentation de la zone
d'étude
Notre étude expérimentale s'est effectuée
à l'UCK, dans les installations précisément dans de bassin
des rejets minéralogiques à côté de l'usine
métallurgique, trouvée le long de la rivière Musonoie, UCK
qui est l'usine à cuivre de Kolwezi a servi de site pour l'étude
(Voir figure 4).
Page | 19
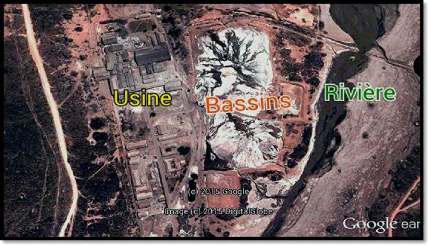
Figure 4: Localisation du site
expérimental de l'usine à cuivre de Kolwezi. (Google earth,
Image
satellitaire)
Cette zone est localisée à 1426 m d'altitude,
sur les coordonnées géographiques de 10°41'08" de latitude
Sud et 25°27'03" de longitude Est. Elle présente une superficie de
120.000 m2, un substrat à texture argilo-limoneux charger en
éléments métalliques tels que : Zn, Cu, Cd, Ge, Ga, Ag par
un dépôt des rejets issu des traitements
hydrométallurgiques.
2.1.2.1. L'origine des bassins à
rejets
L'UCK c'est une nouvelle nomination de l'ex-usine UZK depuis
2008, suite aux faibles demandes du Zinc sur les marchés mondiaux,
l'Usine du Zinc à Kolwezi a changé son entité pour
produire du cuivre. C'est depuis 1953 que l'ex-UZK produisait les Zinc, les
concentrés de zinc grillés (calcine) quittaient Likasi par voie
ferrée vers l'ex-UZK enfin d'être soumis au traitement par voie
hydrométallurgique. Les résidus obtenus après lixiviation
d'acide sont stockés dans des bassins justes à côté
de l'usine, ils sont stockés hors de normes environnementales
(Tshibanda, 2012).
Page | 20

Photo 1: Le bassin des rejets
métallurgiques d'UCK (kandji Décembre 2015)
2.2. Matériels
2.2.1. Matériel biologique
Une population de Microchloa altera constituée
d'individus récoltés d'une population mère située
à une friche minéralurgique aux alentours de la cité l'UZK
et de la rivière Musonoie. La mise en culture a eu lieu le 17
décembre 2015 sur le site décrit ci-haut (UCK).
1. taxonomie
· Règne : vegetaria
· Embranchement : Magnoloiphyta
· Classe : liliopsida
· Ordre : poale
· Famille : poaceae
· Genre : Microchloa
· Espece : Microchloa Altera
Page | 21
2.2.1.1. Microchloa altera
2. La Morphologie de Microchloa
altera
Renvoize, 1974 ; Pope, 1999 ; et Oudtshoorn, 2009 ; in
Shucha, 2010), décrit Microchoa altera des régions
montagneuses d'Afrique de l'Est et du Sud : comme une petite graminée
vivace cespiteuse de 30 à 70 cm de haut et formant des pelouses
compactes et denses (confer la photo)

Photo 2: La touffe de Microchloa
altéra sur un sol pollué à l'UCK, faisant semblant de
se sécher pendant la saison sèche
Les feuilles basales sont filiformes, courbées ou
rarement droites, glabres ou chevelues à la base, avec des
extrémités qui se terminent en angle aigue ou obtus et elles
mesurent 3-25 cm de longueur et 1,5 mm de largeur. Les hampes florales sont non
ramifiées, à l'exception des quelques une qui les sont, elles
portent 1 soit 2 épis à leurs extrémités varient de
2 à 9 cm de long sont droits ou courbés, glabres ou pubescents
à la base et portent deux rangées d'épillets
Les épillets 4 à 5,5 mm de long portent 2
rarement 3 fleurs : la fleur supérieure est mâle ou stérile
tandis que la fleur inférieure est hermaphrodite. Les glumes peuvent
être de tailles égales ou inégales, glabres ou parfois
laineuses.
La description du peuplement révèle que
Microchloa altera est une espèce des `steppes' basses des
hautes altitudes (plus de 1500 mètres) souvent établie sur sol
peu profond de pente mais également présente sur sol bien
drainé. L'espèce est rencontrée également dans les
dembos temporairement engorgés d'eau et parfois sur les
termitières des steppes inondées. Elle est
Page | 22
également rencontrée sur les sols
cuprifères de l'arc cuprifère katangais (Duvigneaud, 1963 ; Pope,
1999; in Shucha, 2010).
L'augmentation du nombre de substrat modifier par
l'activité minière, notamment les remblais miniers, les sols
riches en métaux à proximité des usines
métallurgiques, colluvions métallifères le long des cours
d'eau, bords de route et de voie ferrée enrichis en métaux
lourds, c'est ce qui explique l'éparpillement de cette espèce. Un
autre argument serait que les mouvements des personnes ainsi que de
l'équipement de travail ont probablement disséminés les
semences dans les carrières de l'UCK où l'espèce
était absente.
2.2.2. Les amendements
Le calcaire (CaCO3.MgCO3) et la matière organique
avaient été appliqués comme amendements pour
réduire la biodisponibilité des éléments
métalliques contenus dans le substrat du site d'étude. Le
calcaire utilisé avait été obtenu à l'UCK, c'est un
produit provenant de Likasi, produit par l'usine CCC (Carrière de chaux
et calcaire). Le carbonate de calcium diminue la mobilité des
éléments métalliques par l'augmentation du pH ; la
mobilité du cuivre, par exemple, baisse considérablement à
des pH supérieurs à 6. En outre, l'apport de Ca et Mg, deux
éléments souvent limitant dans les sols tropicaux, peuvent
favoriser la croissance des plantes et la restauration de communautés
vivantes diversifiées dans le sol (Shutcha, 2007).
La matière organique utilisée avait
été prise au dépôt d'ordures ménagères
de la cité UZK. L'utilisation de la matière organique se justifie
par le fait que la quantité de la matière organique et l'un des
facteurs qui a de l'influence sur le statut des éléments
métalliques dans le sol. La matière organique permet
d'immobiliser le Cu en le bloquant sous forme chélatée,
améliore le statut nutritionnel du sol, introduit des micro-organismes,
augmente la capacité d'échange cationique du sol, améliore
la rétention d'eau (Cheong et al. 1998, Walker et al.
2004, Chiu et al. 2006, in Migeon, 2008). Un pH trop
élevé peut entraîner la dissolution de la matière
organique, de même il faut prêter attention à la
dégradation de la matière organique dans le temps, car quand elle
diminue, l'activité des ions Cu2+ augmente aussitôt (McBride 1998;
in Migeon, 2008).
Page | 23
2.3. Méthodes
2.3.1. Traitements et dispositif
expérimental
Une expérimentation a été conduite selon
un dispositif factoriel 32. Deux facteurs ont été pris
en compte pour étudier leurs effets sur la performance de
l'espèce Microchloa altera, et chaque facteur a trois niveaux
:
? Calcaire (3 doses): 0 t.ha-1, 10
t.ha-1 et 20 t.ha-1 (C0, C1 et C2)
? Compost (3 doses) : 0 t/ha, 45 t/ha et 225 t/ha (M0, M1 et
M2)
Le dispositif compte 6 répétitions de 9
parcelles chacune correspondant aux 9 combinaisons Calcaire - Matière
organique (C0M0, C1M0, C2M0, C0M1, C1M1, C2M1, C0M2, C1M2 et C2M2) ceux qui
fera 54 parcelles de 4m2, transplanté avec 30 éclats
de souches par parcelles (5 lignes de 6 éclats des souches par ligne),
le 17 décembre jours après transplantation de Microchloa
altera.
Nous faisons l'étude des effets résiduels des
amendements utilisés deux ans passés, pour faire une comparaison
des résultats obtenus.
Page | 24
22 m

C0M1
M1
C0M0
C0M2
C1M1
M0
2m
M2
C0M2
C1M1
C0M0
C1M2
M1
C1M0
C0M1
C1M2
M0
M2
C1M0
M2
C0M2
M1
C1M1
C1M0
C1M2
M0
C1M0
C0M2
C1M2
M0
C0M0
C0M1
C0M0
M2
C0M1
M1
C1M1
M2
C0M0
C1M2
C0M1
C1M0
C0M0
M0
C1M0
C1M1
C0M2
M1
M2
C0M2
C1M1
C1M2
M1
M0
C0M1
14 m
1 m 0,5 m
2 m
Figure 5 : Le plan du dispositif
expérimental sur le bassin à rejets métallurgiques de
l'UCK
Légende :
C0M0 : Parcelle non amendée
C1M0 : Parcelle amendée avec 10 t/ha du calcaire
C2M0 : Parcelle amendée avec 20 t/ha du calcaire
C0M1 : Parcelle amendée avec 45 t/ha de la
matière organique
C1M1 : Parcelle amendée avec 10 t/ha du calcaire et 45
t/ha de la matière organique
C2M1 : Parcelle amendée avec 20 t/ha du calcaire et 45
t/ha de la matière organique
C0M2 : Parcelle amendée avec 225 t/ha de la
matière organique
C1M2 : Parcelle amendée avec 10 t/ha du calcaire et 225
t/ha de la matière organique
Page | 25
C2M2 : Parcelle amendée avec 20 t/ha du calcaire et 225
t/ha de la matière organique
2.3.2. Observations
Les observations faites sont les suivantes :
? Taux de survie : déterminé sur base
du nombre de plants vivants par rapport au total de ce qui a été
planté au début de l'expérimentation.
? Croissance : Surface d'un plant : estimée
sur base du diamètre moyen des touffes (moyenne du diamètre le
plus long et le plus court).
? Reproduction : taille de la hampe florale.
2.3.3. Analyse des données
Les données collectées ont été
analysées avec le logiciel R version
2.14.0. L'analyse de variance et le test de
comparaison des moyennes (LSD : Least Significant Difference) au seuil
de probabilité de 5% ont été effectués par la
méthode de Tukey. Cette comparaison a été effectuée
entre différents traitements (amendement organique et calcaire) sur
l'espèce M altéra et campagne entre elle.
Page | 26
Chapitre 3. Présentation des résultats
3.1. Arrières-effets du calcaire et de la
matière organique sur le comportement de M. altéra
planté à l'UCK
Tableau 2. Moyennes et écart types des
paramètres végétatifs et de productions de M
altéra
|
Dose calcaire
|
Dose matière organique
|
Taux de
survie à 30 jrs
|
Taux de survie à 90 jrs
|
Diamètre au
collet
|
Longueur de
hampe
|
Nombre de
hampe
|
|
Résultats au cours de la première campagne
(essai mémoire KATOMB, 2014)
|
|
0
|
0 t.ha-1
|
24#177;20,9
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
|
45 t.ha-1
|
46#177;13,7
|
11,6#177;11,4
|
2,3#177;0,9
|
28,6#177;20,5
|
3#177;2,9
|
|
225 t.ha-1
|
62#177;24,1
|
40,8#177;15,9
|
2,5#177;0,9
|
45,2#177;4,7
|
7#177;6,8
|
|
10 t.ha-1
|
0 t.ha-1
|
66#177;12,9
|
47,5#177;21,9
|
3#177;0,9
|
44,6#177;5,2
|
5,7#177;7
|
|
45 t.ha-1
|
53#177;27,01
|
35,8 #177;10,9
|
3,2#177;0,5
|
39,9 #177; 2,2
|
12,3 #177; 7,3
|
|
225 t.ha-1
|
59#177;15,3
|
43,3#177;13,1
|
3,4#177;0,2
|
49,6 #177;6,3
|
13,3#177;6,2
|
|
20 t.ha-1
|
0 t.ha-1
|
75#177;7,9
|
62,5 #177; 13,4
|
3,1#177;0,7
|
42,03 #177;1,3
|
25,3 #177;32,2
|
|
45 t.ha-1
|
54#177;3,2
|
41,6#177;5,7
|
3#177;0,6
|
44,9#177;6,9
|
11,5#177;11,6
|
|
225 t.ha-1
|
80#177;15,9
|
71,2#177;14,8
|
5,4#177;1,6
|
46,03#177;4,5
|
78,5#177;67,3
|
|
Résultats au cours de la deuxième
campagne
|
|
0
|
0 t.ha-1
|
2,5#177;5
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
|
45 t.ha-1
|
24,2#177;33,3
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
|
225 t.ha-1
|
17,5#177;17,1
|
5#177;6,4
|
0,0#177;0,0
|
0,0#177;0,0
|
0,0#177;0,0
|
|
10 t.ha-1
|
0 t.ha-1
|
32,5#177;37,8
|
24,1#177;38,04
|
7,9#177;15,8
|
16,7#177;15,2
|
1#177;2
|
|
45 t.ha-1
|
0,0#177;0,0
|
0,83 #177;1,7
|
0,0#177;0,0
|
0,5 #177;1
|
0,0 #177; 0,0
|
|
225 t.ha-1
|
12,5#177;17,3
|
0,83 #177;1,7
|
0,0#177;0,0
|
0,0 #177;0,0
|
0,0#177;0,0
|
|
20 t.ha-1
|
0 t.ha-1
|
10,5#177;9,7
|
19,2 #177; 25,3
|
1,2#177;2,5
|
8,4 #177;16,7
|
0,8 #177;1,5
|
|
45 t.ha-1
|
5,6#177;3,5
|
20#177;25,5
|
3,3#177;2,4
|
16,5#177;19,2
|
1,2#177;2,5
|
|
225 t.ha-1
|
14,5#177;9,5
|
57,5#177;30,9
|
16,9#177;19,9
|
22,5#177;15,6
|
0,0#177;0,0
|
|
Moyenne doses calcaires
|
|
0 t.ha-1
|
29,3#177;27a
|
9,6#177;16,7b
|
0,7#177;1,3b
|
12,2#177;19,9b
|
2,4#177;6,1b
|
|
10 t.ha-1
|
37,2#177;31,5a
|
25,3#177;25,7ab
|
2,9#177;6,3ab
|
24,5#177;22,1ab
|
8,3 #177;10,9ab
|
|
20 t.ha-1
|
39,9#177;32,6a
|
45,3#177;27,9a
|
5,4#177;9a
|
30 #177;18,8a
|
24,8 #177;49,6a
|
|
Moyenne doses matières organiques
|
|
0 t.ha-1
|
35,1#177;32,2a
|
25,5#177;30,2ab
|
2,5#177;6,4ab
|
17,9#177;20,6b
|
7,4#177;18,6ab
|
|
45 t.ha-1
|
30,5#177;27,8a
|
18,3#177;19,7b
|
1,9#177;1,8b
|
21,7#177;20,8ab
|
5,6 #177;8,8b
|
|
225 t.ha-1
|
40,9#177;31,3a
|
36,5#177;30,1a
|
4,6#177;9,2a
|
27,2 #177;22,5a
|
22,6#177;47,9a
|
|
Moyenne Campagne
|
Page | 27
|
Campagne 1
|
57,7#177;21,8a
|
39,4#177;24,3a
|
2,8#177;1,5a
|
37,8#177;16,31a
|
23,4#177;40,4a
|
|
Campagne 2
|
13,3#177;19,7b
|
14,1#177;25,4b
|
3,2#177;9,2a
|
6,7#177;12,8b
|
0,3#177;1,1b
|
|
Moyenne
|
|
P doses calcaires
|
0,1226
|
0,0000
|
0,0336
|
0,0000
|
0,0024
|
|
P doses matières organiques
|
0,1534
|
0,0023
|
0,2658
|
0,0066
|
0,0176
|
|
P Campagne
|
0,0000
|
0,0000
|
0,7875
|
0,0000
|
0,0000
|
|
P interaction Camp*calcaire
|
0,0220
|
0,2082
|
0,3498
|
0,0192
|
0,0032
|
|
P interaction Campagne*MO
|
0,4496
|
0,6271
|
0.5713
|
0,0108
|
0,0140
|
|
P interaction C*M
|
0,0078
|
0,0096
|
0,0507
|
0,0003
|
0,0074
|
|
P interaction Camp*Calc*MO
|
0,6105
|
0,1107
|
0,1494
|
0,0005
|
0,0393
|
3.1 Influence des amendements calcaire et organique
sur la reprise au cours de deux campagnes
L'effet combiné du calcaire et de la matière
organique sur la reprise de Microchloa altéra est
consigné dans le tableau 2. Cependant, les résultats de l'analyse
de variance révèlent que les amendements appliquées en
2014 ont induit des différences hautement significative
(P=0,0078), du même tableau, il apparait que le
taux de reprise obtenu en première année a été
supérieur par rapport à celui obtenu au cours de la
deuxième campagne, ceci implique que, la reprise des plantes a
été influencé significativement en première
année valeur de probabilité
(0,0000).
3.2 Influence des amendements calcaire et organique
sur la survie au 90ème jour au cours de deux
campagnes
L'analyse de la variance effectuée sur la survie
à 90 jours à la de fin d'expérimentation
révèle une différence très significative
(p= 0,0000 et p=0,0023) entre les traitements
(respectivement calcaire et matière) et la campagne
(p=0,0000). Il en est de même pour leur
interaction (Matière organique * Calcaire) (p=0,0096)
sauf au niveau des interactions entre campagne, matière
organique et calcaire (p >0,05). Cependant, la
survie a été meilleure à la première campagne
(39,4%) qu'à la deuxième (14,1 %) soit une diminution de 54,21%
par rapport la première survie.
Page | 28
3.3 Influence des amendements calcaire et organique
sur le paramètre diamètre au collet au cours deux
campagnes
L'analyse de la variance effectuée à la fin
l'expérimentation montre qu'il n'existe pas des différences
très hautement significatives (p>0,05)
entre les traitements considérés vis-à-vis de leurs
effets sur le diamètre au collet quel que soit la campagne alors que
leurs interactions (matière organique combinée au calcaire) ont
induit une différence significative
(p=0,0507), il en est de même pour l'amendement
calcaire (p=0,0336).
3.4 Influence des amendements calcaire et organique la
longueur de hampe et le nombre de hampe au cours deux campagnes
Quant à la longueur de hampe, le résultat de
l'analyse de la variance effectuée à la fin
l'expérimentation montre qu'il existe des différences très
hautement significatives (p<0,05) entre les
traitements considérés vis-à-vis de leurs effets sur la
longueur de hampe, ceci, quel que soit la campagne. Il en de même pour le
nombre de hampe quel que soit le traitement et campagne mais le nombre et
longueur de hampe a été meilleure à la première
campagne.
Au vue de résultats, la matière organique a agi
comme liant des particules du sol entre eux en agrégats plus
résistants à l'érosion et plus favorables à la
circulation de l'air, à la rétention de l'eau
Page | 29
Chapitre 4. Discussion des résultats
La tendance générale des résultats montre
que les différents paramètres observés sont meilleurs en
première année qu'en deuxième année, sauf pour le
diamètre au collet où une différence significative n'a pas
été observée quant à la campagne. Les
résultats obtenus en première année sont expliqués
par le fait que les amendements organiques et calcaires auraient
amélioré le statut nutritionnel et la CEC grâce à
son pouvoir chelatant, ce qui expliquerait leurs effets hautement significatifs
sur la production des épis et hampes floraux
(P<0,05). Cependant, plusieurs auteurs notamment
(Crecchio et al. 2004 ; Baize, 2000 ; Comifer et al, 2000 et Shutcha,
2010) ont montré que l'application des amendements (organique et
calcaire) améliore les conditions du sol (aération, CEC,
porosité), favorisant ainsi une meilleure croissance des plantes et une
absorption efficace des éléments nutritifs. Ces auteurs
démontrent aussi que ces amendements basiques (calcaire dolomitique)
étant des produits de différentes origines sont capables
d'augmenter le pH d'un sol et d'en améliorer la structure. Ces produits
contiennent généralement du calcium (Ca) et/ou du
magnésium (Mg) en plus des bases (O 2-, OH -, CO 32- suivant le produit
utilisé) qui ont neutralisés l'acidité de ce substrat
favorisant ainsi la survie de M. altéra en élevant son
pH.
En comparant les résultats obtenus par rapport aux
témoins, quel que soit l'amendement, nous constatons une
amélioration progressive des résultats. L'apport des amendements
accru considérablement la reprise, survie, la longueur de hampe ainsi
que le nombre de hampe. Ces effets favorables des amendements sur la production
de M. altéra sur ce substrat pollué sont
expliqués par le fait que la décomposition de la matière
organique et l'augmentation des rendements étaient étroitement
liés à la synchronisation entre la libération des
nutriments et leur assimilation par la plante tels que approuvés par
Cobo et al. (2002) et Palm (1995). On doit rappeler que les
différents traitements n'éliminent pas les ETM, mais qu'ils
réduisent la mobilité en favorisant les réactions de
fixation sur les surfaces échange, de précipitation, en
augmentant le nombre de surface réactionnelle. Des résultats
similaires ont été obtenus par Shutcha et al. (2010)
dans la région de Lubumbashi ont montré que les apports de chaux
et du compost ont permis de réduire la biodisponibilité des
ETM.
Page | 30
et au drainage du sol (Charland et al. 2001) pour
cela M. altéra aurait trouvé des conditions
idéale grâce à ses amendements ce qui lui aurait permis
également de survivre. Par ailleurs, comme démontre les
études faites par Shutcha (2010), la matière organique aurait
bloqué les ETM les rendant ainsi immobiles dans les rejets
minéralisés de Kolwezi. Selon cet auteur, à un pH
supérieur à 5, les éléments nutritifs ne se
combinent pas aux métaux tels que le fer, l'aluminium et
Manganèse pour former des complexes humiques qui seraient de
précipités. Par conséquent, ces polyéléments
sont disponibles dans la solution du sol et indispensables pour la plante
(Soltner, 1986).
Cependant, comparativement aux résultats obtenus
à la première campagne, la diminution constatée au cours
de la deuxième campagne serait expliqué probablement par le fait
que la matière organique utilisée était riche en azote,
qui d'ailleurs se libère rapidement et peut être perdu par
lessivage. Les amendements utilisés ont amélioré tout de
même les conditions du sol ce qui explique les résultats
observés en seconde campagne. Communément, les matières
organiques fraiches ou même tout le sol, en tant que substrat, sont
caractérisés par leur rapport C/N. ce rapport donne une
idée sur la nature des matières organiques et leur degré
de décomposition (Giroux et al., 2007). Cependant, le succès de
cette stratégie dépendra de la qualité du matériel
organique utilisé et de la quantité d'éléments
nutritifs contenus dans ce matériel. Par ailleurs, l'efficacité
fertilisante des amendements organiques sont associées à la
composition des engrais et à leur période d'épandage.
Page | 31
Conclusion
Ce travail évalue les effets résiduels des
amendements organiques et du calcaire utilisés en 2014 sur les rejets
métallurgiques de l'usine à cuivre de Kolwezi (UCK), afin de
réduire la dispersion des éléments traces dans
l'environnement à travers l'érosion hydrique ou
éolienne.
Pour y parvenir, un essai a été installé
suivant un dispositif en tiroir (SPLIT PLOT) composant 2 campagnes, 3 doses
d'amendement calcaire (0 t.ha-1, 10 t.ha-1 et 20
t.ha-1) et 3 d'amendement organique (0 t.ha-1, 45
t.ha-1 et 225 t.ha-1) répétées six
fois.
Cependant, la tangence générale des
résultats obtenus montrent qu'une diminution sur tous les
paramètres observés au cours de la deuxième campagne. Par
ailleurs, bien qu'une diminution des résultats soit d'observée,
l'apport de 20 t.ha-1 des calcaires et 225t.ha-1 de la
matière organique qui a donné les meilleurs résultats quel
que soit la campagne peuvent être recommandable. Les résultats
obtenus en première année sont expliqués par le fait les
amendements organiques et calcaire auraient amélioré le statut
nutritionnel, ce qui expliquerait leurs effets hautement significatifs sur la
production des épis et hampes florales.
Au regard de ces résultats, nous disons que le
succès de la phytostabilisation dépendra de la qualité du
matériel organique et/ou calcaire utilisé et de la
quantité d'éléments nutritifs contenus dans ce
matériel.
Au terme nous pensons dire que les apports des amendements
organiques et du calcaire soient apporté après chaque deux an de
par leurs caractéristiques.
Page | 32
Références bibliographiques
Ademe-Agence de l'Environnement et de la Maitrise de l'Energie
http://www2.ademe.fr/servlet/KBaseShow?sort=-1&cid=96&m=3&catid=10157
Alloway B.J., 1995. Heavy Metals in Soils. Edition2:
Blackie Academic & Professional, 368p. Alloway B. J., 1997. The
mobilization of trace elements in soils. Contaminated soils. INRA.
Paris (France): 133-145 p.
Anonyme, 2009. Technical/Regulatory Guidance,
Phytotechnology Technical and Regulatory Guidance and Decision Trees,
Revised. [Dossier en ligne] in
www.itrcweb.org/Documents/PHYTO-3.
Baize D., 1997. Teneurs totales en éléments
traces métalliques dans les sols (France). INRA Editions, Paris.
408 p.
Baize D., 2000. Teneurs totales en « métaux lourds
» dans les sols français. Résultats généraux
du programme Aspitet. Le Courrier de l'environnement de l'INRA,
39 :39-54.
Baker A.J.M., Walker P.L. 1990. Ecophysiology of metal uptake
by tolerant plant », in: SHAW J. A., Heavy Metal Tolerance in Plants:
Evolutionary Aspects, Florida, CRC Press, 155-177 pp.
Bert V., Deram A., 1999. Guide des phytotechnologies :
utilisation des plantes dans la dépollution et la réhabilitation
des sites contaminés par les métaux lourds, France,
Environnement et développement alternatif.
Bert V., et Deram A., 1999. Guide des phytotechnologies des
plantes dans la décontamination et la réhabilitation des sites
contaminés par les métaux lors. EDA Environnement et
Développement Alternatif Lille. Biotechnol. Agron. Soc.
Environ.
Berti W & Cunningham S. D., 2000. Phytostabilization of
metals. In Raskin I & Ensley BD. Phytoremediation of toxic metals:
using plants to clean up the environment, John Wiley & Sons, Canada.
71-88 p.
Bliefert C., Perraud R., 2001. Chimie de l'environnement :
air, eau, sols, déchets, Paris, De Boeck Université.
Cao X., Ma L.Q., 2004. Effects of compost and phosphate on
plant arsenic accumulation from soils near pressure-treated wood. Environ
Pollut 132:435-442.
Page | 33
Charland M., Cantin S., St Pierre M. A &
Côté, L., 2001. Recherche sur les avantages à utiliser le
compost. Dossier CRIQ 640-PE27158 (R1), Rapport final. Recyc-Québec, 35
p.
Cobo J.G., Barrios E., Kaas D.C.L & Thomas R.J., 2002.
Nitrogen mineralization and crop uptake from surface-applied leaves of green
manure species on a tropical volcanic-ash soil. Biology and fertility of
soils, 36: 87- 92.
Colinet G., (2003). Eléments traces
métalliques dans les sols. Contribution à la connaissance des
déterminants de leur distribution spatiale en région limoneuse
belge. Thèse de doctorat FUSA Gx, 412p.
Comifer, groupe chaulage, 2000. Du laboratoire au champ,
questions vives sur le chaulage. Mars 2000. 9p
Crecchio, C., Curci, M., Pizzigallo, M.D.R., Ricciuti, P.
& Ruggiero, P. 2004. Effects of municipal solid waste compost amendments on
soil enzyme activities and bacterial genetic diversity. Soil Biol.
Biochem, 36: 1595-1605.
Cunningham, S.D., Shann, J.R., Crowley, D.E., & Anderson,
T.A., (1997). Phytoremediation of contaminated water and soil. In E. L. Kruger,
T. A. Anderson, & J. R. Coats (Eds.), Phytoremediation of soil and
water contaminants. Washington, DC: American Chemical Society.ACS
Symposium séries 664: 2-19.
Dechamp C & Meerts P., 2003.La phytoremédiation :
Panacée pour l'environnement ou menace pour la biodiversité ?,
Les Naturalistes belges, 82 :135-148 pp.
Farfel M.R., Orlova A.O, Chaney RL, Lees PSJ, Rohde C &
Ashley P.J., 2005. Biosolids compost amendment for reducing soil lead hazards:
a pilot study of Orgro amendment and grass seeding in urban yards. Sci
Total Environ 340:81-95.
Fertial (les fertilisants d'Algérie), 2010. Manuel :
Utilisation des engrais. Algérie, IFC, 100 ps.
Fwamba F, Muteba JP, Muhiya H et Mpararo E, (2011). Le
rôle de Glencore dans le Partenariat Kamoto Copper Company S.A.R.L (KCC),
Rapport d'enquête Editions (NDS, RND, LICOCO) Kinshasa RDC.
Giroux M., N'Dayegamiye A & Royer R., 2007. Effet des
apports d'automne et printemps de fumiers et des boues mixtes de
papetières sur le rendement, la qualité de la pomme terre et
efficacité de l'azote.
Agrosolutions18(1):25-34.
Page | 34
Guo XM, D.K.Niu, YQ Liu, TZ Du, SZ Xiao & XH Ye., 2004.
Vegetation restoration of different types of barren ecosystems in Jiangxi
province. Pages 293-301 in S. P. M .Y.M. Luo, J. Japenga, F.J. Zhao,
T. Edelman, B. Marschner, L. Newman and T. Vanek, editor. 2nd
International Conference on Soil Pollution and Remediation, Nanjing, China.
Hopkins G. W., 2003. Physiologie végétale,
Bruxelles, De Boeck.
Ineris, 2010. Sites pollues : étude de
l'efficacité des techniques de phytoremédiation-Le projet
PHYTOSTAB » [dossier en ligne] in INERIS [site web]
Kabata-Pendias A. & Pendias H., 2001. Trace elements in
soils and plants, Boca Raton, CRC Press Inc. 3ème Ed.
Kiikliä O., 2002. Remediation through mulching with
organic matter of soil polluted by a copper-nickel smelter. Academic
dissertation in environmental Protection Science, Faculty of agriculture and
Forestery, University of Helsinki. Finnish. Forest Research Institute, Research
papers 831, Vantaa research center, 57 p.
Kumpiene J., Lagerkvist A. & Maurice C., 2008.
Stabilisation of As, Cr, Cu, Pb, and Zn in soil using amendments- A review,
waste management, 28: 215-225 p
Madejo'n E., De Mora A.P., Felipe E., Burgos P. & Cabrera
F., 2006. Soil amendments reduce trace element solubility in a contaminated
soil and allow regrowth of natural vegetation. Environ. Pollut. 139,
40- 52 p.
Mench M, J Vangronsveld, N Lepp, P Bleeker, A Ruttens & W
Geebelen, 2005. Phytostabilisation of métal-contaminated sites. Pages
109-190 in T. N. Springer, ed. Phytoremediation of metal -
contaminated soils. Echevarria G., Morel J. L., Goncharova N. (Eds),
Trest, Czech Republic. Mench M., Vangronsveld J., Lepp N., Bleeker P., Ruttens
A. & Geebelen W. & Morel J. L. 2006. Phytostabilisation of
metal-contaminated sites. Phytoremediation of Metal-Contaminated Soils,
109-190 p. Springer, Netherlands
Migeon A., 2009. Etude de la variabilité naturelle
dans la réponse du peuplier aux métaux: bases physiologiques et
exploitation en phytoremédiation. Thèse, Faculté des
Sciences et Techniques, D.F.D. Biologie Forestière, Université
Henri Poincaré (Nancy-Université) (Ed. INRA) Paris. Palm C.A.,
1995.Contribution of agroforestry trees to nutriment requirements of
intercropped plants. Agroforestry Systems, 30:
105-124.
Page | 35
Pilon-Smits E., 2005. Phytoremediation. Annual Review of
Plant Biology 56:15-39.
Sauvé S, Hendershot W, Allen HE., 2000. Solid-solution
partitioning of metals in contaminated soils: dependence on pH, total metal
burden, and organic matter. Environ Sci Technnol
34:1125- 1131.
Shutcha M., 2007. Phytostabilisation des sols
contaminés par l'activité minière au Katanga: Mise au
point de la culture de Rendlia altera (Rendle) Chiov.
Mémoire de DEA, Faculté des Sciences
Agronomiques/Université de Lubumbashi. Inédit.
Shutcha M., 2010. Phytostabilisation des sols
contaminés en métaux lourds par l'activité minière
au Katanga « Cas du quartier Gécamines/Penga Penga
contaminés en métaux par les émissions de la fonderie de
cuivre de l'Usine Gécamines/Lubumbashi ».Thèse,
Faculté des Sciences Agronomiques département de Gestion des
Ressources Naturelles, Université de Lubumbashi. Inédit.
Soltner D. 2003. Les Bases De La Production
Végétale, Tome I Le Sol Et Son Amélioration,
23ième Edition, Sciences Et Techniques Agricoles, Sainte-Gemmes-Sur
Loire.
Tremel-Schaub A. et, Feix I., 2005. Contamination des
sols. Transfert des sols vers les plantes. ADEME et EDP Sciences (Eds).
Tshibanda K., 2012. Contribution à la recherche
d'un modèle de gestion d'un passif environnemental issu d'un traitement
métallurgique des minerais sulfurés cuivre - zinc en
République Démocratique du Congo. Thèse,
Université libre de bruxelles, Faculté des sciences gestion de
l'environnement. Inedit. 275pg.
Useni S.Y., 2009. Transfert des éléments
métalliques (ETM) dans le sol-plante et évolution des
risqué de contamination de la chaine alimentaire. Etude des cas dans la
ville de Lubumbashi en RDC. Mémoire, UNILU, inédit.
Verkleij J. A. C & Schat H., 1990. Mechanisms of Metal
Tolerance in Higher Plants. In: SHAW J. A., Heavy Metal Tolerance
in Plants: Evolutionary Aspects, Florida, CRC Press, pp. 179-193. Zhou L.
X. & Wong J. W. C., 2001. Effect of dissolved organic matter from sludge
and sludge compost on copper sorption. J. Environ. Qual.
30: 878-883.
Page | 36
Annexe
Données brutes
|
capagne
|
Calcaire
|
M.O
|
T Srv 30 jrs
|
T Srv 90 jrs
|
Nb Hmp 90 jrs
|
Dmt Coilet 120 jrs
|
Lgr Hmp 120 jrs
|
|
campagne 1
|
C0
|
M0
|
8
|
0
|
0
|
0
|
0
|
|
campagne 1
|
C0
|
M0
|
53,3
|
0
|
0
|
0
|
0
|
|
campagne 1
|
C0
|
M0
|
26,6
|
0
|
0
|
0
|
0
|
|
campagne 1
|
C0
|
M0
|
10
|
0
|
0
|
0
|
0
|
|
campagne 1
|
C0
|
M1
|
50
|
26,6
|
2
|
3
|
27,5
|
|
campagne 1
|
C0
|
M1
|
36,6
|
6,6
|
4
|
3
|
42,75
|
|
campagne 1
|
C0
|
M1
|
33,3
|
0
|
0
|
0
|
0
|
|
campagne 1
|
C0
|
M1
|
63,3
|
13,3
|
7
|
3
|
44
|
|
campagne 1
|
C0
|
M2
|
80
|
60
|
24
|
2,6
|
49,8
|
|
campagne 1
|
C0
|
M2
|
83,3
|
46,6
|
0
|
1
|
48,28571
|
|
campagne 1
|
C0
|
M2
|
50
|
33,3
|
19
|
3,2
|
39,85714
|
|
campagne 1
|
C0
|
M2
|
33,3
|
23,3
|
3
|
3
|
42,75
|
|
campagne 1
|
C1
|
M0
|
83,3
|
76,6
|
26
|
3,9
|
37,3
|
|
campagne 1
|
C1
|
M0
|
60
|
46,6
|
15
|
3,7
|
44,8
|
|
campagne 1
|
C1
|
M0
|
66,6
|
43,3
|
4
|
2,4
|
48,5
|
|
campagne 1
|
C1
|
M0
|
53,3
|
23,3
|
1
|
2
|
48
|
|
campagne 1
|
C1
|
M1
|
36,3
|
30
|
17
|
3,7
|
40,77
|
|
campagne 1
|
C1
|
M1
|
30
|
23,3
|
6
|
3,5
|
39
|
|
campagne 1
|
C1
|
M1
|
56,5
|
43,3
|
18
|
2,5
|
42,33333
|
|
campagne 1
|
C1
|
M1
|
90
|
46,6
|
26
|
3
|
37,3
|
|
campagne 1
|
C1
|
M2
|
43,3
|
30
|
13
|
3,5
|
46,2
|
|
campagne 1
|
C1
|
M2
|
56,6
|
36,6
|
13
|
3,7
|
56,66666
|
|
campagne 1
|
C1
|
M2
|
80
|
60
|
38
|
3,2
|
42,71428
|
|
campagne 1
|
C1
|
M2
|
56,6
|
46,6
|
20
|
3,3
|
52,85714
|
|
campagne 1
|
|
M0
|
76,6
|
70
|
23
|
2,6
|
43,6
|
|
campagne 1
|
|
M0
|
80
|
76,6
|
7
|
2,6
|
42
|
|
campagne 1
|
|
M0
|
63,3
|
46,6
|
7
|
4
|
40,33333
|
|
campagne 1
|
|
M0
|
80
|
56,6
|
88
|
3,2
|
42,22222
|
|
campagne 1
|
|
M1
|
50
|
36,6
|
12
|
3,7
|
45,5
|
|
campagne 1
|
|
M1
|
56,6
|
36,6
|
4
|
3,2
|
54
|
|
campagne 1
|
|
M1
|
53,3
|
46,6
|
4
|
2,5
|
43
|
|
campagne 1
|
|
M1
|
56,6
|
46,6
|
31
|
2,6
|
37,3
|
|
campagne 1
|
|
M2
|
83,3
|
76,6
|
38
|
6,9
|
40,625
|
|
campagne 1
|
|
M2
|
90
|
83,3
|
125
|
6,7
|
49,1
|
|
campagne 1
|
|
M2
|
90
|
76,6
|
208
|
4,5
|
49,2
|
|
campagne 1
|
|
M2
|
56,6
|
50
|
42
|
3,6
|
45,22222
|
Page | 37
|
campagne 2
|
C0
|
M0
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M0
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M0
|
10
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M0
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M1
|
13,33
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M1
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M1
|
73,33
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M1
|
10
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M2
|
0
|
13,3333333
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M2
|
20
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M2
|
40
|
6,66666667
|
0
|
0
|
0
|
|
campagne 2
|
C0
|
M2
|
10
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M0
|
86,67
|
80
|
4
|
31,65
|
20
|
|
campagne 2
|
C1
|
M0
|
16,67
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M0
|
0
|
16,6666667
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M0
|
26,67
|
0
|
0
|
0
|
30,5
|
|
campagne 2
|
C1
|
M1
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M1
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M1
|
0
|
0
|
0
|
0
|
2
|
|
campagne 2
|
C1
|
M1
|
0
|
3,33333333
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M2
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M2
|
13,33
|
3,33333333
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M2
|
36,67
|
0
|
0
|
0
|
0
|
|
campagne 2
|
C1
|
M2
|
0
|
0
|
0
|
0
|
0
|
|
campagne 2
|
|
M0
|
13
|
23,3333333
|
0
|
0
|
0
|
|
campagne 2
|
|
M0
|
23
|
53,3333333
|
3
|
4,9
|
33,5
|
|
campagne 2
|
|
M0
|
2
|
0
|
0
|
0
|
0
|
|
campagne 2
|
|
M0
|
4
|
0
|
0
|
0
|
0
|
|
campagne 2
|
|
M1
|
11
|
53,3333333
|
5
|
3,25
|
36
|
|
campagne 2
|
|
M1
|
3
|
0
|
0
|
4,25
|
30
|
|
campagne 2
|
|
M1
|
5
|
26,6666667
|
0
|
5,7
|
0
|
|
campagne 2
|
|
M1
|
4
|
0
|
0
|
0
|
0
|
|
campagne 2
|
|
M2
|
24
|
83,3333333
|
0
|
46,3
|
36
|
|
campagne 2
|
|
M2
|
4
|
13,3333333
|
0
|
3
|
0
|
|
campagne 2
|
|
M2
|
9
|
73,3333333
|
0
|
9
|
26,5
|
|
campagne 2
|
|
M2
|
21
|
60
|
0
|
9,2
|
27,5
|
|
|



