II-MATÉRIEL ET MÉTHODES
II- Matériel et Méthodes
1. Cadre de L'enquête.
En ce qui concerne l'enquête auprès des
phytothérapeutes, trois grandes villes du Togo ainsi que deux
préfectures ont été prises en compte.
· La ville de Lomé, Elle se situe à
l'extrême sud-ouest du Togo, et s'étend le long du littoral du
Golfe de Guinée. C'est la capitale du Togo officiellement,
l'agglomération compte 1.325 416 habitants.
· La ville de Kpalimé, Situé au coeur du pays
éwé, Kpalimé est à 120 km au nord ouest de la
capitale Lomé avec 101 088 habitants. Elle est la quatrième ville
du Togo.
· La ville de Sokodé, Elle compte plus de 123 029
habitants la deuxième ville du Togo Elle est située à 338
km au nord de Lomé (encyclopédie wikipedia, 2008)
· Les préfectures de Tchaoudjo et de Tchamba qui
compte respectivement 318.750 habitants et 216.500 habitants.

Légende
Zones enquêtées
Préfecture de Tchaoudjo
Préfecture de Tchamba Lomé
Sokodé
Kpalimé Tchamba
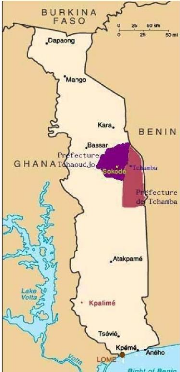
Figure 3: Carte du Togo montrant les zones de
l'enquête ethnopharmacologique.
En ce qui concerne le suivi des paramètres biologiques et
biochimiques.
Les analyses biomédicales se sont déroulées
dans les laboratoires de sérologie et de biochimie de l'institut
national d'hygiène à Lomé et au centre hospitalier
préfectoral de Kpalimé.
Les personnes impliquées dans l'étude sont des
patients du centre CPHYSAM (Centre de Phytothérapie Sensibilisation et
Assistance aux Malades). Ce centre de phytothérapie est situé
dans le quartier Tokoin wuiti à Lomé.
2. Type et Période de l'étude
En ce qui concerne les enquêtes auprès des
phytothérapeutes, c'est une étude prospective qui s'est
déroulée du 26 Août 2007 au 20 Avril 2008.
En ce qui concerne le suivi des patients sous
phytothérapie, il s'agit d'une étude qui s'est
déroulée sur une période de novembre 2007
en mai 2008. Cette étude à deux objectifs.
- Contrôler l'évolution mensuelle des
paramètres biochimiques liés à l'apparition ou à la
persistance d'un problème hépatocellulaire;
- Contrôler la clairance rénale des
phytomédicaments ingérés par les patients.
3. Déroulement de l'enquête
Les fiches d'enquêtes conçues (Annexe I) ont
été distribuées grâce aux associations et aux
regroupements de phytothérapeutes. Ces associations régionales
ont transmises les listes des phytothérapeutes spécialistes dans
le traitement de l'hépatite virale. Les fiches ont été
transmises à ses spécialistes et remplies après des
entretiens avec ces derniers.
3.1. Méthode
Une enquête auprès des phytothérapeutes a
été initiée dans le but de collecter des données
concernant leur méthodologie dans le diagnostic, et dans le suivi de
leurs patients au cours de leur traitement. Il s'avère essentiel
d'aborder et d'éclaircir divers points notamment ceux touchant à
l'innocuité, à la qualité, aux coûts des traitements
et à la connaissance de l'hépatite virale. Ces fiches contiennent
une trentaine de questions.
4. Suivi des paramètres biologiques et
biochimiques
Les personnes recrutées pour cette étude sont des
patients du Centre de Phytothérapie Sensibilisation et Assistance aux
Malades (CPHYSAM).
4.1 Critères d'inclusion
- Patients âgés de 18 à 60 ans;
- Sérologie de l'antigène HBs positive sur plus de
6 mois;
- Patients ayant dans leur sérum un taux d'alanine amino
transférase ou d'Aspartate amino transférase compris entre 41 et
200 UI/L;
- Patients ne souffrant pas d'une complication cardio-vasculaire
ou rénale;
- Patients n'ayant pas été atteints de troubles
mentaux;
- Personne n'étant pas présentement impliqué
dans un traitement à l'alpha interféron ou à tout autre
antiviral dirigé contre le virus de l'hépatite B;
- Personne n'ayant pas été victime d'une
encéphalopathie hépatique;
- Personne n'ayant pas fait usage d'aucune substance
immunosuppresseur;
- Personne n'ayant pas été infecté par l'un
des virus du SIDA;
- Personne ayant librement consenti à suivre le traitement
par les phytomédicaments.
4.2. Critères d'exclusion
- Patients âgés de moins de 18 ans et de plus de 60
ans, femme enceinte ou en cours d'allaitement; - Sérologie de
l'antigène HBs négative;
- Patients ayant dans leur sérum un taux d'Alanine amino
transférase ou d'Aspartate amino transférase inférieur 41
ou supérieur 200 UI/L;
- Personne souffrant d'une complication cardio-vasculaire ou
rénale;
- Personne ayant des troubles mentaux;
- Personne étant impliqué actuellement dans un
traitement à l'alpha interféron ou tout autre antiviral
dirigé contre le virus de l'hépatite B;
- Personne souffrant d'une encéphalopathie
hépatique;
- Personne ayant utilisé dans le passé une
substance immunosuppresseur;
- Personne infectée par l'un des virus du SIDA (VIH1,
VIH2);
- Personne n'ayant pas librement consenti à suivre le
traitement par les phytomédicaments.
4.3. Dosage des paramètres biologiques et
biochimiques
Après l'exploration biologique sur 13 patients, 4 patients
et un témoin ont été retenus pour l'étude.
4.3.1. Prélèvement sanguin
Le sang veineux a été prélevé chez
tous les patients dans un tube sec et propre. Les patients étant
à jeun. Les prélèvements sanguins ont été
centrifugés dans des tubes secs à 3000 tours par minute pendant
10 minutes et les sérums ont été recueillis pour les
dosages.
4.3.2. Le Test sérologique de l'antigène
HBs
L'antigène HBs est révélé par la
technique ELISA. Le kit MONOLISA HBs Ag ULTRA de Bio-Rad
repose sur l'utilisation d'un support solide (puits, microparticules) recouvert
par des anticorps monoclonaux et des anticorps polyclonaux
sélectionnés pour leur capacité à se lier aux
différents sous types de l'antigène HBs. Ce matériel est
associé à un incubateur, un laveur et un
spectrophotomètre.
4.3.3. Suivi des paramètres
biochimiques
Le dosage des paramètres biochimiques a été
réalisé chaque 30 jours pendant 4 mois chez tous les patients.
4.3.3.1. Dosage des transaminases ASAT et
ALAT
Principe
Les dosages sont basés sur la mesure cinétique des
transaminases sériques dans un système réactionnel dont la
finalité est l'oxydation du coenzyme NADH,H.+
L'aspartate aminotransférase (ASAT) catalyse la
transformation de l'aspartate en oxaloacétate. L'oxaloacétate
formé est réduit en malate en présence d'une
quantité connue de coenzyme NADH'H+ et du malate
déshydrogénase (MDH). La cinétique de cette
dernière réaction est déterminée par les mesures
successives de l'absorbance du coenzyme NADH'H+ à 340 nm. De cette
cinétique est déduite la concentration de l'aspartate
aminotransférase (ASAT).
ASAT

Aspartate + á-cétoglutarate Oxaloacétate +
Glutamate
MDH
Oxaloacétate + NADH + H+ Malate +
NAD+
La transamination de l'alanine en pyruvate est
réalisée en présence de l'alanine aminotransférase
(ALAT). Le pyruvate obtenu est réduit en lactate en présence du
coenzyme NADH'H+ et du lactate déshydrogénase (LDH).
La cinétique de cette dernière réaction permet de
déterminer la concentration de l'alanine aminotransférase
(ALAT).
ALAT

Alanine + á-cétoglutarate Pyruvate + Glutamate
LDH

Pyruvate + NADH + H+ Laclate + NAD+
Les contenants des deux flacons R1 et R2 du kit
Spinreact Transaminases (Tableau I et Tableau II) ont
été mélangés pour obtenir un réactif final
stable pendant 21 jours entre 2°c et 8°c.
Ce réactif a été introduit dans l'automate
Lisa 500 plus.
La solution de contrôle (sérum de contrôle)
a été ajoutée à l'automate ainsi que 50 ul de
chaque échantillon de sérum à doser. La calibration de
l'automate et le dosage des sérums ont été ensuite
programmés via un microordinateur intégré au
système. Les différentes lectures de l'absorbance de
NADH'H+ ont été réalisées grâce
à un spectrophotomètre intégré à l'automate.
Les résultats du dosage des transaminases sont déduits et
imprimés par l'automate.
Tableau I : Les réactifs du dosage de l'aspartate
aminotransférase (ASAT).
|
Réactif R1 TRISpH7,8 80mmol/l
L-aspartate 200 mmol/l
|
|
Réactif R2 NADH 0,18 mmol/l
Lactate déshydrogénase (LDH) 800 UI/l
Malate déshydrogénase (MD 600 UI/l
á-Cetoglutarate 12 mmol/l
|
TRIS : Trishydroxyméthylaminométhane, NADH
: Nicotinamide Adénine Dinucléotide réduite
Tableau II : Les réactifs du dosage de l'alanine
aminotransférase (ALAT).
|
Réactif R1 TRIS pH 7, 8 100 mmol/l
L-alanine 500 mmol/l
|
|
Réactif R2 NADH 0,18 mmol/l
Lactate déshydrogénase (LDH) 1200 U/l
á-Cetoglutarate 15 mmol/l
|
TRIS : Trishydroxyméthylaminométhane, NADH
: Nicotinamide Adénine Dinucléotide réduite
4.3.3.3. Le Dosage de la créatinine
Principe
La créatinine réagit avec l'acide picrique en
milieu alcalin (NaOH) pour donner un complexe rouge orangée dont la
densité optique est proportionnelle à la quantité de la
créatinine.
La solution de travail a été obtenue par un
mélange à volume égal des réactifs R1 et R2 du kit
Spinreact créatinine (Tableau III). Le mélange est
stable pendant 10 jours à la température du laboratoire (15 et 32
°c).
Ce réactif a été introduit dans l'automate
Lisa 500 plus. La solution de contrôle (sérum de
contrôle) a été ajoutée à l'automate ainsi
que 50 ul de chaque échantillon de sérum à doser.
La calibration de l'automate et le dosage des sérums ont
été ensuite programmés via un microordinateur
intégré au système. La densité optique du complexe
formé au cours de la réaction a
été mesurée par l'automate. Ensuite, la
concentration de la créatinine dans les sérums a
été déduite et imprimée.
Tableau III : Les réactifs du dosage de la
créatinine
Réactif R1: Acide picrique Acide picrique 17,50 mmol/ l
Réactif R2 : Alcaline réagent Hydroxyde de sodium
0,29 mol/l
Créatinine Etalon Créatinine aqueuse 20 mg/l
4.3.3.4. Le dosage des bilirubines (totale et
directe)
Principe
En présence de DMSO (dimethylsulfoxyde), la bilirubine
totale réagit avec l'acide sulfanilique diazoté pour former un
composé coloré.
La bilirubine conjuguée réagit également en
présence de l'acide sulfanilique diazoté mais cette
réaction s'effectue en l'absence de DMSO.
Pour cette réaction le coffret de réactif
Spinreact bilirubine a été utilisé. 1 ml du
réactif R1 et 50 ul du réactif R3 ont été
mélangés pour obtenir le réactif du dosage de la
bilirubine totale (Tableau IV). 100 ul de l'échantillon de sérum
à doser ont été ajoutés à ce volume.
Après 5 minutes à température de 37°C, la lecture de
l'absorbance à 550 nm a été réalisée contre
les blancs échantillons. On en déduit alors la concentration de
la bilirubine totale.
Pour obtenir le réactif de la bilirubine
conjuguée 1ml du réactif R2 et 50 ul du réactif R3 du
coffret Spinreact bilirubine ont été
mélangés dans les racks (Tableau IV). A ce volume 50 ul
d'échantillon de sérum à doser ont été
ajoutés. Après un temps inférieur à 5 minutes
à température de 37°C, la lecture de l'absorbance à
550 nm a été réalisée contre les blancs
échantillons. La concentration de la bilirubine conjuguée a
été alors déduite.
Tableau IV : Réactifs de dosage des
bilirubines
|
Flacon R1 Bilirubine totale Acide sulfanilique 30 mol/l
DMSO 7 mol/l
Acide chlorhydrique 130 mmol/l
|
|
Flacon R2 Bilirubine directe Acide sulfanilique 30 mmol/l
Acide chlorhydrique 130 mmol/l
|
Flacon R3 Nitrite Nitrite de sodium 0,78 mmol/l
DMSO Dimethylsulfoxyde
4.4. Les Phytomédicaments impliqués dans
l'étude.
Les phytomédicaments impliqués dans cette
étude sont deux produits du centre CPHYSAM Tobacoak's et Tob F6.
Tobacoak's est une alcoolature dilué à 1/ 40 de
couleur verdâtre qui est indiqué contre les infections
microbiennes et virales selon le Promoteur. Cent (100) ml trois fois par jours
est la posologie retenue pendant 4 mois pour un adulte.
Tob F6 une infusion de couleur rouge terreuse, un additif
indiqué contre les troubles hépatiques selon le promoteur. Cent
(100) ml trois fois par jour pendant 4 mois constitue la posologie pour un
adulte.
5. Traitement des donnés
La répartition des phytothérapeutes suivant les
différents critères et l'évolution des moyennes des
paramètres biochimiques ont été fait grâce au
logiciel EXCEL 2007 de Microsoft.
| 


