|

UNIVERSITE DE OUAGADOUGOU
Unité de Formation et
de Recherche
Sciences de la
Vie et de la Terre
(UFR-SVT)
LOME - TOGO
Centre de Recherche
en Sciences
Biologiques
Alimentaires et
Nutritionnelles (CRSBAN)
Pôle Régional
d'Excellence en Biotechnologies
de
Ouagadougou (PREBO)
MEMOIRE
Présenté par
TOUDJI-BANDJE Kodjo
Séfako
Maître es Sciences
Biochimiques
TOGO
Pour l'obtention du :
Diplôme d'Etudes Approfondies en
Biotechnologies
Option: Biotechnologie Microbienne et
Cellulaire
ÉCOLE DOCTORALE RÉGIONALE DU
RA-BIOTECH
Sur le Thème :
APPROCHES MÉTHODOLOGIQUES DES PHYTOTHÉRAPEUTES DU
TOGO
DANS LE TRAITEMENT DE L'HÉPATITE VIRALE :
CAS D'HÉPATITE B CHRONIQUE ACTIVE SOUMIS À UN
TRAITEMENT À
BASE DE PHYTOMÉDICAMENTS.
Soutenu le 25 Février 2009 devant le Jury
:
Président: Pr Alfred S. TRAORE
Membres: Pr Yves TRAORE
Pr Nicolas BARRO
Préface du Président du
RA-BIOTECH.
L'école Doctorale régionale de Ouagadougou
offre une formation doctorale de biotechnologie dans ses options :
Biotechnologie microbienne et cellulaire, Biotechnologie Animale et
Biotechnologie végétale.
Elle regroupe la plus part des Universités de
l'Afrique francophone sub-saharienne en un réseau : le Réseau
Ouest Africain de Biotechnologie (RA-BIOTECH) fruit de la coopération
inter-universitaire et dont le siège est au CRSBAN, à
l'Université de Ouagadougou.
Les Universités et structures de formation des pays
ci-dessous constituent les membres fondateurs de ce réseau :
Bénin, Burkina Faso, Côte d'Ivoire, Guinée-Conakry, Mali,
Niger, Togo et d'autres partenaires comme le Centre International de Recherche
Développement sur l'Elevage en zone Sub-humide (CIRDES)- Bobo Dioulasso
; EISMV-Sénégal.
Ce réseau sous régional
bénéficie de l'appui de plusieurs partenaires de l'enseignement
supérieur (Association des Universités Africaines -AUA, UNESCO,
Banque Mondiale, CAMES, Agence Universitaire de la Francophonie -AUF, Agence
Africaine de Biotechnologie -AAB, etc.
L'école Doctorale que le réseau anime assure
une formation de haut niveau à travers une recherche utilitaire sur
plusieurs thématiques touchant la vie quotidienne des populations
africaines. Cette école a permis au CRSBAN d'être
érigé en pôle régional d'excellence en
Biotechnologie d'une part par l'AUA et d'autre part par l'AUF. Elle accueille
des étudiants de plus de 14 pays d'Afrique centrale de l'Ouest.
Le réseau bénéficie aussi du soutien
de certains spécialistes des biotechnologies des universités du
Nord : Université de la méditerranée (France),
Université Louis Pasteur de Strasbourg (France), Centre de
Génétique Moléculaire de Gif-sur-Yvette-CNRS (Paris
France), Université de liège (Belgique) ; Faculté
Universitaire de Gembloux (Belgique), Université de Rome,
Université Agronomique de Wagenningen .
L'importance des biotechnologies dans la résolution
des problèmes de développement socioéconomiques des pays
de l'Afrique sub-saharienne (Alimentation, Santé Environnement, etc.)
Justifie amplement la mise en place de cette formation. Elle est
cogérée par un comité pédagogique international
africain, constitué par des enseignants, des chercheurs, tous
spécialistes dans les divers domaines des biotechnologies.
La mutualisation des expériences par toutes ces
compétences est un atout majeur pour la formation des ressources
humaines de qualité au profit du continent africain et de
l'humanité.
Pr. Alfred S TRAORE
Professeur titulaire de Biochimie
Microbiologie
CRSBAN/UFR-SVT/Université de Ouagadougou
DÉDICACE
Je dédie ce travail à :
A ma Mère, MENSAH Akoko Délali
Témoignage vivant de la femme vertueuse. Pour ses
nombreux leçons et exemples qu'elle donne sur la bonté, la
charité, l'amour et la foi en Christ.
Puisse Dieu te récompenser un jour pour tous les
sacrifices que tu as faits à l'endroit de mes soeurs et moi et à
l'endroit de tous les autres.
Je t'aime.
A mon Père TOUDJI BANDJE Kokou Coco
Véritable Homme de vision, que ton courage et ton
abnégation à la lutte servent d'exemple à moi et à
mes frères et soeurs.
Tu as été au coeur de ce travail, ce
travail est bien le tien.
A mes Soeurs
Ayons toujours pour chacun d'entre nous cet amour et
cette collégialité dans l'espoir qu'un jour chacun d'entre nous
arrivera à sa quête.
La lutte continue !
I
REMERCIEMENT
Mes Remerciements vont spécialement :
A l'Union Economique et Monétaire Ouest Africain UEMOA
qui par son programme de bourse PACER à apporter un soutient financier
à mes études et à la réalisation de mes travaux de
recherches.
Au programme de la bourse Suédoise ISP / IPICS qui par
leurs appuis financiers ont contribués à la réalisation de
mes travaux.
A toutes les autorités de l'Université de
Lomé (TOGO)
A toutes les autorités de l'Université de
Ouagadougou (BURKINA FASO)
Au Président du comité scientifique du
Réseau Ouest Africain de Biotechnologies (RA-BIOTECH) le Professeur
Alfred S. TRAORE. Je tiens sincèrement à vous exprimer ma
profonde gratitude pour tous vos efforts et la volonté que vous avez
déployé pour nous initier, nous jeunes étudiants du CRSBAN
à la recherche scientifique.
Au Directeur de l'École Supérieure des
Techniques Biologiques et Alimentaires (ESTBA) et Premier Vice-président
du comité scientifique du Réseau Ouest Africain de
Biotechnologies (RA-BIOTECH), Le Professeur Comlan de SOUZA
Pour tous ses suggestions, toute la rigueur et tous les
sacrifices consentis pour mener ce mémoire jusqu'à son terme.
Je vous suis très reconnaissant pour avoir guidé
mes premiers pas dans le monde de la recherche scientifique et surtout pour
votre disponibilité malgré vos multiples occupations.
Au Professeur Yves TRAORE Maître de Conférences en
Immunologie à l'Université de Ouagadougou
Pour tous ses conseils et suggestions et pour tous les sacrifices
consentis pour l'amélioration de ce travail.
Je vous suis très reconnaissant pour avoir accepté
de codiriger ce travail.
II
Au Secrétaire Principale du RA-BIOTECH le Docteur
BENGALY Marcel Daba Maître Assistant de Nutrition. Pour ses suggestions
et ses encouragements. Vous avez tenu un grand rôle dans
l'évolution de toute la promotion 2007. Vous serez toujours à nos
yeux comme un grand frère avisé.
Au Responsable des soutenances du 3ème cycle
Biochimie-Microbiologie-Biotechnologies. Le Professeur Nicolas BARRO pour ses
conseils avisés et pour toute sa disponibilité.
Au Docteur Simplice KAROU enseignant à l'ESTBA
(Université de Lomé)
Pour ses conseils et ses nombreuses suggestions qui ont
contribués à améliorer ce travail.
A Madame la Directrice de l'Institut National d'Hygiène
du Togo, Dr BANLA KERE Abiba et à tout le personnel des laboratoires de
l'Institut Nationale d'Hygiène pour leur disponibilité et tous
les sacrifices qu'ils ont consenti pour cette étude.
Au Docteur Henry KPANLA, à l'assistant médical
AGBEKA et à tout le personnel des laboratoires du Centre Hospitalier
Préfectoral de Kpalimé (Togo). Pour votre disponibilité et
pour votre esprit scientifique.
Au Dr LAWSON Téyi Épidémiologiste au Centre
de transfusion sanguine de Lomé. Pour sa contribution
déterminante.
Au Professeur D. REDAH chef de service
d'Hépato-gastro-entérologie au CHU Campus de Lomé. Pour
ses nombreuses suggestions.
Au Président de l'ONG CERMETRA Monsieur TCHAKONDO T.
Au Docteur AMEYAPOH Maître assistant de Microbiologie et
à tout le personnel du laboratoire de microbiologie de l'ESTBA.
Pour l'esprit scientifique dont vous avez fait preuve au cours de
nos échanges.
III
A toute l'équipe du CRSBAN et particulièrement
aux Professeurs BARRO Nicolas, KABORE Z. Issiaka, TRAORE Yves, OUATTARA A.
Sidiki., DICKO H. Mamadou. Aux Docteurs Cheick OUATTARA A. T., NIKIEMA
Philippe, BENGALY D. Marcel, SAVADOGO Aly, BASSOLE Ismaël N., ILBOUDO A.
Jules, OUEDRAOGO Lamini.
A toutes les personnes qui ont contribuées de prêt
ou de loin à l'amélioration de ce travail.
A mes amis, et à mes Camarades de la promotion CRSBAN
2007. Pour vos contributions inestimables.
IV
SOMMAIRE:
Page
INTRODUCTION 1
I-GÉNÉRALITÉS 3
1.Rappel sur le foie 4
1.1.Anatomie hépatique 4
1.2. Histologie hépatique 4
1.3.Rôle du foie dans les grandes fonctions
métaboliques 5
1.3.1.Le foie et le métabolisme des glucides 5
1.3.2.Le foie et le métabolisme des protides 5
1.3.3.Le foie et le métabolisme des lipides 5
1.3.4.Le foie et le métabolisme des médicaments
6
1.3.5.Le foie et le métabolisme de la bilirubine 6
1.3.6.Le foie et le métabolisme des acides biliaires 6
2.Rappel sur le virus de l'hépatite B 7
2.1.Le VHB un enjeu de santé publique 7
2.1.1.Prévalence 7
2.1.2.Taux de mortalité 7
2.2.Biologie du VHB 7
2.2.1.Organisation du VHB 7
2.2.2.Mode de Transmission 8
2.2.3.Période d'incubation 8
2.3.Évolution de l'hépatite B 8
2.3.1.l'hépatite aiguë 9
2.3.1.1.l'hépatite fulminante 9
2.3.2.l'hépatite chronique 9
2.3.2.1.Portage chronique asymptomatique ..9
2.3.2.2.l'hépatite chronique active ..9
2.3.2.2.1.Évolution vers la cirrhose 10
2.3.2.2.2.Évolution vers le cancer du foie 10
2.3.2.3.3.L'hépatocarcinome 10
3.Diagnostic 10
3.1.Manifestation Clinique 10
3.2.Examen Clinique 11
3.3.Exploration virologique 11
3.3.1.Les marqueurs directs ...11
3.3.2.Les marqueurs indirects ..11
3.3.2.Exploration biochimique .12
3.3.3.Les transaminases sériques ASAT et ALAT 12
3.3.4.La bilirubine 13
3.3.5.Le taux de prothrombine .13
4.Traitements .13
4.1.Médecine conventionnelle 13
4.1.1.L'alpha interféron 13
4.1.2.L'interféron pégylé .14
4.1.3.La Lamivudine 14
4.1.4. L'Adénovir dipivoxil ..14
4.1.5. L'entécavir 15
4.1.6.Les autres analogues nucléosidiques et inhibiteurs
de la polymérase virale 15
4.2.Les effets secondaires et les Résistances aux
molécules antivirales 15
IV
4.3.La Médecine alternative et traditionnelle face
à l'hépatite B 16
4.3.1.La médecine traditionnelle Asiatique 16
4.3.2.La médecine traditionnelle Africaine 17
4.3.2.1.Quelques plantes impliquées dans le traitement de
l'hépatite ...17
4.4. La Promotion de la médecine traditionnelle 17
II-MATÉRIEL ET MÉTHODES 19
1.Cadre de l'étude 20
2.Type et Période de l'étude 21
3.Déroulement de l'enquête .21
3.1.Méthode ..21
4. Suivi Biologique du traitement 21
4.1.Critères d'inclusion 22
4.2.Critères d'exclusion 22
4.3.Dosage des paramètres biologiques et biochimiques
22
4.3.1.Prélevement sanguin .23
4.3.2.Test sérologique de l'antigène HBs ..23
4.3.3.Suivi des paramètres biochimiques ..23
4.3.3.1.Dosage des transaminases ASAT et ALAT .23
4.3.3.2.Dosage de la créatinine 24
4.3.3.3.Dosage de la bilirubine totale et directe 25
4.4.Les phytomédicaments impliqués dans
l'étude 26
5.Traitement des données 26
III-RÉSULTATS 27
1.Les phytothérapeutes identifiés .28
1.1.La formation des phytothérapeutes 28
1.2. Organisation des phytothérapeutes 28
1.3.Les principales maladies traitées par les
phytothérapeutes 29
1.4.Diagnostic de l'hépatite virale 29
1.5.Traitement 30
1.5.1.Durée du traitement 30
1.5.2.Posologie et péremption des phytomédicaments
30
1.5.3.Effets secondaires des phytomédicaments 31
1.6.Les coûts des traitements des phytothérapeutes
31
2.Evolution des paramètres biologiques au cours du
traitement 32
2.1. Patients 32
2.2.Age et Sexe des patients 32
2.2.1.Antécédents des patients 33
2.3.Évolution des paramètres biochimiques 33
2.3.1.Évolution de la teneur en transaminases ALAT 33
2.3.2.Évolution de la teneur en transaminases ASAT 34
2.3.3.Évolution de la teneur en bilirubine
conjuguée 34
2.3.4.Évolution de la teneur en créatinine 35
2.3.5.Évolution des moyennes de la teneur en transaminases
35
2.3.6.Évolution de la moyenne de la teneur en bilirubine
conjuguée ..36
2.3.7.Évolution de la moyenne de la teneur en
créatinine 36
2.3.8.Évolution du marqueur virologique :
l'antigène HBe 37
2.3.9.Évolution du marqueur virologique :
l'antigène HBs 37
3.Difficultés rencontrées 37
V
IV- DISCUSSION 38
1.Enquête auprès des phytothérapeutes 39
2.Approche comparée de la médecine moderne et de la
phytothérapie traditionnelle ........40
3.Evolution des paramètres biologiques et biochimiques
41
V-CONCLUSION ET RECOMMANDATIONS 44
1.Conclusion 45
2.Recommandations et Perspectives 45
VI-RÉFÉRENCES BIBLIOGRAPHIQUES
47
VII- ANNEXES i
1.Lettre de consentement ii
2.Fiche d'enquête iii
VI
LISTE DES TABLEAUX
Tableau I : Les réactifs de dosage de l'aspartate
aminotransférase (ASAT) ....24
Tableau II : Les réactifs de dosage de l'alanine
aminotransférase (ALAT). ...24
Tableau III : Les réactifs de dosage de la
créatinine 25
Tableau IV : Les réactifs de dosage des bilirubines
.....25
Tableau V: Répartition des Phytothérapeutes en
fonction de leurs expériences professionnelles et de
leur sexe 28
Tableau VI : Répartition des maladies les plus
abordées par les phytothérapeutes 29
Tableau VII : Les Principaux signes cliniques
évoqués pour reconnaitre l'hépatite virale 30
Tableau VIII : Variation de la durée du traitement en
fonction des phytothérapeutes 30
Tableau IX : Les effets secondaires évoqués par les
phytothérapeutes ..31
Tableau X : Coûts mensuels des traitements de
l'hépatite virale par les phytothérapeutes 32
Tableau XI : Age et sexe des patients 32
Tableau XII : Antécédents des patients 33
Tableau XIII : Évolution de la teneur en transaminase ALAT
au cours du traitement 34
Tableau XIV : Évolution de la teneur en transaminase ASAT
au cours du traitement 34
Tableau XV : Évolution de la teneur des sérums en
bilirubine conjuguée .35
Tableau XVI : Évolution de la teneur des sérums en
créatinine 35
Tableau XVII : Détection de l'antigène HBe
après 4 mois 37
Tableau XVIII : Détection de l'antigène HBs
après 4 mois 38
VII
LISTE DES FIGURES
Figure 1 : Face diaphragmatique du foie humain, partie
supérieure 4
Figure 2 : Structure de la particule virale du VHB 8
Figure 3 : Carte du Togo Montrant les zones de l'enquête
20
Figure 4 : Évolutions des moyennes des transaminases ASAT
et ALAT 35
Figure 5 : Évolution de la moyenne de la bilirubine
conjuguée 36
Figure 6 : Évolution de la moyenne de la teneur en
créatinine 36
VIII
INTRODUCTION
Introduction
L'hépatite virale est une atteinte inflammatoire du
foie le plus souvent consécutive à l'infection par l'un des cinq
virus de l'hépatite A, B, C, D et E. Tous ces virus peuvent provoquer
une pathologie aiguë dont les symptômes durent plusieurs semaines :
jaunissement de la peau et des yeux (jaunisse), urines foncées, fatigue
extrême, nausées, vomissements et douleurs abdominales. Il faut
parfois plusieurs mois, voire plusieurs années pour se remettre (OMS,
2000). Le virus de l'hépatite B (VHB) est le plus répandu en
Afrique. Les porteurs chroniques représentent plus de 8% de la
population dans toute l'Afrique subsaharienne (WHO, 2004) : le sujet ne se
débarrasse jamais du virus et peut faire de nombreuses années
plus tard une cirrhose ou un cancer du foie. Dans les pays
industrialisés le cancer du foie et la cirrhose sont traités par
la chirurgie et la chimiothérapie. L'hépatite B chronique active
est traitée sur une longue durée en associant l'interféron
alpha à des analogues nucléosidiques modernes. Ces traitements
permettent de supprimer la réplication virale dans 40% à 50% des
cas. Mais il s'agit d'un traitement extrêmement coûteux et souvent
compliqué par des effets secondaires graves, l'induction de HBV mutants
et la fréquence élevée des rechutes (OMS, 2004).
En Afrique le recours aux recettes de la médecine et de
la pharmacopée traditionnelles connaît un regain
d'intérêt (Kabore et al., 1998). L'Organisation Mondiale
de la Santé estime que plus de 80 % de la population africaine a encore
recours à la médecine et à la pharmacopée
traditionnelle en première intention. Bon nombre de ces tradipraticiens
proposent des remèdes à base de plantes médicinales contre
l'hépatite B.
Il nous semble donc opportun de mener d'une part une
enquête auprès des phytothérapeutes
spécialisés dans le traitement des hépatites et de suivre
l'évolution des paramètres biologiques et biochimiques sur
quelques patients atteints d'hépatite B chronique active soumis à
un traitement par les phytomédicaments.
Les objectifs de cette étude sont donc les suivantes :
1- Mener des enquêtes ethnopharmacologiques sur le
traitement de l'hépatite virale ;
2- Sélectionner les phytomédicaments
d'intérêt pour cette étude ;
3- Sélectionner des patients pour le traitement à
base de phytomédicaments ;
4- Suivre l'évolution de quelques paramètres
biologiques et biochimiques au cours de ce traitement.
I- GÉNÉRALITÉS
1. Rappels sur le foie
1.1. Anatomie hépatique
Le foie humain pèse entre 1400 et 1600 grammes. Il est
formé de deux lobes, droit et gauche, séparés par
l'insertion du ligament falciforme. Sur sa face inférieure, on
reconnaît, en avant du hile, le lobe carré, et en arrière,
le lobe caudé ou lobe de Spigel. L'apport sanguin est double. La veine
porte, formée de l'union de la veine splénique et de la veine
mésentérique supérieure, apporte au foie le sang de la
rate et du tube digestif. L'artère hépatique, branche du tronc
coeliaque, apporte au foie du sang artériel. Le sang quitte le foie par
trois veines sus-hépatiques principales, droites, médianes et
gauches. Le sang du lobe de spigel est drainé par deux et quatre veines
sus-hépatiques accessoires qui se jettent directement dans la veine cave
inférieure. Le foie est délimité en secteurs qui sont
subdivisés en segments. Chaque segment reçoit un pédicule
portal qui comprend une branche de l'artère hépatique, une
branche de la veine porte et un canal biliaire.

Figure 1 : Face diaphragmatique du foie humain, partie
supérieure. Source : Benhamou et Erlinger, 1995
1.2. Histologie Hépatique.
L'unité de structure du foie selon la conception classique
est le lobule qui est une formation polyédrique dont chaque angle est
occupé par un espace porte.
Chaque espace porte contient une branche de l'artère
hépatique, une branche de la veine porte et un ou deux canaux
biliaires.
Les cellules hépatiques ou hépatocytes sont
disposées en lames d'une cellule d'épaisseur. Ces lames
délimitent des sinusoïdes à l'intérieur desquels se
fait la circulation sanguine. Les
sinusoïdes convergent vers le centre du lobule et se jettent
dans la veine sus-hépatique. Dans le lobule, on distingue trois zones
:
Centro lobulaires, médio lobulaire et péri
lobulaire (Benhamou et Erlinger, 1995)
1.3. Rôle du Foie dans les grandes fonctions
métaboliques 1.3.1. Rôle du foie dans le métabolisme des
glucides.
La fonction glycogénique du foie est l'une des plus
importantes fonctions hépatiques ; elle joue un rôle important
dans la régulation de la glycémie. Le foie capte le glucose et
les autres oses et les mets en réserve sous forme de glycogène :
c'est la glycogénogenèse ; mais il se débarrasse des
excédents sous forme de triglycérides qui seront
véhiculées jusqu'au tissus adipeux où ils sont mis en
réserve. En fonction des besoins, le glycogène est
dégradé en glucose : c'est la glycogénolyse. La
réserve glycogénique hépatique est faible et
limitée (150 à 200 g chez l'adulte) ; ce qui explique qu'une
néoglucogenèse permet la transformation de l'acide lactique et de
certains acides aminés dits glucoformateurs en glucose (Frexinos et
Buscail, 2003).
1.3.2. Rôle du Foie dans le métabolisme des
protides.
Les acides aminés, une fois arrivés au foie, ont
deux destinées ; ils subissent :
- Soit une dégradation et perdent leur fonction
aminée qui est transformée en urée dans le cycle de Krebs
;
- Soit une synthèse, les transformant en
protéines de structures, en protéines plasmatiques (albumine,
alpha 1-antitrypsine, lipoprotéine, transferrine céruloplasmine
etc.) ou en facteur de coagulation (fibrinogène, prothrombine,
accélérine, proconvertine, facteur Stuart, facteur anti
hémophilique B).
1.3.3. Rôle du foie dans le métabolisme des
lipides.
Le foie reçoit, soit directement par voie portale, soit
indirectement par voie lymphatique, la majeure partie des lipides alimentaires
; il :
- Catabolise certains acides gras par la â-oxydation avec
production d'énergie (dans le cycle de Krebs) ;
- Synthétise de nouveaux acides gras, des
lipoprotéines circulant servant au transport des graisses, la majeure
partie du cholestérol et les acides biliaires.
1.3.4. Foie et métabolisme des
médicaments
La fonction de détoxication hépatique porte
essentiellement sur les composés organiques étrangers à
l'organisme que sont les médicaments et les produits toxiques divers.
Les enzymes capables de transformer ces composés organiques dans le foie
sont très variées et surtout inductibles par des substances
exogènes.
Les principaux mécanismes de détoxication
hépatique comportent le plus souvent deux aspects :
- D'abord les transformations appelées conjugaisons
consistent à attacher une molécule très hydrophile
à la substance indésirable afin de faciliter son passage dans le
sang et son élimination rénale ;
- De plus les cellules de küpffer ont un pouvoir de
phagocytose.
1.3.5. Rôle du foie dans le métabolisme de
la bilirubine.
La bilirubine est un pigment provenant du catabolisme de
l'hémoglobine des hématies sénescentes (80 à 85%)
et de l'érythropoïèse non efficace (15 à 20%) ou des
sources extraérythropoïètiques (5%). Cette bilirubine est la
bilirubine non conjuguée, insoluble dans l'eau et qui est
transportée par l'albumine dans le sang. Arrivée dans le foie,
elle est captée par les hépatocytes et transformée en
bilirubine conjuguée soluble dans l'eau et pouvant être
excrétée par la bile. L'enzyme qui assure la conjugaison de la
bilirubine est la glucuronyl-transférase dont le déficit entraine
:
- La maladie de Gilbert ;
- La maladie de Crigler-Najjar ;
- L'ictère physiologique du nouveau-né.
1.3.6. Rôle du foie dans le métabolisme des
acides biliaires.
Les acides biliaires dosés dans les milieux biologiques
sont : acide cholique et acide chénodésoxycholique. Ils sont
synthétisés par le foie à partir du cholestérol.
Dans le foie, les acides biliaires sont conjugués à la taurine
(1/3) et à la glycérine (2/3), puis sécrétés
de façon continue dans la bile sous la forme de sel de sodium et
stockés dans la vésicule biliaire au cours des périodes
inter digestives. L'alimentation entraîne la vidange biliaire et le
passage des sels biliaires dans la lumière intestinale. Dans le
grêle, 80% des sels biliaires sont déconjugués par les
enzymes bactériennes et sont réabsorbés par la muqueuse,
principalement au niveau de l'iléon puis drainés vers le
parenchyme hépatique par l'intermédiaire du système porte,
c'est le cycle entéro-hépatique qui se reproduit au moins 2 fois
au cours d'un repas.
2. Rappel sur le virus de l'hépatite B (VHB)
2.1. Le VHB un enjeu de santé public
L'Organisation Mondiale de la Santé (OMS) estime que
l'hépatite B est l'une des principales maladies humaines et pose un
sérieux problème de santé publique a l'échelle
mondiale. On estime a 2 milliards le nombre de personnes infectées par
le virus, dont plus 350 a 400 millions deviennent des porteurs chroniques. Ils
peuvent transmettre le virus pendant des années (OMS, 2000). Les
porteurs chroniques sont exposés a un risque élevé de
décès par cirrhose du foie ou cancer du foie. Le vaccin contre
l'hépatite B ne guérit pas les porteurs chroniques, mais il est
efficace a 95% pour prévenir l'apparition d'un état de porteur
chronique. Les personnes infectées dans leur petite enfance sont celles
qui ont le plus de risques de devenir des porteurs chroniques. Ainsi, 90% des
enfants infectés avant l'âge d'un an, et 30% a 50% des enfants
infectés entre un an et quatre ans vont développer une infection
chronique. Le risque de décès par cirrhose et cancer du foie dus
au virus de l'hépatite B est approximativement de 25% (Eugène et
Costentin, 2004). L'Organisation Mondiale de la Santé a
recommandé de vacciner tous les enfants contre l'hépatite B.
Aujourd'hui, 116 pays ont ajouté ce vaccin a leur programme de
vaccination systématique (OMS, 2000).
2.1.1. Prévalence
La séroprévalence varie en générale
d'une région a une autre, on distingue :
- Des zones a forte endémicité où la
prévalence en antigène de surface HBs est supérieure a 8%
(toute l'Afrique sauf le Maghreb, Asie du sud-est, une partie de
l'Amérique latine) ;
- Des zones a endémicité intermédiaire
où la prévalence en antigène de surface HBs est comprise
entre 7% et 3% (Afrique du nord, Russie, Europe de l'est, France, Italie) ;
- Des régions a faible endémicité ou le taux
de prévalence est inférieur a 3% Amérique du nord,
Australie, Angleterre (WHO, 2004).
Au Togo la séroprévalence de l'antigène
HBs est estimée a 11% (Kouassi et al., 2007). Au Burkina elle
est estimée a 12% (Simporé et al., 2004). La Sierra
Leone le Libéria et le Sénégal sont les seuls pays de
l'Afrique subsaharienne dont les taux de prévalences sont
inférieurs a 8%. Il faut noter que ce taux de
séroprévalence varie généralement suivant les
tranches d'âges et suivant que l'on se trouve en zone rurale ou en zone
urbaine (Kramvis et Kew, 2007).
2.1.2. Taux de mortalité
Plus de 500.000 a 700.000 personnes meurent chaque
année de cancer du foie consécutif a une hépatite B
chronique. Cette maladie constitue la première cause de
décès par le cancer dans le monde (OMS, 2004).
2.2. Biologie du virus de l'hépatite B
2.2.1. Organisation morphologique du VHB
Le virus VHB de l'hépatite B appartient à la
famille des hépadnaviridae, famille dont les membres ont une
capacité commune d'induire chez leurs hôtes naturels des
infections chroniques. C'est un virus à tropisme essentiellement
hépatocytaire (Brechot et Pol, 1993). L'ADN du virus VHB d'une taille de
3,2 kbases est circulaire partiellement bicaténaire. Il est
entouré d'une capside constituée de protéine qui
possède une enveloppe lipoprotéique contenant trois
protéines virales l'antigène de surface HBs, l'antigène
HBc insoluble et un antigène HBe soluble.
Le VHB réplique son génome grâce à son
ADN polymérase.

Figure 2 : Structure de la particule virale du
VHB (George et Kepoyer, 2008) 2.2.2. Mode de
Transmission
- Transmission verticale (de la mère
à l'enfant) ;
- Transmission par transfusions sanguines ou de produits sanguins
;
- Transmission iatrogène par
matériel non stérilisé (chirurgie, soins dentaires,
mésothérapie etc.) ; - Transmission par voies sexuelles ;
- Transmission par toxicomanie intraveineuse, tatouage, piercing
(Trepo et al., 2006).
2.2.3. Période d'incubation.
La période d'incubation varie de 45 à 180 jours,
mais la moyenne est de 60 à 90 jours, la durée pouvant augmenter
ou diminuer selon la gravité de l'infection.
2.3. Evolution de l'hépatite B
Dans plus de 80% des cas, les personnes adultes atteintes par
le virus de l'hépatite B vont guérir naturellement sans
développer aucun signe de la maladie. Environ 10% des personnes
atteintes vont développer une hépatite aiguë et pour les 10%
restant l'infection va évoluer vers une chronicité (Moreira, 2003
; Allain et Owusu-Ofori, 2006).
2.3.1. L'hépatite aiguë
Cette forme de la maladie est peu fréquente.
Après une période d'incubation de 10 semaines en moyenne, suivie
d'une phase pré ictérique de 7 jours environ, survient la phase
ictérique. Biologiquement on observe alors une augmentation importante
des transaminases sériques. Le taux de prothrombine est normale ou
modérément abaissé, en tout cas toujours supérieur
à 50 % en l'absence d'évolution sévère (Bertrode,
1997). L'hépatite aiguë est due à la réponse du
système immunitaire face à l'envahissement des
hépatocytes. Elle ne nécessite en général aucun
traitement s'il n'y a pas de complication et les symptômes disparaissent
au bout d'un certain temps.
2.3.1.1. L'hépatite fulminante.
C'est une nécrose massive du foie due à une
réponse exagérée du système immunitaire face
à l'envahissement des hépatocytes par le virus (Moreira, 2003).
Cette forme de la maladie apparaît dans 1% des cas d'hépatite
aiguë. L'hépatite fulminante entraîne une mortalité
à brève échéance dans plus de 80% des cas, seule
une transplantation urgente du foie permet de sauver le malade. Elle est
marquée biologiquement par un taux de prothrombine inférieur
à 50 %, associé à une encéphalopathie
hépatique (Dupeyron, 2001).
2.3.2. L'hépatite chronique
Elle est définie par un portage d'antigène HBs
supérieur à 6 mois après l'épisode
d'hépatite aiguë. L'infection se présente sous des formes
variables, allant du portage asymptomatique; de l'antigène HBs à
l'hépatite chronique, la cirrhose, voire le carcinome
hépatocellulaire.
2.3.2.1. Le Portage chronique asymptomatique
Un tiers des porteurs chroniques sont des porteurs
asymptomatiques leurs transaminases sont normales. Ils peuvent vivre plusieurs
années avec la maladie sans qu'elle ne se déclenche.
2.3.2.2. L'hépatite chronique active
Deux tiers des patients porteurs de l'antigène HBs vont
développer des lésions d'hépatite chronique.
L'évolution se fait schématiquement selon trois phases de
durées variables. La première phase qui dure de quelques mois
à quelques années est une phase de tolérance immunitaire.
Elle est marquée par une multiplication active du virus avec un taux
d'ADN sérique élevé et la présence
d'antigène HBs dans le sérum. La deuxième phase est
caractérisée par une flambée de la réponse
immunitaire qui se traduit par la lyse des hépatocytes infectés
par l'action des lymphocytes T cytotoxiques et des Natural Killers.
L'ictère et l'élévation des transaminases sont donc
liés à la destruction des hépatocytes infectés
(Dupeyron, 2001 ; Perrez, 2004).
2.3.2.2.1. La cirrhose
Environ 20 % à 25 % de toutes les hépatites
chroniques évoluent vers la cirrhose si le traitement n'agit pas
pleinement ou s'il n'est pas respecté. L'état cirrhotique
correspond à une multiplication excessive des cicatrices qui se sont
formées à la suite des agressions répétées
contre le foie (virales, alcool, etc.). Ces « barrières fibreuses
» finissent par entraver la libre circulation du sang dans l'organe. On
observe une augmentation du volume du foie dont les bords deviennent tranchants
et des signes d'hypertension portale (Gelbke, 2008).
2.3.2.2.2. Le cancer du foie
C'est la complication ultime d'une cirrhose. Précisons
cependant qu'un cancer du foie peut aussi résulter d'une cause extra
hépatique (intoxications, aflatoxines) ou tout simplement être
secondaire à un cancer localisé dans un autre organe le cancer du
foie est une tumeur des cellules du parenchyme du foie. Le cancer du foie du
à l'hépatite B concerne environ 15% des cas de cancer (Gelbke,
2008)
2.3.2.2.3. L'hépatocarcinome ou
hépatome.
Il s'agit de la plus fréquente des tumeurs
hépatiques. Elle se développe à la place des cellules du
parenchyme hépatique qui ont une capacité de
sécrétion. Il s'agit de tumeurs bénignes (adénome
solitaire bénin de Cathala) soit malignes (hépatocarcinome,
adénocarcinome, adénocancer hépatique,
épithélioma ou carcinome hépatocellulaire) le plus souvent
secondaires à une cirrhose hépatique. Le patient présente
alors une augmentation de volume du foie de façon isolée
s'accompagnant de douleurs (Gelbke, 2008).
3. Diagnostic
3.1. Manifestations cliniques.
Dans le cas d'une hépatite chronique active, certains
symptômes peuvent apparaître. Une petite fièvre, une
augmentation du volume du foie et/ou de la rate (hépatomégalie
et/ou splénomégalie), des poussées ictériques
(symptômes d'allure pseudo grippale : céphalées, douleurs
articulaires et musculaires, mais aussi nausées, diarrhée, urines
foncées) et des manifestations extra hépatiques, dues aux
dépôts de complexes immuns (ex : péri artérite
noueuse). En cas de cirrhose, on peut retrouver des signes cliniques
d'insuffisance hépatocellulaire et d'hypertension portale.
3.2. Examen clinique
L'examen clinique comporte :
- L'examen général : qui cherche la
température, la tension artérielle, le pouls, le poids, la
taille. - L'examen clinique va rechercher :
· Les signes d'insuffisance hépatocellulaire (foetor
hépatique, astérixis, ictère, hippocratisme digital, ongle
blanc, érythrose palmaire, angiome stellaire).
· Signes d'encéphalopathie hépatique.
· Signes d'hypertension portale notamment la circulation
veineuse collatérale, l'ascite, la splénomégalie (Bagny,
2007).
3.3. Exploration virologique
Le diagnostic des différentes situations cliniques est
effectué par la détection des marqueurs virologiques de
l'infection. Il s'agit soit de méthodes immuno-enzymatiques de type
ELISA (Enzyme Linked Immuno-Sorbent Assay), soit de techniques
moléculaires détectant, quantifiant ou caractérisant la
séquence de l'ADN du virus de l'hépatite B.
3.3.1. Les marqueurs directs :
· L'antigène HBs associé aux enveloppes
virales est aisément mis en évidence dans le sérum des
patients par des techniques immuno-enzymatiques de type ELISA.
· L'antigène HBc n'est pas retrouvé tel quel
dans le sérum.
· Une protéine soluble, dérivée de
la protéine de capside, porte un antigène appelé HBe qui
est parfois détecté dans le sérum en cas de multiplication
virale, également par des techniques immuno-enzymatiques de type
ELISA.
· L'ADN viral circulant associé aux particules
virales infectieuses est mis en évidence par des
techniques d'hybridation moléculaire (Dupeyron,
2001).
3.3.1.2. Les marqueurs indirects :
Ce sont les anticorps secrétés par le patient
lorsqu'il rencontre les différents antigènes du virus B :
l'anticorps anti-HBs, les anticorps anti-HBc IgG, anti-HBc IgM, et l'anticorps
anti-HBe. Ils sont eux aussi détectés par des méthodes
immuno-enzymatiques de type ELISA.
3.3.2. Exploration biochimique
3.3.2.1. Les transaminases sériques ALAT et
ASAT
Les lésions hépatiques sont, en
réalité, dues à un ensemble de réactions
immunologiques à médiation principalement cellulaire. La
destruction des hépatocytes par les lymphocytes T cytotoxique et les
Naturals Killers conduit à la libération d'enzymes
hépatiques, comme l'Alanine amino transférase (ALAT) et
l'Aspartate amino transférase (ASAT). L'augmentation des taux des
transaminases sériques est donc facilement détectable et signe
une cytolyse hépatique importante (Dupeyron, 2001).
> Alanine Amino Transférase ou Sérum
Glutamopyruvate Transférase (SGPT)
On les trouve essentiellement dans le foie, les reins mais
également en quantité plus faible dans les muscles striées
(muscles sous la dépendance de la volonté, contrairement aux
muscles lisses) et dans les globules rouges. Son taux est habituellement de
:
· 8 à 40 unités internationales par litre
chez l'homme.
· 6 à 32 unités internationales par litre
chez la femme.
> Aspartate Amino Transférase ou
Sérum Glutamooxaloacetate Transférase (SGOT)
On les trouve plus spécifiquement dans les muscles
striés, dans les globules rouges et dans
le foie, son taux augmente quand il existe une destruction de
ces cellules. Son taux est
habituellement de :
· 8 à 38 unités internationales par litre
chez l'homme.
· 6 à 31 unités internationales par litre
chez la femme.
Lors d'une hépatite chronique active ces
différentes valeurs peuvent s'élever de jusqu'à 20
fois.
Ces transaminases peuvent également s'élever dans
d'autre cas comme :
· Les parasitoses (présence de parasites dans le
sang) ;
· L'infarctus du myocarde (destruction d'une partie du
muscle cardiaque) ;
· Les attaques musculaires (traumatismes) ;
· Les pancréatites (inflammation du pancréas)
;
· Les surcharges pondérales (obésité,
stéatose : dépôt de graisse dans les cellules de
l'organisme) ;
· Chez les personnes âgées de plus de 60
ans.
3.3.2.2. La Bilirubine
Pigment biliaire, de coloration jaune tirant sur le rouge ou
le brun, issu de la biliverdine, elle-même issue de l'hémoglobine
(constituant principal des globules rouges, destiné à transporter
l'oxygène dans le sang). La bilirubine est le principal colorant de la
bile.
On distingue : La bilirubine direct, appelée
également bilirubine vraie ou non conjuguée, non soluble dans
l'eau. Elle est transportée jusqu'au foie par l'albumine
(protéine) contenue dans le sang. La bilirubine conjuguée,
soluble dans l'eau, provenant de la transformation chimique se faisant à
l'intérieur du foie. Elle est excrétée dans la bile.
À l'intérieur des intestins, la bilirubine conjuguée
permet de colorer les selles en brun, grâce à l'action de
bactéries (Gelbke, 2008).
La bilirubine totale : inférieure à 17
micromole/L chez le sujet normal, est supérieure à cette valeur
au cours des ictères. Les hépatites aiguës et chroniques
actives se caractérisent par un ictère à bilirubine
conjuguée (Dupeyron, 2001).
3.3.2.3. Le taux de Prothrombine
Son dosage permet d'apprécier le degré de
l'insuffisance hépatocellulaire chez le malade. Le taux normal est
supérieur à 70%; ce taux est toujours supérieur à
50% en absence d'évolution sévère de l'hépatite.
4. Les traitements
4.1. La médecine conventionnelle
Le traitement a pour but d'influer sur l'histoire naturelle
de l'hépatite B chronique en raccourcissant sa durée. Il permet
dans certains cas d'éviter l'évolution vers la cirrhose et donc
éviter la survenue du carcinome hépatocellulaire. Le traitement
interrompt la réplication du VHB et donc, avance le moment de la
séroconversion HBe, HBs. La durée du traitement est assez
variable de six mois à une ou plusieurs années (Perrez, 2004).
4.1.1. L'alpha interféron
L'interféron alpha (IFN a) est une cytokine
naturellement produite par le système immunitaire. Au cours de
l'hépatite B chronique, il existe un défaut de production de
l'IFN a par les cellules mononuclées qui pourrait être lié
à un effet inhibiteur du virus lui-même.
L'IFN a a un effet antiviral sur l'infection du VHB via deux
mécanismes. Il a un effet antiviral direct et rapide en inhibant les ARN
viraux et en activant des enzymes ayant une activité antivirale, la
2'5'oligoadénylate synthétase et une protéine kinase.
La 2'5'oligoadénylate synthétase
polymérise 3 à 5 molécules d'ATP par une liaison 2'-5'.
Les oligonucléotides ainsi formés vont activer une RNase, qui va
fragmenter les ARN messagers du virus. De plus, l'IFN a augmente
l'efficacité de la réponse immunitaire vis-à-vis des
cellules hépatiques infectées, en augmentant l'expression des
antigènes d'histocompatibilité de classe I. Il stimule
également l'activité des lymphocytes T helpers et des cellules NK
(Naturel Killer). La destruction des cellules hépatiques
infectées, lors d'un traitement à l'interféron a, conduit
donc à une libération du contenu cellulaire dans la circulation,
d'où un pic du taux plasmatique des transaminases (David et Smuth,
2004).
4.1.2. L'interféron
pégylé
Il existe actuellement deux types d'IFN pégylés
: IFN pégylé a-2a et IFN pégylé a-2b. Il s'agit
d'IFN alpha auxquels on a attaché un groupement
polyéthylène glycol permettant d'allonger la demi-vie de la
molécule. En effet, cette modification chimique augmente le poids
moléculaire de la molécule, diminuant ainsi sa clairance
rénale. Cette pégylation de l'IFN alpha a également
optimisé sa pharmacocinétique et a permis de rendre son
administration hebdomadaire. L'activité antivirale de l'IFN
pégylé est identique à celle de l'IFN a.
Une réponse prolongée et durable après
l'arrêt du traitement par l'interféron n'est observée que
chez 30% des patients en moyenne (Dusheiko et Antonakopoulos, 2007).
4.1.3. La lamivudine
La lamivudine (29,39-dideoxy-39-thiacytidine) est un
L-nucléoside analogue de la didésoxycytidine. Elle inhibe la
polymérase du VHB par incorporation compétitive avec la
didésoxycytidine. Lors d'un traitement à la lamivudine, par
administration quotidienne de 100 mg, le taux sérique d'ADN du VHB chute
considérablement, jusqu'à devenir indétectable dans
certains cas. Cependant, dès l'arrêt du traitement, le taux
revient rapidement à ses valeurs pré
thérapeutiques. Le problème réside dans
le mode d'action de cette molécule. En effet, la lamivudine inhibe la
polymérase mais n'a pas d'action sur la formation initiale d'ADN super
enroulé et le maintien du pool de cet ADN dans les hépatocytes
(Dusheiko et Antonakopoulos, 2007).
4.1.4. L'adéfovir dipivoxil
L'adéfovir, ou PMEA
(9-(2-phosphonylméthoxyéthyl) adénine), appartient
à une famille de drogues antivirales récentes, les phosphonates
de nucléosides acycliques. La forme active diphosphorylée de
l'adéfovir inhibe les virus à ADN et certains rétrovirus.
Le PMEApp, le métabolite actif du PMEA, est un inhibiteur
compétitif du désoxy-ATP, substrat naturel de la
polymérase du VHB. Le PMEApp inhibe également les
polymérases de VHB mutants résistants à la lamivudine ou
au famciclovir (Dusheiko et Antonakopoulos, 2007).
4.1.5. L'entécavir
L'entécavir est un analogue de la cyclopentylguanosine
et inhibe spécifiquement la polymérase du VHB. L'entécavir
a montré son efficacité dans les cas de résistances du
virus VHB à la lamivudine mais cette efficacité est partielle et
nécessite une forte dose de la molécule (David et Smuth,
2004).
4.1.6. Les autres Analogues nucléosidiques et
Inhibiteurs de la polymérase
virale.
Telbivudine Il s'agit d'un L-nucléoside analogue de la
thymidine, qui inhibe spécifiquement l'activité de la
polymérase du VHB.
· Le ténofovir est une molécule proche de
l'adéfovir, c'est un analogue de la didésoxyadénosine. Il
inhibe la polymérase du VHB et du VIH, même dans les formes
résistantes à la lamivudine. L'efficacité du
ténofovir a été démontrée chez des sujets
co-infectés VIHVHB.
· ARA-AMP l'arabinoside adénine monophosphate,
est un analogue de l'adénosine et inhibe également
l'activité de l'ADN polymérase du VHB. Mais, ce composé
étant peu sélectif de l'ADN polymérase virale, il s'est
révélé très toxique (Vochelle et
al.,2007).
D'autres molécules sont en cours d'évaluation
clinique, on peut citer l'emtricitabine (structure proche de la lamivudine), la
clévudine (analogue de pyrimidine), l'elvucitabine et la thymosine.
4.2. Les effets secondaires et les Résistances
du VHB aux molécules antivirales.
Les premières mutations de résistance aux
antiviraux ont été décrites sous monothérapie par
lamivudine avec la mutation M204I/V, substitution d'une méthionine par
une valine ou une isoleucine en position 204 du gène P, dans le motif
YMDD du site actif de la polymérase. L'incidence de cette mutation est
forte : 24 % à un an de traitement, 42 % à 2 ans, 70 % à 4
ans. D'autres mutations de résistance ou de compensation ont ensuite
été décrites et continuent à être
décrites avec les antiviraux actuellement disponibles ou en cours
d'évaluation (adefovir dipivoxil, entécavir, ténofovir,
emtricitabine, clévudine, telbivudine, etc.), avec une incidence
variable et d'éventuelles résistances croisées entre les
différentes molécules (Dusheiko et Antonakopoulos, 2007).
La résistance à l'INF-á, molécule
naturelle est incertaine. Toute fois des mutations au niveau des
protéines de la capside virale ont montré une suppression de
l'induction de la protéine Mx, un effecteur viral important pour la
sensibilité du traitement à l'INF-á (Abel et
AlegriaHartman, 2002).
On note d'importants effets secondaires au niveau de la plus
part de ces inhibiteurs de la polymérase virale. On peut noter que
INF-á, la lamivudine sont les plus tolérables.
4.3. La Médecine alternative et traditionnelle
face à l'hépatite B.
La << Médecine traditionnelle » est un
terme qui englobe à la fois la médecine traditionnelle chinoise,
l'Âyurveda indien et l'Unani arabe et avec diverses formes de
médecine indigène. Les thérapies médicamenteuses
qui impliquent l'usage de médicaments à base de plantes, à
partir d'animaux et/ou minéraux et les thérapies non
médicamenteuses qui sont administrées principalement sans usage
de médicaments. C'est le cas de l'acupuncture, des thérapies
manuelles et des thérapies spirituelles. Dans d'autres pays la
médecine traditionnelle est encore appelée médecine
<< complémentaire », << alternative »ou <<
non conventionnelle » (OMS, 2002).
4.3.1. Médecine traditionnelle asiatique face
à l'hépatite virale.
Selon la médecine chinoise, le Foie est le
siège des émotions primaires et tout particulièrement de
la colère qui, mal ou trop exprimée, risque de créer un
terrain favorable à l'apparition d'une maladie du foie, ou tout
simplement d'aggraver celle d'origine purement physique (Hobbs, 1986).
En phytothérapie, il existe plusieurs
préparations en pharmacopée chinoise destinées à
traiter l'hépatite virale, probablement parce que cette maladie a
longtemps causé de sérieux problèmes en
Asie. Ces préparations n'ont pas fait l'objet
d'études cliniques à large échelle et à long terme
et les études publiées jusqu'à présent sont de
faible qualité méthodologique.
Astragalus membranaceus, l'astragale entre dans la
composition de nombreuses préparations médicinales
traditionnelles couramment utilisées en Chine et ailleurs en Asie. On
lui attribue des propriétés immunostimulantes et antivirales.
Quelques études sur des animaux et sur des humains
(réalisées en Chine) indiquent que l'astragale pourrait aider
à protéger le foie en cas d'hépatite toxique ou
d'hépatite virale B ou C (Natural Standard, 2004).
Schisandra sinensis plusieurs essais sur les animaux
indiquent que les lignanes contenues dans la plante peuvent protéger le
foie, améliorer son fonctionnement et favoriser la
régénération des cellules hépatiques en cas
d'atteinte toxique. Des études cliniques menées en Chine
indiquent que les ingrédients actifs du schisandra peuvent
combattre les hépatites d'origine virale ou médicamenteuse.
Phyllanthus sp, cette plante indigène de
l'Inde est utilisée pour traiter les problèmes du foie en
médecine ayurvédique (la médecine traditionnelle de
linde). Des études préliminaires indiquent que cette plante
possède des propriétés antitoxiques et antivirales contre
le virus de l'hépatite B (Chan et al., 2003).
4.3.2. La médecine traditionnelle
Africaine.
La médecine traditionnelle africaine est un ensemble
de savoirs, de connaissances, de pratiques, de techniques, de
préparations et d'utilisations des substances végétales,
animales et/ou minérales, qui servent à diagnostiquer,
prévenir et/ou éliminer un déséquilibre physique,
mental ou social. C'est le patrimoine thérapeutique de l'Afrique. A
l'heure actuelle, elle est orale ou écrite et les connaissances y
afférentes sont transmises de génération en
génération. L'OMS estime que plus de 80 % de la population
africaine a encore recours à la médecine et à la
pharmacopée traditionnelle. A cet effet, on dénombre un (01)
tradipraticien pour 200 habitants. Aussi, les tradipraticiens sont
consultés en première intention par une majorité des
patients surtout pour les maladies chroniques (OMS, 2002).
4.3.2.1. Quelques plantes impliquées dans le
traitement de l'hépatite B.
Desmodium adscendens, plante herbacée de la
zone équatoriale, rampante ou grimpante sur les troncs d'arbre, de la
famille des fabacées traditionnellement une décoction faite avec
les parties aériennes de cette plante sert à traiter
l'hépatite B et C (Kéita, 1995).
Combretum micrantum, de la famille des
combrétacées est un hépatotrope qui est couramment
utilisé en Afrique sub-saharienne contre la jaunisse et les
hépatites.
Phyllanthus amarus, cette plante de la famille des
euphorbiacées a des activités anti hépatotoxiques. Elle
est utilisée en pharmacopée africaine pour le traitement de la
jaunisse et des troubles hépatiques; elle possède
également une activité antivirale : inactivation de
l'antigène HBs in vitro (Ott et al., 1997).
4.4. La promotion de la médecine
traditionnelle
Les gouvernements sont en train de réagir à
l'utilisation croissante de la Médecine Traditionnelle (MTR). Plusieurs
pays s'attellent actuellement à la réglementation des
médicaments à base de plantes ; le nombre d'États membres
de l'OMS possédant des réglementations relatives aux
médicaments à base de plantes a augmenté de 52 en 1994
à 64 en 2000. Dans certains pays, les structures, les budgets et la
formation consacrés à la MTR connaissent une croissance
progressive. Le nombre grandissant d'instituts nationaux de recherche sur la
MTR dans les pays en voie de développement est également un signe
de l'importance croissante de la MTR. En fait, la plupart des pays en voie de
développement possèdent aujourd'hui des instituts nationaux de
recherche sur la MTR.
En 2000, le comité régional africain de l'OMS,
auquel 25 ministres de la santé étaient présents, a
demandé un soutien pour la création d'un environnement favorable
à la MTR, le développement de directives pour la formulation et
l'évaluation de politiques nationales de MTR et la mise au point de
mécanismes visant à l'amélioration des environnements
économiques et réglementaires pour la production locale de
médicaments traditionnels. Pour maximiser les possibilités de la
MTR en tant que source de soins de santé, plusieurs problèmes
doivent être abordés : politique ; innocuité ;
efficacité et qualité ; accès ; usage rationnel (OMS,
2002).
II-MATÉRIEL ET MÉTHODES
II-MATÉRIEL ET MÉTHODES
II- Matériel et Méthodes
1. Cadre de L'enquête.
En ce qui concerne l'enquête auprès des
phytothérapeutes, trois grandes villes du Togo ainsi que deux
préfectures ont été prises en compte.
· La ville de Lomé, Elle se situe à
l'extrême sud-ouest du Togo, et s'étend le long du littoral du
Golfe de Guinée. C'est la capitale du Togo officiellement,
l'agglomération compte 1.325 416 habitants.
· La ville de Kpalimé, Situé au coeur du pays
éwé, Kpalimé est à 120 km au nord ouest de la
capitale Lomé avec 101 088 habitants. Elle est la quatrième ville
du Togo.
· La ville de Sokodé, Elle compte plus de 123 029
habitants la deuxième ville du Togo Elle est située à 338
km au nord de Lomé (encyclopédie wikipedia, 2008)
· Les préfectures de Tchaoudjo et de Tchamba qui
compte respectivement 318.750 habitants et 216.500 habitants.

Légende
Zones enquêtées
Préfecture de Tchaoudjo
Préfecture de Tchamba Lomé
Sokodé
Kpalimé Tchamba
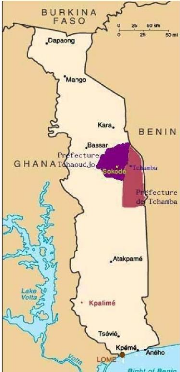
Figure 3: Carte du Togo montrant les zones de
l'enquête ethnopharmacologique.
En ce qui concerne le suivi des paramètres biologiques et
biochimiques.
Les analyses biomédicales se sont déroulées
dans les laboratoires de sérologie et de biochimie de l'institut
national d'hygiène à Lomé et au centre hospitalier
préfectoral de Kpalimé.
Les personnes impliquées dans l'étude sont des
patients du centre CPHYSAM (Centre de Phytothérapie Sensibilisation et
Assistance aux Malades). Ce centre de phytothérapie est situé
dans le quartier Tokoin wuiti à Lomé.
2. Type et Période de l'étude
En ce qui concerne les enquêtes auprès des
phytothérapeutes, c'est une étude prospective qui s'est
déroulée du 26 Août 2007 au 20 Avril 2008.
En ce qui concerne le suivi des patients sous
phytothérapie, il s'agit d'une étude qui s'est
déroulée sur une période de novembre 2007
en mai 2008. Cette étude à deux objectifs.
- Contrôler l'évolution mensuelle des
paramètres biochimiques liés à l'apparition ou à la
persistance d'un problème hépatocellulaire;
- Contrôler la clairance rénale des
phytomédicaments ingérés par les patients.
3. Déroulement de l'enquête
Les fiches d'enquêtes conçues (Annexe I) ont
été distribuées grâce aux associations et aux
regroupements de phytothérapeutes. Ces associations régionales
ont transmises les listes des phytothérapeutes spécialistes dans
le traitement de l'hépatite virale. Les fiches ont été
transmises à ses spécialistes et remplies après des
entretiens avec ces derniers.
3.1. Méthode
Une enquête auprès des phytothérapeutes a
été initiée dans le but de collecter des données
concernant leur méthodologie dans le diagnostic, et dans le suivi de
leurs patients au cours de leur traitement. Il s'avère essentiel
d'aborder et d'éclaircir divers points notamment ceux touchant à
l'innocuité, à la qualité, aux coûts des traitements
et à la connaissance de l'hépatite virale. Ces fiches contiennent
une trentaine de questions.
4. Suivi des paramètres biologiques et
biochimiques
Les personnes recrutées pour cette étude sont des
patients du Centre de Phytothérapie Sensibilisation et Assistance aux
Malades (CPHYSAM).
4.1 Critères d'inclusion
- Patients âgés de 18 à 60 ans;
- Sérologie de l'antigène HBs positive sur plus de
6 mois;
- Patients ayant dans leur sérum un taux d'alanine amino
transférase ou d'Aspartate amino transférase compris entre 41 et
200 UI/L;
- Patients ne souffrant pas d'une complication cardio-vasculaire
ou rénale;
- Patients n'ayant pas été atteints de troubles
mentaux;
- Personne n'étant pas présentement impliqué
dans un traitement à l'alpha interféron ou à tout autre
antiviral dirigé contre le virus de l'hépatite B;
- Personne n'ayant pas été victime d'une
encéphalopathie hépatique;
- Personne n'ayant pas fait usage d'aucune substance
immunosuppresseur;
- Personne n'ayant pas été infecté par l'un
des virus du SIDA;
- Personne ayant librement consenti à suivre le traitement
par les phytomédicaments.
4.2. Critères d'exclusion
- Patients âgés de moins de 18 ans et de plus de 60
ans, femme enceinte ou en cours d'allaitement; - Sérologie de
l'antigène HBs négative;
- Patients ayant dans leur sérum un taux d'Alanine amino
transférase ou d'Aspartate amino transférase inférieur 41
ou supérieur 200 UI/L;
- Personne souffrant d'une complication cardio-vasculaire ou
rénale;
- Personne ayant des troubles mentaux;
- Personne étant impliqué actuellement dans un
traitement à l'alpha interféron ou tout autre antiviral
dirigé contre le virus de l'hépatite B;
- Personne souffrant d'une encéphalopathie
hépatique;
- Personne ayant utilisé dans le passé une
substance immunosuppresseur;
- Personne infectée par l'un des virus du SIDA (VIH1,
VIH2);
- Personne n'ayant pas librement consenti à suivre le
traitement par les phytomédicaments.
4.3. Dosage des paramètres biologiques et
biochimiques
Après l'exploration biologique sur 13 patients, 4 patients
et un témoin ont été retenus pour l'étude.
4.3.1. Prélèvement sanguin
Le sang veineux a été prélevé chez
tous les patients dans un tube sec et propre. Les patients étant
à jeun. Les prélèvements sanguins ont été
centrifugés dans des tubes secs à 3000 tours par minute pendant
10 minutes et les sérums ont été recueillis pour les
dosages.
4.3.2. Le Test sérologique de l'antigène
HBs
L'antigène HBs est révélé par la
technique ELISA. Le kit MONOLISA HBs Ag ULTRA de Bio-Rad
repose sur l'utilisation d'un support solide (puits, microparticules) recouvert
par des anticorps monoclonaux et des anticorps polyclonaux
sélectionnés pour leur capacité à se lier aux
différents sous types de l'antigène HBs. Ce matériel est
associé à un incubateur, un laveur et un
spectrophotomètre.
4.3.3. Suivi des paramètres
biochimiques
Le dosage des paramètres biochimiques a été
réalisé chaque 30 jours pendant 4 mois chez tous les patients.
4.3.3.1. Dosage des transaminases ASAT et
ALAT
Principe
Les dosages sont basés sur la mesure cinétique des
transaminases sériques dans un système réactionnel dont la
finalité est l'oxydation du coenzyme NADH,H.+
L'aspartate aminotransférase (ASAT) catalyse la
transformation de l'aspartate en oxaloacétate. L'oxaloacétate
formé est réduit en malate en présence d'une
quantité connue de coenzyme NADH'H+ et du malate
déshydrogénase (MDH). La cinétique de cette
dernière réaction est déterminée par les mesures
successives de l'absorbance du coenzyme NADH'H+ à 340 nm. De cette
cinétique est déduite la concentration de l'aspartate
aminotransférase (ASAT).
ASAT

Aspartate + á-cétoglutarate Oxaloacétate +
Glutamate
MDH
Oxaloacétate + NADH + H+ Malate +
NAD+
La transamination de l'alanine en pyruvate est
réalisée en présence de l'alanine aminotransférase
(ALAT). Le pyruvate obtenu est réduit en lactate en présence du
coenzyme NADH'H+ et du lactate déshydrogénase (LDH).
La cinétique de cette dernière réaction permet de
déterminer la concentration de l'alanine aminotransférase
(ALAT).
ALAT

Alanine + á-cétoglutarate Pyruvate + Glutamate
LDH

Pyruvate + NADH + H+ Laclate + NAD+
Les contenants des deux flacons R1 et R2 du kit
Spinreact Transaminases (Tableau I et Tableau II) ont
été mélangés pour obtenir un réactif final
stable pendant 21 jours entre 2°c et 8°c.
Ce réactif a été introduit dans l'automate
Lisa 500 plus.
La solution de contrôle (sérum de contrôle)
a été ajoutée à l'automate ainsi que 50 ul de
chaque échantillon de sérum à doser. La calibration de
l'automate et le dosage des sérums ont été ensuite
programmés via un microordinateur intégré au
système. Les différentes lectures de l'absorbance de
NADH'H+ ont été réalisées grâce
à un spectrophotomètre intégré à l'automate.
Les résultats du dosage des transaminases sont déduits et
imprimés par l'automate.
Tableau I : Les réactifs du dosage de l'aspartate
aminotransférase (ASAT).
|
Réactif R1 TRISpH7,8 80mmol/l
L-aspartate 200 mmol/l
|
|
Réactif R2 NADH 0,18 mmol/l
Lactate déshydrogénase (LDH) 800 UI/l
Malate déshydrogénase (MD 600 UI/l
á-Cetoglutarate 12 mmol/l
|
TRIS : Trishydroxyméthylaminométhane, NADH
: Nicotinamide Adénine Dinucléotide réduite
Tableau II : Les réactifs du dosage de l'alanine
aminotransférase (ALAT).
|
Réactif R1 TRIS pH 7, 8 100 mmol/l
L-alanine 500 mmol/l
|
|
Réactif R2 NADH 0,18 mmol/l
Lactate déshydrogénase (LDH) 1200 U/l
á-Cetoglutarate 15 mmol/l
|
TRIS : Trishydroxyméthylaminométhane, NADH
: Nicotinamide Adénine Dinucléotide réduite
4.3.3.3. Le Dosage de la créatinine
Principe
La créatinine réagit avec l'acide picrique en
milieu alcalin (NaOH) pour donner un complexe rouge orangée dont la
densité optique est proportionnelle à la quantité de la
créatinine.
La solution de travail a été obtenue par un
mélange à volume égal des réactifs R1 et R2 du kit
Spinreact créatinine (Tableau III). Le mélange est
stable pendant 10 jours à la température du laboratoire (15 et 32
°c).
Ce réactif a été introduit dans l'automate
Lisa 500 plus. La solution de contrôle (sérum de
contrôle) a été ajoutée à l'automate ainsi
que 50 ul de chaque échantillon de sérum à doser.
La calibration de l'automate et le dosage des sérums ont
été ensuite programmés via un microordinateur
intégré au système. La densité optique du complexe
formé au cours de la réaction a
été mesurée par l'automate. Ensuite, la
concentration de la créatinine dans les sérums a
été déduite et imprimée.
Tableau III : Les réactifs du dosage de la
créatinine
Réactif R1: Acide picrique Acide picrique 17,50 mmol/ l
Réactif R2 : Alcaline réagent Hydroxyde de sodium
0,29 mol/l
Créatinine Etalon Créatinine aqueuse 20 mg/l
4.3.3.4. Le dosage des bilirubines (totale et
directe)
Principe
En présence de DMSO (dimethylsulfoxyde), la bilirubine
totale réagit avec l'acide sulfanilique diazoté pour former un
composé coloré.
La bilirubine conjuguée réagit également en
présence de l'acide sulfanilique diazoté mais cette
réaction s'effectue en l'absence de DMSO.
Pour cette réaction le coffret de réactif
Spinreact bilirubine a été utilisé. 1 ml du
réactif R1 et 50 ul du réactif R3 ont été
mélangés pour obtenir le réactif du dosage de la
bilirubine totale (Tableau IV). 100 ul de l'échantillon de sérum
à doser ont été ajoutés à ce volume.
Après 5 minutes à température de 37°C, la lecture de
l'absorbance à 550 nm a été réalisée contre
les blancs échantillons. On en déduit alors la concentration de
la bilirubine totale.
Pour obtenir le réactif de la bilirubine
conjuguée 1ml du réactif R2 et 50 ul du réactif R3 du
coffret Spinreact bilirubine ont été
mélangés dans les racks (Tableau IV). A ce volume 50 ul
d'échantillon de sérum à doser ont été
ajoutés. Après un temps inférieur à 5 minutes
à température de 37°C, la lecture de l'absorbance à
550 nm a été réalisée contre les blancs
échantillons. La concentration de la bilirubine conjuguée a
été alors déduite.
Tableau IV : Réactifs de dosage des
bilirubines
|
Flacon R1 Bilirubine totale Acide sulfanilique 30 mol/l
DMSO 7 mol/l
Acide chlorhydrique 130 mmol/l
|
|
Flacon R2 Bilirubine directe Acide sulfanilique 30 mmol/l
Acide chlorhydrique 130 mmol/l
|
Flacon R3 Nitrite Nitrite de sodium 0,78 mmol/l
DMSO Dimethylsulfoxyde
4.4. Les Phytomédicaments impliqués dans
l'étude.
Les phytomédicaments impliqués dans cette
étude sont deux produits du centre CPHYSAM Tobacoak's et Tob F6.
Tobacoak's est une alcoolature dilué à 1/ 40 de
couleur verdâtre qui est indiqué contre les infections
microbiennes et virales selon le Promoteur. Cent (100) ml trois fois par jours
est la posologie retenue pendant 4 mois pour un adulte.
Tob F6 une infusion de couleur rouge terreuse, un additif
indiqué contre les troubles hépatiques selon le promoteur. Cent
(100) ml trois fois par jour pendant 4 mois constitue la posologie pour un
adulte.
5. Traitement des donnés
La répartition des phytothérapeutes suivant les
différents critères et l'évolution des moyennes des
paramètres biochimiques ont été fait grâce au
logiciel EXCEL 2007 de Microsoft.
III-RÉSULTATS
III-RÉSULTATS
1. Les phytothérapeutes identifiés
Au cours de notre enquête nous avons eu au total
à interroger 31 phytothérapeutes dont 5 dans la ville de
Lomé, 5 dans la ville de Kpalimé, 5 dans la ville de
Sokodé, 7 dans la ville de Tchamba et 9 dans la préfecture de
Tchaoudjo.
1.1. La formation des phytothérapeutes
Les phytothérapeutes ont acquis leurs savoirs des
plantes médicinales soit grâce à leur formation dans les
centres spécialisés en phytothérapie ou soit en
apprentissage auprès de leurs parents guérisseurs traditionnels ;
pour ceux-ci la connaissance des plantes médicinales a d'abord
été transmise puis se sont ajoutées des connaissances et
expériences personnelles. Au cours de notre enquête nous avons
constaté que :
- 84% des phytothérapeutes viennent d'une famille de
guérisseurs traditionnels; - 13% ont été formés
dans des centres de phytothérapie;
- 3% d'entre eux affirment détenir leurs connaissances sur
les plantes médicinales grâce à des
révélations de songes.
Majoritairement de sexe masculin ils exercent tous depuis une
période relativement longue (Tableau V).
Tableau V : Répartition des
Phytothérapeutes en fonction de leurs expériences
professionnelles et de leur sexe.
|
Temps d'exercice (année)
|
Hommes
|
Femmes
|
|
[0 - 10]
|
05 (16%)
|
02(6%)
|
|
[10 -20]
|
16 (51%)
|
01(3%)
|
|
[20 -30]
|
04 (13%)
|
0
|
|
Plus de 30 ans
|
03 (9%)
|
0
|
1.2. Organisation des phytothérapeutes
Les phytothérapeutes sont organisés en
association. Dans ces associations ils discutent de toutes les questions les
concernant. 87% de ceux qui ont été interrogés
appartiennent à une association nationale ou régionale de
phytothérapeutes.
Une collaboration dans le travail existe et se fait par
affinité. Il s'agit de quelques échanges d'idées et des
transferts de patients vers un spécialiste reconnu dans le traitement
d'une pathologie bien précise. Cette collaboration
concerne 55% des phytothérapeutes interrogés.
Aussi faut-il remarquer que :
- 81% des phytothérapeutes ont des assistants qui les
aident dans la recherche des plantes et dans la préparation des
phytomédicaments;
- 84% d'entre eux ont parfois recourt aux agents de la
santé pour diverses raisons (analyses biomédicales, informations,
transferts de patients).
1.3. Les principales maladies traitées.
Les phytothérapeutes interrogés bien
qu'étant des spécialistes reconnus dans le traitement de
l'hépatite interviennent également dans d'autres pathologies. Le
tableau VI présente la fréquence des maladies les plus
abordées par les phytothérapeutes.
Tableau VI : Autres maladies traitées par les
phytothérapeutes spécialistes de l'hépatite
virale.
Maladies Phytothérapeutes Pourcentage
spécialistes.
Hémorroïdes 10 32%
Paludisme 09 29%
Stérilités féminine et 06
19%
masculine
Morsures de serpent 06 19%
Drépanocytose 06 19%
Troubles cardio-vasculaires 05 16%
1.4. Diagnostic de l'hépatite virale.
La majorité des phytothérapeutes posent le
diagnostic grâce à l'observation des signes cliniques (74%). Mais
26% d'entre eux réclament des analyses biomédicales en
confirmation des signes cliniques. Divers signes cliniques ont
été évoqués le Tableau VII présente la
fréquence des principaux signes cliniques servant à identifier
l'hépatite virale.
Tableau VII : Les Principaux signes cliniques
évoqués pour reconnaître l'hépatite
virale.
Signe clinique Citation Pourcentage
Jaunisse 31 100%
Anorexie 24 77%
Fièvres 11 35%
Douleurs au foie 07 22%
1.5. Traitement
1.5.1. Durée du traitement
La durée du traitement varie d'un phytothérapeute
à l'autre de quelques semaines chez certains elle va jusqu'à
plusieurs années chez d'autres (Tableau VIII).
Tableau VIII : Variation de la durée du
traitement en fonction des
|
phytothérapeutes
|
|
|
|
Durée du traitement
|
Nombre de phytothérapeute
|
Pourcentage
|
|
[1 mois]
|
09
|
29%
|
|
[2 mois]
|
06
|
19%
|
|
[3 mois]
|
05
|
16%
|
|
[3 mois à 6 mois]
|
02
|
06%
|
|
[6 mois à 1 an]
|
05
|
16%
|
|
[plus de 1 an]
|
04
|
13%
|
1.5.2. Posologie et péremption
Il existe des doses pour enfant et pour adulte chez tous les
phytothérapeutes. Ces doses sont basées sur les
expériences personnelles et sur les connaissances acquises lors de leur
formation.
Les dates de péremption sont très variables.
Elles dépendent des formes galéniques, 48% des
phytothérapeutes interrogés ont une date de péremption
précise. Les 52% restant observent l'état du produit avant de
conclure sur sa péremption.
1.5.3. Effets secondaires
58% des phytothérapeutes ont avoués avoir
observé des effets secondaires chez leurs patients suite à
l'administration de leurs produits.
Le Tableau IX présente les effets secondaires
évoqués.
Tableau IX : Les effets secondaires évoqués
par les phytothérapeutes.
Effet Secondaire Citation Pourcentage
Fatigue physique et 12 38%
somnolence
Diarrhée 04 13%
Vomissement 03 9.6%
Allergie cutanée 03 9,6%
Anémie 02 6,4%
1.6. Le coût du traitement de l'hépatite
chez les phytothérapeutes.
Le coût des traitements varie d'un
phytothérapeute à l'autre et dépend de la durée du
traitement. 84% des phytothérapeutes se sont prononcés sur le
coût de leur traitement. Ainsi donc trois d'entre eux reçoivent
des dons en nature (animaux domestiques, provisions) en échange de leur
traitement et 74% des phytothérapeutes perçoivent de l'argent
pour leur traitement. Le Tableau X traduit l'estimation des coûts de
prestation des phytothérapeutes en ce qui concerne l'hépatite
virale.
Tableau X : Les Coûts mensuels des traitements de
l'hépatite virale par les phytothérapeutes.
|
Coût mensuel du traitement des
phytothérapeutes (Franc cfa)
|
Nombre de Phytothérapeute
|
|
[= 5.000]
|
5
|
|
[5.000 à 10.000]
|
6
|
|
[10.000 à 15.000]
|
1
|
|
[20.000 à 25.000]
|
2
|
|
[25.000 à 30.000]
|
2
|
|
[35.000 à 40.000]
|
2
|
|
[50.000 à 60.000]
|
2
|
|
100.000
|
2
|
|
150.000
|
1
|
2. Evolution des paramètres biologiques au cours du
traitement.
2.1. Les Patients
Au cours de notre étude 13 patients ayant
l'antigène HBs dans leur sérum ont été reçus
parmi eux quatre personnes ont développés une infection chronique
active du VHB. Nous avons également recruté un témoin
normal.
2.2. Age et Sexe des patients.
Le Tableau XI montre l'âge et le sexe des patients retenus
pour cette étude.
Tableau XI : Age et sexe des patients
Patient Age Sexe
Patient 1 (témoin) 50 ans Masculin
Patient 2 42 ans Masculin
Patient 3 41 ans Masculin
Patient 4 28 ans Féminin
Patient 5 20 ans Masculin
*Age moyenne = 36,2 ans *Sex-ratio = 4
2.2.1. Antécédents des patients
Le Tableau XII décrit les antécédents en ce
qui concerne les crises d'hépatite aiguë chez les patients.
Tableau XII : Antécédents des malades et du
témoin
|
Patient Test d'antigène HBs
Antécédent sur une
période de 2 ans
|
Patient n°1 (Témoin) Négatif
Aucun
|
Patient n°2 Positif depuis 22 mois 2 Crises
d'hépatite aiguë 1 en
et confirmé 2006 et 1 en 2007
|
Patient n°3 Positif depuis 15 mois
Ictère, hépatite aiguë en 2006
et confirmé
|
Patient n°4 Positif depuis 08 mois Aucun
et confirmé
|
Patient n°5 Positif depuis 18 mois
Ictère, hépatite aiguë 2006
et confirmé
2.3. Evolution des paramètres biochimique
2.3.1. Evolution de la teneur des sérums en
Transaminase ALAT
On peut noter une élévation relative des
transaminases d'un patient à l'autre au début (121 à 41
UI/L). Après un mois de traitement on note la diminution des ALAT chez
tous les patients sauf pour le témoin (Tableau XIII). Après deux
mois de traitement, les valeurs des ALAT passent en dessous de 41UI/L chez tous
les patients. On note qu'au troisième mois le patient n° 2
présente une concentration sérique en ALAT de 66 UI/L cette
hausse est confirmée au quatrième mois à 57 UI/L (Tableau
XIII).
Tableau XIII : Evolution de la teneur des sérums
en Transaminase ALAT au cours du traitement.
Transaminase Patient n°1 Patient n°2 Patient
n°3 Patient n°4 Patient n°5
ALAT (UI/L) (témoin)
To 20 121 71 86 41
1 mois 27 104 41 44 32
2 mois 20 37 27 35 28
3 mois 21 66 27 31 26
4 mois 21 57 24 30 39
To = Début de traitement. Transaminases normales =
41 UI/L
2.3.2. Evolution de la teneur des sérums en
Transaminase ASAT
Les teneurs en ASAT sont élevées au début du
traitement ces teneurs baissent relativement après un mois mais restent
toujours supérieures à 41UI/L chez trois patients. Après
deux mois on note une baisse accentuée des ASAT. Un mois plus tard, on
note la normalisation des ASAT sauf chez le patient n°2 où les ASAT
restent élevées à 64 UI/L puis à 51UI/L au
troisième et quatrième mois (Tableau XIV).
Tableau XIV : Evolution de la teneur des sérums en
Transaminase ASAT au cours du traitement.
|
Transaminase ASAT
|
Patient n°1 (témoin)
|
Patient n°2
|
Patient n°3
|
Patient n°4
|
Patient n°5
|
|
To
|
17
|
116
|
77
|
86
|
70
|
|
1mois
|
21
|
107
|
35
|
61
|
56
|
|
2 mois
|
16
|
44
|
37
|
46
|
40
|
|
3 mois
|
19
|
64
|
28
|
39
|
31
|
|
4 mois
|
20
|
51
|
25
|
36
|
29
|
To = Début de traitement. Transaminases normales
=41 UI/L
2.3.3. Evolution de la teneur des sérums en
bilirubine conjuguée
Les valeurs des bilirubines conjuguées dépassent
les 3 mg/l pour tous les patients sauf pour le témoin (Tableau XV).
Après un mois de traitement ces valeurs sont revenues
à la normale chez tous les patients de cette étude.
La valeur de la bilirubine conjuguée est supérieure
à 3mg/l chez seulement le patient n°2 (Tableau XV).
Tableau XV : Evolution de la teneur des sérums en
bilirubine conjuguée
|
Bilirubine conjuguée (mg/l)
|
Patient n°1 (témoin)
|
Patient n°2
|
Patient n°3
|
Patient n°4
|
Patient n°5
|
|
To
|
2
|
8
|
4
|
5
|
4,44
|
|
1mois
|
2,4
|
1.5
|
3
|
3
|
3
|
|
2 mois
|
2,2
|
1,5
|
4
|
2
|
2
|
|
3 mois
|
2
|
3,4
|
3
|
2
|
3
|
|
4 mois
|
2
|
3,2
|
3
|
2
|
2
|
To = Début de traitement. Bilirubine
conjuguée normale entre 1 mg/l à 3 mg/l
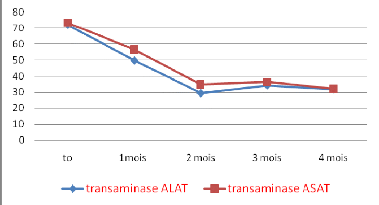
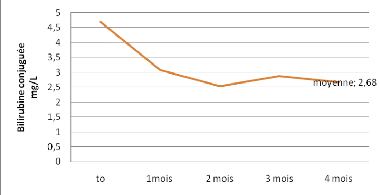
2.3.4. Evolution de la teneur des sérums en
créatinine au cours du traitement.
En début de traitement le taux de créatinine est
inférieur à 13 mg/l.
Ces taux varient légèrement tout au long du
traitement mais restent toujours inférieurs à 13mg/l (Tableau
XVI)
Tableau XVI : Evolution de la teneur des sérums en
créatinine
Créatinine Patient n°1 Patient n°2
Patient n°3 Patient n°4 Patient n°5 (mg/l)
(témoin)
To 8 8 10 10 8
1mois 8 9 10 12 9
2 mois 11 11 11 10 10
3 mois 7 7 11 8 10
4 mois 7 9 11 8 9
To = Début de traitement. Créatinine
normale = 13 mg/i
2.3.5. Evolution de la moyenne de la teneur en
transaminases ASAT et
ALAT.
On note une baisse des moyennes des transaminases au
delà de 41UI/L après deux mois de traitement. Les moyennes sont
restées inférieures à 41 UI/L durant le troisième
et le quatrième mois (Figure 4)
* Valeur normale des Transaminases = 41 UI/L
Figure 4 : Evolutions des moyennes des
transaminases
2.3.6. Evolution de la moyenne de la teneur en bilirubine
conjuguée
La moyenne de la bilirubine conjuguée passe à 3
mg/l chez les patients après 1 mois. Au deuxième mois cette
valeur passe à 2,5 mg/l. Après 3 mois cette valeur remonte
légèrement vers 3 mg/l et après 4 mois elle est à
2,68 mg/l (Figure 5).
* normale de la bilirubine conjuguée comprise entre 1 et
3mg/l.
Figure 5 : Evolution de la moyenne de la bilirubine
conjuguée
2.3.7. Evolution de la moyenne de la teneur en
Créatinine.
La créatinine est inférieure à 9 mg/l en
début de traitement cette valeur passe à 10 mg/l puis à 11
mg/l après deux mois. Après trois mois de traitement cette valeur
est inférieure à 9 mg/l. Au quatrième mois la moyenne des
teneurs en créatinine est de 8,75 mg/l (Figure 6).
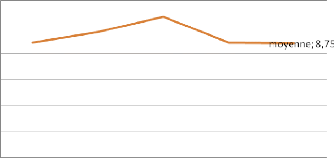
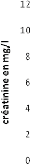
* Valeur normale de la créatinine comprise entre 7 et 13
mg/l.
Figure 6: Evolution de la moyenne de la teneur en
créatinine
2.3.8.Évolution du marqueur virologique :
l'antigène HBe
En début de traitement on note la présence de
l'antigène HBe chez trois patients (Patients n° 2 ; 4 ; 5) et son
absence chez le patient n°3 et le témoin. Après quatre mois
de traitement on observe la persistance de l'antigène HBe chez deux
patients n°2 et n°5 et sa disparition chez le patient n°4
(Tableau XVII)
Tableau XVII : Détection de l'antigène HBe
après 4 mois
|
Marqueur
|
Patient
|
Début
|
Après 4 mois
|
|
Antigène HBe
|
Patient n°1 (Témoin)
|
Négatif
|
Négatif
|
|
Antigène HBe
|
Patient n°2
|
Positif
|
Positif
|
|
Antigène HBe
|
Patient n°3
|
Négatif
|
Négatif
|
|
Antigène HBe
|
Patient n°4
|
Positif
|
Négatif
|
|
Antigène HBe
|
Patient n°5
|
Positif
|
Positif
|
2.3.9.Évolution du marqueur virologique :
l'antigène HBs
L'antigène HBs chez tous les patients est
présent sauf chez le témoin. A la fin du traitement on note la
persistance de l'antigène HBs chez les patients atteints
d'hépatite chronique (Tableau XVIII)
Tableau XVIII : Détection de l'antigène HBs
après 4 mois
|
Marqueur
|
Patient
|
Début
|
Après 4 mois
|
|
Antigène HBs
|
Patient n°1 (Témoin)
|
Négatif
|
Négatif
|
|
Antigène HBs
|
Patient n°2
|
Positif
|
Positif
|
|
Antigène HBs
|
Patient n°3
|
Positif
|
Positif
|
|
Antigène HBs
|
Patient n°4
|
Positif
|
Positif
|
|
Antigène HBs
|
Patient n°5
|
Positif
|
Positif
|
3. Difficultés Rencontrées
Notre étude a souffert du manque de coopération
des phytothérapeutes spécialement ceux de la ville de
Lomé. Nous aurions aimé toucher beaucoup plus de
phytothérapeutes dans la capitale du Togo mais leur réticence
à échanger les informations avec le monde scientifique a
touché significativement l'effectif.
Notre étude a également souffert d'un effectif
réduit en patients atteints d'hépatite chronique active.
IV-DISCUSSION
VI-Discussion
1. Enquête auprès des
phytothérapeutes.
Formation et organisation des
phytothérapeutes.
D'après l'OMS plus de 80% de la population de l'Afrique
subsaharienne a recourt à la médecine traditionnelle et il existe
un tradipraticien pour 200 habitants. Selon le ministère de la
santé du Togo, il existe dans ce pays 9 soignants pour 10.000 habitants
(Kouassi et al., 2007). Il existe donc plus de praticiens de la
médecine traditionnelle que de personnel médical soignant. Les
phytothérapeutes ont été formés par leur propre
famille (84%) ou dans un centre de phytothérapie ceci s'explique par les
réalités historiques et socioculturelles qui soustendent la
pratique de la médecine traditionnelle. La pharmacopée est un
savoir communautaire qui se transmet de génération en
génération par un apprentissage qui se fait au niveau du noyau de
la famille (de père en fils). Aussi faut-il remarquer que les hommes
représentent 90% des phytothérapeutes dans notre enquête,
ceci témoigne de la place accordée aux hommes par rapport aux
femmes dans la transmission de ces savoirs.
La pratique de la phytothérapie est basée sur
des connaissances transmises oralement et sur des expériences
personnelles. Ainsi donc les posologies sont très variables d'un
phytothérapeute à un autre. Elles dépendent
essentiellement de la nature du produit, du stade de la maladie et de
l'âge du patient. Des études de Kerharo et Adam en 1974 d'
Agassounon en 2004 ont trouvé que les doses des phytomédicaments
varient de 1 à 2 cuillérées à café 2
à 3 fois par jour pour les poudres et de 1 à 3 verres 2 à
3 fois par jour pour les décoctions ou les infusions. Notre étude
a recensé des posologies variant entre 1 à 2 verres 2 à 3
fois par jour pour une décoction et 1 à 2
cuillérées à café 2 à 3 fois par jours pour
les poudres. Les dates de péremptions varient d'un
phytothérapeute à un autre. Elles sont établies sur la
base des observations particulières : état physique ; couleur ;
caractéristiques organoleptiques du phytomédicament. Les
principaux effets secondaires cités sont : la fatigue physique et la
somnolence (39%), les diarrhées (13%), les vomissements et les allergies
cutanées (9,6%). Ces résultats confirment ceux de Chan et
al. en 1994 qui rapportent qu'après la prise des
médicaments à base de plantes médicinales, les effets
secondaires généralement présents sont les
diarrhées, les vomissements, des signes neurologiques tels que la
faiblesse généralisée et des signes d'insuffisances
rénales et hépatiques.
2. Approche comparée de la médecine moderne
et de la phytothérapie
traditionnelle
Diagnostic
En médecine conventionnelle il existe les
hépatites toxiques et médicamenteuses, hépatite due
à l'obstruction des voies biliaires, les hépatites virales
aiguës et chroniques. Tous ces hépatopathies sont
décelées à partir d'examens cliniques et d'analyses
biologiques et biochimiques bien précises. La phase aiguë des
différentes formes de la maladie est caractérisée par les
signes ictériques, anorexie, la constipation et des douleurs à
l'hypochondre droit. Pour confirmer une hépatite virale aiguë ou
chronique active il faut mettre en évidence la présence des
marqueurs virologiques (antigènes HBs, HBe). Il convient
également de s'interroger sur le stade de la cytolyse hépatique
par le dosage des transaminases sériques.
Chez les phytothérapeutes, majoritairement (pour 74%)
les seuls signes cliniques servent à établir le diagnostic. Cette
situation est déplorable car les signes cliniques précités
peuvent avoir d'autres origines.
Traitement
En médecine moderne l'hépatite B chronique
active se traite de 6 mois à 1 an voire plus (David et Smuth, 2007). Les
analogues nuléosidiques inhibiteurs de la polymérase du VHB tels
que la lamivudine ou l'adevovir dipivoxil associés à une cytokine
du système immunitaire (l'interféron alpha) sont les
molécules couramment utilisées. Cependant leur efficacité
est limitée en raison des effets secondaires et des rechutes
fréquentes.
D'après notre enquête la durée du
traitement de l'hépatite virale varie d'une semaine à 3 ans, avec
plus de 68% des phytothérapeutes traitant la maladie en moins de 4 mois.
Ce délai est trop court pour espérer une réponse
virologique durable. Cependant, il faut remarquer qu'une partie des
phytothérapeutes semble connaître les différentes formes de
la maladie. La preuve est donnée par la variabilité des
traitements et de leur durée en fonction des cas. Le traitement de
certains phytothérapeutes s'étend sur plus d'un an.
Le coût mensuel moyen du traitement de l'hépatite
virale par les phytothérapeutes s'élève à 23040
FCFA d'après les données de l'enquête. Un traitement
mensuel de l'hépatite B chronique sans les frais de consultation, par
l'interféron alpha associé à la lamivudine coûte
122.000 FCFA par mois. La pharmacopée ou la médecine
traditionnelle est parfois la seule source de soins de santé
financièrement abordable particulièrement pour les pauvres. C'est
la
même remarque qui a été faite lors d'une
étude sur le traitement du paludisme au Ghana (Ahorlu, 1997).
3. Evolution des paramètres biologiques et
biochimiques.
Cadre d'étude.
Le suivi des paramètres biologiques s'est
déroulé dans un centre spécialisé en
phytothérapie CPHYSAM pour les patients de la ville de Lomé et au
centre hospitalier préfectoral de Kpalimé pour les patients de la
ville de Kpalimé. L'étude de Rajkumar et al. en 2007
s'est déroulée dans les hôpitaux de Chennai, Tamilnadu en
Inde, de même que l'Essai clinique de Kéita en 1995 s'est
déroulé à l'hôpital de Bamako au Mali. Nous avons
mené une étude prospective en 3 mois puis le contrôle des
paramètres biologiques en 4 mois ce qui explique en partie la taille
réduit de notre échantillon. Contrairement les travaux de
Rajkumar et al. en 2007 ont enrôlé pour une durée
de 10 mois 25 patients, et ceux de Keita en 1995 qui sur une période de
1 an ont enrôlés 47 patients. Par ailleurs notre étude non
subventionnée est limitée. Elle ne pouvait prendre en charge
qu'un effectif réduit de patients pour les explorations biologiques.
Caractéristiques du Phytomédicament
Tobacoak's
Tobacoak's a fait l'objet d'étude in vitro sur
sa cytotoxicité, sur ses propriétés antimicrobiennes et
antivirales (de Souza et al., 1998) et sur le coeur isolé, le
duodénum, la respiration et la pression artérielle chez le lapin
(Okou-obou et Guede-Guina, 1999). Dans l'étude de Rajkumar et
al. en 2007 sur les capsules HD-03/ES indiquées contre
l'hépatite B chronique active et élaborées à partir
de plantes médicinales de l'Inde. Sur HD-03/ES il a été
réalisé des tests de toxicité aiguë et subaiguë
ainsi que les tests d'activités antivirales. Pour l'étude de
Kéita en 1995, les extraits de Desmodium adscendens ont fait
l'objet de test de toxicité aiguë chez le rat, test
hépato-protecteur et le test de micronoyau sur la souris. Notre
série comporte 4 malades et un témoin contrairement à
l'étude de Rajkumar et al en 2007 qui ne comporte pas de
témoin. Mais en ce qui concerne les malades les deux études ont
distinctement sélectionné les patients atteints d'une
hépatite B chronique active sans antécédent d'une
co-infection virale et dont les limites d'âge sont comprises entre 18 et
60 ans.
On peut également souligner que les deux études
ont éliminé les cas de complications cardio-vasculaires et
rénales, les troubles mentaux et les personnes sous un autre antiviral.
Comme lors des études de Rajkumar et al. en 2007 et de
Kéita en 1995, un dosage mensuel du taux des transaminases (ASAT, ALAT)
et de la bilirubine dans les sérums des patients a été
effectué. Le dosage de la créatinine a
été aussi réalisé pour évaluer la
toxicité des phytomédicaments sur le rein.
Les transaminases ALAT et ASAT
Le but du traitement de l'hépatite chronique active est
la normalisation des transaminases, l'arrêt de la réplication
virale et le rétablissement du foie du point de vue histologique (David
et Smuth, 2004). En ce qui concerne la normalisation des transaminases, signe
qui marque l'arrêt de la cytolyse, nous pouvons dire que le but est
atteint. Car nous pouvons constater qu'après deux mois, trois patients
sur les quatre ont eu la normalisation de leurs transaminases sériques
c'est-à-dire un taux en transaminases ALAT et ASAT inférieur
à 41 UI/L. Les transaminases ALAT sont passées de 71.8#177; 25.36
UI/L à 31.8#177;10.28 UI/L après les 4 mois. Les
phytomédicaments ont donc eu un effet positif sur le
rétablissement général du foie. Chez le patient n°2,
on note qu'après la baisse des transaminases au deuxième mois une
hausse est survenue au troisième et au quatrième mois. On
pourrait penser dans ce cas que le traitement n'est pas encore arrivé
à bloquer totalement la cytolyse hépatique. Seul un dosage de la
charge virale pourra nous permettre de tirer des conclusions plus
précises sur l'effet des phytomédicaments sur ce patient.
L'étude de Keita au Mali sur les 47 cas
d'hépatite chronique a connu la normalisation des transaminases
sériques chez 22 patients après 45 jours de traitement. Dans
l'étude de Rajkumar et al. en 2007 nous avons constaté
également la normalisation des transaminases sériques dans 14 cas
sur 25 patients. Dans cette étude la teneur en transaminases ALAT passe
de 66.5 #177; 11.1UI/L à 39.1 #177; 5.2UI/L en 6 mois.
Dans les travaux publiés par Dusheiko et Antonakopoulos
en 2007, il a été reporté qu'un essai thérapeutique
à la lamivudine sur 60 patients a connu la normalisation des
transaminases de 56% des patients après un an de traitement.
La normalisation des transaminases est une étape
importante vers la guérison. Elle est suivie d'abord d'une importante
baisse de la charge virale et parfois de l'absence de détection des
antigènes HBe, HBs. On peut constater que dans notre étude elle
est survenue dans un délai de deux mois. Ce délai est plus court
comparé à celui reporté lors des essais de Rajkumar et
al. en 2007 et de Dusheiko et Antonakopoulos en 2007 mais plus long
que celui de l'étude de Keita en 1995 qui est de 45 jours.
Evolution de la bilirubine conjuguée
Au cours de notre étude nous avons constaté une
diminution de la teneur des sérums en bilirubine conjuguée de
4.68#177; 0.96 mg/l à 2.68#177; 0.63 mg/l après les 4 mois de
traitement. Comme dans l'étude de Kéita en 1995 et dans
l'étude de Rajkumar et al. en 2007, la
diminution de la teneur en bilirubine conjuguée marque
la fin de l'ictère chez le patient. Au cours des hépatites
virales la bilirubine conjuguée reflux dans le sang (Odou, 2006). Dans
l'étude de Rajkumar et al. en 2007, la teneur en bilirubine
conjuguée passe de 1.3 #177; 0.6mg/l à 1.2 #177; 0.5mg/l en
quatre mois de traitement et de 1.2 #177; 0.5mg/l à 1.1 #177; 0.5mg/l en
six mois de traitement.
Evolution de la teneur en créatinine
La concentration de la créatinine dans le sang
dépend de la capacité d'élimination du rein et de la masse
musculaire. Son évaluation permet d'apprécier un
dysfonctionnement de la filtration rénale. Au cours de notre
étude nous avons constaté une variation de la teneur en
créatinine de 8.8#177;0.96 mg/l à 9#177;1.2 mg/l après 4
mois. Ces taux restent nettement inférieurs à 13 mg/l chez tous
les patients. Ces résultats ne montrent aucun dysfonctionnement des
reins suite à l'administration des phytomédicaments sur la
période de 4 mois. Par contre, l'essai de Hadziyannis et al. en
2006 sur les patients d'hépatite B chronique évoque une
augmentation significative de la teneur en créatinine chez 3% des
patients au cours d'un essai thérapeutique randomisé à
l'Adénovir dipivoxil sur 186 patients.
L'antigène HBe
Après 4 mois de traitement l'antigène HBe a
été retrouvé chez les patients n°5 et n°2 ceci
montre que le virus demeure actif. Par contre chez le patient n°4, on note
la disparition de l'antigène HBe ceci pourrait être dû
à l'arrêt de la réplication du virus. L'antigène HBe
étant l'antigène caractérisant la réplication
virale. Chez le patient n°3 on note l'absence de l'antigène HBe en
début de traitement nous pourrions penser qu'il s'agit d'un cas
d'hépatite B chronique active à antigène HBe
négatif.
L'antigène HBs
L'antigène HBs a été retrouvé chez
tous les patients après les quatre mois de traitement. Ce
résultat était prévisible quelque soit l'efficacité
du traitement on ne pourrait s'attendre à une disparition de
l'antigène de surface du virus en 4 mois. Dans le traitement de
l'hépatite chronique active. On définit la réponse
virologique complète comme l'absence soutenue de l'AgHBs. Cela se
produit chez une minorité de patients après quelques
années. On doit donc recourir à d'autres critères pour
définir la réussite du traitement (réponse virologique
partielle). Ces critères sont :
- Normalisation des transaminases sériques ;
- Séroconversion AgHBe (statut AgHBe positif à
statut anti-HBe positif) ;
- Réduction marquée de l'ADN du VHB avec la charge
virale du VHB inférieure à 105 copies/ml (Thomson et
al., 2005).
CONCLUSION
ET
RECOMMANDATIONS
V-1. Conclusion
Au cours de notre étude nous avons mené d'une
part une enquête auprès de 31 phytothérapeutes des villes
de Lomé, de Kpalimé, de Sokodé, et dans les
préfectures de Tchaoudjo et de Tchamba. Les résultats de nos
enquêtes nous permettent de faire les observations suivantes :
La majorité des phytothérapeutes
interrogés (74%) pose directement le diagnostic de l'hépatite B
chronique active en observant les signes cliniques tels que : la jaunisse, la
constipation, la fièvre, les douleurs au foie. Le temps accordé
au traitement de l'hépatite B chronique active par 68% des
phytothérapeutes est court (inférieure à 4 mois)
comparativement à la durée du traitement par la médecine
moderne (6 mois à 1 ans voire plus). Les phytothérapeutes
interrogés observent des effets secondaires lors du traitement de
l'hépatite tels que : faiblesse physique (38%) diarrhée (13%),
vomissement et allergie cutanée (9.6%). Le coût mensuel du
traitement de l'hépatite par les phytothérapeutes est en moyenne
de 23040 FCFA et est plus faible comparé à celui des
médicaments modernes achetés à la pharmacie qui est de
122.000 FCFA.
En ce qui concerne l'évolution des paramètres
biologiques et biochimiques des patients traités par les
phytomédicaments, il est important de souligner qu'après 4 mois
de traitement on observe : La normalisation des transaminases ASAT et ALAT chez
trois des quatre patients. Ce qui prouve l'arrêt de la cytolyse
hépatique et témoigne de l'effet bénéfique des
phytomédicaments utilisés sur l'évolution de la maladie.
La normalisation du taux de la bilirubine conjuguée chez trois patients
sur les quatre. La valeur de la créatinine reste normale chez tous les
patients.
La disparition de l'antigène HBe chez un patient sur les
trois patients à HBe positif signant existence d'une réponse
virologique liée au traitement.
V-2. Recommandations et Perspectives
VA l'endroit des autorités sanitaires et
scientifiques
- Organiser des formations à l'intention des
phytothérapeutes en vue de les amener à comprendre les
différents aspects et origines des hépatopathies et les
dispositions à prendre pour un traitement plus efficace ;
- Doter les laboratoires du Réseau Ouest-africain de
Biotechnologies de matériels de dosage de tous les marqueurs du virus de
l'hépatite B ;
- Doter les laboratoires du Réseau Ouest-africain de
Biotechnologies de matériels servant à la quantification de la
charge virale du VHB ;
- Évaluer la toxicité chronique des
phytomédicaments ayant fait l'objet de cette étude ;
- Évaluer la charge virale des patients traités par
les phytomédicaments au cours de cette étude ;
- Effectuer le screening des phytomédicaments afin de
déterminer les grands groupes chimiques probablement responsables de
l'effet des Phytomédicaments utilisés.
VA l'endroit des phytothérapeutes
- S'informer auprès du personnel médical sur les
examens et analyses biomédicales nécessaires pour diagnostiquer
les différentes formes d'hépatopathies.
RÉFÉRENCES
BIBLIOGRAPHIQUES
VI-RÉFÉRENCES BIBLIOGRAPHIQUES
ABEL K., ALEGRIA-HARTMAN M. J., 2002. The
relationship between simian immunodeficiency virus RNA levels and the mRNA
levels of alpha/beta interferon's IFN reviews of anti-infection
agents. J. Med. Virol. 76:8433-45.
AGASSOUNON D. T. M., 2004. Évaluation
de la qualité hygiénique : Etude phytochimique et pharmacologique
de quelques plantes de la médecine traditionnelle béninoise.
Thèse de doctorat, Université de Lomé, Togo, pp 178
AHORLU C. K., 1997. Malaria-related beliefs
and behaviour in southern Ghana. In implications for treatment, prevention and
control. Tropical Medicine and International Health, Accra, Ghana,
2 (5), pp 488-490.
ALLAIN J. P., OWUSU-OFORI A., 2006. Approaches
to hepatitis safety in sub-Saharan Africa, Journal compilation. Blackwell
Publishing Ltd. ISBT Science Series 31, pp 48.
ASSOCIATION MEDICALE CANADIENNE, 2004. Grand
public, Maladies Hépatite A et B, Amc.ca. Consulté en Avril 2008
sur Internet.
http://www.cma.ca.
BAGNY A., 2007. Profil étiologique des
hépatopathies cytolytiques, thèse de médecine,
Université de Lomé, Togo, pp 77.
BENHAMOU J. P., ERLINGER S., 1995. Notion
d'anatomie, d'histologie et de physiologie hépatique. In : Maladies du
foie des voies biliaires ; Paris, France, 3ème édition
Flammarion, pp 6-7.
BERTRODE E., 1997. Hépatites virales :
Dépistage, Prévention, Traitement, Expertise Collective Inserm
45 (28), Paris, France, pp 12-21.
BRECHOT C., POL S., 1993. Hépatites
virales, édition Estem sciences en marche, Paris, France, pp
20-47.
CHAN T. Y. K., TOMLISON B., TSE L. K. K., 1994.
Aconitine Poisoning due to Chinese herbal medicines, A review. Veg. et Hum
Toxicol 36: pp 452.
DASHIKI B. G., DIBISCEGLIE A., 2001.
Recombinant leukocyte interferon treatment of chronic hepatitis B. Hepatology.
Samuel CE. Antiviral actions of interferon's. Clin. Microbiol. Rev.;
14:778-809.
DAVID M., SMUTH A., 2004. Treatments for
Hepatitis B, Division of Infectious Diseases. Otho Diesem Co
(45), California, USA, pp745.
DUPEYRON C., 2001, Biologie de l'hépatite
B: Diagnostic et suivi de l'évolution, Edition Estem Sciences en marche,
Creteil France, pp 78-86.
DUSHEIKO G., ANTONAKOPOULOS N., 2007. Current
Treatment of Hepatitis: Recent advances in clinical practice,
57 :105-124; disponible sur internet :
http://gut.bmj.com/cgi/content/full/57/1/105.
EUGENE L., COSTENTIN S., 2004. Les
hépatites virales, 2ème édition Masson, France, pp
12-18.
FREXINOS J., BUSCAIL L., 2003. Rappels .In :
Hépato-gastro-enterologie, proctologie pour le praticien ; 5eme
édition Masson, Paris France, pp 437-443.
HADZIYANNIS S. J., TASSOPOULOS N. C., HEATHCOTE E.
J., 2006. Long term therapy with adefovir dipivoxil for HBeAg-negative
chronic hepatitis B for up to 5 years. Gastroenterology Rew.
131:1743-51.
HOBBS C., 1986. Natural Liver Therapy,
Botanica Press (85) 5:55. California, USA
GEORGE A., KEPOYER A., 2008. Free encyclopedia
wikipedia; image: hepatitis b virus v2, consulté sur
Internet.
http//:en.wikipedia.org/wiki/image:Hepatitis_B_virus_v2.png
GRONGNET J., 2008. Santé : Les
Analyses médicales, Doctissimo. Consulté sur Internet.
http://www.doctissimo.fr/html/sante/analyses/ana_equil_ions06.htm
GELBKE D., 2008. Le Foie In :
Encyclopédie Vulgaris-Médical online, Consulté sur
Internet.
http://www.vulgaris-medical.com/encyclopedie/foie-1947.htm.
KABORE I. Z., GUISSOU P., SOURABIE S., GNANGAO
G., 1998. Elément de monographie sur Nauclea latifolia
(Rubiaceae) chimie, activités biologiques, toxicité. Pharma.
med. trad. Afr. 10 : 42-54.
KEITA A., 1995. Protocole et essais cliniques
sur le Desmodium adscendens. Traditional Medicine Institute - Hospital
of Bamako, Mali.
KERHARO J., ADAM J. G., 1974. Pharmacopée
Sénégalaise Traditionnelle, plantes médicinales et
toxiques. Edition Vigot et frères, Paris, France, pp 150-151.
KRAMVIS A., KEW M. C., 2007. Epidemiology of
hepatitis B virus in Africa, its genotypes and clinical associations of
genotypes. Japan Society of hepatology, Hepatology research
37: S9-S19.
KOUASSI K., DJOKE K., OURO-NILE N., BAKUSA
D., 2007. Principaux indicateurs de santé 2006,
Atelier de validation, Division informations statistiques études et
recherches, Ministère de la santé, Lomé Togo, pp 21-36.
MOREIRA T., 2003. L'hépatite B en Afrique
Subsaharienne: Fardeau sanitaire. In Atelier sur Introduction des Nouveaux
Vaccins dans PEV en Afrique francophone; Saly, Sénégal.
OMS, 2000. Aide-mémoire N°204
Révisé, consulté en 2008 sur Internet
http://www.who.int/mediacentre/factsheets/fs204/fr/
OMS, 2002. Stratégie de l'OMS pour la
médecine traditionnelle pour 2002-2005. WHO/EDM/TRM/2002.
Genève Suisse, pp 26-30.
OMS, 2004. Relevé
épidémiologique hebdomadaire, Le point sur les
épidémies. No. 28, 79, 253-264.
OKOU OBOU C., GUEDE GUINA F., 1999.
Évaluation de la bioactivité de Tobacoak's, une substance
végétale utilisée dans le traitement des infections
à VIH. DEA de Pharmacodynamie Biochimie; Université de Cocody
Abidjan, Cote d'Ivoire, pp 70.
OTT M, THYAGARAJAN S. P., GUPTA S., 1997.
Phyllanthus amarus suppresses hepatitis B virus by interrupting
interaction between HBV enhancer I and cellular transcription factors, Eur.
J. Glin. Invest., 27(11), 908-915.
PERREZ A., 2007. Le virus de
l'hépatite B, Les particules virales hépatite aiguë B:
Evolution sérologique. Evolution schématique des infections HBV.
Consulté sur Internet. http : //
www.educ.necker.fr/cours/poly/hepatologie/Le_virus_de_l_h_patite_B.htm
RAJKUMAR J. S., SEKAR M. G., MITRA S. K.,
2007. Safety and efficacy of oral HD03/ES given for six months in patients with
chronic hepatitis B virus infection, World Journal of Gastroenterology;
13(30): 4103-4107.
ROCHINET A., MEREVET J. P., 2008. Free
encyclopedia Wikipedia: Géographie du Togo, consulté sur
Internet.
http//:en.wikipedia.org/wiki/Togo/Politique_villes_principales_html
SIMPORE J., GRANATA M., BERE A., SANTARELLI R.,
COLUZZI M., 2004. Prevalence of infection by HHV-8, HIV, HCV and HBV
among pregment women in Burkina Faso. J. of Clin. Virol.
31:1 (2004) 78-80.
de SOUZA C., TOUDJI BANDJE C., KOUMAGLO K., KABORE
I.Z., GBEASSOR M., 1998. Évaluation des activités
antibactérienne, antifongiques, antivirales et cytotoxiques in vitro de
Tobacoak's. In Séminaire International sur le Bilan et les Perspectives
dans le Traitement du VIH/ SIDA Ouagadougou. Burkina Faso.
THE NATURAL PHARMACIST, 1999. Natural Product
Encyclopedia, Conditions Viral Hepatitis. consulter sur Internet:
http://
www.consumerlab.com
THOMSON A. B. R., SHAFFER E. A., PARÉ P., ADAMS
P. C., BAIK S. K., BAIN N., GROVER P. T., HEATHCOTE J., KICHIAN G., LEE S. S.,
LEVY G. A., 2005. Principes fondamentaux de gastro-entérologie:
États pathologiques et démarches thérapeutiques;
Janssen-Ortho Inc, 5ème édition. Vancouver, Canada, pp
615-626.
TREPO C., MERLE P., ZOULIM F, 2006.
Hépatites virales B et C, Pathologies Sciences. Paris, France,
pp126-145.
VOCHELLE V., TRÉPO C., MERLE P., 2007.
Treatment of chronic viral hepatitis, Biol. and Gastro. Rev.
16:618-625.
WHO, 2004. Geographic pattern of hepatitis B
prevalence, Department of immunization, Vaccines and Biologicals (IVB).
WHO/CCT/PTD/2004, Geneva Switzerland.
VI-ANNEXES
Annexe I : Fiche d'Enquête destinée aux
phytothérapeutes spécialisés dans le traitement des
hépatites virales au TOGO
N° /.. Date / /
I- Identification du phytothérapeute
1) Nom 2) Prénoms
3) Date et Lieu de Naissance
4)
Sexe: Masculin
Féminin
5) Situation Matrimoniale
Marié(e) Divorcé(e)
Célibataire
6) Nationalité ... 7) Ethnie
8) Nom du centre
9) Adresse (ville, quartier, boîte
postale)
Tel
II- Méthodologie de Travail
10) Depuis combien d'années exercez-vous ce
métier?
11) Comment avez-vous acquis vos savoirs?
12) Appartenez-vous à une association des
phytothérapeutes ? OUI NON
Si Oui
Laquelle?
13) Quelles sont les principales maladies que vous
traitez dans votre centre?
14) Comment nomme-t-on l'hépatite dans votre
langue?
15) Combien de traitements disposez-vous contre les
hépatites ?
16) Comment Diagnostiquez-vous les
Hépatites?
17) Quels sont les médicaments que vous proposez
contre les Hépatites?
18) Sous quelle(s) forme(s) se présentent produits
contre les hépatites? Décoction
Macération Gélule

Alcoolature Pommade ou lotion calcinât
Poudre Autres, Préciser
19) Vos produits sont t'ils élaborés
uniquement à partir de plantes ? OUI NON
Si NON les mélangés vous avec
:
Des organes ou partie d'animaux Des
éléments Minéraux
Autres, Préciser
20) Avez-vous des contre-indications sur ces produits
?
Si OUI, Préciser
21) Pendant combien de temps dure votre
traitement?
22) Donnez-vous les mêmes produits à tous
vos cas d'hépatites? OUI NON
Si NON sur quelle(s) base(s) classez-vous vos
malades?
Autres
Signes Cliniques Analyses Médicales
23) Travaillez-vous avec d'autres
phytothérapeutes? OUI NON
Si OUI Lesquels?
En quoi consiste votre
collaboration?
24) Avez-vous une posologie? OUI
NON
Si OUI Laquelle? Comment l'avez-vous
établie?
25) Avez-vous des dates de péremption pour vos
produits? OUI NON
Si OUI Comment les avez-vous
déterminées?
26) Avez-vous un ou des assistant(s)?
OUI NON
Si OUI combien sont-ils et en quoi consistent leurs
tâches?
27) Quelles sont les améliorations que vous
observées au cours du traitement?
28) A partir de quel moment arrêtez-vous le
traitement?
29)
Votre traitement a t-il évolué avec vos
expériences ? OUI NON
Si OUI, Préciser
30) Avez-vous répertoriez les cas
d'hépatites que vous avez eu à traiter au cours de ces 5
dernières années ? OUI NON

Si OUI
Peut-on avoir accès aux donnés dont vous
disposez sur eux ? OUI NON
31)

Avez-vous constaté des cas d'échecs au
cours de vos traitements ? OUI NON
Si OUI, selon vous quelles pourraient
être les causes de ces échecs?
32) Avez-vous constaté des effets secondaires au
cours de vos traitements? OUI NON
Si OUI, citez-les
33) En cas de complication que faites-vous ?
34) A combien estimez-vous le coût d'un traitement
complet dans votre cas ?
35) Collaborez-vous avec les agents de la
santé? OUI NON
Si OUI en quoi consiste votre collaboration?
36) Que leur reprochez-vous ?
37) Qu'attendrez-vous de leur part ?
39) Avez-vous d'autres informations à nous
apporter?
Annexe 2 : Lettre de consentement
Lettre de consentement
Dans le Cadre d'un mémoire de DEA intitulé
Approches méthodologiques des phytothérapeutes du Togo
dans le traitement de l'hépatite virale: Cas d'hépatite B
chronique active soumis à un traitement à base de
phytomédicaments.
Il est initié une étude dont l'objectif est de
suivre l'évolution certains paramètres biologiques sur des
patients souffrant d'hépatite B chronique sous phytothérapie.
Cette étude a pour but de contrôler l'effet des
phytomédicaments utilisés par les patients sur les
paramètres suivants :
Transaminases sériques ALAT et ASAT
Bilirubine
Créatinine
Antigène HBs et Antigène HBe
L'étude est prévue sur une période
située entre trois et six mois.
Il sera donc demandé aux participants d'effectuer un
prélèvement sanguin chaque trente jours jusqu'à la fin de
cette étude auprès des initiateurs.
Les Résultats de cette étude seront transmis aux
patients. Ses résultats serviront à l'étude avec la
garantie d'anonymat sur les participants.
Ayant lu et compris entièrement ce document :
|
J'accepte de participer Je Refuse de participer
à cette Etude à cette Etude
|
|
Nom et Prénoms
Adresse
Signature
Date
Annexe III
RésuméL'hépatite
B est une atteinte inflammatoire du foie consécutive à
l'infection par le VHB. Son traitement en médecine moderne est
très coûteux et reste limité en raison des effets
secondaires très graves, de l'induction des mutants HBV et de la
fréquence élevée des rechutes. En Afrique son taux de
prévalence est supérieur à 8%, dans ce contexte bon nombre
de phytothérapeutes proposent des remèdes contre cette
maladie.
Nos objectifs sont : Recueillir et analyser les données
sur la méthodologie des phytothérapeutes du Togo dans le
traitement de l'hépatite virale; Suivre l'évolution des
paramètres biologiques des patients traités à base de
phytomédicaments. Pour cela une étude prospective a
été menée sur 31 phytothérapeutes des villes de
Lomé, Kpalimé, Sokodé et dans les préfectures de
Tchaoudjo et de Tchamba.
Les Résultats obtenus montrent que : 84% des
phytothérapeutes viennent d'une famille de guérisseurs, 74% des
phytothérapeutes posent le diagnostic de l'hépatite virale par
l'observation des signes cliniques et 68% d'entre eux traitent la maladie en
moins de 4 mois. Parmi les phytothérapeutes 58% observent des effets
secondaires dus à leurs traitements.
En ce qui concerne le suivi des patients, quatre personnes
atteintes d'hépatite B chronique active et un témoin normal ont
été soumis à un traitement par Tobacoak's et
Tob F6 deux phytomédicaments. Après 4 mois les
résultats se présentent comme suit : Normalisation des
transaminases ALAT et ASAT chez trois patients sur les quatre avec la valeur
moyenne des ALAT qui passe de 71.8#177; 25.36 UI/L à 31.8#177;10.28
UI/L. Normalisation de la bilirubine chez trois patients sur les quatre avec la
moyenne de la bilirubine conjuguée qui passe de 4.68#177; 0.96 mg/l
à 2.68#177; 0.63 mg/l. Le taux de créatine est normal. Il passe
de 8.8#177;0.96 mg/l à 9#177;1.2 mg/l, On note la disparition de
l'antigène HBe chez un patient après les 4 mois de traitement. La
normalisation des transaminases et de la bilirubine constatée, la
disparition de l'antigène HBe après 4 mois sont des signes de
l'arrêt de la destruction des cellules hépatiques et
témoignent d'un début d'une réponse virologique efficace
liée au traitement.
Mots clés: Hépatite B chronique,
Phytomédicaments, Médecine Traditionnelle Africaine
Summary
Hepatitis B is an inflammatory damage of the liver due to HBV
infection .it's treatment in modern medicine is too costly and seems to be
limited due to the very unwanted serious effects of the induction of HBV
mutant's and the high frequency of relapses.
In Africa, it's prevailing percentage rate is superior to 8%.
In a such situation many phytotherapists have put forward treatments. Our
purposes are: to gather and process data on phytotherapist methodogy in the
treatment of viral hepatitis.
To follow the progress of biological parameters of patients
cured with herbal medicines. In this context a prospecting survey was done on
31 phytotherapist's of the cities of Lome, Kpalime, Sokode and in the
prefectures of Tchaoudjo and Tchamba. The results prove that 84% of
phytotherapists inherit the healing power from relatives while 74% diagnosis
viral hepatitis through its clinical symptoms and 68% cure this illness in less
than four mouths.
Concerning the medical aftercare, four patients suffering from
active chronic hepatitis B and one normal witness have been subjected to the
treatment of two herbal medicines: Tobacoak's and Tob F6. After four months,
results came out as follow : the normalization of serum ALAT and ASAT of tree
over four patients with the average value of the ALAT which decreases from
71,8#177;25,36 IU/L to 31,8#177;10,28IU/L. The normalization of bilirubin of
tree patients over four with the average of combined bilirubin witch decreases
from 4,68#177;0,96 mg/l to 2,68#177;0,63 mg/l. The creatinin rate is also
normal and goes from 8,8#177;0,96 mg/l up to 9#177;1,2mg/l. In additional there
is disappearance of antigen HBe from one patient.
The normalization of serum ALAT, ASAT, Bilirubin and
disappearance of antigen HBe were the signs of the stoppage of hepatic cells
destruction and give evidence of virological response caused by treatment.
Keywords: Chronic hepatitis B, Herbal medicines,
Traditional African medicine
| 


