Chapitre I
Revue Bibliographique
Quatre parties constituent le contenu du présent
chapitre. La première partie décrit le stockage d'énergie
par chaleur latente de fusion des MCP. La deuxième partie est
consacrée aux différentes réalisations relatives au
refroidissement des composants électroniques par convection
naturelle/forcée. La troisième partie analyse les travaux
théorique et pratique relatifs au refroidissement des composants
électroniques par stockage de l'énergie dans les MCP. Quant
à la quatrième partie, elle décrit la position du
problème.
1.1 Stockage d'énergie par chaleur latente de
fusion des MCP
Le stockage d'énergie thermique dans un MCP s'effectue
sous formes sensible et
latente.
1.1.1 Stockage d'énergie par chaleur sensible
Ce mode de stockage utilise les propriétés
calorifiques d'un corps. La quantité de chaleur (variation d'enthalpie
à pression fixe) stockée dépend alors de la
capacité calorifique du corps, et de l'écart entre sa
température initiale et la température de stockage.
Si on réchauffe (ou on refroidit) un corps de masse, m,
d'une température initiale, T1, à une température finale,
T2, l'énergie stockée est donnée par sa variation
d'enthalpie:
T2
AH = H -H = ~ mc dT (1.1)
2 1 (T)
p
T1
où cp (T) est la chaleur spécifique à
pression constante du corps.
Si la chaleur spécifique peut être
considérée comme constante dans l'intervalle de
températures [T1,T2] alors (cp (T) = c):
AH = m c p (T -T ) (1.2)
2 1
La quantité de chaleur stockée est
proportionnelle à l'écart de température: ce type de
stockage serait intéressant uniquement pour des grands écarts de
température et une chaleur spécifique élevée.
L'expression permet de distinguer deux cas:
si T2 > T1, le corps stocke la chaleur ;
si T2 < T1, le corps stocke le froid.
On utilise des corps ayant des chaleurs spécifiques
importantes comme le cas de l'eau pour les liquides et des lits de pierres pour
les solides.
1.1.2 Stockage d'énergie par chaleur latente de
fusion
A pression constante, la variation d'enthalpie d'un corps est
égale à la quantité de chaleur échangée lors
de la transformation. La chaleur latente de changement de phase d'un corps pur
à la température T est la variation d'enthalpie de celui-ci
passant d'un état (solide, liquide ou gazeux) à un autre. Ainsi,
la variation d'enthalpie du corps pour passer de l'état (1) à
l'état (2) est égale à la quantité de chaleur
échangée sur l'isobare, Figure 1.1.
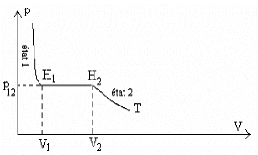
Figure 1.1: Variation d'enthalpie du corps
Le stockage d'énergie par chaleur latente met en jeu
l'énergie due au changement de phase. Soit Tf la température de
changement de phase d'un corps solide pur qui passe de la température
initiale T1 à la température finale T2, avec T1 < Tf < T2.
L'énergie stockée lors de cette transformation est:
T T
f 2
AH= ~ mc (T) dT + m AH + ~ mc
(T) dT (1.3)
p,s f p,l
T T
1 f
où cp,s (T): chaleur spécifique à
pression constante du corps à l'état solide. cp,l (T): chaleur
spécifique à pression constante du corps à l'état
liquide.
A H f : chaleur latente de changement de
phase.
Cette relation comporte deux termes représentant la
chaleur sensible et un terme représentant la chaleur latente, m
A Hf.
Le stockage d'énergie par chaleur latente de fusion est
plus bénéfique comparé à celui par chaleur
sensible. Une quantité importante d'énergie est stockée
lors de la fusion: Par exemple, dans un kilogramme de brique
réfractaire, il est possible de stocker environ 1 kJ pour chaque
degré d'élévation de la température, alors qu'en
faisant fondre un kilogramme de paraffine, environ 250 kJ sont
absorbés.
| 


