|
RÉPUBLIQUE DÉMOCRATIQUE DU
CONGO
ENSEIGNEMENT SUPÉRIEUR ET UNIVERSITAIRE

Institut Supérieur des Techniques Médicales
I. S. T. M. - Kinshasa
B.P. 774 Kinshasa X
EVALUATION DE LA FONCTION HÉPATIQUE DES
PATIENTS SOUMIS AU TRAITEMENT PAR LES TUBERCULOSTATIQUES
(schéma RHZE : Rifampicine-INH-
Pyrazinamide-Ethambutol)
KAKULE MAKOMBANI HENRI
Technicien de laboratoire
Mémoire présenté et
défendu en vue de l'obtention du diplôme de
Licencié en Techniques médicales.
Orientation : Biologie
Médicale
Directeur : Prof NZINGULA
NSENGA
Co-Directeur : Ass. MAKONGA
KABABA
Année Académique : 2007 -
2008
PLAN GENERAL
AVANT-PROPOS
INTRODUCTION
- Objectif général
- Objectifs spécifiques
1ère PARTIE : DONNEES
DE LA LITTERATURE
Chapitre I : LE FOIE ET SES
MALADIES
I.1.
Généralités
I. 2. Les maladies du foie
I. 2. Exploration de la fonction
hépatique
Chap. II : GENERALITES SUR LA
TUBERCULOSE
II.1. Définitions et historique
II.2. Etiologie et infection tuberculeuse
II.3. Le bacille de Koch : culture et isolement
II.4. Epidémiologie de la tuberculose
- dans le monde ;
- en Afrique ;
- en République Démocratique du Congo
Chap. III :
DIAGNOSTIC ET TRAITEMENT DE LA TUBERCULOSE
III.1 Diagnostic
III.1.1. Examens
cliniques
III.1.2. Imagerie
médicale
III.1.3. Examens
biologiques
III.2 Traitement
III.2.1.
Catégorisation
III.2.2. Régime
de traitement
III.2.3.
Conséquence
IIème PARTIE :
PRATIQUE AU LABORATOIRE
CHAP. 4 : MATERIELS ET
METHODES
IV.1 Matériel
IV.1.1 Echantillonnage ;
IV.1.2. Cadre et période
d'étude ;
IV.1.3 Equipement de laboratoire.
IV.2 Méthodes
IV.2.1 choix des méthodes
de dosage ;
IV.2.2. Dosage de ã-GT et
des transaminases ;
IV.2.3. Analyse statistique des
résultats.
Chap. V : RESULTATS &
DISCUSSIONS
V.1 Présentation des
résultats
V.2 Discussion
CONCLUSION
RECOMMANDATIONS
DEDICACE
À l'Eternel Dieu Tout Puissant, qui nous a
comblé de l'intelligence et de la sagesse pour affronter les
difficultés sur cette terre ;
À nos parents, Feu Samuel KAKULE KAHUKA et Mme
Stéphanie KASWERA MBUGHEKI, pour ce qu'ils n'ont jamais cessé
d'être pour nous durant les temps forts de notre formation
scientifique et surtout leur encadrement pour devenir ce que nous sommes,
Nous dédions ce travail.
REMERCIEMENTS
Nous adressons nos sincères remerciements à tous
ceux qui ont, de près ou de loin, contribué à la
réalisation de ce modeste travail ;
Au professeur NZINGULA NSENGA Victor, pour la direction et
l'Assistant MAKONGA KABABA pour l'encadrement pendant la direction de ce
travail ;
Aux Honorables Professeur Abbé Apollinaire MUHOLONGU
et Révérend Pasteur KAKULE MOLO, pour leur soutien spirituel,
matériel et surtout leur encouragement ;
A nos chers frères et Soeurs Bernardin TSONGO
VAYIHEMULA, Emmanuel BARUA, Melchisédech KAMBALE MATITA, Joachim MBULA,
Mamie MATITA, KATEMBO MATITA, Teddy KASONDWA, Pascal MBUSA MULUMBA, Albert
MACHOZI SESETE, Cathy NZIAVAKE, Louis WANGAHEMUKA, Laurent MUSAYI, Pascal MBUSA
MULUMBA, ainsi que tous ceux dont les noms ne sont pas cités, pour leur
inestimable soutien tant moral, matériel, financier que spirituel ;
A notre épouse Mme Christelle MUISA MUHESI, pour son
courage et son optimisme au cours de ces dures années d'études et
son intersubjectivité vraiment réussie que nous ne cessons de
partager ;
Aux couples Pascal KITAMBALA, Fidèle MALIKIDOGO, BOKILO
WANZIRE, Gerry SYAUSWA ainsi qu'aux amis Jean Bosco WALUMONA & Mme MPONDA
ZIPOLE, FEFE BALEKA, Denise LWAYIKONDERA et Lisette BWAKYANAKAZI pour notre
amitié renforçant l'intérêt éducationnel
et scientifique ;
A nos vaillants compagnons de lutte : Aaron KASEREKA
MWATSI, Huguette NDAY KABULO, Jeampy KOMBA, Henriette AKENDA PEMBE, Romaine
KOLA et tant d'autres, pour l'éclat de leurs encouragements.
Que chacun de vous tous trouve ici l'expression de notre
profonde gratitude.
KAKULE MAKOMBANI Henri
AVANT-PROPOS
Vers le début du 20ème siècle,
la tuberculose tuait une personne sur sept en Europe Occidentale. On l'appelait
alors "peste blanche".
Il y a trente (30) ans, la maladie semblait être plus ou
moins contrôlée. L'apparition des résistances aux
antituberculeux, le signalement des cas de plus en plus nombreux dans le monde,
de même qu'une détérioration plus importante de la
situation sanitaire causée par le Sida ont servi des signaux de rappel
pour que l'Organisation Mondiale de la Santé (O.M.S.) déclare en
1993 que la tuberculose constituait une urgence mondiale.
Dès lors, il y a des programmes qui font le suivi du
traitement dans différentes parties du monde.
Le schéma thérapeutique de la tuberculose
recommande l'association de quatre (4) médicaments dont certains
causeraient des perturbations plus ou moins graves dans le fonctionnement
hépatique, étant donné la durée assez longue
qu'exige le traitement.
Ce qui justifie des recherches permanentes visant
l'exploration de cet organe vital dans lesquelles nous nous sommes
engagés avec les difficultés qu'elles comportent.
Devant le scepticisme des malades qui ne font confiance
qu'à leurs médecins, l'irrégularité dans le respect
du schéma de traitement, des difficultés financières
limitant l'acquisition des intrants nécessaires à
l'exécution des manipulations, nous nous sommes dépassés
pour déployer tous les efforts en vue d'atteindre notre objectif.
Nous avons osé et nous croyons être
arrivés.
Nous souhaitons que nos suggestions et recommandations soient
suivies pour l'amélioration de la prise en charge des malades.
INTRODUCTION
1.
Problématique
Depuis un temps, la tuberculose figure sur la liste des
maladies à éradiquer. Dès lors, il y a eu des programmes
qui font le suivi de traitement dans différentes parties du monde.
Le schéma thérapeutique de la tuberculose
recommande l'association de quatre (4) médicaments qui sont : l'INH
(Isoniazide), la Rifampicine, l'Ethambutol (ou la streptomycine) et le
Pyrazinamide. Le traitement dure six à neuf mois.
Parmi les médicaments utilisés dans ce
schéma thérapeutique, la Rifampicine et le Pyrazinamide sont
particulièrement hépatotoxiques surtout à fortes doses.
L'hépatotoxicité de ces produits constitue d'ailleurs l'effet
secondaire le plus redouté dans la chimiothérapie
antituberculeuse avant l'atteinte rénale. Si
l'hépatotoxicité est évidente à fortes doses
(intoxication médicamenteuse aiguë), il n'est pas moins possible
qu'elle survienne à la fin des 6 à 8 mois de traitement.
D'où, il s'avère impérieux de faire un suivi pour
évaluer l'impact de cette association.
Notre étude qui est une exploration, vise à
contrôler l'état fonctionnel du foie pendant la prise des
antituberculeux. Ce contrôle est double : d'une part, nous nous
intéressons à la clairance de métabolisation en
évaluant l'hépato-cytolyse par le dosage des transaminases
sériques et, d'autre part, à l'excrétion biliaire en
évaluant la cholestase par le dosage des
gamma-glutamyl-transférases (ã-GT).
2.
Hypothèse
Au vu des doses thérapeutiques, la littérature
renseigne une élévation des transaminases sériques avec la
Pyrazinamide alors qu'avec la Rifampicine, l'élévation des
transaminases sériques peut être associée à un
ictère qui peut devenir cholestatique.
D'où, faudra-t-il confirmer l'origine de
l'hépatotoxicité : soit c'est une intoxication
médicamenteuse, soit alors une conséquence de la tuberculose
étant donné qu'elle affecte, dans la plupart des cas, le
foie ; mais aussi déterminer si cette hépatite aiguë
constatée manifeste ses effets à titre égal dans la
cytolyse comme dans la cholestase.
3. Objectifs
- Objectif général
L'intérêt de notre travail est de contribuer
à la prise en charge thérapeutique des personnes souffrant de la
tuberculose tenant compte du fait que le schéma thérapeutique est
de 6 à 8 mois.
- Les objectifs spécifiques :
Ø Explorer la fonction hépatique pendant le
traitement antituberculeux par l'évaluation du taux des transaminases et
de la gamma-glutamyl-transférase au début et à la fin du
traitement ;
Ø Localiser les phases cytolytique ou
cholestasique de l'hépatotoxicité ;
4.
Méthodologie
Pour réaliser notre évaluation, la
méthodologie suivante a été suivie :
1) Sélectionner, selon les critères fixés,
des sujets tuberculeux à suivre pendant le traitement par les
antituberculeux ;
2) Prélever des échantillons de sang au
début et au 6ème mois de traitement ;
3) Doser chaque fois sur chaque échantillon les
transaminases et la ã-GT ;
4) Analyser statistiquement des résultats ;
5) Tirer une conclusion.
PREMIERE PARTIE :
DONNEES DE LA LITTERATURE
CHAPITRE I : RAPPEL
ANATOMO-PATHOLOGIQUE DU FOIE
I.1 Anatomie
fonctionnelle du foie
Le foie est un organe essentiel, aux rôles multiples.
Son bon fonctionnement est indispensable à la vie. Il peut être
soumis à de nombreuses agressions. Sa résistance est importante
et malgré ces agressions, il peut longtemps fonctionner sans
qu'aucun trouble ne se manifeste. Cependant, à long terme, des
dégâts irréversibles peuvent se constituer silencieusement.
Il sera alors trop tard, et aucun traitement ne pourra à ce stade
restaurer les fonctions hépatiques. C'est avant qu'il faut agir.
Eliminer la cause d'agression du foie avant que des dommages
irréversibles ne soient installés est la seule façon
d'éviter leur apparition et leurs conséquences.
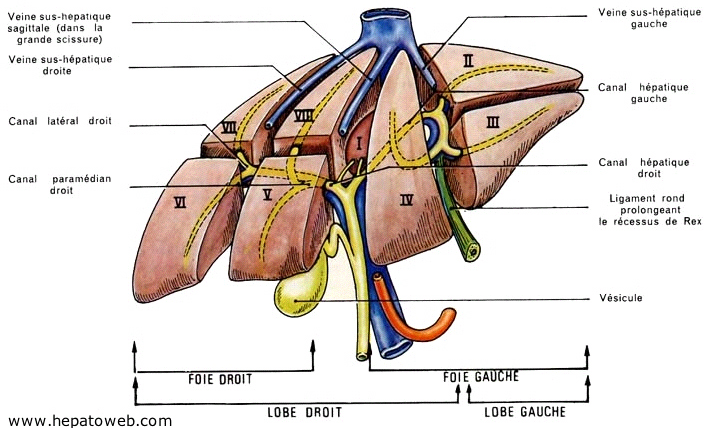
I.2
Physiologie et fonction du foie
Le foie a la particularité de pouvoir se
régénérer, c'est-à-dire que la diminution du
nombre d'hépatocytes due par exemple à leur destruction par une
agression virale ou toxique, ou à l'ablation chirurgicale d'une partie
du foie, sera compensée par la multiplication des cellules
restantes qui vont remplacer les cellules détruites. Le foie peut
être comparé à une usine, ou à un laboratoire, qui a
de multiples fonctions :
Le foie reçoit deux gros
vaisseaux :
- La veine porte qui apporte au foie le sang provenant du tube
digestif où ont été absorbées de
nombreuses substances : Les molécules d'origine alimentaire,
alcool, médicaments pris par voie orale..... ;
- L'artère hépatique qui contient un sang
provenant de l'ensemble de l'organisme, dans lequel circulent de nombreuses
molécules fabriquées par tous les organes, ainsi que les
médicaments administrés par voie intraveineuse.
Après être passé dans le foie, le sang
provenant de la veine porte et de l'artère hépatique passe dans
la veine cave qui le conduit au coeur (partie droite). Il est envoyé
vers les poumons puis revient au coeur (partie gauche). Il est ensuite
propulsé par les artères dans tout l'organisme (cerveau, muscles,
intestins, reins.....), et à nouveau vers le foie par l'artère
hépatique, et le circuit recommence.
La bile est fabriquée par le foie et est conduite
à l'intestin par les voies biliaires.
Les "matières
premières" sont apportées par la veine porte et l'artère
hépatique. Le foie les transforme si nécessaire pour les rendre
utilisables, ou inoffensives. Ces matières premières peuvent
être d'origine extérieure : aliments, alcool,
médicaments..., ou fabriquées par l'organisme : hormones,
bilirubine ...
Le foie est une station
d'épuration
Parmi les substances qui arrivent au foie, certaines sont
toxiques pour l'organisme. Les cellules hépatiques sont capables de les
éliminer dans la bile, ou de les transformer en produits non toxiques
qui passeront dans la circulation générale et seront
éliminées par les reins.
Le foie est une usine de fabrication et un centre
de régulation
Le foie fabrique de très nombreuses protéines
essentielles, comme par exemple celles qui sont indispensables à la
coagulation sanguine (cfr I.3.3).
Le foie intervient dans le métabolisme du glucose, du
cholestérol, du fer et de nombreuses autres substances dont
l'équilibre est indispensable au bon fonctionnement de l'organisme.
Ses multiples fonctions font du foie un organe essentiel au
bon fonctionnement de l'organisme. Du fait de sa place en "première
ligne" vis-à-vis des substances éventuellement toxiques d'origine
alimentaire, il est le premier exposé à cette toxicité.
I.3 Les maladies du
foie
Il existe de nombreuses maladies du foie. Mais les plus
courantes sont : les hépatites et les cirrhoses.
I.3.1 Les hépatites
Les hépatites sont dues à la destruction d'un
nombre plus ou moins important de cellules du foie, pendant une période
plus ou moins longue.
Le responsable de cette destruction est le plus souvent
d'origine extérieure à l'organisme : virus, alcool, certains
médicaments.... plus rarement, les cellules hépatiques sont
altérées par un dérèglement immunitaire.
a. Hépatites aiguës : Une hépatite
aiguë est liée à une agression brutale du foie avec
destruction d'un grand nombre de cellules en peu de temps. Elle peut se
manifester par une jaunisse, une fatigue, des douleurs articulaires, de la
fièvre ; mais elle est le plus souvent silencieuse. Dans la
majorité des cas, l'élimination de l'agent responsable permet la
guérison sans séquelle en moins de six mois. Ces maladies
sont donc le plus souvent bénignes, les réserves
cellulaires étant habituellement suffisantes pour assurer un
fonctionnement satisfaisant du foie, puis sa régénération.
Dans certains cas, heureusement rares, le nombre de cellules
détruites est trop important pour que le foie puisse continuer à
assurer ses fonctions vitales. Il s'agit alors d'une hépatite
fulminante, pouvant être rapidement mortelle.
b. Hépatites chroniques : Si l'agent
responsable n'est pas éliminé au bout de six mois,
l'hépatite devient chronique. Le nombre de cellules hépatiques
détruites tous les jours est modéré, mais la
répétition de ce phénomène pendant des
années peut avoir des conséquences à long terme. Au niveau
microscopique, la vascularisation est perturbée par les réactions
inflammatoires, et de petites zones du foie sont remplacées par un tissu
fibreux, comme celui d'une cicatrice. Avec le temps, cette fibrose devient de
plus en plus importante, et chez certaines personnes, on peut voir se
constituer une cirrhose.
Tableau n° 1 : Caractéristiques des
hépatites A, B, C, D, E et G -1(*)
|
Modes de transmission
|
Symptômes
|
Mesures de protection
|
|
Hépatite A
|
- Transmission, la plupart du temps, par une exposition
à de l'eau contaminée ou à des aliments
préparés avec de l'eau contaminée ;
- Transmission par voie oro-fécale (c'est-à-dire
lorsque des selles contaminées se retrouve dans la bouche d'une personne
à cause d'un mauvais lavage des mains ou que des selles contenant
l'hépatite A contaminent de l'eau qui est ensuite consommée).
|
- Jaunisse (coloration jaune de la peau et des yeux) ;
- Malaises ;
- Perte d'appétit ;
- Maux d'estomac ;
- Urines foncées ;
- Fatigue ;
- La plupart des personnes infectées par l'hépatite
A se rétablissent naturellement.
|
- Vaccin contre l'hépatite A ;
- Se laver les mains adéquatement avant et après
la préparation et la consommation d'aliments
|
|
Hépatite B
|
- Exposition à du sang ou à des organes
contaminés ;
- Relations sexuelles ;
- Transmission de la mère à l'enfant ;
- Partage d'articles personnels avec une personne
infectée (brosse à dents, rasoir, coupe-ongles, aiguille,
matériel pour renifler de la drogue)
|
- Jaunisse ;
- Malaises ;
- Perte d'appétit ;
- Maux d'estomac ;
- Urines foncées ;
- Fatigue ;
- Absence de symptômes possible (au moins 30 % des cas
graves ne présentent aucun symptôme)
|
- Vaccin contre l'hépatite B ;
- Relations sexuelles protégées ;
- Éviter de partager des articles qui peuvent
être contaminés avec du sang (brosse à dents, rasoir,
coupe-ongles, aiguille, matériel pour renifler de la drogue)
|
|
Hépatite C
|
- Exposition à du sang ou à des produits
sanguins contaminés ;
- Transmission de la mère à l'enfant ;
- Relations sexuelles (dans de rares cas) ;
- Partage d'articles personnels avec une personne
infectée (brosse à dents, rasoirs, coupe-ongles, aiguilles,
matériel pour renifler de la drogue)
|
- La majorité des cas ne présentent aucun
symptôme ;
- Possibilité de jaunisse ;
- Malaises ;
- Perte d'appétit ;
- Maux d'estomac ;
- Urines foncées ;
- Fatigue
|
- Éviter de partager des articles qui peuvent être
contaminés avec du sang (brosses à dents, rasoirs, coupe-ongles,
aiguilles, matériel pour renifler de la drogue)
|
|
Hépatite D
|
- N'apparaît habituellement que chez les personnes
déjà infectées par l'hépatite B ;
- Exposition à du sang contaminé et, dans de rares
cas, transmission par les relations sexuelles ;
- Partage d'articles personnels contaminés
|
- Jaunisse ;
- Malaises ;
- Perte d'appétit ;
- Douleur dans la région de l'estomac ;
- Urines foncées ;
- Fatigue ;
- Absence de symptômes possible
|
- Vaccin contre l'hépatite B ;
- Relations sexuelles protégées ;
- Éviter de partager des articles qui peuvent être
contaminés avec du sang (brosse à dents, rasoir, coupe-ongles,
aiguilles, matériel pour renifler de la drogue)
|
|
Hépatite E
|
- Répandue dans les pays en
développement
- Transmission par voie oro-fécale
(c'est-à-dire lorsque des selles contaminées se retrouve dans la
bouche d'une personne à cause d'un mauvais lavage des mains ou que des
selles contenant l'hépatite A contaminent de l'eau qui est ensuite
consommée)
- Transmission la plupart du temps par une exposition
à de l'eau contaminée ou à des aliments
préparés avec de l'eau contaminée
- L'hépatite E
peut être transmise de la mère à l'enfant, mais elle est
plus fréquente chez les adultes
|
- Jaunisse ;
- Malaises ;
- Perte d'appétit ;
- Maux d'estomac ;
- Urines foncées ;
- Fatigue ;
- 90 % des enfants infectés par l'hépatite E ne
présentent aucun symptôme
|
- Se laver les mains adéquatement avant et après la
préparation et la consommation d'aliments ;
- Redoubler de vigilance dans les pays en développement
|
|
Hépatite G
|
- Les sujets atteints sont souvent co-infectés par
d'autres virus, comme l'hépatite C, l'hépatite B et le virus
de l'immunodéficience humaine (VIH) ;
- Exposition à du sang ou à des produits sanguins
infectés ;
- Transmission possible par le partage d'articles personnels
contaminés par le virus ;
- Transmission possible de la mère à l'enfant
à la naissance ;
- Transmission possible pendant les relations sexuelles
|
Absence de symptômes
|
- Vaccin contre l'hépatite B ;
- Relations sexuelles protégées ;
- Éviter de partager des articles qui peuvent être
contaminés avec du sang (brosse à dents, rasoir, coupe-ongles,
aiguilles, matériel pour renifler de la drogue)
|
I.3.2 Les cirrhoses2(*)
La cirrhose se définit comme une atteinte diffuse du
foie associant fibrose annulaire et nodule de régénération
avec désorganisation vasculaire (perte des rapports normaux entre les
systèmes artériel, porte et sus-hépatique). Quelle qu'en
soit la cause, elle résulte d'un processus chronique mettant en jeu les
hépatocytes et les cellules sinusoïdales.
La définition scientifique de la cirrhose est la
présence d'une fibrose à disposition annulaire autour de nodules
de régénération. Concrètement, cela signifie que le
volume occupé par ce tissu cicatriciel inefficace est de plus en plus
important, ce qui peut perturber, à terme ou à un
niveau microscopique, les contacts entre les cellules hépatiques,
isolées par la fibrose, et les vaisseaux sanguins. Toutes les
fonctions d'échange des hépatocytes peuvent donc être
perturbées.
La fibrose constitue également un obstacle à la
circulation sanguine à l'intérieur du foie. Le sang provenant de
la veine porte, dont le débit est important, bute donc sur un obstacle
au niveau du foie, et se trouve donc en "sur-pression". Il va être
orienté vers des circuits de dérivation, utilisant des veines
dont le débit et le volume sont habituellement faibles. L'un
de ces circuits de dérivation, utilisant les veines de l'oesophage
qui se transforment en "varices", cause un risque
d'hémorragie.
Dans l'esprit du public, le mot cirrhose reste souvent
à tort obligatoirement associé à la notion d'alcoolisme.
Même si l'alcool reste, la cause la plus fréquente de cirrhose, il
existe d'autres causes parmi les quelles les plus fréquentes
sont :
- les hépatites chroniques dues au virus B ou au virus
C ;
- l'hémochromatose génétique, surcharge
en fer de l'organisme d'origine génétique qui peut aboutir
à la cirrhose ;
- l'obésité et le diabète peuvent,
également dans certains cas, être responsables de cirrhoses ;
etc.
Il y a deux périodes dans l'évolution des
cirrhoses :
- la période non compliquée ne s'accompagnant
pas de troubles majeurs ;
- la période des complications qui survient ensuite en
manifestant toute la gravité de la cirrhose : troubles de coagulation,
hémorragies digestives, épanchement de liquide dans l'abdomen
(ascite), troubles nerveux (encéphalopathie), fragilité aux
infections, insuffisance rénale....
- La cirrhose expose également au risque de cancer du
foie.
I.4 Exploration
biologique de la fonction hépatique3(*)
L'insuffisance hépato-cellulaire entraîne la
diminution du taux sérique de très nombreuses protéines.
L'albuminémie et le taux de prothrombine sont les marqueurs les plus
utilisés.
En cas de cytolyse, les transaminases
[alanine-aminotransférase (ALAT ou SGPT) et/ou
aspartate-aminotransférase (ASAT ou SGOT)] passent en abondance dans le
sérum. Une hyper-transaminasémie importante, supérieure
à 500 Unités Internationales (20 fois la limite supérieure
de la normale ou 20 N) est observée aux cours des hépatites
aiguës virales, toxiques ou médicamenteuses, ou, plus rarement, par
anoxie : insuffisance cardiaque aiguë, collapsus cardio-vasculaire,
ligature de l'artère hépatique, obstruction aiguë des veines
sus-hépatiques, insuffisance respiratoire aiguë.
Une élévation plus modérée
(jusqu'à 10 N) se voit dans les hépatites alcooliques, les
hépatites chroniques (en particulier d'origine virale), avec ou sans
cirrhose, et au cours de la cholestase ; dans quelques cas de cholestase,
l'élévation des transaminases peut dépasser 20 N au
début de la maladie.
En général, l'élévation des
transaminases prédomine sur l'ALAT. Une élévation
prédominante de l'ASAT oriente vers une hépatite alcoolique, une
nécrose ischémique aiguë ou la prise de certains
médicaments.
La cholestase élève la bilirubine et les
phosphatases alcalines, ainsi que la
gammaglutamyl-transpeptidase (ã-GT). Les phosphatases
alcalines augmentent également au cours de la croissance, de la
grossesse et en cas de lésions osseuses. On peut observer une
augmentation modérée des phosphatases alcalines au cours des
hépatites et des cirrhoses. L'activité sérique de la
ã-GT peut être élevée dans toutes les
maladies hépato-biliaires, dans l'alcoolisme chronique, après la
prise de médicaments inducteurs, au cours de maladies non digestives, de
l'obésité, de l'hyperlipémie ou du diabète ou
quelquefois sans cause décelable. En pratique, son
élévation atteste de l'origine hépatique d'une
élévation des phosphatases alcalines.
En cas de cholestase, il apparaît une baisse du taux de
Quick due à un défaut d'absorption d'une vitamine liposoluble, la
vitamine K, indispensable à la formation des facteurs II, VII et X. Elle
peut être corrigée par administration parentérale de
vitamine K. La vitamine K n'est pas indispensable à la synthèse
hépatique du facteur V dont le taux est diminué au cours de
l'insuffisance hépato-cellulaire, normal ou augmenté en cas de
cholestase.
L'augmentation des phosphatases alcalines et de la
ã-GT, sans ictère (cholestase anictérique) peut
révéler une maladie pancréatique, le cancer secondaire du
foie, les granulomatoses, la cirrhose biliaire primitive et la cholangite
sclérosante primitive.
On observe dans certaines maladies hépatiques
dont la physiopathologie est inflammatoire un ensemble de signes biologiques :
hyper-protidémie, hyper-gamma-globulinémie polyclonale,
élévation des protéines de l'inflammation.
NB : La variation du taux de l'enzyme
5'nucléotidase donne des renseignements spécifiques sur le
fonctionnement hépatique.
Comme susmentionné, notre travail s'intéresse
à doser les transaminases et le gamma-GT. Et ce, pour déterminer
si la toxicité médicamenteuse provoque la cytolyse ou la
cholestase. Ce qui nous pousse à bien fixer l'intérêt
clinique de ces paramètres.
Les organes les plus riches en transaminases sont, par ordre
de concentration décroissante4(*) :
· Pour l'ASAT
(SGOT) :
o Coeur
o muscle squelettique
o foie
o rein
o pancréas
o rate
o poumons
o globules rouges
· ALAT (SGPT) :
o foie (cytoplasmique),
o rein
o coeur
o muscle squelettique
o pancréas
o rate
o poumon
Variations physiologiques et
pathologiques
· Il ya diminution des transaminases dans le cas de :
- Grossesse ;
- Déficit en vitamine B6.
· Il ya augmentation des transaminases dans le cas de
:
- Surcharge pondérale, obésité (surtout
SGPT) ;
- Hépatites virales et infectieuses aiguës ;
- Hépatites médicamenteuses et toxiques ;
- Ischémie hépatique ;
- Atteinte hépatique secondaire à une maladie
auto-immune (lupus, polyarthrite rhumatoïde, sclérodermie,
vascularité) ;
- Hémochromatose ;
- Maladie de Wilson ;
- Tumeurs hépatiques ;
- Alcoolisme (avec cirrhose, hépatite,
stéatose) ;
- Infarctus du myocarde (surtout SGOT) ;
- Myopathies, cytolyse musculaire ;
- La migration d'un calcul des voies biliaires
- les attaques musculaires (traumatismes)
- lors des efforts physiques ;
§ Quotient de Deritis5(*)
Le Quotient de Deritis indique les relations entre
Aspartate-Aminotransférase et/ou Glutamate-Oxaloacetate-Transaminase (
GOT)
et Alanine-Aminotransférase et/ou Glutamate-Pyruvate-Transaminase (
GPT):
Formule : Quotient de Deritis = GOT/GPT
Le secteur de référence du quotient de Deritis
en dimensions s'élève à 0,6 - 0,8.
En simplifiant, on peut dire : Un petit quotient de Deritis
(< 1) parle en faveur de faibles dommages de foie, un grand quotient (>
1) pour des dommages de foie plus sérieux (par ex. :
hépatite
chronique,
...).
Remarques
· Le quotient de Deritis accru peut aussi
apparaître avec un
infarctus
du myocarde aigu.
· Le quotient de Deritis
s'applique dans le
diagnostic
du foie pour pouvoir adopter une déclaration sur le poids d'un
dommage de cellule de foie et/ou d'une
nécrose
de cellule du foie : toutefois c'est environ 80% dans les
Mitochondries
et environ 20% dans le
cytoplasme.
C'est-à-dire, plus des enzymes mitochondriale sont
dégagées, plus l'hépatotoxicité est sérieux.
· Si les valeurs du foie se trouvent autrement dans le
secteur
de référence, un quotient de Deritis accru n'est pas valable.
|
GOT/GPT
(Quotient de Deritis)
|
< 0.6
0,6 - 0,8
> 0.8
|
Hépatite Virale ;
Hépatite toxique (alcool, médicaments
...) ;
Un foie de matière grasse plus
facile ;
Hépatome Cholestasique
Nécrose des cellules hépatiques
Hépatite
du foie de matière grasse chronique
Hépatite réactive
Un plus vieil ictère
Foie d'accumulation
Intoxications aiguës
Cirrhose
Maladies d'autres organes
Participation du foie,
(p. ex. infarctus du myocarde)
Maladies de muscles squelettiques
|
Chapitre II :
GENERALITE SUR TUBERCULOSE
II.1 Définitions & historique de la
tuberculose
II.1.1
Définitions
Selon le dictionnaire médical "La Rousse", la
tuberculose est une maladie infectieuse contagieuse due à une
bactérie, le mycobcaterium tuberculosis ou bacille de
Koch6(*).
La tuberculose est une maladie contagieuse causée par
des bactéries qui se propagent dans l'air : les
mycobactéries. Ces bactéries sont projetées dans l'air
lorsqu'une personne souffrant de tuberculose infectieuse active tousse,
éternue, chante, joue à un instrument à vent ou, dans une
moindre mesure, parle.
La tuberculose active est la plus contagieuse lorsque les
bactéries tuberculeuses sont présentes dans les crachats
(expectorations) de la personne atteinte7(*).
La tuberculose est une maladie infectieuse provoquée
par une mycobactérie qui, sans traitement, provoque la mort de plus de
la moitié des personnes atteintes dans un délai de deux ans. Avec
un traitement adéquat, le malade peut être tout à fait
guéri dans 95% des cas.
Dans le monde, chaque année 8 et 10 millions de
personnes sont atteintes de la tuberculose et près de 2.000.000 de
malades en meurent. Seulement la moitié d'entre elles sont
dépistées, traitées et enregistrées. Un tiers de la
population mondiale est porteur de l'infection tuberculeuse, mais sans
développer la maladie. Lorsque le niveau immunitaire s'affaiblit, la
maladie peut surgir à tout moment8(*).
La tuberculose polypharmacorésistante survient quand
les bactéries tuberculeuses sont résistantes au moins à
l'isoniazide et la Rifampicine, les deux médicaments antituberculeux de
première ligne les plus puissants. La tuberculose
ultra-résistante est résistante à n'importe quelle
fluoroquinolone, et au moins à un des trois médicaments
injectables de deuxième ligne (capréomycine, kanamycine et
l'amikacine), en plus de l'Isoniazide et de la Rifampicine. Cette
définition révisée de la tuberculose
ultra-résistante a été agréée par le Groupe
de travail mondial de l'OMS sur la tuberculose ultra-résistante en
octobre 20069(*).
La tuberculose peut être, d'habitude, traitée par
une association de quatre médicaments antituberculeux standards ou de
première ligne. Si ces médicaments sont mal utilisés ou
mal administrés, la tuberculose polypharmacorésistante peut se
développer. Celle-ci est plus longue à traiter avec les
médicaments de deuxième ligne, qui sont plus onéreux et
provoquent plus d'effets secondaires.
La tuberculose ultra-résistante peut se
développer quand ces médicaments de deuxième ligne sont
aussi mal utilisés ou mal administrés et deviennent donc aussi
inefficaces. Parce que la tuberculose ultra-résistante est
résistante aux médicaments de première ligne et de
deuxième ligne, les options de traitement sont sérieusement
limitées, ainsi d'ailleurs que les chances de guérison.
II.1.2
Historique
Vers le début du 20ème siècle,
la tuberculose tuait une personne sur sept en Europe occidentale. On l'appelait
alors "la peste blanche". L'amélioration des conditions de vie d'abord
et ensuite, l'efficacité du traitement ont permis d'aboutir à une
situation nettement moins catastrophique10(*).
Il y a 30 ans, la maladie semblait être plus ou moins
sous contrôle. Il existait un traitement efficace et la victoire sur la
maladie n'était plus qu'une question de temps. Malheureusement,
l'intérêt pour cette maladie s'estompa de même que les
investissements pour combattre cette maladie : Le monde avait
crié victoire trop tôt !
L'apparition de la résistante aux antituberculeux
à New York, le signalement des cas de plus en plus nombreux dans
l'ancienne Union soviétique, de même qu'une
détérioration importante de la situation sanitaire causée
par le Sida en Afrique sub-saharienne ont servi de signaux de rappel.
L'Organisation mondiale de la santé (O.M.S.) déclara, alors en
1993 que la tuberculose constituait une urgence mondiale.
La pauvreté, le manque d'accès à des
soins de santé de qualité et abordables, le sida, les
déplacements de populations, la
résistance
sans cesse croissante aux médicaments de première ligne, les
crises socio-économiques constituent les éléments qui ont
contribué à favoriser le développement de la
tuberculose.
II.2 Etiologie et infection tuberculeuse
La tuberculose active est causée par des
mycobactéries qui se propagent dans l'air d'une personne à
l'autre. Ces bactéries peuvent rester en suspension dans l'air pendant
des heures.
Le système immunitaire (défenses de l'organisme)
de l'individu peut détruire les bactéries tuberculeuses
inhalées. Si le système immunitaire est incapable de tuer ces
bactéries, celles-ci peuvent demeurer dans l'organisme tout en restant
inactives. Il s'agit alors d'une infection tuberculeuse latente. Si
les bactéries tuberculeuses deviennent actives (se multiplient et
croissent à l'intérieur de l'organisme), on parle alors de
tuberculose active.
Dans la plupart des cas, les personnes infectées par la
tuberculose ne tombent pas malades et ne propagent pas. Par contre, d'autres
personnes développent la maladie11(*) et la propage dans la population.
On contracte une tuberculose résistante aux
médicaments en :
· inhalant des mycobactéries provenant d'une
personne atteinte d'une tuberculose active résistante aux
médicaments ;
· développant une tuberculose active à
nouveau, après avoir déjà été traité.
La tuberculose active est une maladie qui touche
habituellement les voies respiratoires, surtout les poumons. Parfois, les
bactéries tuberculeuses peuvent se propager à d'autres parties du
corps à travers le sang. Dans un tel cas, ces bactéries se
retrouvent le plus souvent dans les ganglions lymphatiques12(*).
Les bactéries tuberculeuses peuvent également
être présentes dans le rein, les os et les articulations,
l'intestin, le cerveau et la moelle épinière, partout dans le
corps (dans le cas de la tuberculose disséminée ou miliaire).
Quand on souffre d'une tuberculose active extra-pulmonaire (en
dehors des poumons), on peut se sentir malade ou faible, perdre du poids, avoir
de la fièvre et des sueurs pendant la nuit. Le patient peut
également éprouver des symptômes dans la région du
corps où se trouvent les bactéries tuberculeuses. Il est parfois
difficile de diagnostiquer la tuberculose active extra-pulmonaire parce que la
radiographie pulmonaire est normale et que les crachats ne contiennent pas de
bactéries tuberculeuses13(*).
L'infection tuberculeuse latente (ITL) : Dans
90% des cas, la tuberculose maladie ne se développera pas : L'infection
tuberculeuse latente est le résultat d'un équilibre entre le
système immunitaire de la personne infectée et les
bactéries. La personne infectée, n'est pas malade, ne
présente aucun symptôme et n'est pas contagieuse.
La tuberculose maladie : Environ 10% des
personnes infectées développeront une tuberculose maladie durant
leur vie. Ce risque diminue avec le temps : il est le plus important pendant
les deux années qui suivent l'infection. (5% des personnes
infectées développent une tuberculose maladie au cours des deux
années qui suivent l'infection, les 5 % autres la développeront
au-delà de deux ans après). Ce risque est plus important
notamment chez les enfants et les personnes dont l'immunité est
affaiblie.
II.3 Le bacille de Koch14(*)
Le bacille de Koch est une espèce bactérienne
dont l'agent est spécifique de l'infection tuberculeuse humaine qui peut
être également secondaire à la tuberculose bovine.
Le Mycobacterium est un genre de bactéries appartenant
à la famille des mycobacteriaceae, de l'ordre des actinomycetales.
Certains Mycobacterium sont des mycobactéries pathogènes pour
l'homme. C'est le cas, par exemple, de Mycobacterium tuberculosis, M. bovis et
M. leprae. Certains sont saprophytes et vivent dans l'organisme sans être
pathogènes. D'autres sont dits atypiques, c'est-à-dire qu'ils
sont parfois pathogènes. C'est le cas, entre autres, de Mycobacterium
avium et de M. xenopi.
II.3.1 Culture et
isolement
La recherche du mycobacterium tuberculosis se fait dans les
sécrétions bronchiques qui sont récupérées
par l'intermédiaire d'un tubage gastrique ou d'une fibroscopie
bronchique (tube qu'on introduit dans les poumons et dans l'estomac pour
prélever les sécrétions). Sa recherche se fait
également dans les crachats ou encore dans le liquide
céphalo-rachidien en cas de méningite. On peut également
rechercher dans les urines.
C'est la culture en milieu de Löwenstein-Jansen
incubé, presque deux mois durant, qui permet de faire le diagnostic de
certitude sur la présence dudit bacille chez un individu. En effet, la
positivité de l'examen direct n'est pas systématique. Il est donc
nécessaire et obligatoire de pratiquer cet examen.
Les sécrétions respiratoires et les urines ainsi
que d'autres prélèvements éventuellement contaminés
par une flore bactérienne doivent être décontaminés
avant d'être ensemencés dans les milieux riches et rendus
sélectifs pour les mycobactéries15(*).
En effet, celles-ci, aérobies strictes, ont des
exigences nutritives et se cultivent lentement. Par contre, les ponctions et
les prélèvements à priori mono-microbiens peuvent
être ensemencés tels quels.
Les milieux de culture :
a. Les milieux solides sélectifs à l'oeuf
coagulé de Löwenstein-Jensen et de Coletsos définissent les
caractères culturaux classiques de M. tuberculosis : colonies rugueuses
de couleur chamois apparaissant sous l'aspect de "verrue" ou de "chou-fleur" en
trois semaines environ après incubation à 37°C en
atmosphère ambiante.
Ces délais sont de 6 semaines pour M. africanum et M.
bovis.
b. Les milieux liquides permettent de réduire les
délais de positivité à quelques jours pour les
prélèvements très riches en bacilles et à un peu
plus de deux semaines en moyenne pour ceux paucibacillaires. Ces milieux
permettent une détection plus sensible et automatisée. En milieu
liquide, M. tuberculosis apparait sous la forme de longues "cordes" mises en
évidence par la coloration de Ziehl-Nelseen. Ce mode de groupement des
bacilles est attribué à la production d'une substance
particulière appelée "cord factor".
c. D'autres milieux liquides sont proposés tel que MB
REDOX® avec une détection visuelle, donc macroscopique.
L'identification classique de M. tuberculosis à partir
des cultures repose sur la morphologie des colonies, sur des
propriétés telle que la production d'acide nicotinique et sur
l'effet bactériostase comme l'acide para-amino-salicylique.
II.3.2
Physiopathologie et Phénomène de Koch16(*)
Au stade initial de tuberculose infection, à porte
d'entrée pulmonaire, M. tuberculosis exprime sa
pathogénicité en se multipliant à l'intérieur des
macrophages alvéolaires qui l'ont phagocyté. Le bacille de Koch
est une bactérie pathogène intracellulaire. La réaction
locale aboutit, en un peu plus d'un mois, à une lésion
histologique caractéristique, le granulome ou tubercule qui est
constitué de cellules épithélioïdes et de cellules
géantes multinucléées entourées d'une couronne
lymphocytaire et centrées par une zone de nécrose
caséeuse. Tout peut s'arrêter à ce stade par un enkystement
et une calcification des lésions suivis d'une auto-stérilisation
spontanée du chancre d'inoculation. C'est la situation la plus
fréquente.
Parfois, certains macrophages infectés pouvant migrer
jusqu'à un ganglion satellite qui empêchera la progression de
l'infection et évoluera aussi vers l'auto-stérilisation. Plus
rarement, si la multiplication bactérienne est importante, le
caséum se ramollit, les bacilles débordent les défenses
ganglionnaires et disséminent dans l'organisme par voie lymphatique puis
sanguine.
Le sujet réceptif entre alors dans la tuberculose
maladie avec une atteinte préférentielle du poumon isolée
ou associée dans les formes graves d'emblée à une miliaire
ou encore plus rarement à une méningo-encéphalite. En
dehors du poumon, la localisation sera plus souvent limitée à
l'appareil génito-urinaire ou ostéo-articulaire, par exemple.
Le phénomène de Koch
révèle les modifications survenues dans l'organisme en
réponse à l'introduction de M. tuberculosis. D'une part, la
réaction locale accélérée correspond à un
état d'hypersensibilité de l'organisme vis-à-vis du
bacille, en particulier des protéines dont la plus importante est la
tuberculine. D'autre part, la résistance à l'infection au point
de la seconde inoculation traduit un état d'immunité
antituberculeuse acquise : l'immunité de surinfection. Celle-ci a un
support cellulaire et non humoral et est à la base de la vaccination
antituberculeuse par le BCG.
II.3.3 Transmission
du bacille de la tuberculose17(*)
Seules les formes respiratoires (pulmonaire, bronchique et
laryngé) sont contagieuses. Le bacille de Koch se transmet par voie
aérienne, par l'intermédiaire des sécrétions
émises par une personne atteinte de tuberculose contagieuse, notamment
en toussant, en crachant ou en éternuant. Les formes extra-respiratoires
ne sont pas contagieuses.
La tuberculose est moins contagieuse que des
maladies comme la grippe. En effet, la transmission nécessite
habituellement des contacts prolongés en milieu confiné, par
exemple vivre dans le même logement que la personne contagieuse et
dépend du degré de contagiosité ainsi que de la
durée de contact avec cette dernière.
Ces conditions expliquent que toutes les personnes en contact
avec un cas de tuberculose ne sont pas systématiquement
infectées. Environ 30% des personnes très exposés à
un cas de tuberculose contagieuse sont infectées. De plus, toutes ne
développeront pas une tuberculose maladie.
L'homme est à la fois le réservoir et l'agent de
transmission du bacille18(*). Les patients chez qui l'examen direct de crachats a
permis l'identification des bacilles sont les plus contagieux. Ils cessent de
l'être après la deuxième semaine de traitement.
Beaucoup plus rare, la tuberculose à Mycobacterium
africanus, qui s'observe sur le continent africain, se transmet d'une
façon comparable à celle de la tuberculose classique et donne des
symptômes similaires. Enfin, il existe une autre forme rare de
tuberculose : la tuberculose bovine, due au mycobacterium bovis,
présente chez les bovins. La contamination se fait par la voie digestive
(ingestion de lait cru).
II.3.4
Émergence de Tuberculoses ultra-résistantes19(*)
L'Organisation mondiale de la Santé (OMS) exprime son
inquiétude quant à l'émergence de tuberculoses
pharmacorésistantes virulentes et demande de renforcer et d'appliquer
les mesures pour éviter une propagation mondiale des souches mortelles.
Cet appel fait suite aux travaux de recherche qui ont établi l'ampleur
du problème posé par la tuberculose UR, une nouvelle menace
tuberculeuse qui ne laisse pratiquement aucune possibilité de traiter
les patients (dont nombre de personnes vivant avec le VIH) avec les
antituberculeux actuels.
Qu'est-ce que la tuberculose à bacilles
ultrarésistants ?
La tuberculose à bacilles multirésistants
(ultrarésistants) désigne des souches de bacilles tuberculeux
résistant à au moins deux des médicaments antituberculeux
de première intention, l'isoniazide et la rifampicine. Par tuberculose
à bacilles ultrarésistants (en anglais : XDR-TB -
Extensive ou Extreme Drug resistant tuberculosis) ou tuberculose
UR, une tuberculose qui résiste à au moins trois des six classes
de médicaments de seconde intention.
On a décrit la tuberculose UR pour la première
fois au début de l'année 2006, à la suite d'une
enquête conjointe de l'OMS et des US Centers for Disease Control and
Prevention (CDC).
Les résistances aux médicaments antituberculeux
apparaissent dans les populations principalement à cause d'une mauvaise
prise en charge des cas de tuberculose, résultant d'une
multiplicité de problèmes : mauvaises habitudes de prescription
par les prestataires de soins, mauvaise qualité des médicaments,
approvisionnement irrégulier ou encore mauvaise observance du traitement
par le patient.
II.4 Epidémiologie de la tuberculose20(*)
Dans le monde : Selon les
estimations, il y a eu en 2005, 8,8 millions de nouveaux cas de tuberculose
dans le monde dont 7,4 millions en Asie et en Afrique subsaharienne. Au cours
de cette même année, on estime que près de 1,6 millions de
personnes sont mortes de la tuberculose ; Parmi celles-ci, 195 000
étaient infectées par le VIH.
Globalement, la prévalence et les taux de
mortalité de la tuberculose sont probablement en diminution depuis
plusieurs années. En 2005, le taux d'incidence est resté stable,
ou a diminué, dans les six régions OMS. Toutefois, le nombre
total de nouveaux cas de tuberculose a continué d'augmenter lentement du
fait du nombre de cas observés dans les régions Afrique,
Méditerranée orientale et Asie du Sud-Est.
Au total, 199 pays et territoires ont notifiés 5
millions d'épisodes de tuberculose en 2005 (nouveaux cas ou rechutes).
Les programmes DOTS (
Dredging Operations Technical
Support) ont signalé 2,3 millions de nouveaux cas de tuberculose
pulmonaire à frottis positif en 2005 et 2,1 millions ont
été enregistrés pour le traitement en 2004.
Bien que la charge de la tuberculose semble diminuer à
l'échelle mondiale, cette baisse n'est pas assez rapide pour atteindre
les cibles fixées par le partenariat ``Halte à la
tuberculose'' : réduire de moitié la prévalence et le
taux de mortalité d'ici 2015 par rapport à 1990. Les
régions des Amériques, de l'Asie du Sud-Est et du Pacifique
occidental sont dans les temps pour y parvenir ; par contre, les
régions de l'Afrique, de la Méditerranée orientale et de
l'Europe ne le sont pas. Ces pays et ces régions auront de plus grandes
chances d'atteindre les cibles s'ils peuvent augmenter les budgets et renforcer
les activités, en accord avec le Plan Mondial.
On distingue les pays à forte incidence (nombre de
nouveaux cas dans une période et pour une population donnée) de
ceux à faible incidence. Les zones géographiques à forte
incidence de tuberculose, selon les estimations de l'OMS21(*), sont :
- Le continent africain dans son ensemble ;
- Le continent asiatique dans son ensemble, y compris les pays
du Proche et Moyen-Orient ;
- Les pays d'Amérique centrale et du sud ;
- Les pays d'Europe Centrale et de l'Est y compris les pays de
l'ex-URSS ;
- Dans l'Union européenne : Bulgarie, Estonie, Hongrie,
Lettonie, Lituanie, Pologne, Portugal, Roumanie.
Aujourd'hui, la tuberculose partage avec le
SIDA la première place comme maladie mortelle dans le monde.
En Afrique22(*) : La répartition des
cas de tuberculose dans le monde est inégale. Plus de 95% des cas et
plus de 98% des décès par tuberculose sont notifiés dans
les pays d'Afrique, d'Asie et d'Amérique latine.
L'Afrique subsaharienne qui représentait en 2002, 11%
de la population mondiale, a notifié cette même année, 24%
des cas de tuberculose toutes formes confondes et 26% des cas de tuberculose
pulmonaire contagieuse. L'incidence estimée de la tuberculose
contagieuse est de 63 pour 100 000 habitants en moyenne mondiale, en Afrique
subsaharienne, elle atteint 149 pour 100 000 habitants.
Malgré l'existence de mesures spécifiques
efficaces (chimiothérapie et vaccination), la tuberculose ne cesse de
progresser dans le monde.
D'après les estimations de l'OMS, l'incidence annuelle
est passée de 7,3 millions en 1996 à 8,8 millions de cas en
2002. On prévoit 9 millions de cas en 2005 et 10 millions de cas en
2025. Près de la moitié des cas seront des cas de tuberculose
pulmonaire à microscopie positive, qui seront alors responsables de la
transmission du bacille dans la collectivité et créeront ainsi de
nouveaux sujets infectés et de nouveaux malades. Le nombre de
décès attribuables à la tuberculose, quant à lui,
diminuera lentement du fait de l'amélioration des mesures de
santé qui tendront à maintenir les malades en vie plus ou moins
longtemps
La région Afrique de l'OMS ne représente que
11% de la population mondiale mais contribue pour 27% au nombre total de cas de
tuberculose signalés en 2003. Plus de 34 pays africains ont des taux de
notification d'au moins 300 cas pour 100 000 habitants par rapport à un
taux inférieur à 15 pour 100 000 habitants dans les pays
développés. Entre 1993 et 2003, le taux de notification de la
tuberculose à frottis positif est passé de 20 à 75 cas
pour 100 000 habitants23(*).
L'incidence de la tuberculose s'est stabilisée dans de
nombreuses parties du monde à l'exception de l'Afrique, de l'Asie du
Sud-est et la région du Pacifique Ouest.
En République Démocratique du Congo
(RDC) 24(*) : Classée
11ème parmi les 22 pays les plus touchés au monde par
la Tuberculose et 4ème en Afrique lors de la
conférence d'Amsterdam en 2002, la RDC a soumis au Fonds Mondial une
proposition pour appuyer le Programme National de Lutte contre la tuberculose
(PNT) afin d'atteindre les objectifs de son plan directeur notamment
guérir 80 % des malades en 2006 et détecter 65 % des cas
attendus.
La République Démocratique du Congo est l'un
des 22 pays les plus atteints par la Tuberculose et le 5ème
pays en Afrique : 95.575 cas de tuberculose ont été
enregistrés sous toutes formes en 2004 (dont 62.519 cas de TPM+
dépistés) contre 87.405 cas en 2003 et 71.992 cas en 2002.
L'étude portait sur environ 47% de la population.
Plus de 85% de nouveaux cas contagieux sont âgés
de 15 à 54 ans avec une prédominance masculine, soit l'âge
de la productivité mais aussi l'âge de forte transmission du
VIH/SIDA. Le taux de succès du traitement est passé de 76% en
1999 à 81% en 2004. L'ampleur de la Tuberculose a pris des proportions
importantes ces dernières années avec l'épidémie de
VIH-SIDA (des études menées à Kinshasa et dans certaines
communautés ont montré que 30 à 50% des tuberculeux ont
une sérologie positive au VIH).
L'augmentation sans cesse croissante du nombre des cas en
Afrique a conduit à la déclaration de la tuberculose comme
urgence en Afrique en 2005 et la RDC en fera de même en 2006.
La RDC qui compte environ 60 millions d'habitants avec une
incidence TPM+ estimée à plus de 150 cas pour 100.000 habitants
s'est fixé comme objectif : « Réduire
considérablement le poids de la tuberculose d'ici 2015 dans le sens des
Objectifs du Millénaire pour le Développement (OMD) et ceux
fixés par le Partenariat pour faire barrage au halte à la
tuberculose » 25(*).
Chapitre III :
DIAGNOSTIC ET TRAITEMENT DE LA TUBERCULOSE
III.1 Diagnostic de la tuberculose
III.1.1 Examens cliniques de la tuberculose
En souffrant d'une tuberculose infectieuse active des voies
respiratoires et/ou de la tuberculose extra-pulmonaire, on se sent
habituellement malade. Le patient éprouve notamment les symptômes
généraux suivants :
§ une mauvaise toux qui dure plus de trois
semaines ;
§ des douleurs thoraciques : cracher des
mucosités (flegme) ou du sang et éprouver des douleurs à
la poitrine en toussant ou en respirant;
§ une faiblesse ou une extrême fatigue
§ une perte de poids ;
§ une perte d'appétit ;
§ des frissons ;
§ de la fièvre et des sueurs nocturnes ;
§ des problèmes, surtout des douleurs, dans la
partie du corps affectée par la maladie.
De part ces symptômes, on peut alors constater :
§ La tuberculose pulmonaire commune26(*) : autrefois
appelée phtisie, provient de la réactivation d'un foyer de
primo-infection pulmonaire : elle se traduit par une altération de
l'état général (fièvre à prédominance
vespérale, fatigue, amaigrissement), des sueurs nocturnes, une toux plus
ou moins grasse, .....
§ La pleurésie tuberculeuse : se
traduit par un essoufflement et par un épanchement pleural causant des
douleurs thoraciques ;
§ La péricardite tuberculeuse : se
signale par des douleurs thoraciques et un épanchement
péricardite progressif ;
§ La tuberculose miliaire : est une forme
particulière grave de la tuberculose se traduisant par un essoufflement
intense ou, chez les sujets âgés, par une altération
importante de l'état général. Elle se caractérise
en outre par la dissémination hématogène (par voie
sanguine) de bacilles vers de multiples organes : méninges,
abdomen, os, organes hématopoïétiques ou
uro-génitaux, glandes surrénales... selon sa localisation, son
expression clinique est alors variable et d'évolution
subaigüe : tuberculose méningée, tuberculose
hématopoïétique, tuberculose génito-urinaire,
tuberculose digestive...
III.1.1.1 Le diagnostic direct :
Il consistant à isoler, à identifier et à
tester la sensibilité aux antituberculeux de la souche provenant d'une
personne malade. Ce qui permet aussi, quand cela s'avère utile, de
soumettre la souche à des comparaisons épidémiologiques.
C'est-à-dire l'intérêt qu'il y a d'isoler la souche de M.
tuberculosis du malade, au besoin en multipliant les prélèvements
comme dans la tuberculose pulmonaire, avant tout traitement.
Il n'existe pas de diagnostic sérologique fiable de la
tuberculose, même si des tests sont régulièrement
proposés. L'intérêt de la recherche d'une
hypersensibilité retardée par intradermoréaction (IDR) ne
se dément pas.
III.1.1.2 Diagnostic différentiel
de la tuberculose pulmonaire :
A ce stade, deux autres espèces (Mycobacterium
africanum et Mycobacterium bovis), peuvent être identifiées.
Morphologiquement, ces BAAR sont de fins bacilles, immobiles, non
sporulés, non capsulés comme M. tuberculosis. En culture
aérobie sur milieux solide, ils poussent en six semaines et se
distinguent par l'aspect de leurs colonies :
Le M. africanum a des colonies rugueuses mais plates tandis
que M. bovis montre de petites colonies non pigmentées et lisses qui ne
grossissent pas.
Si la pathologie et l'épidémiologie de M.
africanum sont similaires à celles de M. tuberculosis, celles-ci sont
différentes pour M. bovis : L'infection humaine résulte d'une
contamination alimentaire (lait bovin) et montre souvent des localisations
extra-pulmonaires (osseuses et ganglionnaires, en particulier).
Prélèvements : ceux-ci
dépendent de la forme clinique de la maladie.
- Dans la forme pulmonaire : l'expectoration matinale
qui ramène des sécrétions broncho-pulmonaires purulentes
est satisfaisante si le malade crache, sinon l'aspiration par tubage, au
réveil, du contenu gastrique, recueille les mucosités
dégluties inconsciemment la nuit. Ces prélèvements
répétés trois jours de suite conviennent au diagnostic
dans la majorité des cas. Si un examen fibroscopique s'avère
nécessaire, l'aspiration du muco-pus peut être utile. Par contre,
si le lavage broncho-alvéolaire permet aussi cette recherche, il n'a pas
d'indication spécifique dans la tuberculose.
- Dans la forme génito-urinaire chez
l'homme : le recueil d'un volume d'urines suffisant le matin, 3 jours
de suite, est indispensable. La spermo-culture peut être entreprise si
nécessaire.
- Les autres formes de tuberculose pourront
être diagnostiquées par ponction : pleurésie,
méningite, arthrite, abcès, ou par différentes biopsies :
osseuse, disco-vertébrale, hépatique, endomètre.
L'hémoculture ne doit avoir que des indications exceptionnelles.
III.1.2 Imagerie médicale
Une radiographie pulmonaire permettra de voir si les poumons
présentent des signes de tuberculose active ; de même pour la
tuberculose extra-pulmonaire, la radiographie donne des preuves fiables pour
confirmer la maladie. Elle permet de diagnostiquer les formes
pulmonaires (et donc contagieuses) de la maladie. Elle est à la base du
diagnostic de la tuberculose maladie et permet un diagnostic précoce
lors du dépistage de la tuberculose.
III.1.3 Examens biologiques de la tuberculose
Les tests de laboratoire à effectuer sont :
a. Examen microscopique des crachats (expectorations),
pour une tuberculose pulmonaire : Examen après coloration de
Ziehl, puis culture sur milieu de Löwsten. Une fois que
l'échantillon a été mis en culture, il est
également testé pour résistance aux médicaments
contre la tuberculose (antibiogramme).
b. Examens bactériologiques :
Les prélèvements bactériologiques permettent
le diagnostic de certitude, car ils mettent en évidence le bacille de la
tuberculose (mycobactérie). Les analyses respiratoires sont
réalisées sur des crachats ou des prélèvements tels
que les tubages gastriques ou lors de fibroscopie bronchique.
c. Intradermoréaction à la tuberculine
(IDR) : L'IDR est avant tout à la base du diagnostic
d'infection tuberculeuse latente. L'intradermoréaction est un test qui
consiste à injecter une goutte de liquide contenant l'antigène
mycobactérien (tuberculine) dans le derme (face antérieure de
l'avant-bras) : injecter 10 UI de tuberculine par voie strictement
intradermique sous un volume de 0,1 ml. La réaction inflammatoire
obtenue (lue 72 heures après) détermine si le sujet a
été antérieurement en contact avec le bacille ou le
vaccin, selon le diamètre d'induration observé ; cependant elle
n'est pas toujours le témoin d'une protection efficace vis-à-vis
du bacille tuberculeux.
Le meilleur moyen de reconnaître l'infection de la
tuberculose est de faire un test cutané. Les autres tests servent
à savoir si la maladie s'est développée.
Trois situations peuvent se présenter de signification
clinique variable :
|
Diamètre mesuré (mm)
|
Signification clinique
|
|
< 5
|
absence
|
|
entre 5 et 10
|
réaction non spécifique ou vaccination par le
BCG
|
|
> 10
|
témoigne d'une infection d'autant que la
réaction est phlycténulaire
|
 
- Lors d'immunodépression, l'interprétation est
plus nuancée : ainsi lors de profonde immunodépression, un
diamètre de 5 mm peut signifier l'infection. Dans les pays à
vaccination continue, l'interférence avec la vaccination par le BCG
complique l'interprétation ; mais dans les pays ne vaccinant pas
par le BCG, l'IDR est un moyen diagnostic essentiel, sensible et
spécifique. La positivité d'une IDR, antérieurement
négative, définit la primo-infection tuberculeuse.
- Il est admis actuellement qu'il n'existe pas de relation
entre la protection contre la tuberculose et la présence d'une
hypersensibilité. Ce fait retire toute signification à la
pratique de l'IDR pour vérifier la présence de
l'hypersensibilité induite par le vaccin BCG. Ainsi les contrôles
pratiqués autrefois après vaccination sont-ils
supprimés.
L'IDR doit être réalisée :
· pour vérifier l'absence de tuberculose-infection
ou de tuberculose-maladie avant la primo vaccination. Toutefois les
nouveau-nés sont vaccinés sans test préalable. Il faut
rappeler qu'en cas de test positif, la vaccination n'a pas lieu d'être
effectuée.
· lors de l'enquête autour d'un cas de
tuberculose : Dans ce cadre, l'IDR est un élément parmi
d'autres (radiographie thoracique, examen clinique, suivi du patient...) pour
déterminer si une contamination a eu lieu. Il faut rappeler qu'une
enquête est toujours nécessaire, que le cas index soit ou non
bacillifère et qu'il s'agisse d'un adulte ou d'un enfant.
· comme aide ponctuelle au diagnostic de la tuberculose,
par exemple dans les tuberculoses extra pulmonaires, ou chaque fois qu'elle
peut être un élément d'orientation diagnostique
nécessaire au médecin.
· comme test de référence dans le cadre de
la surveillance des membres des professions à caractère sanitaire
ou social exposés à la tuberculose : Il faut rappeler que
dans le cas des professionnels exposés, la suppression de la
revaccination rend d'autant plus intéressante cette IDR à
l'embauche, qui a pour but de donner une valeur de référence pour
la surveillance ultérieure.
Test cutané (IDR) positif :
Un test cutané positif pour la tuberculose indique
habituellement que l'on est atteint d'une infection tuberculeuse latente.
D'autres tests devraient être effectués pour s'assurer qu'il n'y a
pas de tuberculose active : L'on peut prescrire une radiographie
pulmonaire ou une analyse de crachats (expectorations) pour la recherche de
bactéries tuberculeuses.
NB : Un test peut être positif
même en l'absence d'une infection tuberculeuse latente chez les personnes
qui ont déjà reçu le vaccin BCG ou qui ont
déjà été infectées par d'autres
bactéries ressemblant à celles de la tuberculose.
Un test cutané négatif :
Un test cutané négatif pour la tuberculose indique
habituellement que pas d'infection tuberculeuse. Un test peut cependant
être négatif, même si infecté depuis peu seulement.
Il faut de trois à huit semaines après l'exposition à un
cas de tuberculose infectieuse active pour que le test cutané devienne
positif.
NB : - Un test peut également
être négatif si le système immunitaire (défenses de
l'organisme) est faible. Par exemple, si l'on est infecté par des
bactéries tuberculeuses et le VIH et/ou le patient souffre d'une
tuberculose active, le test cutané peut être négatif
même si des bactéries tuberculeuses sont présentes dans
l'organisme.
- En plus du test cutané, un test
sanguin de détection de l'infection tuberculeuse latente est
également disponible (au Canada) : il s'agit du Quanti-FERON Gold
In-Tube27(*). Ce test
n'est pas recommandé pour le diagnostic courant de l'infection
tuberculeuse latente et n'est utilisé que dans des circonstances
spéciales.
- Quant au patient séropositif, le
test cutané pourra être négatif même si le germe de
la tuberculose est présent dans l'organisme. D'où penser à
d'autres tests : culture des crachats après test de Ziehl.
En général, une radiographie pulmonaire
indique bien si les poumons sont affectés. Un test cutané et des
tests sur les mucosités crachées sont très importants
- D'autres prélèvements sont possibles en
fonction de la localisation de la tuberculose maladie (ponction lombaire,
prélèvements osseux...)
STRATEGIES COMPLEMENTAIRES DANS L'ENTOURAGE D'UN CAS DE
TUBERCULEUX28(*)

Source :
http://www.med.univ-rennes1.fr/excomp/pneumo78.html
III.2 Traitement de la
tuberculose
La tuberculose peut guérir, mais les germes de la
tuberculose sont tenaces. Pour les tuer, il faudra prendre un médicament
spécial pendant six à neuf mois. Si l'on arrête le
traitement trop tôt, la maladie risque de s'aggraver parce que les germes
de la tuberculose se seront renforcés. Ce qui demandera alors de prendre
des médicaments plus forts pendant une longue période. L'on
risque de n'être jamais guéri29(*).
Le traitement de la tuberculose est la meilleurs
prévention de la tuberculose, car il guérit le malade, rompt la
chaîne de transmission de la maladie et protège la
communauté.
Pour obtenir l'efficacité et le suivi escomptés,
le traitement de la tuberculose doit répondre aux principes de base
ci-après :
- Une classification correcte des cas à
traiter ;
- Un régime thérapeutique standardisé de
courte durée et correct comprenant au moins 3 médicaments dont
ceux dotés d'activité bactéricide majeure pendant la phase
initiale de traitement ;
- Une posologie correcte avec une surveillance
directement du traitement ;
- Une régularité au traitement ;
- Un approvisionnement régulier du malade en
médicament antituberculeux de bonne qualité.
III.2.1 Catégorisation
Selon les priorités de traitement et l'état
bactériologique, on distingue quatre catégories :
- Catégorie 1 : nouveaux
cas de tuberculoses à microscopie positive et autres formes graves de la
maladie, jamais traités (ou traités moins d'un mois). Cette
catégorie comprend :
§ Les cas de tuberculoses pulmonaires à
microscopie positive (les plus nombreuses) ;
§ Les formes graves de la maladie (beaucoup plus rares)
dont le pronostic vital ou fonctionnel peut être
sévère : c'est-à-dire forme hématogène
(miliaire aiguë localisée ou généralisée,
méningite), formes pulmonaires interstitielle (spécialement chez
les immunodéprimés) et certaines formes extra-pulmonaires
sévères telles que la pleurésie massive ou
bilatérale, la péricardite, la méningite, la tuberculose
vertébrale avec troubles neurologiques, les tuberculoses digestives, les
tuberculoses urogénitales.
- Catégorie 2 (Cas de
retraitement) : ce sont habituellement des cas de tuberculose pulmonaire
(exceptionnellement extra-pulmonaire) à microscopie positive. Trois
groupes distincts sont à considérer :
§ Les rechutes définies par la réapparition
des bacilles dans l'expectoration d'un malade considéré comme
guéri auparavant ;
§ Les échecs définis par la présence
de bacilles dans l'expectoration d'un malade, à deux examens successifs
à 15 jours d'intervalle, au 5ème mois du traitement ou
au-delà ;
§ Le cas de reprise de traitement après
interruption de 2 mois ou plus (avec microscopie positive) et ayant reçu
plus d'un mois de traitement.
- Catégorie 3 : Nouveaux
cas de tuberculose pulmonaire à microscopie négative à
lésions peu étendues et autres cas bénins de tuberculose
extra-pulmonaire. Dans cette catégorie, on retrouve :
§ les enfants et des adolescents qui ont des
primo-infections patentes avec opacités pulmonaires (chancre
d'inoculation ou opacités systématisées) ou des petites
lésions pulmonaires non cavitaires et/ou des nodules
étendues ;
§ les tuberculoses extra-pulmonaires dont les plus
fréquentes sont les adénopathies périphériques, les
pleurésies peu abondantes, les tuberculoses osseuses et
ostéo-articulaires des membres.
- Catégorie 4 : Cas
chroniques des patients qui expectorent des bacilles avec un régime de
retraitement complet et supervisé. La majorité de ces malades
présentent une tuberculose multi-résistante.
Pour un traitement préventif, le médicament le
plus couramment employé est l'isoniazide (INH). Il faut 6 à 12
mois pour tuer les germes de la tuberculose. Ces germes demeurent dans
l'organisme à moins de les tuer avec le bon médicament.
L'isoniazide étant même sûre, la plupart
des gens peuvent prendre de ce médicament sans aucun problème.
Parmi les antibiotiques ayant guéri des milliers de
personnes contre la tuberculose active, les plus courants sont :
1) Isoniazide (INH) : symbolisé par
H ;
2) Rifampicine (RMP) : symbolisé par
R ;
3) Pyrazinamide (PZA) : symbolisé par
Z ;
4) Ethambutol (EMB) : symbolisé par
E ;
5) Streptomycine : symbolisé par
S.
NB : Le traitement doit durer au moins
six mois pour détruire toutes les bactéries tuberculeuses.
III.2.2 Régime de traitement :
a) Catégorie 1 et 3 (régime 2 RHZE / 4 RH),
c'est-à-dire que ce schéma comporte deux
phases30(*) :
- Une phase initiale de deux mois (phase intensive)
consistant en une prise quotidienne de la quadruple association : 2
RHZE ;
- Une phase de continuation de quatre mois associant la
Rifampicine et l'Isoniazide (4RH).
NB : S i l'examen direct des crachats reste positif
à la fin du 2ème mois de traitement, la
première phase sera prolongée de 4 semaines.
Tableau I : Nombre de comprimés à
administrer pour chaque tranche de poids en première
catégorie
|
Poids du patient avant le début du traitement
|
Nombre de comprimés à prendre pendant la phase
intensive (RHZE chaque jour)
|
nombre de comprimés à prendre pendant la phase
de continuation (RH chaque jour)
|
|
30 - 39 Kg
|
2
|
2
|
|
40 - 54 Kg
|
3
|
3
|
|
55 - 70 Kg
|
4
|
4
|
|
> 70 Kg
|
5
|
5
|
b) Catégorie 2 (régime 2 SRHZE / 1 RHZE / 5
RHE) : la durée est de huit mois sous surveillance stricte,
étant donné le risque de résistance secondaire aux
antituberculeux.
Le schéma thérapeutique comporte deux
phases :
- La phase intensive de trois mois comportant l'administration
quotidienne de la quadruple association (RHZE) et de la streptomycine ;
mais cette dernière ne sera donné que pendant 60 jours (2
SRHZE / 1 RHZE) ;
- La phase de continuation de cinq mois avec la triple
association en prises quotidiennes sous supervision directe (5 RHE).
NB : - Les cas à frottis positifs à la fin
du 3ème mois de traitement doivent continuer avec les quatre
médicaments pendant quatre semaines encore (RHZE).
- Si le frottis reste positif après le
cinquième mois, le traitement est arrêté et le patient est
référé à un centre spécialisé pour
les tests de sensibilisé et le traitement approprié (cfr. Cas
chronique).
Tableau II : nombre de comprimés à
administrer pour chaque tranche de poids en catégorie 2
|
Poids du patient avant le début du traitement
|
Phase intensive ou 1ère phase :
|
Phase de continuation ou 2ème phase
(5 mois durant)
|
|
Comprimés de RHZE/jr
(pendant 3 mois)
|
Injection quotidienne de Streptomycine
(pendant deux mois)
|
Comprimés de RH/jour
|
Comprimés d'Ethambutol/jr
|
|
30 - 39 Kg
|
2
|
0,5 g
|
2
|
1,5
|
|
40 - 54 Kg
|
3
|
0,75 g
|
3
|
2
|
|
55 - 70 Kg
|
4
|
1 g
|
4
|
3
|
|
> 70 Kg
|
5
|
1 g
|
5
|
3
|
c) Régimes de traitement pour enfants
Tableau III : posologie pour enfants en
catégorie 1 (2 RHZE / 4 RH)
|
Poids du patient avant le début du traitement
|
Nombre de comprimés à prendre par jour pendant
la phase intensive (2 mois)
|
nombre de comprimés à prendre pendant la phase
de continuation (4 mois) :
RH (60 + 30 mg) / jour.
|
|
Comprimé RHZ
(60+30+150 mg) / jr
|
comprimé d'E (400 mg) / jr
|
|
Jusque 7 Kg
|
1
|
-
|
1
|
|
8 - 9 Kg
|
1 ½
|
-
|
1 ½
|
|
10 - 14 Kg
|
2
|
-
|
2
|
|
15 - 19 Kg
|
3
|
-
|
3
|
|
20 - 24 Kg
|
4
|
1
|
4
|
|
25 - 29 Kg
|
5
|
1
|
5
|
Tableau IV : Posologie pour enfants atteints de
la méningite tuberculeuse Catégorie 1 : Méningite
tuberculeuse 2 SRHZE / 4 RH
|
Poids du patient avant le début du traitement
|
Nombre de comprimés à prendre pendant la phase
intensive - 2 mois-
|
nombre de comprimés à prendre pendant la phase
de continuation - 4 mois- :
RH (60 + 30 mg) / jour.
|
|
Comprimé RHZ
(60+30+150 mg) / jr
|
Piqure de streptomycine/jr
|
|
Jusque 7 Kg
|
1
|
0,25
|
1
|
|
8 - 9 Kg
|
1 ½
|
0,25
|
1 ½
|
|
10 - 14 Kg
|
2
|
0,25
|
2
|
|
15 - 19 Kg
|
3
|
0,33
|
3
|
|
20 - 24 Kg
|
4
|
0,50
|
4
|
|
25 - 29 Kg
|
5
|
0,50
|
5
|
Tableau V : Posologie pour enfants atteints d'une
tuberculeuse extra-pulmonaire (Catégorie 3 2 RHZ / 4
RH)
|
Poids du patient avant le début du traitement
|
Nbre de comprimés à prendre par jour pendant la
phase intensive (2 mois) : RHZ : (60+30+150 mg)
|
Nbre de comprimés à prendre par jour pendant la
phase de continuation : RH (60+30mg)
|
|
Jusque 7 Kg
|
1
|
1
|
|
8 - 9 Kg
|
1 ½
|
1 ½
|
|
10 - 14 Kg
|
2
|
2
|
|
15 - 19 Kg
|
3
|
3
|
|
20 - 24 Kg
|
4
|
4
|
|
25 - 29 Kg
|
5
|
5
|
Tableau récapitulatif du traitement des la
tuberculose chez les enfants
|
Présentation clinique
|
Catégorie et régime
|
|
Tuberculose pulmonaire à microscopie positive
|
Catégorie 1 : 2RHZE / 4 RH
|
|
Tuberculose à microscopie négative avec des
lésions parenchymateuses importantes
|
Idem
|
|
Tuberculose extra-pulmonaire sévère (abdominale,
péricardique, etc.)
|
Idem
|
|
Méningite tuberculeuse
|
Idem
|
|
Tuberculeuse à microscopie négative, mais
extra-pulmonaire (adénite tuberculeuse, lymphadénopathie
médiastinale)
|
Catégorie 3 : 2 RHZE / 4RH
|
NB : Pour la méningite
tuberculeuse, la streptomycine est recommandée à la place de
l'Ethambutol, car ce dernier ne traverse pas la barrière
hémato-encéphalique.
d) Cas particuliers
- Femmes enceintes : Elles doivent être bien
informées qu'un traitement correctement suivi garantit une bonne
évolution de sa grossesse.
Ø Pour toute femme en période de
procréation, il faut se renseigner sur l'existence éventuelle
d'une grossesse avant le début du traitement ;
Ø Les antituberculeux de première intention ne
constituent aucun danger et ne sont pas contre-indiqués durant la
grossesse ;
Ø La streptomycine à cause de sa toxicité
pour l'appareil auditif du foetus, constitue une contre-indication absolue.
- Allaitement :
Ø La femme qui allaite devrait bénéficier
d'une cure importante sans interruption, y compris lorsque le traitement
contient de la streptomycine ;
Ø Le traitement de la mère constitue la
meilleure prévention de la transmission mère-enfant ;
Ø L'allaitement ne doit pas être interrompu
à cause du traitement antituberculeux ;
Ø Si la mère est encore en phase intensive,
l'enfant recevra un traitement préventif à l'Isoniazide pendant
six mois et la vaccination au BCG sera proposée à la fin de ce
traitement préventif.
III.2.3 Conséquences du traitement antituberculeux31(*)
Les médicaments utilisés pour traiter la
tuberculose active sont relativement sûrs. Parfois, ces
médicaments peuvent avoir des effets secondaires. Certains effets
secondaires sont mineurs, d'autres sont plus graves, c'est-à-dire
majeurs.
Les effets secondaires graves suivants peuvent se
manifester lors de la prise des médicaments :
1. Effets secondaires mineurs : ne nécessitent pas
une interruption du traitement, ni une suspension du médicament
responsable, car ils régressent le plus souvent spontanément
après quelques jours.
- Streptomycine : provoque des réactions
locales au point d'injection, sensation de constriction de la face et autour de
la bouche pendant quelques minutes.
- Isoniazide : excitation plus ou moins
euphorique, plus rarement de l'insomnie ;
- Rifampicine : colore les urines et d'autres
secrétions en rouge-orange. D'où il faut en avertir le malade
pour qu'il ne s'alarme pas ; de troubles gastro-intestinaux, anorexie,
.... ;
- Ethambutol : peut entraîner une
augmentation du taux d'acide urique avec arthralgies et présente
une toxicité hépatique ;
- Pyrazinamide : provoque de la nausée et
manque d'appétit, des douleurs articulaires de type gouteux, avec
gonflement des articulations.
2. Effets secondaires majeurs : imposent l'interruption
des du traitement ou de la prise des médicaments en cause, avec
présentation immédiate du malade au médecin responsable de
l'application du P.A.T.I.
- Streptomycine : est toxique par accumulation
pour la 8ème paire de nerfs crâniens,
c'est-à-dire le nerf auditif. Si les troubles vestibulaires (vertiges)
qu'elle entraine sont susceptibles de régresser après
l'arrêt du traitement, la surdité est, par contre,
définitive. Tel est le cas des malades âgés ou ayant
reçu plus de streptomycine dans le passé.
- Isoniazide : entraîne une névrite
périphérique, surtout sensitive, peut s'observer, essentiellement
chez les malades en état de malnutrition.
NB : Utilisé en association avec
la Rifampicine, l'INH peut provoquer une hépatite. D'où, à
l'augmentation excessive des transaminases pendant le traitement, s'impose
l'arrêt du traitement jusqu'au rétablissement de ces
paramètres.
- Rifampicine : en association, l'Isoniazide, la
Rifampicine et la Pyrazinamide sont responsables d'hépatite
médicamenteuse, la Pyrazinamide étant le plus
hépatotoxique.
- Ethambutol : provoque très rarement la
névrite rétrobulbaire et des réactions
d'hypersensibilité : des neuropathies
périphériques.
- Pyrazinamide : peut entraîner une
hépatite (Cfr. Rifampicine et INH). Les manifestations articulaires sont
rarement importantes.
IIème PARTIE : PRATIQUE AU
LABORATOIRE
Chapitre IV :
MATERIEL ET METHODES
IV.1 Matériel
IV.1.1 Echantillonnage
Notre population d'étude était constituée
des sujets tuberculeux de l'Est de la ville de Kinshasa.
De cette population, nous avons sélectionné les
sujets qui ne présentaient pas de coïnfection et plus
particulièrement les malades souffrant de la tuberculose sans un terrain
de VIH et ceux n'ayant pas un antécédent hépatique.
Nous avons ainsi retenu dans notre étude 49 sujets,
pour cas témoins, et 50 sujets tuberculeux de deux sexes
répondant aux conditions suivantes :
- N'avoir pas reçu aucun traitement avant le
prélèvement ;
- Etre un nouveau cas de tuberculose pulmonaire
avéré par des examens de laboratoire ;
- Avoir accepté volontairement et verbalement de
participer à l'étude.
Pour identifier les cas de VIH, nous nous sommes servis des
Kits de "Détermine" de dépistage, tandis que les
antécédents hépatiques étaient
détectés à partir des fiches de consultation.
Tous les sujets retenus dans l'étude étaient
des malades reçus en consultation dans les centres de santé qui
prennent gratuitement en charge ce type des malades et qui sont situés
dans les communes de Masina, Limete et Barumbu.
IV.1.2 Cadre
et période d'étude
Nous avons travaillé sur des prélèvements
effectués en deux périodes : Dans un premier moment, au
début du traitement (juillet 2008) et au sixième mois,
c'est-à-dire à la fin du traitement (décembre 2008).
Les échantillons biologiques prélevés
étaient constitués du sang veineux à partir duquel nous
avons extrait le sérum. Celui-ci constituait le véritable
échantillon de travail dans lequel nous avons dosé les enzymes
hépatiques (ã-GT, GOT et GPT).
IV.1.3 Equipement et réactifs de laboratoire
Le sang prélevé au centre de santé
était acheminé au laboratoire de la Clinique de la Commission
Electorale Indépendante où nous avons effectués nos
analyses : extraire le sérum et procéder au dosage des
enzymes précitées. Trois heures de temps s'écoulaient
entre le prélèvement et le dosage.
Le sang était prélevé au pli du coude
dans un tube sec, puis centrifugé à 2000 tours/minute grâce
à la centrifugeuse de marque Labofuge.
Pour réaliser les analyses, nous nous sommes servis de
l'équipement et réactifs de laboratoire ci-après :
- Un spectrophotomètre UV série 1247, de marque
Visual/70VB0357 ;
- Des seringues à 5 cc à usage unique ;
- Tubes à essai ;
- Les Kits de dosage :
§ Kit SGOT : fabriqué par la maison CYPRESS,
série HBEO6, Lot Soc-64A, péremption : novembre 2009
§ Kit SGPT : fabriqué par la maison CYPRESS,
série HBE07, lot SPC-77, péremption : août 2010
§ Kit ã-GT : fabriqué par la maison
CYPRESS, série HBEO5, lot B-93, péremption : juin 2009.
- Composition des réactifs
§ Kit SGOT
|
Composition
|
Concentration
|
Quantité
|
|
Réactif 1
|
Tampon TRIS pH 7,8
L- Asparate
|
80 mmol/l
200 mmol/l
|
1x235 ml
|
|
Réactif 2
|
NADH
LDH
MDH
á-cétoglutarate
|
0,18 mmol/l
800 mmol/l
600 mmol/l
12 mmol/l
|
15x1reagent
|
§ Kit SGPT
|
Composition
|
Concentration
|
Quantité
|
|
Réactif 1
|
TRIS Buffer pH 7,8
L- Alanine
|
80 mmol/l
200 mmol/l
|
1x235 ml
|
|
Réactif 2
|
NADH
LDH
á-cétoglutarate
|
0,18 mmol/l
1200 mmol/l
15 mmol/l
|
15x1reagent
|
§ Kit ã-GT
|
Composition
|
Concentration
|
Quantité
|
|
Réactif 1
|
Tampon Tris pH 8,6
L- Alanine
|
100 mmol/l
200 mmol/l
|
1x235 ml
|
|
Réactif 2
Substrat
|
Glycylglycine
L-ã-glutamyl-3-carboxy-4-nitroanilide
|
100 mmol/l
3 mmol/l
|
15x1reagent
|
IV.2 Méthodes
IV.2.1 Choix des méthodes de dosage
L'activité des enzymes hépatiques a
été déterminée par la méthode
cinétique. Le choix porté sur cette méthode a
été orienté par sa grande fiabilité. C'est, en
effet, une méthode spécifique, très sensible, et pratique.
Elle est reproductible et permet de visualiser l'activité
enzymatique.
Nous avons suivi le mode opératoire indiqué par
la maison CYPRESS fabriquant les kits des réactifs que nous avons
exploités.
IV.2.2 Dosage de la Gamma-Glutamyl-Transférase
(ã-GT) et des transaminases [GOT ou ASAT et GPT ou ALAT]
1. Principe de la méthode de dosage :
Détermination cinétique d'activité de ã-GT, GOT
(ASAT) et de GPT (ALAT) selon les réactions ci-dessous.
La lecture de l'absorbance initiale au photomètre et
des absorbances toutes les minutes pendant trois minutes permet de calculer la
différence entre les absorbances et les différences d'absorbances
moyenne par minute de NADH dont la vitesse de consommation est
déterminée photométriquement et est directement
proportionnelle à l'activité de l'enzyme dans
l'échantillon selon le cas (ã-GT ou du GOT ou du GPT).
- Pour ã-GT :
L-ã-glutamyl-3-carboxi-p-nitroanilide + glycylglycine
ã-GT
L- ã-glutamylglycine - 5-amino-2-nitrobenzène
- Pour GOT :
á-cétoglutarate + Asparate GOT
Glutamate + oxaloacétate
Oxaloacétique MDH Malate
NADH+ + H+ NAD
- Pour GPT
á-cétoglutarate + Alanine GPT Glutamate
+ pyruvate
Pyruvate LDH lactate
NADH+ + H+ NAD

2. Mode opératoire :
- Préparation des réactifs :
Ø Dissolvez une tablette R2 (NADH
0,18mmol/litre) dans 15 ml du tampon R1 (tampon tris 80 mmol/litre
de pH = 7,8)
Ø Couvrir de capuchon et mélanger pour dissoudre
le contenu.
Cette solution de travail est stable pendant 72 heures
entre 15 - 25°C ou 21 jours entre 2-8°C.
- Réalisation du test :
Ø Prélever 1 ml de solution de travail ;
Ø Prélever 0,10 ml de
l'échantillon ;
Ø Mélanger et attendre une minute ;
Ø Lire l'absorbance initiale à 340 nm ;
Ø démarrer le chrono et lire les absorbances
toutes les minutes pendant trois minutes.
Ø Calculer la différence entre les absorbances
et les différences d'absorbance moyenne par minute.
3. Valeurs de références32(*) :
- Femme : < 32 UI/litre
- Homme : < 40 UI/litre
IV.2.3 Analyse statistique des résultats
Pour l'analyse de nos données, nous devons analyser
l'effet de l'affection hépatique selon le sexe et l'âge aux fins
d'en déterminer les personnes les plus affectées ainsi que la
tranche d'âge plus affectée. D'où, faudra-t-il calculer la
moyenne, la variance et même déterminer la classe modale.
Nous nous servirons de tests statistiques tels que la moyenne,
la variance, la comparaison des moyennes et des variances des cas
témoins et des sujets tuberculeux au début et à la fin du
traitement ainsi que la comparaison des proportions des sujets dont les taux
des transaminases sont élevés dans le premier dosage et le
second. Ce qui permettrait de confirmer la présence ou l'absence
d'affection hépatique (hépatite médicamenteuse) et de
déterminer la phase la plus concernée (cytolyse ou
cholestase).
De ce fait, nous nous servirons du test statistique
d'écart-réduit afin d'en tirer la conclusion à partir des
formules ci-dessous :
Comparaison des moyennes  ; ;
Comparaison des variances 
et comparaison des proportions  et/ou et/ou 
Chapitre V :
RESULTATS & DISCUSSION
V.1
Présentation des résultats
Tableau VI : Répartition des sujets
tuberculeux, selon le sexe,
|
Sexe
|
Effectif
|
fréquence
|
|
M
|
26
|
52 %
|
|
F
|
24
|
48 %
|
|
Total
|
50
|
100 %
|
Commentaire :
Sur 50 sujets tuberculeux, nous avons 26 de sexe masculin,
soit 52% et 24 de sexe féminin, soit 48% de la population
d'étude.
Tableau n° VII : Répartition des
sujets tuberculeux selon l'âge
|
Age (ans)
|
Ci
|
ni
|
f (%)
|
|
16 - 25
26 - 35
36 - 45
46 - 55
56 - 65
|
20,5
30,5
40,5
50,5
60,5
|
16
13
12
6
3
|
32
26
24
12
6
|
|
Total
|
|
50
|
100
|
Légende :
Ci = centre de classe
ni = effectif de classe
Au vu du tableau ci-haut, nous constatons que 94 % des sujets
sont âgés de 16-55ans ; et l'âge moyen des patients
tuberculeux est de 33,9 ans #177; 12,2 ans.
Tableau VIII : Répartition des moyennes, des
variances et des écart-types
|
Population
Activité
|
Témoins
|
Tuberculeux
|
|
1er dosage
|
2ème dosage
|
|
X
|
S2
|
S
|
X
|
S2
|
S
|
X
|
S2
|
S
|
|
GOT
(UI/litre)
|
24,2
|
111,8
|
10,57
|
20,8
|
163,6
|
12,79
|
30,6
|
184,3
|
13,58
|
|
GPT
(UI/litre
|
19,2
|
95,8
|
9,79
|
15,4
|
85,5
|
9,24
|
15,6
|
136,4
|
11,68
|
|
-GT
(UI/litre)
|
31,3
|
315,4
|
17,76
|
35,2
|
365,4
|
19,11
|
33,0
|
203,1
|
14,25
|
Les données de ce tableau montrent que les moyennes de
GOT, GPT et -GT des cas témoins, des sujets malades au début et
à la fin du traitement sont dans la fourchette des valeurs de
référence.
Tableau IX : Comparaison des moyennes et des
variances des populations d'étude.
|
Tests statistiques
|
Cas témoins & 1er
dosage
|
1er dosage & 2ème
dosage
|
|
GOT
|
GPT
|
-GT
|
GOT
|
GPT
|
-GT
|
|
Comparaison des variances
|
1,31
|
0,40
|
0,52
|
0,42
|
1,58
|
1,94
|
|
Comparaison des moyennes
|
1,45
|
1,99
|
1,06
|
0,095
|
3,70
|
0,65
|
|
Observation
|
|
|
|
|
-
|
|
NB :  1,96 1,96
La comparaison des variances comme celle des moyennes
d'activité enzymatique chez les témoins et les patients
tuberculeux au début et à la fin du traitement conduit à
des résultats d'écart-réduit inférieur à
l'écart tabulaire, exceptée la comparaison des moyennes des GPT
au début et au 6ème mois de traitement ; elle est
de 3,70.
Tableau IX : Répartition des sujets selon
les taux des transaminases et ã-GT au début et
6ème mois de traitement.
|
Dosage
|
proportion de taux des transaminases élevées
|
proportion de taux des -GT élevés
|
Proportion de taux des transaminases et -GT
élevés
|
Proportion de taux des transaminases et -GT normal
|
|
1er dosage
|
|
|
|
|
|
2ème dosage
|
|
|
|
|
Commentaire : La proportion des sujets tuberculeux
présentant un taux élevé d'activité enzymatique est
de 44% au début du traitement et 46% au 6ème mois du
traitement. Tandis que celle des sujets présentant un taux normal
d'activité enzymatique est de 56 % au début du traitement alors
qu'elle est de 54% au 6ème mois du traitement
V.2 Discussion
Au regard de la littérature, il est
révélé que plus de 85 % des sujets souffrant de la
tuberculose sont compris dans la tranche d'âge de 15 à 54 ans,
avec une prédominance masculine. Ce qui confirme les données des
tableaux VI et VII où nous avons constaté que 94 % des cas sont
compris entre 16 et 55 ans, avec 52 % des sujets masculins contre 48% des
sujets féminins.
Les données du tableau VIII révèlent que
la comparaison des variances et des moyennes d'activité enzymatique chez
les cas témoins et les sujets tuberculeux au début du traitement
confirment une absence d'affection de la fonction hépatique avant tout
traitement par les antituberculeux.
Par contre, la comparaison des variances et des moyennes
d'activité enzymatique chez les sujets tuberculeux au début et au
6ème mois de traitement prouvent qu'il y a une
altération de la fonction hépatique à la fin dudit
traitement.
De même, en tenant compte des données du tableau
IX, avec la comparaison des proportions des taux des transaminases
sérique et -GT, il se révèle une augmentation
d'activité enzymatique. Or, nous sommes sans ignorer que toute
augmentation du taux des transaminases sériques et -GT reflète
une altération hépatique. Etant donné que pendant le
traitement, la prise des boissons alcooliques est prohibée, cette
augmentation d'activité enzymatique serait due, soit à la
toxicité des médicaments administrés (qui se
révèle au niveau du foie), d'une part ; soit alors à
une lésion d'autres organes (rein, pancréas, coeur, ....)
survenue pendant le traitement, d'autre part.
Excluant la deuxième part, il est question, dans notre
travail, de déterminer si l'hépatotoxicité aiguë se
manifesterait dans la cytolyse ou dans la cholestase au même degré
d'altération. De même, déterminer si cette hépatite
constatée provient de la médication ou de la maladie
même.
De surcroît, la littérature nous relate que
quelques médicaments présentent des effets secondaires majeurs
hépatotoxiques dont les antituberculeux, entre autre, la Rifampicine, la
pyrazinamide..... Ce qui appuie aussi nos données ci-haut
trouvées : L'hépatotoxicité aiguë serait due
à la médication par les antituberculeux.
Au regard des données du même tableau, la
comparaison des proportions montre que l'altération n'affecte pas les
deux phases (cytolytique et cholestasique) au même degré :
Elle serait plus cholestasique que cytolytique, vu que nous avons 20 cas (soit
40%) dont le taux de -GT est élevé et 10 cas (soit 20%) dont le
taux des transaminases est élevé au 6ème mois
de traitement par les antituberculeux.
CONCLUSION
En comparant les variances des transaminases et -GT des
non-tuberculeux (cas témoins) et celles des patients au début du
traitement antituberculeux, nous constatons qu'il n'y a pas d'altération
hépatique.
Par contre, en s'appuyant sur la même comparaison, mais
dans un même échantillon des patients au début et au
6ème mois du traitement antituberculeux, nous constatons
qu'il y a altération hépatique. Ce que révèlent
aussi les résultats de la comparaison des proportions des taux normaux
et élevés des transaminases et de la -GT au début et au
6ème mois de traitement desdits paramètres chez les
mêmes patients. Cette hépatite est plus cholestasique que
cytolytique
Au regard de l'âge, nous trouvons que la tuberculose
sévit plus les adolescents (soit 32% de 16 à 25 ans) que les
personnes âgées (soit 6% de 56 à 65 ans).
En définitive, l'hépatite aiguë
constatée à la fin du traitement antituberculeux est
médicamenteuse et non due à la tuberculose. Cette première
a plus d'effets dans la cholestase que dans la cytolyse.
RECOMMANDATIONS
Ø Au Pouvoir Public (Ministère de
Santé Publique)
Augmenter la capacité de la mise en terme
financière pour une bonne prise en charge des tuberculeux, et ce pour
arriver à éradiquer la tuberculose ;
Ø Aux formations
médicales
Faire régulièrement le screening biologique (GOT
& GPT.....) des malades sous traitement antituberculeux pour un bon
suivi de traitement sans perturbation organique ;
Ø Aux scientifiques
- Elaborer des études plus approfondies sur les sujets
dans les différents aspects de la maladie pour son
éradication ;
- Pour nous compléter, doser les 5' nucléotidase,
le taux des bilirubines et phosphatases alcalines aux fins de fixer les
pouvoirs décideurs.
- Arriver à réduire la durée du traitement
antituberculeux en modifiant les molécules médicamenteuses
desdits antituberculeux afin d'éviter les conséquences de la
médication à longue durée
Ø Aux patients
Faire la sensibilisation des masses dans le but de la
non-stigmatisation : La tuberculose n'est pas une maladie
inguérissable. Tout le monde peut la contracté. D'où,
mettre en évidence les mesures préventives.
BIBLIOGRAPHIE
I. Livres
1. Agence de la Santé Publique de Canada,
février 2008, "Tuberculose infectieuse", PHAO/ASP-FC-17F.
2. Agence de la Santé Publique du Canada, 2008, Fiche
d'information sur la tuberculose.
3. Boulahbal et P. Chaulet, 2004, "La tuberculose en
Afrique : épidémiologie et mesures de lutte",
Médecine tropicale.
4. Bureau National de la tuberculose (BNT-Zaïre), 1989,
"Programme Anti-tuberculeux intégré (P.A.T.I.)",
2ème édition.
5. Carola Strang et coll., "Larousse Médical",
nouvelle édition, Paris, Cedex, 2006
6. Kathleen DESKA & Timothy J. PAGANA, 1992, "Diagnostic
and laboratory test reference", 2nd ed., p. 944
7. Organisation Mondiale de la Santé (OMS), mars 2008,
"Aide-mémoire EURO/01/07", Genève, Berlin, Copenhague.
8. Organisation Mondiale de la Santé (OMS),
"Journée mondiale de lutte contre la tuberculose : Elément
de rapport du 24 mars 2007.
9. Programme National de Lutte contre la Tuberculose (PNT),
2008, "Le médecin face à la tuberculose dans la stratégie
de renforcement du système de santé", draft-inédit,
Kinshasa.
10. Programme National de Lutte contre la Tuberculose (PNT),
2007, "Situation épidémiologique de la tuberculose en RDC",
Kinshasa.
11. R. MURRAY et Coll., 2002, "Biochimie de HARPER",
25ème éd. Les Presses de l'Université de Laval,
de Boeck, 933 P.
12. Union Africaine, mai 2006, "Rapport du sommet
spécial de l'Union Africaine sur le VIH, la tuberculose et le
paludisme", Abuja.
13. Yves Deugnier, 2005, "Anatomie-physiologie du foie",
Université Rennes 1, « polycopie de sémiologie du
foie et des voies biliaires »,
14. P.Métais, J. Agneray et coll., 1990, Biochimie
clinique, tome1 "Biochimie analytique", 2ème édition
SIMEP, Paris, France, 259P.
II. Sites Internet
1.
http://www.fondationdamien.org/les_maladies_cibles/tuberculose.cfm
2.
http://www.fondationdamien.org/les_maladies_cibles/tuberculose.cfm
3.
http://www.phac-aspc.gc.ca/tbpc-latb/fa-fi/infecttb-fra.php
4.
http://www.pntrdc.canalblog.com/
5. http://www.snfge.org/
6.
http://www.vulgaris-medical.com/encyclopedie/
III. Notes des cours
1. Prof ENGO B., "Notes de cours de Biochimie
médicale", 1ère Licence biologie Médicale,
ISTM-Kinshasa, 2006 - 2007, inédit, p. 128
2. Prof OKENGE Ngongo, "Cours de statistique
inférentielle", 1ère licence Biologie Médicale,
ISTM-Kinshasa, inédit, 2004-2005, p.288
TABLE DES MATIERES
PLAN GENERAL
i
DEDICACE
iii
REMERCIEMENTS
iv
AVANT-PROPOS
v
INTRODUCTION
1
PREMIERE PARTIE : DONNEES DE LA
LITTERATURE
3
CHAPITRE I : RAPPEL
ANATOMO-PATHOLOGIQUE DU FOIE
3
I.1 Anatomie fonctionnelle du foie
3
I.2 Physiologie et fonction du foie
4
I.3 Les maladies du foie
5
I.3.1 Les hépatites
5
I.3.2 Les cirrhoses
8
I.4 Exploration biologique de la fonction
hépatique
9
Chapitre II : GENERALITE SUR
TUBERCULOSE
14
II.1 Définitions & historique de
la tuberculose
14
II.1.1 Définitions
14
II.1.2 Historique
15
II.2 Etiologie et infection tuberculeuse
16
II.3 Le bacille de Koch
18
II.3.1 Culture et isolement
18
II.3.2 Physiopathologie et
Phénomène de Koch
19
II.3.3 Transmission du bacille de la
tuberculose
20
II.3.4 Émergence de Tuberculoses
ultra-résistantes
21
II.4 Epidémiologie de la
tuberculose
22
Chapitre III : DIAGNOSTIC ET
TRAITEMENT DE LA TUBERCULOSE
26
III.1 Diagnostic de la tuberculose
26
III.1.1 Examens cliniques de la
tuberculose
26
III.1.2 Imagerie
médicale
28
III.1.3 Examens biologiques de la
tuberculose
29
III.2 Traitement de la tuberculose
34
III.2.1 Catégorisation
34
III.2.2 Régime de
traitement :
36
III.2.3 Conséquences du
traitement antituberculeux
41
IIème PARTIE :
PRATIQUE AU LABORATOIRE
43
Chapitre IV : MATERIEL ET METHODES
43
IV.1 Matériel
43
IV.1.1 Echantillonnage
43
IV.1.2 Cadre et période
d'étude
44
IV.1.3 Equipement et réactifs de
laboratoire
44
IV.2 Méthodes
45
IV.2.1 Choix des méthodes de
dosage
45
IV.2.2 Dosage de la ã-GT et des
transaminases
46
IV.2.3 Analyse statistique des
résultats
47
Chapitre V : RESULTATS &
DISCUSSION
49
V.1 Présentation des
résultats
49
V.2 Discussion
51
CONCLUSION
53
RECOMMANDATIONS
54
BIBLIOGRAPHIE
55
TABLE DES MATIERES
57
ANNEXES 59
ANNEXES
ANNEXE 1 : RESULTAT DE DOSAGE
A. Activité enzymatique des sujets
témoins (non tuberculeux)
|
N°
|
Sexe
|
Age (ans)
|
GOT
(UI/litre)
|
GPT
(UI/litre)
|
ã-GT
(UI/litre)
|
|
1. M
|
58
|
11,1
|
10,7
|
16
|
|
2. M
|
38
|
12,6
|
10,1
|
21
|
|
3. F
|
24
|
19,3
|
23,4
|
31
|
|
4. F
|
30
|
27,0
|
6,2
|
19
|
|
5. F
|
19
|
14,6
|
15,0
|
20
|
|
6. M
|
21
|
19,0
|
16,0
|
17
|
|
7. M
|
53
|
28,1
|
26,2
|
33
|
|
8. F
|
27
|
17,7
|
17,1
|
12
|
|
9. M
|
40
|
24,3
|
36,1
|
31
|
|
10. M
|
32
|
6,5
|
17,1
|
27
|
|
11. M
|
41
|
26,6
|
37,3
|
36
|
|
12. F
|
41
|
22,7
|
19,2
|
29
|
|
13. F
|
39
|
11,0
|
13,1
|
21
|
|
14. M
|
52
|
20,9
|
17,6
|
32
|
|
15. M
|
35
|
15,1
|
9,2
|
22
|
|
16. M
|
58
|
14,3
|
11,1
|
10
|
|
17. F
|
46
|
13,1
|
5,6
|
38
|
|
18. M
|
40
|
36,0
|
41,2
|
93
|
|
19. F
|
32
|
14,4
|
6,7
|
3
|
|
20. M
|
26
|
10 ,1
|
16,2
|
55
|
|
21. M
|
41
|
31,1
|
45,0
|
129
|
|
22. M
|
56
|
20,5
|
14,8
|
43
|
|
23. M
|
20
|
23,3
|
24,3
|
53
|
|
24. F
|
26
|
20,6
|
24,4
|
15
|
|
N°
|
Sexe
|
Age (ans)
|
GOT
(UI/litre)
|
GPT
(UI/litre)
|
ã-GT
(UI/litre)
|
|
25. M
|
31
|
18,7
|
24,0
|
109
|
|
26. M
|
29
|
20,2
|
16,3
|
31
|
|
27. M
|
40
|
31,9
|
21,4
|
13
|
|
28. M
|
36
|
39,1
|
32 ,8
|
37
|
|
29. M
|
37
|
40,0
|
24,4
|
51
|
|
30. M
|
32
|
35,3
|
39,6
|
54
|
|
31. M
|
47
|
33,9
|
29,2
|
29
|
|
32. F
|
34
|
31,1
|
12,6
|
63
|
|
33. M
|
42
|
33,3
|
31,4
|
34
|
|
34. M
|
55
|
23,0
|
17,4
|
48
|
|
35. M
|
35
|
26,9
|
20,8
|
32
|
|
36. M
|
28
|
12,5
|
15,0
|
21
|
|
37. M
|
37
|
20,1
|
15,3
|
40
|
|
38. M
|
39
|
27,6
|
22,2
|
28
|
|
39. M
|
43
|
23,0
|
24,8
|
38
|
|
40. F
|
41
|
36,3
|
18, 9
|
15
|
|
41. F
|
39
|
40,1
|
18,3
|
20
|
|
42. M
|
42
|
30,6
|
11,7
|
14
|
|
43. F
|
26
|
24,3
|
20,1
|
8
|
|
44. M
|
34
|
31,3
|
13,2
|
54
|
|
45. M
|
46
|
47,0
|
28,4
|
32
|
|
46. F
|
35
|
19,6
|
11,9
|
16
|
|
47. M
|
57
|
40,4
|
24,4
|
20
|
|
48. F
|
43
|
56,0
|
16,3
|
18
|
|
49. M
|
29
|
31,2
|
18,9
|
24
|
B. Présentation des résultats de dosage
au début et au 6ème mois du traitement
N°
|
Code
|
Sexe
|
Age (ans)
|
Premier dosage
|
Deuxième dosage
|
GOT (UI/litre)
|
GPT (UI/litre)
|
ã-GT (UI/litre)
|
Rapport GOT/GTP
|
GOT (UI/litre)
|
GPT (UI/litre)
|
ã-GT (UI/litre)
|
Rapport GOT/GTP
|
|
1. 258 B
|
F
|
29
|
47,2
|
30,7
|
39
|
1,54
|
31,3
|
16,8
|
38
|
1,86
|
|
2. 273 B
|
F
|
16
|
26,6
|
14,3
|
37
|
1,86
|
32,1
|
6,4
|
34
|
5,02
|
|
3. 274 B
|
M
|
38
|
44,3
|
25,9
|
53
|
1,71
|
41,0
|
30,9
|
39
|
1,33
|
|
4. 285 B
|
M
|
55
|
27,8
|
12,7
|
8
|
2,19
|
26,8
|
8,5
|
25
|
3,15
|
|
5. 289 B
|
M
|
48
|
25,7
|
11,7
|
44
|
2,20
|
24,0
|
13,1
|
32
|
1,83
|
|
6. 291 B
|
M
|
41
|
22,8
|
14,1
|
12
|
1,62
|
16,1
|
10,9
|
28
|
1,48
|
|
7. 294 B
|
M
|
29
|
21,8
|
19,6
|
43
|
1,11
|
38,7
|
11,8
|
36
|
3,28
|
|
8. 295 B
|
M
|
40
|
26,2
|
11,3
|
32
|
2,32
|
22,4
|
5,8
|
93
|
3,86
|
|
9. 302 B
|
M
|
34
|
33,5
|
12,9
|
36
|
2,60
|
30,8
|
6,9
|
17
|
4,46
|
|
10. 303 B
|
M
|
30
|
39,8
|
21,7
|
49
|
1,83
|
40,2
|
21,6
|
45
|
1,86
|
|
11. 304 B
|
M
|
23
|
39,8
|
37,6
|
44
|
1,06
|
42,3
|
39,0
|
43
|
1,08
|
|
12. 305 B
|
F
|
30
|
39,0
|
21,4
|
45
|
1,82
|
24,8
|
19,7
|
57
|
1,26
|
|
13. 307 B
|
M
|
24
|
12,1
|
14,8
|
24
|
0,82
|
22,0
|
10,1
|
14
|
2,18
|
|
14. 233Li
|
F
|
24
|
15,0
|
15,0
|
7
|
1,00
|
12,4
|
10,3
|
9
|
1,20
|
|
15. 234 Li
|
F
|
43
|
15,2
|
7,3
|
57
|
2,08
|
32,1
|
27,0
|
47
|
1,19
|
|
16. 235 Li
|
F
|
65
|
19,4
|
26,8
|
32
|
0,72
|
19,7
|
10,5
|
27
|
1,88
|
|
17. 238 Li
|
M
|
16
|
35,0
|
39,0
|
35
|
0,90
|
42,1
|
38,6
|
22
|
1,09
|
|
18. 243 li
|
M
|
21
|
35,9
|
17,2
|
29
|
2,09
|
29,2
|
12,3
|
30
|
2,37
|
|
19. 248 Li
|
M
|
20
|
36,8
|
27,4
|
66
|
1,34
|
30,0
|
17,2
|
28
|
1,74
|
|
20. 251 Li
|
F
|
27
|
4,7
|
11,1
|
51
|
0,42
|
20,1
|
18,4
|
51
|
1,09
|
|
21. 254 Li
|
M
|
34
|
20,0
|
12,1
|
39
|
1,65
|
33,1
|
9,7
|
44
|
3,41
|
|
22. 256 Li
|
F
|
58
|
20,3
|
6,3
|
19
|
3,22
|
40,0
|
17,4
|
39
|
2,30
|
|
23. 258 Li
|
F
|
26
|
4,9
|
7,3
|
17
|
0,67
|
10,2
|
8,8
|
13
|
1,16
|
|
24. 262 Li
|
M
|
23
|
10,0
|
24,1
|
32
|
0,41
|
24,1
|
12,6
|
24
|
1,91
|
|
25. 263 Li
|
F
|
18
|
9,1
|
29,9
|
20
|
0,30
|
27,0
|
25,5
|
27
|
1,06
|
|
26. 264 Li
|
M
|
23
|
31,0
|
18,0
|
40
|
1,72
|
30,0
|
16,3
|
28
|
1,84
|
|
27. 265 Li
|
F
|
25
|
12,4
|
10,3
|
4
|
1,20
|
28,7
|
24,6
|
20
|
1,17
|
|
28. 266 Li
|
F
|
33
|
16,6
|
3,4
|
14
|
4,88
|
17,0
|
10,1
|
9
|
1,68
|
|
29. 271 Li
|
F
|
24
|
19,0
|
10,6
|
43
|
1,79
|
22,3
|
11,6
|
27
|
1,92
|
|
30. 200 P
|
M
|
40
|
25,0
|
9,7
|
81
|
2,58
|
35,3
|
29,7
|
53
|
1,19
|
|
31. 217 P
|
M
|
47
|
16,9
|
19,8
|
55
|
0,85
|
35,2
|
30,1
|
45
|
1,17
|
|
32. 230P
|
M
|
50
|
21,0
|
26,2
|
38
|
0,80
|
32,5
|
13,5
|
88
|
2,41
|
|
33. 233 P
|
F
|
21
|
10.5
|
15,0
|
13
|
0,70
|
12,6
|
10,3
|
9
|
1,22
|
|
34. 235 P
|
M
|
38
|
24,9
|
23,0
|
44
|
1,08
|
17,3
|
32,
|
45
|
0,54
|
|
35. 236 P
|
F
|
34
|
9,2
|
8,6
|
17
|
1,07
|
14,3
|
10,9
|
20
|
1,31
|
|
36. 241 P
|
M
|
41
|
29,0
|
19,1
|
36
|
1,52
|
87,8
|
83,4
|
360
|
1,05
|
|
37. 242 P
|
M
|
63
|
14,0
|
9,9
|
65
|
1,41
|
24,2
|
6,0
|
38
|
4,03
|
|
38. 253 P
|
F
|
21
|
7.2
|
5,0
|
14
|
1,44
|
34,0
|
10,5
|
13
|
3,24
|
|
39. 255 P
|
F
|
38
|
13,2
|
10,1
|
19
|
1,31
|
75,1
|
23,9
|
42
|
3,14
|
|
40. 258 P
|
F
|
20
|
22,2
|
15,9
|
68
|
1,40
|
62,2
|
18,9
|
70
|
3,29
|
|
41. 265 P
|
M
|
31
|
6,5
|
7,7
|
56
|
0,84
|
45,9
|
26,8
|
46
|
1,71
|
|
42. 274 P
|
M
|
36
|
4,2
|
5,4
|
21
|
0,78
|
10,1
|
7,9
|
13
|
1,28
|
|
43. 281 P
|
M
|
48
|
7,2
|
20,8
|
48
|
0,35
|
33,8
|
8,0
|
31
|
4,23
|
|
44. 282 P
|
M
|
26
|
20,7
|
13,6
|
64
|
1,52
|
41,8
|
22,5
|
52
|
1,86
|
|
45. 284 P
|
F
|
42
|
3,1
|
9,1
|
11
|
0,34
|
27,0
|
9,0
|
17
|
3,00
|
|
46. 285 P
|
F
|
20
|
10,7
|
3,5
|
12
|
3,06
|
24,5
|
4,6
|
10
|
5,33
|
|
47. 286 P
|
M
|
50
|
35,3
|
11,1
|
79
|
3,18
|
41,2
|
25,2
|
53
|
1,63
|
|
48. 295 P
|
M
|
39
|
34,7
|
16,4
|
81
|
2,12
|
45,3
|
17,1
|
47
|
2,65
|
|
49. 302 P
|
F
|
32
|
3,9
|
2,5
|
19
|
1,56
|
31,0
|
13,4
|
19
|
2,31
|
|
50. 307 P
|
M
|
36
|
18,3
|
15,5
|
46
|
1,18
|
40,1
|
12,6
|
26
|
3,18
|
Annexe 2 : Quelques tableaux
synthétiques de la biochimie des maladies hépatiques33(*)

Augmentation des SGPT / ALAT34(*)

Source :
http://www.esculape.com/hepatogastro/hepatopathie_biochim.html
Cholestase35(*)

Source :
http://www.esculape.com/hepatogastro/cholestase2001.html
Augmentation des phosphatases alcalines et/ou des
Gamma-GT36(*)

HEPATITES MEDICAMENTEUSES37(*)

ALCOOLISME CHRONIQUE38(*)

NB :
Le dosage de
CDT : Carbohydrate
Déficient Transferrine est plus spécifique de la
consommation alcoolique que les gamma-GT.
![]() ![]()
* 1 Agence de la santé
publique du Canada, Tuberculose infectieuse active, PHAC/ASPC-FS-17F
(02-2008)
* 2 Yves Deugnier,
Anatomie-physiologie du foie, Université Rennes 1,
« Polycopié de Sémiologie du foie et des voies
biliaires », 2005.
* 3
http://www.snfge.org/
* 4
http://www.vulgaris-medical.com/encyclopedie/
* 5
http://www.ma.uni-heidelberg.de/inst/ikc/ikc-quotienten.html
* 6 Carola Strang et
alliés, Larousse médicale, Nouvelle édition, Paris Cedex,
2006, p. 1069-1071 ;
* 7
http://www.phac-aspc.gc.ca/tbpc-latb/fa-fi/pdf/fa-fi-fra.pdf
(Agence de la santé Publique du Canada, Fiche d'information sur la
tuberculose, 2008).
* 8
http://www.fondationdamien.org/les_maladies_cibles/tuberculose.cfm
* 9 Organisation Mondiale de la
Santé, Aide-mémoire EURO/01/07, Genève, Berlin et
Copenhague mars 2007.
* 10
http://www.fondationdamien.org/les_maladies_cibles/tuberculose.cfm
* 11
http://www.phac-aspc.gc.ca/tbpc-latb/fa-fi/infecttb-fra.php
* 12
http://www.phac-aspc.gc.ca/tbpc-latb/fa-fi/pdf/fa-fi-fra.pdf
(Fiche d'information sur la tuberculose, Agence de la santé Publique du
Canada, 2008.
* 13
http://www.phac-aspc.gc.ca/tbpc-latb/fa-fi/index-fra.php
* 14
http://www.vulgaris-medical.com/encyclopedie/koch-(bacille-de)-5387.html
* 15
http://www.microbes-edu.org/etudiant/mycobacterium1.htm
* 16
http://www.microbes-edu.org/etudiant/mycobacterium1.htm
* 17
http://www.sante.gouv.fr/htm/dossiers/tuberculose/generalites.htm
: op. cit.
* 18 Carola Strang et al., op.
cit
* 19
http://www.pntrdc.canalblog.com/
* 20
http://www.santepub.fr/blog/spip.php?article36
(Eléments issus du
rapport
2007 de l'OMS à propos de la lutte contre la tuberculose :
journée mondial de lutte contre la tuberculose, le 24 mars 2007)
* 21
http://www.sante.gouv.fr/htm/dossiers/tuberculose/generalites.htm
* 22 F. Boulahbal et P.
Chaulet, La Tuberculose en Afrique : épidémiologie et
mesures de lutte, Médecine Tropicale, 2004.
* 23 Union Africaine :
Rapport du sommet spécial de l'Union Africaine sur le VIH, la
Tuberculose et le Paludisme, Abuja, mai 2006, p. 7
* 24 Programme National de
Lutte contre la Lèpre et la Tuberculose (PNLT) : Situation
épidémiologique de la Tuberculose et de la Lèpre en RDC,
Kinshasa, 2007.
* 25 Programme National de
lutte contre la Tuberculose, Le Médecin face à la tuberculose
dans la stratégie de renforcement du système de santé,
Draft, Kinshasa, 2008, p.9-11
* 26 Carola Strang et al., op.
cit.
* 27
http://www.phac-aspc.gc.ca/tbpc-latb/fa-fi/pdf/fa-fi-fra.pdf :
op cit.
* 28
http://www.med.univ-rennes1.fr/excomp/pneumo78.html
* 29 Bureau National de
Tuberculose (BNT) au Zaïre, Programme National Anti-tuberculeux
Intégré « P.A.T.I. »,
2ème édition, 1989, p. 62-94.
* 30 Programme National de
Lutte contre la Tuberculose (PNT), Module sur le P.A.T.I. IV, version
provisoire, inédit, Kinshasa, août 2007
* 31 Programme National
Anti-tuberculeux Intégré (P.A.T.I.), op cit.
* 32 Kaplan A et Al., 1984,
Gendler S. -GT, Clin Chem the C.V. Mosby, Saint Louis, Torronto, Princeton, pp
1220-1223 (CYPRESS DIAGNOSTICS :
www.doagnostic.be)
* 33
http://www.esculape.com/hepatogastro/hepatopathie_biochim.html
* 34
http://www.esculape.com/hepatogastro/sgpt_augent2001.html
* 35
http://www.esculape.com/hepatogastro/cholestase2001.html
* 36
http://www.esculape.com/hepatogastro/pal-ggt2001.html
* 37
http://www.esculape.com/hepatogastro/hepatiteiatro_2001.html
* 38
http://www.esculape.com/hepatogastro/alcoolism_chronik2001.html
|
|



