|
HAUTE ECOLE LOUVAIN EN HAINAUT
Catégorie
technique
Type long
Master en sciences de l'ingénieur industriel
finalité Electromécanique
Etude de l'initiation et de la
propagation de la détonation dans
les aérosols de kérosène liquide
Directeur de stage : Bernard VEYSSIERE
Travail de fin d'étude présenté par
Ghiles BERREFAS en vue de l'obtention du grade de Master en sciences de
l'ingénieur industriel finalité
Electromécanique
Avant-propos
Les travaux de recherche présentés dans ce
travail de fin d'étude ont été effectués à
l'institut P' dans le département D2 « Fluides, Thermique,
Combustion » au sein de l'axe de détonique situé sur le site
du Futuroscope.
Je tiens à remercier Monsieur Bernard VEYSSIERE,
directeur au sein de l'axe détonique en sa qualité de tuteur et
je le remercie pour m'avoir proposé cette thématique de recherche
et de m'avoir encadré durant ces 5 mois de stage. Je suis
particulièrement reconnaissant par sa disponibilité et l'ensemble
des précieux conseils apportés au cours du stage.
Je voudrais remercier particulièrement Monsieur Vincent
MONTASSIER, qui a énormément investi, de son temps et de sa
personne, plus qu'indispensable à la réalisation des dispositifs
expérimentaux. Je lui exprime également ma gratitude pour son
partage de connaissances et ses compétences techniques mais aussi pour
son sens de l'humour et le travail dans la bonne humeur.
Je remercie également Alain CLAVERIE pour ses
explications du système de fonctionnement par PDI. Mes remerciements
vont aussi à Florent VIROT et Pierre VIDAL pour leurs aides dans
l'analyse de la structure cellulaire et les notions de différents
régimes de détonation. J'ai réellement
apprécié les échanges avec mon collègue
thésard Stéphane BOULAL avec qui j'ai passé de très
bons moments durant ce stage.
Je remercie l'ensemble du corps professoral de l'ISICHt pour
m'avoir transmis les connaissances de base qui m'ont permis d'effectuer ce
stage. Plus particulièrement, je voudrais exprimer ma gratitude envers
Monsieur Adrien POURBAIX et Monsieur Christophe SPENS, professeurs à la
Haute Ecole Louvain en Hainaut, ISICht pour leur suivi, je les remercie d'avoir
été mes coordinateurs de stage en institut.
Le travail au cours de ce stage était laborieux mais
très agréable car il s'est déroulé dans de
très bonnes conditions. Chacune des personnes que j'ai
rencontrées durant ce stage, ont contribué à leur
manière, à ce que la tâche soit agréable. Je suis
ainsi reconnaissant envers tout le personnel du laboratoire qui a
consacré, en plus de l'attribution normale de ses tâches, du temps
et de l'énergie pour effectuer un dépannage. Merci pour la
contribution de chacun.
Enfin, je remercie toutes les personnes, familles et amis,
pour votre soutien tout au long de ces années d'études et votre
collaboration afin de m'aider au mieux dans la rédaction de ce
mémoire.
Table des matières
Introduction 1
Chapitre 1 5
1 Détonations en phase gazeuse et détonations
hétérogènes gouttelettes liquide/gaz 5
1.1. Généralités sur les détonations
en phase gazeuse 5
1.1.1. Introduction 5
1.1.2. Modélisation de la détonation [Chapman, 1899
; Jouguet 1905] 5
1.1.3. Modèle de Zeldovich - Von Neumann - Döring
(ZND) 9
1.2. Détonation en milieu hétérogènes
gaz/gouttelettes liquides 10
1.2.1. Les détonations hétérogènes
10
1.2.2. Synthèse des principaux travaux antérieurs
10
1.3. La structure cellulaire 12
1.3.1. Structure cellulaire tridimensionnelle 12
1.3.2. Structure cellulaire des détonations
hétérogènes 13
Chapitre 2 15
2. Influence des mécanismes de
désintégration et de vaporisation des gouttelettes sur la
détonation
des aérosols de carburants liquides 15
2.1 Propagation d'une détonation en présence
d'aérosols de gouttelettes liquides 15
2.2 Mode et régime de désintégration de
gouttelettes liquides 16
2.2.1 Désintégration d'un jet liquide 16
2.2.2 Modes et régimes de désintégration de
gouttelettes liquides 18
2.2.2.1 Modèle d'atomisation secondaire 18
2.2.2.2 Modèle de Reitz Diwakar [Reitz, 1986] 18
2.2.3 Caractéristiques des gouttelettes et leur mesure
19
2.2.3.1 Grandeurs caractéristiques des gouttelettes issus
d'un aérosol 19
2.2.3.2 Techniques de mesures granulométrique de
l'aérosol 21
2.3 Mécanisme de vaporisation des gouttelettes liquides
21
2.4 Diamètre de gouttelette et déficit de
célérité de détonation
hétérogène 23
Chapitre 3 25
3. Montage expérimental 25
3.1 Introduction 25
3.2 Le tube à détonation 25
3.3 Le tube à choc 28
3.4 Génération des aérosols de gouttelettes
liquides 28
3.4.1. Les atomiseurs ultrasoniques 29
3.4.2. Le générateur 30
3.4.3. Alimentation de l'atomiseur 30
3.5 Dispositifs de mesure 31
3.5.1 Granulométrie de l'aérosol 31
3.5.2 Mesure de la célérité et de la
pression de détonation 31
3.5.3 Enregistrement de la structure cellulaire 32
3.6 Système de commande et protocole 32
3.6.1 Système de commande 32
3.6.2 Protocole d'essai 33
Chapitre 4 35
4 Caractérisation de la distribution
granulométrique des gouttelettes d'un aérosol 35
4.1 Introduction 35
4.2 Méthode de mesure granulométrique par PDI
(Phase Doppler Interferometry) 35
4.2.1 Principe de mesure par PDI 35
4.2.2 Montage expérimental et protocole d'essai 39
4.3 Etude de la distribution granulométrique des
gouttelettes produites par les atomiseurs 41
4.3.1 Atomiseur ultrasonique 41
4.3.2 Variation du D10 et D32 en fonction du débit
d'oxydant 44
4.3.3 Conclusions 46
Chapitre 5 47
5 Les mélanges réactifs 47
5.1 Introduction 47
5.2 Produits étudiés 47
5.3 Caractéristiques de détonation CJ 50
5.4 Détermination de la richesse du mélange 51
6. Etude expérimentale de l'influence de la taille des
gouttelettes sur la détonation d'aérosols de
carburants liquides 53
6.1 Introduction 53
6.2 Initiation de la détonation par un tube à choc
(booster) 53
6.3 Détonation dans le mélange d'aérosol de
gouttelettes de kérosène/air 55
6.3.1 Formation de la détonation 55
6.3.2 Célérité de détonation 56
6.3.3 Pression de détonation 61
6.3.4 Structure cellulaire de détonation 62
6.3.5 Influence de la pression initiale du booster 63
6.3.5.1 Célérité de détonation 64
6.3.5.2 Pression de détonation 65
6.3.6 Synthèse des résultats obtenus pour le
mélange kérosène/air 66
6.3.7 Bilan pour le mélange kérosène/air
68
6.4 Détonation dans le mélange d'aérosol de
gouttelettes de kérosène/air suroxygéné 69
6.4.1 Richesse r = 1 69
a. Formation de la détonation 69
b. Célérité de la détonation 70
c. Pression de détonation 71
6.4.2 Richesse r = 1,3 72
a. Célérité de détonation 72
b. Pression de la détonation 73
6.4.3 Synthèse des résultats obtenus pour les
mélanges kérosène/air suroxygéné 74
Synthèse et conclusion 75
Bibliographie 77
Annexes 79
Annexe AI : Etude à l'état Chapman-Jouguet (CJ)
79
Annexe AII : Calibrage du système d'atomisation de
gouttelettes et détermination de la richesse 83
a. Introduction 83
b. Calibrage massique 83
c. Détermination de la richesse 85
i. Introduction 85
ii. Méthodologie de calcul de la richesse 85
d. Vitesse et temps de balayage dans le tube 92
Annexe AIII: Specification Jet-A1 de l'American Society for
Testing and Materials (ASTM) 96
Annexe AIV : Calcul des caractéristiques de la
bouteille de mélange O2 + 2 N2 par la méthode des
pressions partielles via EES. 97
Table des figures
FIGURE 1.1 - L'ONDE DE DETONATION DANS DIFFERENTS SYSTEMES DE
COORDONNEES (A) PAR RAPPORT AU
LABORATOIRE ET (B) PAR RAPPORT A L'ONDE 6
FIGURE 1.2 - DROITE DE RAYLEIGH-MICHELSON ET ADIABATIQUE DE
CRUSSARD DANS LE PLAN (p, y) 8
FIGURE 1.3 - PRINCIPE DU MODELE DE ZEDOVICH VON NEUMAN DORING
9
FIGURE 1.4 - DROITE DE RAYLEIGH-MICHELSON, ADIABATIQUE
D'HUGUONIOT ET ADIABATIQUE DE CRUSSARD
DANS LE PLAN (p, y) 10
FIGURE 1.5 - SCHEMA
D'UNE CELLULE DE DETONATION ET DE LA VARIATION DE LA CELERITE DE L'ONDE DE
DETONATION LE LONG DE L'AXE DE LA CELLULE 12
FIGURE 2.1 - DESCRIPTION SCHEMATIQUE D'UNE DETONATION DANS UN
AEROSOL DE GOUTTELETTES 15
FIGURE 2.2 - MODE DE FRAGMENTATION MECANIQUE D'UN JET LIQUIDE
DANS UN MILIEU GAZEUX SELON REITZ
[1987] 17
FIGURE 2.3 - SCHEMA DESCRIPTION DU BAG BREAKUP 18
FIGURE 2.4 - SCHEMA DESCRIPTION DU STRIPPING BREAKUP 19
FIGURE 3.1 - SCHEMA DU MONTAGE EXPERIMENTAL 26
FIGURE 3.2 - MONTAGE EXPERIMENTAL 27
FIGURE 3.3 - GAMME DE FREQUENCE ULTRASONIQUE ET DESINTEGRATION
D'UN FILM LIQUIDE PAR ATOMISATION
ULTRASONIQUE 29
FIGURE 3.4 - GENERATEUR DE GOUTTELETTES LIQUIDES (ATOMISEUR
ULTRASONIQUE) 30
FIGURE 3.5 - TABLEAU DE COMMANDE DU DISPOSITIF D'ALIMENTATION DE
DEBIT EN OXYDANT (ROTAMETRE
D'OXYDANT A DROITE) 31
FIGURE 3.6 - TABLEAU DE COMMANDE ET DE CONTROLE DE SECURITE 33
FIGURE 4.1 - PRINCIPE DE MESURE GRANULOMETRIQUE PAR PDI (PHASE
DOPPLER INTERFEROMETER) 36
FIGURE 4.2 - INTERACTION DES FAISCEAUX LASERS AVEC UNE
GOUTTELETTE LIQUIDE 37
FIGURE 4.3 - PRINCIPE DE DETECTION DES RAYONS LUMINEUX REFRACTES
37
FIGURE 4.4 - VARIATION DU DEPHASAGE EN FONCTION DE LA TAILLE DES
GOUTTELETTES 38
FIGURE 4.5 - PRINCIPE DE MESURE DE VELOCIMETRIE DES GOUTTELETTES
39
FIGURE 4.6 - DISPOSITIF DE MESURE GRANULOMETRIQUE PAR PDI 40
FIGURE 4.7 - SPECTRE GRANULOMETRIQUE D'UN AEROSOL D'EAU A UNE
COTE D'OBSERVATION Z = 160 MM,
????AIR = 1,42 M3/H 42
FIGURE 4.8
- SPECTRE GRANULOMETRIQUE D'UN AEROSOL DE (A) KEROSENE JET-A1, (B) DODECANE A
UNE COTE
D'OBSERVATION Z = 160 MM, ????AIR = 1,42
M3/H 42
FIGURE 4.9 - EVOLUTION DE LA GRANULOMETRIE D'AEROSOLS
D'EAU GENERES PAR L'ATOMISEUR EN FONCTION DU
DEBIT D'AIR POUR DIFFERENTES COTES D'OBSERVATION Z 44
FIGURE 4.10 - VARIATION DE LA GRANULOMETRIE D'AEROSOLS DE
KEROSENE ET DODECANE GENERES PAR
L'ATOMISEUR EN FONCTION DE LA RICHESSE A UNE COTE D'OBSERVATION Z
= 16 CM 45
FIGURE 5.1 - EVOLUTION DE LA CELERITE IDEALE CJ DE DETONATION DU
MELANGE KEROSENE ~ AIR EN
FONCTION DE LA RICHESSE 50
FIGURE 6.1- EVOLUTION DE LA CELERITE DE LA DETONATION EN FONCTION
DE LA DISTANCE DE PROPAGATION
DANS LE TUBE PRINCIPALE INITIE PAR UN BOOSTER SEUL DE
PREMELANGE C2H4/O2 54
FIGURE 6.2 - SIGNAUX DE PRESSION LE LONG DU TUBE
PRINCIPAL AVEC BOOSTER SEUL DE PREMELANGE C2H4/O2
SOUS 2 BARS DE PRESSION INITIALE 54
FIGURE 6.3 - PROFILS DE
PRESSION ET DIAGRAMME DE MARCHE, ENREGISTRES EN K1, K2, K3, K4, K5, K6 ET K7
DE LA DETONATION DU MELANGE KEROSENE/AIR, C11H22 + 16,5 (O2 +
3.76); R=1,1 ET D0 = 5uM 55
FIGURE 6.4 - CELERITE MOYENNE DU FRONT EN
FONCTION DE LA DISTANCE DE PROPAGATION ET ENREGISTREMENT
DE LA STRUCTURE CELLULAIRE POUR LE MELANGE KEROSENE/AIR AVEC
UNE RICHESSE = 1,1 56
FIGURE 6.5 - ENREGISTREMENT DE LA STRUCTURE CELLULAIRE DU MELANGE
KEROSENE/AIR - R=1,1 - TEST 1 57
FIGURE 6.6 - PROFILS DE PRESSION ET DIAGRAMME DE MARCHE,
ENREGISTRES EN K1, K2, K3, K4, K5, K6 ET K7
DE LA DETONATION DU MELANGE KEROSENE/AIR, C11H22 + 16,5 (O2 +
3.76); R=1,3 ET D0 = 5uM 58
FIGURE 6.7 - CELERITE MOYENNE DU FRONT EN
FONCTION DE LA DISTANCE DE PROPAGATION ET ENREGISTREMENT
DE LA STRUCTURE CELLULAIRE POUR LE MELANGE KEROSENE/AIR AVEC
UNE RICHESSE = 1,3 59
FIGURE 6.8 - ENREGISTREMENT DE LA STRUCTURE CELLULAIRE DU MELANGE
KEROSENE/AIR - R=1,3 - TEST 4 60
FIGURE 6.9 - ENREGISTREMENT DE LA STRUCTURE CELLULAIRE DU MELANGE
KEROSENE/AIR - R=1,3 - TEST 5 60
FIGURE 6.10 - ENREGISTREMENT DE LA STRUCTURE CELLULAIRE DU
MELANGE KEROSENE/AIR - R=1,3 - TEST 6 60
FIGURE 6.11 - PROFILS DE PRESSIONS DES CAPTEURS K4, K5, K6 ET K7
EN FIN DE PROPAGATION DANS LE TUBE A
DETONATION POUR LE MELANGE KEROSENE/AIR AVEC UNE RICHESSE =
1,3 61
FIGURE 6.12 - PRINCIPE DE DETERMINATION DE LA VALEUR EXPERIMENTALE DE
LA PRESSION DE DETONATION PEXP
62
FIGURE 6.13 - CELERITE DU FRONT DE DETONATION EN FONCTION
DE LA DISTANCE DE PROPAGATION DANS LE TUBE A DETONATION POUR LE MELANGE
KEROSENE/AIR AVEC UNE RICHESSE = 1,5 ET PRESSION BOOSTER 2
BARS. 63
FIGURE 6.14 - CELERITE DU FRONT DE DETONATION EN
FONCTION DE LA DISTANCE DE PROPAGATION DANS LE
TUBE A DETONATION POUR LE MELANGE KEROSENE/AIR AVEC UNE
RICHESSE = 1,5 ET BOOSTER DE 3 BARS. 64 FIGURE 6.15 - PROFILS DE PRESSIONS DES
CAPTEURS K4, K5, K6 ET K7 EN FIN DE PROPAGATION DANS LE TUBE A
DETONATION POUR LE MELANGE KEROSENE/AIR AVEC UNE RICHESSE =
1,5 ET BOOSTER DE 3 BARS 65
FIGURE 6.16 - EVOLUTION DE LA CELERITE MOYENNE
DE DETONATION EXPERIMENTALE DEXP EN FONCTION DE LA
RICHESSE DU MELANGE REACTIF KEROSENE/AIR 66
FIGURE 6.17 -
EVOLUTION DE LA PRESSION MOYENNE DE DETONATION EXPERIMENTALE PEXP EN FONCTION
DE LA
RICHESSE DU MELANGE DU MELANGE REACTIF KEROSENE/AIR
67
FIGURE 6.18 - EVOLUTION DE LA TAILLE DE LA CELLULE DE DETONATION EN
FONCTION DE LA RICHESSE DU
MELANGE DU MELANGE REACTIF KEROSENE/AIR 67
FIGURE 6.19 - PROFILS DE PRESSION ET DIAGRAMME DE MARCHE,
ENREGISTRES EN K1, K2, K3, K4, K5, K6 ET K7
DE LA DETONATION DU MELANGE KEROSENE + (O2+2N2); R=1 ET D0 =
5uM 69
FIGURE 6.20 - CELERITE DU FRONT DE DETONATION EN FONCTION DE LA
DISTANCE DE PROPAGATION DANS LE
TUBE A DETONATION DU MELANGE KEROSENE + (O2+2N2); R=1 ET D0 =
5uM 70
FIGURE 6.21 - PROFILS DE PRESSIONS DES CAPTEURS K4, K5, K6 ET K7 EN
FIN DE PROPAGATION DANS LE TUBE A
DETONATION DU MELANGE KEROSENE + (O2+2N2); R=1 ET D0 = 5uM
71
FIGURE 6.22 - CELERITE DU FRONT DE DETONATION EN FONCTION DE LA DISTANCE
DE PROPAGATION DANS LE
TUBE A DETONATION DU MELANGE KEROSENE + (O2+2N2); R=1,3 ET D0
= 5uM 72
FIGURE 6.23 - PROFILS DE PRESSIONS DES CAPTEURS K4, K5, K6 ET K7 EN
FIN DE PROPAGATION DANS LE TUBE A
DETONATION DU MELANGE KEROSENE + (O2+2N2); R=1,3 ET D0 = 5uM
73
FIGURE 6.24 - ENREGISTREMENT DE LA STRUCTURE CELLULAIRE DU MELANGE
KEROSENE + (O2 + 2 N2), R=1 -
TEST 10 74
FIGURE 6.25 - ENREGISTREMENT DE LA STRUCTURE
CELLULAIRE DU MELANGE KEROSENE + (O2 + 2 N2), R=1,3 -
TEST 11 74
FIGURE AII.1 - CALIBRAGE EN MASSE DE L'ATOMISEUR AVEC DE L'EAU A
DIFFERENTS DEBITS D'AIR DE REFERENCE
83
FIGURE AII.2 - EVOLUTION DE LA RICHESSE DU KEROSENE JET-A1 AVEC
LE DEBIT D'AIR POUR L'ATOMISEUR DE
GOUTTELETTES DE 5 uM ET COURBE DE TENDANCE DE TYPE PUISSANCE
88
FIGURE AII.3 - EVOLUTION DE LA RICHESSE DU DODECANE AVEC LE DEBIT D'AIR
POUR L'ATOMISEUR DE
GOUTTELETTES DE 5 uM ET COURBE DE TENDANCE DE TYPE PUISSANCE
90
FIGURE AII.4 - COMPARAISON DES PLAGES DE RICHESSE ENTRE LES ATOMISEURS
GENERANT DES TAILLES DE
GOUTTELETTES DE 5 uM ET 8uM (COURBE DE TENDANCE DE TYPE
PUISSANCE) 91
Table des tableaux
TABLEAU 3.1 - DISTANCES ENTRE CAPTEURS 31
TABLEAU 4.1 - GAMMES DE MESURE DE TAILLE ET DE VITESSE DES
GOUTTELETTES 36
TABLEAU 4.2 - RESULTATS DE MESURE AVEC L'ATOMISEUR 43
TABLEAU 5.1 - FORMULE CHIMIQUE DU KEROSENE CONVENTIONNEL 48
TABLEAU 5.2 - COMPARATIF DE QUELQUES CARACTERISTIQUES
CHIMIQUES ET PHYSIQUES ENTRE LE JET-A1 ET LE
C11H22 49
TABLEAU 5.3 - CARACTERISTIQUES PHYSIQUES ET CHIMIQUES DU
DODECANE 49
TABLEAU 5.4 - CELERITE ET PRESSION DE DETONATION CJ POUR
DIFFERENTS RATIO O2/N2 51
TABLEAU 6.1 - CONDITIONS EXPERIMENTALES DES DIFFERENTS TESTS
REALISES 53
TABLEAU A.1 - CARACTERISTIQUES DE DETONATION CJ POUR UN GAZ
POLYTROPIQUE A F CONSTANT SOUS
L'HYPOTHESE D'UN CHOC FORT 82
TABLEAU AII.1 - RESULTATS DE L'ETALONNAGE EN MASSE DE
L'ATOMISEUR AVEC DU DODECANE C12H26 84
TABLEAU AII.2 - RESULTATS DE L'ETALONNAGE EN MASSE DE
L'ATOMISEUR AVEC DU KEROSENE JET-A1 84
TABLEAU AII.3 - VALEURS DE RICHESSE DU KEROSENE JET-A1
OBTENUES POUR DIFFERENTS COUPLES DE
TRAVAIL (MJET-A1;MAIR) 87
TABLEAU AII.4 - RECAPITULATIF DES VALEURS DE RICHESSE DU
DODECANE C12H26 OBTENUES 90
TABLEAU AII.5 - VALEURS DE RICHESSE DU DODECANE OBTENUES DANS
LES TRAVAUX ANTERIEURS REALISES PAR
MODOU MAR (2012) 91
TABLEAU AII.6 - TEMPS DE MONTEE DES GOUTTELETTES AU SEIN DU
TUBE A DETONATION 93
TABLEAU AII.7 - NOMBRE DE REYNOLDS RE EN FONCTION DU DEBIT
D'AIR DE TRAVAIL 94
TABLEAU AIII.1 - SPECIFICATIONS ASTM DU KEROSENE JET-A1 96
Page | 1
Introduction
L'étude de la détonation dans les
aérosols de carburants liquides, dispersés sous forme
d'aérosols de fines gouttelettes, est un domaine d'étude
relativement récent qui intéresse la sécurité
industrielle, le domaine militaire et de défense ou encore le domaine
aéronautique notamment en propulsion.
En effet, pour optimiser la sécurité dans le
domaine de la propulsion aéronautique et spatiale, il est
nécessaire de mieux connaître le risque de détonation dans
le cas d'éclatement des réservoirs et de dispersion sous forme
pulvérisée. Il s'agit également d'éviter toutes
explosions accidentelles de suspensions d'aérosols de gouttelettes
combustibles. En 1975, l'explosion de l'usine chimique de Flixborough a
entrainé la vaporisation de 45 tonnes de cyclohexane chaud et sous
pression à la suite de la rupture d'une conduite engendrant des
dégâts dans un rayon d'un peu plus de 2km.
Concernant le domaine militaire, les premières
générations d'armes à effet de souffle furent
conçues à la fin des années 1960, mais c'est vers le
milieu des années 1970 qu'apparaissent les premières versions
d'armes plus efficaces, désignées sous l'appellation de FAE
(Fuel-Air Explosives). Récemment, des conceptions proches ont
été créées sous la désignation d'explosifs
thermobariques ou explosifs à effet de souffle augmenté. Dans ces
systèmes explosifs, un matériau combustible est dispersé
dans l'air, au moment de l'explosion initiale de la munition, afin de
créer un brouillard (poussière ou aérosols liquides). Ce
brouillard de combustible est mis en détonation et engendre une onde de
souffle qui génère de grandes surpressions, ainsi qu'une boule de
feu. Dans ce type d'armes, les niveaux de surpression peuvent atteindre 2 fois
la surpression créée par des armes conventionnelles.
Toutefois, l'application la plus intéressante concerne
le domaine de la propulsion et consiste à utiliser ce type de
système réactif hétérogène pour la
propulsion par onde de détonation. De nombreuses recherches en ce
domaine ont déjà été effectuées depuis les
années 40 mais c'est vers la fin des années 90 que les premiers
moteurs utilisant ce principe de fonctionnement fait l'objet de
développements dans le secteur aéronautique et spatial. Ces
moteurs seront connus sous le nom de moteur à détonation
pulsée (Pulsed Detonation Engine, PDE) ou moteur à
détonation rotative (RDE). Parmi les solutions envisagées pour
faire
Page | 2
fonctionner le PDE, l'utilisation d'aérosols de
gouttelettes liquides injectés dans la chambre de combustion est une
voie prometteuse.
Comparativement aux connaissances sur les détonations
gazeuses homogènes, les connaissances sur celles des mélanges
hétérogènes gaz-aérosols de gouttelettes liquides
sont limitées. Cela s'explique notamment en raison des
difficultés de réalisation d'expériences dans des
aérosols de caractéristiques bien contrôlées et
reproductibles et la complexité de la détonation dans ce type de
milieu. Modou MAR [2012] et Mohamed El-Amine BENHAMMED [2012], durant leur
thèse, ont tous deux contribué à la compréhension
des processus physiques et chimiques qui entrent en jeu dans les
détonations hétérogènes d'aérosols de
gouttelettes liquides d'hydrocarbures en atmosphère oxydante.
L'étude de la structure cellulaire de détonation s'est faite avec
une intention toute particulière car en ce domaine, les résultats
sont quasiment inexistants. MAR s'est concentré sur l'influence de la
granulométrie sur la détonation et BENHAMMED a
étudié l'influence de la cinétique chimique sur le
phénomène de détonation.
L'objectif de ce mémoire sera d'alimenter la base de
données existantes sur le sujet, et dont la nouveauté sera de
travailler avec un nouvel atomiseur permettant de produire des aérosols
de granulométrie théoriquement inférieur à 5 um.
Une autre nouveauté sera de travailler avec un carburant utilisé
en propulsion qui est le JET-A1 et, éventuellement, des monergols.
Ce travail de fin d'étude est organisé autour de
7 chapitres et scindé en deux parties. La première est
consacrée à l'état de l'art sur les détonations
organisée en deux chapitres :
Le chapitre 1 rappelle les notions générales des
détonations à travers une étude bibliographique. Les
différentes notions employées tout au long de ce mémoire
sont progressivement introduites.
Le chapitre 2 est consacré aux modes de
désintégration des gouttelettes par interaction avec une onde de
choc.
La deuxième partie est dédiée à
l'étude expérimentale des détonations de mélanges
hétérogènes et s'organisera autour de quatre chapitres
:
Le chapitre 3 décrit le dispositif expérimental
et les techniques d'analyse qui lui sont associées.
Page | 3
Le chapitre 4 présente la caractérisation
granulométrique des aérosols.
Le chapitre 5 détaille les mélanges
réactifs utilisés pour cette étude, la phase
d'étalonnage de l'atomiseur générant les gouttelettes
ainsi que le calcul des paramètres de travail (couple de débits,
richesse, vitesse, temps de balayage,...).
Le chapitre 6 présente les résultats
expérimentaux obtenus dans des aérosols de carburant liquides.
Enfin, ce travail de fin d'étude s'achèvera par
un chapitre de synthèse des résultats expérimentaux ainsi
qu'une conclusion.
Page | 4
Page | 5
Chapitre 1
1 Détonations en phase gazeuse et
détonations hétérogènes gouttelettes
liquide/gaz
1.1. Généralités sur les
détonations en phase gazeuse
1.1.1. Introduction
Dans les années 1870-1883, les premières
observations des détonations en phase gazeuse ont vu le jour. Ce n'est
qu'en 1881, que Berthelot et Vieille ainsi que Mallard et Le Chatelier mettent
en évidence un phénomène de propagation stationnaire
d'ondes supersoniques de combustion. Ce phénomène sera
nommé onde explosive et actuellement connu sous l'appellation de
détonation.
Le premier modèle de détonation voit le jour
avec Chapman [1889] et Jouguet [1905]. Ce modèle assimile la
détonation à une discontinuité monodimensionnelle plane se
propageant avec une célérité supersonique dans un fluide
réactif supposé parfait et qui transforme instantanément
le fluide réactif (milieu des gaz frais) en produits de
détonation c'est-à-dire en gaz brûlés à
l'équilibre thermodynamique dit état final « Chapman-Jouguet
» CJ.
Zeldovitch, Von Neumann et Döring ont proposé dans
les années 40, un modèle plus réaliste décrivant
l'onde de détonation plane et stationnaire comme étant une onde
de choc dont la propagation supersonique est entretenue par les
réactions chimiques qu'elle initie avec un certain délai.
1.1.2. Modélisation de la détonation
[Chapman, 1899 ; Jouguet 1905]
Le modèle Chapman-Jouget (CJ) assimile la
détonation à une surface de discontinuité plane,
d'épaisseur infiniment mince, perpendiculaire à
l'écoulement et totalement réactive qui se propage à la
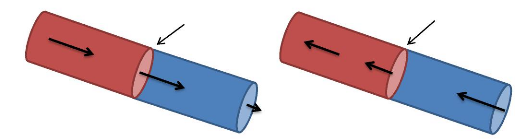
célérité D. L'onde de détonation ? se
déplace à une célérité de propagation D dans
le référentiel lié au laboratoire. (figure 1.1)
Gaz frais
????, ????, ????, ????
Gaz brûlés E
W1
D
????, ????, ????, ????
W0
Gaz brûlés
Gaz frais
????, ????, ????, ????
E
??1
????, ????, ????, ????
D
??0
référentiel lié au laboratoire (a)
référentiel lié à l'onde (b)
Figure 1.1 - L'onde de détonation dans
différents systèmes de coordonnées (a) par rapport au
laboratoire et (b) par rapport à l'onde
W0 = -(D - ??0) ???? W1 = -(D - ??1) (1.1)
avec : W0 et W1 qui sont respectivement la
vitesse du gaz frais et des gaz brûlés par rapport à l'onde
de détonation.
Ce modèle a pour hypothèses que :
· l'onde de détonation est supposée plane,
monodimensionnelle et stationnaire.
· le mélange réactif est parfait et
uniforme
· l'écoulement est adiabatique, sans pertes
d'énergie aux parois et les phénomènes de dissipation sont
négligés.
Les équations de conservation de masse, de
quantité de mouvement et d'énergie par rapport au
référentiel lié à l'onde découlent de ces
hypothèses :
??1W1 = ??0W0 (1.2)
??1W12 = ??0W02 (1.3)
h1 +
|
W2
1
2
|
= h0 +
|
W2
0 (1.4)
2
|
|
Page | 6
Page | 7
Où ??, ?? ???? h représentent respectivement la
masse volumique, la pression et l'enthalpie absolue. Par combinaison de
l'équation de conservation de masse (1.2) et celle de
la quantité de mouvement (1.3) dans un plan (??, ??)
(figure 1.2) avec ?? = 1/?? qui est le volume spécifique,
l'expression du débit massique est la suivante :
??2
-??2 = -??0 = 0
??0 2
|
??1 - ??0
= (1.5)
??1 - ??0
|
|
De cette équation (1.5) et par combinaison de (1.2) et
(1.3), on trouve les vitesses relatives à l'onde :
??1 - ??0
??0 = ??0v (1.6)
??0 - ??1
??1 - ??0
??1 = ??1v (1.7)
??0 - ??1
En substituant ??0 ???? ??1 à
l'équation de conservation d'énergie (1.4) à l'aide des
expressions (1.6) et (1.7), l'équation de l'adiabatique dynamique ou
adiabatique de Crussard dans le plan (??, ??) est obtenu :
1
h1 - h0 = 2 (??1 - ??0)(??0 + ??1) (1.8)
En ajoutant la chaleur de réaction ?????? = -??? h* =
h0* - h1* ( h* est l'enthalpie
de
^ ^
référence à la température ??*),
et l'enthalpie sensible h
|
telle que : h
|
= h - h*.
|
|
Il vient :
1
^ - h0
h1 ^ - ??P?? = 2 (??1 - ??0)(??0 + ??1) (1.9)
P

zone de détonations
fortes
zone de détonations
faibles
Pcj
Po
F
CJ
f
v
Page | 8
Figure 1.2 - Droite de Rayleigh-Michelson et
adiabatique de Crussard dans le plan (p, y)
L'étude de l'existence de solutions physiques au
système peut être illustrée par la représentation
dans le plan (P, y). Les droites de Rayleigh-Michelson (RM) et
l'adiabatique de Crussard (C) issues des conditions initiales du mélange
réactif, sont représentées à la figure 1.2. Trois
cas existent :
· la droite de Rayleigh-Michelson n'a pas d'intersection
avec l'adiabatique de Crussard, il n'y a donc pas de solution pour la
propagation de la détonation.
· la droite de Rayleigh-Michelson coupe la droite de
Crussard en deux points « F » et « f » se situant
respectivement dans une zone de détonations « fortes » et une
zone de détonations « faibles ». Il est à noter que les
détonations faibles n'ont jamais été observées
expérimentalement, seul le point F est observé pour des
célérités D supérieures à
Dcj.
· la droite de Rayleigh-Michelson est tangente à
l'adiabatique de Crussard au point CJ dit Chapman-Jouguet : cette solution
unique correspond à une propagation d'onde de détonation sonique
par rapport aux gaz brûlés, cela permet à l'onde de ne pas
être rattrapée par une onde de détente, et donc de se
propager de façon stable et autonome. En ce point, la
célérité de détonation est minimale.
Graphiquement, lorsque la pression atteint une valeur
au-delà de Pcj , la zone de détonations fortes est
atteinte, en deçà de celle-ci la zone de détonations
faibles est atteinte. (cf. Annexe AI : étude détaillée
de l'état Chapman-Jouguet)
1.1.3. Modèle de Zeldovich - Von Neumann -
Döring (ZND)
Le modèle de Chapman Jouguet possède
l'inconvénient de ne pas prendre en compte l'évolution du milieu
réactif entre l'état initial et l'état final. Zeldovich,
Von Neumann et Döring ont pris en compte l'extension de la zone de
réaction qui s'appuie sur la description physique d'une onde de
détonation afin d'établir un modèle. Ce modèle ZND
permet ainsi d'associer la cinétique chimique au processus
thermodynamique du modèle CJ.
Dans ce modèle, la détonation est définie
comme la propagation d'une onde d'épaisseur finie monodimensionnelle,
plane et stationnaire dans un milieu réactif. La zone de réaction
est alors scindée en deux parties : un choc frontal
considéré comme inerte provoque une augmentation brutale de la
pression et de la température des gaz frais (état ZND,
compression du mélange de façon adiabatique),
générant après une période d'induction l'initiation
de réactions chimiques (zone de combustion amorcée par
auto-allumage). L'énergie libérée par la combustion
entretient l'onde de choc. Le temps d'induction est compté entre le
passage du choc et l'instant où le maximum d'énergie est
libéré. Il est associé à la longueur d'induction
Äi (figure 1.3). A la sortie de la zone de réaction, lorsque
l'ensemble de l'énergie chimique a été
libérée, l'écoulement est sonique par rapport aux gaz
brûlés : on retrouve alors l'état CJ du modèle
précédent.

Gaz brûlés (état final)
TCJ
PCJ
T,P
TZND
P0 x
T0
PZND
Gaz choqués
DCJ
Gaz frais (état initial)
Pic ZND
Page | 9
Recombinaison
Zone d'induction Äi
Figure 1.3 - Principe du modèle de
Zedovich Von Neuman Doring
VZND
vcJ
v0
P
PZND
ZND
CJ
PcJ
P0
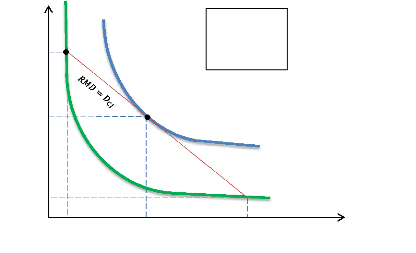
Figure 1.4 - Droite de Rayleigh-Michelson,
adiabatique d'Huguoniot et adiabatique de Crussard dans le plan (p,
y)
v
Crussard
Rayleigh-Michelson Huguoniot
Page | 10
L'intersection de la droite de Rayleigh-Michelson, tangente
à l'adiabatique de Crussard, avec l'adiabatique d'Huguoniot correspond
aux caractéristiques du point ZND (figure 1.4), obtenue à partir
de l'équation (1.9) en considérant QPT
= 0. L'adiabatique d'Huguoniot représente la compression
adiabatique du milieu réactif par l'onde de choc. La réaction
chimique fait passer le mélange de l'état ZND à
l'état CJ avec augmentation du volume spécifique.
1.2. Détonation en milieu
hétérogènes gaz/gouttelettes liquides
1.2.1. Les détonations
hétérogènes
Les premières études de détonations de
gouttelettes liquides ont débutées dans les années
cinquante. Burgoyne et Cohen ont observé une détonation ou
quasi-détonation d'aérosols liquides en atmosphère
oxydante en 1954. Ce n'est que dans les années 80 et jusqu'au milieu des
années 90 que des études sur la détonation
d'aérosols de carburants liquides ont été menées
pour déterminer la détonabilité de ces mélanges.
Toutefois, les résultats expérimentaux restent en nombre
limité.
1.2.2. Synthèse des principaux travaux
antérieurs
Dans les années 50, les premières études
de détonations de gouttelettes liquides ont vu le jour. C'est en 1954
que Burgoyne et Cohen ont observé une détonation
d'aérosols liquides en atmosphère oxydante. Entre les
années 80 et 90, des études pour déterminer des limites de
détonabilité ont été réalisées sur
des aérosols de carburants liquides.
Page | 11
Les applications en lien avec ces recherches, concernent le
domaine de l'aéronautique, des applications en matière de
propulsion, les réacteurs aéronautiques, les moteurs diesels mais
aussi la sécurité industrielle ainsi que des applications de
défense. Récemment, le moteur à détonation
pulsée (PDE, Pulse Detonation Engine) suscite un intérêt
croissant. L'utilisation de carburants liquides dans le PDE présente
l'avantage de réduire le volume et le poids du moteur.
Dans les années 60, les travaux de Williams concernent
l'analyse théorique monodimensionnelle des détonations de
brouillard de gouttelettes liquides très peu volatiles en
atmosphère gazeuse. Par la suite, Webber [1962] et Cramer [1963] ont
conduit des expériences systématiques sur la détonation
d'aérosols liquides. Cramer relève que la
désintégration mécanique des gouttelettes est
nécessaire pour produire un aérosol de gouttelettes de taille
inférieure à 10 um afin d'apporter une quantité suffisante
de vapeur pour entretenir la détonation. De plus, il remarque qu'une
richesse élevée est une condition favorable à l'entretien
de la détonation. D'autres études ont été
menées dans la seconde moitié des années 60. De ces
études est ressorti que la structure de l'onde de détonation d'un
mélange hétérogène constitué
d'aérosols de gouttelettes liquides est plus complexe que celle d'une
détonation gazeuse. Durant les années 90, des études
concernant l'initiation et la détonabilité de mélanges
biphasiques ont vu le jour : citons les travaux de Benedick et al. [1989],
Boiko et al. [1991]; Dabora et al. [1991], Papavassilou et al. [1993] ... Plus
particulièrement, les travaux de Brophy et al. [2000] et Zhang et al.
[2001] ont établis une série de résultats concernant la
détonabilité de différents carburants suivant leur taille
de gouttelettes et différentes méthodes d'initiation.
Globalement, l'ensemble des travaux expérimentaux
effectué sur les détonations hétérogènes
gaz/gouttelettes, beaucoup moins avancé que l'étude des
détonations en phase gazeuse, montre que si les gouttelettes sont de
tailles assez petites, ces détonations peuvent se propager à des
célérités suffisamment proches de celles observées
en phase gazeuse. Par contre, pour les tailles de gouttelettes d'aérosol
plus importantes, de l'ordre du millimètre, la détonation pour
les mélanges biphasiques est difficilement observable. De plus, la
célérité observée est souvent inférieure
à la célérité du mélange gazeux
équivalent. Toutefois, les pertes pariétales, la divergence de
l'écoulement, la combustion incomplète des gouttelettes avant le
plan CJ et la déperdition d'énergie libérée due
à son transport vers l'arrière de l'onde de choc sont
considérés comme étant la cause du déficit en
célérité.
Page | 12
1.3. La structure cellulaire
1.3.1. Structure cellulaire tridimensionnelle
L'onde de détonation possède une structure
réelle beaucoup plus complexe que celle présentée dans les
modèles de CJ et ZND. C'est en 1927 que Campbell et Woodhead ont
montré le caractère non plan de la détonation. La
structure tridimensionnelle de détonation a été mise en
évidence grâce à des procédés optiques
[Voitsekhovskii et al.,1958], [White, 1961] et par la technique des traces sur
les feuilles de suie [Denisov et Troshin, 1960], [Shchelkin et Troshin, 1965],
[Strehhlow et al., 1967]. La propagation d'une onde de détonation se
réalise avec la formation de points triples, résultant de la
collision de :
? l'onde incidente, qui se propage dans la direction de la
propagation dans le tube
? l'onde de Mach, qui est une onde transverse forte
? l'onde réfléchie, qui est également une
onde transverse
Les points triples évoluent de manière
périodique sur le front dans la direction perpendiculaire à la
direction de propagation. La trajectoire de ces points triples prend alors la
forme de cellules (figure 1.5) dites « cellules de détonation
» [Denisov et Troshin, 1962].
L'ensemble des chocs de tête se déplace dans le
sens longitudinal avec une célérité proche en moyenne de
la valeur DCJ. En effet, sur l'axe longitudinal d'une cellule
élémentaire, la célérité du choc varie de
1,6 ~ 1,8 DCJ à 0,8 ~ 0,6 DCJ. (figure 1.5)

Figure 1.5 - Schéma d'une cellule de
détonation et de la variation de la célérité de
l'onde de détonation le long de l'axe de la
cellule
Page | 13
1.3.2. Structure cellulaire des détonations
hétérogènes
Les preuves expérimentales de l'existence de la
structure cellulaire de détonation dans les milieux
hétérogènes biphasiques gaz/gouttelettes liquides sont en
nombre très restreint notamment pour les expériences
réalisées dans les conditions standards de température et
de pression (T = 293 K et 1 bar).
Quelques études expérimentales ont
été réalisées soit dans des aérosols
très volatils, soit après préchauffage du mélange,
ou encore à des pressions initiales très basses. Dans toutes ces
situations, le carburant était vaporisé dans des proportions
très importantes avant l'initiation de la détonation.
Papavassilou et al. [1993] ont étudié la
détonation dans un tube vertical des aérosols de décane de
5 um dans de l'oxygène pur à température et pression
ambiante. Ils ont observé l'amorçage de la détonation dans
des mélanges décane/oxygène et une propagation
stationnaire et autonome de la détonation même pour les
mélanges hétérogènes à la température
ambiante. Ils ont trouvé que les célérités
mesurées sont inférieures de 10 % aux
célérités théoriques CJ des mélanges gazeux
équivalents. Pour les mélanges très pauvres (r < 0,6),
le déficit en célérité est très important.
Ils ont observé une structure cellulaire similaire à celle
observée en phase gazeuse. Dans un certain nombre d'expériences,
les gouttelettes de carburant ont été vaporisées par
chauffage préalable du tube.
La comparaison de la taille de la structure cellulaire de
détonation pour les mêmes mélanges, d'une part, en phase
condensée hétérogène et, d'autre part, en phase
vapeur homogène indique que les processus physiques intervenant dans la
détonation des aérosols sont responsables de l'augmentation de la
taille de la cellule de détonation.
Les études antérieures, expérimentales ou
numériques, montrent que la détonation n'a été
obtenue que dans le cas de gouttelettes suffisamment fines et une
pré-vaporisation importante. Toutefois, des travaux récents
[Modou MAR, 2012] ont montré que l'on pouvait observer des
détonations d'aérosols dans l'air dans les conditions standards
de température et de pression à condition que les gouttelettes
initiales soient suffisamment fines.
Page | 14
Page | 15
Chapitre 2
2. Influence des mécanismes de
désintégration et de vaporisation des gouttelettes sur la
détonation des aérosols de carburants liquides
Ce chapitre a pour but d'exposer les phénomènes
présents lors de l'interaction d'un aérosol de gouttelettes
liquides avec une onde de choc incidente, incluant le processus de
déformation et désintégration des gouttelettes ainsi que
le processus de vaporisation de celles-ci.
2.1 Propagation d'une détonation en présence
d'aérosols de gouttelettes liquides
Le schéma reprend la description de la structure d'une
détonation hétérogène dans des
aérosols de gouttelettes : Onde de choc

Sens de propagation
Gaz brûlés
Zone de gouttelettes en suspension
Zone d'induction
Zone de réaction
Figure 2.1 - Description schématique
d'une détonation dans un aérosol de gouttelettes
? Au sein du mélange frais (gouttelettes en
suspension), se déplace un front de choc incident en comprimant et
chauffant la phase gazeuse du milieu hétérogène de la
même manière que lors d'une détonation en phase gazeuse.
Considérant la vitesse des gouttelettes au niveau du front comme nulle,
une grande différence entre les vitesses matérielles des gaz et
des gouttelettes dans l'écoulement apparait derrière le front.
? Une déformation et une désintégration
rapide des gouttelettes constituant la phase dispersée [Nicholls, 1969]
s'explique par le fait que l'écoulement convectif derrière l'onde
de choc est caractérisé par des valeurs élevées des
nombres de Weber et de Reynolds. Les nombres de Weber et de Reynolds sont des
nombres sans dimension, le
Page | 16
premier correspond au rapport des forces d'inertie et la
tension superficielle du liquide, et le second, permet de caractériser
un écoulement, en particulier sa nature et son régime laminaire,
transitoire ou encore turbulent.
? les fines gouttelettes obtenues par la
désintégration se mélangent avec la phase gazeuse
comprimée, s'échauffent et se vaporisent rapidement sous l'effet
de l'écoulement convectif, pour finalement s'enflammer. La propagation
de la détonation est assurée par la combustion du mélange
dans la zone de réaction.
? des explosions secondaires locales peuvent apparaître
dans le cas de grosses gouttelettes et engendrer des ondes de chocs
secondaires. Ces ondes peuvent rattraper l'onde de choc de tête et
renforcer la propagation de l'onde de détonation.
Dabora et al. [1979] soulignent que la mise en vitesse de la
phase dispersée se produit avec un délai derrière le front
de détonation, de par l'inertie et la densité des gouttelettes
liquides. Ce phénomène de relaxation a pour conséquence
directe d'allonger les temps d'induction et de réaction, ce qui peut se
traduire par un déficit de la célérité de
détonation et par un découplage du front de combustion et du
front de choc. Un déficit trop important de
célérité peut conduire une extinction de la
détonation, en raison d'une désintégration initiale des
gouttelettes insuffisante (gouttelettes très grosses, faible pression de
vapeur saturante).
2.2 Mode et régime de désintégration
de gouttelettes liquides
2.2.1 Désintégration d'un jet liquide
Quand un jet liquide débouche à
l'atmosphère sous forme de cylindre, la compétition entre forces
cohésives et forces « destructrices » à la surface du
jet donne lieu à des oscillations et des perturbations. Rayleigh a
montré que le jet est par nature instable et que les oscillations
s'amplifient jusqu'à désintégration en gouttes. Les
gouttes ainsi formées peuvent être elles-mêmes instables,
d'où possibilité d'atomisation secondaire. Ce n'est que si la
longueur disponible pour le jet est inférieure à la distance
à laquelle la désintégration se produit qu'il peut
paraître stable.
Plusieurs mécanismes de fragmentation se
succèdent lorsque l'on augmente progressivement la vitesse du jet. Le
premier (pour des écoulements très lents c'est à dire
à bas nombre de Reynolds) est le mécanisme de Rayleigh,
instabilité dynamique intrinsèque au jet, qui conduit à
des gouttes dont le diamètre est supérieur à celle de la
buse.
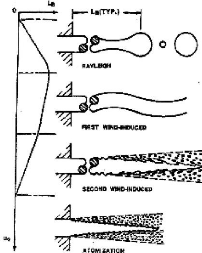
Lorsque la vitesse du jet augmente, les forces
aérodynamiques renforcent le mécanisme de Rayleigh, produisant
des gouttes dont la distribution granulométrique est plus
dispersée. Reitz parle de « first wind induced breakup »
(première zone d'instabilité aérodynamique), pour lequel
la fragmentation se produit au bout d'un nombre important de diamètres
en aval de l'orifice, et pour lequel le diamètre des gouttes reste de
l'ordre du diamètre du jet. Arrive ensuite le « second wind induced
breakup » (deuxième zone d'instabilité
aérodynamique), lié à des petites vagues à la
surface du jet. La fragmentation a lieu après quelques diamètres
de l'orifice seulement et le diamètre des gouttes est très
inférieur au diamètre de l'orifice car le jet est
déstabilisé par la force aérodynamique de cisaillement. Si
la vitesse d'injection augmente encore, la force de cisaillement devient telle
que le jet se désintègre dès la sortie de l'orifice et les
tailles de gouttelettes sont très fines.
Page | 17
Figure 2.2 - Mode de fragmentation
mécanique d'un jet liquide dans un milieu gazeux selon Reitz [1987]
2.2.2 Modes et régimes de
désintégration de gouttelettes liquides
2.2.2.1 Modèle d'atomisation secondaire
L'atomisation secondaire concerne la fragmentation des
gouttelettes issues de l'atomisation primaire du jet sous l'effet de
l'accélération imposée par un écoulement externe.
Le passage à la désintégration secondaire est
favorisée lorsque les nombres de Weber We et de Reynolds Re sont grands
et que la différence de vitesse entre les phases gazeuses et liquides
est grande.
De nombreux modèles d'atomisation secondaire existent
et le but de cette partie n'est pas de dresser une liste exhaustive. Beaucoup
de modèles sont disponibles dans la littérature, citons Hsiang
[1992], Shraiber [1996], Patterson [1998]. Seront décrits, ici,
simplement des modèles représentatifs. Un modèle
d'atomisation secondaire sera présenté au point 2.2.2.2.
2.2.2.2 Modèle de Reitz Diwakar [Reitz, 1986]
Ce modèle de fractionnement secondaire a
été développé à partir des
corrélations obtenues par Nicholls [Nicholls, 1972]. À partir de
ces travaux, Reitz et Diwakar [Reitz, 1986] ont proposé de retenir trois
types de fractionnement secondaire qui dépendent directement du nombre
de Weber gazeux de la goutte.
? Le bag breakup - « Cassure en parachute »
(We>12)
Ce premier régime d'atomisation a lieu pour des nombres
de Weber gazeux supérieurs à 12. La gouttelette est
déformée par l'écoulement d'air. Elle forme alors un sac
dont la membrane se rompt en petites gouttelettes, ne laissant intact qu'un
anneau qui, lui-même, se fractionne en plus petites gouttelettes.
Page | 18
Figure 2.3 - Schéma Description du bag
breakup
Page | 19
? Le stripping breakup - « atomisation par
arrachement » (We>100)
Dans cette configuration, l'écoulement gazeux est plus
rapide et le nombre de Weber est supérieur à 100. Il y a alors
arrachage de ligaments liquides sur les bords des gouttelettes sous la
contrainte de cisaillement aérodynamique imposé par
l'écoulement. Ces ligaments sont ensuite rapidement
fractionnés.

Figure 2.4 - Schéma Description du
stripping breakup
Pour les nombres de Weber compris entre 12 et 100, d'autres modes
de désintégration existent, il est possible de trouver dans la
littérature une explication pour chacun de ces modes
présentés en détail par Shraiber et al. [1996].
2.2.3 Caractéristiques des gouttelettes et leur
mesure
2.2.3.1 Grandeurs caractéristiques des gouttelettes
issus d'un aérosol
Un aérosol se définit comme un brouillard de
gouttelettes issues de l'atomisation d'un jet primaire évoluant dans un
milieu gazeux. Les gouttelettes constituant l'aérosol ont des tailles et
des vitesses différentes. Toutefois, il est nécessaire de
chiffrer ces grandeurs.
Les gouttelettes liquides sont supposées
sphériques, leurs tailles sont donc représentées par leur
diamètre. La distribution des tailles est représentée en
nombre ou en volume sous forme d'histogramme. Cet histogramme contient
plusieurs plages de diamètres caractéristiques. Dès lors,
pour chaque distribution de gouttelettes, deux familles de diamètres
caractéristiques sont associées à savoir les
diamètres moyens et les diamètres représentatifs de la
distribution.
? Les diamètres moyens :
D10 : diamètre correspondant à la moyenne
numérique des diamètres des gouttelettes de l'aérosol
appelé « Arithmetic Mean Diameter (AMD) et il se définit
:
Page | 20
? ?? ????(??)????
??10 = (2.1)
? ?? ????(??)
avec ????(??) et ???? étant respectivement le nombre de
gouttelettes et le diamètre géométrique de chaque
gouttelette.
D20 : diamètre de la gouttelette dont la surface est la
surface moyenne des gouttelettes de l'aérosol considéré,
il est défini comme :
??20v??????(??)????2 (2.2)
= ??? ????(??)
D30 : correspond à la gouttelette dont le volume est le
volume moyen des gouttelettes de l'aérosol considéré.
??30 = v? ????(??)???? 3
3 ?? (2.3)
??? ????(??)
D32 : correspond au diamètre de la gouttelette qui a le
même rapport volume sur surface que celui de la totalité de
l'aérosol. Ce diamètre est intéressant pour les
aérosols pour lesquels la vaporisation joue un rôle important. Ce
diamètre est appelé « Sauter Mean Diameter (SMD) » et
se définit comme :
? ????(??)????3
?? (2.4)
??? ????(??) ????2
? Les diamètres représentatifs :
La distribution volumique de gouttelettes est une autre
manière de caractériser une distribution de gouttelettes. Ces
diamètres sont déterminés à partir de la fraction
volumique de l'aérosol noté fV et du volume total noté
tV.
???
6????(??)????3
??
???? = ???? ???????? ???? = ?????(??)????
?? (2.5)
3
Page | 21
2.2.3.2 Techniques de mesures granulométrique de
l'aérosol
De nombreuses techniques de mesures granulométriques
existent, le choix de la technique dépend des paramètres à
étudier et de l'environnement du milieu étudié. Les
principales techniques de mesure utilisées de nos jours sont des
systèmes optiques qui offrent l'avantage d'être rapides et non
intrusifs. Deux grandes techniques de mesure d'aérosols sont
utilisées :
? La granulométrie à diffraction : la mesure est
effectuée à l'aide d'un faisceau laser se basant sur la
théorie de Mie de diffusion de la lumière [J. Swithenbank et al.,
1976]. Le principe est basé sur l'interaction du faisceau avec la
gouttelette, le faisceau de diffraction sur la gouttelette présente un
angle de déviation dépendant de la taille de la gouttelette
rencontrée. Cette méthode permet d'obtenir la distribution
volumique des tailles de gouttelettes présentes dans le volume de
mesure.
? Le PDI (Phase Doppler Interferometer), le PDPA (Phase
Doppler Particule Analyser) dont le principe s'appuie sur la théorie de
la diffusion de Mie de la lumière. Le volume de mesure est
délimité par la cohérence des faisceaux lasers par paires
de deux, formant ainsi un réseau de franges. Lorsque la gouttelette
traverse le volume délimité par les faisceaux, le mouvement
crée une lumière diffusée qui sera
récupérée au voisinage de l'ange de diffusion. Le
déphasage entre signaux est ainsi récupéré, ce
dernier est proportionnel à la vitesse et au diamètre de la
gouttelette. Une distribution granulométrique numérique de
tailles et de vitesses caractérisant l'aérosol est ainsi
obtenue.
2.3 Mécanisme de vaporisation des gouttelettes
liquides
De nombreux modèles d'évaporation sont
disponibles dans la littérature. Les principales différences
entre ces modèles sont liées à la modélisation de
la phase liquide qui contrôle le débit d'évaporation de la
gouttelette dans une atmosphère gazeuse à haute
température. Citons quelques un de ces modèles :
1. Modèle à température constante de
gouttelette (loi en d2),
2. Modèle à conductivité du liquide
infinie (température de la gouttelette uniforme mais variant avec le
temps),
3. Modèle de chauffage de la gouttelette
transitoire,
4.
Page | 22
Modèle à conductivité effective,
5. Modèle basé sur la solution des
équations de Navier-Stockes.
Le modèle classique d'évaporation a
été élaboré par Godsave [1953], Spalding [1953],
Goldsmith & Penner [1954] et Wise et al. [1955].
Les hypothèses du modèle standard menant
à la loi en d2 sont applicables pour l'évaporation de
gouttelettes mono-constituantes et sont les suivantes :
· La symétrie sphérique car les effets de
la convection naturelle et forcée sont négligés en
supposant que la goutte est immobile par rapport au milieu ambiant.
· La goutte est isolée et plongée dans un
environnement au repos.
· Les processus sont considérés comme
isobares et la pression est égale à celle du milieu ambiant.
· Les propriétés de la phase gazeuse
(capacité calorifique, conductivité thermique et coefficient de
diffusion) sont constantes. Le nombre de Lewis est supposé égal
à l'unité. Soit l'égalité entre le nombre de
Schmidt et le nombre de Prandtl.
· Les phénomènes sont quasi-stationnaires
dans la phase liquide. La température de la goutte est uniforme et
constante.
· La phase gazeuse est quasi-stationnaire, ce qui
signifie que l'écoulement s'adapte instantanément aux conditions,
aux limites et aux dimensions de la goutte. Tenant compte de cette
hypothèse et de la précédente, on peut constater que le
débit de vapeur est constant.
· Le changement de phase entre le liquide et sa vapeur
est beaucoup plus rapide que le phénomène de transport dans la
phase gazeuse, ce qui entraîne un équilibre liquide-vapeur
à tout instant à la surface de la goutte, qui est à la
pression de vapeur saturante correspondant à la température de
surface de la goutte.
· Les phénomènes de décomposition
de la phase gazeuse, le rayonnement, les effets de Soret (la diffusion massique
provenant d'un gradient thermique), et de Dufour (flux de chaleur produit par
un gradient de concentration) sont négligés.
De par ces hypothèses, la loi en d2 est
établie et décrit l'évolution du diamètre initial
d'une gouttelette d en fonction du temps t :
??2 = ??0 2 - ??.?? (2.6)
Page | 23
avec d étant le diamètre instantané de la
goutte, d0 est son diamètre initial, t est le temps et K
représente le taux de vaporisation définit par :
Pyaz
K = 8 Dyaz ln(1 + B) (2.7)
Pliquide
Où Dgaz représente la diffusivité,
Pyaz et Pliquide sont les densités
respectives de la vapeur et du combustible en présence à la
température de gouttelette et B est la constante de transfert de
Spalding.
Brophy et al. [1998 ,2000] ont montré que la vitesse
à laquelle des mélanges combustible/air atteignent
l'équilibre dépend du taux de transfert de chaleur entre l'air et
les gouttelettes, de la pression de vapeur saturante du combustible.
D'où l'importance de connaitre le taux de vaporisation.
2.4 Diamètre de gouttelette et déficit de
célérité de détonation
hétérogène
Pour des gouttelettes de petites tailles devant
l'épaisseur de la zone d'induction, le comportement de la
détonation est identique à celui d'une détonation gazeuse.
Par contre, dans le cas d'une gouttelette de taille importante, la zone
d'induction doit inclure la phase de désintégration et
d'évaporation partielle des gouttelettes. La propagation de la
détonation dépend donc de la désintégration des
gouttelettes et de leur temps de combustion dans la zone de réaction
[Dabora et al., 1969, Bar-Or et al., 1981, Lin et al., 1984].
Les expériences menées sur les espèces
chimiques de faible volatilité, telles que le kérosène,
ont montré qu'existait un déficit en
célérité de 23,5% par rapport à la
célérité de détonation idéal CJ. Par contre,
dans le cas d'espèces à volatilité plus importante, cas de
l'heptane par exemple, le déficit n'est que de 3.3 %. De ces
observations, on en conclut que pour des combustibles de volatilité
importante, il y a peu de différence au point de vue de la
célérité entre le cas où l'on vaporise
partiellement ou complétement les gouttelettes liquides. Lin [1984] a
montré que pour la détonation de combustibles peu volatils, la
longueur d'induction augmente ce qui veut dire qu'une énergie
élevée est requise pour l'initiation de la détonation.
Dabora et al. [1969] ont montré l'influence de la
taille des gouttelettes sur la détonabilité des mélanges.
Il s'avère que plus la taille de gouttelettes est petite, plus on
atteint le régime stable de détonation. Pour les gouttelettes de
taille allant de 290 à 940 um, le déficit
Page | 24
de célérité va de 2 à 10% tandis
que pour les tailles de l'ordre de 2600 um, le déficit peut atteindre
30%. Les pertes aux parois sont considérées comme le facteur
dominant expliquant ce déficit en célérité,
à cause de l'augmentation de la longueur d'induction.
Page | 25
Chapitre 3
3. Montage expérimental
3.1 Introduction
Dans ce chapitre, l'ensemble des éléments
constituant le dispositif expérimental, ainsi que les différentes
techniques de mesure et procédures expérimentales mises en oeuvre
lors des expériences seront décrits. Le montage
expérimental a été conçu pour permette de produire
des aérosols de carburants, de caractéristiques
contrôlées sur toute la longueur du tube, et d'enregistrer les
caractéristiques de la structure cellulaire de détonation (taille
et régularité). Cela a pour objectif de pouvoir acquérir
de nouvelles connaissances sur les détonations
hétérogènes gouttelettes liquides/gaz et sur leurs
caractéristiques.
3.2 Le tube à détonation
Le tube à détonation vertical (figure 3.1 et
3.2) est constitué dans sa partie principale de tronçons de
section carré de 53*53 mm. Il est composé de bas en haut :
· d'un dispositif de génération de
l'aérosol,
· d'une électrovanne à boule, à
commande électropneumatique, permettant la fermeture du tube à
détonation,
· d'un tube à choc auxiliaire pour l'initiation
de la détonation du mélange,
· de six tronçons de section carrée 53*53
mm instrumentés, le tronçon terminal permettant l'enregistre ment
de la structure cellulaire de détonation,
· d'une électrovanne à boule similaire
à celle du bas du tube permettant la fermeture du tube à sa
partie supérieure (la distance entre ces deux électrovannes est
de 4,036m),
· d'un tube d'évacuation vers l'extérieur
de la pièce.
· Le tube à détonation est
instrumenté sur toute la longueur et l'ensemble des opérations
expérimentales est piloté par un dispositif de commande et de
sécurité géré par logiciel informatique.

Evacuation des gaz brûlés
Prémélanges C2H4 + 3O2
Figure 3.1 - Schéma du montage
expérimental
Page | 26
Pompe à vide
Membrane en mylar
Jauge de contrainte (MKS 4000)
Booster (tube à choc)
Système
d'amorçage
Bouteille des prémélanges
Tube à détonation
Electrovanne
Système de
production
d'aérosols
de
carburants liquides
Plaque de suie
(Chambre
d'enregistrement)
Mélange biphasique
K7
K6
K5
K4
K3
K2
K1
Electrovanne
Acquisition de données
Capteurs
piézoélectriques
Partie supérieure tube Chambre d'enregistrement

Partie inférieure tube
Tube à choc « booster »
Figure 3.2 - Montage expérimental
Page | 27
Page | 28
3.3 Le tube à choc
Dans les détonations gazeuses, un dispositif à
spirale de Schelkin est souvent utilisé pour amorcer la
détonation. Ce dispositif permet d'obtenir une longueur de
pré-détonation la plus courte possible. Mais ce dispositif
engendre des perturbations importantes lors de l'écoulement de
l'aérosol de gouttelettes dans la première partie du tube
à détonation ce qui engendrerait des dépôts non
négligeables de gouttelettes sur les parois du tube.
Le tube à choc remplit le rôle de dispositif
d'amorçage, l'amorçage de mélange
hétérogène est réalisé par une onde de choc.
Celle-ci est générée par la détonation d'un
mélange contenu dans un tube à choc auxiliaire, dit booster,
débouchant dans le tube principal, au-dessus de la vanne
inférieure de fermeture du tube (la distance entre le point de
raccordement et la vanne supérieure de fermeture du tube est de 3,9 m).
Ce tube à choc (figure 3.1) est de section circulaire de diamètre
69 mm et de longueur 1,7 m avec une capacité de volume de 6 litres. Il
est muni à ses deux extrémités de deux brides permettant
d'une part de le connecter au tube à détonation principal par
l'intermédiaire d'une membrane en mylar intercalée entre deux
joints toriques, et, d'autre part, de fermer l'extrémité
opposée par un couvercle muni du système d'allumage par
inflammateur électrique. Ce tube à choc est connecté
à une croix de distribution comportant 4 vannes pour la connexion
à une pompe à vide, à une jauge de pression (MKS PR 4000)
et à un réservoir de mélange, ce qui permet de faire le
vide dans le tube , puis de le remplir avec un prémélange
réactif d'éthylène ~ oxygène
stoechiométrique, préparé au préalable par la
méthode des pressions partielles et stocké dans un
réservoir sous pression. La pression initiale du
prémélange est de 2 bars ou 3 bars.
3.4 Génération des aérosols de
gouttelettes liquides
Le remplissage du tube à détonation, de
manière uniforme, sur toute sa longueur avec un aérosol de
caractéristiques contrôlées et reproductibles était
l'une des principales difficultés. Les méthodes traditionnelles
de génération d'un aérosol par injecteur mécanique,
ne permettent pas de satisfaire cette condition. En effet, par injection
mécanique l'aérosol se désintègre de façon
non contrôlée en une série aléatoire de ligaments et
de gouttelettes de diverses tailles. De plus, l'atomisation du liquide
nécessite des vitesses très élevées entre les
différents fluides. L'écoulement qu'engendre cette technique est
très turbulent lors du remplissage du tube, avec comme
inconvénient de favoriser les dépôts de gouttelettes aux
parois. Les aérosols sont donc produits en utilisant la technique des
atomiseurs ultrasoniques.
Page | 29
3.4.1. Les atomiseurs ultrasoniques
Le principe de fonctionnement des atomiseurs ultrasoniques
utilisés, est celui décrit par Lacas et al. [1994]. La technique
des atomiseurs ultrasoniques consiste à créer des
instabilités hydrodynamiques à la surface d'un film liquide en le
soumettant à des fréquences d'excitation ultrasoniques. Avec
cette gamme de fréquence d'excitation appliquée, la
désintégration du film est obtenue (figure 3.3).
Le liquide va alors développer en surface des ondes
capillaires transverses. La longueur d'onde des vibrations créées
est fonction de la fréquence, de la tension superficielle du liquide,
ainsi que de sa masse volumique. Dans le cas où l'amplitude des ondes
générées est suffisante, le film liquide est
déstabilisé en une série de petites gouttelettes.

Figure 3.3 - Gamme de fréquence
ultrasonique et désintégration d'un film liquide par atomisation
ultrasonique
Les gouttelettes ainsi formées ont leur
diamètre d0 relié à la fréquence d'excitation f par
la formule de Kelvin :
1 3
d0 = 2 v o???? (3.1)
P????2
Où : k est une constante empirique (typiquement 0,25 -
0,33), o?? représente la tension surfacique de la
gouttelette et P?? sa densité.
L'ensemble des gouttelettes forme un aérosol au-dessus
du film liquide dans une atmosphère gazeuse à vitesse nulle.
Page | 30
3.4.2. Le générateur
Pour l'expérience, un nouveau type de
générateur de gouttelettes (figure 3.4) venant du commerce est
utilisé, son fonctionnement est basé sur le principe des
atomiseurs ultrasoniques.
Le fonctionnement est basé sur la mise en vibration
d'une lame métallique situé sous une couche d'eau ou de
carburants. Celui-ci devrait couvrir une plage de granulométrie
permettant de passer en dessous de 5 um. (Etude plus approfondie de la
granulométrie au chapitre 4)

Figure 3.4 - Générateur de
gouttelettes liquides (atomiseur ultrasonique)
3.4.3. Alimentation de l'atomiseur
? Le débit d'oxydant est contrôlé par un
rotamètre "Brooks" (GT/1000, flotteur : 8 - RS14), dont la sortie est
reliée à la base d'un boitier mélangeur où
l'admission se fait en trois points différents
? L'ensemble des rotamètres et des vannes de
contrôle des circuits d'alimentation est regroupé sur un tableau
de commande que l'on peut voir sur la figure 3.5.

Page | 31
Figure 3.5 - Tableau de commande du dispositif
d'alimentation de débit en oxydant (rotamètre d'oxydant à
droite)
3.5 Dispositifs de mesure
3.5.1 Granulométrie de l'aérosol
Ce point est abordé en détail au chapitre 4.
3.5.2 Mesure de la célérité et de
la pression de détonation
Le tube est instrumenté, sur toute sa longueur, de
capteur de pression piézoélectriques Kistler 603B dont le temps
de réponse est de 1 us. Ces capteurs sont positionnés en sept
points, répartis le long du tube à 1350 mm, 1850 mm, 2091 mm,
2591 mm, 2821 mm, 2956 mm et 3126 mm à partir du point d'initiation. Ces
différents capteurs sont reliés à des amplificateurs de
charges Kistler Type 5011. Le tableau 3.1 reprend les distances entre
capteurs.
Capteurs
|
0-K1
|
K1-K2
|
K2-K3
|
K3-K4
|
K4-K5
|
K5-K6
|
K6-K7
|
Distances (mm)
|
1350
|
500
|
241
|
500
|
230
|
135
|
170
|
|
Tableau 3.1 - Distances entre capteurs
Page | 32
Afin de filtrer les vibrations acoustiques se propageant dans
les parois du tube, chaque capteur est inséré dans un support en
téflon. Ils sont maintenus par une entretoise et une vis de serrage. Le
support est ensuite monté sur la paroi du tube principal. Afin
d'éviter des problèmes de dérive de signaux pouvant
être provoqués par des sollicitations thermiques, une couche de
graisse protectrice en silicone couvre la partie sensible métallique du
capteur.
Les signaux délivrés par les amplificateurs de
charge sont envoyés sur une unité centrale « Graphtec Hard
Disk Logger GL1100 ». Cette unité centrale possède 8 voies
ainsi qu'une vitesse d'échantillonnage pouvant aller jusqu'à 25
ns, celle-ci étant pilotée par un ordinateur. L'enregistrement
des sept signaux de pression provenant des capteurs se fait ainsi de
manière synchronisé dès l'allumage. La
célérité moyenne de détonation se déduit par
la connaissance du temps de passage du front de discontinuité incident
et le signal de pression permet de déterminer sa valeur et son
évolution.
3.5.3 Enregistrement de la structure cellulaire
L'existence d'un régime de détonation se fait
par l'analyse des structures cellulaires tridimensionnelles obtenu par
l'intermédiaire de plaque rectangulaires (420 mm * 53 mm). L'une des
faces, polie « miroir », est enduite d'un dépôt de suie
afin de mettre en évidence une éventuelle structure par la
méthode des traces de Mach. En effet, les points triples
caractéristiques de la structure inscrivent la trace de leur trajectoire
en arrachant les particules de suie en raison des niveaux élevés
de température et pression existant à ces points. Un
enregistrement bidimensionnel de la structure tridimensionnelle est ainsi
obtenu et la taille, la forme et la régularité sont ainsi
étudiés.
3.6 Système de commande et protocole
3.6.1 Système de commande
Un système automatisé régi par un
logiciel géré par ordinateur permet de commander et
contrôler l'ensemble des opérations de remplissage du tube
à détonation, d'isolement du tube par fermeture des
électrovannes, d'arrêt des débits des fluides et de mise
à feu. Ce logiciel intègre également la gestion de tous
les dispositifs de sécurité permettant ainsi d'éviter tous
risques d'incidents, de manipulations ou encore toutes pannes et
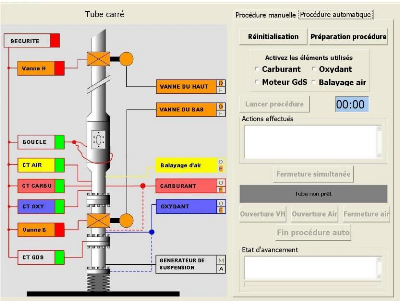
dysfonctionnements. La figure 3.6 reproduit le tableau de commande et de
contrôle du logiciel.
Page | 33
Figure 3.6 - Tableau de commande et de
contrôle de sécurité
3.6.2 Protocole d'essai
Pour des raisons de sécurité, l'ensemble du
tube est tout d'abord mis sous vide afin de localiser des éventuelles
fuites. Un protocole bien défini est à suivre et ce pour
n'importe quel type de tirs :
Phase préparatoire
· Mise sous tension de l'ensemble des appareils de
contrôle,
· Enfumage des plaques de suie et fixation de ces plaques
sur leur support,
· Mise en route du logiciel de commande de la
procédure, des systèmes d'acquisition de données, des
électrovannes, du boîtier d'alimentation électrique de
l'injecteur,
· Test de fonctionnement de l'enregistreur
"Graphtec",
· Mise en place de la membrane en mylar entre tube
principal et tube à choc,
· Mise en place du système d'initiation par
inflammateur,
· Verrouillage de la boucle de
sécurité.
Page | 34
Phase de remplissage du tube
· Faire le vide dans le tube de
pré-détonation,
· Remplissage du prémélange C2H4/O2, dans le
tube à choc sous 2 bars ou 3 bars,
· Lancement de la procédure automatique : vannes
haute et basse ouvertes, ouverture des circuits d'alimentation en oxydant et du
générateur d'aérosols,
· Branchement des conducteurs électriques du
dispositif de mise à feu,
· Réglage des débitmètres carburant et
oxydant selon la richesse désirée,
· Mise en marche de l'atomiseur, et accouplement à
la partie inférieure du tube principal,
· Remplissage du tube principal par balayage des
différents composants : aérosol de carburants et air.
Phase de tir
· Mise sous tension électrique de commande de mise
à feu,
· Activation des amplificateurs de charge,
· Fermeture simultanée des vannes d'alimentation en
carburant et en air et des électrovannes de fermeture du tube; retrait
de l'atomiseur,
· Initiation du tir (activation de la touche départ
du "Graphtec"),
· Mise à feu.
Acquisition de données
· Sauvegarde des données à partir du
"Graphtec",
· Mise en position "stand-by" des amplificateurs de
charge,
· Ouverture de la vanne haute (vanne basse fermée),
et mise en route du balayage d'air et sa connexion au tube de
pré-détonation (évacuation des gaz
brûlés),
· Arrêt du balayage d'air,
· Dégager le support de l'atomiseur du tube
principal,
· Ouverture de la vanne basse
· Nettoyage et remise en état du tube,
· Exploitation des données.
Page | 35
Chapitre 4
4 Caractérisation de la distribution
granulométrique des gouttelettes d'un aérosol
4.1 Introduction
Ce chapitre a pour but de déterminer la
granulométrie des aérosols générés par
l'atomiseur utilisé pour nos expériences. Pour comprendre le
dispositif expérimental utilisé, deux points seront
développés.
Le premier consistera à expliquer le principe de
mesure de la granulométrie par PDI (Phase Doppler Interferometry),
celui-ci permet d'obtenir la caractéristique de la distribution en terme
de diamètre moyen (D10) et diamètre de sauter SMD (D32).
Deuxièmement, l'analyse des histogrammes de distributions de
gouttelettes, et l'évolution des diamètres D10 et D32 en fonction
du débit d'air de travail seront abordées.
4.2 Méthode de mesure granulométrique par
PDI (Phase Doppler Interferometry)
La détermination de la granulométrie des
aérosols se fait par la technique de mesure par
interférométrie Phase Doppler PDI dont l'avantage est
d'être non intrusive.
4.2.1 Principe de mesure par PDI
Le principe de mesure repose sur l'utilisation de la
cohérence de deux faisceaux laser produit par un émetteur, qui
crée un réseau de franges d'interférence dans un volume,
et l'analyse des signaux résultant du passage des gouttelettes au sein
de ce réseau de franges, appelées « bouffées Doppler
». La figure 4.1 représente la disposition des composants
(émetteur et récepteur) du système de mesure. Il est
important de focaliser précisément le point d'intersection des
faisceaux lasers et le point définissant la zone de mesure, et de
positionner le récepteur dans l'axe des rayons réfléchis
par les gouttelettes, de manière à positionner le système
optique du récepteur sur le volume de mesure. Les angles de collection
de l'axe du récepteur sont typiquement de 30 ou 40° par rapport aux
rayons lasers issus de l'émetteur. Durant l'expérience, l'angle a
été fixé à 40° pour optimiser la
réfraction du 1er ordre.

Page | 36
Figure 4.1 - Principe de mesure
granulométrique par PDI (Phase Doppler Interferometer)
Les lasers vert et bleu, respectivement de longueur d'onde de
532 et 473 nm, sont issus de l'émetteur. Une gamme de focales de 350
à 2000 mm est disponible. Pour la partie expérimentale, deux
focales de longueur de 500 mm sont utilisés, l'une pour
l'émetteur, et l'autre pour le récepteur. Ces focales permettent
d'effectuer des mesures dans les gammes de tailles de gouttelettes allant de
1,5 à 160 um. Les caractéristiques des focales sont reprises dans
le tableau 4.1.
Focale émetteur
(mm)
|
Focale récepteur
(mm)
|
Gamme de tailles
mesurables (um)
|
Vitesse min (m/s)
|
Vitesse max (m/s)
|
500
|
500
|
1.5~160
|
-100
|
400
|
|
Tableau 4.1 - Gammes de mesure de taille et
de vitesse des gouttelettes
L'indice de réfraction est un paramètre
important qui caractérise la vitesse de la lumière à
travers les gouttelettes de l'aérosol. Il est de l'ordre de 1,33 pour
les gouttelettes d'eau. Pour nos autres liquides de travail l'indice change :
soit 1,42 pour le dodécane et 1,45 pour le kérosène.
Page | 37
La granulométrie
L'interaction entre le faisceau laser incident et la
gouttelette liquide sphérique est représenté à la
figure 4.2. Le point intéressant est la réfraction du
1er ordre et les variations de phases qui s'ensuivent. Les
méthodes de mesures reposent sur la variation de trajet optique des
faisceaux lors du passage à travers la gouttelette vue par des
détecteurs placés à des angles azimutaux différents
(figure 4.3). Cette variation est à l'origine du déphasage entre
le rayon incident et le rayon réfracté.
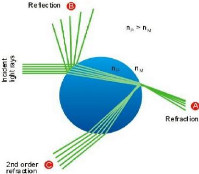
Figure 4.2 - Interaction des faisceaux lasers
avec une gouttelette liquide
Connaissant la distance séparant les
détecteurs, la longueur d'onde du laser et le déphasage entre les
deux signaux à chaque « bouffée Doppler », la taille de
la gouttelette peut être calculée. Dans ce cas-ci, trois
photomultiplicateurs (PM, 1, 2, 3) sont utilisés pour effectuer des
mesures de déphasage. Ces mesures servent à vérifier la
sphéricité des gouttelettes mais également à
éliminer les gouttelettes ayant un déphasage de plus de 360°
qui sortent de la gamme d'échantillon mesurable.

Figure 4.3 - Principe de détection des
rayons lumineux réfractés
La détermination du diamètre de gouttelettes
repose sur le fait que le déphasage spatial Ö est proportionnel
à la taille des gouttelettes présentes dans le volume de mesure.
Le déphasage ??1-2 entre deux photomultiplicateurs est calculé
comme suit : ??1-2 = (??1-2/?? ) * 360, où P est la période du
signal sinusoïdal issu de la bouffé e Doppler.
La mesure du déphasage ??1-2 permet donc de remonter
au déphasage spatial et ainsi au diamètre de la gouttelette.
Cependant, trois photomultiplicateurs (PM, 1, 2, 3) sont nécessaires
pour une mesure correcte du diamètre de la gouttelette, car, l'analyse
de la déviation des faisceaux laser dans la gouttelette repose sur les
lois de l'optique géométrique qui ne sont applicables qu'à
des gouttelettes sphériques. La comparaison entre les mesures des PM
(1-2) et des PM (1-3) (figure 4.4) permet ainsi de vérifier cette
sphéricité, et de valider les gouttelettes pour lesquelles les
mesures sont exactes. De plus, l'utilisation d'un troisième
photomultiplicateur permet l'élimination directe des gouttelettes
dépassant la borne supérieure de la gamme de diamètre
mesurable (avec un déphasage de plus de 360°).

Page | 38
Figure 4.4 - Variation du déphasage en
fonction de la taille des gouttelettes
La vélocimétrie
Cette technique s'appuie sur l'utilisation de la
cohérence de deux faisceaux lasers pour créer un réseau de
franges d'interférence dans un volume de mesure (typiquement quelque
mm3, cf. figure 4.5) et d'utiliser ce réseau de franges pour
analyser le signal lumineux obtenu par le passage d'une gouttelette liquide.

Page | 39
Figure 4.5 - Principe de mesure de
vélocimétrie des gouttelettes
L'intersection de deux faisceaux lasers cohérents
permet d'obtenir un réseau d'interfranges connu, et la gouttelette
animée d'une vitesse non nulle, diffuse la lumière modulée
au passage du réseau. Il s'ensuit un signal sinusoïdal de
période correspondant au passage de la gouttelette d'une raie à
la suivante (pourvu que la taille de la gouttelette soit inférieure
à l'interfrange). La connaissance de l'interfrange et de la
période de passage de la gouttelette permet de calculer la vitesse de la
gouttelette dans le plan des franges et perpendiculairement au réseau de
franges.
4.2.2 Montage expérimental et protocole
d'essai
Le montage expérimental utilisé pour les
mesures de granulométrie est photographié sur la figure 4.6. Il
comporte :
- le générateur d'aérosols,
- un tube transparent cylindrique en plexiglas, de
diamètre 53 mm, fixé à la sortie de
l'atomiseur,
- un bâti d'assemblage,
- l'émetteur de faisceaux lasers (bleu et vert),
- le récepteur fixé sur un bâti
- le système d'alimentation en oxydant et en carburant
(cf. chapitre 3),
- le système d'acquisition et d'exploitation de
données
Le protocole d'essai suivi est le suivant :
- mise en route des appareils et initialisation de la
granulométrie en faisant une acquisition en l'absence d'émission
de rayon laser,
- calibrage du laser ; réglage des distances focales;
réglage de l'amplitude et de la fréquence du signal Doppler,
indication de l'indice de réfraction, réglage du gain (une valeur
de 350 V est typiquement employée),
- réglage de la bonne convergence des faisceaux laser
dans la zone de mesure,
- réglage du critère de sphéricité
des gouttelettes,
- choix du nombre d'échantillons mesurés, les
valeurs typiques sont de 5.000 à 10.000 gouttelettes. La bonne
représentation statistique des plus grosses gouttelettes dans la
distribution exige un grand nombre d'échantillons,
- mise en marche du générateur d'aérosols,
réglage des débits de liquide et d'oxydant, - démarrage de
l'acquisition de données ; le système réalise
l'acquisition jusqu'à ce que le nombre d'échantillons soit
atteint,
- enregistrement et sauvegarde des données.

Emetteur
Injecteur ultrasonique
Tube
Récepteur
Figure 4.6 - Dispositif de mesure
granulométrique par PDI
Page | 40
Page | 41
4.3 Etude de la distribution granulométrique des
gouttelettes produites par les atomiseurs
La distribution granulométrique des aérosols
générés par l'atomiseur sera étudiée dans ce
paragraphe. Tout d'abord, les expériences sont effectuées sur des
aérosols d'eau ensuite sur différents carburants. Les
caractéristiques intéressantes sont le diamètre moyen D10,
le diamètre de sauter D32, les histogrammes du nombre de gouttelettes et
le LWC (Liquid Water Content), défini comme étant la masse des
gouttelettes liquides dans un volume de l'espace donné. Il est
exprimé en g/m3 et se calcule via la formule suivante :
??
??????= 6 ?? D30
3 ND (4.1)
Où ND ( 1
????3) représente le nombre de gouttelettes par
unité de volume dans l'espace de
mesure et D30, correspond à la gouttelette
dont le volume est le volume moyen des gouttelettes de l'aérosol
considéré.
Différentes séries de mesures ont
été effectuées en faisait varier certains
paramètres :
? le débit d'air d'entrainement de l'aérosol
? la hauteur du point de mesure dans le tube au-dessus de
l'atomiseur.
Les essais ont été effectués sur des
échantillons de 10000 gouttelettes.
4.3.1 Atomiseur ultrasonique
Les histogrammes ont été obtenu pour un
aérosol d'eau à une hauteur z = 50 mm et 160 mm au-dessus de
l'atomiseur pour différentes valeurs de débits d'air
d'entrainement. Ces mesures de granulométrie sont effectuées au
centre de l'écoulement. Sur ces histogrammes, la répartition du
nombre de gouttelettes en fonction de leur diamètre peut être
observée. L'allure de l'histogramme est gaussienne, le diamètre
pris comme valeur représentative pour les expériences de
détonation est le diamètre moyen D10 qui prend en compte les
autres diamètres de gouttelettes par pondération de leur nombre
dans le volume de mesure.
Nombre de gouttelettes
|
2500 2000 1500 1000 500
0
|
|
|
1 3 5 7 9 11 13 15 17 19 21 Diamètre des goutellettes
[um]
Figure 4.7 - Spectre granulométrique d'un
aérosol d'eau à une cote d'observation z = 160 mm,
????air = 1,42 m3/h
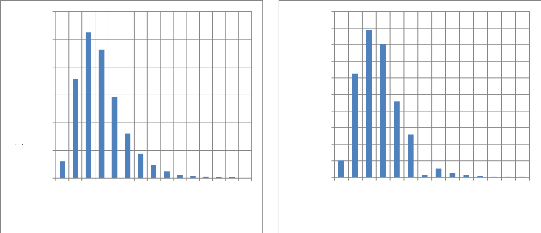
1 3 5 7 9 11 13 15 17 19 21 23 25 27 29
Diamètre des goutellettes [um]
(a)
Nombre de goutellettes
3000
2500
2000
1500
1000
500
0
1 3 5 7 9 11 13 15 17 19 21 23 25 27
Diamètre des goutellettes [um]
(b)
Nombre de goutellettes
4500
4000
5000
3500
3000
2500
2000
1500
1000
500
0
Figure 4.8 - Spectre granulométrique d'un
aérosol de (a) kérosène Jet-A1, (b) dodécane
à une cote d'observation z = 160 mm, ????air = 1,42
m3/h
Avec le même atomiseur et dans la même
configuration, des mesures granulométriques avec le
kérosène Jet-A1 et le dodécane ont été
prises. Les Figures 4.8 (a) et (b), donnent la distribution des gouttelettes
à une cote d'observation z = 16 cm. On constate qu'avec le
dodécane (figure 4.8 (b)) la majorité des gouttelettes a une
taille comprise entre 3 et 11 ìm avec un maxima centré autour de
6 ìm. Le calcul de la moyenne arithmétique du D10 par le
système PDI renvoie une valeur D10 = 4,3 ìm (tableau 4.2).
Concernant le kérosène, le maximum est centré à
environ 6 ìm. La majorité des gouttelettes de
kérosène ont une taille variant de 3 à 13 ìm et le
diamètre moyen D10 est de 4,7 ìm. La présence de plus
grosses gouttelettes dans l'aérosol de kérosène se traduit
par des diamètres SMD (D32) plus importants que dans le cas du
dodécane.
Page | 42
Page | 43
Z [cm]
|
D10 [um]
|
D32 [um]
|
D30 [um]
|
LWC [g/m3]
|
Kérosène Jet-A1
|
16
|
4,7
|
73,6
|
15,9
|
16,47
|
Dodécane
|
16
|
4,3
|
69,1
|
14
|
10,78
|
|
Tableau 4.2 - Résultats de mesure avec
l'atomiseur
Le tableau reprend les informations principales permettant de
caractériser l'aérosol. Par comparaison des LWC avec le
kérosène et le dodécane dans les mêmes conditions
opératoires, on voit que ce paramètre est plus
élevé pour le kérosène. Cela est dû au fait
que la masse volumique est plus élevée et que ce carburant est
peu volatil d'où une proportion de phase liquide plus importante.
Pour l'ensemble des mesures effectuées, les
diamètres D10 mesurés varient entre 4 et 6 um en fonction de la
dispersion expérimentale et de la nature du liquide testé. Pour
la suite, afin de faciliter l'analyse expérimentale au chapitre 6, un
diamètre moyen unique des gouttelettes pour tous les aérosols
produits avec cet atomiseur est fixé. L'atomiseur générant
majoritairement des gouttelettes de taille de 5 um le diamètre sera
alors fixé à D10 = 5 um.
Page | 44
4.3.2 Variation du D10 et D32 en fonction du
débit d'oxydant
Les figures montrent la variation des diamètres D10 et
D32 dans des aérosols de gouttelettes d'eau en fonction du débit
d'air et ceux pour deux cotes d'observations z différentes par rapport
à la sortie du jet liquide. Pour le débit d'air d'entrainement,
celui-ci à peu d'influence sur la valeur de D10 et D32. Cependant, ces
deux paramètres dépendent fortement de la cote d'observation.

0,00 0,50 1,00 1,50 2,00 2,50 3,00 3,50 4,00 4,50 5,00
Débit d'air [m3/h]
Cote z=5cm Cote z=16cm
14
12
10
D10 [um)
8
6
4
2
0
0,00 0,50 1,00 1,50 2,00 2,50 3,00 3,50 4,00 4,50 5,00
Débit d'air [m3/h]
Cote z=5cm Cote z=16cm
120
100
80
D32 [um]
60
40
20
0
Figure 4.9 - Evolution de la
granulométrie d'aérosols d'eau générés par
l'atomiseur en fonction du débit d'air pour différentes
cotes d'observation z
Page | 45
Le travail réalisé par Modou MAR [2012], montre
qu'à partir d'une hauteur donnée, la valeur de débit d'air
a peu d'influence sur la valeur de D10 et D32. Cela serait probablement
dû à la vitesse d'écoulement faible, excepté
à une cote z = 50 mm où une dispersion de la taille des
gouttelettes est observée.
Ces comportements sont également observés dans
le cas d'un aérosol de dodécane et de kérosène.
Dès lors, quelle que soit la valeur de la richesse du mélange, la
taille des gouttelettes est la même. Cependant, une différence
notable est constaté pour les variations du diamètre de sauter
D32. Cela pourrait être dû à l'instabilité du nombre
des très grosses gouttelettes qui ont un poids important dans le calcul
de SMD.
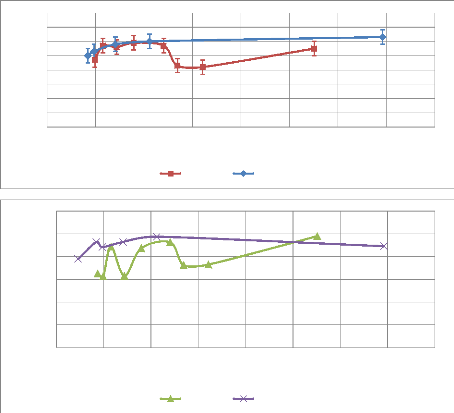
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60
Richesse
Kérosène Dodécane
8,0
7,0
6,0
5,0
D10 [um]
4,0
3,0
2,0
1,0
0,0
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60
Richesse
Kérosène Dodécane
120,0
100,0
80,0
D32 [um]
60,0
40,0
20,0
0,0
Figure 4.10 - Variation de la
granulométrie d'aérosols de kérosène et
dodécane générés par l'atomiseur en fonction de
la
richesse à une cote d'observation z = 16 cm
Page | 46
Idéalement, il aurait fallu effectuer nos mesures
granulométriques à une hauteur de 3 ou 4 m. Malheureusement, il
n'est pas possible dans les conditions de cette étude de procéder
à des mesures de granulométries à ces hauteurs
d'observation.
4.3.3 Conclusions
Les mesures granulométriques par la méthode PDI
effectuées sur des aérosols générés par
l'atomiseur, ont conduit aux résultats suivant :
? la distribution granulométrique des aérosols
produits est de type gaussien, avec un écart type maxima de 11 um
? le débit d'air a peu d'influence sur les valeurs du
diamètre moyen D10 et sur le diamètre de sauter D32. Toutefois,
une dispersion en D32 est constatée à cause du poids relatif des
grosses gouttelettes dans le calcul du D32.
? Le générateur d'aérosols fournit des
gouttelettes de taille comprise entre 4 et 6 um. Pour la suite des travaux, une
taille de diamètre moyen unique sera prise en compte à savoir d0
= 5um.
Page | 47
Chapitre 5
5 Les mélanges réactifs
5.1 Introduction
Ce chapitre abordera la présentation des
mélanges réactifs étudiés à savoir comme
produit principal, le kérosène Jet-A1, et comme produit
secondaire le dodécane.
5.2 Produits étudiés
? Kérosène Jet-A1
Le kérosène est essentiellement utilisé
dans la fabrication de carburant pour l'aviation (turboréacteur et
turbopropulseur) notamment le Jet A-1, le principal d'entre eux. Le Jet A-1 est
le carburéacteur le plus utilisé, il est destiné à
l'alimentation des avions à réaction civils et militaires (avions
équipés de turboréacteurs). Ce dernier est obtenu à
partir de pétrole brut selon une coupe de distillation comprise entre
150 et 250°C. Il est constitué de centaines de composés
(environ 300 produits "majoritaires") dont la chaîne carbonée est
principalement comprise entre 9 et 15 atomes de carbones (C9 à C15).
Les contraintes propres aux applications aéronautiques
(volume disponible, conditions rencontrées en altitude,
sécurité d'utilisation) font du kérosène un produit
aux spécifications sévères et soigneusement
contrôlées à tous les stades de son élaboration,
depuis la fabrication jusqu'au stockage avant distribution. Le Jet A-1, comme
tous les carburants, ne possède pas une composition figée mais
est défini selon un ensemble de normes ou spécifications, les
normes les plus courantes proviennent de l'American Society for Testing and
Materials ou ASTM. (cf. Annexes AIII)
Les kérosènes Jet A et Jet A-1 sont
composés de milliers d'hydrocarbures. On y retrouve principalement une
composition volumique de 80 % d'hydrocarbures saturés, tels que les
paraffines linéaires, ramifiées ou cycliques, 15 à 20 %
d'espèces mono voire bi-aromatiques et moins de 5 %
d'oléfines.
Le kérosène Jet-A1 répond à des
caractéristiques bien définies et strictes, liées aux
conditions d'utilisation en sol ou en vol. Ce carburéacteur doit pouvoir
répondre aux contraintes liées au moteur et à son
fonctionnement comme :
·
Page | 48
la viscosité, la densité et le point de
congélation (-47°C pour le Jet-A1) ;
· la chaleur de combustion ;
· le pouvoir corrosif et lubrifiant ;
· la stabilité thermique.
D'autres contraintes dépendent des conditions de
sécurités (stockage et manutention), de vol ou environnementales
comme :
· le point éclair (« flash point »)
définissant la température la plus basse à laquelle le
liquide fournit suffisamment de vapeur pour former en contact avec l'air, un
mélange gazeux qui peut s'enflammer au contact d'une source
d'énergie calorifique mais insuffisante pour entretenir la
déflagration (combustion) ;
· la conductivité électrique. Le
kérosène possède une faible conductivité
électrique, il peut potentiellement se produire une décharge
électrique brusque, par accumulation des charges
électrostatiques, qui enflammera le mélange air ~ carburant. La
conductivité électrique du Jet-A1 est comprise entre 0,5 et 4,5
pS/cm ;
· le point de congélation (« freezing point
») doit se situer à la température la plus basse (-47°C
pour le Jet-A1) afin d'éviter que le carburéacteur gèle en
altitude et entraine de sérieux dysfonctionnements du moteur.
La composition chimique du kérosène
n'étant pas connue avec exactitude pour des raisons de secret
professionnel, il nous a fallu trouver une molécule s'approchant au
mieux des caractéristiques du Jet-A1.
Il s'avère que dans la littérature le
kérosène est souvent assimilé, selon la source, à
une formule chimique variant de ??10,9??20,9 à ??12??23
(tableau 5.1). Quelques caractéristiques chimiques et physiques de
comparaison avec le Jet-A1 sont reprises dans le tableau 5.2.
Sources Formule chimique approchée
Gracia-Salcedo et al. ??12??23
Edwards et Maurice ??11??21
Martel ??11.6??22
Guéret ??11??22
Nguyen et Ying ??11??23
Tableau 5.1 - Formule chimique du
kérosène conventionnel
Page | 49
|
JET-A1
|
C11H22
|
|
Density [g/cm3]
|
0,7825
|
0,79
|
|
Boiling Point [°C]
|
130 ~ 290
|
218,4
|
|
Flash Point [°C]
|
>38
|
73,7
|
|
Indice réfraction
|
1,45 ~ 1,46
|
1,433
|
Tableau 5.2 - Comparatif de quelques
caractéristiques chimiques et physiques entre le JET-A1 et le C11H22
Au regard des grandeurs ci-dessus, les valeurs étant
relativement proches, l'hypothèse consistera à approximer le
kérosène par une molécule de C11H22 pour pouvoir
évaluer la richesse. Tout au long de ce travail, la formule chimique
approchée du kérosène adoptée est celle de
Guéret.
? Dodécane
Le dodécane est un alcane linéaire de formule
brute C12H26. C'est un liquide huileux de la série des
paraffines. Il possède 355 isomères structuraux. Ces
dernières années, le dodécane a retenu l'attention comme
possible substitut aux carburants à base de kérosène tels
que le Jet-A, le S-8, et d'autres carburants d'aviation conventionnels. Il est
considéré comme un substitut de carburant de deuxième
génération, conçu pour émuler la vitesse de flamme
laminaire, supplantant largement le n-décane, principalement en raison
de sa masse moléculaire plus élevée et de son ratio
hydrogène/carbone qui correspond mieux à ceux des n-alcanes de
carburéacteurs. Ses caractéristiques sont résumées
dans le tableau 5.3.
|
Propriétés chimiques et physiques
Formule brute C12H26
|
|
MC12H26 [g/mole]
|
170,3348 #177; 0,0114
C 84,62 %, H 15,39 %
|
|
Diamètre moléculaire
|
0,761 nm
|
|
T° fusion
|
-9,65 °C
|
|
T° ébullition
|
216,32 °C
|
|
Masse volumique
|
0,7455 g/cm3 à 24,95 °C
|
|
T° d'auto-inflammation
|
200 °C
|
|
Point d'éclair
|
74 °C
|
|
Viscosité dynamique
|
1,324 mPa.s à 24,95 °C
0,891 mPa.s à
49,95 °C
|
|
Point critique
|
1 820 kPa, 385,1 °C
|
Tableau 5.3 - Caractéristiques
physiques et chimiques du dodécane
5.3 Caractéristiques de détonation CJ
Les caractéristiques idéales de
détonation en célérité et pression sont
calculées à partir d'un logiciel de thermochimie GASEQ pour les
conditions initiales T0=298K et P0=1bar. Ces caractéristiques serviront
de base de comparaison avec les résultats expérimentaux
exposés au chapitre 6. Il est à noter que ce logiciel ne fournit
des résultats que pour les molécules gazeuses alors que notre
molécule de travail est un liquide. Néanmoins, la valeur de
célérité de détonation obtenue par ce logiciel
donne un bon ordre de grandeur des célérités, assez proche
d'un cas où la molécule serait liquide. L'évolution de la
célérité de détonation CJ en fonction de la
richesse est indiquée sur la figure 5.1, ainsi que sur le tableau
5.4.

0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60 1,80 2,00
Richesse
D [m/s]
2100
1900
1700
1500
1300
1100
900
700
500
Figure 5.1 - Evolution de la
célérité idéale CJ de détonation du
mélange kérosène ~ air en fonction de la richesse
Page | 50
Page | 51
|
Richesse
|
DCJ [m/s]
|
PCJ [bar]
|
Nb mole O2
|
Nb mole N2
|
|
0,38
|
872,46
|
4,303
|
43,61
|
163,99
|
|
0,51
|
1232,61
|
8,388
|
32,47
|
122,09
|
|
0,61
|
1417,74
|
11,09
|
27,13
|
102,00
|
|
0,57
|
1348,77
|
10,034
|
29,06
|
109,28
|
|
0,68
|
1521,44
|
12,791
|
24,34
|
91,51
|
|
0,63
|
1447,74
|
11,568
|
26,30
|
98,88
|
|
0,64
|
1470,21
|
11,933
|
25,69
|
96,61
|
|
0,67
|
1508,31
|
12,568
|
24,68
|
92,81
|
|
0,94
|
1784,41
|
17,772
|
17,57
|
66,08
|
|
1,00
|
1808,48
|
18,301
|
16,50
|
62,04
|
|
1,16
|
1838,03
|
19,026
|
14,18
|
53,31
|
|
1,21
|
1840,96
|
19,121
|
13,63
|
51,24
|
|
1,40
|
1837,84
|
19,192
|
11,79
|
44,31
|
|
1,50
|
1829,34
|
19,084
|
11,00
|
41,36
|
|
1,60
|
1818,3
|
18,923
|
10,31
|
38,78
|
|
1,80
|
1791,54
|
18,504
|
9,17
|
34,47
|
Tableau 5.4 - Célérité et
pression de détonation CJ pour différents ratio O2/N2
5.4 Détermination de la richesse du
mélange
La méthodologie et les résultats des essais
effectués pour étalonner les débits de liquide fournis par
l'atomiseur, ainsi que la détermination de la richesse du mélange
réactif qui en découle sont exposés dans l'annexe
AII.
Page | 52
Page | 53
Chapitre 6
6. Etude expérimentale de l'influence de la
taille des gouttelettes sur la détonation d'aérosols de
carburants liquides
6.1 Introduction
Ce chapitre a pour but d'exposer les résultats
expérimentaux sur la formation de la détonation dans les
aérosols des carburants étudiés. Afin de
caractériser la détonation, des mesures de
célérité et de pression sont effectuées et les
caractéristiques de la structure cellulaire sont également
étudiées. Ces résultats permettront de mettre en
évidence l'influence éventuelle de la granulométrie sur la
détonation des carburants étudiés.
Pour l'ensemble des expériences effectuées, les
conditions expérimentales correspondantes sont reprises dans le tableau
6.1.
|
Dispositif
d'atomisation
|
Dispositif
d'amorçage
|
Conditions initiales de tir
|
Dimensions
de la plaque
de suie (mm)
|
|
Taille de l'aérosol
(um)
|
Prémélange
gazeux
|
Pression
d'initiation
(bars)
|
Inflammateur
|
Température
(K)
|
Pression
(bars)
|
420 * 53
|
|
5
|
C2H4/O2
richesse 1
|
2 ou 3
|
Electrique
|
293
|
1
|
Tableau 6.1 - Conditions expérimentales
des différents tests réalisés
6.2 Initiation de la détonation par un tube à
choc (booster)
Le dispositif d'amorçage de la détonation se
fait par tube à choc dont le fonctionnement est décrit au
chapitre 3. Ce dispositif permet d'obtenir la propagation d'un choc sur toute
la longueur du tube. Dans un premier temps, les caractéristiques de
l'onde de choc produite par le booster seul dans le tube principal sont
étudiées pour les conditions initiales suivantes :
? prémélange C2H4/O2 stoechiométrique
sous 2 bars de pression initiale, ? prémélange C2H4/O2
stoechiométrique sous 3 bars de pression initiale
Les célérités moyennes du choc en
fonction de la distance de propagation le long du tube principal sont
indiquées à la figure 6.1. Les courbes montrent que quelle que
soit la pression initiale, l'onde de choc ralentit lors de sa propagation. On
notera que sous une pression initiale de 3 bars, la
célérité du choc est supérieure à celle
initiée sous 2 bars, ce qui serait à priori une situation plus
favorable à la transition choc/détonation pour amorcer la
détonation.
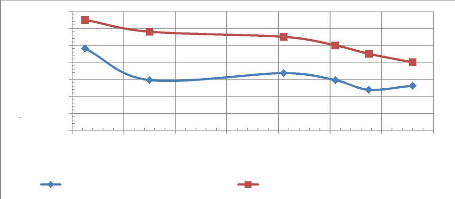
Célérité de choc (m/s)
1500,00
1400,00
1300,00
1200,00
1100,00
1000,00
900,00
800,00
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Booster seul - Pression initiale 2 bars Booster seul - Pression
initiale 3 bars
Figure 6.1- Evolution de la
célérité de la détonation en fonction de la
distance de propagation dans le tube principale initié
par un booster
seul de prémélange C2H4/O2
Les signaux de pression enregistrés lors de la
propagation du choc sont reproduits sur la figure 6.2.
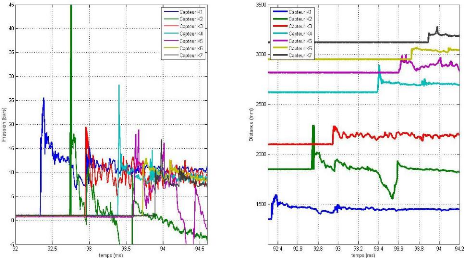
Figure 6.2 - Signaux de pression le long du tube
principal avec booster seul de prémélange C2H4/O2 sous 2 bars de
pression
initiale
Page | 54
Page | 55
Cette expérience sera utilisée par la suite
comme base de comparaison avec les valeurs de célérité et
de pression enregistrées dans le cas du booster + mélange
réactif.
6.3 Détonation dans le mélange
d'aérosol de gouttelettes de kérosène/air
Nous présentons ici, les résultats des
expériences effectuées sur la détonation
hétérogène du mélange kérosène Jet-A1
~ Air. Les gouttelettes sont de taille moyenne 5 à 6 um et le domaine de
richesse est compris entre 1,1 et 1,5. Le but est de se placer dans conditions
optimales pour faciliter l'établissement d'une détonation stable
et autonome en vue d'obtenir des structures cellulaires.
La détonation s'effectue avec un booster contenant un
prémélange ??2??4/??2 sous 2 bars de pression
initiale.
6.3.1 Formation de la détonation
Après la détonation du prémélange
introduit dans le booster, la membrane de mylar est rompue et un choc est
généré dans le tube principal et se propage jusqu'à
la partie supérieure du tube. Sur la figure 6.3, l'évolution de
la pression dans le tube à détonation enregistrée entre
les capteurs K1 et K7 est représentée pour une richesse r =
1,1.

Figure 6.3 - Profils de pression et diagramme
de marche, enregistrés en K1, K2, K3, K4, K5, K6 et K7 de la
détonation du
mélange Kérosène/Air, C11H22 +
16,5 (O2 + 3.76); r=1,1 et d0 = 5um
6.3.2 Célérité de
détonation

K7
K6
K5
Célérité de détonation (m/s)
1600,00
1500,00
1400,00
1300,00
1200,00
1100,00
1000,00
900,00
800,00
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Test 2,3 ~ Kérosène/Air ~ r=1,1 ~ Booster
seul H4/O2 à 2 bars
Booster seul Test 2 Test 3

Aucune structure cellulaire relevée sur la plaque de
suie
Page | 56
Capteur K4 Capteur K5 Capteur K6 Capteur K7
Figure 6.4 - Célérité
moyenne du front en fonction de la distance de propagation et enregistrement de
la structure cellulaire pour le mélange kérosène/air avec
une richesse = 1,1
La figure 6.4 montre que la célérité
décroit à partir de 1400 m/s jusqu'à passer à une
valeur de célérité inférieure à celle du
booster seul, il n'y a donc pas détonation mais bien extinction puisque
dans ce cas-ci, la célérité ne se stabilise pas à
une valeur constante. Le système tend à revenir vers
l'état caractérisé au point 6.2 lors du tir booster
seul.
Trois tests ont été réalisés pour
cette valeur de richesse afin de tester la reproductibilité des
résultats, deux d'entre eux ont fourni les mêmes constations
repris à la figure 6.4. Toutefois, l'un des tests a fourni une structure
cellulaire bien particulière (figure 6.5) cependant le système
d'acquisition de pression ne s'est pas mis en marche suite à un
problème d'ordre électrique sur le système. Les valeurs de
pressions et de célérité sont donc

inconnues pour ce test.
Sens de propagation
Figure 6.5 - Enregistrement de la structure
cellulaire du mélange kérosène/air - r=1,1 - Test 1
L'enregistrement révèle sur la plaque de suie
une structure de type hélicoïdale. Cette structure est bien connue
et s'obtient souvent lorsque l'on est proche des limites de détonation.
N'ayant pas obtenu de structure avec les autres tests, la richesse 1,1
correspond surement à la limite inférieure de
détonabilité de l'aérosol de kérosène. Afin
d'essayer d'initier de nouveau une détonation, l'amorçage de
nouveaux essais ont été effectuée à une pression
initiale du booster de 3 bars et une richesse de 1,3. Les enregistrements de
pression sont reproduits sur la figure 6.6 et ceux de
célérité et de la structure cellulaire sur les figures 6.7
à 6.10.
Page | 57
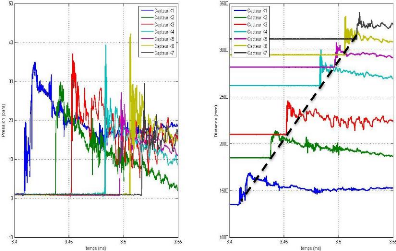
Page | 58
Figure 6.6 - Profils de pression et diagramme de
marche, enregistrés en K1, K2, K3, K4, K5, K6 et K7 de la
détonation du mélange Kérosène/Air, C11H22 + 16,5
(O2 + 3.76); r=1,3 et d0 = 5um
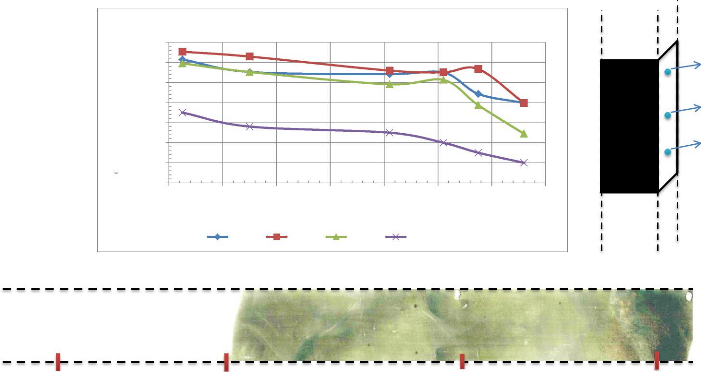
Célérité de détonation (m/s)
1800,00
1700,00
1600,00
1500,00
1400,00
1300,00
1200,00
1100,00
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Test 4,5,6 ~ Kérosène/Air ~ r=1,3 ~ Booster
H4/O2 à 3 bars
Test 4 Test 5 Test 6 Booster seul
K7
K6
K5
Page | 59
Capteur K4 Capteur K6
Capteur K5 Capteur K7
Figure 6.7 - Célérité
moyenne du front en fonction de la distance de propagation et enregistrement de
la structure cellulaire pour le mélange kérosène/air avec
une richesse = 1,3

? Structures cellulaires enregistrées
pour ce mélange
Sens de propagation
Figure 6.8 - Enregistrement de la structure
cellulaire du mélange kérosène/air - r=1,3 - Test 4

Figure 6.9 - Enregistrement de la structure
cellulaire du mélange kérosène/air - r=1,3 - Test 5
Figure 6.10 - Enregistrement de la structure
cellulaire du mélange kérosène/air - r=1,3 - Test 6
La figure 6.7 montre que la célérité
décroit jusqu'à une valeur de #177; 1500 m/s. Les figures 6.8
à 6.10 montrent différentes structures, en effet à la
figure 6.9 on observe une demi-cellule de cellule plus large que le tube
>> 53 mm.
Page | 60
6.3.3 Pression de détonation
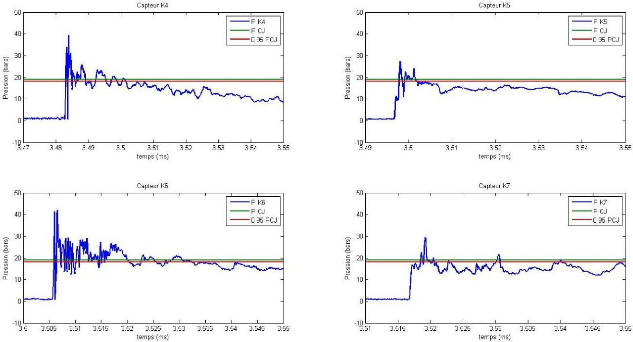
Page | 61
Figure 6.11 - Profils de pressions des capteurs
K4, K5, K6 et K7 en fin de propagation dans le tube à détonation
pour le mélange kérosène/air avec une richesse = 1,3
Page | 62
La détermination de la pression de détonation
n'est pas simple car le signal de pression comporte une plage importante de
fluctuations. La lecture de pression qui correspond à la pression de
détonation au point CJ est donc difficile. De plus, l'identification des
points ZND et CJ est entachée d'incertitude. En effet, si la taille des
cellules est grande, la position relative du capteur de pression par rapport
à la trajectoire du point triple joue un rôle important sur
l'amplitude des pressions enregistrées au point de mesure.
En général, la détermination graphique de
la pression de détonation est obtenue par l'intersection du front de
choc avec la droite reproduisant l'évolution moyenne du signal
après le pic de pression (figure 6.12).

Figure 6.12 - Principe de détermination
de la valeur expérimentale de la pression de détonation Pexp
Les pressions idéales PCJ sont obtenues en utilisant le
logiciel de thermochimie GASEQ (cf. Chapitre 5) et servent de base de
comparaison avec la pression expérimentale mesuré Pexp. La
détonation pourra être considérée stable et autonome
si la célérité du front reste constante au niveau des
capteurs K5 ... K7 et que la pression expérimentale Pexp reste comprise
entre 0,95 PCJ et PCJ. Dans les expériences présentes, il n'est
pas sûr que le régime de propagation observé soit
complétement autonome.
6.3.4 Structure cellulaire de détonation
Les enregistrements effectués sur les plaques de suie
(figure 6.8, 6.9 et 6.10) fournissent pour les mêmes conditions
expérimentales des résultats différents. A la figure 6.8,
il semblerait que l'on voit des cellules entières, tandis qu'à la
figure 6.9 il semblerait que cela
Page | 63
correspond à de la demi-cellule ou à une
structure hélicoïdale. Concernant la figure 6.10, on voit une trace
en début de plaque uniquement. Ces différentes observations
indiquent que le régime de propagation dans ces conditions est proche de
la limite de détonabilité. Après l'examen qualitatif des
structures cellulaires, une taille de la cellule peut être estimée
comme supérieure à 53 mm.
6.3.5 Influence de la pression initiale du booster
Afin de compléter l'étude du
kérosène, d'autres tests expérimentaux ont
été réalisés cette fois-ci à une richesse
plus élevé, à savoir 1,5 et avec une pression initiale de
booster de 2 bars et 3 bars. Les résultats précédents ont
montré que le kérosène est difficile à
détoner et qu'une chute de célérité assez
importante apparait entre les capteurs K6 et K7. Ce dernier
phénomène est constaté de nouveau dans le cas d'un
allumage du mélange r=1,5 avec un booster de 2 bars (figure 6.13).
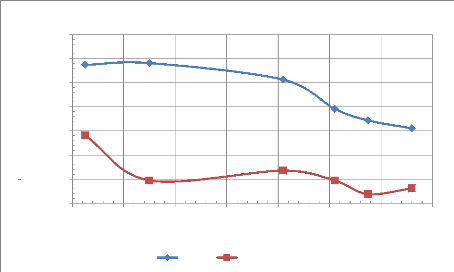
Célérité de détonation (m/s)
1700,00
1600,00
1500,00
1400,00
1300,00
1200,00
1100,00
1000,00
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Test 8 ~ Kérosène/Air ~
r=1,5 ~ Booster H4/O2 à 2 bars
Test 8 Booster 2 bars
Figure 6.13 - Célérité du
front de détonation en fonction de la distance de propagation dans le
tube à détonation pour le
mélange
kérosène/air avec une richesse = 1,5 et pression booster 2
bars.
Aucune structure cellulaire n'a été
observée dans ce test. L'évolution de
célérité montre que celle-ci ne se stabilise pas et
diminue progressivement jusqu'à une valeur de 1300 m/s. Ce test confirme
que pour initier une détonation avec le kérosène une
pression au booster importante est nécessaire.
Page | 64
Dans le cas d'un allumage avec un booster de 3 bars, les
observations sont les suivantes : 6.3.5.1 Célérité
de détonation

Célérité de détonation (m/s)
1900,00
1800,00
1700,00
1600,00
1500,00
1400,00
1300,00
1200,00
1100,00
1000,00
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Test 9 ~ Kérosène/Air ~
r=1,5 ~ Booster H4/O2 3 bars
Booster 3 bars Test 9 DCJ
K7
K6
K5
Capteur K4 Capteur K6 Capteur K7
Capteur K5
Figure 6.14 - Célérité du
front de détonation en fonction de la distance de propagation dans le
tube à détonation pour le mélange
kérosène/air avec une richesse = 1,5 et booster de 3 bars.
6.3.5.2 Pression de détonation
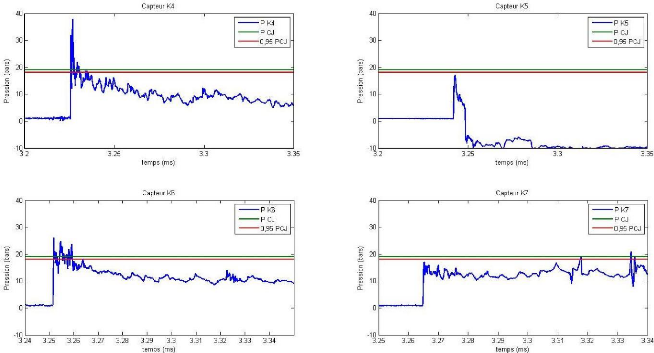
Page | 65
Figure 6.15 - Profils de pressions des capteurs
K4, K5, K6 et K7 en fin de propagation dans le tube à détonation
pour le mélange kérosène/air avec une richesse = 1,5 et
booster de 3 bars
Page | 66
6.3.6 Synthèse des résultats obtenus pour
le mélange kérosène/air ? Célérité
moyenne de détonation
L'évolution de la célérité moyenne
de détonation déterminée expérimentalement Dexp en
fonction de la richesse est indiquée à la figure 6.16. Il en
ressort qu'à richesse faible, le déficit de
célérité est de l'ordre de 15%, cet écart a
tendance à diminuer puisque à une richesse de 1,3 le
déficit est de 12% et à la richesse 1,5 il n'est plus que de
10%.
Cependant, les valeurs de célérité
expérimentales restent inférieures aux valeurs de
célérités idéales DCJ (calculées avec le
logiciel de thermochimie GASEQ, le mélange en phase gazeuse, alors que
dans cette étude expérimentale, le kérosène
utilisé est à l'état liquide). En prenant en compte cette
remarque, le déficit de célérité est probablement
plus faible.
1 1,1 1,2 1,3 1,4 1,5 1,6
richesse
Dexp DCJ 0,85 DCJ 0,9 DCJ

Célérité de détonation (m/s)
1900
1800
1700
1600
1500
1400
1300
1200
1100
1000
Figure 6.16 - Evolution de la
célérité moyenne de détonation expérimentale
Dexp en fonction de la richesse du mélange
réactif kérosène/air
? Pression de détonation
Les pressions mesurées juste à l'arrière
du front de détonation sont rassemblées sur la figure 6.17 et
comparées aux valeurs de pressions idéales PCJ.
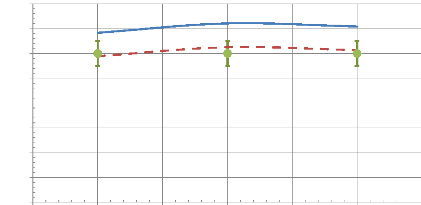
Pression de détonation (bars)
20
19
18
17
16
15
14
13
12
1 1,1 1,2 1,3 1,4 1,5 1,6
richesse
Pexp PCJ 0,95 PCJ
Page | 67
Figure 6.17 - Evolution de la pression moyenne
de détonation expérimentale Pexp en fonction de la richesse du
mélange du mélange réactif kérosène/air
La figure 6.17 montre une évolution de la pression
expérimentale très similaire à celle de la pression
moyenne de détonation de Chapman-Jouguet.
? Structure cellulaire
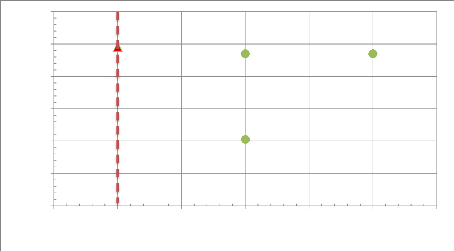
ë (mm) Pas P(mm)
132
112
92
72
32
52
12
1 1,1 1,2 1,3 1,4 1,5 1,6
richesse
Figure 6.18 - Evolution de la taille de la
cellule de détonation en fonction de la richesse du mélange du
mélange réactif
kérosène/air
Page | 68
La figure 6.18 montre différentes structures
cellulaires obtenues en fonction de la richesse. Pour une richesse r = 1,1, ce
régime particulier correspond à de l'hélicoïdale et
se caractérise par un pas de détonation de l'ordre de 110 mm. A
richesse plus élevée r = 1,3 et r = 1,5, on observe une
demi-cellule de cellule plus large que le tube >> 53 mm (#177; 106
mm).
6.3.7 Bilan pour le mélange
kérosène/air
Les expériences dans les aérosols de
kérosène dans l'air montrent qu'il est possible d'initier la
détonation sans vaporisation préalable, bien que
l'amorçage soit difficile. En effet, pour l'initiation une
énergie importante est nécessaire, et le régime de
détonation n'a pas toujours été atteint pour les tirs
réalisés à une pression de booster de 2 bars. Une pression
de 3 bars était plus favorable. La détonation s'initie mais on ne
peut affirmer avoir atteint un régime stable et autonome, la distance
d'observation étant insuffisante pour trancher.
La structure tridimensionnelle de détonation est mise
en évidence pour ces mélanges biphasiques. Différents
régimes de propagation ont été observés et dans
certains cas pour les mêmes conditions expérimentales. Plusieurs
structures cellulaires ont été relevées pour des
conditions identiques : hélicoïdale, demi-cellule, cellule
entière. La dimension de ces structures est importante. Tout cela montre
que le comportement est proche des limites de propagation. De manière
générale, ce mélange biphasique est difficile à
faire détoner.
Remarque : La plupart des évolutions de
célérité moyenne sont qualitativement identiques. Entre le
capteur K4 et K5, une baisse de célérité est à
chaque fois constatée et ce, même pour le cas du booster seul.
Cela peut s'expliquer par la géométrie du tube, en effet, entre
K4 et K5 se trouve un léger changement de section. Au départ, le
tube carré a une forme arrondie au niveau des angles et une fois
arrivé au niveau de la chambre d'enregistrement de la cellule les coins
sont de forme aigue. Ce changement de section qui se produit à 2,75 m du
bas du tube peut expliquer la décélération locale du
front.
6.4 Détonation dans le mélange
d'aérosol de gouttelettes de kérosène/air
suroxygéné
Quelques expériences ont été
effectuées sur la détonation hétérogène du
mélange kérosène Jet-A1 ~ Air suroxygéné (O2
+ 2N2). Un mélange avec de l'air suroxygéné est
utilisé afin de diminuer la taille de cellule. (Mélange air
suroxygéné cf Annexes AIV)
6.4.1 Richesse r = 1
a. Formation de la détonation
La figure 6.19 reprend l'évolution de la pression de
détonation du mélange kérosène air
suroxygéné à richesse 1, entre les capteurs K1 et K7.
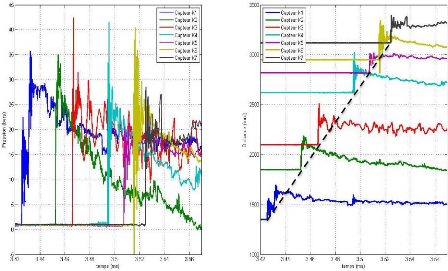
Page | 69
Figure 6.19 - Profils de pression et diagramme
de marche, enregistrés en K1, K2, K3, K4, K5, K6 et K7 de la
détonation du mélange Kérosène + (O2+2N2); r=1 et
d0 = 5um
b. Célérité de la
détonation

Célérité de détonation (m/s)
1900,00
1800,00
1700,00
1600,00
1500,00
1400,00
1300,00
1200,00
1100,00
1000,00
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Test 10 ~ Kérosène +
(O2+2N2) ~ r=1 ~
Booster H4/O2 à 3 bars
Booster 3 bars DCJ Test 10
K7
K6
K5
Page | 70
Capteur K4 Capteur K6 Capteur K7
Capteur K5
Figure 6.20 - Célérité du
front de détonation en fonction de la distance de propagation dans le
tube à détonation du mélange Kérosène +
(O2+2N2); r=1 et d0 = 5um
c. Pression de détonation

Page | 71
Figure 6.21 - Profils de pressions des capteurs
K4, K5, K6 et K7 en fin de propagation dans le tube à détonation
du mélange Kérosène + (O2+2N2); r=1 et d0 = 5um
Page | 72
6.4.2 Richesse r = 1,3
a. Célérité de
détonation

Célérité de détonation (m/s)
2000,00
1900,00
1800,00
1700,00
1600,00
1500,00
1400,00
1300,00
1200,00
1100,00
1000,00
Test 11 ~ Kérosène +
(O2+2N2) ~ r=1,3 ~
Booster H4/O2 à 3 bars
1800 2000 2200 2400 2600 2800 3000 3200
distance de propagation (mm)
Booster 3 bars DCJ Test 11
K7
K6
K5
Capteur K4 Capteur K6 Capteur K7
Capteur K5
Figure 6.22 - Célérité du
front de détonation en fonction de la distance de propagation dans le
tube à détonation du mélange Kérosène +
(O2+2N2); r=1,3 et d0 = 5um
b. Pression de la détonation

Page | 73
Figure 6.23 - Profils de pressions des
capteurs K4, K5, K6 et K7 en fin de propagation dans le tube à
détonation du mélange Kérosène + (O2+2N2); r=1,3 et
d0 = 5um
6.4.3 Synthèse des résultats obtenus pour
les mélanges kérosène/air suroxygéné
L'analyse des évolutions de
célérité et des profils de pression ainsi que de la
structure cellulaire, permet d'affirmer qu'une détonation stable et
autonome est atteinte et cela pour les deux richesses étudiées.
En effet, la figure 6.19 montre que la détonation est formée
dès le capteur K1, les pics de pression sont relativement
élevés et la célérité de détonation
est quasi-constante. L'évolution de la célérité
moyenne de détonation comme le montre la figure 6.20, est très
proche de la valeur théorique de Chapman Jouguet. Le déficit de
célérité mesuré est de 3%. La pression
expérimentale mesurée à partir des profils de pressions de
la figure 6.21 est de l'ordre de 18,1 bars soit très proche de la
pression idéale de Chapman Jouguet qui est de 18,3 bars. Les mêmes
constatations sont faites pour l'expérience à richesse plus
élevée r =1,3. En effet, l'analyse de l'évolution de
célérité et du profil de pression ainsi que de la
structure cellulaire obtenue (figure 6.22 et 6.23) permettent d'affirmer
l'établissement d'un régime de détonation autonome.
Le kérosène détone difficilement avec de
l'air, par contre avec de l'air suroxygéné, sa
réactivité est plus importante. En effet, un régime de
détonation multicellulaires est obtenu (figure 6.24 et 6.25). La taille
caractéristique des cellules de détonation X est de l'ordre de 30
mm à richesse 1 et de 22 mm à une richesse de 1,3. Dans la
configuration expérimentale considérée, le
kérosène peut détonner avec de l'air
suroxygéné, sans vaporisation préalable des
gouttelettes.

ë
Figure 6.24 - Enregistrement de la structure
cellulaire du mélange kérosène + (O2 + 2 N2), r=1 - Test
10
L
L
ë
Figure 6.25 - Enregistrement de la structure
cellulaire du mélange kérosène + (O2 + 2 N2), r=1,3 - Test
11
Page | 74
Page | 75
Synthèse et conclusion
L'objectif de ce TFE était d'apporter une meilleure
connaissance des caractéristiques et des mécanismes de
propagation des détonations dans des milieux
hétérogènes composés d'aérosols de
gouttelettes liquides de kérosène dans une atmosphère
gazeuse oxydante. Le travail a consisté à mettre en
évidence l'existence de la structure cellulaire de détonation,
avec un aérosol de gouttelettes de kérosène de taille 5
um. Ainsi, une étude purement expérimentale a été
menée.
Le montage expérimental mis au point pour cette
étude est composé principalement d'un tube à
détonation vertical, d'environ 4 m de longueur et de section
carrée 53*53 mm. Le tube est instrumenté sur toute sa longueur de
capteurs de pressions pour suivre l'évolution de la pression et de la
célérité au cours de la propagation de l'onde incidente,
ainsi que de plaques disposées en paroi permettant le relevé de
la structure cellulaire par la méthode des traces de suie, sur une
distance de 400 mm. Cette installation possède une
caractéristique importante qui est la génération de
l'aérosol par atomiseur ultrasonique. La méthodologie
utilisée permet de remplir le tube à détonation sur toute
sa longueur tout en ayant des aérosols de caractéristiques
contrôlées et une distribution granulométrique quasi
monodispersée.
Les expériences ont été
réalisées avec du kérosène Jet-A1 dispersé
dans de l'air pour une granulométrie d'aérosols de 5 um, dans des
conditions de température et de pression ambiante.
Les résultats ont mis en évidence qu'il
était possible d'observer les traces de la structure cellulaire de
détonation dans les mélanges d'aérosols de gouttelettes
liquides combustibles étudiés. Ce résultat est important,
puisque les résultats expérimentaux obtenus sont novateurs.
Il a été possible durant la phase
expérimentale, de dégager des conditions opératoires
permettant d'initier des détonations dans des aérosols
dispersés dans l'air. Par contre, il est très difficile
d'affirmer si la détonation obtenue est stable et autonome, ce qui
nécessiterait l'observation de la propagation du front sur une distance
plus longue. Néanmoins, dans le cas du mélange avec l'air
suroxygéné, il semble qu'un régime de propagation de
détonation stable et autonome ait été atteint.
Page | 76
En conséquence, il apparait que les aérosols de
gouttelettes liquides de kérosène dans l'air, de
granulométrie suffisamment petite, peuvent détoner. La plupart
des travaux antérieurs s'accordaient à dire qu'il était
très difficile, voire même impossible, de faire détoner cet
aérosol dans de l'air. Les détonations n'étaient obtenues
que dans de l'oxygène pur ou dans le cas d'air mais avec un
préchauffage permettant la vaporisation des gouttelettes afin de
générer la propagation en phase gazeuse.
Ce travail complète les travaux antérieurs
réalisés sur l'influence de la granulométrie sur la
détonation des mélanges diphasiques et montre que la
granulométrie des gouttelettes est un paramètre physique
influençant la détonation.
L'ensemble des résultats obtenus montre que le
kérosène Jet-A1 est un carburant difficile à faire
détoner avec l'air. L'influence de la granulométrie des
gouttelettes sur les mécanismes de propagation des détonations en
milieu biphasique doivent être poursuivis. En effet, les résultats
ont été obtenus avec une granulométrie très fine.
La taille des cellules de détonation obtenues avec le
kérosène est assez importante. Il est donc nécessaire
d'étudier plus en détail l'influence de la richesse, de la
granulométrie et de la dilution du mélange sur la
détonation du kérosène.
Des perspectives peuvent être envisagées afin
d'améliorer les résultats obtenus avec le kérosène.
La taille de la cellule obtenue étant de l'ordre de grandeur de la
section du tube, une manière de la diminuer serait d'agir sur la
réactivité du mélange par exemple en travaillant à
des conditions de pression supérieure à 1 atm dans le tube
à détonation, tout en veillant à conserver des
caractéristiques d'aérosols reproductibles. Une autre voie
explorable est l'utilisation de mélange hybrides deux combustibles (l'un
gazeux, l'autre liquide) + un oxydant.
Page | 77
Bibliographie
[1] Benmahammed M. A., « Détonations dans les
aérosols de gouttelettes liquides réactives. Etude de l'influence
des propriétés physicochimiques de la phase liquide et de
l'oxydant gazeux » Thèse de doctorat ENSMA, Poitiers, janvier
2013.
[2] Castanet G.; « Etude aérothermique d'un jet
de gouttes monodispersé en évaporation et en combustion à
l'aide de méthodes optiques », Thèse de doctorat,
Vandoeuvre-lès-Nancy, 1er Octobre 2004.
[3] Chang C.T., Farrell P.V., 1998, Spray characteristics and
near injector tip effects of injection pressure and ambient density, Comodia,
p. 1973.
[4] Lassauce A. ; « Visualisation, granulométrie et
évaporation de gouttes et de sprays - Etude dans une atmosphère
close et pressurisée » Thèse de doctorat, Alès, 22
février 2011.
[5] Lebas R. ; « Modélisation Eulérienne de
l'Atomisation Haute Pression Influences sur la Vaporisation et la Combustion
Induite » Thèse de doctorat, Rouen, 26 octobre 2007.
[6] Mar M., « Détonations dans les aérosols
de gouttelettes liquides réactives. Etude de l'influence de la
granulométrie des gouttelettes » Thèse de doctorat ENSMA,
Poitiers, 26 janvier 2012
[7] Reitz, R.D. and Diwakar, R., «Structure of
High-Pressure Fuel Spray, » SAE Technical Paper Series 870598.
[8] Reitz R.D. Modeling atomization processes in high-pressure
vaporizing sprays. Atom. SprayTech, 3: 309-337, 1987.
[9] Reitz R.D. and Diwakar R. Effect of drop break-up on fuel
sprays. Technical Report 860469, SAE paper, 1986.
[10]
Page | 78
Reitz R.D. Atomization and other break-up regimes of a liquid
jet. PhD thesis, Princeton University USA, 1978.
[11] Reitz R.D. et Bracco F.V. - Mechanisms of breakup of round
liquid jets. In: Encyclopedia of Fluid Mechanics. pp. 233-249. - NJ, 1986. 34,
36, 43.
[12] Abdellah TOUIL. ; « Modélisation des jets
diphasiques liquide vapeur et du « rain out » » Thèse de
doctorat, Saint Etienne, 2 janvier 2004.
[13] Virot F. « Contribution à l'étude
expérimentale et numérique du régime
hélicoïdal de détonation dans les systèmes H2, CH4,
C2H6 - O2 dilués ou non par N2 ou Ar. » Thèse de Docteur
Ingénieur, ENSMA, Université de Poitiers (France), 2009.
[14] Woldon Fickett and William C. Davis; « Detonation
Theory and Experiment ». Dover Publication, INC. Mineola, New York,
1997
[15] Fan Zhang; « Shock Wave Science and Technology
Reference Library Volume 6 », Detonation Dynamics, Publisher Springer,
2012.
[16] Edwards T., «Kerosene Fuels for Aerospace
Propulsion-Composition and Properties, 38th AIAA/ASME/SAE/ASEE Joint
Propulsion Conference and Exhibit, 7-10 July 2002, Paper 2002-3874,
Indianapolis, Indiana
[17] P. Dagaut and M. Cathonnet, « The ignition, oxidation
and combustion of kerosene: A review of experimental and kinetic modelling
», Energy and Combustion, 2006, vol. 32.
Annexes
Annexe AI : Etude à l'état
Chapman-Jouguet (CJ)
En différenciant l'équation (1.8) et en sachant
que h0, ??0, ??0 sont des constantes, on obtient :
1
??h1 = ??1????1 + ??1????1 = 2 [????1(??0 + ??1) + ????1(??1 -
??0)] (1.10)
Où ?? représente l'entropie.
Le point Chapman-Jouguet (CJ) correspond à
l'état de mélange réactif où la condition de
tangence entre la droite de Rayleigh-Michelson et l'adiabatique de Crussard est
satisfaite, dans ce cas ????1 = 0.
???? = ??1 - ??0 = ??1 (1.11)
( ????)?? ??0 + ??1
Où ??1 représente la célérité
du son. Avec l'équation (1.10), on en déduit :
2 = ????1
2 +
????1
??2??1
2 > 0 (1.12)
????1
??2??1 ??0 - ??1 ??2??1
2??1
1
2??1
L'équation (1.12) montre dans le plan (??, ??) que le
point CJ correspond à un minimum d'entropie sur la branche des
détonations. Dès lors, la condition de sonicité au point
de tangence CJ est établie comme suit :
|
2??1
|
??2??1
|
??2
1
|
??1 - ??0
|
??12 + ????1
??12 = 0 = ??1 - ??1 (1.13)
|
|
=
??0 - ??1
|
|
|
????1
|
??0 - ??1
|
Page | 79
On a alors ??1 = ??1.
Cas des gaz polytropiques :
Le gaz polytropique est un gaz qui obéit à la loi
des gaz parfaits ???? = ???? et qui vérifie
??
la relation ?????? = ???????? (avec ?? = ???? le rapport
des chaleurs massiques et ?? = où
???? ????
????: masse molaire). De ces expressions, de nombreuses
simplifications apparaissent pour les équations (1.2), (1.3) et (1.4) en
supposant que l'enthalpie vaut h = ?????? = ?????? ??-1 et en tenant
compte de la chaleur libérée par les
réactions chimiques Q reliant h0 et h1. Dès lors, le
système devient :
??1 - ??0
|??0| = ?? - ??0 = ??0v (1.14)
??0 - ??1
|??0| - |??1| = ??1 - ??0 = v(??1 - ??0)(í0 + ??1)
(1.15)
|
??1??1
??1 ??0
??1 - 1
|
??0??0
|
1
?? = 2 (??1 - ??0)(??0 + ??1) (1.16)
|
|
??0 - 1
|
(- ???? = ??1 ??1 = ??1 - ??0
????)(1.17) ??1 ??1 ??0 - ??1
|
Si la détonation est dite forte c'est-à-dire que
??2 » ??02 = ??0
??0
??0
|
, ??0 étant la célérité du
|
son, les valeurs de ??0, ??1 peuvent
différer fortement lorsqu'il y a une forte libération
d'énergie.
Le rapport ??1 peut s'exprimer à l'aide
de l'équation (1.16) :
??0
??0 + 1
= ??0
??0 + 1
??0
1
??1
??0 - 1
??0+ 2????0
??1 ??0 - 1 ??1 ??1
(1.18)
(1.19)
??0[ 2
??1 - 1 ??1 - ??0 2 - 1 ??0 - 2??0??
??02 = (??- ??0)2 =
(??1 - ??0) (??0 + 1
??0 - 1 ??1 + ??0)
Page | 80
Des équations (1.14) et (1.15) en substituant
??1 il vient :
La condition de tangence (1.17) s'écrit comme ceci :
|
??1
|
??12
|
=
|
0
|
(1.20)
(1.21)
(1.22)
(1.23)
|
|
??1 ??0 ??1
??0
=
|
|
??0
??1 1) ??1 1
|
|
(??1 +
??0 -
Ou encore :
(??1 - ??0)
|
|
??0 ??1 =
- ??0
??1 (??1 + 1) - ??0
Dès lors d'après (1.14) on peut écrire :
??0(?? - ??0)2 = ??1 (??1 + 1) - ??0
On injecte ainsi ??1 dans l'expression (1.19)
4 2
??0 (??12 - 1)??
2(??- ??0 [ ??12 - ??0
]
(??-
) )
|
|
- + 2
??0 ??0 (??0 - 1)??0 ??0
|
+ 2
??0
|
La solution de cette équation, dans le cas de
détonation, est fournie par Stanyukovich :
|
|
|
|
|
|
|
?? - ??0 =
??0 v(??1
|
-
|
1
)
|
??
|
??0
+
|
+ ??1
|
|
2
|
|
2
??0
|
(??0
|
|
- 1)??0
+ v(??1 + 1
2 ) ?? 2 + ??0 - ??1 (1.24)
??0 (??0 - 1)??0
Avec la chaleur de réaction Q qui peut s'exprimer comme
ceci :
4
(?? - ??0 + ??12
??02 ??0 2
??0 )
(?? - ??0) ??0
??12 - ??0
(1.25)
(??0 - 1)??0
)
??=
??12 - 1
2
2
Le tableau A.1 reprend les grandeurs caractéristiques
à l'état CJ dans un gaz polytropique avec ?? constant (?? = ??0 =
??1) , et dans le cas d'un choc forts ??2 »
??02 .
Page | 81
Page | 82
|
|
|
Gaz idéal Cp constant
|
|
|
Gaz idéal Cp constant et choc fort ??2 »
??02
|
|
??
|
-
|
??0
=
|
|
|
|
|
|
??
1
v(??2 -
v(??2 - 1
|
1
|
??
|
|
??= v2(??2 - 1)??
??0??2
|
|
??0
|
??1
??0
|
2 ) 2 + +
??0 2
1 ??0
= + 1)
((?? -
??0)2
|
)
|
??0 2
|
|
?? + 1 ??0
??1 ??0 ?? + 1 ??0
= = +
|
??1 =
?? + 1
??1 ?? + 1
=
|
|
??0 ??1 ?? ????1
??1 ??1??1
=
|
??0 ??
T1 ?? ??2
=
|
|
??0 ??0??0
??1 = ??1 = v??????1
??1 + ??1 = ?? - ??0
|
2
??0 ?? + 1 ??0
????
|
|
??1 =
?? + 1
??
|
|
??1 = ??+ 1
|
Tableau A.1 - Caractéristiques de
détonation CJ pour un gaz polytropique à ã constant sous
l'hypothèse d'un choc fort
Page | 83
Annexe AII : Calibrage du système d'atomisation
de gouttelettes
et détermination de la
richesse
a. Introduction
Un étalonnage en masse de l'atomiseur de 5 um doit
être réalisé afin de connaître le débit
liquide injecté dans le tube en fonction du débit d'air
d'entrainement. La technique utilisée consiste simplement à
mettre l'atomiseur sur une balance précise au centième de gramme
près, le mettre en fonctionnement durant un temps de trois minutes et de
relever à chaque intervalle de quinze secondes, la perte de masse. Dans
un premier temps, le calibrage massique est réalisé avec de l'eau
afin de voir le comportement de l'atomiseur et par après avec le
kérosène et dodécane. Ultérieurement, la courbe de
richesse sera établie et le calcul des caractéristiques de
vitesse et temps de balayage seront effectués.
b. Calibrage massique
Dans un premier temps afin de voir le comportement de
l'atomiseur, celui-ci est étalonné avec de l'eau. Les
résultats sont repris à la figure AII.1

dm (g)
14
12
10
8
4
6
2
0
0 20 40 60 80 100 120 140 160 180
t (s)
m_AIR ref = 50 m_AIR ref = 80
m_AIR ref = 120 m_AIR ref = 30
m_AIR ref = 90 m_AIR ref = 110
Linéaire (m_AIR ref = 50) Linéaire (m_AIR ref =
80)
Linéaire (m_AIR ref = 120) Linéaire (m_AIR ref =
30)
Linéaire (m_AIR ref = 90) Linéaire (m_AIR ref =
110)
y = 0,0448x R2 = 0,9993
y = 0,0467x R2 = 0,9976
y = 0,0672x R2 = 0,9985
y = 0,0435x R2 = 0,9905
Perte de masse en fonction du temps
y = 0,0478x R2 = 0,9957
y = 0,0743x R2 = 0,9993
Figure AII.1 - Calibrage en masse de
l'atomiseur avec de l'eau à différents débits d'air de
référence
Après calibrage, la figure AII.1 montre que la perte de
masse reste linéaire et ce, peu importe le débit d'air
d'entrainement de référence. Cet étalonnage permet ainsi
d'établir les différents couples (mAir,mCarburant)
nécessaires au calcul de la richesse (exposé au point c). Une
Page | 84
différence est à noter avec cet atomiseur. En
effet, l'atomiseur utilisé en 2012 par Modou MAR produisait une perte de
masse en liquide constante quel que soit le débit d'air de
référence, ce qui n'est pas le cas de ce dernier.
L'étalonnage est également réalisé avec le
kérosène et le dodécane. Les résultats sont
reportés dans les tableaux AII.1 et AII.2
|
Indication mAIR
120
|
mAIR [m3/h]
5,68
|
mC12H26 [g/h]
30,24
|
mAIR [kg/h]
7,34
|
m C12H26 [kg/h]
0,030
|
|
100
|
4,71
|
9,36
|
6,09
|
0,009
|
|
90
|
4,32
|
11,53
|
5,59
|
0,012
|
|
80
|
3,81
|
14,4
|
4,92
|
0,014
|
|
65
|
3,23
|
16,34
|
4,17
|
0,016
|
|
50
|
2,45
|
20,52
|
3,17
|
0,021
|
|
40
|
1,87
|
28,8
|
2,42
|
0,029
|
|
30
|
1,42
|
25,2
|
1,84
|
0,025
|
|
25
|
1,23
|
31,68
|
1,59
|
0,032
|
|
20
|
0,94
|
36,36
|
1,22
|
0,036
|
|
10
|
0,45
|
56,88
|
0,58
|
0,057
|
Tableau AII.1 - Résultats de
l'étalonnage en masse de l'atomiseur avec du dodécane C12H26
|
Indication mAIR
120
|
mAIR [m3/h]
5,68
|
mJET-A1 [g/h]
68,43
|
mAIR [kg/h]
7,34
|
mJET-A1 [kg/h]
0,068
|
|
110
|
5,26
|
68,14
|
6,80
|
0,068
|
|
100
|
4,71
|
68,04
|
6,09
|
0,068
|
|
90
|
4,32
|
65,62
|
5,59
|
0,066
|
|
80
|
3,81
|
62,28
|
4,92
|
0,062
|
|
65
|
3,23
|
61,63
|
4,18
|
0,062
|
|
50
|
2,45
|
58,32
|
3,17
|
0,058
|
|
40
|
1,87
|
55,44
|
2,42
|
0,055
|
|
30
|
1,42
|
56,52
|
1,84
|
0,057
|
|
25
|
1,23
|
54,72
|
1,59
|
0,055
|
|
20
|
0,94
|
49,94
|
1,22
|
0,050
|
|
10
|
0,45
|
41,04
|
0,58
|
0,041
|
Tableau AII.2 - Résultats de
l'étalonnage en masse de l'atomiseur avec du kérosène
JET-A1
c. Détermination de la richesse
i. Introduction
La richesse se définit comme un rapport de masses.
Celle-ci (notée Ö), s'écrit :
'P = Dosage massique stoe??hiomét??ique
D????
= (5.1)
D????
Dosage massique ??éel
Dans nos expériences, les valeurs de débit d'air
de travail sont connues. A ces débits correspond une valeur de
débit de liquide bien définie, déduite de
l'étalonnage massique du paragraphe b. Enfin, à partir de la
composition chimique du mélange, la richesse sera calculée.
ii. Méthodologie de calcul de la
richesse
? Kérosène
1. Méthode 1
Equation chimique à la stoechiométrie
c'est-à-dire quand la richesse vaut 1 :
|
'P?? ??11H22 +
|
17.5
0.21 (0.21 ??2 + 0.79N2) ? ????2 + H2?? + N2 (5.2)
|
Il est à noter que l'équation n'est pas
pondérée mais nous ne nous intéressons qu'à la
partie des réactifs pour chiffrer la richesse.
Connaissant les débits et les masses molaires des
composants, l'expression du nombre de moles/h de liquide X??????
correspondant au nombre de moles/h d'air X?????? peut être
établi. Par conséquent, la richesse 'P?? peut se
calculer par simple règle de trois par rapport à la
stoechiométrie. La relation suivante est ainsi établie :
X = Masse molai??e du fluide
m
= M Fmole
h ] (5.2)
Débit du fluide
Page | 85
|
X??????
'P?? = X??????
|
17.5
* (5.3)
0.21
|
2. Méthode 2
Pour confirmer les résultats obtenus, le calcul de la
richesse se fera suivant une autre méthode.
Le calcul consistera à procéder par un rapport de
dosage massique. Cela consistera à procéder au rapport du dosage
massique réel ?????? par rapport au dosage massique dans les conditions
stoechiométrique.
L'équation d'équilibre chimique à la
stoechiométrie est la suivante :
|
1 2 H2O + 3,76?? (x +
C??H ?? + ?? (x + y 4) (O2 + 3,76N2) ?
xCO2 + y
C11H22 + ??????(O2 + 3,76N2) ? 12CO2 + 13H2O + ??????
N2
1 y 22
le (x 11
|
y
4) N2
= 16,5
|
(5.4)
(5.5)
(5.6)
|
|
avec + 4) = +
c??efficien?? s????echi??mé????ique ?????? = ?? 4
|
Détermination de la valeur du dosage massique à
la stoechiométrie :
Dans le dosage stoechiométrique, il y a une mole de
carburant de masse égale à 154.29 g. De plus, il y a de l'air
dont la masse vaut 16.5 * 4.76 * 28.96 = 2274.52 g.
Par définition, le dosage massique :
?? = Masse d'ai??????
= = 0.068 (5.7)
2275
.52
Page | 86
Ce dosage massique calculé est celui correspondant
à la stoechiométrie et sera noté ??????. Connaissant
maintenant ?????? procédons au calcul du dosage réel ?????? avec
les valeurs obtenues par étalonnage pour ainsi chiffrer la richesse
selon le rapport de dosage massique :
ö JET-A1= ?????? (5.8)
??????
Page | 87
Comparatif des résultats obtenus par les 2
méthodes :
|
(mJET-A1;mAIR) [kg/h]
(0,068 ; 7,34)
|
ö JET-A1 Méthode 1
0,15
|
ö JET-A1 Méthode 2
0,14
|
|
(0,068 ;
|
6,80)
|
0,16
|
0,15
|
|
(0,068 ;
|
6,09)
|
0,17
|
0,16
|
|
(0,066 ;
|
5,59)
|
0,18
|
0,17
|
|
(0,062 ;
|
4,92)
|
0,20
|
0,19
|
|
(0,062 ;
|
4,18)
|
0,23
|
0,22
|
|
(0,058 ;
|
3,17)
|
0,29
|
0,27
|
|
(0,055 ;
|
2,42)
|
0,36
|
0,34
|
|
(0,057 ;
|
1,84)
|
0,48
|
0,45
|
|
(0,068 ;
|
1,84)
|
0,58
|
0,54
|
|
(0,055 ;
|
1,59)
|
0,54
|
0,51
|
|
(0,050 ;
|
1,22)
|
0,64
|
0,61
|
|
(0,041 ;
|
0,58)
|
1,10
|
1,04
|
Tableau AII.3 - Valeurs de richesse du
kérosène JET-A1 obtenues pour différents couples de
travail (mJET-A1;mAIR)
Les valeurs de richesse obtenues suivant les 2 méthodes
sont relativement proches. Les débits de liquide obtenus avec la
technologie du brumisateur de gouttelettes de 5 um sont relativement petits.
La plus grande valeur de richesse obtenue est de l'ordre de
1,1 et celle-ci s'obtient avec un débit d'air de l'ordre de 0.58 kg/h.
Lorsque le débit d'air est très important, nous sommes en
excès d'air d'où les valeurs plus petites de richesse et donc
moins de chance d'obtenir une détonation. L'évolution de la
richesse est reportée graphiquement à la figure AII.2.

Débit d'air [m3/h]
4,00
6,00
3,00
2,00
0,00
5,00
1,00
0,00 0,20 0,40 0,60 0,80 1,00 1,20
Richesse
Evolution de la richesse en fonction du débit
d'air
y = 0,576x-1,192
Figure AII.2 - Evolution de la richesse du
kérosène JET-A1 avec le débit d'air pour l'atomiseur de
gouttelettes de 5 um et
courbe de tendance de type puissance
La plage de richesse étant définie, afin de tenter
d'initier une détonation, les richesses de travail seront fixées
entre 1 et 1,2 et les résultats exposés au chapitre 6.
? Dodécane
La même démarche est tenue ici avec le
dodécane. Un comparatif sera ensuite réalisé avec les
résultats antérieurs obtenus par Modou MAR (2012) qui a
travaillé avec atomiseur générant des tailles de
gouttelettes de l'ordre de 8 um.
Calcul de la richesse
1. Méthode 1
Equation chimique à la stoechiométrie
c'est-à-dire quand la richesse vaut 1 :
|
???? C12H26 +
|
17.5
0.21 (0.21 ??2 + 0.79N2) ? C??2 + H2?? + N2 (5.9)
|
X = Masse molaire du fluide
m M Fmole
h ] (5.10)
Débit du fluide
Page | 88
|
????????
???? = ????????
|
17.5
* (5.11)
0.21
|
2. Méthode 2
L'équation d'équilibre chimique à la
stoechiométrie est la suivante :
C??H ?? + ??(x + y 4)(??2 + 3,76N2) ? xC??2
+ y 2 H2?? + 3,76??(x + y 4) N2 (5.12)
C12H26 + ??????(??2 + 3,76N2) ? 12C??2 + 13H2?? +
?????? N2 (5.13)
avec le c??efficien?? s????echi??mé????ique ?????? = ?? (x
+ y 4) = 12 + 26 4 = 18,5 (5.14)
Détermination de la valeur du dosage massique à
la stoechiométrie :
Dans le dosage stoechiométrique, il y a une mole de
carburant de masse égale à 170.33 g. De plus, il y a de l'air
dont la masse vaut 18.5 * 4.76 * 28.96 = 2550.52 g.
Par définition, le dosage massique :
?? = Masse d'ai??????
= = 0.067 (5.15)
2550
.52
Page | 89
Ce dosage massique calculé est celui correspondant
à la stoechiométrie et sera noté ??????. Connaissant
maintenant ?????? procédons au calcul du dosage réel ?????? avec
les valeurs obtenues par étalonnage pour ainsi chiffrer la richesse
selon le rapport de dosage massique :
??C12H26 = ?????? (5.16)
??????
Page | 90
Comparatif des résultats obtenus par les 2
méthodes :
|
(mC12H26;mAIR) [kg/h]
(0,068 ; 7,34)
|
ö C12H26 Méthode 1
0,06
|
ö C12H26 Méthode 2
0,06
|
|
(0,068 ;
|
6,80)
|
0,02
|
0,02
|
|
(0,068 ;
|
6,09)
|
0,03
|
0,03
|
|
(0,066 ;
|
5,59)
|
0,04
|
0,04
|
|
(0,062 ;
|
4,92)
|
0,06
|
0,06
|
|
(0,062 ;
|
4,18)
|
0,09
|
0,10
|
|
(0,058 ;
|
3,17)
|
0,17
|
0,18
|
|
(0,055 ;
|
2,42)
|
0,19
|
0,21
|
|
(0,057 ;
|
1,84)
|
0,24
|
0,25
|
|
(0,068 ;
|
1,84)
|
0,28
|
0,30
|
|
(0,055 ;
|
1,59)
|
0,42
|
0,45
|
|
(0,050 ;
|
1,22)
|
1,39
|
1,46
|
Tableau AII.4 - Récapitulatif des
valeurs de richesse du dodécane C12H26 obtenues
Les deux méthodes de calcul donnent quasiment les
mêmes valeurs de richesse. La valeur de richesse ö la plus
élevée, avoisine les 1,4 ~ 1,5 et s'obtient pour une valeur de
débit d'air de l'ordre de 1,22 kg/h. Sous forme graphique,
l'évolution de la richesse est indiquée sur la figure AII.3.

Débit d'air [m3/h]
4,00
6,00
3,00
2,00
0,00
5,00
1,00
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60
Richesse
Evolution de la richesse en fonction du débit
d'air
y = 0,5853x-0,603
Figure AII.3 - Evolution de la richesse du
dodécane avec le débit d'air pour l'atomiseur de gouttelettes de
5 um et courbe de
tendance de type puissance
? Comparaison avec les résultats
antérieurs
Les conditions des expérimentés de Modou MAR
avec le dodécane sont identiques aux nôtres mais l'atomiseur
utilisé est différent. En effet, celui-ci permet de
générer des tailles de gouttelettes de l'ordre de 8 um. Modou MAR
[2012] a travaillé dans une plage de débits d'air comprise entre
2 et 5 m3/h. Dans son cas, le débit de liquide est constant
quel que soit la valeur de débit d'air, sa valeur est de 0,21 l/h.
La richesse correspondante est calculée sur le tableau
AII.5 et la comparaison avec nos résultats sur la figure AII.4:
|
m C12H26 [kg/h]
|
m AIR [kg/h]
|
X C12H26 [mole/h]
|
X AIR [mole/h]
|
ö C12H26
|
|
0,158
|
5,69
|
0,925
|
196,450
|
0,39
|
|
0,158
|
4,53
|
0,925
|
156,267
|
0,49
|
|
0,158
|
3,36
|
0,925
|
116,084
|
0,66
|
|
0,158
|
2,72
|
0,925
|
93,760
|
0,82
|
Tableau AII.5 - Valeurs de richesse du
dodécane obtenues dans les travaux antérieurs
réalisés par Modou MAR (2012)

Débit d'air [m3/h]
4,00
6,00
3,00
2,00
0,00
5,00
1,00
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60
Richesse
Evolution de la richesse en fonction du débit
d'air
Atomiseur 5um Atomiseur 8um
Puissance (Atomiseur 5um) Puissance (Atomiseur 8um)
y = 1,7258x-1
y = 0,5853x-0,603
Figure AII.4 - Comparaison des plages de
richesse entre les atomiseurs générant des tailles de
gouttelettes de 5 um et 8um (courbe de tendance de type puissance)
Page | 91
Le fait d'avoir changé de brumisateur modifie
considérablement les résultats. La plage de richesse est
complétement différente et cela peut se justifier par une
différence de fonctionnement technologique du brumisateur.
La plage de richesse avec l'atomiseur de 5 um est beaucoup
plus petite que celle obtenue avec l'atomiseur de gouttelettes de 8 um pour une
même plage de débit d'air de travail. Cela peut s'expliquer par le
fait que pour un même débit d'air, le brumisateur
générant des plus petites tailles de gouttelettes travaille avec
un débit de liquide très petit par rapport à l'autre. Pour
un même débit d'air, la proportion de liquide est
différente d'un facteur 10, d'où des plages de richesses
différentes. Vu les proportions de liquides mise en jeu, il sera
nécessaire de travailler à bas débit d'air pour le
brumisateur de 5 um afin d'avoir une valeur importante de richesse et optimiser
ainsi la probabilité de détonation.
d. Vitesse et temps de balayage dans le tube
Il est important de pouvoir chiffrer le temps
nécessaire au balayage des gouttelettes dans le tube, ainsi que la
vitesse d'entrainement de celles-ci afin de savoir si elle sera suffisante pour
vaincre la force due à la pesanteur, et ainsi atteindre le haut du tube.
Le tube à détonation est un tube de section carrée de
53*53 mm et de longueur de 4,036 m. Chiffrons le temps de balayage au sein du
tube.

L = 4,036 m
Q AIR
La relation reliant le débit à la section est la
suivante :
M
3600
= V * S (5.17)
avec
m3
* m : débit volumique du fluide
|
h
|
|
*
m
V : vitesse d'entrainement des gouttelettes
s
* S : section d'étude m2
La vitesse est considérée comme constante.
Dès lors, son expression peut s'écrire :
L dt
?x
V = ?t
m
-, 3600
at * S -, dt = L * S * 3600 (5.18)
m
Page | 92
Temps de balayage 2 ou 3 * dt (5.19)
Page | 93
Les valeurs de temps de balayage en fonction du débit
d'air sont reprises dans le tableau AII.6.
|
???? AIR [m3/h]
|
Ventrainement [m/s]
|
?t [s]
|
tbalayage [s]
|
|
1,42
|
0,14
|
28,74
|
57,48
|
|
1,23
|
0,12
|
33,18
|
66,36
|
|
0,94
|
0,09
|
43,42
|
86,84
|
|
0,45
|
0,04
|
90,70
|
181,4
|
Tableau AII.6 - Temps de montée des
gouttelettes au sein du tube à détonation
Fixer un temps de balayage entre 3 et 4 min sera donc suffisant
pour assurer le balayage au sein du tube. Il reste maintenant à
vérifier si nos vitesses d'entrainements sont suffisantes pour que les
gouttelettes montent jusqu'en haut du tube.
Pour cela, il faut calculer la vitesse de chute d'une particule
dans l'air. Pour les gouttelettes de petites tailles, le modèle de
Stokes est envisageable.
La vitesse de chute diminue, le nombre de Reynolds devient faible
devant l'unité et le mécanisme de frottement dominant n'est pas
l'inertie. La force de friction est alors donnée par la formule suivante
:
??
??= ??0 2 ?? (5.20)
Où ??0 désigne la viscosité dynamique de
l'air, ?? le diamètre de la gouttelette et ?? la vitesse de chute de la
goutte.
Le poids d'une goutte sphérique de diamètre ??
s'écrit :
3
4
?? = 3 ?? (?? 2) ???? (5.21)
Où ?? est la masse volumique du liquide
considéré et ?? est l'accélération de la pesanteur.
L'équilibre de ces forces permet d'obtenir l'expression de la vitesse de
chute :
2
4 3 ?? (?? 2) ????
?? = (5.22)
??0
Les tests granulométriques par méthode PDI ont
fait ressortir des tailles de gouttelettes de l'ordre de 4 à 6 um. En
moyenne, le diamètre avoisine les 5 um, dès lors la vitesse de
chute dans l'air sera égale à :
Page | 94
Vchute kérosène =
|
2
4 3 T1 * (5 * 10-6
2 ) * 782,5 * 9,81
|
cm
= 1,17
s
|
|
1,71 * 10-5
|
|
Vchute dodécane =
|
2
4 3 T1 * (5 * 10-6
2 ) * 750 * 9,81
|
cm
= 1,13
s
|
|
1,71 * 10-5
|
Le modèle de Stokes n'est applicable que pour les tailles
de gouttelettes très petites et si le nombre de Reynolds est
inférieur à l'unité. Vérifions cette
dernière condition (tableau 5.9)
V * d
Re = ?0 (5.23)
|
???? AIR [m3/h]
5,68
|
VENTRAINEMENT [m/s]
0,56
|
Re
0,16
|
|
4,71
|
0,47
|
0,14
|
|
4,32
|
0,43
|
0,12
|
|
3,81
|
0,38
|
0,11
|
|
3,23
|
0,32
|
0,09
|
|
2,45
|
0,24
|
0,07
|
|
1,87
|
0,18
|
0,05
|
|
1,42
|
0,14
|
0,04
|
|
1,42
|
0,14
|
0,04
|
|
1,23
|
0,12
|
0,04
|
|
0,94
|
0,09
|
0,03
|
|
0,45
|
0,04
|
0,01
|
Tableau AII.7 - Nombre de Reynolds Re en
fonction du débit d'air de travail
Ce modèle considère également que les
gouttelettes sont parfaitement sphériques, c'est-à-dire la
situation où les forces capillaires dominent la friction de l'air, qui
serait susceptible de déformer les gouttes. La force capillaire typique
est proportionnelle à la taille de la gouttelette R et à la
tension superficielle y qui est une force par unité de longueur. On peut
se la représenter comme la force de tension de surface appliquée
par une moitié de la goutte sur l'autre moitié. Pour qu'une
goutte soit considéré comme sphérique, il faut donc que la
condition suivante soit vérifiée :
Ffriction air < Fcapillaire (5.24)
ñaV2R2 < yR (5.25)
Page | 95
En remplaçant Vpar l'expression obtenue en (5.21), le
critère devient :
2
5 ã?0
R < v = ? (5.26)
16 9 ð2ñañ2g2
En résumé, la gouttelette sera sphérique
si son rayon ne dépasse pas la longueur capillaire ? du liquide
utilisée. Vérifions cette dernière condition sachant que
:
- la tension superficielle du kérosène ã est
comprise entre 0.023 et 0.032 N/m
- la viscosité de l'air ?0 vaut 1,71 * 10-5
Pa.s
- la densité de l'air ñ?? vaut 1,292
kg/m3
- la densité du kérosène ñ vaut 782,5
kg/m3
- la force de pesanteur g vaut 9,81 m/s2
En remplaçant les données dans l'équation
(5.26), la longueur capillaire ? = 8,717*10-5 m. Soit 87,17 um, le
rayon de nos gouttelettes R valant 2,5 um, la condition de
sphéricité est vérifiée.
Notons également que le modèle de Stokes reste
en adéquation avec le test de mesure de granulométrie par PDI
(cf. Chapitre 4). En effet, durant cette phase expérimentale,
des mesures de vitesse de gouttelettes sont relevés et la montée
des gouttelettes au sein du tube a été observée durant la
phase de calibrage du système avec le tube en plexiglas.
e. Conclusion
Pour conclure ce chapitre, concernant l'atomiseur
utilisé, changer le débitmètre utilisé afin de
minimiser l'erreur sur la richesse. En effet, un constructeur garantit en
général sur l'instrumentation, une imprécision minime
entre 5 et 95% de l'échelle de mesure, alors que notre plage de travail
se situe entre 0 et 5% de l'échelle où la précision qui
règne sur cette gamme est inconnue.
Annexe AIII: Specification Jet-A1 de l'American Society
for Testing and Materials
(ASTM)

Tableau AIII.1 - Specifications ASTM du
kérosène Jet-A1
Page | 96
Page | 97
Annexe AIV : Calcul des caractéristiques de la
bouteille de mélange O2 + 2 N2 par
la méthode des pressions partielles via
EES.
// Equation à la stoechiométrie avec l'air
+ caractéristiques -> C11H22 + z (O2 + 3,76 N2) // //
Caractéristiques connus par calibrage cf. Chapitre 5 //
r = 1,5 /* Richesse */
z_st = 16,5 /* Dosage massique stoechiométrique */
z= z_st/r /* Dosage massique réel */
nb_moles_O_2 = z /* Nombre de moles O2*/
nb_moles_N_2 = z/r * 3,76 /* Nombre de moles N2*/
Q_air = 0,3 /* Débit massique d'air [kg/h] */
Q_c = 0,031 /* Débit massique de carburant [kg/h] */
// Conversion en indication débitmètre de
travail // ind_Q_air = (20,919*Q_air / 1,293) + 0,134
// Pour ces mêmes caractéristiques de
travail, si proportion du mélange change, et qu'on utilise de l'air
suroxygéné -> C11H22 + â (O2 + 2 N2) //
// Calcul rapport de débit et de la nouvelle
richesse et pression partielle //
beta = Q_air/ Q_c /* Dosage massique réel */
r_newmélange = z_st/beta*(3/4,76) /* Calcul de la nouvelle
richesse */
nb_moles_O_2_new = beta /* Nombre de mole de O2 */
nb_moles_N_2_new = beta/r_newmélange*2 /* Nombre de moles
de N2*/
// Calcul de la fraction massique de O2 et de N2
//
x_O_2 = nb_moles_O_2_new/( nb_moles_O_2_new+nb_moles_N_2_new)
x_N_2=1-x_O_2
// Temps de balayage en secondes et volume en litres //
// Dimension tube //
L = 4,036 /* Longueur tube en mètre */
S = 0,053 * 0,053 /* Section tube en mètre carré
*/
t_balayage =( (L/Q_air/1,293)*S*3600*2) /* Calcul du temps de
balayage en
secondes */
Volume_3manip = t_balayage * 3 * (Q_air/1,293)/3600*1000 /*
Calcul du volume nécessaire pour un
total de 3 manipulations */
Volume_manip = Volume_3manip / 3 /* Volume pour une manipulation
*/
p_bouteille = 12 /* On fixe une pression de 12 bars dans
la bouteille */
V_bouteille = 43 /* Capacité de la bouteille 43
litres*/
p_O_2 = x_O_2 * p_bouteille /* Pression partielle en O2 */
P_N_2 = x_N_2 * p_bouteille /* Pression partielle en N2 */
| 


