|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page i
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
SOMMAIRE
DEDICACE iv
REMERCIEMENTS v
LISTE DES ABREVIATIONS ET SYMBOLES vi
LISTE DES FIGURES vii
LISTE DES SCHEMAS viii
LISTE DES TABLEAUX ix
RESUME x
ABSTRACT xi
INTRODUCTION GENERALE 1
CHAPITRE I :PARTIE THEORIQUE 3
I. Etude botanique 4
I.1 Place de Mostuea batesii dans la systématique
moderne 4
I.2 Les Loganiaceae 5
I.3 Généralité sur le genre Mostuea
6
I.3.1 Bref historique 6
I.3.2 Description botanique 6
I.4 Généralités sur l'espèce
Mostuea batesii 7
I.4.1 Description botanique 7
I.4.2 Distribution de Mostuea batesii 8
I.4.3 Usages de Mostuea batesii en médecine
traditionnelle 9
II. Travaux antérieurs sur le genre
Mostuea 9
II.1 Les alcaloïdes 10
II.1.1 Généralités 10
II.1.1.1 Définition 10
II.1.1.2 Nomenclature 11
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page ii
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
II.1.2 Classification et structure des alcaloïdes 11
II.1.2.1. Classification des alcaloïdes suivant leurs
structures 11
II.1.2.1.1 Alcaloïdes avec azote(s) exocyclique(s)et
amine(s) aliphatique(s) 12
II.1.2.1.2 Alcaloïdes de la putrescine, de la spermidine et
de la spermine. 14
II.1.2.1.3 Alcaloïdes peptidiques. 14
II.1.2.1.4 Alcaloïdes terpéniques et
stéroïdaux. 14
II.1.2.1.5 Alcaloïdes hétérocycliques ou
alcaloïdes vrais. 16
II.1.3 Classification des alcaloïdes suivant leur
biogenèse 19
II.1.4 Caractérisation des alcaloïdes 20
II.1.5 Propriétés physicochimiques des
alcaloïdes 20
II.1.5.1 Caractère physique 20
II.1.5.2 Caractère chimique 20
II.1.6 Biosynthèse 21
II.1.6.1 Précurseur des alcaloïdes 21
II.1.6.2 Principe et biosynthèse des alcaloïdes
quinoléiques 23
II.2 Quelques alcaloïdes isolés du genre
Mostuea 25
II.3 Importance des alcaloïdes 26
CHAPITRE II :RESULTATS ET DISCUSSION 28
I. EXTRACTION ET ISOLEMENT DES COMPOSES 29
I.1 Elucidation des structures des composés isolés
31
I.1.1 Elucidation de la structure de GB1 31
I.1.2 Elucidation de la structure GB5 ; 40
CONCLUSION GENERALE 47
CHAPITRE III :PARTIE EXPERIMENTALE 49
I. Généralités 50
I.1 Appareillage 50
I.2 Matériel végétal 50
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page iii
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I.3 Extraction, isolement et caractérisation des
composés GB 51
I.3.1 Extraction 51
I.3.2 Séparation chromatographique 51
I.4 Caratéristiquesphysico-chimiques des composés
isolés 55
II TESTS CARACTERISTIQUES DES COMPOSES ISOLES
56
II.1 Test de Dragendorf 56
II.2 Test de Molish 57
Références bibliographiques 58
Lexique 60
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

DEDICACES
Je dédie ce mémoire
A
PapaNkuinkeu Robert
et
Maman Nkuinkeu Clarice.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page iv
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page v
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
REMERCIEMENTS
Mes remerciements vont :
Au Professeur Nkengfack A . E., Chef de Département de
Chimie Organique, qui a bien voulu m'accepter dans son équipe de
recherche.
Au Dr Mkounga P. chargé de cours, pour m'avoir
proposé ce sujet, pour sa disponibilité, ses conseils, et pour
avoir dirigé ce travail avec rigueur jusqu'au bout. Je tiens à
lui exprimer toute ma gratitude et ma profonde admiration.
A tous les enseignants du Département de Chimie
Organique pour leurs déterminations à donner à tous les
étudiants du Département une formation de qualité.
Au Dr Ouahouo B. pour son soutien moral.
Au Dr Tsamo A. pour l'enregistrement des spectres ;
A tous mes ainés de Laboratoire, plus
particulièrement à Gompe G., Mfifen A., Nangmo P. et Maza H.,
pour leurs encouragements, leurs conseils et l'intérêt qu'ils ont
porté à ce travail.
A mes camarades de Laboratoire : Pagna J., Fenkam S., Anamo G.
et Ngueguim S. avec qui j'ai passé des moments formidables lors de la
préparation du mémoire ;
A mes camarades de promotion notamment Wouamba S., Yanmo
H.,pour l'accueil fraternel qu'ils ont fait à mon égard.
A maman Nkwaten E. pour tout son soutien moral, financier et
affectif.
A ma soeur et monfrère: Nkuinkeu S. et Tchawa A. pour
leurs encouragements.
A tous ceux qui, de près ou de loin, ont contribué
à la réalisation de ce travail.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page vi
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
LISTE DES ABREVIATIONS, SYMBOLES ET
CONVENTIONS
°C Degré Celsius
CC Chromatographie sur colonne
CCM Chromatographie sur couche mince
d Doublet
DEPT Distortionless enhancement by polarisation transfer
DMSO DimethylSulfoxyde
ESI Electron spray ionization
g Gramme
Hex Hexane
HMBC Heteronuclear Multiple Bond Coherence
HNC Herbier National Du Cameroun
HSQC Heteronuclear Single Quantum Correlation
J Constante de couplage
MHz Mégahertz
mL Millilitre
mm: Millimètre
nm Nanomètre
PF Point de fusion
ppm: Partie par million
q Quartet
RMN C Résonance magnétique nucléaire du
carbone
RMN H Résonance magnétique nucléaire du
proton
s Singulet
SM Spectrometrie de masse
TMS TétraMéthylSilane
UV UltraViolet
ä Echelle de déplacement chimique
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page vii
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
LISTE DES FIGURES
Figure 1: Carte de localisation des Loganiaceae 6
Figure 2: Mostuea batesii (HNC) 8
Figure 3 : Carte de localisation de Mostuea batesii
en Afrique 8
Figure 4 : Spectre de masse ESI du composé GB1 31
Figure 5 : DEPT 90 (5a), Spectre carbone large bande (5c),
DEPT 135(5b) de GB1 33
Figure 6: Spectre RMN 1Hdu composé GB1 35
Figure 7 : Spectre HSQC du composé GB1 36
Figure 8: Spectre HSQC élargi du composé GB1
36
Figure 9 : Spectre HSQC du composé GB1 37
Figure 10: Spectre HSQC du composé GB1 37
Figure 11: Spectre de masse ESI du composé GB5 40
Figure 12: Spectre carbone large bande du composé GB5
(DMSO-d6, 125 MHz) 41
Figure 13: Spectre DEPT du composé GB5 41
Figure 14:Spectre HSQC du composé GB5 élargit
42
Figure 15: Spectre HSQC du composé GB5 42
Figure 16: Corrélations HSQC du composé GB5
43
Figure 17: Spectre RMN1H (DMSO-d6, 500
MHz) 44
Figure 18: Spectre COSY du composé GB5 45
Figure 19: Spectre COSY élargi de ä 3 à 4
du composé GB5 46
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page viii
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
LISTE DES SCHEMAS :
Schéma 1: Classification systématique de
Mostuea batesii Baker dans le règne végétal 4
Schéma 2 : Mécanisme général de la
biosynthèse des alcaloïdes 23
Schéma3: Biosynthèse des alcaloïdes
quinoléique 24
Schéma4: Protocole d'extraction et d'isolement des
composés GB à partir des racines de
Mostuea batesii 30
Schéma 5 : Squelette de la camptothecine 32
Schéma 6 : Squelette de la camptothecine 34
Schéma 7: Corrélations H-H sur la camptothecine
38
Schéma 8 : Structure du sucrose 47
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page ix
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
LISTE DES TABLEAUX
Tableau 1 : Répartitions de Mostuea batesii au
Cameroun 9
Tableau 2:Quelques Alcaloïdes avec azote(s)
exocyclique(s) et amine(s) aliphatique(s) 13
Tableau 3 : Alcaloïdes terpéniques et
stéroïdaux 15
Tableau 4: Alcaloïdes hétérocycliques ou
alcaloïdes vrais. 16
Tableau 5: Quelques alcaloïdes isolés du genre
Mostuea 25
Tableau 6 : Données spectrales de RMN 1H
(DMSO-d6 ; 500MHz)et de RMN 13C (DMSO-
d6 ; 125MHz) du composé GB1 39
Tableau 7 : Données spectrales de RMN 1H (DMSO-d6 ;
500MHz)et de RMN 13C (DMSO-
d6 ; 125MHz) du composé GB5 47
Tableau 8: Chromatogramme de l'extrait brut 53
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page x
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
RESUME
Le présent travail porte sur l'isolement, la
purification et la caractérisation des métabolites secondaires
des racines de Mostuea batesii, plante médicinale camerounaise
de la famille des Loganiaceae.
L'extrait au méthanol, des racines de cette plante a
conduit au moyen des méthodes chromatographiques usuelles (CC et CCM),
cinq composés indexés de GB1 à GB5. Parmi ces cinq
composés deux ont été entièrement
caractérisés. Il s'agit :
-
D'un alcaloïde quinoléique, la camptothecine
(GB1).
- D'un sucre, le saccharose communément appelé
sucrose (GB5)
Les structures de ces composés ont été
élucidées à l'aide des méthodes spectroscopiques
usuelles ( RMN à une et deux dimensions, spectrometrie de masse) et par
comparaison de leurs données spectroscopiques avec celles de la
littérature.
Mots-clés : Loganiaceae; Mostuea
batesii; camptothecine; sucrose.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page xi
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
ABSTRACT
In this work, we report on the isolation, purification and
characterization of secondary metabolites from the methanol extract of the root
of Mostuea batesii, a Cameroonian medicinal plant belonging to the
Loganiaceae family.
Chromatographic separation of the methanol extract using usual
chromatographics methods (CC and Thin Layer Chromatographic) led to the
isolation of five compounds labeled GB1 to GB5. Among these five compounds two
were entirely characterized, these include:
- A quinoleic alkaloid known as camptothecin (GB1)
- A saccharose commonly named sucrose (GB5)
The structures of these compounds were elucidated using
spectroscopic techniques (one and two dimension NMR, mass spectrometry) and by
comparison of their spectroscopic data with those of the literature.
Keywords: Loganiaceae; Mostuea
batesii; camptothecin; sucrose.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 1
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
INTRODUCTION GENERALE
Au cours des dernières décennies, les recherches
scientifiques les plus modernes n'ont fait que confirmer le bien fondé
des vertus thérapeutiques des plantes utilisées de façon
empirique depuis les millénaires par l'homme pour éliminer le
déséquilibre physique ou mental. Ce savoir ancestral, transmis de
générations en générations est de nos jours, devenu
une mine précieuse d'informations pour les chercheurs.
Malgré les progrès de la médecine moderne
basés sur les médicaments de synthèse, la majeure partie
de la population des pays en voie de développement a recours aux
ressources végétales pour des soins de santé primaire
(OMS, 2010). De plus le continent africain regorge des plantes
médicinales très diversifiées (Mangambu.,2013).
Selon l'Organisation Mondiale de la Santé, plus de 80% des populations
africaines ont recours à la médecine traditionnelle pour faire
face aux problèmes de santé (OMS, 2010).
Mais, pour que les plantes puissent être
utilisées de manière efficace et sans aucun danger pour les
populations, une meilleure connaissance de la composition chimique de leurs
extraits ainsi qu'une bonne évaluation de leur toxicité
s'imposent (Hostettman, 1997). D'où l'intérêt de
l'étude des substances naturelles.
Cette étude passe par l'inventaire des plantes
médicinales, leur identification, leur récolte suivie de la
préparation des différents extraits, l'évaluation de leur
activité biologique, l'isolement et la caractérisation des
métabolites secondaires contenus dans ceux-ci, suivis de
l'évaluation biologique des composés purs isolés.
C'est fort de cette importance que le Département de
Chimie Organique s'est orienté dans la recherche des nouveaux agents
chimiothérapeutiques issus des plantes.
C'est donc dans ce cadre qu'il m'a été
confié, l'étude phytochimique de l'extrait méthanolique
des racines de Mostuea batesii, plante de la famille des Loganiaceae.
Le choix de cette plante a été motivé, non seulement par
le fait qu'elle soit utilisée en général en
médécine traditionnelle comme aphrodisiaque et
hallucinogène, mais aussi que l'espèce Mostuea batesii
en particulier n'a pas fait l'objet d'études phytochimiques
poussées à notre connaissance.
Les objectifs spécifiques de notre travail se
présentent comme suit :
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 2
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
> L'identification et la récolte de la plante
Mostuea batesii ;
> L'isolement et purification des composés contenus
dans l'extrait des racines de la plante Mostuea batesii ;
> Détermination de la structure des composés
isolés. Le plan de la rédaction s'articulera autour de trois
chapitres:
> Une revue de la littérature faisant la
synthèse des travaux réalisés antérieurement ;
> Les résultats et discussion présentant les
résultats phytochimiques obtenus au cours de notre étude qui
s'achèveront par une conclusion générale ;
> La partie expérimentale fera ressortir les
matériels et méthodes ;
> Le mémoire s'achèvera par une liste des
références bibliographiques.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 3
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
CHAPITRE I :
PARTIE THEORIQUE
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I. Aperçu botanique
I.1 Place de Mostuea batesii dans la systématique
moderne
Mostuea batesii appartient à la famille des
Loganiaceae. Les Loganiaceae forment avec les Gentaniaceae, les Theligenaceae,
les Dialipetalaceae, les Gelsemiaceae, les Rubiaceae et les Apocynaceae l'ordre
des Gentianales (Edwin, 2012). Les Gentianales appartiennent à la classe
des Magnioliopsida, sous-classe Asteridae, division Magnoliophyta et sous
règne des Tracheobionta (Watson et Dallwitz, 1992).
Classification systématique
Règne : Plantae

MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 4
Sous règne: Tracheobionta
|
|
Division : Magnoliophyta
|
|
Classe : Magnoliopsida
|
|
Sous-classes : Asteridae
|
|
Ordre : Gentianales
|
|
Famille : Loganiaceae
|
|
Genre : Mostuea
|
|
Espèce : Mostuea batesii
Baker
|
Tableau 1: Classification
systématique deMostuea batesiiBaker dans le règne
végétal
(Watson et Dallwitz, 1992)
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 5
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I.2 Aperçu botnique sur les Loganiaceae
Les Loganiaceae sont des arbres, des arbustes ou des lianes
aux feuilles presque opposées, parfois simples. Les stipules peuvent
être présentes ou absentes, les inflorescences sont
paniculées, corymbeuses ou parfois capituliformes. Les fleurs sont
bisexuées et généralement actinomorphes, subactinomorphes
(c'est le cas du genre Mostuea) ou zygomorphes (cas de
Usteria). Les sépales valvaires ou imbriqués
possèdent une corolle tubuleuse avec 4 à 16 lobes qui sont
confortés, imbriqués ou valvaires. Les étamines
insérées sur la corolle sont au même nombre que les lobes
de la corolle et alternent avec eux. Celles-ci sont exceptionnellement une
seule (cas du genre Usteria) et présente des anthères
à deux loges s'ouvrant par une fente longitudinale. L'ovaire
supère, a 1 à 4 loges avec un style simple. Les ovules sont en
petit nombre ou nombreuses, rarement une seule, elles sont axiles ou presque
basilaires. Les fruits sont des capsules, des baies ou des drupes. Les graines
parfois ailées présentent un embryon droit, situé au
milieu d'un endosperme charnu ou cartilagineux (Aubreville et Jean, 1972).
La famille des Loganiaceae contient 30 genres et plus de 600
espèces (Edwin, 2012). On retrouve environ 29 genres et 500
espèces dans les zones tropicales et subtropicales. En revanche, elles
sont absentes en Europe (Li-Ping-tao, 1996). La délimitation de la
famille des Loganiaceae a été à l'origine de plusieurs
questions et débats, c'est pour cette raison que le nombre
d'espèces peut varier d'un auteur à un autre (Olusola, 2011).
Ceci étant dû au fait qu'il apparaît certaines similitudes
entre les genres du même ordre. C'est le cas de Mostuea de la
famille des Loganiaceae et Gelsemium de la famille des Gelseminaceae
qui semblent assez similaire (Leeuwenberg,1961).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 6
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
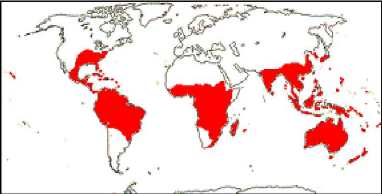
Répartition globale des Loganiaceae
Figure 1: Carte de localisation
des Loganiaceae (Heywood, 1985)°
I.3 Généralité sur le genre
Mostuea I.3.1 Bref historique
La caractérisation et l'identification du genre
Mostuea ont connu une évolution progressive. En effet, la
première identification date de 1854 par Didrichsen. Quelques
années plus tard, de nombreux chercheurs à l'instar de Oliver,
Baker, Baillon et Hooker identifient les synonymes de Mostuea, en
occurence les genres Leptocladus et Coinochalmys
respectivement. Mais ce sont les travaux de Baillon et Baker en 1903 qui
ont permis d'uniformiser cette description (Leeuwenberg, 1961).
I.3.2 Description botanique
Les Mostuea sont des arbres ou des arbustes, parfois
des lianes généralement bien ramifiées ; les stipules sont
membraneuses et soudées (Leeuwenberg, 1961).
Les feuilles sont opposées et courtement
pétiolées ; le limbe est ordinairement papyracé à
l'état sec, de forme et de grandeur variable ; ové et
étroitement elliptique, il est entier ou faiblement
sinué-denté (Leeuwenberg, 1961).
Les inflorescences sont axillaires ou terminales,
généralement obliques et incomplètement dichasiales, uni
ou multiforme, parfois capituliformes (Leeuwenberg, 1961).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 7
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Les fleurs sont pentamères. Les sépales sont
ovés, linéaires et soudés à la base. La corolle est
en entonnoir. Les lobes sont imbriqués dans le bouton, et sont presque
égaux, étalés, orbiculaires ou suborbiculaires. Les
étamines sont inclues ou souvent exsertes, notamment dans le cas des
étamines longues. Les filets sont pubescents ou parfois glabres. Ils
sont insérés au quart ou au tiers du tube inférieur de la
corolle, sont également allongés et sont plus ou moins
inégaux. Les anthères sont orbiculaires ou oblongues ; les loges
sont séparées. Les ovaires sont ovoïdes, à deux loges
; le style est caduc, finement pubescent avec poils glandulifères ; Le
stigmate est deux fois bifurqué à lobes étroits ; et les
ovules sont deux par loges (Leeuwenberg, 1961).
Les fruits sont capsulaires, obcordés, bilobés
ou rarement ellipsoïdes, aplatis et loculicides à 4 valves ; les
loges sont à 1 ou 2 graines. Les graines sont en plan convexe (ou non si
le fruit est ellipsoïde), obliquement ovée ou orbiculaire, à
dense pubescence apprimées dans les espèces africaines
(Leeuwenberg, 1961).
I.4 Généralités sur l'espèce
Mostuea batesii I.4.1 Description botanique
Mostuea batesii est un arbuste atteignant 1,5 m de
hauteur. Ses feuilles sont opposées, simples à stipules poilues
à l'extérieur. Les inflorescences sont en cyme de 1-3 fleurs. Les
pétioles poilus atteignent 0,5-8 mm de long. Le limbe est elliptique ou
oblong-elliptique à base, obliquement cunéiforme et arrondie. Les
fleurs sont bisexuées, légèrement zygomorphes, et souvent
sessiles. Les sépales sont fusionnés à la base, leurs
formes varient de l'ovales-lancéolés à
l'ovales-linéaires, de 2,5-6 mm de long, et sont poilus à
l'extérieur ; la corolle est blanche jaune à la base, son tube en
entonnoir a une longueur de 7-11 mm de long, poilue à l'extérieur
dans sa partie supérieure est glabre dans sa partie inférieure.
Son intérieur est glabre sauf à proximité du point
d'insertion des étamines, les lobes sont de 1,5-
3 mm de long; les étamines sont libres, incluses ou
exsertes. L'ovaire supère, ovoïde, de 0,5-1 mm de long, garni de
quelques poils à l'apex. Les fruits sont en capsules bilobées de
5,5-8 mm × 11-13 mm ; et sont également poilues, bruns moyen,
à 4 valves comprenant 2 à
4 graines. Les Graines sont planes-convexes(De-ruijter, 2007).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 8
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

Figure 2: Mostuea batesii
(HNC) I.4.2 Distribution de Mostuea batesii
Les travaux de Leeuwenberg donnent une idée de la
répartition géographique de Mostuea en Afrique. Ils
indiquent où Mostuea se trouve autour de l'équateur
comme le montre la figure ci-dessous(Leeuwenberg, 1961).

Cameroun
Gabon
Nigeria
R.D.C
Ouganda
Mostuea batessii
Figure 3 : Carte de localisation de
Mostuea batesii en Afrique (leeuwenberg, 1961)
Centre
Est
Littoral
Sud-ouest
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Selon l'herbier national du Cameroun, les Mostuea batesii
se rencontrent généralement dans les Régions du
Centre, de l'Est, du Littoral et du Sud-ouest comme présenté dans
le tableau 1 ci-après :
Tableau 1 : Repartions de Mostuea
batesii au Cameroun
Région Localité
|
Près du village Lobo 50 Km de Yaoundé Mont Eloumdem
(Yaoundé)
Forêt Essong passant par Nanga-Eboko
|
5 Km au Nord de Lomié
Mont Nlonako, (5km de Nkongsamba)
Nord-est Dibombé
Muyuka
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 9
I.4.3 Usages de Mostuea batesii en médecine
traditionnelle
Au Gabon, la racine râpée de Mostuea batesii
s'utilise pour lutter contre le sommeil ou pour ses vertus aphrodisiaques;
son action est similaire à celle de Tabernanthe iboga Baill.
elle se consomme seule ou combiner à Tabernanthe iboga; un
usage prolongé peut mener à des troubles cérébraux.
En Centrafrique, la décoction des racines est prise par les enfants pour
son action vermifuge. Les plantes du genre Mostuea sont largement
utilisées par les populations forestières pour ses effets
hallucinogènes (De-ruijter, 2007). Quelles sont les travaux chimiques
déjà effectués sur le genre Mostuea ?
II. Travaux antérieurs sur le genre Mostuea
Les plantes du genre Mostuea ont fait l'objet de
nombreux travaux chimiques qui ont conduit à l'isolement et la
caractérisation des métabolites secondaires dont les plus
représentatifs appartiennent à la classe des alcaloïdes
(Jin-ruiet al., 1999).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 10
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
II.1 Les alcaloïdes II.1.1
Généralités
Le terme alcaloïde a été proposé
pour la première fois en 1819 par W. Meissner, durant ses investigations
sur le Veratrum (plante vivace vénéneuse, des
Liliaceae).Le terme alcaloïde provient de la combinaison de
«alkali», d'où la signification substance avec un
caractère alcalin. La racine «alkali» provient, quant à
elle, de l'arabe «al-qâly», signifiant «cendre de
plante» ou «soude», synonyme de l'anglais «potash» ,
ou potasse en français et était utilisé en Europe jusqu'au
milieu du XVIII ième siècle. Les alcaloïdes sont
des métabolites secondaires couramment consommés dans le monde
notamment sous forme de caféine 54 dans le thé
(Aniszewski, 2007). D'une manière générale, les
alcaloïdes se retrouvent dans plusieurs organismes vivants. Bien que la
majorité proviennent des plantes, on peut aussi les rencontrer chez :
v Les mousses (exemple: lycopodine 1, de
Lycopodium complanatum);
v Les champignons (exemple: l'ergine 2, de
l'ergot de seigle);
v Les bactéries (exemple: pyocyanine 3,
de Pseudomonas aeruginosa);
v et les animaux supérieurs (exemple:
adrénaline 4, castoramine 5 du muscle)
(Guillaume, 2013).

Lycopodine
2
3
Pyocyanine
OH
N
H
OH
OH
4
Adrenaline
Castoramine
N
O
5
HO O
NMe
N O
1 N
H
O
N
N
Ergine
.
II.1.1.1 Définition
La définition du terme alcaloïde n'est pas
facile. Pour les biologistes, les alcaloïdes peuvent se définir
comme tout composé chimique biologiquement actif et
hétérocyclique, pouvant avoir une activité
pharmacologique. Cette définition n'est pas générale; en
effet, une définition courte et exacte des alcaloïdes n'est pas
possible sans exception. Les
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 11
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
chimistes proposent une définition en des termes
purement chimiques. Selon eux les alcaloïdes se définissent comme
tout groupe ou tout complexe hétérocyclique de composés
possédant au moins un atome d'azote, ayant une forte activité
physiologique et gardant ses propriétés basiques. Malgré
les différences, les définitions sont presque similaires. Pour
généraliser, le caractère basique des alcaloïdes est
employé (Aniszewski, 2007).
II.1.1.2 Nomenclature
La plupart des noms des alcaloïdes se terminent par
ine. Leurs noms triviaux dérivent, soit du nom du chimiste qui l'a
isolé, comme la pelletiérine de Pelletier, soit des plantes
où elles ont été isolées pour la première
fois, comme la cocaïne de la coca, la caféine du café; soit
de son activité biologique tel que l'émétine (un
émétique est un médicament qui provoque le vomissement)
(Bassène, 2012).
II.1.2 Classification et structure des
alcaloïdes
Les alcaloïdes ont des structures
hétérogènes parfois complexes et sont
caractérisés par la présence d'un ou de plusieurs atomes
d'azotes (Bassène, 2012). Les principaux critères de
classification des alcaloïdes varient selon leurs origines
biogénétiques, leurs structures et leurs propriétés
spectroscopiques et/ou spectrométriques (chromophores en spectroscopie
UV, systèmes cycliques en spectrométrie de masse). Il n'existe
donc aucune classification générale et systématique des
alcaloïdes. C'est ainsi que Réné Milcent nous
présente dans son ouvrage intitulé «Chimie Organique des
Hétérocycles» une classification suivant un ordre
biogénétique tandis que Guillaume Belanger nous ressort dans son
livre intitulé «Chimie Organique Hétérocyclique»
une classification des alcaloïdes suivant leurs structures et leurs
squelettes de base
II.1.2.1 Classification des alcaloïdes suivant
leurs structures
Dans le livre de Guillaume Belanger la classification des
alcaloïdes propose :
Alcaloïdes avec azote(s) exocyclique(s) et amine(s)
aliphatique(s) Alcaloïdes de la putrescine, de la spermidine et de la
spermine. Alcaloïdes peptidiques.
Alcaloïdes terpéniques et stéroïdaux.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 12
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Alcaloïdes hétérocycliques (alcaloïdes
vrais)
II.1.2.1.1 Alcaloïdes avec azote(s)
exocyclique(s)et amine(s) aliphatique(s)
Cette classe regroupe tous les alcaloïdes avec azote
exocycliques et amines aliphatiques et comporte six catégories que sont
: les alcaloïdes de l'Erythrophleum, les dérivés de
phénylalkylamines, les dérivés de benzylamine, les
colchicines, les cathédulines et alcaloïdes du Khat ainsi que
muscarines. Le tableau 2 ci-dessous donne des exemples d'alcaloïdes par
catégories (Guillaume, 2013).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 13
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Tableau 2: Quelques
alcaloïdes avec azote(s) exocyclique(s) et amine(s) aliphatique(s)
Origines
|
Structures
|
|
Référence
|
Alcaloïdes de l'Erythrophleum.
|
O N
O
HO O
6
(-) cassaine
|
|
Guillaume
B.,2013
|
Alcaloïdes dérivés de la
phénylalkylamine.
|
N
OH
HN MeO OMe
OMe OMe
8
(-) éphédrine uvariopsamine
|
|
|
OMe OMe
MeO MeO
A A
MeO B MeO B
7O C 7
HN HN
MeO MeO
O O
9 10
(-) colchicine (+)
colchicine
|
O
|
|
C
O
NH2 NH2
11 12
|
|
|
|
HO HO
N N
O X O X
13 14
(+)-muscarine (-)-allomuscarine
|
|
|
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
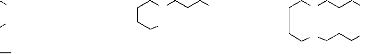
II.1.2.1.2 Alcaloïdes de la putrescine,de la
spermidine et de la spermine.
Les trois bases aliphatiques putrescine 15,
spermidine 16 et spermine 17 se retrouvent
dans plusieurs alcaloïdes largement répandus. Leurs
dérivés proviennent surtout des combinaisons avec des acides gras
ou des acides cinnamiques, et sont généralement simple(Guillaume,
2013).
15
16
17
H
N
N
H
NH2
NH2
NH2
NH2
NH2
N
H
NH2
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 14
Putrescine
Spermidine Spermine
II.1.2.1.3 Alcaloïdes peptidiques.
Les alcaloïdes peptidiques sont divisés surtout
en trois catégories, dont deux sont isolés des Rhamnaceae. Leurs
squelettes de base est complexe. La mucronine A 18 est l'un
des plus simple une troisième catégorie est celle des
alcaloïdes de l'ergot de seigle 19,
présentés ci-dessous (Guillaume, 2013).
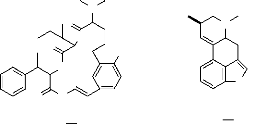
Mucronine A
acide (+)-lysergique
N
NH
OMe
O
O
NH
N
H
N
O
NH
18
II.1.2.1.4 Alcaloïdes terpéniques et
stéroïdaux.
19
Les alcaloïdes terpéniques et stéroïdaux
sont les alcaloïdes dont le squelette de base est terpenique. On
distingue, les alcaloïdes monoterpéniques, sesquiterpeniques et
triterpéniques (Guillaume, 2013). Le tableau ci-après illustre
quelques alcaloïdes de ce type.
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Tableau 3 : Alcaloïdes
terpéniques et stéroïdaux
Classe
|
Squelette de base
|
Structures
|
|
Référence
|
Alcaloïdes diterpéniques
|
RNN
20
|
O
OH
21
(-)-atisine
|
|
Guillaume
B.,
2013
|
|
|
22
|
23
|
|
|
O
HO P O O
O P
O
24
Pyrophosphate
géranylgéranyle
|
HO
ACO O
ACO
O
25 O
|
OH
N
|
|
|
|
|
26
steroides
|
N
N
27
|
|
|
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 15
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
II.1.2.1.5 Alcaloïdes hétérocycliques
ou alcaloïdes vrais.
Les alcaloïdes hétérocycliques ont un ou
deux atome(s) d'azote. Pour la section suivante, seuls quelques exemples
représentatifs de chaque classe seront donnés (Guillaume,
2013).
Tableau 4: Alcaloïdes
hétérocycliques ou alcaloïdes vrais.
Classe
|
Structures
|
Référence
|
Alcaloïdes
dérivés de
la
pyrrolidine
|
MeO
OMe
N
28
Mésembrénol
|
Guillaume
B., 2013
|
Alcaloïdes
dérivés de
la
pipéridine
|
|
N
29
|
N
N
30
|
|
|
|
|
Tropinone N
O
31
|
(-)-cocaine N
COOH
O
32 O
|
|
N H
O
N
H H
33 H3COOC
Ajmalicine
|
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 16
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Classe
|
Structures
|
Référence
|
Alcaloïdes
dérivés de
l'histamine,
de
l'imidazole et de
la guanidine
|
H2N
H N
N N N N N O
N
N
34 35 36
|
Guillaume
B., 2013
|
|
|
HO OH
H N N
H3CO
N
N O
37 H38
Quinkline (+)-méloscine
|
|
HO
MeO NH
HO
MeO
MeO NH
MeO
39 40
|
|
|
AlcaloïdesN dérivés de laN
N
N
40 41 OH
|
|
|
O OH
N O
42 OH
3,4-dihydro-2,4-dihydroxy-1,4-benzoxazin-3(2H)-one
|
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 17
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Classe
|
|
|
Structures
|
Référence
|
Alcaloïdes
dérivés de
la
pyrrolizidine
|
|
|
|
Guillaume
B., 2013
|
|
|
|
|
N
43
|
|
|
|
(-)-rétronécanol
OH
O
HO N
|
|
|
|
44
(-)-sérratinine
N
|
|
|
|
|
N
|
H
N
N
|
N
N
H O
46
Cyclopeptine
OH O
H
N N
N N
|
|
|
|
47
Purine
|
|
48 49
Xanthine
Théobromine
O OH
N
HN OH
H2N N N
50
(-)-bioptéridine
|
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 18
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 19
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
II.1.3 Classification des alcaloïdes suivant leur
biogenèse
Du point de vue biogénétique et selon Hegmauer,
il existe trois classes d'alcaloïdes: les alcaloïdes vrais, les
protoalcaloïdes et les pseudoalcaloïdes (Milcent, 2003).
Les alcaloïdes vrais, qui
représentent le plus grand nombre, ont un large spectre
d'activité biologique et sont très basiques. Leur basicité
est due à un atome d'azote contenu dans un hétérocycle
(Milcent, 2003); leur biosynthèse s'effectue à partir des acides
aminés tel que la L-lysine, la L-ornitine, la L-tryptophane, la
L-tyrosine, la L-phénylalanine, la L-histidine (Aniszewski, 2007). Ils
sont sous forme de sels de divers acides dans la plante. Le représentant
simple de cette classe est la pyrrolidine 51 (Milcent,
2003).
N
H
51
la pyrrolidine
Les protoalcaloïdes sont des
alcaloïdes dont l'atome d'azote ne fait pas partie de
l'hétérocycle. Ils dérivent aussi des acides aminés
et sont souvent appelés « alcaloïdes biologiques ». Ils
sont solubles dans l'eau. C'est le cas de la mescaline 52
(Milcent, 2003).
OMe
52
Mescaline
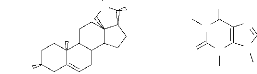
Les pseudoalcaloïdes ne dérivent
pas d'acides aminés. Ils sont pour la plupart basique; et
sontreprésentés par les alcaloïdes stéroïdaux et
les purines telles que la conessine
53 et la caféine54
(Milcent, 2003).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 20
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Me
N Me
Me
(Me)2N
O
N N
N
N
O
54
53
Conessine
Cafeine
II.1.4 Caractérisation des alcaloïdes
La caractérisation des alcaloïdes se fait sur des
extraits aqueux acides; par précipitation des sels d'alcaloïdes
avec des réactifs généraux: Avec le réactif de
Valser-Meyer, on obtient un précipité blanc-jaunâtre et un
précipité rouge-orangé avec le réactif de
Dragendorf. Le réactif iodoplatinate de potassium est un
révélateur utilisé pour les alcaloïdes en CCM
(Bassène, 2012).
II.1.5 Propriétés physicochimiques des
alcaloïdes
II.1.5.1 Caractère physique
Les alcaloïdes sont des solides cristallisés
lorsqu'ils sont oxygénés avec un poids moléculaire
élevé; et des liquides entrainables à la vapeur d'eau
s'ils sont non oxygénés et de faible poids moléculaire.
Leur saveur est généralement amère (Bassène,
2012).
? Solubilité
La solubilité des alcaloïdes dépend de la
forme dans laquelle ils se trouvent. En milieu alcalin; les alcaloïdes
sont sous forme de base (libre) et sont insolubles dans l'eau; mais soluble
dans les solvants apolaires (éther, benzène, chloroforme,
etc...). En milieu acide les alcaloïdes sont sous forme de sels; ils sont
solubles dans l'eau, mais insolubles dans les solvants organiques apolaires.
L'alcool est capable de dissoudre les deux formes (base; sels). Ce comportement
intéressant va engendrer trois méthodes d'extractions à
savoir: extraction par l'eau acide, extraction par l'alcool, extraction par
solvant organique (Bassène, 2012).
II.1.5.2 Caractère chimique
Les alcaloïdes donnent des précipités avec
certains réactifs tels que l'acide picrique, l'acide phosphotungstique
et les réactifs iodés tel que le réactif iodoioduré
(Boucharat ); le
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
réactif iodomercurate de potassium (reactif de
Velsermeyer): le réactif iodobismutite de potassium (réactif de
dragendorff) (Bassène, 2012).
II.1.6 Biosynthèse
Guignard dans son livre intitulé « Biochimie
Végétale » indique que la synthèse des
alcaloïdes s'éffectue au niveau du réticulum endoplasmique;
les alcaloïdes se concentrent ensuite dans la vacuole. Pour ce qui est du
pavot, il s'agit des vacuoles spécialisés
développées en lactifères. De façon
générale; la production d'alcaloïdes s'observent dans les
tissus en voie de croissance (jeunes racines; jeunes feuilles) (Guignard,
1996).
La pénétration à travers le tonoplaste
se fait sous forme moléculaire neutres lipophiles. Le pH acide de la
vacuole ionise l'alcaloïde dont la capacité transmembranaire se
trouve réduite: il en résulte une accumulation intravacuolaire de
l'alcaloïde (Guignard, 1996).
Fréquemment les alcaloïdes s'accumulent en des
emplacements différents de leur lieu de synthèse. Par exemple
dans le tabac, la nicotine est synthétisée au niveau des racines;
puis elle migre vers le feuillage. Absente dans les graines, elle se forme
dès la germination de la plantule (Guignard, 1996).
Des modifications de structure peuvent se produire lors de
ces transferts. C'est ainsi que la nicotine est déméthylée
au niveau des feuilles en nornicotine (Guignard, 1996).
II.1.6.1 Précurseur des
alcaloïdes
Les alcaloïdes ont 5 principaux précurseurs qui
sont : la L-ornithine 56 et la L-lysine 55
(aminoacide diaminé) , la L- phénylalanine
58, la L-tyrosine 59 et le L-
tryptophane 57 (aminoacide aromatique). Le point de
départ de nombreux alcaloïdes; plus rarement l'asparagine; la
proline, le glutamate, l'histidine, auxquels il faut ajouter des corps de
structures voisines comprenant un carboxyle d'azote: nicotinate, anthranilate
(Guignard, 1996).
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 21
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 22
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Acides aminés aliphatiques
H O
OH H O
H2N C C OH
CH2
HC CH3
H2C NH2
H2N C C
CH2 CH2 CH2 CH2
NH2
55 56
L-lysine
L-Ornitine
Acides aminés aromatiques
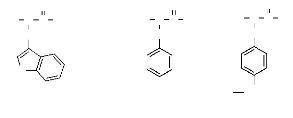
O
OH
H
H2N C C
CH2
57
OH
L-tyrosine
L-tryptophane
L-phénylalanine
H
H2N C C
CH2
O
OH
H
H2N C C
CH2
O
OH
HN
58 59
v La L-ornihine 56 (acide
aminé non protéique) et la L-lysine 55 sont
à l'origine des alcaloïdes à cycle pyrrolizidine et
quinolizidine : tels que les alcaloïdes tropaniques et la cocaïne
32 (Guignard; 1996).
v La L-tyrosine 59 et la
L-phénylalanine 58; qui sont les acides aminés
aromatiques sont précurseurs pour leur part du groupe des
alcaloïdes isoquinoléiques (Guignard, 1996).
v Le tryptophane 57 est à
l'origine de la quasi-totalité des alcaloïdes indoliques, mais
intervient rarement seul (Guignard, 1996).
Les alcaloïdes indolo-monoterpéniques sont les
plus nombreux : on les rencontre chez les Asteridae ligneuses : Loganiaceae,
Apocynaceae-Asclépiadaceae ,Rubiaceaechez ces dernières un
réarrangement tardif substitue le noyau quinoléique au noyau
indole (Guignard, 1996).
v A côté de ce trois grandes classes
d'alcaloïdes issus des précurseurs précédents, on
distingue les alcaloïdes monoterpéniques et les alcaloïdes
dérivés de la purine (caféine 54,
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 23
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
théobromine 49) que certains d'ailleurs
ne considèrent pas comme alcaloïdes véritables. (Guignard,
1996)
II.1.6.2 Principe et biosynthèse des
alcaloïdes quinoléiques
La réaction élémentaire de la
biosynthèse des alcaloïdes est la désamination et la
décarboxylation, comme le présente le schéma suivant
(Aniszewski, 2007).
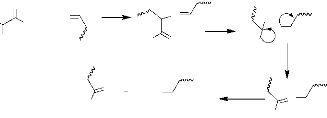
O
OH
NH2
+ O N
HO O
-CO2
H
N
H
O
H
H2N
N
H
Schéma 2 : Mécanisme
général de la biosynthèse des alcaloïdes
+H2O
Pour ce qui est des alcaloïdes quinoléiques qui
retiennent notre attention, en raison du fait que la quasi-totalité des
alcaloïdes isolés du genre Mostuea sont de cette classe,
leur biosynthèse suit le mécanisme général
précédent avec comme précurseur le tryptophane 60
comme l'indique le schéma 3 ci-dessous.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 24
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
COOH

O
NH2
60
64
N
Tryptophane
O
N
H
Camptothecin
N
O
NH2
61
H
HO N
H
N
OH
HO
N
H
H3CO
N
Cinchonidine
NADPH
N
Décarboxylation
62
O
OH
Tryptane
N
H
Secologanine
O
O
Strictosamide
N
H
H
H
H OGly
N
H
N
O
Pumiloside
H
H OGly
H
H3CO2C
Strictosidine
H
OGly
NH
N
H
OH
N
66
Cinchonamine
N
H
H
N
H
OH
HO
N
H
N H H CHO
H
Corynantheal
H
NADPH
O N
H
N
OH
H
N
H
N
NADPH
NADPH
H3CO
70
Cinchonine N
O
63
69
65
67
68
72
71
Quinkline
Schéma3: Biosynthèse des
alcaloïdes quinoléique (Aniszewski, 2007)
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
III. Quelques alcaloïdes isolés du genre
Mostuea
C'est à Jin-rui et collaborateurs que l'on doit en 1999
les premiers travaux sur le genre Mostuea plus
précisément sur l'espèce Mostuea brunonis. Ces
travaux ont conduit à l'isolement et la caractérisation de 6
alcaloïdes appartenant à la classe des alcaloïdes
quinoléiques représentés dans le tableau ci-dessous.
Tableau 5: Quelques alcaloïdes
isolés du genre Mostuea
|
Noms
|
Structures
|
Sources
|
Référence
|
|
-R=H camptothecin -R=â-D-glu
20-O-â- glucopyranosylcamptothecin
|
1-R=H
2-R=â-D-glu 73
O
N
|
Mostuea
brunonis
|
Jin-rui et al
1999
|
|
Deoxypumiloside
|
N
O
OR O
O
N
74
|
|
R=H strictosamide R=COCH3
2'-O-acetylstrictosamide
|
N
H
O
H H
O
HO OH O
HO O
O
N
N
H O
H
O H
75
|
|
Topotecane
|
HO O
3-R=H OR
4-R=COCH3
HO HO
Me2N
HO O
N
N
O
76 OH O
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 25
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 26
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
IV. Importance des alcaloïdes
> Dans la chimiotaxonomie
Les alcaloïdes permettent souvent pour des genres ou des
espèces apparentés, d'en préciser la phylogénie :
ceux dont les molécules sont les plus simples se rencontrent chez les
moins évolués. Plus rarement, c'est une même série
d'alcaloïdes qui caractérisent des taxons plus ou moins importants.
C'est ainsi que les Magnoliales, Ranunculales et Papavérales ont des
alcaloïdes dérivés de la benzylisoquinoléine
(réticuline des Annonaceae, tubocurarine des Ménispermaceae). De
même, la présence des alcaloïdes indoliques rencontrés
chez les Loganiaceae (strychnines), les Apocynaceaes-Asclepiadaceae (vincamine)
et les Rubiaceaes (quinine) confirme la parenté de ces Astéridae
(Guignard ,1996).
> En pharmacologie
Les alcaloïdes ont des propriétés et
potentialités pharmacologiques diverses et variées. C'est le cas
notamment des alcaloïdes de l'ergot de seigle qui ont une activité
sur les systèmes musculaires, vasculaires et nerveux. Ils ont aussi une
action sur les processus biologiques contrôlés par le
système de l'hypothalamus. La coniine 29 connue en 399
avant Jésus Christ est une toxine puissante utilisée par les
plantes insectivores comme agent paralysant. La morphine et ses sels sont
classés comme analgésiques nicotiniques ; celui-ci est contenu
dans l'opium. La nicotine 30 est un alcaloïde toxique
dont la dose de 40 mg est mortelle pour l'homme ; suite à une paralysie
du système respiratoire. La nicotine 30 a des effets
importants sur le système cardiovasculaire ; vasoconstriction
périphérique ; tachycardie atriale et augmentation des pressions
systolique et diastolique. Environ 50% des fumeurs meurent de maladies
cardiaques et 20% de cancer de la langue (Milcent, 2003).
Les alcaloïdes de l'erythrophleum sont connus pour leurs
propriétés anesthésiques et agissent aussi sur le coeur.
Le khat est un arbuste connu depuis environ 1300 ans, qui pousse dans les
vallées de la Somalie et du Yemen, mais aussi en Éthiopie et au
Kenya. Ses feuilles, lorsque mâchées, mènent à un
état d'euphorie. L'isomère 9 de la colchicine,
est un anti-inflammatoire et analgésique thérapeutique
spécifique de la crise aigüe de goutte, elle est utilisée
dans le traitement de l'hypotension au cours de l'anesthésie
générale et de l'anesthésie locorégionale,
rachidienne ou péridurale. L'ajmalicine 33 (et
yohimbine) sont utilisés en
pharmacie comme vasodilatateur périphérique
électif des artérioles (augmente le flux
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 27
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
musculaire et cérébral (antiischémique)
). Les quinquinas de Cinchona appelés « Poudre des jésuite
» sont capables de guérir les fièvres. Ce remède
restera secret longtemps. Les quinquinas ont des propriétés
antipaludéennes et ont longtemps été utilisés en
pharmacie pour la lutte contre le paludisme (Vercautoren, 2011).
En raison de ce large spectre des alcaloïdes, il nous a
paru intéressant de faire une investigation d'une plante riche en
alcaloïdes comme Mostuea batesii.
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
CHAPITRE II :
RESULTATS ET DISCUSSION
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 28
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 29
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I. EXTRACTION ET ISOLEMENT DES COMPOSES
Les racines de Mostuea batesii ont été
récoltées le 3 février 2014 au Mont Eloundem dans la
localité de Mbankomo (Région du Centre Cameroun).
Après découpage, séchage et broyage,
1,048 Kg de poudre obtenue a été extraite à froid par
macération au méthanol pendant 48 h, ce qui a permis d'obtenir
après filtration et évaporation du solvant, 90 g d'extrait brut
de couleur marronne foncée.
La chromatographie sur colonne de gel de silice de cet extrait
dans le système Hexane/acétate a conduit à l'isolement de
5 composés indexés de GB1 à GB5. Dans la suite de cette
présentation, nous allons élucider la structure de deux d'entre
eux à savoir : GB1 et GB5.
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

Racines de Mostuea batesii
Découpage Séchage Broyage

1,048 Kg de poudre
Extraction au MeOH
CC sucessives sur gel de silice dans le mélange Hexane
/Acétate

GB4
GB3
GB5
GB1
GB2

90 g d'extrait brut
Poudre résiduelle
Schéma4:Protocole d'extraction et
d'isolement des composés GB à partir des racines de
Mostuea batesii
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 30
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I.1 Elucidation des structures de deux des composes
isolés
I.1.1 Elucidation de la structure de GB1
Le composé GB1 précipite sous forme d'aiguille
de couleur blanche dans le mélange Hex/AcOEt 45%. Soluble dans le DMSO,
il répond positivement au test de Dragendorf et de Valser-Mayer,
caractéristiques des alcaloïdes.
Son spectre de masse ESI en mode positif présente le
pic de l'ion pseudomoléculaire [M+H].+ à m/z=349 ;1
d'intensité relative égale à 54,5 Compatible avec la
formule brute C20H17O4N2, par conséquent GB1 a pour formule brute
0H16O4N2 et renferme de ce fait 14 degrés d'insaturation.
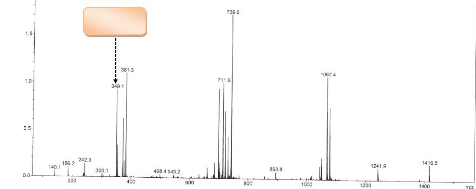
[M+H ]+.
Figure 4 : Spectre de masse ESI du
composé GB1
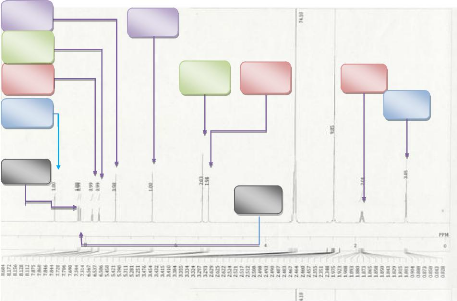
Son spectre de RMN 13C (DMSO -d6; 125MHz)
complètement découplé large bande fait ressortir 20
signaux correspondant aux 20 atomes de carbones présent dans sa formule
brute. L'analyse de ces signaux au moyen des techniques HSQC et DEPT met en
exergue:
> 3 méthylènes hybridés
sp3à äC 30,3/äH 1,92 ; äC 50,3/ äH 5,27;
à äC 65,3/ äH 5,41 ;
> 1 méthyle à äC 7,8/ äH 0,88 ;
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 31
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 32
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
? 6 méthynes à SC 131,6 /SH 8,67 ;SC 127,9 /SH
8,23 ;SC 127,7 /SH 7,84 ;SC=130,4 /SH 7,86 ;SC=128,5/ SH 8,28 ; SC 96,7 /SH
7,68 ; tous hybridés sp2
Parmi les dix signaux restant correspondant aux carbones
quaternaires, neuf sont hybridés sp2 parmi lesquels : deux
carbonyles des esters et des amides respectivement à SC 172,5 ; SC 156,9
; et un carbone hybridé sp3oxygené à SC
72,4.
L'ensemble de ces données indiquent que le
composé GB1 possède un squelette de base de type camptothecine,
qui est un alcaloïde quinoléique. (Long-Ze et al., 1990 ;
Jin-Rui et al., 1999)
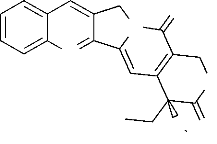
O
N
N
O
OHO
Schéma 5 : Squelette de la
camptothecine
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 33
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

5C= 172,5
C=O
5C= 156,9
a
c
b
Figure 5 : Spectre carbone large bande du
composé (c) DEPT 90 (a), DEPT 135 (b) de GB1
Son spectre RMN 1H fait apparaitre un ensemble de
signaux constitués :
D'un système de 4 protons appartenant à un noyau
aromatique orthodisubstitué constitué de deux doublets à
5=8,13 et à 5 = 8,18; de deux triplet à 5=7,84et à 5=7,86
;
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 34
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
D'un singulet de proton échangeable à l'eau
deutérée à SH 6,52 correspondant à un proton
alcoolique, qui compte tenu de son déplacement, serait
chélaté.
De deux singulets de méthylène à S 5,41
et à SH 5,27 fortement déblindé d'une part par un
hétéroatome et d'une autre part par le cône d'anisotropie
magnétique.
Un système d'un triplet de trois protons à S
0,88 et un doublet de quadruplet de deux protons à SH 1,92 correspondant
au groupement éthyle lié à un carbone quaternaire.
Au regard des déductions obtenus à partir du
spectre carbone, il ressort que le groupement hydroxyle de l'alcool et
l'éthyle sont à positionner sur le squelette de base. Nous y
sommes parvenu par comparaison de nos données spectrales à celle
décrit dans la littérature. Ce qui nous a permis de positionner
le groupement OH et éthyle sur le même carbone (C-20). La
structure du compose GB1 est :
10
9
8
7
6
4
5
N
O
16a
16 17
15
20 O
21
O O
H
11
12
13
N
1
2 3
14
18
19
Schéma 6 : Squelette de la
camptothecine
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Les infomations spectrales décrites ci-dessus nous ont
permis de proposer GB1 la structure suivante qui est celle de la camptothecine,
composé anticancereux dont les données de RMN 13C ont
été publiées pour la première fois par Long-Ze en
1990. L'attribution du spectre proton est représenté dans la
figure ci-dessous.
H 12
H 14
H 10
H 11
H 7
H-O
H 17 H 5 H 19
H 9
H 18
Figure 6: Spectre RMN 1Hdu
composé GB1
L'analyse du spectre HSQC nous permet d'attribuer les protons
non échangeables à l'eau deutérée et permet, de ce
fait, de localiser le proton alcoolique comme le décrit les spectres
suivants.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 35
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 36
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

Proton aloolique H 20
Figure 7 : Spectre HSQC du
composé GB1

H 19
H 18
C 18
|
Figure 8:Spectre HSQC élargi du
composé GB1
|
C 19
|
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

H 7
H 14
C 14
C 7
Figure 9: Spectre HSQC du
composé GB1
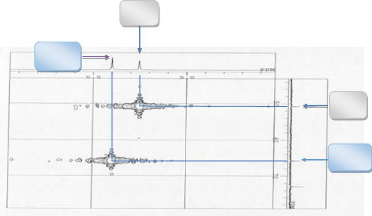
H 17
H 5
C 17
C 5
Figure 10:Spectre HSQC du composé
GB1
Le composé GB1 a été identifié
comme étant la camptothecine, isolée pour la première fois
du genre Mostuea par Jin Rui et collaborateurs, montrant ainsi
l'apport des alcaloïdes dans la chimiotaxonomie. Les corrélations
observées sont représentées dans le schéma
ci-dessous.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 37
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 38
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

O
H
O
H
H
H
H
H H H
9
6
4
H
10
N
8
7
5
H
16a
O
H
H
H
11
12
13
N1 2 3
16
17
14
15
O
H
H
H
20
21
18 19
Schéma 7:
Corrélations H-H sur la camptothecine
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Tableau 6 : données spectrales de
RMN 1H (DMSO-d6, 500MHz) et de RMN 13C
(DMSO-d6 ; 500 MHz)
|
Positions
|
1H en ppm [nH, m, J
(Hz)]
|
13C en ppm (m)
|
*13C
|
|
1
|
/
|
/
|
/
|
|
2
|
/
|
152,6 (s)
|
153,9
|
|
3
|
/
|
147,5 (s)
|
146,2
|
|
4
|
/
|
/
|
/
|
|
5
|
5,27 (2H,s)
|
50,3(t)
|
51,4
|
|
6
|
/
|
129,8(s)
|
130,9
|
|
7
|
8,67 (1H,s)
|
131,6 (d)
|
133,3
|
|
8
|
/
|
129,0 (s)
|
129,9
|
|
9
|
8,13 (1H, d, 8Hz)
|
127,9 (d)
|
129,7
|
|
10
|
7,84 (1H, t, 8,8Hz)
|
127,7 (d)
|
129,1
|
|
11
|
7,86 (1H, t, 8,8Hz)
|
130,4 (d)
|
131,9
|
|
12
|
8,18 (1H, d, 8 Hz)
|
128,5 (d)
|
129,8
|
|
13
|
/
|
150,0 (s)
|
149,6
|
|
14
|
7,33 (1H,s)
|
96,7 (d)
|
101,5
|
|
15
|
/
|
147,9 (s)
|
149,2
|
|
16
|
/
|
119,1 (s)
|
122,0
|
|
16a
|
/
|
156,9 (s)
|
168,3
|
|
17
|
5,41 (2H, s)
|
65,3 (t)
|
67,8
|
|
18
|
0,88 (3H, t, 8Hz)
|
7,8 (q)
|
8,4
|
|
19
|
1,92 (2H, dq, 8 Hz)
|
30,3 (t)
|
33,9
|
|
20
|
/
|
72,4 (s)
|
79,1
|
|
6,52 (1H,s)
|
Proton alcoolique
|
|
|
21
|
/
|
172,5 (s)
|
171,1
|
*C données 13C de la littérature
dans chloroforme deutéré (Jin-Rui et al.,
1999)
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 39
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I.1.2 Elucidation de la structure GB5 ;
Le composé GB5 précipite sous forme d'aiguille
de couleur rose dans le mélange Hex/AcOet 70%. Soluble dans le DMSO et
aussi dans l'eau. Il répond positivement au test de Molish,
caractéristique des sucres.
Son spectre de masse ESI en mode négatif
présente le pic de l'ion pseudomoléculaire [M-H].+.
à m/z=341 d'intensité relative égale à 31,91 ; donc
l'analyse à haute résolution nous a permit d'attribuer la formule
brute C12H21O11 , par conséquent GB5 pour formule brute
C12H22O11 comportant deux degrés d'insaturation.
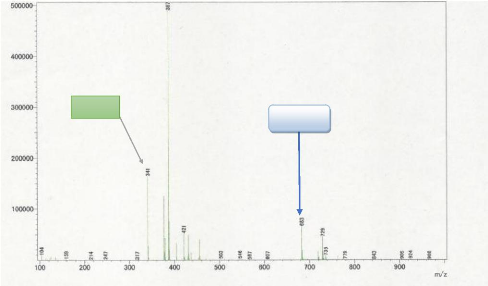
[M-H]+.
[2M-H]+.
Figure 11 : Spectre de masse ESI du
composé GB5
Son spectre de RMN 13C (DMSO-d6
;125MHz) complètement découplé large bande
fait ressortir 12 signaux de carbone correspondants aux 12 atomes de carbone
présents dans la formule brute. L'analyse de ces signaux au moyen des
techniques HSQC et DEPT fait ressortir :
Deux carbones anomériques l'un quaternaire à
äC 104,1 et l'autre tertiaire à äC 91,78/ äH 5,18
suggérant que notre sucre est un dimère non symétrique
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 40
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 41
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
3 méthylènes à SC 60,5/SH 3,37 ; SC 62,1 /
SH 3,56 ; SC 62,1/SH 3,46. l'indiquant
que l'un des monomères possède un cycle à
cinq tandis que l'autre sera à six.
Le reste étant les sept signaux des méthynes
hybridés sp3 tous oxygénés.

Carbone quaternaire sp3
Figure 12 : Spectre carbone large bande
du composé GB5
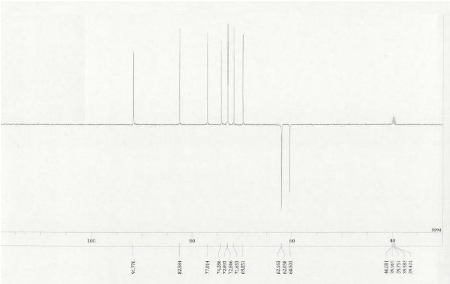
Figure 13:Spectre DEPT du
composé GB5
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
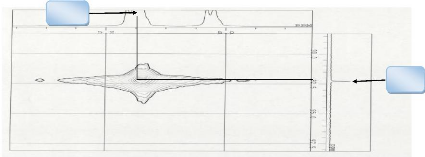
H1
C 1
Figure 14:Spectre HSQCdu composé
GB5 élargit

Groupements O-H entre äH= 4 à 5 ppm
Figure 15:Spectre HSQC du composé
GB5
Le spectre HSQC nous permet également de
déterminer les hydrogènes (non échangeables à l'eau
lourde) à leurs carbones respectivement, comme l'illustre les figures
ci-dessous :
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 42
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
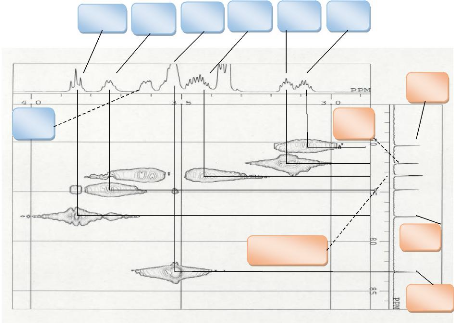
5'-H
3'-H 4'-H 6'-H 3-H 2-H 4-H
3-C et 5'-H
2-C
3'-C
4-C
6'-C
Figure 16: Corrélations HSQC du
composé GB5
L'analyse de son spectre de RMN 1H fait apparaitre
plusieurs signaux intégrants au total 22 protons associés aux 22
protons de la formule brute. Le spectre étant enregistré dans le
DMSO-d6 à une fréquence de 500,16 MHz. Le spectre HSQC
nous permet de distinguer les protons échangeables à l'eau
lourde, confirmant ainsi l'attribution de la formule brute.Nous pouvons
observer sur ce spectre :
Les protons des hydroxyles à S= 4 à 5 (exception
pour le proton anomerique)
Les protons des méthynes entre S= 3 à 4
Les attributions peuvent être observées sur les
figures ci-dessous.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 43
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
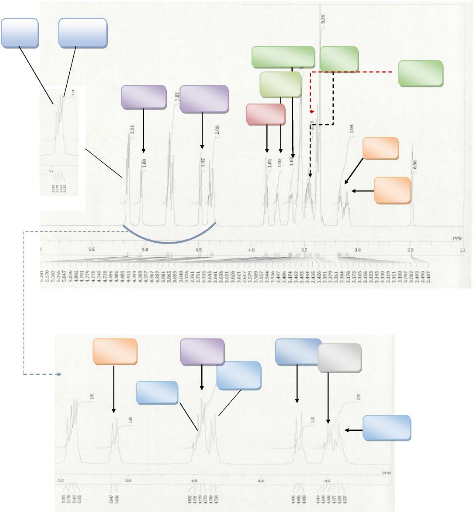
1-H
4'-OH
2-OH
2-OH
1'-OH
2'-OH
3-OH
4-OH
3'-H
5'-H-5H 4'-H
2'-OH
6-OH
3-H
2-H
6'-OH
4-H
1'-H
Figure 17: Spectre
RMN1H
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 44
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Son spectre COSY est difficilement exploitable compte tenu des
valeurs identiques de la plupart des constantes de couplage. Cependant quelques
corrélations ont pu être exploitées comme la
présente les figures ci-contre.
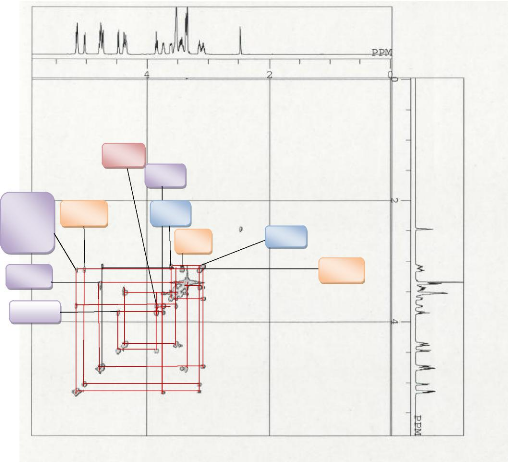
H-1
Et
4'-OH
3-OH
2'-OH
2-OH
3'-H
4'-H 5'-H
3-H
4-H
2-H
Figure 18 :Spectre COSY du composé
GB5
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 45
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
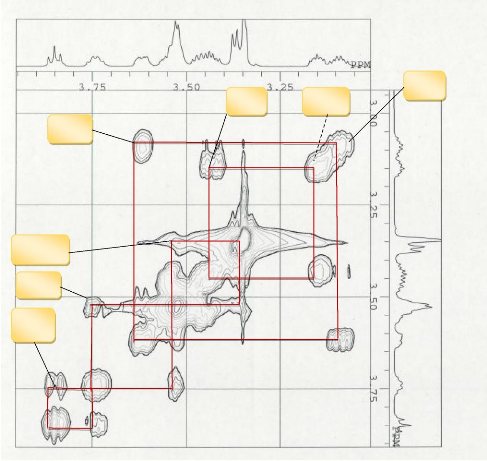
H6-H6'
4'-H
5'-H
5-H
3-H
2-H
4-H
Figure 19:Spectre COSY élargit du
composé GB5
La structure GB5 a été établit d'une part
par comparaison de ses données spectrales à celle décrit
dans la littérature par Naoki et collaborateur et d'autre part au fait
que le seul dimère possible en C12 ayant 3 méthylènes et 2
insaturation n'est autre que le sucrose. La structure suivante étant
celle du saccharose ; elle a été proposée pour le
composé GB5, elle est la forme de transport qui permet les mouvements
des glucides entre les différentes zones de synthèse,
d'utilisation et de mise en réserve dans la plante.
Le spectre est difficilement exploitable parce qu'il a
été enregistré à 25°C, pour obtenir un spectre
de bonne résolution un enregistrement à 90°C serait
recommandé selon Noaki et collaborateurs.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 46
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 47
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
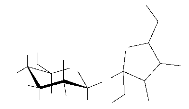
H
HO
HO
O
O
OH
H OH
HO OH
H
H
HO
Schéma 8: structure du
sucrose
Tableau 7 : Données spectrales de
RMN 1H (DMSO-d6 ; 500MHz) et de RMN 13C (DMSO-d6 ; 125MHz) du composé
GB5
Positions 1H (ppm) [nH, m, J (Hz)] 13C en
ppm
|
1
|
H
|
5,18 (1H)
|
92,1
|
|
2
|
H
|
3,17 (1H, m)
|
71,7
|
|
3
|
H
|
O
OH H
3,474 (1H,m)
|
72,8
|
|
4
|
H
|
3,09 (1H, m)
|
70,0
|
|
5
|
H
|
3,62 (1H, m)
|
82,6
|
|
6
|
H
|
3,54 (2H, d, 5Hz)
|
62,1
|
1'
|
H
|
3,38 (2H, d, 6Hz)
|
62,2
|
2'
|
/
|
/
|
104,1
|
3'
|
H
|
3,87 (1H, t, 8Hz)
|
77,0
|
4'
|
H
|
3,751 (1H, q, 9Hz)
|
74,3
|
5'
|
H
|
3,641(1H, m)
|
72,9
|
6'
|
|
H
|
3,57 (2H , d, 5Hz)
|
62,1
|
|
|
Positions
|
1H en ppm [nH, m, J (Hz)]
|
13C en ppm
|
|
2
|
O-H
|
5,04 (1H,d, Hz)
|
71,7
|
|
3
|
O-H
|
4,78 (1H, d, 5Hz)
|
72,8
|
|
4
|
O-H
|
4,74 (1H, d, 5Hz)
|
70,0
|
|
6
|
O-H
|
4,41 (1H,t, 5Hz)
|
62,1
|
|
1'
|
O-H
|
4,80 (1H, t, 6Hz)
|
62,2
|
3'
|
O-H
|
4,49 (1H, d, 5Hz)
|
77,0
|
4'
|
|
O-H
|
5,16 (1H, d, 4Hz)
|
74,3
|
|
|
6'
|
O-H
|
4,37 (1H, t, 5Hz)
|
82,6
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 48
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
CONCLUSION GENERALE
Notre travail sur l'extrait au MeOH des racines de Mostuea
batesii, a conduit à l'isolement au moyen des méthodes
chromatographiques usuelles (chromatographie sur colonne) cinq composés
indexés de GB1 à GB5; deux d'entre eux ont été
entièrement caractérisés, il s'agit :
D'un alcaloïde : la camptothecine.
D'un sucre : le saccharose
L'élucidation des structures de ces composés a
été rendue possible grâce à l'interprétation
rigoureuse de leurs données spectroscopiques, en particulier la RMN
1H et la RMN 13C à une et deux dimensions et la
spectrométrie de masse et aussi par comparaison de leurs données
spectrales avec celles de la littérature.
Nous nous proposons, dans la suite de notre travail,
d'élucider et de déterminer les structures autres composés
isolés et de poursuivre les travaux sur les extraits des autres parties
de la plante à savoir : les tiges et les feuilles.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 49
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
CHAPITRE III :
PARTIE EXPERIMENTALE
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 50
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I. Généralités
I.1 Appareillage
Les points de fusions ont été
déterminés à l'aide du banc de Kolfer et ne sont pas
Corrigés.
Les différentes masses ont été
mesurées sur une balance COBOS, model D-600-SX et SARTORIUS,
précision 1/1000.
La chromatographie sur colonne a été
effectuée à l'aide d'une silice de type Merck, de
granulométrie 60-80 um. Celle sur couche mince a été
réalisée sur des plaques en aluminium recouvertes de gel de
silice 60F254, de type Merck et d'épaisseur 0,2 mm. Les
taches ont été révélées sous lumière
ultraviolette de radiation 254-366 nm, et sous vapeur d'iode.
De larges récipients en verre (ampoule à
décantée et erlenmeyer) ont été utilisées
pour la macération des racines de Mostuea batesii. Les extraits
obtenus ont été filtrés et concentrés avec un
évaporateur rotatif de type Heidolph connecté à un
circulateur d'eau du fabricant LAUDA type WKL 230.
Les spectres de masse ont été enregistrés
sur un spectromètre de type VARIAN.
Les spectres RMN à une et deux dimensions ont
été enregistrés sur un spectromètre de type
BRUCKER, (RMN1H: 500,16 MHz, RMN 13C : 125 MHz); les
composés étant tous dissous dans le DMSO. Les déplacements
chimiques sont exprimés dans l'échelle ä en ppm par rapport
au TMS pris comme référence. Les constantes de couplage (J) sont
exprimées en Hertz (Hz).
I.2 Matériel végétal
Les racines de Mostuea batesii ont été
récoltées le 03 février 2014 dans la localité de
Mbankomo (centre du Cameroun). L'identification a été faite
à l'Herbier National du Cameroun où un échantillon a
été déposé sous le numéro 38660 en
comparaison avec le numéro du collecteur Letouzey qui est 15036.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 51
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
I.3 Extraction, isolement et caractérisation des
composés GB
I.3.1 Extraction
Après la récolte, les racines de Mostuea
batesii ont été séchées,
découpées et broyées. Après toutes ces
opérations, 1,048 kg de poudre ont été obtenues et ont
été extraite par macération à froid à
température ambiante, au méthanol pendant 48 heures. Après
filtration et évaporation du solvant, 90 g d'extrait brut a
été obtenu soit un rendement de 8,59% dont 5 g ont
été prélevés pour les tests biologiques.
I.3.2 Séparation chromatographique
L'extrait restant a été fixé sur 100 g de
silice de granulométrie 40-63 um et introduit dans une colonne de
diamètre 4,5 Cm. Les fractions de 100 mL ont été
collectées et regroupées sur la base de la CCM comparative. Comme
l'indique le protocole d'extraction (schéma 4) et le tableau
chromatographique (tableau 8).
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)

Poudre résiduelle
GB1 0,5g GB2 0,6g GB3 0,8g GB4 0,5g GB5 1g
Racines de Mostuea batesii
1,048 Kg de poudre
Découpage Séchage Broyage
Extraction au MeOH
90 g d'extrait brut
CC
successives
Schéma 4: Protocole
d'extraction et d'isolement des composés GB à partir des racines
de
Mostuea batesii
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 52
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Tableau 7: Chromatogramme de l'extrait
brut
|
Solvant d'élution
|
Fractions
|
Séries
|
Observation
|
|
Hex
|
1-20
|
S1
|
Obtention de l'huile
|
|
5% Hex / AcOEt
|
21-50
|
Solution incolore présentant une trainée non
visible à l'UV mais visible à l'iode
|
|
10% Hex / AcOEt
|
51- 80
|
S2
|
Solution de couleur verdâtre présentant environ 5
taches visible à l'UV et à l'iode
|
|
81-115
|
S3
|
Solution de couleur verdâtre présentant environ 5
taches visibles à l'UV et à l'iode
|
|
15% Hex / AcOEt
|
116-143
|
Solution de couleur marronne présentant 2 taches
visibles à l'UV et à l'iode
|
|
20% Hex / AcOEt
|
144-174
|
|
30% Hex / AcOEt
|
175-246
|
|
40% Hex / AcOEt
|
247-202
|
|
203-287
|
S4
|
Solution de couleur marronne présentant 6 taches
visibles à l'UV et à l'iode
|
|
288-315
|
S5
|
Solution de couleur maronne dans laquelle précipite les
cristaux de couleur blanche (GB1) visible à l'UV et
à l'iode
|
|
316-339
|
Solution de couleur maronne dans laquelle précipite les
cristaux de couleur blanche (GB2) visible à l'UV et
à l'iode
|
|
340-349
|
Solution de couleur jaunâtre présentant 6 taches
visibles à l'UV et à l'iode
|
|
45% Hex / AcOEt
|
350-386
|
|
50% Hex / AcOEt
|
387-398
|
|
399-443
|
S6
|
Solution de couleur jaunâtre dans laquelle
précipite les cristaux de couleur blanche (GB3) visible
à l'UV et à l'iode
|
|
444-459
|
|
50% Hex / AcOEt
|
460-472
|
S7
|
Solution de couleur jaunâtre présentant plusieurs
taches visibles à l'UV et à l'iode
|
|
473-474
|
|
60% Hex / AcOEt
|
475-484
|
|
Solution de couleur jaunâtre dans laquelle
précipite les cristaux de couleur blanche (GB4) visible
à l'UV et à l'iode
|
|
70% Hex / AcOEt
|
485-496
|
Solution de couleur maronne dans laquelle précipite
|
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 53
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
|
|
|
les cristaux de couleur blanche (GB5) visible
à l'UV et à l'iode
|
|
497-504
|
Solution de couleur jaunâtre présentant 7 taches
visibles à l'UV et à l'iode
|
|
80% Hex / AcOEt
|
505-538
|
|
AcOEt
|
539-559
|
|
560-569
|
|
10%AcOEt/MeOH
|
570-577
|
|
578-654
|
S8
|
Solution de couleur jaunâtre présentant les
plusieurs taches visibles à l'UV et à l'iode
|
|
20%AcOEt/MeOH
|
655-684
|
S9
|
Solution de couleur jaunâtre présentant plusieurs
taches visibles à l'UV et à l'iode
|
|
30%AcOEt/MeOH
|
685-698
|
|
40%AcOEt/MeOH
|
699-717
|
|
50%AcOEt/MeOH
|
718-742
|
S10
|
Lavage
|
I.3.3 protocole d'obtention des composés
> Traitement de la série S5:
Les fractions 288-315 ont été regroupées
sur la base de la CCM analytique. Laissées au repos pendant 20 minutes
il s'est formé un précipité blanc qui a été
filtré puis lavé. Une CCM de ce produit nous a montré
qu'il est pur, nous l'avons indexé GB1.
Les fractions 324-339 ont été regroupées
sur la base de la CCM analytique. Laissées au repos pendant 30
minutes,donnent un précipité blanc. Celui-ci a été
filtré puis lavé. Sa CCM montre qu'il est pur, nous l'avons
indexé GB2.
> Traitement de la série S6 :
Les fractions 399-443 regroupées sur la base de la CCM
analytique et laissées au repos pendant 45 minutes il s'est formé
un précipité blanc qui a été filtré puis
lavé. Une CCM de ce produit nous a montré qu'il est pur, nous
l'avons indexé GB3.
> Traitement de la série S7 :
Les fractions 475-484 ont été regroupées
sur la base de la CCM analytique. Laissées au repos pendant 2 heures, il
s'est formé un précipité blanc qui a été
filtré puis lavé. Sa CCM nous montre qu'il est pur, nous l'avons
indexé GB4.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 54
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Les fractions 485-496 ont été regroupées
sur la base de la CCM analytique. Laissées au repos pendant 55 minutes,
il s'est formé un précipité blanc qui a été
filtré puis lavé. Sa CCM montre qu'il est pur, nous l'avons
indexé GB5.
I.4 Caractéristiques physico-chimiques des
composés isolés
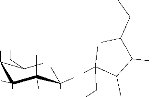

Composé GB1
Le composé GB1 a été identifié
comme étant la camptothecine
Couleur : blanche
Aspect : solide dans le système Hex / AcOEt 45%
Révélation : I2 et UV
PF : 260 oC
F.B : C20H16N2O4
Test de Dragendorf: positif
Spectre de masse ESI [M-H]+. à m/z =
349,1
Spectre de masse ESI de GB1 : Figure 4
Spectre de RMN 1H (500 MHz, DMSO) de GB1 : Figure
14
Spectre de RMN 13C (125 MHz, DMSO) de GB1 : Figure
15
Spectre 1H-1H COSY de GB1 : Figure 16
Spectre HSQC de GB1 : Figure 17
Composé GB5
Le composé GB5 a été identifié
comme étant un sucrose
Couleur : blanche
Aspect : solidedans le système Hex / AcOEt 70%
Révélation : I2 et UV
PF :185,5 oC
F.B.: C12H22O11
Test de Liebermann Molish: positif
H
HO
O
O
OH H
H
77
H OH
N
O
H
O
HO OH
N
HO
OH
O
OH
O
O
78
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 55
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 56
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Spectre de masse ESI [M-H]+ à m/z = 341
Spectre de masse ESI de GB5 : Figure 11
Spectre de RMN 1H (500 MHz, DMSO) de GB5 :
Figure
Spectre de RMN 13C (125 MHz, DMSO) de GB5 :
Figure
Spectre 1H-1H COSY de GB5 : Figure 16
Spectre HSQC de GB5 : Figure 17
II TESTS CARACTERISTIQUES DES COMPOSES ISOLES
II.1 Test de Dragendorf
Ce test a pour but de révéler la présence
des alcaloïdes. Le réactif est l'iodobismutite de potassium.
Préparation du réactif de
Dragendorf
Solution A : 850 g de nitrate de bismuth sont
dissous dans un mélange contenant 10 mL d'acide acétique glacial
et 40 mL d'eau.
Solution B : 8 g de KI sont dissous dans 20 mL
d'eau.
La solution utilisée est constituée de 5mL de la
solution A, 5 mL de la solution B, 20mL d'acide acétique glacial et 70
mL d'acétate d'éthyle (ou d'eau).
Dragendorf modifié par Schultz
Solution mère : préparer une
solution avec :
Iodure de potassium 7 g
Eau distillé 18mL
Acide chlorhydrique 3mL
Porter à ébullition et ajouter par quantité
1,5 g de sous nitrate de bismuth. Après refroidissement, 1,5 g d'iode
sont ajoutés ; puis diluer avec un volume égal d'eau
Mode operatoire
20 mL d'extrait sont évaporés à sec dans
une capsule en porcelaine. 10 mL de HCl 10 % sont ajoutés. Mettre dans
trois tubes hémolyse environ 1 mL de solution extractive ;
vérifier que le pH est entre 1 et 2. Ajouter 2 à 3 gouttes de
réactif de Dragendorf.
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Résultats et interprétations
On observe un précipité rouge orangé
Révélation sur plaque CCM avec
l'iodoplatinate de potassium Préparation de l'iodoplatinate de
potassium
Formule 1 : 3mL d'une solution aqueuse
à 2,5 % d'acide hexachloroplatinique sont dilués par 97 mL d'eau.
Ajouter 100 mL d'une solution de KI à 1,5%. Ce mélange est
dilué au 1/10 avant utilisation.
Formule 2 : dissoudre 0, 25 g de chlorure
platinique et 5 g d'iodure de potassium dans 100mL d'eau. Ajouter 2 mL de HCl
concentré
II.2 Test de Molish
Ce test permet de mettre en évidence la présence
d'un sucre dans une molécule. Mode opératoire
:
Préparation du réactif de
Molish: 50 mL de réactif se prépare en dissolvant 1 g de
á-naphtol dans 50 mL d'éthanol ; dissoudre son produit dans un
tube à essai, y ajouter 1 ml de réactif de Molish, et en faisant
couler lentement sur la paroi du tube 1 ml d'acide sulfurique
concentré.
Résultat et interprétation
La formation d'un anneau violet marque la présence d'un
sucre dans la molécule.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 57
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 58
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Références bibliographiques
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 59
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Aniszewski T., (2007). Alkaloid-secret of life,
biological significance, application, andécologie role, ELESIER,
Netherland, p 316.
Aubreville, A. et Jean. F., (1972).Flore du
Gabon-19-loganiacées. Muséum National d'Histoire Naturelle,
Paris, France, p 153.
Bassène E., (2012). Initiation à
la recherche sur les substances naturelles, Presse Universitaire de Dakar,
Dakar, Sénégal, p 130.
De-ruijter A.,(2007).Mostuea batesii
Baker. Plant Resources of Tropical Africa , Ressources
végétales de l'Afrique Tropicale, Ed. Prota , Wageningen, Pays
Bas., p 300
De-Smet, P.A.G.M., (1996). Some
Ethnopharmacological notes on African Hallucinogens. Journal of
Ethnopharmacology, 50, pp 141-146.
Edwin W., N.L., (2012). Loganiaceae of
Africa, Europe Exposition Journal Bioscience,6, p
1962-1973.
Guignard J. , (1996). Biochimie
Végétale, Paris, Masson. , p255.
Guillaume B., (2013). Chimie Organique
Hétérocyclique cor 706, Sherbrooke, Ed.Automne,p128.
Heywood V., (1985). Las plantas con flores. Ed.
Reverté. España, p329. Hostettmann K., (1997).
Tout savoir sur les pouvoirs des plantes, París, Fabre, p
319.
Jin-rui ,Yali . Hallack,John et Michael,
(1999).20-O-â-Glucopyranosyl Camptothecin from
Mostueabrunonis: A Potential Camptothecin Pro-Drug with Improved
Solubility,Journal of Natural Product, 62(10), pp 1427-1429.
Leeuwenberg J., (1961).The Loganiaceae of
Africa, Ed. Mandelingen Van, pp30. Li ping T. et Leeuwenberg J.,
(1996). Loganiaceae,Flora of China; 15, p320-338
Long-Ze et Geofferey, (1990). RMN 13C
assignments of camptothecin, Journal of Natural Product, 53, pp
186-189.
Mangambu, (2013). Taxonomie et biogeographie des
ptéridophytes de l'écosystème forester des montagnes du
parc de Kahuzi-Biega à l'Est de la R.D; congo.Geo-Eco-trop; p 463.
Milcent R., (2003). Chimie des
hétérocycles, avenue de Hoggar, EDP sciences, pp856.
Noaki K., Hideki O., Fukushi E.,Shuichi O., et Kawa J.,
(2008). Structural Analysis of two Trisaccharides isolated from
Fermented beverage of Plant Extract, open geoscience, 1, pp 25-30.
Olusua T.,Oluwatoy T. et Okowokudejo O., ( 2013).
Morphological Study of Loganiaceae diversities in West Africa,
Journal of Biology Agricultura and Healthcare,.3, pp11.
OMS, (2010).Stratégie pour la
médecine traditionnelle, Genève, p 201.
Vercautoren, (2011). Cours de pharmacognosie,
université de Montpellier, pp 318. Watson L. et Dallwitz J.,
(1992), The Families of Flowering Plants,Ed. Reverté, p 200.
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 60
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Lexique
MEMOIRE PRESENTE ET SOUTENU PAR TCHAPO D. C. EMAR Page 61
Constituants chimiques des racines de Mostuea batesii
Baker (Loganiaceae)
Analgésique : Substance qui abolit la
sensibilité de la douleur.
Anesthésique : Substance qui provoque une
insensibilité locale ou générale.
Antibiotique : Substance chimique produite par
des micro-organismes ayant le pouvoir d'entraver la croissance des
bactéries ou d'autres micro-organismes et même de les
détruire en solution très diluée.
Corymbe : Mode d'inflorescence dans lequel les
pédoncules sont de longueur différente et divergeante de telle
sorte que les fleurs soient sur un même plan
Cyme : Mode d'inflorescence constitué par
un axe principal à l'extrémité duquel se trouve une fleur,
et qui porte également un ou plusieurs axes latéraux se ramifiant
de la même manière
Emétique : Substance qui provoque le
vomissement.
Glabre : Qui n'est pas pubescent
Infère : Terme qualifiant un ovaire
placé comme s'il était sous la fleur
Inflorescence : Manière donc les fleurs
sont disposées sur la plante qui le porte
Limbe : Partie large des feuilles
Ovoïde : Qui a la forme d'un oeuf
Pétiole : Partie rétrécie
de la feuille qui lui sert de support
Spermaphyte : Plante qui se reproduit par la
graine
Stipule : Petite feuille supplémentaire,
réduite le plus souvent à la nervure médiane et produite
par expansion du pétiole, qui s'insère de chaque
côté de la base de certaines feuilles.
Vermifuge : Substance qui provoque l'expulsion
des vers intestinaux
| 


